Đáp án
1A
2D
3C
4D
5D
6C
7A
8D
9A
10A
11A
12C
13C
14C
15B
16D
17C
18A
19C
20B
21D
22B
23B
24D
25B
26A
27A
28D
29D
30C
31C
32C
33D
34D
35C
36B
37D
38D
39C
40B
Đáp án Đề minh họa số 10 thi Tốt Nghiệp Trung học Phổ Thông 2024 môn Hóa học
Câu 1 [21212]: Số nguyên tử oxi trong một phân tử chất béo là
A, 6.
B, 2.
C, 4.
D, 8.
HD: Chất béo là trieste của glixerol và axit béo
⇒ Chất béo có dạng (RCOO)3C3H5 với R là gốc hiđrocacbon.
⇒ số nguyên tử oxi trong phân tử chất béo là 3 × 2 = 6.
⇒ Chất béo có dạng (RCOO)3C3H5 với R là gốc hiđrocacbon.
⇒ số nguyên tử oxi trong phân tử chất béo là 3 × 2 = 6.
Câu 2 [342776]: Công thức phân tử của benzen là
A, C2H2.
B, C8H8.
C, C2H4.
D, C6H6.
HD: Công thức của benzen:

⇝ Chọn đáp án D. ♠

⇝ Chọn đáp án D. ♠
Câu 3 [679847]: Chất nào sau đây là chất điện li yếu?
A, HCl.
B, KNO3.
C, CH3COOH.
D, NaOH.
HD: Chất điện li yếu là những chất trong dung dịch nước chỉ điện li một phần thành các ion còn phần lớn tồn tại ở dạng phân tử. Quá trình điện li là quá trình thuận nghịch (trong phương trình điện li dùng dấu mũi tên hai chiều ⇄).
❌ A. HCl → H+ + Cl–.
❌ B. KNO3 → K+ + NO3–.
✔️ C. CH3COOH ⇄ CH3COO– + H+.
❌ D. NaOH → Na+ + OH–.
❌ A. HCl → H+ + Cl–.
❌ B. KNO3 → K+ + NO3–.
✔️ C. CH3COOH ⇄ CH3COO– + H+.
❌ D. NaOH → Na+ + OH–.
Câu 4 [60189]: Chất nào sau đây không dùng để làm mềm nước cứng tạm thời?
A, Na3PO4.
B, Ca(OH)2.
C, Na2CO3.
D, HCl.
Giải:
Nước cứng tạm thời có chứa các ion Mg2+; Ca2+; HCO3–
A. 2Na3PO4 + 3Mg2+ Mg3(PO4)2 (kết tủa) + 6Na+ (tương tự với Ca2+)
Mg3(PO4)2 (kết tủa) + 6Na+ (tương tự với Ca2+)
 Na3PO4 làm mềm được
Na3PO4 làm mềm được
B. OH– + HCO3– CO32– + H2O
CO32– + H2O
CO32– + Ca2+ CaCO3 (kết tủa) (tương tự với Mg2+)
CaCO3 (kết tủa) (tương tự với Mg2+)
 Ca(OH)2 làm mềm được.
Ca(OH)2 làm mềm được.
C. CO32– + Ca2+ CaCO3 (tương tự với Mg2+)
CaCO3 (tương tự với Mg2+)
 Vậy Na2CO3 làm mềm được
Vậy Na2CO3 làm mềm được
D. HCl không làm mềm được nước cứng tạm thời.
Đáp án D.
Nước cứng tạm thời có chứa các ion Mg2+; Ca2+; HCO3–
A. 2Na3PO4 + 3Mg2+
 Mg3(PO4)2 (kết tủa) + 6Na+ (tương tự với Ca2+)
Mg3(PO4)2 (kết tủa) + 6Na+ (tương tự với Ca2+) Na3PO4 làm mềm được
Na3PO4 làm mềm đượcB. OH– + HCO3–
 CO32– + H2O
CO32– + H2OCO32– + Ca2+
 CaCO3 (kết tủa) (tương tự với Mg2+)
CaCO3 (kết tủa) (tương tự với Mg2+) Ca(OH)2 làm mềm được.
Ca(OH)2 làm mềm được.C. CO32– + Ca2+
 CaCO3 (tương tự với Mg2+)
CaCO3 (tương tự với Mg2+) Vậy Na2CO3 làm mềm được
Vậy Na2CO3 làm mềm đượcD. HCl không làm mềm được nước cứng tạm thời.
Đáp án D.
Câu 5 [61754]: Trong các khoáng vật dưới đây, khoáng vật nào không chứa CaCO3?
A, Canxit.
B, Đolomit.
C, Đá hoa.
D, Magiezit.
HD: Thành phần chính của các khoảng vật:
☑ A. canxit: CaCO3. ☑ B. đolomit: CaCO3.MgCO3.
☑ C. đá hoa: CaCO3. ☒ D. magiezit: MgCO3. ❒
☑ A. canxit: CaCO3. ☑ B. đolomit: CaCO3.MgCO3.
☑ C. đá hoa: CaCO3. ☒ D. magiezit: MgCO3. ❒
Câu 6 [311952]: Oxit E được dùng trong sản xuất nước giải khát có gaz, bảo quản thực phẩm (dạng nước đá khô), dập tắt đám cháy. Công thức hóa học của E là
A, CO.
B, SO2.
C, CO2.
D, P2O5.
HD: Nước đá khô là CO2 rắn dùng bảo quản thực phẩm.
Khí CO2 không duy trì sự cháy nên dùng dập tắt đám cháy (trừ đám cháy kim loại,...)
CO2 bão hòa dùng làm chất tạo gas trong nước giải khát.
⇝ Công thức hóa học của E là CO2. ❒
Khí CO2 không duy trì sự cháy nên dùng dập tắt đám cháy (trừ đám cháy kim loại,...)
CO2 bão hòa dùng làm chất tạo gas trong nước giải khát.
⇝ Công thức hóa học của E là CO2. ❒
Câu 7 [255067]: Kim loại Fe không bị oxi hoá bởi dung dịch nào sau đây?
A, ZnCl2.
B, HCl.
C, AgNO3.
D, CuSO4.
HD: Dãy điện hoá: 
⇝ Fe không bị oxi hoá bởi Zn2+ ⇝ Chọn đáp án A. ♥

⇝ Fe không bị oxi hoá bởi Zn2+ ⇝ Chọn đáp án A. ♥
Câu 8 [983256]: Kim loại nào sau đây có nhiệt độ nóng chảy thấp nhất?
A, Li.
B, Cu.
C, Ag.
D, Hg.
HD: Ở nhiệt độ thường, thủy ngân Hg là chất lỏng, có nhiệt độ sôi thấp nhất.
Đối lập, vonfram (W) có nhiệt độ sôi cao nhất.
Đối lập, vonfram (W) có nhiệt độ sôi cao nhất.
Câu 9 [973549]: Oxit nào sau đây là oxit axit?
A, CrO3.
B, FeO.
C, Cr2O3.
D, Fe2O3.
HD: CrO3 là một oxit axit, tác dụng với nước, tạo thành hỗn hợp axit (chỉ tồn tại trong dung dịch):
• CrO3 + H2O → H2CrO4 (axit cromic).
• 2CrO3 + H2O → H2Cr2O7 (axit đicromic).
• CrO3 + H2O → H2CrO4 (axit cromic).
• 2CrO3 + H2O → H2Cr2O7 (axit đicromic).
Câu 10 [58595]: Trong số các ion sau: Fe3+, Cu2+, Fe2+, và Al3+, ion có tính oxi hóa mạnh nhất là
A, Fe3+.
B, Cu2+.
C, Fe2+.
D, Al3+.
HD:
Thứ tự tăng dần tính oxi hóa: Al3+, Fe2+, Cu2+, Fe3+.
Thứ tự tăng dần tính oxi hóa: Al3+, Fe2+, Cu2+, Fe3+.
Câu 11 [679789]: Công thức của nhôm clorua là
A, AlCl3.
B, Al2(SO4)3.
C, Al(NO3)3.
D, AlBr3.
HD: Phân tích các đáp án:
| Cấu tạo | AlCl3 | Al2(SO4)3 | Al(NO3)3 | AlBr3 |
| Tên gọi | nhôm clorua | nhôm sunfat | nhôm nitrat | nhôm bromua |
| (✔️) | (❌) | (❌) | (❌) |
Câu 12 [679701]: Chất nào sau đây thuộc loại đisaccarit?
A, Glucozơ.
B, Fructozơ.
C, Saccarozơ.
D, Tinh bột.
HD: Bài học phân loại hợp chất cacbohiđrat:

⇒ Trong 4 phương án, saccarozơ là đisaccarit ⇝ Chọn đáp án C. ♣

⇒ Trong 4 phương án, saccarozơ là đisaccarit ⇝ Chọn đáp án C. ♣
Câu 13 [229153]: Số nguyên tử hiđro có trong phân tử đipeptit Gly-Ala bằng
A, 11.
B, 12.
C, 10.
D, 13.
Đáp án: C
Câu 14 [679243]: Trong công nghiệp, kim loại nào sau đây chỉ được điều chế bằng phương pháp điện phân nóng chảy?
A, Fe.
B, Cu.
C, Mg.
D, Ag.
HD: Bài học về điều chế kim loại:
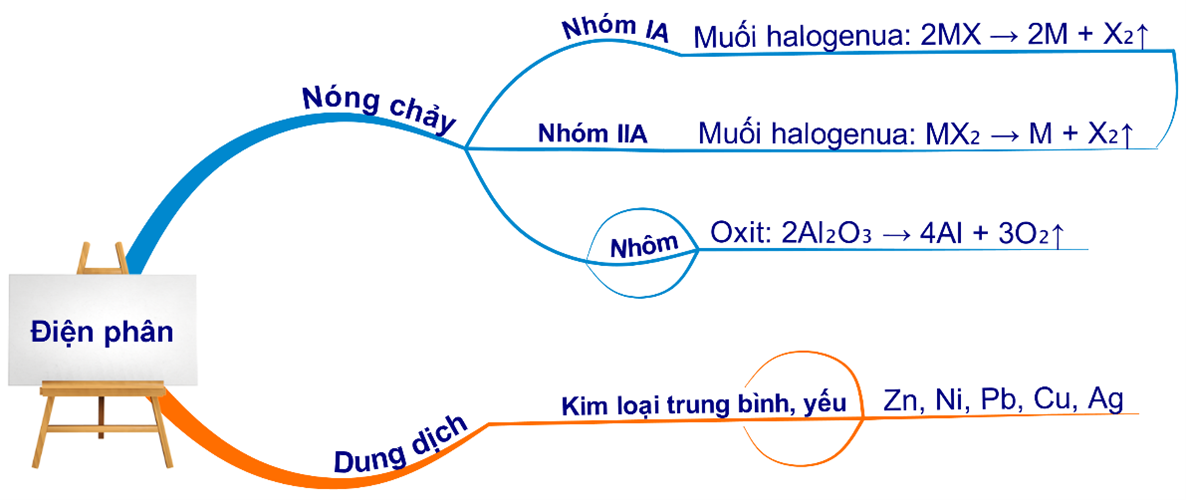
⇒ Mg là kim loại kiềm thổ, chỉ điều chế được bằng phương pháp điện phân nóng chảy.

⇒ Mg là kim loại kiềm thổ, chỉ điều chế được bằng phương pháp điện phân nóng chảy.
Câu 15 [59862]: Cho dung dịch NaHSO4 dư vào dung dịch chất X, thu được kết tủa màu trắng. Chất X là
A, NaOH.
B, BaCl2.
C, NaHCO3.
D, NaAlO2.
HD: Phân tích các đáp án:
❌ A. NaOH + NaHSO4 → Na2SO4 + H2O.
✔️ B. BaCl2 + NaHSO4 → NaCl + HCl + BaSO4↓ (trắng).
❌ C. NaHCO3 + NaHSO4 → Na2SO4 + CO2↑ + H2O.
❌ D. NaAlO2 + NaHSO4 + H2O → Al(OH)3↓ (trắng) + Na2SO4.
► Tuy nhiên, sau đó NaHSO4 dùng dư nên 6NaHSO4 + 2Al(OH)3 → Al2(SO4)3 + 3Na2SO4 + 3H2O.
❌ A. NaOH + NaHSO4 → Na2SO4 + H2O.
✔️ B. BaCl2 + NaHSO4 → NaCl + HCl + BaSO4↓ (trắng).
❌ C. NaHCO3 + NaHSO4 → Na2SO4 + CO2↑ + H2O.
❌ D. NaAlO2 + NaHSO4 + H2O → Al(OH)3↓ (trắng) + Na2SO4.
► Tuy nhiên, sau đó NaHSO4 dùng dư nên 6NaHSO4 + 2Al(OH)3 → Al2(SO4)3 + 3Na2SO4 + 3H2O.
Câu 16 [679245]: Hợp chất H2NCH2COOH có tên là
A, valin.
B, lysin.
C, alanin.
D, glyxin.
Chọn đáp án D.
★ Phân tích 4 đáp án

★ Phân tích 4 đáp án

Câu 17 [7073]: Chất X có công thức phân tử C4H8O2. Khi cho X tác dụng với dung dịch NaOH, đun nóng, sau phản ứng thu được chất Y có công thức CHO2Na. Công thức của X là
A, CH3COOC2H5.
B, HCOOC2H5.
C, HCOOC3H7.
D, C2H5COOCH3.
Giải: Este đơn chức có dạng RCOOR' được tạo từ HCOOH (Vì muối là HCOONa)
⇒ R chính là H. Bảo toàn nguyên tố ⇒ R là –C3H7
⇒ Este đó có CTCT thu gọn là HCOOC3H7 ⇒ Chọn C.
⇒ R chính là H. Bảo toàn nguyên tố ⇒ R là –C3H7
⇒ Este đó có CTCT thu gọn là HCOOC3H7 ⇒ Chọn C.
Câu 18 [679352]: Trùng hợp propilen thu được polime có tên gọi là
A, polipropilen.
B, polietilen.
C, polistiren.
D, poli(vinyl clorua).
HD: Trùng hợp propilen CH3CH=CH2 thu được tương ứng polipropilen –(CH(CH3)–CH2)n–.


Câu 19 [352287]: Công thức hóa học của phèn chua là
A, Na2SO4.Al2(SO4)3.24H2O.
B, Li2SO4.Al2(SO4)3.24H2O.
C, K2SO4.Al2(SO4)3.24H2O.
D, (NH4)2SO4.Al2(SO4)3.24H2O.
Đáp án: C
Câu 20 [679543]: Kim loại nào sau đây không tan được trong dung dịch HCl?
A, Al.
B, Ag.
C, Zn.
D, Mg.
HD: Dãy hoạt động kim loại: Mg > Al > Zn > (H)axit > Ag.
⇒ Ag không tan được trong dung dịch HCl.
⇒ Ag không tan được trong dung dịch HCl.
Câu 21 [60622]: Cho dung dịch Ba(OH)2 dư vào dung dịch gồm FeSO4 và H2SO4, lọc lấy kết tủa rồi đem nung trong không khí đến khối lượng không đổi thu được chất rắn là
A, Fe2O3 và BaO.
B, FeO và BaSO4.
C, FeO và BaO.
D, Fe2O3 và BaSO4.
Giải: 
||⇒ nung trong không khí thì: 4Fe(OH)2 + O2 2Fe2O3 + 4H2O.
2Fe2O3 + 4H2O.
BaSO4 không bị phân hủy ⇒ rắn gồm Fe2O3 và BaSO4 ⇒ chọn D.

||⇒ nung trong không khí thì: 4Fe(OH)2 + O2
 2Fe2O3 + 4H2O.
2Fe2O3 + 4H2O.BaSO4 không bị phân hủy ⇒ rắn gồm Fe2O3 và BaSO4 ⇒ chọn D.
Câu 22 [506979]: Đun nóng 8,8 gam etyl axetat CH3COOCH2CH3 với dung dịch NaOH dư, khi phản ứng xảy ra hoàn toàn, khối lượng của ancol thu được là
A, 4,4 gam.
B, 4,6 gam.
C, 4,2 gam.
D, 8,2 gam.
HD: Phản ứng: CH3COOC2H5 + NaOH –––to–→ CH3COONa + C2H5OH.
neste = 8,8 ÷ 88 = 0,1 mol ⇒ nancol = 0,1 mol ⇒ mancol = 0,1 × 46 = 4,6 gam.
neste = 8,8 ÷ 88 = 0,1 mol ⇒ nancol = 0,1 mol ⇒ mancol = 0,1 × 46 = 4,6 gam.
Câu 23 [983262]: Phát biểu nào sau đây đúng?
A, Tơ nilon-6,6 được điều chế bằng phản ứng trùng hợp.
B, Tơ poliamit kém bền trong môi trường axit.
C, Cao su thiên nhiên có thành phần chính là polibutađien.
D, Tơ xenlulozơ axetat thuộc loại tơ tổng hợp.
HD: Phân tích các đáp án:
❌ A. sai vì nilon-6,6 được điều chế bằng phản ứng trùng ngưng:

✔️ B. đúng vì liên kết amit CO–NH kém bền trong cả môi trường axit và bazơ, dễ bị thuỷ phân.
❌ C. sai vì thành phần chính cao su thiên nhiên là poliisopren.
❌ D. sai vì tơ xenlulozơ axetat thuộc loại tơ bán tổng hợp (nhân tạo).
❌ A. sai vì nilon-6,6 được điều chế bằng phản ứng trùng ngưng:

✔️ B. đúng vì liên kết amit CO–NH kém bền trong cả môi trường axit và bazơ, dễ bị thuỷ phân.
❌ C. sai vì thành phần chính cao su thiên nhiên là poliisopren.
❌ D. sai vì tơ xenlulozơ axetat thuộc loại tơ bán tổng hợp (nhân tạo).
Câu 24 [334137]: Cho dãy các chất: tinh bột, xenlulozơ, glucozơ, fructozơ, saccarozơ. Số chất trong dãy thuộc loại polisaccarit là
A, 3.
B, 1.
C, 4.
D, 2.
HD: Bài học phân loại:
![567242[LG].png](https://m.moon.vn/Images/Teachers/rongden_167/ProS2018/TAP%20II/567242[LG].png)
Có 2 chất trong dãy thuộc loại polisaccarit là xenlulozơ và tinh bột ⇝ Chọn đáp án D. ♠
![567242[LG].png](https://m.moon.vn/Images/Teachers/rongden_167/ProS2018/TAP%20II/567242[LG].png)
Có 2 chất trong dãy thuộc loại polisaccarit là xenlulozơ và tinh bột ⇝ Chọn đáp án D. ♠
Câu 25 [339120]:
Este X có công thức phân tử C8H8O2 khi đun nóng với dung dịch NaOH dư thu được dung dịch chứa hai muối. Số công thức cấu tạo thoả mãn X là
A, 3.
B, 4.
C, 5.
D, 6.
Este X có công thức phân tử C8H8O2 có π + v= 5
X thủy phân tạo 2 muối → X có dạng RCOOC6H4X
Các đồng phân thỏa mãn gồm HCOOC6H4CH3( CH3 ở vị trí ortho), HCOOC6H4CH3 (CH3 ở vị trí meta), HCOOC6H4CH3 ( CH3 ở vị trí para) và CH3COOC6H4
Đáp án B.
X thủy phân tạo 2 muối → X có dạng RCOOC6H4X
Các đồng phân thỏa mãn gồm HCOOC6H4CH3( CH3 ở vị trí ortho), HCOOC6H4CH3 (CH3 ở vị trí meta), HCOOC6H4CH3 ( CH3 ở vị trí para) và CH3COOC6H4
Đáp án B.
Câu 26 [136588]: Ngâm một lá kẽm trong 100 ml dung dịch AgNO3 0,1M. Sau khi phản ứng xảy ra hoàn toàn, khối lượng Ag được tạo thành là
A, 1,08 gam.
B, 2,16 gam.
C, 10,80 gam.
D, 5,40 gam.
HD: Ta có:  ⇒ Zn + 2AgNO3 → Zn(NO3)2 + 2Ag.
⇒ Zn + 2AgNO3 → Zn(NO3)2 + 2Ag.
Giả thiết nAgNO3 = 0,1 mol; phản ứng hoàn toàn nên thu được 0,1 mol Ag
⇒ m = 1,08 gam ⇝ Chọn đáp án C. ♣
 ⇒ Zn + 2AgNO3 → Zn(NO3)2 + 2Ag.
⇒ Zn + 2AgNO3 → Zn(NO3)2 + 2Ag.
Giả thiết nAgNO3 = 0,1 mol; phản ứng hoàn toàn nên thu được 0,1 mol Ag
⇒ m = 1,08 gam ⇝ Chọn đáp án C. ♣
Câu 27 [184917]: Từ m kg mùn cưa chứa 50% xenlulozơ (còn lại là tạp chất trơ) sản xuất được 80 kg glucozơ với hiệu suất toàn bộ quá trình là 80%. Giá trị của m là
A, 180.
B, 162.
C, 360.
D, 720.
Đáp án: A
Câu 28 [508706]: Đốt cháy hoàn toàn một amino axit X (phân tử có một nhóm NH2) thu được 8,8 gam CO2 và 1,12 lít N2. Công thức phân tử của X là
A, C3H7NO2.
B, C4H9NO2.
C, C2H7NO2.
D, C2H5NO2.
HD: X + O2 –––to–→ 0,2 mol CO2 + ? mol H2O + 0,05 mol N2.
Amino axit X chỉ chứa 1 nhóm NH2 ⇒ nX = 2nN2 = 0,1 mol.
⇒ Số Camino axit X = 0,2 ÷ 0,1 = 2.
► Chỉ có duy nhất amino axit H2NCH2COOH có 2C.
⇝ Yêu cầu công thức phân tử của X là C2H5NO2.
Amino axit X chỉ chứa 1 nhóm NH2 ⇒ nX = 2nN2 = 0,1 mol.
⇒ Số Camino axit X = 0,2 ÷ 0,1 = 2.
► Chỉ có duy nhất amino axit H2NCH2COOH có 2C.
⇝ Yêu cầu công thức phân tử của X là C2H5NO2.
Câu 29 [352288]: Phát biểu nào sau đây đúng?
A, Nhôm là kim loại có tính lưỡng tính.
B, Thạch cao nung có công thức CaSO4.2H2O, được dùng để bó bột, đắp tượng, đúc khuôn,...
C, Điện phân dung dịch AlCl3 (điện cực bằng than chì) thu được kim loại Al ở catot.
D, Bột chữa cháy trong bình cứu hỏa thường là NaHCO3.
HD: Phân tích các đáp án:
❌ A. sai vì không có kim loại có tính lưỡng tính. Nhiều bạn nhầm lẫn giữa việc Al có phản ứng với HCl, NaOH mà cho rằng nó lưỡng tính là sai. Ví như các chất protein hay chất béo thủy phân trong HCl, NaOH mà lại nói chúng có tính lưỡng tính ư?
❌ B. sai, ứng dụng đó là của thạch cao nung chứ không phải thạch cao sống:

❌ C. sai vì thứ tự điện phân:

⇝ nên điện phân AlCl3 không thể thu được Al.
✔️ D. đúng, bình chữa cháy bột có bột NaHCO3 và khí N2.
❌ A. sai vì không có kim loại có tính lưỡng tính. Nhiều bạn nhầm lẫn giữa việc Al có phản ứng với HCl, NaOH mà cho rằng nó lưỡng tính là sai. Ví như các chất protein hay chất béo thủy phân trong HCl, NaOH mà lại nói chúng có tính lưỡng tính ư?
❌ B. sai, ứng dụng đó là của thạch cao nung chứ không phải thạch cao sống:

❌ C. sai vì thứ tự điện phân:

⇝ nên điện phân AlCl3 không thể thu được Al.
✔️ D. đúng, bình chữa cháy bột có bột NaHCO3 và khí N2.
Câu 30 [135753]: Cho 14,3 gam hỗn hợp X gồm Mg, Al, Zn tác dụng với O2 dư, thu được 22,3 gam hỗm hợp 3 oxit kim loại. Nếu cho 14,3 gam X tác dụng hết với dung dịch HCl thì thu được V lít khí H2 (đktc). Giá trị của V là
A, 22,4.
B, 5,6.
C, 11,2.
D, 8,96.
Giải: BTe: nH2 = nO =  = 0,5 mol ⇒ V = 11,2 lít.
= 0,5 mol ⇒ V = 11,2 lít.
 = 0,5 mol ⇒ V = 11,2 lít.
= 0,5 mol ⇒ V = 11,2 lít.
Câu 31 [52058]: Cho các phát biểu sau:
(a) Các kim loại đều tác dụng với oxi tạo ra oxit.
(b) Kim loại nhôm được điều chế trong công nghiệp bằng phương pháp nhiệt luyện.
(c) Miếng gang để trong không khí ẩm xảy ra ăn mòn điện hóa.
(d) Khi điện phân dung dịch CuSO4 (điện cực trơ) ở catot thu được kim loại.
(e) Các kim loại đều có ánh kim và độ cứng lớn.
(g) Cho mẩu Na vào dung dịch FeSO4 thu được kim loại Fe.
Số phát biểu sai là
(a) Các kim loại đều tác dụng với oxi tạo ra oxit.
(b) Kim loại nhôm được điều chế trong công nghiệp bằng phương pháp nhiệt luyện.
(c) Miếng gang để trong không khí ẩm xảy ra ăn mòn điện hóa.
(d) Khi điện phân dung dịch CuSO4 (điện cực trơ) ở catot thu được kim loại.
(e) Các kim loại đều có ánh kim và độ cứng lớn.
(g) Cho mẩu Na vào dung dịch FeSO4 thu được kim loại Fe.
Số phát biểu sai là
A, 3.
B, 2.
C, 4.
D, 5.
HD: Phân tích các phát biểu:
❌ (a) sai vì "lửa thử vàng - gian nan thử sức" ⇝ O2 không tác dụng được với Ag, Au, Pt,...
❌ (b) sai, trong CN nhôm được điều chế bằng pp điện phân nóng chảy Al2O3 từ quặng boxit.
✔️ (c) đúng vì trong gang có cặp điện cực Fe-C, không khí ẩm là môi trường điện li ⇝ xảy ra ăn mòn điện hoá.
✔️ (d) đúng, catot (cực âm (–)) là nơi cation Cu2+ tìm về, tại đó Cu2+ + 2e → Cu nên thu được kim loại Cu bám ở catot.
❌ (e) sai vì ánh kim đúng nhưng về độ cứng là tính chất vật lí riêng, các kim loại kiềm mềm, độ cứng thấp.
❌ (g) sai vì Na + H2O trước tạo NaOH + H2↑; sau đó 2NaOH + FeSO4 → Fe(OH)2↓ + Na2SO4 chứ không có phản ứng Na đẩy Fe2+ thành Fe.
⇝ có 4/6 phát biểu sai ⇝ Chọn đáp án C. ♣
❌ (a) sai vì "lửa thử vàng - gian nan thử sức" ⇝ O2 không tác dụng được với Ag, Au, Pt,...
❌ (b) sai, trong CN nhôm được điều chế bằng pp điện phân nóng chảy Al2O3 từ quặng boxit.
✔️ (c) đúng vì trong gang có cặp điện cực Fe-C, không khí ẩm là môi trường điện li ⇝ xảy ra ăn mòn điện hoá.
✔️ (d) đúng, catot (cực âm (–)) là nơi cation Cu2+ tìm về, tại đó Cu2+ + 2e → Cu nên thu được kim loại Cu bám ở catot.
❌ (e) sai vì ánh kim đúng nhưng về độ cứng là tính chất vật lí riêng, các kim loại kiềm mềm, độ cứng thấp.
❌ (g) sai vì Na + H2O trước tạo NaOH + H2↑; sau đó 2NaOH + FeSO4 → Fe(OH)2↓ + Na2SO4 chứ không có phản ứng Na đẩy Fe2+ thành Fe.
⇝ có 4/6 phát biểu sai ⇝ Chọn đáp án C. ♣
Câu 32 [352289]: Thực hiện thí nghiệm so sánh khả năng phản ứng với H2O của Na, Mg, Al như sau:
Bước 1: Rót nước vào ống nghiệm thứ nhất (3/4 ống), thêm vài giọt phenolphatalein; đặt vào giá ống nghiệm sau đó bỏ vào đó một mẩu natri bằng hạt gạo.
Bước 2: Rót vào ống nghiệm thứ hai và thứ ba khoảng 5 ml nước, thêm vài giọt phenolphatalein, sau đó đặt vào giá ống nghiệm rồi bỏ vào ống thứ hai một mẩu Mg và ống nghiệm thứ ba một mẩu Al sau đó đun nóng.
Phát biểu nào sau đây không đúng?
Bước 1: Rót nước vào ống nghiệm thứ nhất (3/4 ống), thêm vài giọt phenolphatalein; đặt vào giá ống nghiệm sau đó bỏ vào đó một mẩu natri bằng hạt gạo.
Bước 2: Rót vào ống nghiệm thứ hai và thứ ba khoảng 5 ml nước, thêm vài giọt phenolphatalein, sau đó đặt vào giá ống nghiệm rồi bỏ vào ống thứ hai một mẩu Mg và ống nghiệm thứ ba một mẩu Al sau đó đun nóng.
Phát biểu nào sau đây không đúng?
A, Sau bước 1, dung dịch trong ống nghiệm có màu hồng.
B, Sau bước 2, dung dịch trong ống nghiệm chứa Mg có màu hồng.
C, Sau bước 2, dung dịch trong ống nghiệm chứa Al không màu do có môi trường axit.
D, Thí nghiệm trên chứng tỏ khả năng phản ứng với nước của Na, Mg, Al là giảm dần.
- Hiện tượng:
+ Ống 1: Khí thoát ra mạnh, dung dịch có có màu hồng.
Na + H2O → NaOH + 1/2H2
+ Ống 2 ban đầu không có hiện tượng nhưng khi đun nóng thì phản ứng bắt đầu xảy ra, hiện tượng có khí thoát ra và dung dịch Mg(OH)2 có tính bazơ yếu nhưng dung dịch vẫn có màu hồng.
Mg + H2O → Mg(OH)2 + H2
+ Ống 3 không có hiện tượng vì Al có lớp Al2O3 bên ngoài bền nên không phản ứng với H2O kể cả khi đun nóng.
✔️ A Đúng vì dung dịch NaOH có môi trường bazơ nên dung dịch chứa phenolphtalein sẽ có màu hồng.
✔️ B Đúng vì dung dịch Mg(OH)2 có tính bazơ yếu nhưng dung dịch vẫn có màu hồng.
❌ C Sai vì Al có lớp Al2O3 bên ngoài bền nên không phản ứng với H2O kể cả khi đun nóng.
✔️ D Đúng vì Na phản ứng ở nhiệt độ thường, Mg chỉ phản ứng khi đun nóng, Al không phản ứng.
+ Ống 1: Khí thoát ra mạnh, dung dịch có có màu hồng.
Na + H2O → NaOH + 1/2H2
+ Ống 2 ban đầu không có hiện tượng nhưng khi đun nóng thì phản ứng bắt đầu xảy ra, hiện tượng có khí thoát ra và dung dịch Mg(OH)2 có tính bazơ yếu nhưng dung dịch vẫn có màu hồng.
Mg + H2O → Mg(OH)2 + H2
+ Ống 3 không có hiện tượng vì Al có lớp Al2O3 bên ngoài bền nên không phản ứng với H2O kể cả khi đun nóng.
✔️ A Đúng vì dung dịch NaOH có môi trường bazơ nên dung dịch chứa phenolphtalein sẽ có màu hồng.
✔️ B Đúng vì dung dịch Mg(OH)2 có tính bazơ yếu nhưng dung dịch vẫn có màu hồng.
❌ C Sai vì Al có lớp Al2O3 bên ngoài bền nên không phản ứng với H2O kể cả khi đun nóng.
✔️ D Đúng vì Na phản ứng ở nhiệt độ thường, Mg chỉ phản ứng khi đun nóng, Al không phản ứng.
Câu 33 [908884]: Hỗn hợp X gồm Cu, CuO, Fe, Fe2O3. Hòa tan m gam X trong dung dịch chứa 1,05 mol HCl (dư 25% so với lượng phản ứng), thu được 0,07 mol H2 và 250 gam dung dịch Y. Mặt khác, hòa tan hết m gam X trong dung dịch H2SO4 đặc nóng, thu được dung dịch Z (chứa 3 chất tan) và 0,1 mol SO2 (sản phẩm khử duy nhất của H2SO4). Cho Z tác dụng với dung dịch Ba(OH)2 dư, thu được kết tủa T. Nung T trong không khí đến khối lượng không đổi, thu được 136,85 gam chất rắn. Nồng độ phần trăm FeCl3 trong Y là
A, 3,25%.
B, 5,20%.
C, 3,90%.
D, 2,60%.
HD: ☆ Giải X + HCl: ta có nHCl phản ứng = 1,05 ÷ 1,25 = 0,84 mol.
• bảo toàn e mở rộng: ∑nH+ phản ứng = 2nO trong oxit + 2nH2 ⇒ nO trong oxit = 0,35 mol.
☆ Giải X + H2SO4: chú ý nFe > nH2 = 0,07 mol ⇒ nếu H2SO4 dùng dư thì Fe → Fe3+
⇒ 2nSO2↑ > 3nFe = 0,21 ⇒ trái giả thiết ⇒ H2SO4 hết.
⇒ Z gồm 3 chất tan là a mol FeSO4; b mol CuSO4 và c mol Fe2(SO4)3.
• bảo toàn e gián tiếp: ∑nSO42– trong muối = nSO2 + nO trong oxit = 0,45 mol.
⇒ a + b + 3c = 0,45 và có 0,45 mol BaSO4 trong chất rắn cuối cùng.
136,85 gam gồm 0,45 mol BaSO4 + (½a + c) mol Fe2O3 + b mol CuO.
⇒ 160 × (½a + c) + 80c + 0,45 × 233 = 136,85 ⇒ a + b + 2c = 0,4.
Vậy giải ra (a + b) = 0,3 và c = 0,05 mol.
Quay lại với yêu cầu ở dung dịch Y: gồm x mol FeCl2 + y mol CuCl2 + z mol FeCl3.
Bảo toàn nguyên tố Cl: ∑nCl– trong muối = 2x + 2y + 3z = 0,84.
Mà ∑nnguyên tố kim loại trong muối Y = ∑nnguyên tố kim loại trong muối Z
⇄ x + y + z = a + b + 2c = 0,4 ⇒ giải (x + y) = 0,36 và z = 0,04 mol.
► Đề cũng chỉ yêu cầu liên quan đến FeCl3 thôi (vì có hỏi FeCl2 hay CuCl2 thì cũng chưa đủ giả thiết để giải)
⇒ Yêu cầu C%mFeCl3 = 0,04 × 162,5 ÷ 250 × 100% = 2,60% ⇝ Chọn đáp án D. ♣
• bảo toàn e mở rộng: ∑nH+ phản ứng = 2nO trong oxit + 2nH2 ⇒ nO trong oxit = 0,35 mol.
☆ Giải X + H2SO4: chú ý nFe > nH2 = 0,07 mol ⇒ nếu H2SO4 dùng dư thì Fe → Fe3+
⇒ 2nSO2↑ > 3nFe = 0,21 ⇒ trái giả thiết ⇒ H2SO4 hết.
⇒ Z gồm 3 chất tan là a mol FeSO4; b mol CuSO4 và c mol Fe2(SO4)3.
• bảo toàn e gián tiếp: ∑nSO42– trong muối = nSO2 + nO trong oxit = 0,45 mol.
⇒ a + b + 3c = 0,45 và có 0,45 mol BaSO4 trong chất rắn cuối cùng.
136,85 gam gồm 0,45 mol BaSO4 + (½a + c) mol Fe2O3 + b mol CuO.
⇒ 160 × (½a + c) + 80c + 0,45 × 233 = 136,85 ⇒ a + b + 2c = 0,4.
Vậy giải ra (a + b) = 0,3 và c = 0,05 mol.
Quay lại với yêu cầu ở dung dịch Y: gồm x mol FeCl2 + y mol CuCl2 + z mol FeCl3.
Bảo toàn nguyên tố Cl: ∑nCl– trong muối = 2x + 2y + 3z = 0,84.
Mà ∑nnguyên tố kim loại trong muối Y = ∑nnguyên tố kim loại trong muối Z
⇄ x + y + z = a + b + 2c = 0,4 ⇒ giải (x + y) = 0,36 và z = 0,04 mol.
► Đề cũng chỉ yêu cầu liên quan đến FeCl3 thôi (vì có hỏi FeCl2 hay CuCl2 thì cũng chưa đủ giả thiết để giải)
⇒ Yêu cầu C%mFeCl3 = 0,04 × 162,5 ÷ 250 × 100% = 2,60% ⇝ Chọn đáp án D. ♣
Câu 34 [184836]: Cho hơi nước đi qua than nung đỏ, thu được 0,735 mol hỗn hợp khí X (gồm CO, CO2 và H2). Cho toàn bộ X tác dụng hết với CuO (dư, nung nóng) thu được hỗn hợp chất rắn Y. Hòa tan hoàn toàn Y bằng dung dịch H2SO4 (đặc, nóng, dư) thu được 0,57 mol SO2 (sản phẩm khử duy nhất). Phần trăm thể tích của khí CO trong X là
A, 61,22%.
B, 22,45%.
C, 20,41%.
D, 16,33%.
Đáp án: D
Câu 35 [306156]: Hỗn hợp X gồm 0,08 mol vinyl axetilen; 0,06 mol axetilen; 0,06 mol propilen và 0,6 mol H2. Đun nóng hỗn hợp X có mặt Ni làm xúc tác một thời gian thu được hỗn hợp Y có tỉ khối so với He bằng 4,72. Lấy 0,75 mol hỗn hợp Y tác dụng vừa đủ V ml dung dịch Br2 1M. Giá trị của V là
A, 120.
B, 150.
C, 180.
D, 240.
HD: X gồm 0,08 mol C4H4; 0,06 mol C2H2; 0,06 mol C3H6 và 0,6 mol H2
||→ mX = 0,08 × 52 + 0,06 × 26 + 0,6 × 2 = 9,44 gam; nX = 0,8 mol; ∑nπ trong X = 0,42 mol.
♦ X –––to–→ Y ||→ mX = mY = 9,44 gam; mà MY = 4,72 × 4 = 18,88 → nY = 0,5 mol.
Theo đó, nH2 phản ứng = nX – nY = 0,3 mol. ♦ 1H2 phản ứng + 1π trong X
||→ ∑nπ trong Y = 0,42 – 0,3 = 0,12 mol. 1π + 1Br2 nên
nếu lấy 0,75 mol Y ⇄ tương ứng có 0,18 mol π thì nBr2 phản ứng = 0,18 mol
Vậy, yêu cầu V = 180 ml. Chọn đáp án C. ♣.
p/s: cần phản xạ + đánh dấu ở yêu cầu Y là giá trị khác (0,75 mol và 0,5 mol).
||→ mX = 0,08 × 52 + 0,06 × 26 + 0,6 × 2 = 9,44 gam; nX = 0,8 mol; ∑nπ trong X = 0,42 mol.
♦ X –––to–→ Y ||→ mX = mY = 9,44 gam; mà MY = 4,72 × 4 = 18,88 → nY = 0,5 mol.
Theo đó, nH2 phản ứng = nX – nY = 0,3 mol. ♦ 1H2 phản ứng + 1π trong X
||→ ∑nπ trong Y = 0,42 – 0,3 = 0,12 mol. 1π + 1Br2 nên
nếu lấy 0,75 mol Y ⇄ tương ứng có 0,18 mol π thì nBr2 phản ứng = 0,18 mol
Vậy, yêu cầu V = 180 ml. Chọn đáp án C. ♣.
p/s: cần phản xạ + đánh dấu ở yêu cầu Y là giá trị khác (0,75 mol và 0,5 mol).
Câu 36 [275384]: Cho E (C3H6O3) và F (C4H6O5) là các chất hữu cơ mạch hở. Trong phân tử chất F chứa đồng thời các nhóm -OH, -COO- và -COOH. Cho các chuyển hóa sau:
(1) E + NaOH → X + Y;
(2) F + NaOH → X + H2O;
(3) X + HCl → Z + NaCl.
Biết X, Y, Z là các hợp chất hữu cơ. Cho các phát biểu sau:
(a) Chất X có số nguyên tử oxi bằng số nguyên tử hiđro.
(b) Phân tử chất E chứa đồng thời nhóm -OH và nhóm -COOH.
(c) Trong công nghiệp, chất Y được điều chế trực tiếp từ etilen.
(d) Nhiệt độ sôi của chất Y nhỏ hơn nhiệt độ sôi của ancol etylic.
(đ) 1 mol chất Z tác dụng với Na dư thu được tối đa 1 mol khí H2.
Số phát biểu đúng là
(1) E + NaOH → X + Y;
(2) F + NaOH → X + H2O;
(3) X + HCl → Z + NaCl.
Biết X, Y, Z là các hợp chất hữu cơ. Cho các phát biểu sau:
(a) Chất X có số nguyên tử oxi bằng số nguyên tử hiđro.
(b) Phân tử chất E chứa đồng thời nhóm -OH và nhóm -COOH.
(c) Trong công nghiệp, chất Y được điều chế trực tiếp từ etilen.
(d) Nhiệt độ sôi của chất Y nhỏ hơn nhiệt độ sôi của ancol etylic.
(đ) 1 mol chất Z tác dụng với Na dư thu được tối đa 1 mol khí H2.
Số phát biểu đúng là
A, 4.
B, 3.
C, 5.
D, 2.
HD: (1) C3H6O3 + NaOH → X + Y ||⇒ cấu tạo E là HOCH2COOCH3 hoặc CH3COOCH2CH2OH hoặc HCOOCH2CHCH2OH (1 đồng phân dịch OH vào giữa nữa).
(2) F + NaOH → X + H2O ||⇒ F chứa nhóm chức axit COOH; 3O còn lại trong F thì có 2 trong chức este COOC và còn lại 1O trong nhóm OH nữa. Mà thủy phân F này thì chỉ thu được chất X và H2O ⇒ F là HOCH2COOCH2COOH ⇒ X là HOCH2COONa ⇒ E là HOCH2COOCH3 ⇒ Y là CH3OH. Từ X ⇒ Z là HOCH2COOH.
☆ Phân tích các phát biểu:
✔️ (a) đúng vì công thức phân tử X là C2H3O3Na đúng là số H = số O.
❌ (b) sai theo phân tích trên E là HOCH2COOCH3 không có nhóm COOH.
❌ (c) sai vì CH3OH không điều chế trực tiếp từ etilen CH2=CH2.
✔️ (d) đúng vì cùng dãy ancol thì số C tăng thì nhiệt độ sôi tăng ⇒ CH3OH có nhiệt độ sôi nhỏ hơn C2H5OH.
✔️ (đ) đúng vì 1HOCH2COOH + 2Na → NaOCH2COONa + 1H2↑.
⇝ có 3/5 phát biểu đúng ⇝ Chọn đáp án B. ♦
(2) F + NaOH → X + H2O ||⇒ F chứa nhóm chức axit COOH; 3O còn lại trong F thì có 2 trong chức este COOC và còn lại 1O trong nhóm OH nữa. Mà thủy phân F này thì chỉ thu được chất X và H2O ⇒ F là HOCH2COOCH2COOH ⇒ X là HOCH2COONa ⇒ E là HOCH2COOCH3 ⇒ Y là CH3OH. Từ X ⇒ Z là HOCH2COOH.
☆ Phân tích các phát biểu:
✔️ (a) đúng vì công thức phân tử X là C2H3O3Na đúng là số H = số O.
❌ (b) sai theo phân tích trên E là HOCH2COOCH3 không có nhóm COOH.
❌ (c) sai vì CH3OH không điều chế trực tiếp từ etilen CH2=CH2.
✔️ (d) đúng vì cùng dãy ancol thì số C tăng thì nhiệt độ sôi tăng ⇒ CH3OH có nhiệt độ sôi nhỏ hơn C2H5OH.
✔️ (đ) đúng vì 1HOCH2COOH + 2Na → NaOCH2COONa + 1H2↑.
⇝ có 3/5 phát biểu đúng ⇝ Chọn đáp án B. ♦
Câu 37 [9874]: Hỗn hợp X chứa 3 este mạch hở, trong phân tử chỉ chứa một loại nhóm chức và được tạo ra từ các axit cacboxylic có mạch không phân nhánh. Đốt cháy hoàn toàn 0,2 mol X cần dùng 0,52 mol O2, thu được 0,48 mol H2O. Đun nóng 24,96 gam X cần dùng 560 ml dung dịch NaOH 0,75M thu được hỗn hợp Y chứa các ancol có tổng khối lượng là 13,38 gam và hỗn hợp Z gồm hai muối, trong đó có a gam muối T và b gam muối E (MT < ME). Tỉ lệ a : b có giá trị gần nhất với giá trị nào sau đây?
A, 0,6
B, 1,2
C, 0,8
D, 1,4
Giải: ► GIẢ SỬ 24,96(g) X gấp k lần 0,2 mol X ⇒ 24,96(g) X ứng với 0,2k mol X
và đốt cần 0,52k mol O2 → sinh ra 0,48k mol H2O. Lại có:
nCOO = nNaOH = 0,42 mol. Bảo toàn nguyên tố Oxi: nCO2 = (0,42 + 0,28k) mol
● Bảo toàn khối lượng : 24,96 + 32 × 0,52k = 44 × (0,42 + 0,28k) + 18 × 0,48k
||⇒ k = 1,5 ⇒ Ctb = 0,84 ÷ 0,3 = 2,8 ⇒ X chứa HCOOCH3
► nCOO > nX || X tạo bởi các axit mạch không phân nhánh ⇒ X gồm este đơn chức và 2 chức
Đặt neste đơn chức = x; neste 2 chức = y ⇒ nX = x + y = 0,3 mol; nNaOH = x + 2y = 0,42 mol
||⇒ Giải hệ có: x = 0,18 mol; y = 0,12 mol ||► GIẢ SỬ X gồm 2 este đơn chức
⇒ Ctb (este đơn chức) > 2 ⇒ số C của este 2 chức < (0,84 – 0,18 × 2) ÷ 0,12 = 4
⇒ Vô lí vì este 2 chức nhỏ nhất là (COOCH3)2 và (HCOO)2C2H4 đều chức 4C
⇒ X gồm 1 este đơn chức và 2 este 2 chức. Mặt khác: trong X ta có
nC = nCO2 = 0,84 mol; nO = 2nCOO = 0,84 mol; Mà HCOOCH3 ≡ C2H4O2 có số C = số O
Và 2 este 2 chức còn lại có cùng số O ⇒ 2 este 2 chức có số C = số O = 4
||⇒ 2 este còn lại là (COOCH3)2 và (HCOO)2C2H4 ⇒ T là HCOONa và E là (COONa)2
► Đặt nHCOONa = z; n(COONa)2 = t ⇒ nNaOH = z + 2t = 0,42 mol.
Bảo toàn khối lượng: mZ = 68z + 134t = 24,96 + 0,42 × 40 – 13,38
||⇒ Giải hệ có: z = 0,24 mol; t = 0,09 mol ⇒ a : b = 68z : 134t = 1,35 ⇒ Chọn D
và đốt cần 0,52k mol O2 → sinh ra 0,48k mol H2O. Lại có:
nCOO = nNaOH = 0,42 mol. Bảo toàn nguyên tố Oxi: nCO2 = (0,42 + 0,28k) mol
● Bảo toàn khối lượng : 24,96 + 32 × 0,52k = 44 × (0,42 + 0,28k) + 18 × 0,48k
||⇒ k = 1,5 ⇒ Ctb = 0,84 ÷ 0,3 = 2,8 ⇒ X chứa HCOOCH3
► nCOO > nX || X tạo bởi các axit mạch không phân nhánh ⇒ X gồm este đơn chức và 2 chức
Đặt neste đơn chức = x; neste 2 chức = y ⇒ nX = x + y = 0,3 mol; nNaOH = x + 2y = 0,42 mol
||⇒ Giải hệ có: x = 0,18 mol; y = 0,12 mol ||► GIẢ SỬ X gồm 2 este đơn chức
⇒ Ctb (este đơn chức) > 2 ⇒ số C của este 2 chức < (0,84 – 0,18 × 2) ÷ 0,12 = 4
⇒ Vô lí vì este 2 chức nhỏ nhất là (COOCH3)2 và (HCOO)2C2H4 đều chức 4C
⇒ X gồm 1 este đơn chức và 2 este 2 chức. Mặt khác: trong X ta có
nC = nCO2 = 0,84 mol; nO = 2nCOO = 0,84 mol; Mà HCOOCH3 ≡ C2H4O2 có số C = số O
Và 2 este 2 chức còn lại có cùng số O ⇒ 2 este 2 chức có số C = số O = 4
||⇒ 2 este còn lại là (COOCH3)2 và (HCOO)2C2H4 ⇒ T là HCOONa và E là (COONa)2
► Đặt nHCOONa = z; n(COONa)2 = t ⇒ nNaOH = z + 2t = 0,42 mol.
Bảo toàn khối lượng: mZ = 68z + 134t = 24,96 + 0,42 × 40 – 13,38
||⇒ Giải hệ có: z = 0,24 mol; t = 0,09 mol ⇒ a : b = 68z : 134t = 1,35 ⇒ Chọn D
Câu 38 [26103]: Cho các phát biểu sau:
(a) Trong môi trường kiềm, các peptit đều có phản ứng màu biure.
(b) Poliacrilonitrin được dùng để sản xuất tơ tổng hợp.
(c) Etanol được dùng để sản xuất xăng E5 với 5% thể tích.
(d) Các amino axit đều có tính chất lưỡng tính.
(e) Các chất béo đều bị thủy phân tạo thành glixerol.
Số phát biểu đúng là
(a) Trong môi trường kiềm, các peptit đều có phản ứng màu biure.
(b) Poliacrilonitrin được dùng để sản xuất tơ tổng hợp.
(c) Etanol được dùng để sản xuất xăng E5 với 5% thể tích.
(d) Các amino axit đều có tính chất lưỡng tính.
(e) Các chất béo đều bị thủy phân tạo thành glixerol.
Số phát biểu đúng là
A, 5.
B, 2.
C, 3.
D, 4.
HD: Xem xét - phân tích các phát biểu:
(a) sai vì đipeptit không có phản ứng màu biure.
(b) đúng Poliacrilonitrin sản xuất tơ nitrin (tơ olon).
(c) đúng. Xem lại bookID = 311953
(d) đúng. Phân tử amino axit chứa đồng thời nhóm COOH và NH2.
(e) đúng. Chất béo là trieste của glixerol và axit béo. ❒
(a) sai vì đipeptit không có phản ứng màu biure.
(b) đúng Poliacrilonitrin sản xuất tơ nitrin (tơ olon).
(c) đúng. Xem lại bookID = 311953
(d) đúng. Phân tử amino axit chứa đồng thời nhóm COOH và NH2.
(e) đúng. Chất béo là trieste của glixerol và axit béo. ❒
Câu 39 [184841]: Cho m gam hỗn hợp X ( gồm Na, Na2O, Ba và BaO) vào H2O dư, thu được dung dịch Y và 0,06 mol H2. Sục từ từ đến hết 0,12 mol CO2 vào Y, thu được dung dịch Z và kết tủa BaCO3. Sự phụ thuộc của số mol kết tủa BaCO3 (a mol) vào số mol CO2 (b mol) được biểu diễn theo đồ thị bên.

Cho từ từ đến hết Z vào 30 ml dung dịch HCl 1M, thu được 0,02 mol CO2. Biết các phản ứng đều xảy ra hoàn toàn. Giá trị của m là

Cho từ từ đến hết Z vào 30 ml dung dịch HCl 1M, thu được 0,02 mol CO2. Biết các phản ứng đều xảy ra hoàn toàn. Giá trị của m là
A, 8,24.
B, 5,00.
C, 8,88.
D, 7,64.
Đáp án: C
Câu 40 [352290]: Cao su lưu hóa được tạo thành do việc trộn cao su thiên nhiên (poliisopren) với các thành phần khác nhau, trong đó có lưu huỳnh để tạo thành một tổ hợp. Sau đó đem lưu hóa để tạo thành cao su. Trong cao su lưu hóa có chứa 2% lưu huỳnh về khối lượng, biết rằng cứ một khoảng số lượng mắt xích nhất định thì sẽ xuất hiện 1 cầu nối đisunfua -S-S- và tại đó, 2 nguyên tử lưu huỳnh sẽ thay thế 2 nguyên tử hidro trong một mắt xích.
Cho các phát biểu sau:
(a) Cao su lưu hóa là polime thiên nhiên.
(b) Khoảng 46 mắt xích isopren sẽ có một cầu nối đisunfua -S-S-
(c) Cao su lưu hóa có tính đàn hồi, chịu nhiệt, lâu mòn hơn cao su thường.
(d) Phản ứng tổng hợp cao su lưu hóa từ cao su thiên nhiên là phản ứng trùng ngưng.
Số phát biểu đúng là
Cho các phát biểu sau:
(a) Cao su lưu hóa là polime thiên nhiên.
(b) Khoảng 46 mắt xích isopren sẽ có một cầu nối đisunfua -S-S-
(c) Cao su lưu hóa có tính đàn hồi, chịu nhiệt, lâu mòn hơn cao su thường.
(d) Phản ứng tổng hợp cao su lưu hóa từ cao su thiên nhiên là phản ứng trùng ngưng.
Số phát biểu đúng là
A, 2.
B, 4.
C, 3.
D, 1.
HD: Lưu hóa cao su:

☆ Phân tích các phát biểu:
❌ (a) sai vì tác động vào polime thiên nhiên → cao su lưu hóa thì đây là polime nhân tạo hay bán tổng hợp.
✔️ (b) đúng vì giả sử nC5H8 thì mất 2H thay bằng cầu nối -S-S- → tạo C5nH8n – 2S2 có tỉ lệ %S = 2% ⇒ 64 : (68n + 62) × 100% = 2% ⇒ n = 43.
✔️ (c) đúng theo tính chất và giá trị của việc lưu hóa cao su.
❌ (d) sai vì chú ý phản ứng trùng ngưng là một quá trình nhiều phân tử nhỏ (monome) liên kết với nhau thành phân tử lớn (polime cao phân tử) đồng thời giải phóng nhiều phần tử nhỏ như H2O, HCl, CO2. Ở đây kết hợp polime + lưu huỳnh nên không thỏa mãn định nghĩa.
⇝ có 2/4 phát biểu đúng ⇝ Chọn đáp án A. ♥

☆ Phân tích các phát biểu:
❌ (a) sai vì tác động vào polime thiên nhiên → cao su lưu hóa thì đây là polime nhân tạo hay bán tổng hợp.
✔️ (b) đúng vì giả sử nC5H8 thì mất 2H thay bằng cầu nối -S-S- → tạo C5nH8n – 2S2 có tỉ lệ %S = 2% ⇒ 64 : (68n + 62) × 100% = 2% ⇒ n = 43.
✔️ (c) đúng theo tính chất và giá trị của việc lưu hóa cao su.
❌ (d) sai vì chú ý phản ứng trùng ngưng là một quá trình nhiều phân tử nhỏ (monome) liên kết với nhau thành phân tử lớn (polime cao phân tử) đồng thời giải phóng nhiều phần tử nhỏ như H2O, HCl, CO2. Ở đây kết hợp polime + lưu huỳnh nên không thỏa mãn định nghĩa.
⇝ có 2/4 phát biểu đúng ⇝ Chọn đáp án A. ♥