Đáp án
1D
2D
3A
4D
5D
6D
7C
8B
9B
10A
11A
12C
13D
14C
15D
16A
17A
18C
19D
20C
21B
22C
23D
24A
25C
26B
27C
28C
29B
30D
31D
32D
33C
34B
35C
36D
37D
38D
39B
40A
Đáp án Đề minh họa số 12 thi Tốt Nghiệp Trung học Phổ Thông 2024 môn Hóa học
Câu 1 [911587]: Ở nhiệt độ thường, kim loại Fe phản ứng được với dung dịch
A, FeCl2.
B, NaCl.
C, MgCl2.
D, CuCl2.
HD: Thứ tự các kim loại trong dãy điện hoá: Na > Mg > Fe > Cu.
⇒ Fe đẩy được muối đồng để thu được kim loại Cu tương ứng.
Phản ứng: Fe + CuCl2 → FeCl2 + Cu.
⇒ Fe đẩy được muối đồng để thu được kim loại Cu tương ứng.
Phản ứng: Fe + CuCl2 → FeCl2 + Cu.
Câu 2 [60303]: Nhôm (Al) khử được ion kim loại của muối nào sau đây trong dung dịch?
A, NaNO3.
B, Ba(NO3)2.
C, Mg(NO3)2.
D, Fe(NO3)2.
HD: Thứ tự dãy điện hoá: 
⇒ Al chỉ khử được ion Fe2+ trong muối Fe(NO3)2:
2Al + 3Fe(NO3)2 → 2Al(NO3)3 + 3Fe ⇝ Chọn đáp án D. ♠

⇒ Al chỉ khử được ion Fe2+ trong muối Fe(NO3)2:
2Al + 3Fe(NO3)2 → 2Al(NO3)3 + 3Fe ⇝ Chọn đáp án D. ♠
Câu 3 [24148]: Peptit X có công thức cấu tạo Gly-Ala-Gly-Glu có số liên kết peptit là
A, 3.
B, 2.
C, 5.
D, 4.
HD: Giữa phân tử Gly-Ala-Gly-Glu có 3 gạch "–" chính là 3 liên kết peptit ⇝ Chọn đáp án A. ♥
Câu 4 [352916]: Cho thanh kim loại Cu vào dung dịch chất nào sau đây sẽ xảy ra hiện tượng ăn mòn điện hóa học?
A, FeCl3.
B, FeCl2.
C, ZnSO4.
D, AgNO3.
Đáp án: D
Câu 5 [60084]: Chất nào sau đây tác dụng với Ba(OH)2 tạo kết tủa?
A, NaCl.
B, KNO3.
C, KCl.
D, Ba(HCO3)2.
HD:
OH– + HCO3– → CO32– + H2O.
CO32– + Ba2+ → BaCO3.
Vậy Ba(HCO3)2 tác dụng với Ba(OH)2 tạo kết tủa.
OH– + HCO3– → CO32– + H2O.
CO32– + Ba2+ → BaCO3.
Vậy Ba(HCO3)2 tác dụng với Ba(OH)2 tạo kết tủa.
Câu 6 [982244]: Cho Fe(OH)2 phản ứng với dung dịch H2SO4 loãng dư, tạo ra muối nào sau đây?
A, FeS.
B, FeSO3
C, Fe2(SO4)3.
D, FeSO4.
HD: Phản ứng: Fe(OH)2 + H2SO4 loãng → FeSO4 + 2H2O.
► Nếu sử dụng H2SO4 đặc nóng thì xảy ra phản ứng oxi hoá khử:
2Fe(OH)2 + 4H2SO4 → Fe2(SO4)3 + SO2↑ + 6H2O.
► Nếu sử dụng H2SO4 đặc nóng thì xảy ra phản ứng oxi hoá khử:
2Fe(OH)2 + 4H2SO4 → Fe2(SO4)3 + SO2↑ + 6H2O.
Câu 7 [59858]: Công thức chung của oxit kim loại thuộc nhóm IA là
A, R2O3.
B, RO2.
C, R2O.
D, RO.
HD Kim loại thuộc nhóm IA có 1 electron ở lớp ngoài cùng → Oxit kim loại thuộc nhóm IA là R2O → Đáp án đúng là đáp án C
Câu 8 [679435]: Etyl propionat là este có mùi thơm của dứa. Công thức của etyl propionat là
A, HCOOC2H5.
B, C2H5COOC2H5.
C, C2H5COOCH3.
D, CH3COOCH3.

Este etyl butirat (C3H7COOC2H5) và etyl propionat (C2H5COOC2H5) có mùi thơm của dứa.
Câu 9 [679603]: Kim loại nào sau đây được điều chế bằng phương pháp điện phân nóng chảy?
A, Fe.
B, Na.
C, Cu.
D, Ag.
HD: Bài học điện phân điều chế kim loại:
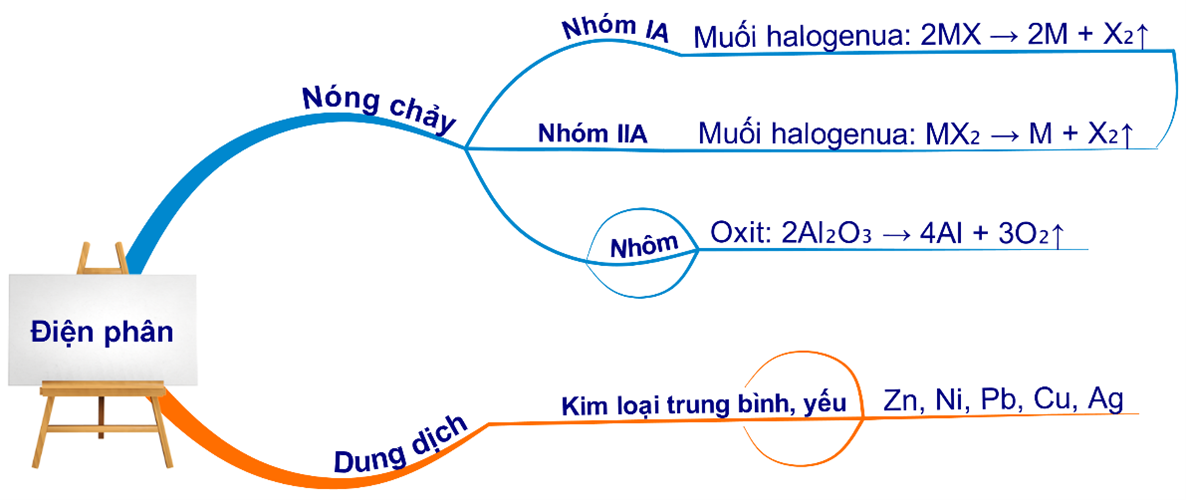
⇝ Na được điều chế bằng cách điện phân nóng chảy.

⇝ Na được điều chế bằng cách điện phân nóng chảy.
Câu 10 [679841]: Chất nào sau đây có phản ứng trùng hợp?
A, Etilen.
B, Etylen glicol.
C, Etylamin.
D, Axit axetic.
HD: Phân tích các đáp án:
⇒ chỉ có etilen cấu tạo có nối đôi C=C có khả năng trùng hợp để tạo polime tương ứng là polietilen (PE) ⇝ Chọn đáp án A. ♥
| Hợp chất | A. Etilen. | B. Etylen glicol. | C. Etylamin. | D. Axit axetic. |
| Cấu tạo | CH2=CH2 | HOCH2CH2OH | CH3CH2OH | CH3COOH |
Câu 11 [901467]: Chất nào sau đây là muối trung hòa?
A, NH4NO3.
B, NH4HCO3.
C, KHSO4.
D, KHCO3.
HD: Phân loại muối:
• Muối trung hòa là muối mà anion gốc axit không còn hiđro có khả năng phân li ra H+ (hiđro có tính axit). Ví dụ: NaCl; (CH3COO)2Ca; (NH4)2SO4;...
• Muối axit là muối vẫn còn hiđro có khả năng phân li ra H+. Ví dụ: NaHCO3; KHSO4; NaH2PO4; K2HPO4;...
⇒ NH4HCO3; KHSO4 và KHCO3 là các muối axit; chỉ có NH4NO3 là muối trung hoà ⇝ Chọn đáp án A. ♥
• Muối trung hòa là muối mà anion gốc axit không còn hiđro có khả năng phân li ra H+ (hiđro có tính axit). Ví dụ: NaCl; (CH3COO)2Ca; (NH4)2SO4;...
• Muối axit là muối vẫn còn hiđro có khả năng phân li ra H+. Ví dụ: NaHCO3; KHSO4; NaH2PO4; K2HPO4;...
⇒ NH4HCO3; KHSO4 và KHCO3 là các muối axit; chỉ có NH4NO3 là muối trung hoà ⇝ Chọn đáp án A. ♥
Câu 12 [59816]: Ở nhiệt độ thường, nitơ phản ứng được với kim loại nào sau đây?
A, Mg.
B, Al.
C, Li.
D, Na.
HD: Ở nhiệt độ thường, nitơ phản ứng được với kim loại Li:
6Li + N2 → 2Li3N. ❒
6Li + N2 → 2Li3N. ❒
Câu 13 [61643]: Khi làm thí nghiệm với H2SO4 đặc, nóng thường sinh ra khí SO2. Để hạn chế tốt nhất khí SO2 thoát ra gây ô nhiễm môi trường, người ta nút ống nghiệm bằng bông tẩm dung dịch nào sau đây?
A, Cồn.
B, Giấm ăn.
C, Muối ăn.
D, Xút.
HD: SO2 là oxit axit, phản ứng được với xút tạo muối:
SO2 + NaOH → NaHSO3.
⇒ bông tẩm xút sẽ hạn chế khí SO2 thoát ra môi trường trong quá trình làm thí nghiệm. ❒
SO2 + NaOH → NaHSO3.
⇒ bông tẩm xút sẽ hạn chế khí SO2 thoát ra môi trường trong quá trình làm thí nghiệm. ❒
Câu 14 [20862]: Trong phân tử triolein có bao nhiêu liên kết C=O?
A, 6.
B, 2.
C, 3.
D, 4.
HD: triolein là chất béo ⇝ là triglixerit, là trieste, chứa 3 nhóm COO
⇒ phân tử triolein chứa 3 liên kết C=O (3πC=O). ❒
⇒ phân tử triolein chứa 3 liên kết C=O (3πC=O). ❒
Câu 15 [60682]: Kim loại phổ biến nhất trong vỏ trái đất là
A, Sắt, Fe.
B, Crom, Cr.
C, Đồng, Cu.
D, Nhôm, Al.
Kim loại phổ biến nhất trong vỏ trái đất là Al chiếm khoảng 1/3 số kim loại trong vỏ trái đất
Đáp án D.
Đáp án D.
Câu 16 [341040]: Số nguyên tử hiđro (H) trong phân tử etylen glicol là
A, 8.
B, 6.
C, 4.
D, 10.
HD:
CTPT của etylen glicol là C2H4(OH)2 hay C2H6O2.
Vậy có 6 nguyên tử hiđro (H) trong phân tử etylen glicol. Chọn A.
CTPT của etylen glicol là C2H4(OH)2 hay C2H6O2.
Vậy có 6 nguyên tử hiđro (H) trong phân tử etylen glicol. Chọn A.
Câu 17 [17080]: Cho vài giọt phenolphtalein vào dung dịch etylamin thì dung dịch chuyển thành
A, màu hồng.
B, màu đỏ.
C, màu tím.
D, màu xanh.
HD: Phân tích:
![572247[LG].png](https://m.moon.vn/Images/Teachers/rongden_167/ProS2018/TAP%20II/572247[LG].png)
⇝ vài giọt phenolphtalein cho vào dung dịch etylamin thì chuyển thành màu hồng. ❒
![572247[LG].png](https://m.moon.vn/Images/Teachers/rongden_167/ProS2018/TAP%20II/572247[LG].png)
⇝ vài giọt phenolphtalein cho vào dung dịch etylamin thì chuyển thành màu hồng. ❒
Câu 18 [679313]: Crom có số oxi hóa +6 trong hợp chất nào sau đây?
A, NaCrO2.
B, Cr2O3.
C, K2Cr2O7.
D, CrSO4.

Câu 19 [982278]: Kim loại nào sau đây tác dụng với H2O ở nhiệt độ thường?
A, Cu.
B, Au.
C, Ag.
D, Ba.
HD: Bài học về kim loại tác dụng với nước:

⇒ đáp án thoả mãn là D. Ba. Phản ứng: Ba + 2H2O → Ba(OH)2 + H2↑.

⇒ đáp án thoả mãn là D. Ba. Phản ứng: Ba + 2H2O → Ba(OH)2 + H2↑.
Câu 20 [973513]: Dung dịch nào sau đây có phản ứng tráng bạc?
A, Metyl axetat.
B, Glyxin.
C, Fructozơ.
D, Saccarozơ.
HD: trong môi trường bazơ (do có NH3), fructozơ chuyển hoá thành glucozơ ⇝ có phản ứng tráng bạc, sơ đồ:

Câu 21 [311813]: Hoà tan m gam hỗn hợp gồm KHCO3 và CaCO3 trong lượng dư dung dịch HCl. Sau khi các phản ứng xảy ra hoàn toàn, thu được 11,2 lít khí CO2 (đktc). Giá trị của m là
A, 40
B, 50
C, 60
D, 100
Giải: Vì MKHCO3 = MCaCO3 = 100
BT cacbon ⇒ nKHCO3 + nCaCO3 = nCO2 = 0,5 mol
⇒ m = 0,5 × 100 = 50 gam ⇒ Chọn B
BT cacbon ⇒ nKHCO3 + nCaCO3 = nCO2 = 0,5 mol
⇒ m = 0,5 × 100 = 50 gam ⇒ Chọn B
Câu 22 [20399]: Phát biểu nào sau đây là sai?
A, Tơ visco là tơ bán tổng hợp.
B, Tơ xenlulozơ triaxetat là tơ hóa học.
C, Tơ nilon-6,6 là tơ nhân tạo.
D, Sợi bông, tơ tằm đều là tơ thiên nhiên.
HD:
![577864[LG].png](https://m.moon.vn/Images/Teachers/rongden_167/ProS2018/TAP%20II/577864[LG].png)
⇒ nilon-6,6 thuộc loại tơ tổng hợp → chọn đáp án C. ♣.
![577864[LG].png](https://m.moon.vn/Images/Teachers/rongden_167/ProS2018/TAP%20II/577864[LG].png)
⇒ nilon-6,6 thuộc loại tơ tổng hợp → chọn đáp án C. ♣.
Câu 23 [352917]: Thí nghiệm nào sau đây không xảy ra phản ứng hóa học?
A, Sục khí H2SO4 vào dung dịch Ba(NO3)2.
B, Cho CaO vào H2O.
C, Cho Na2CO3 vào dung dịch CH3COOH.
D, Sục khí CO2 vào dung dịch Al(OH)3.
Đáp án: D
Câu 24 [12053]: Cho m gam glucozơ lên men thành ancol etylic, thu được 5,6 lít CO2 (đktc). Giá trị của m là
A, 22,50.
B, 45,00.
C, 11,25.
D, 14,40.
Giải: 1Glucozơ → 2C2H5OH + 2CO2
||⇒ m = 5,6 ÷ 22,4 ÷ 2 × 180 = 22,5 gam ⇒ chọn A.
||⇒ m = 5,6 ÷ 22,4 ÷ 2 × 180 = 22,5 gam ⇒ chọn A.
Câu 25 [310924]: Để trung hòa 25 gam dung dịch của một amin đơn chức X nồng độ 12,4% cần dùng 100 ml dung dịch HCl 1M. Công thức phân tử của X là
A, C3H5N.
B, C2H7N.
C, CH5N.
D, C3H7N.
HD: Ta có mX = 25 × 0,124 = 3,1 gam.
X là amin đơn chức nên X + HCl → X(HCl).
Giả thiết nHCl = 0,1 mol ⇒ nX = 0,1 mol ⇒ MX = 3,1 : 0,1 = 31
|⇝ Tương ứng công thức phân tử của amin X là CH5N (metylamin). ❒
X là amin đơn chức nên X + HCl → X(HCl).
Giả thiết nHCl = 0,1 mol ⇒ nX = 0,1 mol ⇒ MX = 3,1 : 0,1 = 31
|⇝ Tương ứng công thức phân tử của amin X là CH5N (metylamin). ❒
Câu 26 [12321]: Thuỷ phân hoàn toàn tinh bột trong dung dịch axit vô cơ loãng, thu được chất hữu cơ X. Cho X phản ứng với khí H2 (xúc tác Ni, to), thu được chất hữu cơ Y. Các chất X, Y lần lượt là
A, glucozơ, etanol.
B, glucozơ, sobitol.
C, glucozơ, fructozơ.
D, glucozơ, saccarozơ.
HD: Các phản ứng hóa học xảy ra theo sơ đồ:
![567153[LG2].png](https://m.moon.vn/Images/Teachers/rongden_167/ProS2018/TAP%20II/567153[LG2].png)
![567312[LG].png](https://m.moon.vn/Images/Teachers/rongden_167/ProS2018/TAP%20II/567312[LG].png)
⇝ Tương ứng các chất X là glucozơ và Y là sobitol. ❒
![567153[LG2].png](https://m.moon.vn/Images/Teachers/rongden_167/ProS2018/TAP%20II/567153[LG2].png)
⇝ Tương ứng các chất X là glucozơ và Y là sobitol. ❒
Câu 27 [352918]: Đốt cháy m gam kim loại M (có hóa trị không đổi) trong 3,36 lít khí O2 đến phản ứng hoàn toàn được 12,9 gam chất rắn X. Hòa tan hết X trong dung dịch H2SO4 dư thu được 0,84 lít khí H2. Các thể tích khí đều đo ở đktc, kim loại M là
A, Ca.
B, Zn.
C, Mg.
D, Al.
Đáp án: C
Câu 28 [339250]: Xà phòng hoá hỗn hợp gồm CH3COOCH3 và CH3COOC2H5 thu được sản phẩm gồm:
A, hai muối và hai rượu
B, hai muối và một rượu
C, một muối và hai rượu
D, một muối và một rượu
Đáp án: C
Câu 29 [981939]: Hòa tan Fe3O4 bằng lượng vừa đủ dung dịch H2SO4 loãng, thu được dung dịch X. Có bao nhiêu chất khi cho vào X thì xảy ra phản ứng hóa học trong các chất: NaOH, Ag, Ba(NO3)2, NaCl?
A, 3.
B, 2.
C, 1.
D, 4.
HD: Phản ứng: Fe3O4 + 4H2SO4 → Fe2(SO4)3 + FeSO4 + 4H2O.
axit dùng vừa đủ nên X thu được chỉ chứa muối: Fe2(SO4)3 và FeSO4.
Các chất có phản ứng với dung dịch thu được gồm:
• NaOH: Fe2+ + 2OH– → Fe(OH)2↓ và Fe3+ + 3OH– → Fe(OH)3↓.
• Ba(NO3)2: Ba2+ + SO42+ → BaSO4↓
Ag và NaCl không có phản ứng xảy ra ⇝ 2/4 chất thoả mãn ⇝ Chọn đáp án B. ♦
axit dùng vừa đủ nên X thu được chỉ chứa muối: Fe2(SO4)3 và FeSO4.
Các chất có phản ứng với dung dịch thu được gồm:
• NaOH: Fe2+ + 2OH– → Fe(OH)2↓ và Fe3+ + 3OH– → Fe(OH)3↓.
• Ba(NO3)2: Ba2+ + SO42+ → BaSO4↓
Ag và NaCl không có phản ứng xảy ra ⇝ 2/4 chất thoả mãn ⇝ Chọn đáp án B. ♦
Câu 30 [352948]: Cho m gam este E có công thức phân tử C3H6O2 tác dụng với 200 ml dung dịch KOH 0,7M, sau phản ứng cô cạn dung dịch thu được 12,04 gam chất rắn khan. Giá trị của m là
A, 7,20.
B, 10,36.
C, 10,56.
D, 7,40.
Đáp án: D
Câu 31 [275050]: Cho các phát biểu sau:
(a) Isoamyl axetat có mùi thơm của chuối chín.
(b) Lưu hóa cao su buna thu được cao su buna-S.
(c) Đun nóng mỡ lợn với dung dịch NaOH đặc, thu được xà phòng.
(d) Nhỏ vài giọt dung dịch I2 vào lát cắt của củ khoai lang xuất hiện màu xanh tím.
(đ) Nhỏ dung dịch Gly-Val vào ống nghiệm chứa Cu(OH)2 xuất hiện hợp chất màu tím.
Số phát biểu đúng là
(a) Isoamyl axetat có mùi thơm của chuối chín.
(b) Lưu hóa cao su buna thu được cao su buna-S.
(c) Đun nóng mỡ lợn với dung dịch NaOH đặc, thu được xà phòng.
(d) Nhỏ vài giọt dung dịch I2 vào lát cắt của củ khoai lang xuất hiện màu xanh tím.
(đ) Nhỏ dung dịch Gly-Val vào ống nghiệm chứa Cu(OH)2 xuất hiện hợp chất màu tím.
Số phát biểu đúng là
A, 5.
B, 4.
C, 2.
D, 3.
HD: Phân tích các phát biểu:
✔️ (a) đúng, xem lại bài học mùi este.
❌ (b) sai, lưu hóa cao su thì thu được cao su lưu hóa, còn cao su buna-S là đồng trùng hợp butađien và stiren (S này là viết tắt của Stiren chứ không phải S lưu huỳnh).
✔️ (c) đúng, mỡ lợn có thành phần chất béo, thủy phân thu được muối natri của axit béo là xà phòng.
✔️ (d) đúng, lát cắt khoai chứa tinh bột sẽ phản ứng màu với I2 → màu xanh tím.
❌ (đ) sai vì Gly-Val là đipeptit không có phản ứng màu biure nên không xuất hiện màu tím đặc trưng.
⇝ có 3/5 phát biểu đúng ⇝ Chọn đáp án D. ♠
✔️ (a) đúng, xem lại bài học mùi este.
❌ (b) sai, lưu hóa cao su thì thu được cao su lưu hóa, còn cao su buna-S là đồng trùng hợp butađien và stiren (S này là viết tắt của Stiren chứ không phải S lưu huỳnh).
✔️ (c) đúng, mỡ lợn có thành phần chất béo, thủy phân thu được muối natri của axit béo là xà phòng.
✔️ (d) đúng, lát cắt khoai chứa tinh bột sẽ phản ứng màu với I2 → màu xanh tím.
❌ (đ) sai vì Gly-Val là đipeptit không có phản ứng màu biure nên không xuất hiện màu tím đặc trưng.
⇝ có 3/5 phát biểu đúng ⇝ Chọn đáp án D. ♠
Câu 32 [973610]: Tiến hành các thí nghiệm sau:
(a) Đốt dây Mg trong không khí.
(b) Sục khí Cl2 vào dung dịch FeSO4.
(c) Cho dung dịch H2SO4 loãng vào dung dịch Fe(NO3)2.
(d) Cho Br2 vào dung dịch hỗn hợp NaCrO2 và NaOH.
(e) Sục khí CO2 vào dung dịch Ca(OH)2.
(g) Đun sôi dung dịch Ca(HCO3)2.
Số thí nghiệm xảy ra phản ứng oxi hóa-khử là
(a) Đốt dây Mg trong không khí.
(b) Sục khí Cl2 vào dung dịch FeSO4.
(c) Cho dung dịch H2SO4 loãng vào dung dịch Fe(NO3)2.
(d) Cho Br2 vào dung dịch hỗn hợp NaCrO2 và NaOH.
(e) Sục khí CO2 vào dung dịch Ca(OH)2.
(g) Đun sôi dung dịch Ca(HCO3)2.
Số thí nghiệm xảy ra phản ứng oxi hóa-khử là
A, 3.
B, 5.
C, 2.
D, 4.
HD: Phân tích các thí nghiệm, phản ứng xảy ra:
✔️ (a) 2Mg + O2 ––to→ 2MgO.
✔️ (b) 3Cl2 + 6FeSO4 → 2Fe2(SO4)3 + 2FeCl3.
✔️ (c) 3Fe2+ + 4H+ + NO3– → 3Fe3+ + NO + 2H2O.
✔️ (d) 3Br2 + 2NaCrO2 + 8NaOH → 2Na2CrO4 + 6NaBr + 4H2O.
❌ (e) CO2 + Ca(OH)2 → CaCO3↓ + H2O.
❌ (g) Ca(HCO3)2 ––to→ CaCO3↓ + CO2↑ + H2O.
⇝ có 4/6 thí nghiệm xảy ra phản ứng oxi - hoá khử ⇝ Chọn đáp án D. ♠
✔️ (a) 2Mg + O2 ––to→ 2MgO.
✔️ (b) 3Cl2 + 6FeSO4 → 2Fe2(SO4)3 + 2FeCl3.
✔️ (c) 3Fe2+ + 4H+ + NO3– → 3Fe3+ + NO + 2H2O.
✔️ (d) 3Br2 + 2NaCrO2 + 8NaOH → 2Na2CrO4 + 6NaBr + 4H2O.
❌ (e) CO2 + Ca(OH)2 → CaCO3↓ + H2O.
❌ (g) Ca(HCO3)2 ––to→ CaCO3↓ + CO2↑ + H2O.
⇝ có 4/6 thí nghiệm xảy ra phản ứng oxi - hoá khử ⇝ Chọn đáp án D. ♠
Câu 33 [276559]: Để bón cho một loại cây phát triển tốt thì giai đoạn bón thúc cần dùng phân thích hợp NPK 4-12-7. Tỉ lệ khối lượng các mẫu (NH4)2SO4, Ca(H2PO4)2 và KCl cần trộn xấp xỉ với tỉ lệ nào sau đây?
A, 1,78 : 1,7 : 1.
B, 1,8 : 1,77 : 1.
C, 1,7 : 1,78 : 1.
D, 2 : 2 : 1.
HD: ► Nhận xét: mỗi mẫu chất cần lấy chỉ có đúng 1 thành phần dinh dưỡng ⇝ bài toán dễ.
Quan sát 4 đáp án, tỉ lệ mKCl được chọn luôn là 1 nên để thuận lợi ta lấy mKCl = 1 gam.
⇒ nKCl = 1/74,5 mol ⇒ mK2O = 94/149 gam.
Lại có phân NPK loại 4-12-7 ⇒ mphân NPK = 94/149 ÷ 0,07 = 9400/1043 gam.
Từ đó: %mN trong NPK = 4% × 9400/1043 ⇒ nN = Ans ÷ 14
⇒ m(NH4)2SO4 = Ans ÷ 2 × 132 = 1,7 gam.
%mP2O5 = 12% × 9400/1043 ⇒ nCa(H2PO4)2 = Ans ÷ 142
⇒ mCa(H2PO4)2 = Ans × 234 = 1,78 gam.
⇒ Yêu cầu tỉ lệ cần trộn là 1,7 : 1,78 : 1 ⇝ Chọn đáp án C. ♣
Quan sát 4 đáp án, tỉ lệ mKCl được chọn luôn là 1 nên để thuận lợi ta lấy mKCl = 1 gam.
⇒ nKCl = 1/74,5 mol ⇒ mK2O = 94/149 gam.
Lại có phân NPK loại 4-12-7 ⇒ mphân NPK = 94/149 ÷ 0,07 = 9400/1043 gam.
Từ đó: %mN trong NPK = 4% × 9400/1043 ⇒ nN = Ans ÷ 14
⇒ m(NH4)2SO4 = Ans ÷ 2 × 132 = 1,7 gam.
%mP2O5 = 12% × 9400/1043 ⇒ nCa(H2PO4)2 = Ans ÷ 142
⇒ mCa(H2PO4)2 = Ans × 234 = 1,78 gam.
⇒ Yêu cầu tỉ lệ cần trộn là 1,7 : 1,78 : 1 ⇝ Chọn đáp án C. ♣

Câu 34 [281751]: Hỗn hợp E gồm 2 triglixerit X và Y (biết MY>MX>820). Cho m gam E tác dụng với dung dịch NaOH (vừa đủ), thu được glixerol và hỗn hợp gồm ba muối natri panmitat, natri oleat và natri stearat theo tỉ lệ mol lần lượt là 2:2:1. Mặt khác, cho m gam E tác dụng hết với H2 (xúc tác Ni, to) thu được 42,82 gam hỗn hợp G. Phần trăm khối lượng của X trong E gần nhất với giá trị nào sau đây?
A, 63.
B, 59.
C, 37.
D, 41.
Đáp án: B
Câu 35 [276494]: Một mẫu cồn X (thành phần chính là C2H5OH) có lẫn metanol (CH3OH). Khi được đốt cháy hoàn toàn, 1 mol CH3OH tỏa ra lượng nhiệt là 716 kJ và 1 mol C2H5OH tỏa ra lượng nhiệt là 1370 kJ. Tiến hành đốt cháy 10 gam cồn X thấy toả ra nhiệt lượng 291,9 kJ. Xác định phần trăm khối lượng tạp chất metanol trong X.
A, 9,6%.
B, 6,4%.
C, 8,0%.
D, 11,2%.
HD: Giả sử 10 gam cồn X gồm a mol CH3OH và b mol C2H5OH ⇒ 32a + 46b = 10.
Theo giả thiết, ta có:
• Đốt a mol CH3OH tỏa ra nhiệt lượng là 716a kJ.
• Đốt b mol C2H5OH tỏa ra nhiệt lượng là 1370b kJ.
⇒ Tổng nhiệt lượng tỏa ra khi đốt 10 gam cồn X là 716a + 1370b = 291,9 kJ.
Giải hệ các phương trình trên ta được a = 0,025 mol và b = 0,2 mol.
⇝ %mtạp chất CH3OH trong X = 0,025 × 32 ÷ 10 × 100% = 8,0% ⇝ Chọn đáp án C. ♣
Theo giả thiết, ta có:
• Đốt a mol CH3OH tỏa ra nhiệt lượng là 716a kJ.
• Đốt b mol C2H5OH tỏa ra nhiệt lượng là 1370b kJ.
⇒ Tổng nhiệt lượng tỏa ra khi đốt 10 gam cồn X là 716a + 1370b = 291,9 kJ.
Giải hệ các phương trình trên ta được a = 0,025 mol và b = 0,2 mol.
⇝ %mtạp chất CH3OH trong X = 0,025 × 32 ÷ 10 × 100% = 8,0% ⇝ Chọn đáp án C. ♣
Câu 36 [224964]: Lấy m gam hỗn hợp rắn gồm Mg, Zn, FeCO3, FeS2 (trong đó nguyên tố oxi chiếm 16,71% khối lượng hỗn hợp) nung trong bình chứa 0,16 mol O2, sau phản ứng hoàn toàn thu được hỗn hợp chất rắn X không chứa nguyên tố lưu huỳnh và hỗn hợp khí Y (có tỉ khối so với H2 là 27). Cho X vào dung dịch chứa 0,72 mol HCl và 0,03 mol NaNO3, sau phản ứng hoàn toàn thấy dung dịch thu được chỉ chứa muối clorua và 1,12 lít (đktc) hỗn hợp hai khí thoát ra có khối lượng là 0,66 gam (trong đó có một khí hóa nâu ngoài không khí). Giá trị m gần nhất với giá trị nào sau đây?
A, 22.
B, 24.
C, 25.
D, 23.
HD: Khí hoá nâu là NO → chứng tỏ X có tính khử ⇒ O2 hết ⇒ Y gồm CO2 và SO2.
Sơ đồ quá trình:
Mhai khí = 0,66 ÷ 0,05 = 13,2 chứng tỏ có H2 và NO; giải hệ khí ⇒ nH2 = 0,03 và nNO = 0,02.
► Có dấu hiệu để sử dụng bảo toàn electron mở rộng, tuy nhiên có cách dễ hơn như sau:
bảo toàn N có ngay nNH4+ = 0,01 mol ⇒ nH2O = 0,31 mol theo bảo toàn H.
⇒ nO trong X = 0,24 mol theo bảo toàn nguyên tố O.
☆ Quay lại bài toán nhiệt phân, khí Y gồm a mol CO2 và a mol SO2.
Sơ đồ:

Bảo toàn C có a mol FeCO3 ⇒ bảo toàn O: 3a + 0,16 × 2 = 0,24 + 2a + 2a ⇒ a = 0,08 mol.
Biết O chiếm 16,71% khối lượng hỗn hợp ⇒ m = 0,08 × 3 × 16 ÷ 0,1671 ≈ 22,98 gam.
Sơ đồ quá trình:
Mhai khí = 0,66 ÷ 0,05 = 13,2 chứng tỏ có H2 và NO; giải hệ khí ⇒ nH2 = 0,03 và nNO = 0,02.
► Có dấu hiệu để sử dụng bảo toàn electron mở rộng, tuy nhiên có cách dễ hơn như sau:
bảo toàn N có ngay nNH4+ = 0,01 mol ⇒ nH2O = 0,31 mol theo bảo toàn H.
⇒ nO trong X = 0,24 mol theo bảo toàn nguyên tố O.
☆ Quay lại bài toán nhiệt phân, khí Y gồm a mol CO2 và a mol SO2.
Sơ đồ:

Bảo toàn C có a mol FeCO3 ⇒ bảo toàn O: 3a + 0,16 × 2 = 0,24 + 2a + 2a ⇒ a = 0,08 mol.
Biết O chiếm 16,71% khối lượng hỗn hợp ⇒ m = 0,08 × 3 × 16 ÷ 0,1671 ≈ 22,98 gam.
Câu 37 [352919]: Đốt cháy hoàn toàn 0,2 mol hỗn hợp M gồm ba chất hữu cơ mạch hở X, Y, Z (chỉ chứa nhóm chức este, MX < MY < MZ) cần dùng 28,224 lít O2 (đktc), thu được 58,08 gam CO2 và 14,4 gam H2O. Mặt khác hiđro hóa hoàn toàn 0,2 mol M bằng lượng H2 vừa đủ (xúc tác Ni, t°), thu được hỗn hợp N gồm hai hợp chất hữu cơ. Đun nóng toàn bộ N với dung dịch NaOH vừa đủ, thu được hỗn hợp P gồm 3 muối của 3 axit cacboxylic đơn chức và hỗn hợp Q gồm hai ancol no hơn kém nhau một nguyên tử cacbon. Tỉ khối hơi của Q so với H2 bằng 35,5. Phần trăm khối lượng của Y trong hỗn hợp M gần nhất với giá trị nào sau đây?
A, 6,19%.
B, 13,13%.
C, 9,08%.
D, 8,96%.
Đáp án: D
Câu 38 [138629]: Tiến hành điện phân dung dịch CuSO4 và NaCl bằng điện cực trơ, màng ngăn xốp với cường dòng điện không đổi, (bỏ qua sự hòa tan của các khí trong nước) ta có kết quả ghi theo bảng sau:
Giá trị của t là
| Thời gian | Khối lượng catot tăng | Anot | Khối lượng dung dịch giảm |
| 3088 (giây) | m (gam) | Thu được khí Cl2 duy nhất | 10,80 (gam) |
| 6176 (giây) | 2m (gam) | Khí thoát ra | 18,30 (gam) |
| t (giây) | 2,5m (gam) | Khí thoát ra | 22,04 (gam) |
Giá trị của t là
A, 8299.
B, 7720.
C, 8685.
D, 8878.
Giải: ► Nhận xét: Do tăng thời gian điện phân thì m catot vẫn tăng
⇒ Cu2+ chưa bị điện phân hết tại 3088(s) và 6176(s).
► Xét tại 3088(s): quy đổi sản phẩm thành tách ra về 10,8(g) CuCl2
⇒ nCuCl2 = 0,08 mol ⇒ ne = 0,08 × 2 = 0,16 mol ⇒ I = 5A.
► Xét tại 6176(s): thời gian tăng gấp đôi ⇒ ne = 0,16 × 2 = 0,32 mol.
Quy đổi sản phẩm tách ra về CuO và CuCl2 với số mol x và y.
mdung dịch giảm = 80x + 135y = 18,3(g); ne = 2x + 2y = 0,32 mol.
||⇒ giải hệ có: x = 0,06 mol; y = 0,1 mol ⇒ nCl2 = 0,1 mol.
► Xét tại t(s): quy đổi sản phẩm tách ra về CuO, CuCl2 và CÓ THỂ CÓ H2O.
nCu = 2,5 × 0,08 = 0,2 mol; nCuCl2 = 0,1 mol ⇒ nCuO = 0,2 – 0,1 = 0,1 mol.
||⇒ mCuO + mCuCl2 = 21,5(g) < 22,04(g) ⇒ còn H2O ⇒ nH2O = 0,03 mol.
● ne = 0,1 × 2 + 0,1 × 2 + 0,03 × 2 = 0,46 mol ⇒ t = 8878(s) ⇒ chọn D.
⇒ Cu2+ chưa bị điện phân hết tại 3088(s) và 6176(s).
► Xét tại 3088(s): quy đổi sản phẩm thành tách ra về 10,8(g) CuCl2
⇒ nCuCl2 = 0,08 mol ⇒ ne = 0,08 × 2 = 0,16 mol ⇒ I = 5A.
► Xét tại 6176(s): thời gian tăng gấp đôi ⇒ ne = 0,16 × 2 = 0,32 mol.
Quy đổi sản phẩm tách ra về CuO và CuCl2 với số mol x và y.
mdung dịch giảm = 80x + 135y = 18,3(g); ne = 2x + 2y = 0,32 mol.
||⇒ giải hệ có: x = 0,06 mol; y = 0,1 mol ⇒ nCl2 = 0,1 mol.
► Xét tại t(s): quy đổi sản phẩm tách ra về CuO, CuCl2 và CÓ THỂ CÓ H2O.
nCu = 2,5 × 0,08 = 0,2 mol; nCuCl2 = 0,1 mol ⇒ nCuO = 0,2 – 0,1 = 0,1 mol.
||⇒ mCuO + mCuCl2 = 21,5(g) < 22,04(g) ⇒ còn H2O ⇒ nH2O = 0,03 mol.
● ne = 0,1 × 2 + 0,1 × 2 + 0,03 × 2 = 0,46 mol ⇒ t = 8878(s) ⇒ chọn D.
Câu 39 [679732]: Cho sơ đồ các phản ứng theo đúng tỉ lệ mol:
(a) X Y + CO2 (b) Y + H2O → Z
Y + CO2 (b) Y + H2O → Z
(c) T + Z → R + X + H2O (d) 2T + Z → Q + X + 2H2O
Các chất R, Q thỏa mãn sơ đồ trên lần lượt là
(a) X
 Y + CO2 (b) Y + H2O → Z
Y + CO2 (b) Y + H2O → Z(c) T + Z → R + X + H2O (d) 2T + Z → Q + X + 2H2O
Các chất R, Q thỏa mãn sơ đồ trên lần lượt là
A, NaHCO3, Ca(OH)2.
B, NaOH, Na2CO3.
C, Na2CO3, NaOH.
D, Ca(OH)2, NaHCO3.
HD: Hợp chất của Na và Ca, bị nhiệt phân tạo khí CO2 và chất Y có khả năng phản ứng với nước ⇒ X là CaCO3. Tương ứng Y là CaO và Z là Ca(OH)2 ⇒ T là NaHCO3 (phản ứng với Ca(OH)2 theo tỉ lệ 1 : 1 hoặc 2 : 1).
Theo đó, các phản ứng xảy ra lần lượt là:
• CaCO3 –––to–→ CaO + CO2↑.
• CaO + H2O → Ca(OH)2.
• NaHCO3 + Ca(OH)2 → NaOH (R) + CaCO3↓ (X) + H2O.
• 2NaHCO3 + Ca(OH)2 → Na2CO3 (Q) + CaCO3↓ + 2H2O.
Vậy, tương ứng chất R và Q lần lượt là NaOH và Na2CO3 ⇝ Chọn đáp án B. ♦
Theo đó, các phản ứng xảy ra lần lượt là:
• CaCO3 –––to–→ CaO + CO2↑.
• CaO + H2O → Ca(OH)2.
• NaHCO3 + Ca(OH)2 → NaOH (R) + CaCO3↓ (X) + H2O.
• 2NaHCO3 + Ca(OH)2 → Na2CO3 (Q) + CaCO3↓ + 2H2O.
Vậy, tương ứng chất R và Q lần lượt là NaOH và Na2CO3 ⇝ Chọn đáp án B. ♦
Câu 40 [982785]: Từ hợp chất hữu cơ X (C6H6O5, mạch hở), thực hiện sơ đồ phản ứng (hệ số phương trình biểu thị đúng tỉ lệ mol):
(1) X + 2NaOH → Y + Z + H2O. (2) Y + H2SO4 → T + Na2SO4.
(3) nZ + nG → Poli(etylen terephtalat) + nH2O.
Cho các phát biểu sau:
(a) Đốt cháy Y, thu được sản phẩm gồm CO2, H2O và Na2CO3.
(b) Chất T cộng Br2 theo tỉ lệ mol 1 : 1.
(c) Chất G là axit cacboxylic no, hai chức.
(d) Chất X có mạch cacbon không phân nhánh.
(e) Chất Z có nhiệt độ sôi cao hơn axit oxalic.
Số phát biểu đúng là
(1) X + 2NaOH → Y + Z + H2O. (2) Y + H2SO4 → T + Na2SO4.
(3) nZ + nG → Poli(etylen terephtalat) + nH2O.
Cho các phát biểu sau:
(a) Đốt cháy Y, thu được sản phẩm gồm CO2, H2O và Na2CO3.
(b) Chất T cộng Br2 theo tỉ lệ mol 1 : 1.
(c) Chất G là axit cacboxylic no, hai chức.
(d) Chất X có mạch cacbon không phân nhánh.
(e) Chất Z có nhiệt độ sôi cao hơn axit oxalic.
Số phát biểu đúng là
A, 1.
B, 3.
C, 2.
D, 4.
HD: Xuất phát từ phản ứng (c) trùng ngưng điều chế tơ lapsan:

► (b) cho biết Y là muối ⇒ Z là ancol nên Z là C2H4(OH)2; còn G là axit C6H4(COOH)2.
Quay lại (a): C6H6O5 + 2NaOH → Y + C2H4(OH)2 + H2O.
⇒ CTPT của Y là C4O4Na2 tương ứng với cấu tạo NaOOC–C≡C–COONa.
⇒ Cấu tạo của X là HOOC–C≡C–COO–CH2CH2OH và T là HOOC–C≡C–COOH.
☆ Phân tích các phát biểu:
❌ (a) sai vì muối Y không có H, làm sao đốt ra H2O được.
❌ (b) sai vì nối ba C≡C trong T có thể cộng với 2Br2.
❌ (c) sai vì G có vòng benzen, lấy đâu ra no.
✔️ (d) đúng theo cấu tạo X phân tích trên.
❌ (e) sai vì HOCH2CH2OH (ancol Z) có nhiệt sôi thấp hơn so với HOOC–COOH (axit oxalic).
⇝ Chỉ có 1/5 phát biểu đúng ⇝ Chọn đáp án A. ♥

► (b) cho biết Y là muối ⇒ Z là ancol nên Z là C2H4(OH)2; còn G là axit C6H4(COOH)2.
Quay lại (a): C6H6O5 + 2NaOH → Y + C2H4(OH)2 + H2O.
⇒ CTPT của Y là C4O4Na2 tương ứng với cấu tạo NaOOC–C≡C–COONa.
⇒ Cấu tạo của X là HOOC–C≡C–COO–CH2CH2OH và T là HOOC–C≡C–COOH.
☆ Phân tích các phát biểu:
❌ (a) sai vì muối Y không có H, làm sao đốt ra H2O được.
❌ (b) sai vì nối ba C≡C trong T có thể cộng với 2Br2.
❌ (c) sai vì G có vòng benzen, lấy đâu ra no.
✔️ (d) đúng theo cấu tạo X phân tích trên.
❌ (e) sai vì HOCH2CH2OH (ancol Z) có nhiệt sôi thấp hơn so với HOOC–COOH (axit oxalic).
⇝ Chỉ có 1/5 phát biểu đúng ⇝ Chọn đáp án A. ♥