Đáp án
1C
2D
3B
4A
5B
6B
7A
8D
9B
10A
11C
12D
13D
14A
15B
16A
17D
18A
19D
20D
21C
22C
23C
24D
25A
26C
27A
28C
29B
30B
31B
32A
33B
34A
35C
36D
37A
38D
39B
40A
Đáp án Đề minh họa số 2 thi Tốt Nghiệp Trung học Phổ Thông 2024 môn Hóa học
Câu 1 [982006]: Etyl axetat có công thức là
A, C2H5COOCH3.
B, CH3COOCH3.
C, CH3COOC2H5.
D, C2H3COOCH3.
HD: Gốc ankyl etyl là C2H5; gốc muối axetat là CH3COO.
⇒ Ghép lại thành este tương ứng etyl axetat: CH3COOC2H5.
⇒ Ghép lại thành este tương ứng etyl axetat: CH3COOC2H5.
Câu 2 [911550]: Tên gọi của hợp chất CH3COOH là
A, axit fomic.
B, ancol etylic.
C, anđehit axetic.
D, axit axetic.
HD: Phân tích các đáp án: (Chú ý pH của nước = 7).
| Tên gọi | axit fomic | ancol etylic | anđehit axetic | axit axetic |
| Cấu tạo | HCOOH | C2H5OH | CH3CHO | CH3COOH |
| ❌ | ❌ | ❌ | ✔️ |
Câu 3 [982019]: Dung dịch nào sau đây làm quỳ tím chuyển sang màu xanh?
A, NaCl.
B, NaOH.
C, KNO3.
D, KCl.
HD: Phân tích các đáp án:
| Dung dịch | NaCl | NaOH | KNO3 | KCl |
| pH | = 7 | > 7 | = 7 | = 7 |
| Quỳ tím | không đổi (❌) | hoá xanh (✔️) | không đổi (❌) | không đổi (❌) |
Câu 4 [60158]: Chất nào sau đây gây ra tính cứng tạm thời của nước?
A, Ca(HCO3)2.
B, NaOH.
C, CaCl2.
D, HCl.
HD:
Ca(HCO3)2 có chứa HCO3– gây ra tính cứng tạm thời của nước.
Ca(HCO3)2 có chứa HCO3– gây ra tính cứng tạm thời của nước.
Câu 5 [311874]: Trong tự nhiên, canxi sunfat tồn tại dưới dạng muối ngậm nước (CaSO4.2H2O) được gọi là
A, vôi sống.
B, thạch cao sống.
C, vôi tôi.
D, đá vôi.
HD: ☆ Ghi nhớ:
• CaSO4.2H2O: có đủ nước (.2H2O) là thạch cao sống.
• Từ thạch cao sống, nung lên sẽ bay hơi mất nước:
– Nếu mất một phần nước: CaSO4.H2O hay CaSO4.½H2O thì gọi là thạch cao nung.
– Nếu mất hết nước được muối khan CaSO4 thì gọi là thạch cao khan. ❒
• CaSO4.2H2O: có đủ nước (.2H2O) là thạch cao sống.
• Từ thạch cao sống, nung lên sẽ bay hơi mất nước:
– Nếu mất một phần nước: CaSO4.H2O hay CaSO4.½H2O thì gọi là thạch cao nung.
– Nếu mất hết nước được muối khan CaSO4 thì gọi là thạch cao khan. ❒
Câu 6 [983255]: Khi đốt cháy các nhiên liệu hóa thạch (như than đá, dầu mỏ, khi đốt) thường sinh ra khí X. Khí X không màu, có mùi hắc, độc, nặng hơn không khí và gây ra mưa axit. Khí X là
A, N2.
B, SO2.
C, O2.
D, CH4.
HD: Ta hít thở O2 hằng ngày nên loại đáp án C.
Mkhông khí ≈ 29 > MN2 = 28 > MCH4 = 16 ⇝ loại A và D ⇝ Chọn đáp án B. ♦
► Nhiên liệu hoá thạch thường lẫn lưu huỳnh (S), khi đốt: S + O2 → SO2 (X).
Khí SO2 không màu, có mùi hắc, độc, nặng hơn không khí và gây ra mưa axit.
Mkhông khí ≈ 29 > MN2 = 28 > MCH4 = 16 ⇝ loại A và D ⇝ Chọn đáp án B. ♦
► Nhiên liệu hoá thạch thường lẫn lưu huỳnh (S), khi đốt: S + O2 → SO2 (X).
Khí SO2 không màu, có mùi hắc, độc, nặng hơn không khí và gây ra mưa axit.
Câu 7 [982760]: Cho FeO tác dụng với dung dịch HCl dư, sinh ra chất nào sau đây?
A, FeCl2.
B, Fe(OH)2.
C, FeCl3.
D, H2.
HD: Phản ứng xảy ra: FeO + 2HCl → FeCl2 + H2O.
Câu 8 [890472]: Trong các kim loại sau, kim loại nào mềm nhất?
A, Fe.
B, Mg.
C, Cu.
D, Cs
HD: Kim loại mềm nhất trong 4 phương án là Cs.
"Rắn như thép (Fe), vững như đồng (Cu)
Đội ngũ ta trùng trùng điệp điệp
Cao như núi, dài như sông
Chií ta lớn như biển động trước mặt".
"Rắn như thép (Fe), vững như đồng (Cu)
Đội ngũ ta trùng trùng điệp điệp
Cao như núi, dài như sông
Chií ta lớn như biển động trước mặt".
Câu 9 [184899]: Hợp chất Cr(OH)3 có tên là
A, crom(III) hiđroxit.
B, crom(II) hiđroxit.
C, crom(II) oxit.
D, crom(III) oxit.
Crom là kim loại có nhiều hóa trị nên khi gọi tên cần thêm hóa trị của kim loại.
→ Cr(OH)3 có tên là Crom(III) hiđroxit.
→ Cr(OH)3 có tên là Crom(III) hiđroxit.
Câu 10 [982267]: Kim loại nào sau đây có tính khử yếu hơn kim loại Ag?
A, Au.
B, K.
C, Zn.
D, Mg.
HD: Sắp xếp theo dãy điện hoá: K > Mg > Zn > Ag > Au
⇒ Kim loại Au (vàng) có tính khử yếu hơn kim loại Ag.
⇒ Kim loại Au (vàng) có tính khử yếu hơn kim loại Ag.
Câu 11 [310977]: Nhôm hiđroxit (Al(OH)3) tan trong dung dịch nào sau đây?
A, NaNO3.
B, NaCl.
C, NaOH.
D, NaAlO2.
HD: Nhôm hiđroxit (Al(OH)3) tan trong dung dịch NaOH:
Al(OH)3 + NaOH → NaAlO2 + 2H2O. ❒
Al(OH)3 + NaOH → NaAlO2 + 2H2O. ❒
Câu 12 [908853]: Chất nào sau đây là đipeptit?
A, Ala-Gly-Ala.
B, Ala-Ala-Ala.
C, Gly-Gly-Gly.
D, Ala-Gly.
HD: mono = 1; đi = 2; tri = 3; tetra là 4,...
⇒ Đáp án A, B, C tương ứng là các tripeptit; còn D là đipeptit.
⇒ Đáp án A, B, C tương ứng là các tripeptit; còn D là đipeptit.
Câu 13 [679793]: Số nguyên tử oxi trong phân tử glucozơ là
A, 3.
B, 4.
C, 5.
D, 6.
HD: Cùng ngắm lại công thức cấu tạo mạch hở phân tử glucozơ:

⇒ Đếm ra có 6 nguyên tử oxi trong phân tử glucozơ.

⇒ Đếm ra có 6 nguyên tử oxi trong phân tử glucozơ.
Câu 14 [59433]: Kim loại nào sau đây có thể điều chế được bằng phương pháp điện phân dung dịch?
A, Cu.
B, K.
C, Al.
D, Mg.
HD: ☆ Phương pháp điện phân:
• Điện phân chất điện li nóng chảy (muối, bazơ, oxit) để điều chế những kim loại có tính khử mạnh như K, Na, Ca, Al,...
• Điện phân dung dịch chất điện li (dung dịch muối) để điều chế những kim loại có tính khử yếu và trung bình như Zn, Fe, Sn, Pb, Cu, Hg, Ag,...
|⇝ Đồng (Cu) là kim loại duy nhất trong 4 đáp án điều chế được bằng phương pháp điện phân dung dịch. ❒
• Điện phân chất điện li nóng chảy (muối, bazơ, oxit) để điều chế những kim loại có tính khử mạnh như K, Na, Ca, Al,...
• Điện phân dung dịch chất điện li (dung dịch muối) để điều chế những kim loại có tính khử yếu và trung bình như Zn, Fe, Sn, Pb, Cu, Hg, Ag,...
|⇝ Đồng (Cu) là kim loại duy nhất trong 4 đáp án điều chế được bằng phương pháp điện phân dung dịch. ❒
Câu 15 [982218]: Natri clorua được dùng để làm gia vị thức ăn, điều chế natri, xút, nước Gia-ven. Công thức của natri clorua là
A, Na2CO3.
B, NaCl.
C, NaHCO3.
D, KCl.
HD: Phân tích các đáp án:
| Công thức | A. Na2CO3. | B. NaCl. | C. NaHCO3. | D. KCl. |
| Tên gọi | natri cacbonat | natri clorua (✔️) | natri hiđrocacbonat | kali clorua |
Câu 16 [14686]: Hợp chất CH3CH2NH2 có tên gọi là
A, etylamin.
B, metanamin.
C, đimetylamin.
D, metylamin.
Giải: Amin CH3CH2NH2 có tên gọi là etylamin.
⇒ Chọn A
⇒ Chọn A
Câu 17 [982035]: Thủy phân tripanmitin ((C15H31COO)3C3H5) trong dung dịch NaOH thu được ancol có công thức là
A, C2H5OH.
B, C2H4(OH)2.
C, CH3OH.
D, C3H5(OH)3.
HD: Thuỷ phân chất béo luôn thu được ancol là glixerol: C3H5(OH)3.
Ví dụ: (C15H31COO)3C3H5 + 3NaOH → 3C15H31COONa + C3H5(OH)3.
⇒ đáp án thoả mãn là D.
Ví dụ: (C15H31COO)3C3H5 + 3NaOH → 3C15H31COONa + C3H5(OH)3.
⇒ đáp án thoả mãn là D.
Câu 18 [20370]: Monome được dùng để điều chế polistiren (PS) là
A, C6H5CH=CH2.
B, CH2=CHCH=CH2.
C, CH2=CH2.
D, CH2=CHCH3.
Giải: Polistiren được điều chế bằng cách trùng hợp stiren:
nC6H5CH=CH2 [-CH2-CH(C6H5)-]n ⇒ chọn A.
[-CH2-CH(C6H5)-]n ⇒ chọn A.
nC6H5CH=CH2
 [-CH2-CH(C6H5)-]n ⇒ chọn A.
[-CH2-CH(C6H5)-]n ⇒ chọn A.
Câu 19 [311335]: Sục khí CO2 dư vào dung dịch nào sau đây thu được kết tủa?
A, NaNO3.
B, NaCl.
C, NaOH.
D, NaAlO2.
HD: CO2 không phản ứng được với dung dịch NaNO3 và NaCl.
Còn lại: NaOH + CO2 (dư) → NaHCO3 (không có kết tủa).
☆ Chỉ có: CO2 + 2H2O + NaAlO2 → NaHCO3 + Al(OH)3↓. ❒
Còn lại: NaOH + CO2 (dư) → NaHCO3 (không có kết tủa).
☆ Chỉ có: CO2 + 2H2O + NaAlO2 → NaHCO3 + Al(OH)3↓. ❒
Câu 20 [58064]: Kim loại nào sau đây không phản ứng với dung dịch CuSO4?
A, Zn.
B, Al.
C, Fe.
D, Ag.
HD: Thứ tự các kim loại trong dãy điện hóa: Al > Zn > Fe > Cu > Ag.
⇒ Kim loại Ag không phản ứng được với dung dịch CuSO4. ❒
⇒ Kim loại Ag không phản ứng được với dung dịch CuSO4. ❒
Câu 21 [906761]: Cho dung dịch NaOH dư vào dung dịch FeSO4 và dung dịch Fe2(SO4)3, thu được kết tủa X. Cho X tác dụng với dung dịch HNO3 dư, thu được dung dịch chứa muối
A, Fe(NO3)2 và NaNO3.
B, Fe(NO3)3 và NaNO3.
C, Fe(NO3)3.
D, Fe(NO3)2.
HD: Các phản ứng xảy ra:
• 2NaOH + FeSO4 → Fe(OH)2↓ + Na2SO4.
• 6NaOH + Fe2(SO4)3 → 2Fe(OH)3↓ + 3Na2SO4.
⇒ Kết tủa X gồm Fe(OH)2 và Fe(OH)3. Sau đó:
• Fe(OH)3 + 3HNO3 → Fe(NO3)3 + 3H2O.
• 3Fe(OH)2 + 10HNO3 → 3Fe(NO3)3 + NO + 8H2O.
⇒ Dung dịch muối sau quá trình chỉ chứa Fe(NO3)3 mà thôi.
• 2NaOH + FeSO4 → Fe(OH)2↓ + Na2SO4.
• 6NaOH + Fe2(SO4)3 → 2Fe(OH)3↓ + 3Na2SO4.
⇒ Kết tủa X gồm Fe(OH)2 và Fe(OH)3. Sau đó:
• Fe(OH)3 + 3HNO3 → Fe(NO3)3 + 3H2O.
• 3Fe(OH)2 + 10HNO3 → 3Fe(NO3)3 + NO + 8H2O.
⇒ Dung dịch muối sau quá trình chỉ chứa Fe(NO3)3 mà thôi.
Câu 22 [955436]: Đốt cháy hoàn toàn 1,0 gam một este (không no, mạch hở, phân tử chứa hai liên kết π) thu được 0,72 gam nước. Công thức phân tử của este là
A, C3H4O2.
B, C4H6O2.
C, C5H8O2.
D, C6H10O2.
HD: este không no, mạch hở, phân tử chứa hai liên kết π có dạng CnH2n – 2O2.
☆ Đốt 1,0 gam CnH2n – 2O2 + O2 ––to→ ? mol CO2 + 0,04 mol H2O.
► Biến đổi a mol CnH2n – 2O2 = CO2.Cn – 1H2n – 2.
⇒ Tách 1,0 gam este thành a mol CO2 + 0,04 mol cụm CH2
⇒ a = (1,0 – 0,04 × 14) ÷ 44 = 0,01 mol.
⇒ 2n – 2 = ∑số H = 0,04 ÷ 0,01 × 2 ⇒ n = 5 cho biết CTPT este là C5H8O2.
☆ Đốt 1,0 gam CnH2n – 2O2 + O2 ––to→ ? mol CO2 + 0,04 mol H2O.
► Biến đổi a mol CnH2n – 2O2 = CO2.Cn – 1H2n – 2.
⇒ Tách 1,0 gam este thành a mol CO2 + 0,04 mol cụm CH2
⇒ a = (1,0 – 0,04 × 14) ÷ 44 = 0,01 mol.
⇒ 2n – 2 = ∑số H = 0,04 ÷ 0,01 × 2 ⇒ n = 5 cho biết CTPT este là C5H8O2.
Câu 23 [305381]: Phát biểu nào sau đây là sai?
A, Nước mía có khả năng tác dụng với đồng(II) hiđroxit.
B, Gạo nếp dẻo hơn gạo tẻ do chứa nhiều amilopectin hơn.
C, Số nguyên tử cacbon trong phân tử chất béo là số chẵn.
D, Phản ứng thủy phân chất béo luôn tạo thành glixerol.
✔️ A. Đúng vì trong nước mía chứa saccarozơ. Trong saccarozơ có chứa các nhóm OH liền kề nên có thể phản ứng được với Cu(OH)2.
✔️ B. Đúng vì trong gạo nếp chứa hàm lượng amilopectin cao hơn. Amilopectin có cấu trúc mạch phân nhánh, tạo ra số lượng liên kết nhiều hơn → Gạo nếp sẽ dẻo hơn gạo tẻ.
❌ C. Sai vì trong phân tử chất béo (chỉ chứa 3 nguyên tố C, H, O) thì số lượng nguyên tử H luôn chẵn, còn số lượng nguyên tử C thì có thể chẵn, có thể lẻ.
✔️D. Đúng vì chất béo là trieste của glixerol nên khi thủy phân sẽ thu được glixerol.
✔️ B. Đúng vì trong gạo nếp chứa hàm lượng amilopectin cao hơn. Amilopectin có cấu trúc mạch phân nhánh, tạo ra số lượng liên kết nhiều hơn → Gạo nếp sẽ dẻo hơn gạo tẻ.
❌ C. Sai vì trong phân tử chất béo (chỉ chứa 3 nguyên tố C, H, O) thì số lượng nguyên tử H luôn chẵn, còn số lượng nguyên tử C thì có thể chẵn, có thể lẻ.
✔️D. Đúng vì chất béo là trieste của glixerol nên khi thủy phân sẽ thu được glixerol.
Câu 24 [982283]: Cho các polime sau: poli(vinyl clorua), poli(etylen terephtalat), polietilen, nilon-6,6. Số polime tổng hợp là
A, 3.
B, 2.
C, 1.
D, 4.
HD: Bài học phân loại tơ:
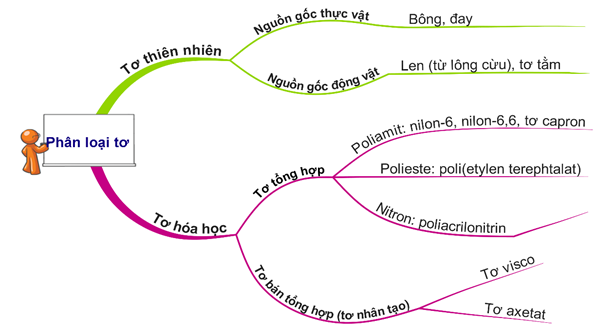
⇝ Cả 4 tơ trong dãy đều là tơ tổng hợp ⇝ Chọn đáp án D. ♠

⇝ Cả 4 tơ trong dãy đều là tơ tổng hợp ⇝ Chọn đáp án D. ♠
Câu 25 [352137]: Thực hiện phản ứng este hóa giữa glixerol với hai axit cacboxylic là HCOOH và CH3COOH thu được tối đa bao nhiêu este ba chức?
A, 6.
B, 4.
C, 3.
D, 5.
Este hóa giữa glixerol với hai axit cacboxylic là HCOOH và CH3COOH thu được tối đa 6 este ba chức có công thức như sau:
![599755[LG].png](https://ai.moon.vn/Images/Teachers/trancongminh/599755[LG].png)
![599755[LG].png](https://ai.moon.vn/Images/Teachers/trancongminh/599755[LG].png)
Câu 26 [139465]: Ngâm một đinh sắt trong 200 ml dung dịch CuSO4 x(M). Sau khi phản ứng kết thúc lấy đinh sắt ra khỏi dung dịch rửa nhẹ, làm khô đinh sắt tăng thêm 3,2 gam. Giá trị của x là
A, 0,4.
B, 0,8.
C, 2,0.
D, 0,2.
HD: ☆ Phản ứng: Fe + CuSO4 → FeSO4 + Cu.
► Nhận xét: cứ 1 mol CuSO4 phản ứng thì làm mất 1 mol Fe và tạo thêm 1 mol Cu
⇝ Khối lượng thanh sắt tăng thêm tương ứng 64 – 56 = 8 gam.
Theo đó, để thanh sắt tăng thêm 3,2 gam thì tương ứng
số mol CuSO4 phản ứng là 3,2 : 8 = 0,4 mol.
Vậy, giá trị của x = 0,4 : 0,2 = 2,0. ❒
► Nhận xét: cứ 1 mol CuSO4 phản ứng thì làm mất 1 mol Fe và tạo thêm 1 mol Cu
⇝ Khối lượng thanh sắt tăng thêm tương ứng 64 – 56 = 8 gam.
Theo đó, để thanh sắt tăng thêm 3,2 gam thì tương ứng
số mol CuSO4 phản ứng là 3,2 : 8 = 0,4 mol.
Vậy, giá trị của x = 0,4 : 0,2 = 2,0. ❒
Câu 27 [679764]: Cho 90 gam glucozơ lên men rượu với hiệu suất 80%, thu được m gam C2H5OH. Giá trị của m là
A, 36,8.
B, 18,4.
C, 23,0.
D, 46,0.
HD: Phản ứng lên men rượu:

Giả thiết nglucozơ = 0,5 mol, hiệu suất 80% = 0,8
⇒ nC2H5OH = 0,5 × 2 × 0,8 = 0,8 mol ⇒ m = mC2H5OH = 0,8 × 46 = 36,8 gam.
Giả thiết nglucozơ = 0,5 mol, hiệu suất 80% = 0,8
⇒ nC2H5OH = 0,5 × 2 × 0,8 = 0,8 mol ⇒ m = mC2H5OH = 0,8 × 46 = 36,8 gam.
Câu 28 [981938]: Cho m gam H2NCH2COOH phản ứng hoàn toàn với dung dịch HCl dư, thu được 6,69 gam muối. Giá trị của m là
A, 2,25.
B, 3,00.
C, 4,50.
D, 5,25.
HD: Phản ứng: H2NCH2COOH + HCl → ClH3NCH2COOH.
Giả thiết nmuối = 6,69 ÷ (75 + 36,5) = 0,06 mol.
⇒ Yêu cầu: m = 0,06 × 75 = 4,5 gam.
Giả thiết nmuối = 6,69 ÷ (75 + 36,5) = 0,06 mol.
⇒ Yêu cầu: m = 0,06 × 75 = 4,5 gam.
Câu 29 [352138]: Phát biểu nào sau đây không đúng?
A, Sắt có trong hemoglobin (huyết cầu tố) của máu.
B, Kim loại Li được dùng làm tế bào quang điện.
C, Nhôm là kim loại phổ biến nhất trong vỏ Trái Đất.
D, Đun nóng thạch cao sống thu được thạnh cao nung.
✔️ A. Đúng.
❌ B. Sai vì kim loại Cs được dùng làm tế bào quang điện.
✔️ C. Đúng vì nhôm chiếm 17% khối lớp chất rắn của Trái Đất, nhiều nhất trong tất cả các kim loại.
✔️ D. Đúng vì thạch cao sống CaSO4.2H2O khi nung nóng sẽ mất dần nước để hình thành thạch cao nung CaSO4.H2O.
❌ B. Sai vì kim loại Cs được dùng làm tế bào quang điện.
✔️ C. Đúng vì nhôm chiếm 17% khối lớp chất rắn của Trái Đất, nhiều nhất trong tất cả các kim loại.
✔️ D. Đúng vì thạch cao sống CaSO4.2H2O khi nung nóng sẽ mất dần nước để hình thành thạch cao nung CaSO4.H2O.
Câu 30 [679363]: Dẫn khí CO dư qua ống sứ đựng 7,2 gam bột FeO nung nóng, thu được hỗn hợp khí X. Cho toàn bộ X vào nước vôi trong dư, thu được m gam kết tủa. Biết các phản ứng xảy ra hoàn toàn. Giá trị của m là
A, 5,0.
B, 10,0.
C, 7,2.
D, 15,0.
Phản ứng: CO + FeO → Fe + CO2.
Có 7,2 gam FeO tương ứng 0,1 mol FeO → sinh ra 0,1 mol CO2 theo tỉ lệ.
Sau đó: CO2 + Ca(OH)2 → CaCO3↓ + H2O.
Vậy, m gam kết tủa là 0,1 mol CaCO3 → m = 10,0 gam.
Có 7,2 gam FeO tương ứng 0,1 mol FeO → sinh ra 0,1 mol CO2 theo tỉ lệ.
Sau đó: CO2 + Ca(OH)2 → CaCO3↓ + H2O.
Vậy, m gam kết tủa là 0,1 mol CaCO3 → m = 10,0 gam.
Câu 31 [973569]: Thực hiện các thí nghiệm sau:
(a) Đun sôi nước cứng tạm thời.
(b) Cho phèn chua vào lượng dư dung dịch Ba(OH)2.
(c) Cho dung dịch NaOH dư vào dung dịch AlCl3.
(d) Sục khí CO2 đến dư vào dung dịch Ca(OH)2.
(e) Cho NaOH dư vào dung dịch Ca(HCO3)2.
(g) Cho dung dịch HCl dư vào dung dịch NaAlO2.
Sau khi kết thúc các phản ứng, số thí nghiệm thu được kết tủa là
(a) Đun sôi nước cứng tạm thời.
(b) Cho phèn chua vào lượng dư dung dịch Ba(OH)2.
(c) Cho dung dịch NaOH dư vào dung dịch AlCl3.
(d) Sục khí CO2 đến dư vào dung dịch Ca(OH)2.
(e) Cho NaOH dư vào dung dịch Ca(HCO3)2.
(g) Cho dung dịch HCl dư vào dung dịch NaAlO2.
Sau khi kết thúc các phản ứng, số thí nghiệm thu được kết tủa là
A, 2.
B, 3.
C, 5.
D, 4.
HD: Phân tích, các phản ứng xảy ra ở các thí nghiệm:
✔️ (a) Ca(HCO3)2 ––to→ CaCO3↓ + CO2 + H2O.
✔️ (b) Phèn chua vào nước: K2SO4.Al2(SO4)3.24H2O → K+ + Al3+ + SO42–
⇒ xảy ra phản ứng: Ba2+ + SO42– → BaSO4↓.
❌ (c) 3NaOH + AlCl3 → Al(OH)3↓ + 3NaCl.
sau đó do NaOH dư nên NaOH + Al(OH)3 → NaAlO2 + 2H2O.
❌ (d) CO2 + Ca(OH)2 → CaCO3↓ + H2O.
sau đó do CO2 dư nên CO2 + H2O + CaCO3 → Ca(HCO3)2.
✔️ (e) 2NaOH + Ca(HCO3)2 → CaCO3↓ + Na2CO3 + 2H2O.
❌ (g) HCl + H2O + NaAlO2 → Al(OH)3 + NaCl.
sau đó do HCl dư nên 3HCl + Al(OH)3 → AlCl3 + 3H2O.
⇝ có 3/6 thí nghiệm thoả mãn yêu cầu thu được kết tủa ⇝ Chọn đáp án B. ♦
✔️ (a) Ca(HCO3)2 ––to→ CaCO3↓ + CO2 + H2O.
✔️ (b) Phèn chua vào nước: K2SO4.Al2(SO4)3.24H2O → K+ + Al3+ + SO42–
⇒ xảy ra phản ứng: Ba2+ + SO42– → BaSO4↓.
❌ (c) 3NaOH + AlCl3 → Al(OH)3↓ + 3NaCl.
sau đó do NaOH dư nên NaOH + Al(OH)3 → NaAlO2 + 2H2O.
❌ (d) CO2 + Ca(OH)2 → CaCO3↓ + H2O.
sau đó do CO2 dư nên CO2 + H2O + CaCO3 → Ca(HCO3)2.
✔️ (e) 2NaOH + Ca(HCO3)2 → CaCO3↓ + Na2CO3 + 2H2O.
❌ (g) HCl + H2O + NaAlO2 → Al(OH)3 + NaCl.
sau đó do HCl dư nên 3HCl + Al(OH)3 → AlCl3 + 3H2O.
⇝ có 3/6 thí nghiệm thoả mãn yêu cầu thu được kết tủa ⇝ Chọn đáp án B. ♦
Câu 32 [352139]: Tiến hành thí nghiệm theo các bước sau:
Bước 1: Cho một đinh sắt đã cạo sạch gỉ vào ống nghiệm.
Bước 2: Thêm tiếp vào ống nghiệm 4-5 ml dung dịch H2SO4 loãng.
Bước 3: Lấy đinh sắt ra rồi nhỏ dần từng giọt dung dịch KMnO4 trong H2SO4 loãng vào ống nghiệm và lắc đều. Cho các phát biểu sau:
(a) Sau bước 2, dung dịch trong ống nghiệm chuyển dần sang màu xanh lam.
(b) Khi thêm từng giọt dung dịch KMnO4 vào dung dịch trong ống nghiệm, thấy màu tím phân tán vào dung dịch rồi biến mất.
(c) Ở bước 3, hợp chất sắt(II) bị oxi hóa thành hợp chất sắt(III).
(d) Ở bước 3, Mn6+ trong hợp chất KMnO4 bị khử về Mn+2 trong muối MnSO4.
(e) Ở bước 2, nếu thay dung dịch H2SO4 loãng bằng dung dịch H2SO4 đặc thì hiện tượng ở bước 3 không có gì thay đổi.
Số phát biểu đúng là
Bước 1: Cho một đinh sắt đã cạo sạch gỉ vào ống nghiệm.
Bước 2: Thêm tiếp vào ống nghiệm 4-5 ml dung dịch H2SO4 loãng.
Bước 3: Lấy đinh sắt ra rồi nhỏ dần từng giọt dung dịch KMnO4 trong H2SO4 loãng vào ống nghiệm và lắc đều. Cho các phát biểu sau:
(a) Sau bước 2, dung dịch trong ống nghiệm chuyển dần sang màu xanh lam.
(b) Khi thêm từng giọt dung dịch KMnO4 vào dung dịch trong ống nghiệm, thấy màu tím phân tán vào dung dịch rồi biến mất.
(c) Ở bước 3, hợp chất sắt(II) bị oxi hóa thành hợp chất sắt(III).
(d) Ở bước 3, Mn6+ trong hợp chất KMnO4 bị khử về Mn+2 trong muối MnSO4.
(e) Ở bước 2, nếu thay dung dịch H2SO4 loãng bằng dung dịch H2SO4 đặc thì hiện tượng ở bước 3 không có gì thay đổi.
Số phát biểu đúng là
A, 2.
B, 4.
C, 3.
D, 1.
Bước 1: Làm sạch đinh sắt.
Bước 2: Thêm H2SO4 vào ống nghiệm
Fe + H2SO4 → FeSO4 + H2.
Bước 3: Thêm KMnO4 vào ống nghiệm
10FeSO4 + 2KMnO4 + 8H2SO4 → 5Fe2(SO4)3 + 2MnSO4 + K2SO4 + 8H2O.
❌ (a) Sai vì sau bước 2, dung dịch chứa FeSO4 không màu.
✔️ (b) Đúng vì KMnO4 tan vào trong dung dịch, phản ứng với FeSO4 chuyển thành dung dịch không màu → Dung dịch KMnO4 mất màu.
✔️ (c) Đúng vì Fe trong FeSO4 là Fe(II), trong Fe2(SO4)3 là Fe(III).
❌ (d) Sai vì Mn trong KMnO4 là Mn +7.
❌ (e) Sai vì nếu dùng H2SO4 đặc thì Fe sẽ bị oxi hóa lên Fe(III).
2Fe + 6H2SO4 → Fe2(SO4)3 + 3SO2 + 6H2O.
Sau bước 2 thì dung dịch chứa Fe2(SO4)3 và sẽ không phản ứng với KMnO4 ở bước 3 → Không xảy ra hiện tượng mất màu.
Bước 2: Thêm H2SO4 vào ống nghiệm
Fe + H2SO4 → FeSO4 + H2.
Bước 3: Thêm KMnO4 vào ống nghiệm
10FeSO4 + 2KMnO4 + 8H2SO4 → 5Fe2(SO4)3 + 2MnSO4 + K2SO4 + 8H2O.
❌ (a) Sai vì sau bước 2, dung dịch chứa FeSO4 không màu.
✔️ (b) Đúng vì KMnO4 tan vào trong dung dịch, phản ứng với FeSO4 chuyển thành dung dịch không màu → Dung dịch KMnO4 mất màu.
✔️ (c) Đúng vì Fe trong FeSO4 là Fe(II), trong Fe2(SO4)3 là Fe(III).
❌ (d) Sai vì Mn trong KMnO4 là Mn +7.
❌ (e) Sai vì nếu dùng H2SO4 đặc thì Fe sẽ bị oxi hóa lên Fe(III).
2Fe + 6H2SO4 → Fe2(SO4)3 + 3SO2 + 6H2O.
Sau bước 2 thì dung dịch chứa Fe2(SO4)3 và sẽ không phản ứng với KMnO4 ở bước 3 → Không xảy ra hiện tượng mất màu.
Câu 33 [906809]: Nhiệt phân hoàn toàn 11,88 gam X (là muối ở dạng ngậm nước), thu được hỗn hợp Y (gồm khí và hơi) và 3,24 gam một chất rắn Z. Hấp thụ hết Y vào nước, thu được dung dịch T. Cho 80 ml dung dịch NaOH 1M vào T, thu được dung dịch chỉ chứa một muối, khối lượng của muối là 6,8 gam. Phần trăm khối lượng nguyên tố oxi trong X là
A, 53,87%.
B, 64,65%.
C, 59,26%.
D, 48.48%.
HD: 0,08 mol NaOH → một muối duy nhất Na? nặng 23,8 gam.
Thực hiện: 6,8 ÷ 0,08 = 85 = 23 + 62 ⇒ cho biết muối là NaNO3.
Theo đó Y gồm hơi H2O và khí NO2 + O2 với đúng tỉ lệ 4 : 1 để sau đó:
4NO2 + O2 + 2H2O → 4HNO3.
NaOH + HNO3 → NaNO3 + H2O.
► Phân tích: muối dạng M(NO3)n ⇒ oxit dạng M2On: khối lượng 3,24 gam.
Mà nO trong oxit = ½nNO3 = 0,04 mol ⇒ mM = 2,6.
Ta có M ÷ n = 2,6 ÷ (0,04 × 2) = 65/2 cho biết M là kim loại kẽm (Zn); hóa trị II.
⇒ 11,88 gam X dạng Zn(NO3)2.nH2O với số mol 0,04 ⇒ n = 6.
Vậy, X là Zn(NO3)2.6H2O ⇝ yêu cầu %mO trong X ≈ 64,65%.
Thực hiện: 6,8 ÷ 0,08 = 85 = 23 + 62 ⇒ cho biết muối là NaNO3.
Theo đó Y gồm hơi H2O và khí NO2 + O2 với đúng tỉ lệ 4 : 1 để sau đó:
4NO2 + O2 + 2H2O → 4HNO3.
NaOH + HNO3 → NaNO3 + H2O.
► Phân tích: muối dạng M(NO3)n ⇒ oxit dạng M2On: khối lượng 3,24 gam.
Mà nO trong oxit = ½nNO3 = 0,04 mol ⇒ mM = 2,6.
Ta có M ÷ n = 2,6 ÷ (0,04 × 2) = 65/2 cho biết M là kim loại kẽm (Zn); hóa trị II.
⇒ 11,88 gam X dạng Zn(NO3)2.nH2O với số mol 0,04 ⇒ n = 6.
Vậy, X là Zn(NO3)2.6H2O ⇝ yêu cầu %mO trong X ≈ 64,65%.
Câu 34 [161626]: Cho hơi nước đi qua than nóng đỏ thu được hỗn hợp khí X gồm CO, H2 và CO2. Dẫn toàn bộ X qua dung dịch Ba(OH)2 đư thu được m gam kết tủa. Lượng khí còn lại cho từ từ qua ống đựng FeO nung nóng sau phản ứng thu được chất rắn Y và khí Z. Hòa tan hoàn toàn Y bằng dung dịch H2SO4 đặc, nóng dư thấy thoát ra 1,456 lít khí SO2 và số mol H2SO4 đã phản ứng là 0,14 mol. Mặt khác, khí Z được hấp thụ bởi dung dịch nước vôi trong dư thu được 1 gam kết tủa. Biết các phản ứng trên xảy ra hoàn toàn. Giá trị của m là
A, 1,970.
B, 3,940.
C, 2,955.
D, 4,925.
HD: Phản ứng: (Fe; O) + 0,14 mol H2SO4 → Fe2(SO4)3 + 0,065 mol SO2↑ + H2O.
Bảo toàn electron mở rộng: ∑nH+ = 4nSO2 + 2nO trong Y ⇒ nO trong Y = 0,01 mol.
Lại có theo bảo toàn nguyên tố S ⇒ nFe2(SO4)3 = 0,025 mol ⇒ nFe = 0,05 mol.
Quan sát: 0,05 mol FeO ⇝ (0,05 mol Fe; 0,01 mol O) ||⇒ nO bị CO, H2 lấy = 0,04 mol.
Tinh tế xử lí nhẹ nhàng bài toán khí than ướt: C + H2O → (CO; H2) + CO2.
Cần 0,04 mol O để chuyển hết (CO; H2) → CO2 + H2O ⇒ nC = 0,02 mol.
Lại có Z chứa 0,01 mol CO2 (do Z tạo 1 gam kết tủa với Ca(OH)2 dư)
⇒ nCO2 trong X = 0,01 mol ⇒ m gam kết tủa là 0,01 mol BaCO3 ⇒ m = 1,97 gam. ❒
Bảo toàn electron mở rộng: ∑nH+ = 4nSO2 + 2nO trong Y ⇒ nO trong Y = 0,01 mol.
Lại có theo bảo toàn nguyên tố S ⇒ nFe2(SO4)3 = 0,025 mol ⇒ nFe = 0,05 mol.
Quan sát: 0,05 mol FeO ⇝ (0,05 mol Fe; 0,01 mol O) ||⇒ nO bị CO, H2 lấy = 0,04 mol.
Tinh tế xử lí nhẹ nhàng bài toán khí than ướt: C + H2O → (CO; H2) + CO2.
Cần 0,04 mol O để chuyển hết (CO; H2) → CO2 + H2O ⇒ nC = 0,02 mol.
Lại có Z chứa 0,01 mol CO2 (do Z tạo 1 gam kết tủa với Ca(OH)2 dư)
⇒ nCO2 trong X = 0,01 mol ⇒ m gam kết tủa là 0,01 mol BaCO3 ⇒ m = 1,97 gam. ❒
Câu 35 [352140]: Hỗn hợp E gồm hai hiđrocacbon mạch hở X, Y biết MX < MY. Cho 0,15 mol E, có khối lượng 5,3 gam, vào lượng dư dung dịch AgNO3 trong NH3 thu được 26,7 gam hỗn hợp kết tủa. Biết các phản ứng xảy ra hoàn toàn. Phần trăm khối lượng của Y trong E là
A, 50,24%.
B, 68,23%.
C, 75,47%.
D, 53,96%.
* Áp dụng ĐLBTKL và tỉ lệ của AgNO3; NH3 và NH4NO3 đều bằng nhau.
→
Ta có:
→ Trong E chứa 2 ankin: Đặt ankin phản ứng với AgNO3 theo tỉ lệ 1 : 1 là B và ankin phản ứng với AgNO3 theo tỉ lệ 1 : 2 là A.
Ta có E gồm: A (a mol) và B (b mol).
a + b = 0,15. → a = 0,05.
2a + b = 0,2. → b = 0,1.
Theo đề bài: ME = 5,3 : 0,15 = 35,3 → Trong E có HC≡CH (0,05) và R-C≡CH (0,1).
Ta có: 0,05×26 + (R+25)×0,1 = 5,3 → R = 15 (CH3).
Vậy
→ Chọn đáp án C.
→

Ta có:

→ Trong E chứa 2 ankin: Đặt ankin phản ứng với AgNO3 theo tỉ lệ 1 : 1 là B và ankin phản ứng với AgNO3 theo tỉ lệ 1 : 2 là A.
Ta có E gồm: A (a mol) và B (b mol).
a + b = 0,15. → a = 0,05.
2a + b = 0,2. → b = 0,1.
Theo đề bài: ME = 5,3 : 0,15 = 35,3 → Trong E có HC≡CH (0,05) và R-C≡CH (0,1).
Ta có: 0,05×26 + (R+25)×0,1 = 5,3 → R = 15 (CH3).
Vậy

→ Chọn đáp án C.
Câu 36 [352141]: Phân tích nguyên tố và phân tích phổ khối lượng (phổ MS) hai hợp chất hữu cơ mạch hở E, F cho cùng kết quả phần trăm khối lượng cacbon, hiđro, oxi lần lượt là 40,68%; 5,08%; 54,24% và cùng có phân tử khối bằng 118. Từ E, F thực hiện sơ đồ các phản ứng sau theo đúng tỉ lệ mol:
E + 2NaOH → 2Y + Z; F + 2NaOH → Y + T + X
Biết: X và Z là các ancol có số nhóm chức khác nhau; T là chất hữu cơ no, mạch hở.
Phát biểu nào sau đây đúng?
E + 2NaOH → 2Y + Z; F + 2NaOH → Y + T + X
Biết: X và Z là các ancol có số nhóm chức khác nhau; T là chất hữu cơ no, mạch hở.
Phát biểu nào sau đây đúng?
A, Có hai công thức cấu tạo thoả mãn tính chất của E.
B, Chất X có khả năng tham gia phản ứng tráng bạc.
C, Chất Z thuộc dãy đồng đẳng ancol etylic.
D, Phân tử T có số nguyên tử hiđro và oxi bằng nhau.
Đặt CTPT của E và F là CxHyOz.
 → x = 4.
→ x = 4.
 → y = 6.
→ y = 6.
 → z = 4.
→ z = 4.
Vậy CTPT của E và F là C4H6O4 (k = 2).
F tạo 3 sản phẩm hữu cơ nên CTCT của F phải là:
HCOO-CH2COO-CH3 (F) + 2NaOH → HCOONa (Y) + HO-CH2COONa (T) + CH3OH (X).
E phản ứng với 2NaOH tạo ra 2Y và ancol Z.
(HCOO)2C2H4 (E) + 2NaOH → 2HCOONa (Y) + C2H4(OH)2 (Z) .
❌ A. Sai vì E chỉ có 1 công thức cấu tạo duy nhất.
❌ B. Sai vì X là CH3OH không tham gia phản ứng tráng bạc.
❌ C. Sai vì Z là C2H4(OH)2, không thuộc dãy đồng đẳng của ancol etylic C2H5OH.
✔️ D. Đúng vì T có CTPT C2H3O3Na, số nguyên tử H bằng số nguyên tử O.
→ Chọn đáp án D.
 → x = 4.
→ x = 4.
 → y = 6.
→ y = 6.
 → z = 4.
→ z = 4.
Vậy CTPT của E và F là C4H6O4 (k = 2).
F tạo 3 sản phẩm hữu cơ nên CTCT của F phải là:
HCOO-CH2COO-CH3 (F) + 2NaOH → HCOONa (Y) + HO-CH2COONa (T) + CH3OH (X).
E phản ứng với 2NaOH tạo ra 2Y và ancol Z.
(HCOO)2C2H4 (E) + 2NaOH → 2HCOONa (Y) + C2H4(OH)2 (Z) .
❌ A. Sai vì E chỉ có 1 công thức cấu tạo duy nhất.
❌ B. Sai vì X là CH3OH không tham gia phản ứng tráng bạc.
❌ C. Sai vì Z là C2H4(OH)2, không thuộc dãy đồng đẳng của ancol etylic C2H5OH.
✔️ D. Đúng vì T có CTPT C2H3O3Na, số nguyên tử H bằng số nguyên tử O.
→ Chọn đáp án D.
Câu 37 [906774]: Hỗn hợp E gồm ba este mạch hở X, Y, Z trong đó có một este hai chức và hai este đơn chức, MX < MY < MZ. Cho 24,66 gam E tác dụng hoàn toàn với dung dịch NaOH dư, thu được hỗn hợp gồm các ancol no và 26,42 gam hỗn hợp muối của hai axit cacboxylic kế tiếp nhau trong dãy đồng đẳng. Khi đốt cháy hoàn toàn 24,66 gam E thì cần 1,285 mol O2, thu được H2O và 1,09 mol CO2. Khối lượng của X trong 24,66 gam E là
A, 5,18 gam.
B, 6,16 gam.
C, 2,96 gam.
D, 3,48 gam.
HD: ☆ Giải đốt E gồm 1,09 mol C + 0,99 mol H2 + 0,3 mol O2.
có este đơn chức nên ⇒ 2 axit đồng đẳng đều đơn chức. Muối dạng RCOONa.
mmuối = 26,42 gam ⇒ Mmuối = 26,42 ÷ 0,3 ≈ 88,07.
⇒ Cho biết hai muối với số mol là 0,17 mol CH3COONa và 0,13 mol C2H5COONa.
Bảo toàn C, H, O ⇒ Thành phần ancol gồm 0,36 mol C + 0,56 mol H2 + 0,3 mol O.
⇒ nancol hai chức = nancol đơn chức = 0,1 mol.
Nếu số C ancol hai chức ≥ 3 thì Cancol đơn chức < (0,36 – 0,1 × 3) ÷ 0,1 = 0,6 không thoả mãn
⇒ Cancol hai chức = 2 tương ứng là C2H4(OH)2.
Vậy, este 2 chức Z chỉ có thể là CH3COOCH2CH2OOCC2H5: 0,1 mol.
⇒ hai este còn lại là 0,07 mol CH3COOR và 0,03 mol C2H5COOR'.
Nghiệm nguyên: 0,07CR + 0,03CR' = 0,16 ⇄ 7CR + 3CR' = 16 ⇒ CR = 1 và CR' = 3.
⇒ Tương ứng có 0,07 mol CH3COOCH3 (X) và 0,03 mol C2H5COOC3H7 (Y).
⇒ Yêu cầu mX trong E = 0,07 × 74 = 5,18 gam.
có este đơn chức nên ⇒ 2 axit đồng đẳng đều đơn chức. Muối dạng RCOONa.
mmuối = 26,42 gam ⇒ Mmuối = 26,42 ÷ 0,3 ≈ 88,07.
⇒ Cho biết hai muối với số mol là 0,17 mol CH3COONa và 0,13 mol C2H5COONa.
Bảo toàn C, H, O ⇒ Thành phần ancol gồm 0,36 mol C + 0,56 mol H2 + 0,3 mol O.
⇒ nancol hai chức = nancol đơn chức = 0,1 mol.
Nếu số C ancol hai chức ≥ 3 thì Cancol đơn chức < (0,36 – 0,1 × 3) ÷ 0,1 = 0,6 không thoả mãn
⇒ Cancol hai chức = 2 tương ứng là C2H4(OH)2.
Vậy, este 2 chức Z chỉ có thể là CH3COOCH2CH2OOCC2H5: 0,1 mol.
⇒ hai este còn lại là 0,07 mol CH3COOR và 0,03 mol C2H5COOR'.
Nghiệm nguyên: 0,07CR + 0,03CR' = 0,16 ⇄ 7CR + 3CR' = 16 ⇒ CR = 1 và CR' = 3.
⇒ Tương ứng có 0,07 mol CH3COOCH3 (X) và 0,03 mol C2H5COOC3H7 (Y).
⇒ Yêu cầu mX trong E = 0,07 × 74 = 5,18 gam.
Câu 38 [24420]: Cho các phát biểu sau:
(a) Muối mononatri của axit glutamic là thành phần chính của bột ngọt.
(b) Liên kết peptit là liên kết -CONH- giữa hai gốc α- aminoaxit.
(c) Trong phân tử tetrapeptit Ala-Glu-Val-Gly, amino axit đầu C là Ala.
(d) Tất cả các protein đều tan trong nước tạo thành dung dịch keo.
(e) Thủy phân hoàn toàn protein đơn giản thu được các α- aminoaxit.
Số phát biểu đúng là
(a) Muối mononatri của axit glutamic là thành phần chính của bột ngọt.
(b) Liên kết peptit là liên kết -CONH- giữa hai gốc α- aminoaxit.
(c) Trong phân tử tetrapeptit Ala-Glu-Val-Gly, amino axit đầu C là Ala.
(d) Tất cả các protein đều tan trong nước tạo thành dung dịch keo.
(e) Thủy phân hoàn toàn protein đơn giản thu được các α- aminoaxit.
Số phát biểu đúng là
A, 2.
B, 4.
C, 5.
D, 3.
Trong phân tử tetrapeptit Ala-Glu-Val-Gly, amino axit đầu C là Gly → c sai
protein dạng sừng không tan trong nước → d sai
Đáp án D.
protein dạng sừng không tan trong nước → d sai
Đáp án D.
Câu 39 [352667]: Cho rất từ từ 300 ml dung dịch HCl 1M vào 200 ml dung dịch X chứa Na2CO3 và NaHCO3, thu được 500 ml dung dịch Y và khí CO2. Sự phụ thuộc của số mol khí CO2 (a mol) vào thể tích dung dịch HCl 1M (V ml) được biểu diễn theo đồ thị bên. Biết dung dịch Y có pH = 1. Nếu cho rất từ từ 200 ml dung dịch X vào 175 ml dung dịch HCl 1M, thu được b mol CO2. Giá trị của b là
A, 0,095.
B, 0,140.
C, 0,125.
D, 0,130.
Dung dịch X gồm Na2CO3 (a mol) và NaHCO3 (b mol).
Khi cho từ từ HCl vào dung dịch X
Sau phản ứng, dung dịch Y có pH = 1 < 7 → môi trường axit → HCl dư.
Ta có pH = 1 → CH+ = 0,1 (M) → nH+ = 0,1×0,5 = 0,05 mol.
Ta có: 0,3 - (2a + b) = 0,05. (I)
Mặt khác: số mol khí CO2 = 0,2 → a + b = 0,2. (II)
Từ (I) và (II) → a = 0,05 và b = 0,15.
Suy ra trong dung dịch X: tỉ lệ Na2CO3 và NaHCO3 là 1 : 3.
Khi cho 200 ml X vào dung dịch HCl thì Na2CO3 và NaHCO3 ngay lập tức sẽ phản ứng với HCl.
Ta có: 5k = 0,175 → k = 0,035.
Vậy nCO2 = 4k = 4×0,035= 0,14 mol.
Khi cho từ từ HCl vào dung dịch X

Sau phản ứng, dung dịch Y có pH = 1 < 7 → môi trường axit → HCl dư.
Ta có pH = 1 → CH+ = 0,1 (M) → nH+ = 0,1×0,5 = 0,05 mol.
Ta có: 0,3 - (2a + b) = 0,05. (I)
Mặt khác: số mol khí CO2 = 0,2 → a + b = 0,2. (II)
Từ (I) và (II) → a = 0,05 và b = 0,15.
Suy ra trong dung dịch X: tỉ lệ Na2CO3 và NaHCO3 là 1 : 3.
Khi cho 200 ml X vào dung dịch HCl thì Na2CO3 và NaHCO3 ngay lập tức sẽ phản ứng với HCl.

Ta có: 5k = 0,175 → k = 0,035.
Vậy nCO2 = 4k = 4×0,035= 0,14 mol.
Câu 40 [352142]: PMMA hay poli(metyl metacrylat) là một polime được điều chế từ metyl metacrylat. PMMA được sử dụng để sản xuất nhiều loại nhựa dẻo, trong đó có tấm nhựa mica. Tấm nhựa Mica có thể trong suốt hoặc có nhiều màu sắc, mang đến nhiều sự lựa chọn đa dạng khác nhau trong nghành dịch vụ. Tấm Mica trong suốt thường được so sánh với kính hay thủy tinh. Nó có tỷ trọng chỉ bằng 1 nửa so với thủy tinh, ánh sáng có thể đi xuyên qua 98%, cực kì bền, khó rạn nứt.
Cho các phát biểu sau:
(a) PPMA có thành phần nguyên tố hóa học giống thủy tinh vô cơ.
(b) Các phân tử metyl metacrylat kết hợp với nhau và tách đi các phân tử nước để hình thành PPMA.
(c) PPMA thuộc loại polieste.
(d) Phản ứng tổng hợp PPMA từ metyl metacrylat là phản ứng trùng hợp.
(e) Trong một mắt xích PCA, phần trăm khối lượng cacbon là 69,78%.
Số phát biểu đúng là
Cho các phát biểu sau:
(a) PPMA có thành phần nguyên tố hóa học giống thủy tinh vô cơ.
(b) Các phân tử metyl metacrylat kết hợp với nhau và tách đi các phân tử nước để hình thành PPMA.
(c) PPMA thuộc loại polieste.
(d) Phản ứng tổng hợp PPMA từ metyl metacrylat là phản ứng trùng hợp.
(e) Trong một mắt xích PCA, phần trăm khối lượng cacbon là 69,78%.
Số phát biểu đúng là
A, 2.
B, 3.
C, 4.
D, 1.
❌ (a) Sai vì PPMA có thành phần nguyên tố hóa học là C, H, O còn thủy tinh vô cơ là SiO2, thành phần nguyên tố là Si và O.
❌ (b) Sai vì các phân tử metyl metacrylat kết hợp với nhau để hình thành PPMA theo phản ứng trùng hợp nên không tách ra các phân tử H2O.
❌ (c) Sai vì các mắt xích được liên kết với nhau bằng nhóm COO thì sẽ tạo thành polieste còn PPMA chỉ chứa nhóm COO trong phân tử.
✔️ (d) Đúng vì metyl metacrylat chứa nối đôi, các phân tử sẽ kết hợp với nhau tạo thành PPMA theo phản ứng trùng hợp.
❌ (e) Sai vì một mắt xích PPMA là C5H8O2.
→
❌ (b) Sai vì các phân tử metyl metacrylat kết hợp với nhau để hình thành PPMA theo phản ứng trùng hợp nên không tách ra các phân tử H2O.
❌ (c) Sai vì các mắt xích được liên kết với nhau bằng nhóm COO thì sẽ tạo thành polieste còn PPMA chỉ chứa nhóm COO trong phân tử.
✔️ (d) Đúng vì metyl metacrylat chứa nối đôi, các phân tử sẽ kết hợp với nhau tạo thành PPMA theo phản ứng trùng hợp.
❌ (e) Sai vì một mắt xích PPMA là C5H8O2.
→
