Đáp án
1A
2D
3A
4A
5B
6C
7A
8D
9A
10D
11C
12C
13B
14B
15A
16C
17C
18B
19D
20A
21D
22A
23C
24D
25C
26D
27C
28C
29C
30B
31D
32B
33B
34D
35B
36B
37D
38B
39B
40B
Đáp án Đề minh họa số 25 thi Tốt Nghiệp Trung học Phổ Thông 2024 môn Hóa học
Câu 1 [225757]: Chất nào sau đây tác dụng với dung dịch NaOH, tạo ra kết tủa?
A, MgCl2.
B, CO2.
C, HNO3.
D, KNO3.
HD: Các phản ứng hoá học xảy ra:
✔️ A. MgCl2 + 2NaOH → Mg(OH)2 + 2NaCl.
❌ B. CO2 + 2NaOH → Na2CO3 + H2O.
❌ C. HNO3 + NaOH → NaNO3 + H2O.
❌ D. KNO3 + NaOH → không xảy ra phản ứng.
✔️ A. MgCl2 + 2NaOH → Mg(OH)2 + 2NaCl.
❌ B. CO2 + 2NaOH → Na2CO3 + H2O.
❌ C. HNO3 + NaOH → NaNO3 + H2O.
❌ D. KNO3 + NaOH → không xảy ra phản ứng.
Câu 2 [20983]: Loại dầu, mỡ nào dưới đây không phải là lipit?
A, Mỡ động vật.
B, Dầu thực vật.
C, Dầu cá.
D, Dầu mazut.
HD: Dầu mazut là một loại hiđrocacbon (thành phần C, H)
⇒ dầu mazut không phải là lipit.!
còn lại, mỡ động vật, dầu thực vật, dầu cá là chất béo; một thành phần của lipit. ❒
⇒ dầu mazut không phải là lipit.!
còn lại, mỡ động vật, dầu thực vật, dầu cá là chất béo; một thành phần của lipit. ❒
Câu 3 [340748]: Chất nào sau đây thuộc loại ancol đa chức?
A, Etylenglicol.
B, Phenol.
C, Etanol.
D, Etanđial.
HD: Phân tích các đáp án - cấu tạo tương ứng với tên gọi:
• A. Etylen glicol: C2H4(OH)2: ancol hai chức.
• B. Phenol: C6H5OH: thuộc dãy đồng đẳng phenol.
• C. Etanol: C2H5OH: ancol đơn chức.
• D. Etanđial: (CHO)2: anđehit hai chức.
• A. Etylen glicol: C2H4(OH)2: ancol hai chức.
• B. Phenol: C6H5OH: thuộc dãy đồng đẳng phenol.
• C. Etanol: C2H5OH: ancol đơn chức.
• D. Etanđial: (CHO)2: anđehit hai chức.
Câu 4 [679258]: Thủy phân hoàn toàn 1 mol peptit mạch hở X chỉ thu được 3 mol Gly và 1 mol Ala. Số liên kết peptit trong phân tử X là
A, 3.
B, 4.
C, 2.
D, 1.
Chọn đáp án A.
Một cấu tạo thỏa mãn của X là Gly–Gly–Gly–Ala → có 3 liên kết peptit trong phân tử.
Một cấu tạo thỏa mãn của X là Gly–Gly–Gly–Ala → có 3 liên kết peptit trong phân tử.
Câu 5 [679708]: Chất nào sau đây làm mềm được nước có tính cứng vĩnh cửu?
A, NaCl.
B, Na2CO3.
C, NaNO3.
D, Na2SO4.
HD: Dung dịch muối Na2CO3 có ion CO32– kết tủa được các ion Ca2+; Mg2+ làm mềm nước cứng:
☆ Phản ứng: Ca2+ + CO32– → CaCO3↓.
☆ Phản ứng: Ca2+ + CO32– → CaCO3↓.
Câu 6 [60261]: Kim loại Al không tan trong dung dịch nào sau đây?
A, HCl.
B, NaOH.
C, NaCl.
D, H2SO4 loãng.
Giải: Ta có các phản ứng:
2Al + 6HCl → 2AlCl3 + 3H2
2Al + 2NaOH + 2H2O → 2NaAlO2 + 3H2
2Al + 3H2SO4 → Al2(SO4)3 + 3H2
⇒ Chọn C
2Al + 6HCl → 2AlCl3 + 3H2
2Al + 2NaOH + 2H2O → 2NaAlO2 + 3H2
2Al + 3H2SO4 → Al2(SO4)3 + 3H2
⇒ Chọn C
Câu 7 [57685]: Kim loại X dẫn điện tốt nhất ở nhiệt độ thường. Kim loại Y có nhiệt độ nóng chảy cao, dùng làm dây tóc bóng đèn. Kim loại X, Y lần lượt là
A, Ag, W.
B, Cu, W.
C, Ag, Cr.
D, Au, W.
Giải: Kim loại dẫn nhiệt tốt nhất là bạc (Ag).
Kim loại có tonc cao nhất là Wolfram (W).
⇒ Chọn A
Kim loại có tonc cao nhất là Wolfram (W).
⇒ Chọn A
Câu 8 [228867]: Cho Fe tác dụng với lượng dư dung dịch chất X (loãng), thu được muối sắt(III). Chất X là
A, CuSO4.
B, NaNO3.
C, H2SO4.
D, AgNO3.
HD: Phân tích các đáp án:
❌ A. Fe + CuSO4 → FeSO4 (sắt(II) sunfat) + Cu.
❌ B. Fe + NaNO3 → không xảy ra phản ứng.
❌ C. Fe + H2SO4 → FeSO4 (sắt(II) sunfat) + H2↑.
✔️ D. Fe + 2AgNO3 → Fe(NO3)2 + 2Ag↓.
Sau đó do AgNO3 dư nên: Fe(NO3)2 + AgNO3 → Fe(NO3)3 (sắt(III) nitrat) + Ag↓.
❌ A. Fe + CuSO4 → FeSO4 (sắt(II) sunfat) + Cu.
❌ B. Fe + NaNO3 → không xảy ra phản ứng.
❌ C. Fe + H2SO4 → FeSO4 (sắt(II) sunfat) + H2↑.
✔️ D. Fe + 2AgNO3 → Fe(NO3)2 + 2Ag↓.
Sau đó do AgNO3 dư nên: Fe(NO3)2 + AgNO3 → Fe(NO3)3 (sắt(III) nitrat) + Ag↓.
Câu 9 [58152]: Kim loại M phản ứng được với dung dịch HCl, với dung dịch HNO3 đặc nguội. Kim loại M là
A, Mg.
B, Ag.
C, Fe.
D, Al.
HD:
Ag không phản ứng với HCl, phản ứng được với HNO3 đặc nguội.
Fe, Al phản ứng với HCl, không phản ứng với HNO3 đặc nguội.
Chỉ có Mg thỏa mãn.
Ag không phản ứng với HCl, phản ứng được với HNO3 đặc nguội.
Fe, Al phản ứng với HCl, không phản ứng với HNO3 đặc nguội.
Chỉ có Mg thỏa mãn.
Câu 10 [982008]: Chất X có công thức Fe(NO3)2. Tên gọi của X là
A, sắt(III) oxit.
B, sắt(III) nitrat.
C, sắt(II) oxit.
D, sắt(II) nitrat.
HD: Phân tích các đáp án:
| Tên gọi | A. sắt(III) oxit. | B. sắt(III) nitrat. | C. sắt(II) oxit. | D. sắt(II) nitrat. |
| Công thức | Fe2O3 | Fe(NO3)3 | FeO | Fe(NO3)2 (✔️) |
Câu 11 [679851]: Chất X có công thức H2NCH(CH3)COOH. Tên gọi của X là
A, glyxin.
B, valin.
C, alanin.
D, lysin.
HD: Phân tích các đáp án:
| Hợp chất | Glyxin | Valin | Alanin | Lysin |
| Cấu tạo | H2NCH2COOH | H2NC4H9COOH | H2NCH(CH3)COOH | (H2N)2C5H9COOH |
| ❌ | ❌ | ✔️ | ❌ |
Câu 12 [228627]: Hai kim loại Mg và Ba thuộc phân nhóm nào sau đây trong bảng tuần hoàn?
A, IA.
B, IIIA.
C, IIA.
D, VA.
Đáp án: C
Câu 13 [911581]: Chất nào sau đây là muối axit?
A, KNO3.
B, NaHSO4.
C, NaCl.
D, Na2SO4.
HD: ► Muối axit là muối vẫn còn hiđro có khả năng phân li ra H+. Ví dụ: NaHCO3; KHSO4; NaH2PO4; K2HPO4;...
⇒ NaHSO4 là muối axit: NaHSO4 ⇄ Na+ + H+ + SO42–.
⇒ NaHSO4 là muối axit: NaHSO4 ⇄ Na+ + H+ + SO42–.
Câu 14 [906795]: Ion kim loại nào sau đây có tính oxi hóa mạnh nhất?
A, K+.
B, Ag+.
C, Mg2+.
D, Fe2+.
Thứ tự tính oxi hóa: K+ < Mg2+ < Fe2+ < Ag+.
Câu 15 [679754]: Este nào sau đây tác dụng với NaOH thu được ancol etylic?
A, CH3COOC2H5.
B, CH3COOC3H7.
C, C2H5COOCH3.
D, HCOOCH3.
HD: Ancol etylic có cấu tạo là C2H5OH. Phân tích các đáp án:
✔️ A. CH3COOC2H5 + NaOH → CH3COONa + C2H5OH.
❌ B. CH3COOC3H7 + NaOH → CH3COONa + C3H7OH.
❌ C. C2H5COOCH3 + NaOH → C2H5COONa + CH3OH.
❌ D. HCOOCH3 + NaOH → HCOONa + CH3OH.
✔️ A. CH3COOC2H5 + NaOH → CH3COONa + C2H5OH.
❌ B. CH3COOC3H7 + NaOH → CH3COONa + C3H7OH.
❌ C. C2H5COOCH3 + NaOH → C2H5COONa + CH3OH.
❌ D. HCOOCH3 + NaOH → HCOONa + CH3OH.
Câu 16 [334036]: Policrilonitrin có thành phân hóa học gồm các nguyên tố là
A, C, H.
B, C, H, Cl.
C, C, H. N.
D, C, H, N, O.
HD: Policrilonitrin được trùng hợp từ monome acrilonitrin có công thức CH2=CH-CN.
||→ thành phần hóa học chỉ gồm 3 nguyên tố là C, H, N. Chọn đáp án C. ♣.
||→ thành phần hóa học chỉ gồm 3 nguyên tố là C, H, N. Chọn đáp án C. ♣.
Câu 17 [906778]: Khí thải của một số nhà máy có chứa khí sunfurơ gây ô nhiễm không khí. Công thức của khí sunfurơ là
A, H2S.
B, NO2.
C, SO2.
D, NO.
★ Tránh nhầm lẫn: H2S là khí hiđro sunfua; còn khí sunfurơ là SO2.
Câu 18 [981881]: Kim loại nào sau đây được điều chế bằng phương pháp điện phân nóng chảy?
A, Cu.
B, K.
C, Au.
D, Ag.
HD: Trong dãy hoạt động các kim loại, từ Li → Al: các kim loại được điều chế bằng pp điện phân nóng chảy.
Câu 19 [223316]: Kim loại kiềm được dùng làm tế bào quang điện là
A, Kali.
B, Liti.
C, Natri.
D, Xesi.
Xesi là kim loại được dùng làm tế bào quang điện.
Câu 20 [679360]: [THPTQG 2018]: Fructozơ là một loại monosaccarit có nhiều trong mật ong, có vị ngọt sắc. Công thức phân tử của fructozơ là
A, C6H12O6.
B, (C6H10O5)n.
C, C2H4O2.
D, C12H22O11.
Fructozơ và glucozơ là đồng phân, có cùng công thức phân tử là C6H12O6 (M = 180).
Câu 21 [11866]: Để phân biệt glucozơ và saccarozơ, người ta dùng thuốc thử nào sau đây?
A, Dung dịch HCl.
B, Dung dịch H2SO4.
C, H2 (xúc tác Ni, đun nóng).
D, Dung dịch AgNO3 trong NH3.
HD: Glucozơ có phản ứng tráng bạc (tác dụng với AgNO3/NH3):

Hiện tượng: xuất hiện kết tủa màu tráng bạc Ag.
Còn saccarozơ không có phản ứng xảy ra. ❒

Hiện tượng: xuất hiện kết tủa màu tráng bạc Ag.
Còn saccarozơ không có phản ứng xảy ra. ❒
Câu 22 [8380]: Xà phòng hóa hoàn toàn 17,6 gam CH3COOC2H5 trong dung dịch NaOH (vừa đủ), thu được dung dịch chứa m gam muối. Giá trị của m là
A, 16,4.
B, 9,6.
C, 19,2.
D, 8,2.
Giải: Ta có phản ứng: CH3COOC2H5 + NaOH → CH3COONa + C2H5OH.
Mà nEste = 17,6 ÷ 88 = 0,2 mol ⇒ nCH3COONa = 0,2 mol.
⇒ mMuối = 0,2 × (15 + 44 + 23) = 16,4 gam ⇒ Chọn A
Mà nEste = 17,6 ÷ 88 = 0,2 mol ⇒ nCH3COONa = 0,2 mol.
⇒ mMuối = 0,2 × (15 + 44 + 23) = 16,4 gam ⇒ Chọn A
Câu 23 [353449]: Cho hỗn hợp gồm Fe và FeCO3 phản ứng với lượng dư dung dịch H2SO4 loãng, sau phản ứng thu được dung dịch chứa muối nào sau đây?
A, Fe2(SO4)3.
B, Fe(OH)2.
C, FeSO4.
D, FeS.
PTHH xảy ra như sau:
Fe + H2SO4 → FeSO4 + H2
FeCO3 + H2SO4 →FeSO4 + CO2 + H2O
Muối thu được sau phản ứng là FeSO4.
Fe + H2SO4 → FeSO4 + H2
FeCO3 + H2SO4 →FeSO4 + CO2 + H2O
Muối thu được sau phản ứng là FeSO4.
Câu 24 [911516]: Cho m gam glucozơ (C6H12O6) tác dụng hết với lượng dư dung dịch AgNO3 trong NH3, thu được 3,24 gam Ag. Giá trị của m là
A, 1,35.
B, 1,80.
C, 5,40.
D, 2,70.
HD: Tỉ lệ tráng bạc: 1glucozơ –––AgNO3/NH3, to–→ 2Ag.
Giả thiết nAg = 0,03 mol ⇒ nglucozơ = 0,015 mol ⇒ m = 0,015 × 180 = 2,70 gam.
Giả thiết nAg = 0,03 mol ⇒ nglucozơ = 0,015 mol ⇒ m = 0,015 × 180 = 2,70 gam.
Câu 25 [120056]: Cho 1,17 gam một kim loại kiềm tác dụng với nước dư, sau phản ứng thu được 0,336 lít khí H2 (đktc). Kim loại kiềm là
A, Li.
B, Rb.
C, K.
D, Na.
HD: Phản ứng của kim loại kiềm M với nước: M + H2O → MOH + ½.H2↑.
Giả thiết nH2↑ = 0,015 mol ⇒ nM = 2 × 0,015 = 0,03 mol.
Mà mM = 1,17 gam ⇒ M = 1,17 ÷ 0,03 = 39 ⇝ cho biết M là kali (K). ❒
Giả thiết nH2↑ = 0,015 mol ⇒ nM = 2 × 0,015 = 0,03 mol.
Mà mM = 1,17 gam ⇒ M = 1,17 ÷ 0,03 = 39 ⇝ cho biết M là kali (K). ❒
Câu 26 [17225]: Cho 9,85 gam hỗn hợp gồm hai amin đơn chức tác dụng vừa đủ với V ml dung dịch HCl 1M, thu được dung dịch chứa 18,975 gam hỗn hợp muối. Giá trị của V là
A, 300.
B, 450.
C, 400.
D, 250.
HD: amin đơn chức nên 1 phân tử HCl "nhập" vào 1 phân tử amin tạo muối:
9,85 gam hỗn hợp hai amin + ? gam HCl → 18,975 gam hỗn hợp muối.
⇝ Bảo toàn khối lượng có mHCl = 9,125 gam ⇒ nHCl = 0,25 mol ⇒ V = 250 ml. ❒
9,85 gam hỗn hợp hai amin + ? gam HCl → 18,975 gam hỗn hợp muối.
⇝ Bảo toàn khối lượng có mHCl = 9,125 gam ⇒ nHCl = 0,25 mol ⇒ V = 250 ml. ❒
Câu 27 [982794]: Có bao nhiêu polime được điều chế bằng phản ứng trùng hợp trong các polime: polietilen, poli(vinyl clorua), poli(metyl metacrylat), poliacrilonitrin?
A, 1.
B, 2.
C, 4.
D, 3.
HD: Bài học điều chế polime tổng hợp:
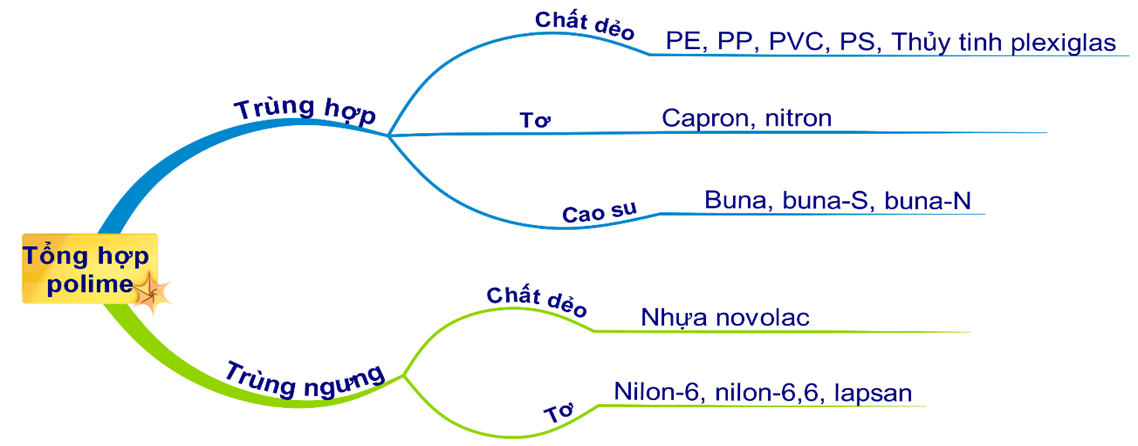
⇝ Tất cả các polime trong dãy: polietilen, poli(vinyl clorua), poli(metyl metacrylat), poliacrilonitrin đều điều chế được bẳng phản ứng trùng hợp.

⇝ Tất cả các polime trong dãy: polietilen, poli(vinyl clorua), poli(metyl metacrylat), poliacrilonitrin đều điều chế được bẳng phản ứng trùng hợp.
Câu 28 [62509]: Phản ứng giữa các chất nào sau đây không tạo ra hai muối?
A, NO2 và dung dịch NaOH dư.
B, Ba(HCO3)2 và dung dịch KOH dư.
C, Fe3O4 và dung dịch HNO3 dư.
D, Fe3O4 và dung dịch HCl dư.
HD: 2NO2 + 2NaOH → NaNO2 + NaNO3 + H2O.
Ba(HCO3)2 + 2KOH → K2CO3 + BaCO3 + 2H2O.
3Fe3O4 + 28HNO3 → 9Fe(NO3)3 + NO + 14H2O.
Fe3O4 + 8HCl → FeCl2 + 2FeCl3 + 4H2O.
Ba(HCO3)2 + 2KOH → K2CO3 + BaCO3 + 2H2O.
3Fe3O4 + 28HNO3 → 9Fe(NO3)3 + NO + 14H2O.
Fe3O4 + 8HCl → FeCl2 + 2FeCl3 + 4H2O.
Câu 29 [135843]: Cho 2,38 gam hỗn hợp gồm Zn và Al phản ứng vừa đủ với dung dịch H2SO4 loãng, thu được m gam muối trung hòa và 1,792 lít khí H2 (đktc). Giá trị của m là
A, 8,52.
B, 14,16.
C, 10,06.
D, 10,22.
HD: cả Zn và Al đều phản ứng với dung dịch H2SO4 loãng :
Zn + H2SO4 → ZnSO4 + H2↑ || 2Al + 3H2SO4 → Al2(SO4)3 + 3H2↑.
gọi nZ = x mol; nAl = y mol ⇒ 65x + 27y = 2,38 gam.
từ phương trình phản ứng có: x + 1,5y = ∑nH2↑ = 0,08 mol.
⇒ giải hệ được x = 0,02 mol; y = 0,04 mol.
⇒ m = mmuối = 161x + 171y = 10,06 gam.
➤ nhanh hơn: để ý ∑nSO42– trong muối = nH2 = 0,08 mol.
⇒ m = mmuối = mkim loại + mSO42– = 2,38 + 0,08 × 96 = 10,06 gam.
Zn + H2SO4 → ZnSO4 + H2↑ || 2Al + 3H2SO4 → Al2(SO4)3 + 3H2↑.
gọi nZ = x mol; nAl = y mol ⇒ 65x + 27y = 2,38 gam.
từ phương trình phản ứng có: x + 1,5y = ∑nH2↑ = 0,08 mol.
⇒ giải hệ được x = 0,02 mol; y = 0,04 mol.
⇒ m = mmuối = 161x + 171y = 10,06 gam.
➤ nhanh hơn: để ý ∑nSO42– trong muối = nH2 = 0,08 mol.
⇒ m = mmuối = mkim loại + mSO42– = 2,38 + 0,08 × 96 = 10,06 gam.
Câu 30 [6785]: Phát biểu nào sau đây không đúng?
A, Isoamyl axetat có mùi thơm của chuối chín.
B, Các este thường dễ tan trong nước.
C, Benzyl axetat có mùi thơm của hoa nhài.
D, Một số este của axit terephtalic được dùng làm chất dẻo.
HD: ► Bài học về tính chất vật lý của este:

⇒ các phát biểu A và C đúng, B sai. Phát biểu D đúng. Chương trình có nhắc đến poli(etylen terephtalat) đó vừa là tơ sợi, vừa là chất dẻo có ứng dụng phổ biến. Tham khảo nguồn

⇒ các phát biểu A và C đúng, B sai. Phát biểu D đúng. Chương trình có nhắc đến poli(etylen terephtalat) đó vừa là tơ sợi, vừa là chất dẻo có ứng dụng phổ biến. Tham khảo nguồn
Câu 31 [233901]: Hỗn hợp E gồm Fe, Fe3O4, Fe2O3 và FeS2. Nung 19,36 gam E trong bình kín chứa 0,245 mol O2 thu được chất rắn X (chỉ gồm Fe và các oxit) và 0,15 mol khí SO2. Hòa tan hết X trong dung dịch HCl nồng độ 5,84% thu được 1,68 lít khí H2 và dung dịch Y chỉ chứa muối. Cho tiếp dung dịch AgNO3 dư vào Y thu được 102,3 gam kết tủa gồm Ag và AgCl. Biết các phản ứng xảy ra hoàn toàn. Nồng độ phần trăm của muối FeCl2 trong Y gần nhất với giá trị nào sau đây?
A, 3,82%.
B, 3,54%.
C, 4,14%.
D, 4,85%.
HD: 19,36 gam E + 0,245 mol O2 → X + 0,15 mol SO2.
⇒ BTKL ta có ngay mX = 19,36 + 0,245 × 32 – 0,15 × 64 = 17,6 gam.
Xét toàn bộ quá trình X (Fe; O) + HCl, sau đó AgNO3 dư → (Ag; AgCl)↓ + Fe(NO3)3 + H2↑ + H2O.
Gọi nFe/X = a mol và nO/X = b mol thì 56a + 16b = 17,6.
Bảo toàn electron: 3nFe = 2nH2 + 2nO/X + nAg ⇒ nAg = (3a – 2b – 0,15) mol.
Lại có nH2O = b mol ⇒ nHCl = (2b + 0,15) mol theo bảo toàn O và H.
⇒ nAgCl = nCl– = (2b + 0,15) mol ⇒ ∑m↓ = 143,5 × (2b + 0,15) + 108 × (3a – 2b – 0,15) = 102,3.
⇒ Giải hệ các phương trình ta được: a = 0,25 mol và b = 0,225 mol.
Vậy, kết tủa gồm 0,15 mol Ag và 0,6 mol AgCl.
⇒ Trực tiếp sinh ra Ag là do 0,15 mol FeCl2 trong Y.
Lại có ∑nHCl = 0,6 mol ⇒ mdung dịch HCl = 375 gam.
⇒ mdung dịch Y = mdung dịch HCl + mX – mH2↑ = 392,45 gam.
⇒ Yêu cầu C%mFeCl2 trong Y = 0,15 × 127 ÷ 392,45 × 100% ≈ 4,85%.
⇒ BTKL ta có ngay mX = 19,36 + 0,245 × 32 – 0,15 × 64 = 17,6 gam.
Xét toàn bộ quá trình X (Fe; O) + HCl, sau đó AgNO3 dư → (Ag; AgCl)↓ + Fe(NO3)3 + H2↑ + H2O.
Gọi nFe/X = a mol và nO/X = b mol thì 56a + 16b = 17,6.
Bảo toàn electron: 3nFe = 2nH2 + 2nO/X + nAg ⇒ nAg = (3a – 2b – 0,15) mol.
Lại có nH2O = b mol ⇒ nHCl = (2b + 0,15) mol theo bảo toàn O và H.
⇒ nAgCl = nCl– = (2b + 0,15) mol ⇒ ∑m↓ = 143,5 × (2b + 0,15) + 108 × (3a – 2b – 0,15) = 102,3.
⇒ Giải hệ các phương trình ta được: a = 0,25 mol và b = 0,225 mol.
Vậy, kết tủa gồm 0,15 mol Ag và 0,6 mol AgCl.
⇒ Trực tiếp sinh ra Ag là do 0,15 mol FeCl2 trong Y.
Lại có ∑nHCl = 0,6 mol ⇒ mdung dịch HCl = 375 gam.
⇒ mdung dịch Y = mdung dịch HCl + mX – mH2↑ = 392,45 gam.
⇒ Yêu cầu C%mFeCl2 trong Y = 0,15 × 127 ÷ 392,45 × 100% ≈ 4,85%.
Câu 32 [26085]: Cho các phát biểu sau:
(a) Chất béo nhẹ hơn nước và không tan trong nước.
(b) Mật ong và nước ép quả nho chín đều có phản ứng tráng bạc.
(c) Tơ visco và tơ axetat đều có nguồn gốc từ xenlulozơ.
(d) Dung dịch lòng trắng trứng gà bị đông tụ khi đun nóng.
(e) Axit cacboxylic có lực axit mạnh hơn phenol và ancol.
Số phát biểu đúng là
(a) Chất béo nhẹ hơn nước và không tan trong nước.
(b) Mật ong và nước ép quả nho chín đều có phản ứng tráng bạc.
(c) Tơ visco và tơ axetat đều có nguồn gốc từ xenlulozơ.
(d) Dung dịch lòng trắng trứng gà bị đông tụ khi đun nóng.
(e) Axit cacboxylic có lực axit mạnh hơn phenol và ancol.
Số phát biểu đúng là
A, 3.
B, 5.
C, 2.
D, 4.
HD: Xem xét - phân tích các phát biểu:
(a) đúng. Chất béo nhẹ hơn nước, không tan trong nước nên nổi trên mặt nước.
(b) đúng. trong mật ong và nước ép quả nho chín chứa nhiều glucozơ, fructozơ có phản ứng tráng bạc:

(c) đúng. Tơ visco và tơ axetat đều có nguồn gốc từ xenlulozơ.
(d) đúng. Hiện tượng đông tụ của protein.
(e) đúng. Thứ tự lực axit: axit cacboxylic > phenol > ancol.
⇝ Cả 5 phát biểu đều đúng. ❒
(a) đúng. Chất béo nhẹ hơn nước, không tan trong nước nên nổi trên mặt nước.
(b) đúng. trong mật ong và nước ép quả nho chín chứa nhiều glucozơ, fructozơ có phản ứng tráng bạc:
(c) đúng. Tơ visco và tơ axetat đều có nguồn gốc từ xenlulozơ.
(d) đúng. Hiện tượng đông tụ của protein.
(e) đúng. Thứ tự lực axit: axit cacboxylic > phenol > ancol.
⇝ Cả 5 phát biểu đều đúng. ❒
Câu 33 [229173]: Cho biết X, Y, Z, T, E là các hợp chất vô cơ khác nhau của kim loại, thõa mãn sơ đồ phản ứng sau:

Cho biết hai chất X, Z có phân tử khối bằng nhau và tác dụng với HCl đều tạo khí cacbonic, mỗi mũi tên chỉ biểu diễn cho một phản ứng. Các chất Y, E thỏa mãn sơ đồ trên lần lượt là

Cho biết hai chất X, Z có phân tử khối bằng nhau và tác dụng với HCl đều tạo khí cacbonic, mỗi mũi tên chỉ biểu diễn cho một phản ứng. Các chất Y, E thỏa mãn sơ đồ trên lần lượt là
A, Ca(HCO3)2, KHCO3.
B, Ca(OH)2, KOH.
C, Ba(OH)2, K2CO3.
D, Ca(OH)2, K2CO3.
MX = MZ và X, Z + HCl đều tạo CO2 nên chọn X là KHCO3, Z là CaCO3.
Y là Ca(OH)2
T là K2CO3
E là KOH
Các phương trình hóa học xảy ra như sau:
2KHCO3 + Ca(OH)2 → CaCO3 + K2CO3 + H2O
K2CO3 + Ca(OH)2 → CaCO3 + 2KOH
KOH + KHCO3 →K2CO3+ H2O
K2CO3 + Ca(OH)2 → CaCO3 + 2KOH
Y là Ca(OH)2
T là K2CO3
E là KOH
Các phương trình hóa học xảy ra như sau:
2KHCO3 + Ca(OH)2 → CaCO3 + K2CO3 + H2O
K2CO3 + Ca(OH)2 → CaCO3 + 2KOH
KOH + KHCO3 →K2CO3+ H2O
K2CO3 + Ca(OH)2 → CaCO3 + 2KOH
Câu 34 [311691]: Hòa tan hoàn toàn m gam hỗn hợp CuSO4.5H2O và NaCl vào nước, thu được dung dịch X. Tiến hành điện phân X với các điện cực trơ, màng ngăn xốp, dòng điện có cường độ không đổi. Kết quả quá trình điện phân được ghi lại ở bảng sau:
Giả sử hiệu suất điện phân là 100%, bỏ qua sự bay hơi của nước. Giá trị của m gần nhất với
| Thời gian điện phân (giây) | t | 2t | 3t | t |
| Tổng số mol khí thu được trên cả hai điện cực (mol) | 0,040 | 0,100 | 0,150 | 0,195 |
Giả sử hiệu suất điện phân là 100%, bỏ qua sự bay hơi của nước. Giá trị của m gần nhất với
A, 11.
B, 12.
C, 10.
D, 13.
HD: Gọi các điểm A(t; 0,04); B(2t; 0,1); C(3t; 0,15) và D(4t; 0,195).
Để ý các khoảng tăng khí: t → 2t: 0,06 mol; 2t → 3t: 0,05 mol; 3t → 4t: 0,45 mol.

► Nhận xét: ba khoảng giá trị khác nhau nên không thể có 3 điểm cùng nằm trên một đoạn OM; MN hoặc NP (*).
☆ Hướng giải: Chọn I = 2 × 96500.
• Nếu A thuộc đoạn OM, để B, C, D không cùng thuộc NP thì chắc chắn B phải thuộc MN.
Như vậy, t giây thu được 0,04 mol Cl2 → ne trao đổi (t) = 0,08 mol.
Thời gian 2t giây thu được a mol Cl2 và b mol O2. Theo tỉ lệ ne trao đổi (2t) = 0,16 mol.
→ Ta có: a + b = 0,1 và 2a + 4b = 0,16. Giải a = 0,12 và b = – 0,02 (loại).
⇒ Như vậy, A chỉ có thể thuộc MN. Cũng theo (*), B thuộc MN và C, D thuộc NP còn lại.
Luôn có PK = 1,5NK nên 0,195 – 0,15 = 1,5(4t – 3t) → t = 0,03.
Nếu thuộc TH1: IM = 2IN nên (2t – t) = 2 × (0,1 – 0,04) → t = 0,12 (loại).
Nếu thuộc TH2: IN = 2IM nên (0,1 – 0,04) = 2 × (2t – t) → t = 0,03 (thỏa mãn).
☆ Xét điểm A(0,03; 0,04) thuộc đoạn MN trên đồ thị TH2; ne trao đổi (t) = 2t = 0,06 mol.
anot chỉ thoát ra 0,06 ÷ 2 = 0,03 mol Cl2 → catot thoát ra 0,01 mol H2.
Có H2 chứng tỏ Cu2+ bị điện phân hết → ∑nCu = (0,06 – 0,01 × 2) ÷ 2 = 0,02 mol.
☆ Xét điểm C(0,09; 0,15) thuộc đoạn NP trên đồ thị TH2; ne trao đổi (3t) = 0,06 × 3 = 0,18 mol.
Bảo toàn e bên catot → số mol H2↑ bằng (0,18 – 0,02 × 2) ÷ 2 = 0,07 mol.
→ Bên anot tương ứng thu được 0,08 mol gồm a mol Cl2 và b mol O2.

→ ∑nCl = 0,14 mol → số mol NaCl ban đầu là 0,14 mol.
Vậy m gam hỗn hợp gồm 0,02 mol CuSO4.5H2O và 0,14 mol NaCl → m = 13,19 gam.
Để ý các khoảng tăng khí: t → 2t: 0,06 mol; 2t → 3t: 0,05 mol; 3t → 4t: 0,45 mol.

► Nhận xét: ba khoảng giá trị khác nhau nên không thể có 3 điểm cùng nằm trên một đoạn OM; MN hoặc NP (*).
☆ Hướng giải: Chọn I = 2 × 96500.
• Nếu A thuộc đoạn OM, để B, C, D không cùng thuộc NP thì chắc chắn B phải thuộc MN.
Như vậy, t giây thu được 0,04 mol Cl2 → ne trao đổi (t) = 0,08 mol.
Thời gian 2t giây thu được a mol Cl2 và b mol O2. Theo tỉ lệ ne trao đổi (2t) = 0,16 mol.
→ Ta có: a + b = 0,1 và 2a + 4b = 0,16. Giải a = 0,12 và b = – 0,02 (loại).
⇒ Như vậy, A chỉ có thể thuộc MN. Cũng theo (*), B thuộc MN và C, D thuộc NP còn lại.
Luôn có PK = 1,5NK nên 0,195 – 0,15 = 1,5(4t – 3t) → t = 0,03.
Nếu thuộc TH1: IM = 2IN nên (2t – t) = 2 × (0,1 – 0,04) → t = 0,12 (loại).
Nếu thuộc TH2: IN = 2IM nên (0,1 – 0,04) = 2 × (2t – t) → t = 0,03 (thỏa mãn).
☆ Xét điểm A(0,03; 0,04) thuộc đoạn MN trên đồ thị TH2; ne trao đổi (t) = 2t = 0,06 mol.
anot chỉ thoát ra 0,06 ÷ 2 = 0,03 mol Cl2 → catot thoát ra 0,01 mol H2.
Có H2 chứng tỏ Cu2+ bị điện phân hết → ∑nCu = (0,06 – 0,01 × 2) ÷ 2 = 0,02 mol.
☆ Xét điểm C(0,09; 0,15) thuộc đoạn NP trên đồ thị TH2; ne trao đổi (3t) = 0,06 × 3 = 0,18 mol.
Bảo toàn e bên catot → số mol H2↑ bằng (0,18 – 0,02 × 2) ÷ 2 = 0,07 mol.
→ Bên anot tương ứng thu được 0,08 mol gồm a mol Cl2 và b mol O2.

→ ∑nCl = 0,14 mol → số mol NaCl ban đầu là 0,14 mol.
Vậy m gam hỗn hợp gồm 0,02 mol CuSO4.5H2O và 0,14 mol NaCl → m = 13,19 gam.
Câu 35 [266039]: Este X đa chức, no, mạch hở có công thức phân tử dạng CnH8On. Xà phòng hoá hoàn toàn X bởi dung dịch NaOH dư thu được hỗn hợp Y gồm 2 muối E và F (ME < MF) của 2 axit cacboxylic hơn kém nhau 1 nguyên tử Cacbon và hỗn hợp ancol Z gồm hai chất G và T (MG < MT) cũng hơn kém nhau 1 nguyên tử cacbon trong phân tử.
Cho các phát biểu sau:
(a) Có hai công thức cấu tạo của E thỏa mãn sơ đồ trên.
(b) Các chất trong Y đều có khả năng tráng bạc.
(c) Từ etilen có thể tạo ra T bằng một phản ứng .
(d) Đốt cháy hoàn toàn F thu được hỗn hợp Na2CO3, CO2, H2O.
(e) Từ G điều chế axit axetic là phương pháp hiện đại
Số phát biểu đúng là
Cho các phát biểu sau:
(a) Có hai công thức cấu tạo của E thỏa mãn sơ đồ trên.
(b) Các chất trong Y đều có khả năng tráng bạc.
(c) Từ etilen có thể tạo ra T bằng một phản ứng .
(d) Đốt cháy hoàn toàn F thu được hỗn hợp Na2CO3, CO2, H2O.
(e) Từ G điều chế axit axetic là phương pháp hiện đại
Số phát biểu đúng là
A, 1.
B, 2.
C, 4.
D, 3.
- X đa chức, no, mạch hở mà tác dụng với NaOH cho 2 muối + 2 ancol.
Vậy X có 3 chức.
X có dạng: R1-COO-R2-OOC-R3-COO-R4.
- Mà X có 6 nguyên tử oxi => n = 6 => công thức của X là C6H8O6.
- X thu được 2 muối hơn kém nhau 1C và 2 ancol hơn kém nhau 1C.
=> CTCT của X là HCOO-C2H4-OOC-COO-CH3.
Vậy E là HCOONa; F là (COONa)2; G là CH3OH; T là C2H4(OH)2.
(a) sai, E chỉ có 1 công thức cấu tạo thỏa mãn.
(b) sai, F không tráng bạc.
(c) đúng, PTHH: 3C2H4 + 2KMnO4 + 4H2O→3C2H4(OH)2 + 2MnO2 + 2KOH.
(d) sai, PTHH: 2(COONa)2 + O2 → 2Na2CO3 + 2CO2.
(e) đúng, PTHH: CH3OH + CO → CH3COOH.
Vậy X có 3 chức.
X có dạng: R1-COO-R2-OOC-R3-COO-R4.
- Mà X có 6 nguyên tử oxi => n = 6 => công thức của X là C6H8O6.
- X thu được 2 muối hơn kém nhau 1C và 2 ancol hơn kém nhau 1C.
=> CTCT của X là HCOO-C2H4-OOC-COO-CH3.
Vậy E là HCOONa; F là (COONa)2; G là CH3OH; T là C2H4(OH)2.
(a) sai, E chỉ có 1 công thức cấu tạo thỏa mãn.
(b) sai, F không tráng bạc.
(c) đúng, PTHH: 3C2H4 + 2KMnO4 + 4H2O→3C2H4(OH)2 + 2MnO2 + 2KOH.
(d) sai, PTHH: 2(COONa)2 + O2 → 2Na2CO3 + 2CO2.
(e) đúng, PTHH: CH3OH + CO → CH3COOH.
Câu 36 [973620]: Tiến hành các thí nghiệm sau:
(a) Cho kim loại Cu vào dung dịch FeCl3 dư.
(b) Điện phân dung dịch AgNO3 (điện cực trơ).
(c) Nung nóng hỗn hợp bột Al và FeO (không có không khí).
(d) Cho kim loại Ba vào dung dịch CuSO4 dư.
(e) Điện phân Al2O3 nóng chảy.
Số thí nghiệm tạo thành kim loại là
(a) Cho kim loại Cu vào dung dịch FeCl3 dư.
(b) Điện phân dung dịch AgNO3 (điện cực trơ).
(c) Nung nóng hỗn hợp bột Al và FeO (không có không khí).
(d) Cho kim loại Ba vào dung dịch CuSO4 dư.
(e) Điện phân Al2O3 nóng chảy.
Số thí nghiệm tạo thành kim loại là
A, 5.
B, 3.
C, 2.
D, 4.
HD: Các phản ứng xảy ra khi tiến hành các thí nghiệm:
❌ (a) Cu + 2FeCl3 → CuCl2 + 2FeCl2.
✔️ (b) 4AgNO3 + 2H2O –––đpdd–→ 4Ag↓ + O2↑ + 4HNO3 (pp điện phân).
✔️ (c) 2Al + 3FeO –––to–→ 3Fe + Al2O3 (pp nhiệt nhôm).
❌ (d) Ba + 2H2O → Ba(OH)2 + H2↑, sau đó Ba(OH)2 + CuSO4 → BaSO4↓ + Cu(OH)2↓.
✔️ (e) 2Al2O3 –––đpnc–→ 4Al + 3O2↑ (pp điện phân).
⇝ Có 3/5 thí nghiệm thoả mãn yêu cầu ⇝ Chọn đáp án B. ♦
❌ (a) Cu + 2FeCl3 → CuCl2 + 2FeCl2.
✔️ (b) 4AgNO3 + 2H2O –––đpdd–→ 4Ag↓ + O2↑ + 4HNO3 (pp điện phân).
✔️ (c) 2Al + 3FeO –––to–→ 3Fe + Al2O3 (pp nhiệt nhôm).
❌ (d) Ba + 2H2O → Ba(OH)2 + H2↑, sau đó Ba(OH)2 + CuSO4 → BaSO4↓ + Cu(OH)2↓.
✔️ (e) 2Al2O3 –––đpnc–→ 4Al + 3O2↑ (pp điện phân).
⇝ Có 3/5 thí nghiệm thoả mãn yêu cầu ⇝ Chọn đáp án B. ♦
Câu 37 [233900]: Cho X là axit cacboxylic đơn chức, mạch hở, Y là ancol no, đa chức, mạch hở. Đun hỗn hợp gồm 3 mol X, 1 mol Y với xúc tác H2SO4 đặc (giả sử chỉ xảy ra phản ứng este hóa giữa X và Y) thu được 2,5 mol hỗn hợp E gồm X, Y và các sản phẩm hữu cơ (trong đó có chất Z chỉ chứa nhóm chức este). Tiến hành các thí nghiệm sau:
Thí nghiệm 1: Cho 0,5 mol E tác dụng với Na dư, sau phản ứng hoàn toàn thu được 0,3 mol khí H2.
Thí nghiệm 2: Cho 0,5 mol E vào dung dịch brom dư thì có tối đa 1,2 mol Br2 tham gia phản ứng cộng.
Thí nghiệm 3: Đốt cháy hoàn toàn 0,5 mol E cần vừa đủ 2,2 mol khí O2 thu được CO2 và H2O.
Biết có 10% axit X ban đầu đã chuyển thành Z. Phần trăm khối lượng của Z trong E là
Thí nghiệm 1: Cho 0,5 mol E tác dụng với Na dư, sau phản ứng hoàn toàn thu được 0,3 mol khí H2.
Thí nghiệm 2: Cho 0,5 mol E vào dung dịch brom dư thì có tối đa 1,2 mol Br2 tham gia phản ứng cộng.
Thí nghiệm 3: Đốt cháy hoàn toàn 0,5 mol E cần vừa đủ 2,2 mol khí O2 thu được CO2 và H2O.
Biết có 10% axit X ban đầu đã chuyển thành Z. Phần trăm khối lượng của Z trong E là
A, 10,55%.
B, 7,06%.
C, 7,13%.
D, 9,02%.
HD: Đồng nhất số liệu: gấp 5 tất cả các số liệu ở mỗi thí nghiệm.!
Chú ý tỉ lệ este hoá: –COOH (1 chức axit) + –OH (1 chức ancol) → COO (1 chức este) + H2O (1 nước).
Có hai chú ý đặc biệt ở hệ phản ứng este hoá này:
•1: số mol các chất trước và sau bảo toàn: naxit + nancol = neste + nH2O.
•2: xét phản ứng với Na của hỗn hợp (axit - ancol) tạo 1 mol thì (este; nước) chỉ tạo 0,5 mol ⇒ ta nói cứ 1 mol H2O được tạo thành thì số mol H2 sinh ra giảm một nửa.
► E phức tạp ⇝ tư duy quy đổi về xử lý hỗn hợp axit - ancol ban đầu.
☆ Sử dụng •1: số mol H2Oeste hoá = 3 + 1 – 2,5 = 1,5 mol.
☆ Sử dụng •2: do có 1,5 mol H2O nên nếu để 3 mol X và 1 mol Y tác dụng với Na thì số mol H2 sinh ra là 1,5 + 1,5 = 3,0 mol.
Axit dạng CnH?O2 và ancol dạng CmH2m + 2O?? ⇒ nH2↑ = 3 ÷ 2 + ?? ÷ 2 = 3 ⇒ ?? = 3.
☆ TN2: nBr2 = 6 mol ⇒ số πC=C = 6 ÷ 3 = 2 ⇒ ? = 2n – 4.
☆ Đốt (3 mol X + 1 mol Y) hay đốt 2,5 mol E cần cùng 11 mol O2.
⇒ Giải đốt: 3 mol CnH2n – 4O2 + 1 mol CmH2m + 2O3 + 11 mol O2 → a mol CO2 + b mol H2O.
Tương quan đốt: a – b = ∑nCO2 – ∑nH2O = 3 × 2 – 1 = 5.
Lại theo bảo toàn O: 2a + b = 3 × 2 + 1 × 3 + 11 × 2.
Giải hệ các phương trình có: a = 12 và b = 7
⇒ xây dựng phương trình nghiệm nguyên: 3n + m = 12 ⇒ Thoả mãn là m = n = 3.
⇒ axit tương ứng: HC≡C-COOH và ancol là C3H5(OH)3.
Z chỉ chứa chức este ⇒ cấu tạo: (HC≡C-COO)3C3H5.
naxit tạo Z = 3 × 0,10 = 0,3 mol ⇒ nZ = 0,1 mol.
mE = mX + mY – mH2O = 275 gam.
⇒ Yêu cầu C%mZ/E = 0,1 × 248 ÷ 275 × 100% ≈ 9,02%. ⇝ Chọn đáp án D. ♠
Chú ý tỉ lệ este hoá: –COOH (1 chức axit) + –OH (1 chức ancol) → COO (1 chức este) + H2O (1 nước).
Có hai chú ý đặc biệt ở hệ phản ứng este hoá này:
•1: số mol các chất trước và sau bảo toàn: naxit + nancol = neste + nH2O.
•2: xét phản ứng với Na của hỗn hợp (axit - ancol) tạo 1 mol thì (este; nước) chỉ tạo 0,5 mol ⇒ ta nói cứ 1 mol H2O được tạo thành thì số mol H2 sinh ra giảm một nửa.
► E phức tạp ⇝ tư duy quy đổi về xử lý hỗn hợp axit - ancol ban đầu.
☆ Sử dụng •1: số mol H2Oeste hoá = 3 + 1 – 2,5 = 1,5 mol.
☆ Sử dụng •2: do có 1,5 mol H2O nên nếu để 3 mol X và 1 mol Y tác dụng với Na thì số mol H2 sinh ra là 1,5 + 1,5 = 3,0 mol.
Axit dạng CnH?O2 và ancol dạng CmH2m + 2O?? ⇒ nH2↑ = 3 ÷ 2 + ?? ÷ 2 = 3 ⇒ ?? = 3.
☆ TN2: nBr2 = 6 mol ⇒ số πC=C = 6 ÷ 3 = 2 ⇒ ? = 2n – 4.
☆ Đốt (3 mol X + 1 mol Y) hay đốt 2,5 mol E cần cùng 11 mol O2.
⇒ Giải đốt: 3 mol CnH2n – 4O2 + 1 mol CmH2m + 2O3 + 11 mol O2 → a mol CO2 + b mol H2O.
Tương quan đốt: a – b = ∑nCO2 – ∑nH2O = 3 × 2 – 1 = 5.
Lại theo bảo toàn O: 2a + b = 3 × 2 + 1 × 3 + 11 × 2.
Giải hệ các phương trình có: a = 12 và b = 7
⇒ xây dựng phương trình nghiệm nguyên: 3n + m = 12 ⇒ Thoả mãn là m = n = 3.
⇒ axit tương ứng: HC≡C-COOH và ancol là C3H5(OH)3.
Z chỉ chứa chức este ⇒ cấu tạo: (HC≡C-COO)3C3H5.
naxit tạo Z = 3 × 0,10 = 0,3 mol ⇒ nZ = 0,1 mol.
mE = mX + mY – mH2O = 275 gam.
⇒ Yêu cầu C%mZ/E = 0,1 × 248 ÷ 275 × 100% ≈ 9,02%. ⇝ Chọn đáp án D. ♠
Câu 38 [983275]: Hỗn hợp E gồm axit oleic, axit panmitic và triglixerit X (tỉ lệ mol tương ứng là 1 : 2 : 4). Đốt cháy hoàn toàn m gam E cần vừa đủ 7,43 mol O2, thu được CO2 và H2O. Mặt khác, cho m gam E tác dụng hết với lượng dư dung dịch NaOH đun nóng, thu được sản phẩm hữu cơ gồm glixerol và 86 gam hỗn hợp hai muối. Phần trăm khối lượng của X trong E là
A, 81,21%.
B, 80,74%.
C, 81,66%.
D, 80,24%.
HD: Triglixerit dạng (RCOO)3C3H5 = 3RCOOH.C3H2 → Quy đổi hỗn hợp ban đầu:
m gam E gồm a mol C15H31COOH; b mol C17H33COOH và c mol C3H2.
Từ tỉ lệ giả thiết 1 : 2 : 4 ⇒ ∑gốc axit = (1 + 2 + 4 × 3)/4(gốc glixerol) ⇒ 4(a + b) = 15c.
• Giải đốt E thu được (16a + 18b + 3c) mol CO2 và (16a + 17b + c) mol H2O.
⇒ bảo toàn nguyên tố O: 2a + 2b + 7,43 × 2 = 2 × (16a + 18b + 3c) + (16a + 17b + c).
• Giải thuỷ phân, mmuối = 278a + 304b = 86,0 gam.
Giải hệ các phương trình ta được a = 0,2; b = 0,1 và c = 0,08.
⇝ E quy đổi gồm 0,08 mol C3H2 + 0,2 mol C15H31COOH + 0,1 mol C17H33COOH.
Ghép lại ⇒ X chỉ có thể chứa đúng 2 gốc C15H31COO và 1 gốc C17H33COO.
⇒ E gồm 0,08 mol (C15H31COO)2(C17H33COO)C3H5 + 0,04 mol C15H31COOH và 0,02 mol C17H33COOH.
⇒ m = mE = 0,08 × 832 + 0,04 × 256 + 0,02 × 282 = 82,44 gam.
⇒ Yêu cầu %mX/E = 0,08 × 832 ÷ 82,44 × 100% ≈ 80,74%.
m gam E gồm a mol C15H31COOH; b mol C17H33COOH và c mol C3H2.
Từ tỉ lệ giả thiết 1 : 2 : 4 ⇒ ∑gốc axit = (1 + 2 + 4 × 3)/4(gốc glixerol) ⇒ 4(a + b) = 15c.
• Giải đốt E thu được (16a + 18b + 3c) mol CO2 và (16a + 17b + c) mol H2O.
⇒ bảo toàn nguyên tố O: 2a + 2b + 7,43 × 2 = 2 × (16a + 18b + 3c) + (16a + 17b + c).
• Giải thuỷ phân, mmuối = 278a + 304b = 86,0 gam.
Giải hệ các phương trình ta được a = 0,2; b = 0,1 và c = 0,08.
⇝ E quy đổi gồm 0,08 mol C3H2 + 0,2 mol C15H31COOH + 0,1 mol C17H33COOH.
Ghép lại ⇒ X chỉ có thể chứa đúng 2 gốc C15H31COO và 1 gốc C17H33COO.
⇒ E gồm 0,08 mol (C15H31COO)2(C17H33COO)C3H5 + 0,04 mol C15H31COOH và 0,02 mol C17H33COOH.
⇒ m = mE = 0,08 × 832 + 0,04 × 256 + 0,02 × 282 = 82,44 gam.
⇒ Yêu cầu %mX/E = 0,08 × 832 ÷ 82,44 × 100% ≈ 80,74%.
Câu 39 [679768]: Nung nóng hỗn hợp X gồm metan, etilen, propin, vinyl axetilen và a mol H2 có Ni xúc tác (chỉ xảy ra phản ứng cộng H2) thu được 0,2 mol hỗn hợp Y (gồm các hiđrocacbon) có tỉ khối so với H2 là 14,5. Biết 0,2 mol Y phản ứng tối đa với 0,1 mol Br2 trong dung dịch. Giá trị của a là
A, 0,05.
B, 0,10.
C, 0,15.
D, 0,20.
HD: ► Metan: CH4; etilen: C2H4; propin: C3H4 và vinylaxetilen: C4H4.
⇒ điểm chung: cùng 4H ⇒ Quy X gồm C?H4 và a mol H2.
X ––Ni, to→ 0,2 mol Y (gồm các hiđrocacbon) ⇒ nC?H4 = nY = 0,2 mol.
► Tinh tế xử lý: xét toàn bộ quá trình thì để làm no 0,2 mol C?H4 cần a mol H2 và 0,1 mol Br2.
⇒ Quy về làm no 0,2 mol C?H4 cần (a + 0,1) mol H2 tạo thành (14,5 × 2 × 0,2 + 0,1 × 2 = 6,0) gam ankan.
Tương quan 1C ⇄ 1π ⇄ 1Br ⇄ 1H2 ⇒ 0,2 mol CH4 + (a + 0,1) mol CH2 → 6,0 gam ankan
⇒ 0,2 × 16 + 14 × (a + 0,1) = 6,0 ⇒ a = 0,10 mol ⇝ Chọn đáp án B. ♦
⇒ điểm chung: cùng 4H ⇒ Quy X gồm C?H4 và a mol H2.
X ––Ni, to→ 0,2 mol Y (gồm các hiđrocacbon) ⇒ nC?H4 = nY = 0,2 mol.
► Tinh tế xử lý: xét toàn bộ quá trình thì để làm no 0,2 mol C?H4 cần a mol H2 và 0,1 mol Br2.
⇒ Quy về làm no 0,2 mol C?H4 cần (a + 0,1) mol H2 tạo thành (14,5 × 2 × 0,2 + 0,1 × 2 = 6,0) gam ankan.
Tương quan 1C ⇄ 1π ⇄ 1Br ⇄ 1H2 ⇒ 0,2 mol CH4 + (a + 0,1) mol CH2 → 6,0 gam ankan
⇒ 0,2 × 16 + 14 × (a + 0,1) = 6,0 ⇒ a = 0,10 mol ⇝ Chọn đáp án B. ♦
Câu 40 [116782]: Cho khí CO lấy dư đi qua một ống chứa (0,4 mol Fe3O4; 0,2 mol Al2O3; 0,3 mol K2O; 0,4 mol CuO) nung nóng đến các phản ứng xảy ra hoàn toàn, thu được x gam chất rắn trong ống. Giá trị của x là
A, 141,4.
B, 154,6.
C, 166,2.
D, 173,1.
HD: CO dư chỉ khử được Fe3O4; CuO về kim loại thôi, còn Al2O3 và K2O thì không.
Tuy nhiên, ☠ ► NOTE phản ứng K2O + CO2 (sinh ra từ CO) → K2CO3.
||→ chính xác x gồm 1,2 mol Fe + 0,2 mol Al2O3 + 0,4 mol Cu và 0,3 mol K2CO3.
||→ Yêu cầu giá trị của x = 154,6 gam. Chọn B. ♦.
☠ p/s: một bài tập tưởng chừng đơn giản nhưng rất dễ mất trọn 0,2 điểm.! cần đánh dấu và nhớ rằng đây là lần sai đầu tiên cũng là cuối cùng.!
Tuy nhiên, ☠ ► NOTE phản ứng K2O + CO2 (sinh ra từ CO) → K2CO3.
||→ chính xác x gồm 1,2 mol Fe + 0,2 mol Al2O3 + 0,4 mol Cu và 0,3 mol K2CO3.
||→ Yêu cầu giá trị của x = 154,6 gam. Chọn B. ♦.
☠ p/s: một bài tập tưởng chừng đơn giản nhưng rất dễ mất trọn 0,2 điểm.! cần đánh dấu và nhớ rằng đây là lần sai đầu tiên cũng là cuối cùng.!