Đáp án
1D
2B
3B
4A
5C
6C
7C
8B
9B
10C
11D
12C
13D
14A
15B
16B
17C
18D
19B
20C
21A
22C
23C
24B
25C
26B
27B
28A
29D
30C
31A
32A
33C
34B
35B
36D
37C
38D
39A
40C
Đáp án Đề minh họa số 26 thi Tốt Nghiệp Trung học Phổ Thông 2024 môn Hóa học
Câu 1 [60331]: Al(OH)3 không phản ứng với dung dịch nào đây?
A, HCl.
B, NaOH.
C, H2SO4.
D, Na2SO4.
Giải: Vì Al(OH)3 là 1 hyđroxit lưỡng tính ⇒ có thể tác dụng với axit và bazo.
⇒ Chọn D
⇒ Chọn D
Câu 2 [982212]: Crom có số oxi hóa +6 trong hợp chất nào sau đây?
A, CrO.
B, K2Cr2O7.
C, KCrO2.
D, Cr2O3.
HD: Phân tích các đáp án:
| Công thức | A. CrO. | B. K2Cr2O7. | C. KCrO2. | D. Cr2O3. |
| Số oxi hoá của crom | +2 | +6 (✔️) | +3 | +3 |
Câu 3 [679834]: Kim loại nào sau đây là kim loại kiềm?
A, Cu.
B, Na.
C, Mg.
D, Al.
HD: Mẹo nhỏ: Lính nào không rượu cà fê.
⇒ Dãy kim loại kiềm: Li Na K Rb Cs Fr.
⇒ Dãy kim loại kiềm: Li Na K Rb Cs Fr.
Câu 4 [973545]: Muối nào sau đây dễ bị phân hủy khi đun nóng?
A, Ca(HCO3)2.
B, Na2SO4.
C, CaCl2.
D, NaCl.
HD: Các muối hiđrocacbonat đều kém bền nhiệt, dễ bị phân huỷ:
Tổng quát: 2HCO3– ––to→ CO22– + CO2↑ + H2O.
⇝ Trong 4 phương án, thoả mãn là đáp án A. Ca(HCO3)2.
Tổng quát: 2HCO3– ––to→ CO22– + CO2↑ + H2O.
⇝ Trong 4 phương án, thoả mãn là đáp án A. Ca(HCO3)2.
Câu 5 [49139]: Công thức hóa học của vôi sống (canxi oxit) là
A, CO.
B, Ca2O.
C, CaO.
D, CaO2.
Gợi ý:
Vôi sống (canxi oxit) được tạo nên từ 2 nguyên tố, đó là Ca và O.
Ca hóa trị II, O hóa trị II. Do đó, theo quy tắc hóa trị, ta có CTHH của vôi sống là CaO.
→ Đáp án C.
Vôi sống (canxi oxit) được tạo nên từ 2 nguyên tố, đó là Ca và O.
Ca hóa trị II, O hóa trị II. Do đó, theo quy tắc hóa trị, ta có CTHH của vôi sống là CaO.
→ Đáp án C.
Câu 6 [224895]: Ion nào sau đây có tính oxi hóa mạnh nhất?
A, Mg2+.
B, Zn2+.
C, Cu2+.
D, K+.
HD: Thứ tự dãy điện hoá: 
⇒ Theo chiều trái qua phải: "tử tăng" ⇝ tính oxi hoá của Cu2+ mạnh nhất ⇝ Chọn đáp án C. ♣

⇒ Theo chiều trái qua phải: "tử tăng" ⇝ tính oxi hoá của Cu2+ mạnh nhất ⇝ Chọn đáp án C. ♣
Câu 7 [21878]: Khi đốt cháy hoàn toàn một loại vật liệu X, bằng ôxi thu được sản phẩm cháy gồm CO2, H2O và N2. Vật liệu X có thể là
A, cao su buna-S.
B, tơ axetat.
C, tơ olon.
D, tơ visco.
Giải: Sinh ra N2 ⇒ phải chứa N ⇒ chỉ có C thỏa mãn.
Câu 8 [982520]: Số nguyên tử oxi trong phân tử alanin là
A, 4.
B, 2.
C, 1.
D, 3.
HD: Công thức phân tử alanin là:

⇒ Số nguyên tử oxi trong phân tử alanin là 2.

⇒ Số nguyên tử oxi trong phân tử alanin là 2.
Câu 9 [982501]: Dung dịch muối nào sau đây trong nước có môi trường axit, có khả năng làm quỳ tím hóa đỏ?
A, K2CO3.
B, KHSO4.
C, KNO3.
D, K2SO4.
HD: Trong dung dịch:KHSO4 → K+ + H+ + SO42–
⇒ dung dịch có môi trường axit, pH < 7, làm quỳ tím hoá đỏ.
► Còn lại: dung dịch K2SO4 và KNO3 đều có pH = 7, không làm quỳ tím đổi màu; K2CO3 có pH > 7, làm quỳ tím hoá xanh.
⇒ dung dịch có môi trường axit, pH < 7, làm quỳ tím hoá đỏ.
► Còn lại: dung dịch K2SO4 và KNO3 đều có pH = 7, không làm quỳ tím đổi màu; K2CO3 có pH > 7, làm quỳ tím hoá xanh.
Câu 10 [679753]: Công thức của axit stearic là
A, C2H5COOH.
B, CH3COOH.
C, C17H35COOH.
D, HCOOH.
HD: Phân tích các đáp án:
| Công thức | C2H5COOH | CH3COOH | C17H35COOH | HCOOH |
| Tên gọi | axit propionic | axit axetic | axit stearic | axit fomic |
| ❌ | ❌ | ✔️ | ❌ |
Câu 11 [62586]: Khi để vôi sống trong không khí ẩm một thời gian sẽ có hiện tượng một phần bị chuyển hóa trở lại thành đá vôi. Khí nào sau đây là tác nhân gây ra hiện tượng trên?
A, Freon.
B, Metan.
C, Cacbon monooxit.
D, Cacbon đioxit.
HD: Vôi sống CaO để trong không khí ẩm thì CaO + H2O → Ca(OH)2. Sau đó: Ca(OH)2 + CO2 → CaCO3 + H2O.
CO2 là nguyên nhân làm một phần vôi sống để trong không khí ẩm bị chuyển hóa trở lại thành đá vôi.
CO2 là nguyên nhân làm một phần vôi sống để trong không khí ẩm bị chuyển hóa trở lại thành đá vôi.
Câu 12 [908860]: Ở nhiệt độ thường, kim loại Al tan hoàn toàn trong lượng dư dung dịch nào sau đây?
A, KCl.
B, NaCl.
C, NaOH.
D, NaNO3.
HD: Kim loại Al có thể tác dụng và tan được với axit mạnh và bazơ mạnh:
• 2Al + 6HCl → 2AlCl3 + 3H2O.
• 2Al + 2NaOH + 2H2O → 2NaAlO2 + 3H2↑.
⇒ trong 4 phương án, thoả mãn là đáp án C.
• 2Al + 6HCl → 2AlCl3 + 3H2O.
• 2Al + 2NaOH + 2H2O → 2NaAlO2 + 3H2↑.
⇒ trong 4 phương án, thoả mãn là đáp án C.
Câu 13 [334303]: Chất không có khả năng hòa tan được Cu(OH)2 là
A, axit axetic.
B, Ala-Ala-Gly.
C, glucozơ.
D, Phenol.
HD: Bài học:
2.png)
⇒ trong các chất, chỉ có phenol: C6H5OH không có khả năng hoà tan Cu(OH)3 ⇝ Chọn đáp án D. ♠
2.png)
⇒ trong các chất, chỉ có phenol: C6H5OH không có khả năng hoà tan Cu(OH)3 ⇝ Chọn đáp án D. ♠
Câu 14 [14321]: Chất nào sau đây còn có tên gọi là đường nho?
A, Glucozơ.
B, Saccarozơ.
C, Fructozơ.
D, Tinh bột.
HD: NHỚ và nên NHỚ theo hệ thống. ví dụ ở đây là tên gọi:
• Glucozơ còn được gọi là đường nho vì có nhiều trong quả nho. fructozơ có nhiều trong mật ong.
• saccarozơ là đường mía, đường củ cải, đường thốt nốt, ....; mantozơ là đường mạch nha....
Tương tự, muốn nhớ độ ngọt ta cũng thống kê ra là ok hết.
Tóm lại ở bài tập này đáp án cần chọn là A. ♥.
• Glucozơ còn được gọi là đường nho vì có nhiều trong quả nho. fructozơ có nhiều trong mật ong.
• saccarozơ là đường mía, đường củ cải, đường thốt nốt, ....; mantozơ là đường mạch nha....
Tương tự, muốn nhớ độ ngọt ta cũng thống kê ra là ok hết.
Tóm lại ở bài tập này đáp án cần chọn là A. ♥.
Câu 15 [61749]: Giấy "bạc" được làm từ quá trình dát mỏng các miếng kim loại
A, Cu.
B, Al.
C, Zn.
D, Ag.
HD: Giấy "bạc" là loại nhôm cán mỏng, dùng để bọc gói, tạo hình, lưu giữ hương vị, mùi thơm của thực phẩm khi chế biến thức ăn. "Bạc" ở đây ý chỉ màu trắng bạc của nhôm chứ không phải là nói đến kim loại bạc (Ag). Ngoài ra, có thể dát được những lá nhôm mỏng 0,01 mm dùng làm giấy gói kẹo, gói thuốc lá...


Câu 16 [908849]: Sắt(III) hiđroxit là chất rắn màu nâu đỏ. Công thức của sắt(III) hiđroxit là
A, Fe(OH)2.
B, Fe(OH)3.
C, FeCO3.
D, Fe3O4.
HD: Phân tích các đáp án:
| Cấu tạo | Fe(OH)2 | Fe(OH)3 | FeCO3 | Fe3O4 |
| Tên gọi | Sắt(II) hiđroxit | Sắt(III) hiđroxit | Sắt(II) cacbonat | Oxit sắt từ |
| ❌ | ✔️ | ❌ | ❌ |
Câu 17 [983252]: Este X được tạo bởi ancol metylic và axit axetic. Công thức của X là
A, HCOOC2H5.
B, CH3COOC2H5.
C, CH3COOCH3.
D, HCOOCH3.
HD: ancol metylic: CH3OH; axit axetic: CH3COOH
⇒ Este tương ứng tạo thành có cấu tạo là CH3COOCH3 (metyl axetat).
⇒ Este tương ứng tạo thành có cấu tạo là CH3COOCH3 (metyl axetat).
Câu 18 [982215]: Ở nhiệt độ cao, H2 khử được oxit nào sau đây?
A, CaO.
B, K2O.
C, Na2O.
D, CuO.
HD: Oxit các kim loại từ Al trở lên không bị khử bởi H2.
Chỉ có CuO bị khử: CuO + H2 –––to–→ Cu + H2O.
Chỉ có CuO bị khử: CuO + H2 –––to–→ Cu + H2O.
Câu 19 [679787]: Kim loại Fe tác dụng với dung dịch nào sau đây sinh ra khí H2?
A, HNO3 đặc, nóng.
B, HCl.
C, CuSO4.
D, H2SO4 đặc, nóng.
HD: Các phản ứng xảy ra khi cho Fe tác dụng các đáp án:
❌ A. Fe + 6HNO3 đặc ––to→ Fe(NO3)3 + 3NO2 + 3H2O.
✔️ B. Fe + 2HCl → FeCl2 + H2↑.
❌ C. Fe + CuSO4 → FeSO4 + Cu.
❌ D. 2Fe + 6H2SO4 đặc ––to→ Fe2(SO4)3 + 3SO2↑ + 6H2O.
❌ A. Fe + 6HNO3 đặc ––to→ Fe(NO3)3 + 3NO2 + 3H2O.
✔️ B. Fe + 2HCl → FeCl2 + H2↑.
❌ C. Fe + CuSO4 → FeSO4 + Cu.
❌ D. 2Fe + 6H2SO4 đặc ––to→ Fe2(SO4)3 + 3SO2↑ + 6H2O.
Câu 20 [908868]: Công thức phân tử của ethyl alcohol là
A, C3H8O3.
B, CH4O.
C, C2H6O.
D, C2H4O2.
HD: Công thức phân tử của ethyl alcohol (C2H5OH) là C2H6O.
Câu 21 [981800]: Cho m gam H2NCH2COOH phản ứng hoàn toàn với dung dịch NaOH dư, thu được 1,94 gam muối. Giá trị của m là
A, 1,5.
B, 2,0.
C, 3,5.
D, 3,0.
HD: Phản ứng: H2NCH2COOH + NaOH → H2NCH2COONa + H2O.
nmuối = 1,94 ÷ (75 + 22) = 0,02 mol ⇒ nGly = 0,02 mol.
⇒ m = mGly = 0,02 × 75 = 1,50 gam. ⇝ Chọn đáp án A. ♥
nmuối = 1,94 ÷ (75 + 22) = 0,02 mol ⇒ nGly = 0,02 mol.
⇒ m = mGly = 0,02 × 75 = 1,50 gam. ⇝ Chọn đáp án A. ♥
Câu 22 [982243]: Cho 10,6 gam Na2CO3 tác dụng hết với dung dịch HCl dư, thu được V lít khí CO2. Giá trị của V là
A, 1,12.
B, 3,36.
C, 2,24.
D, 4,48.
HD: Phản ứng: Na2CO3 + 2HCl → 2NaCl + CO2↑ + H2O.
Giả thiết nNa2CO3 = 0,1 mol ⇒ nCO2↑ = 0,1 mol ⇝ V = 2,24 lít ⇝ Chọn đáp án C. ♣
Giả thiết nNa2CO3 = 0,1 mol ⇒ nCO2↑ = 0,1 mol ⇝ V = 2,24 lít ⇝ Chọn đáp án C. ♣
Câu 23 [982239]: Thủy phân hoàn toàn m gam tinh bột thành glucozơ. Cho toàn bộ glucozơ tham gia phản ứng tráng bạc (hiệu suất 100%), thu được 32,4 gam Ag. Giá trị của m là
A, 27,0.
B, 48,6.
C, 24,3.
D, 54,0.
HD: Diễn biến quá trình bài tập:


Giả thiết: nAg = 0,3 mol ⇒ nglucozơ = 0,15 mol.
⇒ nC6H10O5 = 0,15 mol ⇒ mtinh bột = 0,15 × 162 = 24,3 gam ⇝ Chọn đáp án C. ♣


Giả thiết: nAg = 0,3 mol ⇒ nglucozơ = 0,15 mol.
⇒ nC6H10O5 = 0,15 mol ⇒ mtinh bột = 0,15 × 162 = 24,3 gam ⇝ Chọn đáp án C. ♣
Câu 24 [906798]: Có bao nhiêu tơ tổng hợp trong các tơ: xenlulozơ axetat, visco, nitron, nilon-6,6?
A, 1.
B, 2.
C, 3.
D, 4.
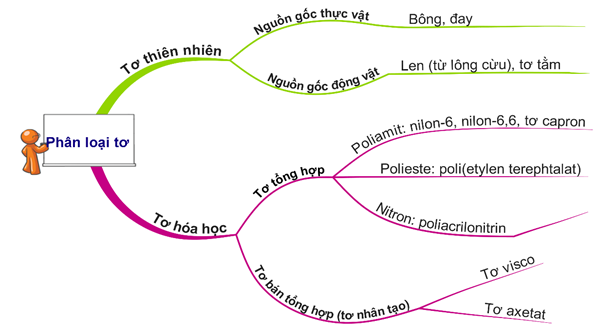
⇝ Có 2 tơ bán tổng hợp là visco và xenlulozơ axetat; 2 tơ tổng hợp là nitron và nilon-6,6.
Câu 25 [973561]: Phát biểu nào sau đây sai?
A, Glucozơ và saccarozơ đều là cacbohiđrat.
B, Trong dung dịch, glucozơ và fructozơ đều hòa tan được Cu(OH)2.
C, Glucozơ và saccarozơ đều có phản ứng tráng bạc.
D, Glucozơ và fructozơ là đồng phân của nhau.
HD: Phân tích các phát biểu:
✔️ A. đúng. glucozơ, fructozơ, saccarozơ, tinh bột, xenlulozơ đều là cacbohiđrat.
✔️ B. đúng vì glucozơ và fructozơ có tính chất của poliancol:
2.png)
❌ C. sai vì saccarozơ không có phản ứng tráng bạc. còn glucozơ thì có:

✔️ D. đúng vì glucozơ và fructozơ có cùng công thức phân tử C6H12O6.
✔️ A. đúng. glucozơ, fructozơ, saccarozơ, tinh bột, xenlulozơ đều là cacbohiđrat.
✔️ B. đúng vì glucozơ và fructozơ có tính chất của poliancol:
❌ C. sai vì saccarozơ không có phản ứng tráng bạc. còn glucozơ thì có:

✔️ D. đúng vì glucozơ và fructozơ có cùng công thức phân tử C6H12O6.
Câu 26 [679756]: Hòa tan hoàn toàn 2,8 gam Fe trong dung dịch HCl dư, thu được V lít khí H2. Giá trị của V là
A, 3,36.
B, 1,12.
C, 6,72.
D, 4,48.
HD: Bảo toàn electron ta có 2nFe = 2nH2 ⇒ nH2 = 2,8 ÷ 56 = 0,05 mol
⇒ V = 1,12 lít. ⇝ Chọn đáp án B. ♦
⇒ V = 1,12 lít. ⇝ Chọn đáp án B. ♦
Câu 27 [5541]: Khi đun nóng chất X có công thức phân tử C3H6O2 với dung dịch NaOH thu được CH3COONa. Công thức cấu tạo của X là
A, C2H5COOH.
B, CH3COOCH3
C, CH3COOC2H5 .
D, HCOOC2H5.
HD: X có 3C, tạo muối có 2C nên gốc ancol có 1C là CH3OH.
|⇝ Cấu tạo của X là CH3COOCH3: metyl axetat.
☆ Phản ứng: CH3COOCH3 + NaOH → CH3COONa + CH3OH. ❒
|⇝ Cấu tạo của X là CH3COOCH3: metyl axetat.
☆ Phản ứng: CH3COOCH3 + NaOH → CH3COONa + CH3OH. ❒
Câu 28 [311343]: Ở điều kiện thường, chất nào sau đây không phản ứng với dung dịch H2SO4 loãng?
A, FeCl3.
B, Fe2O3.
C, Fe3O4.
D, Fe(OH)3.
HD: ☆ FeCl3 không phản ứng được với dung dịch H2SO4. Còn lại:
☑ B. Fe2O3 + 3H2SO4 → Fe2(SO4)3 + 3H2O.
☑ C. Fe3O4 + 4H2SO4 → FeSO4 + Fe2(SO4)3 + 4H2O.
☑ D. 2Fe(OH)3 + 3H2SO4 → Fe2(SO4)3 + 3H2O. ❒
☑ B. Fe2O3 + 3H2SO4 → Fe2(SO4)3 + 3H2O.
☑ C. Fe3O4 + 4H2SO4 → FeSO4 + Fe2(SO4)3 + 4H2O.
☑ D. 2Fe(OH)3 + 3H2SO4 → Fe2(SO4)3 + 3H2O. ❒
Câu 29 [983274]: Nung nóng một lượng butan trong bình kín (với xúc tác thích hợp), thu được 0,48 mol hỗn hợp X gồm H2 và các hiđrocacbon mạch hở (CH4, C2H4, C2H6, C3H6, C4H8, C4H10). Cho toàn bộ X vào bình chứa dung dịch Br2 dư thì có tối đa a mol Br2 phản ứng, khối lượng bình tăng 8,26 gam và thoát ra hỗn hợp khí Y. Đốt cháy hoàn toàn Y cần vừa đủ 0,74 mol O2, thu được CO2 và H2O. Giá trị của a là
A, 0,24.
B, 0,25.
C, 0,21.
D, 0,23.
HD: bình brom tăng 8,26 gam là do 0,59 mol cụm CH2 (quy các anken về CH2).
Đốt 0,59 mol CH2 cần 0,59 × 1,5 mol O2
⇒ đốt b mol C4H10 ban đầu cần 0,59 × 1,5 + 0,74 = 1,625 mol O2.
⇒ bảo toàn nguyên tố O: 4b × 2 + 5b = 1,625 × 2 ⇒ b = 0,25 mol.
Chú ý: anken được tách ra từ C4H10 ban đầu nên nY = nC4H10 ban đầu.
Mà ∑nanken = nX – nY ⇒ a = nBr2 phản ứng = ∑nanken = 0,48 – 0,25 = 0,23 mol.
Đốt 0,59 mol CH2 cần 0,59 × 1,5 mol O2
⇒ đốt b mol C4H10 ban đầu cần 0,59 × 1,5 + 0,74 = 1,625 mol O2.
⇒ bảo toàn nguyên tố O: 4b × 2 + 5b = 1,625 × 2 ⇒ b = 0,25 mol.
Chú ý: anken được tách ra từ C4H10 ban đầu nên nY = nC4H10 ban đầu.
Mà ∑nanken = nX – nY ⇒ a = nBr2 phản ứng = ∑nanken = 0,48 – 0,25 = 0,23 mol.
Câu 30 [908878]: Cho sơ đồ chuyển hóa:

Biết: X, Y, Z, E là các hợp chất khác nhau và khác BaCO3; mỗi mũi tên ứng với một phương trình hóa học của phản ứng giữa hai chất tương ứng. Các chất X, Y thỏa mãn sơ đồ trên lần lượt là

Biết: X, Y, Z, E là các hợp chất khác nhau và khác BaCO3; mỗi mũi tên ứng với một phương trình hóa học của phản ứng giữa hai chất tương ứng. Các chất X, Y thỏa mãn sơ đồ trên lần lượt là
A, NaHCO3, BaCl2.
B, NaHCO3, Ba(OH)2.
C, CO2, Ba(OH)2.
D, CO2, BaCl2.
HD: ► Quan sát 4 đáp án thì X là NaHCO3 hoặc CO2.
mà NaOH + NaHCO3 → Na2CO3 + H2O nên Z ≡ E không thoả mãn.
⇒ X là CO2; NaOH + CO2 có 2 phản ứng:
• NaOH + CO2 → NaHCO3.
• 2NaOH + CO2 → Na2CO3 + H2O.
Lại có Z + Y → NaOH nên Y chứa nhóm OH ⇒ Ba(OH)2.
Các phản ứng xảy ra tiếp theo:
• Ba(OH)2 + Na2CO3 → BaCO3 + 2NaOH.
• Ba(OH)2 + NaHCO3 → BaCO3 + NaOH + H2O.
Hoặc Ba(OH)2 + 2NaHCO3 → BaCO3 + Na2CO3 + 2H2O.
mà NaOH + NaHCO3 → Na2CO3 + H2O nên Z ≡ E không thoả mãn.
⇒ X là CO2; NaOH + CO2 có 2 phản ứng:
• NaOH + CO2 → NaHCO3.
• 2NaOH + CO2 → Na2CO3 + H2O.
Lại có Z + Y → NaOH nên Y chứa nhóm OH ⇒ Ba(OH)2.
Các phản ứng xảy ra tiếp theo:
• Ba(OH)2 + Na2CO3 → BaCO3 + 2NaOH.
• Ba(OH)2 + NaHCO3 → BaCO3 + NaOH + H2O.
Hoặc Ba(OH)2 + 2NaHCO3 → BaCO3 + Na2CO3 + 2H2O.
Câu 31 [679812]: Xà phòng hóa hoàn toàn m gam hỗn hợp E gồm các triglixerit bằng dung dịch NaOH, thu được glixerol và hỗn hợp X gồm ba muối C17HxCOONa, C15H31COONa, C17HyCOONa có tỉ lệ mol tương ứng là 3 : 4 : 5. Hiđro hóa hoàn toàn m gam E, thu được 68,96 gam hỗn hợp Y. Nếu đốt cháy hoàn toàn m gam E thì cần vừa đủ 6,14 mol O2. Giá trị của m là
A, 68,40.
B, 60,20.
C, 68,80.
D, 68,84.
HD: Gọi công thức trung bình các triglixerit trong E là (RCOO)3C3H5.
Giả sử: E + NaOH → 3a mol C17HxCOONa + 4a mol C15H31COONa + 5a mol C17HyCOONa + ? C3H5(OH)3.
⇒ nE = nglixerol = (3a + 4a + 5a) ÷ 3 = 4a mol ⇒ số Ctrung bình E = 55.
Hiđro hoá E: C55H?O6 + b mol H2 → C55H106O6 (no).
⇒ nE = nY = 68,96 ÷ 862 = 0,08 = 4a ⇒ a = 0,02 mol.
Giải đốt 0,08 mol C55H106O6 cần 6,28 mol O2.
Lại có đốt 0,08 mol E cần 6,14 mol O2 ⇒ đốt b mol H2 cần 0,14 mol O2
⇒ b = 0,28 mol ⇒ m = mE = 68,96 – 0,28 × 2 = 68,40 gam.
Giả sử: E + NaOH → 3a mol C17HxCOONa + 4a mol C15H31COONa + 5a mol C17HyCOONa + ? C3H5(OH)3.
⇒ nE = nglixerol = (3a + 4a + 5a) ÷ 3 = 4a mol ⇒ số Ctrung bình E = 55.
Hiđro hoá E: C55H?O6 + b mol H2 → C55H106O6 (no).
⇒ nE = nY = 68,96 ÷ 862 = 0,08 = 4a ⇒ a = 0,02 mol.
Giải đốt 0,08 mol C55H106O6 cần 6,28 mol O2.
Lại có đốt 0,08 mol E cần 6,14 mol O2 ⇒ đốt b mol H2 cần 0,14 mol O2
⇒ b = 0,28 mol ⇒ m = mE = 68,96 – 0,28 × 2 = 68,40 gam.
Câu 32 [906813]: Cho hỗn hợp E gồm ba chất X, Y và ancol propylic. X, Y là hai amin kế tiếp trong cùng dãy đồng đẳng; phân tử X, Y đều có hai nhóm NH2 và gốc hiđrocacbon không no; MX < MY. Khi đốt cháy hết 0,5 mol E cần vừa đủ 2,755 mol O2, thu được H2O, N2 và 1,77 mol CO2. Phần trăm khối lượng của X trong E là
A, 30,90%.
B, 19,35%.
C, 52,34%.
D, 49,75%.
HD: ► Tách amin thành dạng CH2 + N + H; C3H8O = 3CH2 + 1H2O.
☆ Quy giải đốt:
► Nhận xét: N và H2O không cần O2 để đốt nên tìm ra số H là 0,4 mol.
Trong đó: ancol propylic: C3H8O = 3CH2 + H2O.
• Amin hai chức, có 1π, ví dụ: H2NCH=CHNH2 ⇄ 2CH2 + NH.
• Amin hai chức, có 2π, ví dụ H2NC≡CNH2 ⇄ 2CH2 + N.
• Amin hai chức, có 3π, ví dụ H2NC≡C-CH=CH2NH2 ⇄ 4CH2 + NH–1…
⇥ Thấy ngay, nếu amin có hơn 1π thì số mol H quy đổi sẽ là 0, hoặc là số âm.
Mà tính toán lại ra là 0,4 nên rõ amin có đúng 1π; cụm NH ⇒ tỉ lệ nN = nH quy đổi = 0,4 mol.
Amin hai chức nên nX + nY = 0,4 ÷ 2 = 0,2 mol ⇒ nancol = 0,5 – 0,2 = 0,3 mol.
⇒ Tương ứng nH2O quy đổi = 0,3 mol ⇒ tính ra khối lượng E là 36,18 gam.
Lại theo bảo toàn C ta có số Ctrung bình X, Y = (1,77 – 0,3 × 3) ÷ 0,2 = 4,35.
⇒ cho biết hai amin tương ứng là 0,13 mol C4H10N2 (X) và 0,07 mol C5H12N2 (Y).
⇒ Yêu cầu: %mY trong E = 0,07 × 100 ÷ 36,18 × 100% ≈ 19,35%.
☆ Quy giải đốt:

► Nhận xét: N và H2O không cần O2 để đốt nên tìm ra số H là 0,4 mol.
Trong đó: ancol propylic: C3H8O = 3CH2 + H2O.
• Amin hai chức, có 1π, ví dụ: H2NCH=CHNH2 ⇄ 2CH2 + NH.
• Amin hai chức, có 2π, ví dụ H2NC≡CNH2 ⇄ 2CH2 + N.
• Amin hai chức, có 3π, ví dụ H2NC≡C-CH=CH2NH2 ⇄ 4CH2 + NH–1…
⇥ Thấy ngay, nếu amin có hơn 1π thì số mol H quy đổi sẽ là 0, hoặc là số âm.
Mà tính toán lại ra là 0,4 nên rõ amin có đúng 1π; cụm NH ⇒ tỉ lệ nN = nH quy đổi = 0,4 mol.
Amin hai chức nên nX + nY = 0,4 ÷ 2 = 0,2 mol ⇒ nancol = 0,5 – 0,2 = 0,3 mol.
⇒ Tương ứng nH2O quy đổi = 0,3 mol ⇒ tính ra khối lượng E là 36,18 gam.
Lại theo bảo toàn C ta có số Ctrung bình X, Y = (1,77 – 0,3 × 3) ÷ 0,2 = 4,35.
⇒ cho biết hai amin tương ứng là 0,13 mol C4H10N2 (X) và 0,07 mol C5H12N2 (Y).
⇒ Yêu cầu: %mY trong E = 0,07 × 100 ÷ 36,18 × 100% ≈ 19,35%.
Câu 33 [982259]: Tiến hành thí nghiệm theo các bước:
Bước 1: Cho 5 giọt dung dịch CuSO4 0,5% vào ống nghiệm sạch.
Bước 2: Thêm 1 ml dung dịch NaOH 10% vào ống nghiệm, lắc đều, gạn phần dung dịch, giữ lại kết tủa.
Bước 3: Thêm tiếp 2 ml dung dịch glucozơ 1% vào ống nghiệm, lắc đều.
Phát biểu nào sau đây sai?
Bước 1: Cho 5 giọt dung dịch CuSO4 0,5% vào ống nghiệm sạch.
Bước 2: Thêm 1 ml dung dịch NaOH 10% vào ống nghiệm, lắc đều, gạn phần dung dịch, giữ lại kết tủa.
Bước 3: Thêm tiếp 2 ml dung dịch glucozơ 1% vào ống nghiệm, lắc đều.
Phát biểu nào sau đây sai?
A, Thí nghiệm trên chứng minh glucozơ có nhiều nhóm OH ở vị trí kề nhau.
B, Sau bước 3, kết tủa đã bị hòa tan, thu được dung dịch màu xanh lam.
C, Ở bước 3, glucozơ bị oxi hóa thành axit gluconic.
D, Ở bước 2, trong ống nghiệm xuất hiện kết tủa màu xanh.
HD: Phân tích thí nghiệm:
Bước 1 + bước 2 xảy ra: CuSO4 + 2NaOH → Cu(OH)2↓ + Na2SO4.
⇒ Chuẩn bị hoá chất: Cu(OH)2↓/OH–.
⇝ Bước 3: glucozơ hoà tan Cu(OH)2 tạo phức tan màu xanh đặc trưng (theo tính chất poliancol). phản ứng:
2C6H12O6 + Cu(OH)2 → (C6H11O6)2Cu (phức tan) + 2H2O.
⇒ Phân tích các phát biểu:
✔️ A. đúng. glucozơ có phản ứng chứng minh tính chất poliancol.
✔️ B. đúng theo hiện tượng thí nghiệm phân tích trên.
❌ C. sai vì không xảy ra phản ứng oxi hoá khử như phương trình trên.
✔️ D. đúng vì kết tủa Cu(OH)2↓ được tạo thành và có màu xanh.
Bước 1 + bước 2 xảy ra: CuSO4 + 2NaOH → Cu(OH)2↓ + Na2SO4.
⇒ Chuẩn bị hoá chất: Cu(OH)2↓/OH–.
⇝ Bước 3: glucozơ hoà tan Cu(OH)2 tạo phức tan màu xanh đặc trưng (theo tính chất poliancol). phản ứng:
2C6H12O6 + Cu(OH)2 → (C6H11O6)2Cu (phức tan) + 2H2O.
⇒ Phân tích các phát biểu:
✔️ A. đúng. glucozơ có phản ứng chứng minh tính chất poliancol.
✔️ B. đúng theo hiện tượng thí nghiệm phân tích trên.
❌ C. sai vì không xảy ra phản ứng oxi hoá khử như phương trình trên.
✔️ D. đúng vì kết tủa Cu(OH)2↓ được tạo thành và có màu xanh.
Câu 34 [136752]: Cho hỗn hợp X gồm Al và Mg tác dụng với 1 lít dung dịch gồm AgNO3 a mol/l và Cu(NO3)2 2a mol/l, thu được 45,2 gam chất rắn Y. Cho Y tác dụng với dung dịch H2SO4 đặc, nóng (dư), thu được 7,84 lít khí SO2 (ở đktc, là sản phẩm khử duy nhất). Biết các phản ứng xảy ra hoàn toàn. Giá trị của a là
A, 0,25.
B, 0,30.
C, 0,15.
D, 0,20.

Câu 35 [982298]: Hỗn hợp T gồm ba este mạch hở X (đơn chức), Y (hai chức), Z (ba chức) đều được tạo thành từ axit cacboxylic có mạch cacbon không phân nhánh và ancol. Đốt cháy hoàn toàn a gam T, thu được H2O và 1,54 mol CO2. Xà phòng hóa hoàn toàn a gam T bằng lượng vừa đủ 620 ml dung dịch NaOH 1M, thu được hỗn hợp F gồm hai muối có cùng số nguyên tử cacbon trong phân tử và 19,44 gam hỗn hợp E gồm hai ancol. Đốt cháy toàn bộ F thu được H2O, Na2CO3 và 0,61 mol CO2. Khối lượng của Y trong a gam T là
A, 2,36 gam.
B, 5,84 gam.
C, 4,72 gam.
D, 2,92 gam.
HD: Thuỷ phân este: –COO– + NaOH → –COONa (muối) + –OH (ancol).
Giả thiết nNaOH = 0,62 mol ⇒ nCOONa = 0,62 mol
⇒ đốt muối thu được 0,31 mol Na2CO3 + 0,61 mol CO2 ⇒ ∑nC = 0,92 mol.
► Axit có mạch không phân nhánh thì chỉ có thể là đơn chức hoặc hai chức.
❌ Nhẩm nhanh: nếu muối cùng C cùng đơn chức: CnH?O2Na ⇒ n = 0,92 ÷ 0,62 ≈ 1,48 (ktm).
❌ Tương tự nếu muối cùng C cùng hai chức: CnH?O4Na2 ⇒ n = 0,92 ÷ 0,31 ≈ 2,97 (ktm).
✔️ ⇒ hai muối gồm a mol CnH?O2Na và b mol CnH??O4Na2 ⇒ a + 2b = 0,62 và (a + b) × n = 0,92 ⇒ chặn 1,48 < n < 2,97 ⇒ n = 2.
⇒ Giải ra hỗn hợp muối gồm 0,3 mol CH3COONa và 0,16 mol (COONa)2.
☆ Giải ancol: nOH = nNaOH = 0,62 mol; nC ancol = ∑nC/T – ∑nC/muối = 1,54 – 0,92 = 0,62 mol.
► Điểm đặc biệt với ancol: nC = nO. Lại có este X đơn chức nên luôn có 1 ancol đơn chức CH3OH rồi.
• nếu ancol còn lại 2 chức thì đó là C2H4(OH)2. Giải hệ số mol có 0,22 mol CH3OH và 0,2 mol C2H4(OH)2.
☆ Tổ hợp lại: X là CH3COOCH3; Y là (CH3COO)2C2H4 hoặc (COOCH3)2; Z là CH3COOCH2CH2OOC-COOCH3.
❌ Nếu Y là (COOCH3)2 có ngay nZ = 0,2 mol ⇒ nY = 0,16 – 0,2 ⇝ không thoả mãn.
✔️ Nếu Y là (CH3COO)2C2H4 giải hệ số mol nX = 0,06 mol; nY = 0,04 mol và nZ = 0,16 mol.
• nếu ancol còn lại 3 chức thì đó là C3H5(OH)3. Giải hệ số mol có 0,32 mol CH3OH và 0,1 mol C3H5(OH)3 ⇒ có 0,1 mol Z là (CH3COO)3C3H5 ⇒ nCH3COONa thu được = 0,1 × 3 + nX > 0,3 mất rồi ⇝ loại.
Vậy, chỉ có một TH trên thoả mãn mà thôi, ứng với mY/T = 5,84 gam.
Giả thiết nNaOH = 0,62 mol ⇒ nCOONa = 0,62 mol
⇒ đốt muối thu được 0,31 mol Na2CO3 + 0,61 mol CO2 ⇒ ∑nC = 0,92 mol.
► Axit có mạch không phân nhánh thì chỉ có thể là đơn chức hoặc hai chức.
❌ Nhẩm nhanh: nếu muối cùng C cùng đơn chức: CnH?O2Na ⇒ n = 0,92 ÷ 0,62 ≈ 1,48 (ktm).
❌ Tương tự nếu muối cùng C cùng hai chức: CnH?O4Na2 ⇒ n = 0,92 ÷ 0,31 ≈ 2,97 (ktm).
✔️ ⇒ hai muối gồm a mol CnH?O2Na và b mol CnH??O4Na2 ⇒ a + 2b = 0,62 và (a + b) × n = 0,92 ⇒ chặn 1,48 < n < 2,97 ⇒ n = 2.
⇒ Giải ra hỗn hợp muối gồm 0,3 mol CH3COONa và 0,16 mol (COONa)2.
☆ Giải ancol: nOH = nNaOH = 0,62 mol; nC ancol = ∑nC/T – ∑nC/muối = 1,54 – 0,92 = 0,62 mol.
► Điểm đặc biệt với ancol: nC = nO. Lại có este X đơn chức nên luôn có 1 ancol đơn chức CH3OH rồi.
• nếu ancol còn lại 2 chức thì đó là C2H4(OH)2. Giải hệ số mol có 0,22 mol CH3OH và 0,2 mol C2H4(OH)2.
☆ Tổ hợp lại: X là CH3COOCH3; Y là (CH3COO)2C2H4 hoặc (COOCH3)2; Z là CH3COOCH2CH2OOC-COOCH3.
❌ Nếu Y là (COOCH3)2 có ngay nZ = 0,2 mol ⇒ nY = 0,16 – 0,2 ⇝ không thoả mãn.
✔️ Nếu Y là (CH3COO)2C2H4 giải hệ số mol nX = 0,06 mol; nY = 0,04 mol và nZ = 0,16 mol.
• nếu ancol còn lại 3 chức thì đó là C3H5(OH)3. Giải hệ số mol có 0,32 mol CH3OH và 0,1 mol C3H5(OH)3 ⇒ có 0,1 mol Z là (CH3COO)3C3H5 ⇒ nCH3COONa thu được = 0,1 × 3 + nX > 0,3 mất rồi ⇝ loại.
Vậy, chỉ có một TH trên thoả mãn mà thôi, ứng với mY/T = 5,84 gam.
Câu 36 [908885]: Hòa tan hoàn toàn 27,54 gam Al2O3 bằng một lượng vừa đủ dung dịch HNO3, thu được 267,5 gam dung dịch X. Làm lạnh X đến 10oC thì có m gam tinh thể Al(NO3)3.9H2O tách ra. Biết ở 10oC, cứ 100 gam nước hòa tan được tối đa 67,25 gam Al(NO3)3. Giá trị của m gần nhất với giá trị nào sau đây?
A, 26.
B, 84.
C, 22.
D, 45.
HD: Phản ứng vừa đủ: Al2O3 + 6HNO3 → 2Al(NO3)3 + 3H2O.
Giả thiết nAl2O3 = 27,54 ÷ 102 = 0,27 mol ⇒ nAl(NO3)3 = 0,54 mol.
⇒ 267,5 gam dung dịch X gồm 115,02 gam Al(NO3)3 + 152,48 gam H2O.
Giả sử có a mol Al(NO3)3.9H2O tách ra khi làm lạnh X về 20oC ⇒ m = 375a.
Dung dịch thu được gồm (115,02 – 213a) gam Al(NO3)3 và (152,48 – 162a) gam H2O.
Mà ở 10°C, cứ 100 gam H2O hòa tan được tối đa 67,25 gam Al(NO3)3
⇒ Tỉ lệ (115,02 – 213a) ÷ (152,48 – 162a) = 67,25 ÷ 100 ⇒ a ≈ 0,12 ⇒ m ≈ 45.
Giả thiết nAl2O3 = 27,54 ÷ 102 = 0,27 mol ⇒ nAl(NO3)3 = 0,54 mol.
⇒ 267,5 gam dung dịch X gồm 115,02 gam Al(NO3)3 + 152,48 gam H2O.
Giả sử có a mol Al(NO3)3.9H2O tách ra khi làm lạnh X về 20oC ⇒ m = 375a.
Dung dịch thu được gồm (115,02 – 213a) gam Al(NO3)3 và (152,48 – 162a) gam H2O.
Mà ở 10°C, cứ 100 gam H2O hòa tan được tối đa 67,25 gam Al(NO3)3
⇒ Tỉ lệ (115,02 – 213a) ÷ (152,48 – 162a) = 67,25 ÷ 100 ⇒ a ≈ 0,12 ⇒ m ≈ 45.
Câu 37 [26089]: Cho các phát biểu sau:
(a) Tristearin và tripanmitin đều thuộc loại triglixerit.
(b) Ở dạng mạch hở, phân tử glucozơ và fructozơ đều có nhóm chức anđehit.
(c) Thủy phân hoàn toàn các este không no đều thu được anđehit hoặc xeton.
(d) Nicotin là một loại amin rất độc có trong cây thuốc lá.
(e) Axit cacboxylic có nhiệt độ sôi cao hơn ancol có cùng phân tử khối.
Số phát biểu đúng là
(a) Tristearin và tripanmitin đều thuộc loại triglixerit.
(b) Ở dạng mạch hở, phân tử glucozơ và fructozơ đều có nhóm chức anđehit.
(c) Thủy phân hoàn toàn các este không no đều thu được anđehit hoặc xeton.
(d) Nicotin là một loại amin rất độc có trong cây thuốc lá.
(e) Axit cacboxylic có nhiệt độ sôi cao hơn ancol có cùng phân tử khối.
Số phát biểu đúng là
A, 4.
B, 5.
C, 3.
D, 2.
HD: Xem xét - phân tích các phát biểu:
☑ (a) đúng. Triglixerit ta biết là tristearin, triolein, trilinolein và tripanmitin.
☒ (b) sai. vì cấu tạo của fructozơ mạch hở có nhóm xeton, không phải anđehit.
☒ (c) sai. Ví dụ CH2=CHCOOCH3 + NaOH → CH2=CHCOONa + CH3OH (ancol metylic).
hay CH3COOCH2CH=CH2 + NaOH → CH3COONa + CH2=CHCH2OH (ancol anlylic).
☑ (d) đúng. Nicotin: C10H14N2 là một amin độc có trong cây thuốc lá.
⇝ Hút thuốc lá có hại cho sức khỏe.!
☑ (e) đúng. Axit cacboxylic có nhiệt độ sôi cao hơn ancol có cùng phân tử khối.
cái này liên quan đến lực liên kết hiđro liên phân tử của axit cacboxylic > ancol tương ứng.
⇝ có tất cả 3 phát biểu đúng. ❒
☑ (a) đúng. Triglixerit ta biết là tristearin, triolein, trilinolein và tripanmitin.
☒ (b) sai. vì cấu tạo của fructozơ mạch hở có nhóm xeton, không phải anđehit.
☒ (c) sai. Ví dụ CH2=CHCOOCH3 + NaOH → CH2=CHCOONa + CH3OH (ancol metylic).
hay CH3COOCH2CH=CH2 + NaOH → CH3COONa + CH2=CHCH2OH (ancol anlylic).
☑ (d) đúng. Nicotin: C10H14N2 là một amin độc có trong cây thuốc lá.
⇝ Hút thuốc lá có hại cho sức khỏe.!
☑ (e) đúng. Axit cacboxylic có nhiệt độ sôi cao hơn ancol có cùng phân tử khối.
cái này liên quan đến lực liên kết hiđro liên phân tử của axit cacboxylic > ancol tương ứng.
⇝ có tất cả 3 phát biểu đúng. ❒
Câu 38 [983276]: Cho các sơ đồ phản ứng xảy ra theo đúng tỉ lệ mol:
E + 2NaOH → Y + 2Z
F + 2NaOH → Z + T + H2O
Biết E, F đều là các hợp chất hữu cơ no, mạch hở, có công thức phân tử C4H6O4, được tạo thành từ axit cacboxylic và ancol. Cho các phát biểu sau:
(a) Chất T tác dụng với dung dịch HCl sinh ra axit fomic.
(b) Chất Z có nhiệt độ sôi thấp hơn ancol etylic.
(c) Chất E có khả năng tham gia phản ứng tráng bạc.
(d) Đun nóng Z với dung dịch H2SO4 đặc ở 170°C, thu được anken.
(e) Chất F tác dụng với dung dịch NaHCO3, sinh ra khí CO2.
Số phát biểu đúng là
E + 2NaOH → Y + 2Z
F + 2NaOH → Z + T + H2O
Biết E, F đều là các hợp chất hữu cơ no, mạch hở, có công thức phân tử C4H6O4, được tạo thành từ axit cacboxylic và ancol. Cho các phát biểu sau:
(a) Chất T tác dụng với dung dịch HCl sinh ra axit fomic.
(b) Chất Z có nhiệt độ sôi thấp hơn ancol etylic.
(c) Chất E có khả năng tham gia phản ứng tráng bạc.
(d) Đun nóng Z với dung dịch H2SO4 đặc ở 170°C, thu được anken.
(e) Chất F tác dụng với dung dịch NaHCO3, sinh ra khí CO2.
Số phát biểu đúng là
A, 4.
B, 5.
C, 3.
D, 2.
HD: Ta có CE = CY + 2CZ = 4 ⇒ CY = 2; CZ = 1 tương ứng Z là CH3OH và Y là (COONa)2.
CF = CZ + CT = 4 ⇒ CT = 3 ⇒ T là CH2(COONa)2.
Vậy cấu tạo E là (COOCH3)2 còn F là HOOCCH2COOCH3.
⇝ Phân tích các phát biểu tương ứng:
❌ (a) sai vì T là CH2(COONa)2 + 2HCl → CH2(COOH)2 (axit malonic) + 2NaCl.
✔️ (b) đúng vì nhiệt độ sôi của Z (CH3OH) nhỏ hơn ancol etylic (C2H5OH).
❌ (c) sai vì E là (COOCH3)2 không có khả năng tham gia phản ứng tráng bạc.
❌ (d) sai vì Z là CH3OH là ancol có 1C không tách nước được để tạo anken.
✔️ (e) đúng vì F là tạp chức có chứa chức axit cacboxylic nên có phản ứng:
HOOCCH2COOCH3 + NaHCO3 → NaOOCCH2COOCH3 + CO2↑ + H2O.
⇝ Có 2/5 phát biểu đúng ⇝ Chọn đáp án D. ♠
CF = CZ + CT = 4 ⇒ CT = 3 ⇒ T là CH2(COONa)2.
Vậy cấu tạo E là (COOCH3)2 còn F là HOOCCH2COOCH3.
⇝ Phân tích các phát biểu tương ứng:
❌ (a) sai vì T là CH2(COONa)2 + 2HCl → CH2(COOH)2 (axit malonic) + 2NaCl.
✔️ (b) đúng vì nhiệt độ sôi của Z (CH3OH) nhỏ hơn ancol etylic (C2H5OH).
❌ (c) sai vì E là (COOCH3)2 không có khả năng tham gia phản ứng tráng bạc.
❌ (d) sai vì Z là CH3OH là ancol có 1C không tách nước được để tạo anken.
✔️ (e) đúng vì F là tạp chức có chứa chức axit cacboxylic nên có phản ứng:
HOOCCH2COOCH3 + NaHCO3 → NaOOCCH2COOCH3 + CO2↑ + H2O.
⇝ Có 2/5 phát biểu đúng ⇝ Chọn đáp án D. ♠
Câu 39 [983277]: Hỗn hợp X gồm Cu, CuO, Fe, Fe3O4. Hòa tan hết m gam X trong dung dịch chứa 0,775 mol HCl (dư 25% so với lượng phản ứng), thu được 0,06 mol H2 và 250 gam dung dịch Y. Mặt khác, hòa tan hết m gam X trong dung dịch H2SO4 đặc nóng, thu được dung dịch Z (chứa 3 chất tan) và 0,09 mol SO2 (sản phẩm khử duy nhất của H2SO4). Cho Z tác dụng với dung dịch Ba(OH)2 dư, thu được kết tủa T. Nung T trong không khí đến khối lượng không đổi, thu được 103,22 gam chất rắn. Nồng độ phần trăm FeCl3 trong Y là
A, 1,30%.
B, 2,60%.
C, 3,25%.
D, 3,90%.
HD: ☆ Giải X + HCl: ta có nHCl phản ứng = 0,775 ÷ 1,25 = 0,62 mol.
• bảo toàn e mở rộng: ∑nH+ phản ứng = 2nO trong oxit + 2nH2 ⇒ nO trong oxit = 0,25 mol.
☆ Giải X + H2SO4: chú ý nFe > nH2 = 0,06 mol ⇒ nếu H2SO4 dùng dư thì Fe → Fe3+
⇒ 2nSO2↑ > 3nFe = 0,18 ⇒ trái giả thiết ⇒ H2SO4 hết.
⇒ Z gồm 3 chất tan là a mol FeSO4; b mol CuSO4 và c mol Fe2(SO4)3.
• bảo toàn e gián tiếp: ∑nSO42– trong muối = nSO2 + nO trong oxit = 0,34 mol.
⇒ a + b + 3c = 0,34 và có 0,34 mol BaSO4 trong chất rắn cuối cùng.
103,22 gam gồm 0,34 mol BaSO4 + (½a + c) mol Fe2O3 + b mol CuO.
⇒ 160 × (½a + c) + 80c + 0,34 × 233 = 103,22 ⇒ a + b + 2c = 0,3.
Vậy giải ra (a + b) = 0,22 và c = 0,04 mol.
Quay lại với yêu cầu ở dung dịch Y: gồm x mol FeCl2 + y mol CuCl2 + z mol FeCl3.
Bảo toàn nguyên tố Cl: ∑nCl– trong muối = 2x + 2y + 3z = 0,62.
Mà ∑nnguyên tố kim loại trong muối Y = ∑nnguyên tố kim loại trong muối Z
⇄ x + y + z = a + b + 2c = 0,3 ⇒ giải (x + y) = 0,28 và z = 0,02 mol.
► Đề cũng chỉ yêu cầu liên quan đến FeCl3 thôi (vì có hỏi FeCl2 hay CuCl2 thì cũng chưa đủ giả thiết để giải)
⇒ Yêu cầu C%mFeCl3 = 0,02 × 162,5 ÷ 250 × 100% = 1,30% ⇝ Chọn đáp án A. ♥
• bảo toàn e mở rộng: ∑nH+ phản ứng = 2nO trong oxit + 2nH2 ⇒ nO trong oxit = 0,25 mol.
☆ Giải X + H2SO4: chú ý nFe > nH2 = 0,06 mol ⇒ nếu H2SO4 dùng dư thì Fe → Fe3+
⇒ 2nSO2↑ > 3nFe = 0,18 ⇒ trái giả thiết ⇒ H2SO4 hết.
⇒ Z gồm 3 chất tan là a mol FeSO4; b mol CuSO4 và c mol Fe2(SO4)3.
• bảo toàn e gián tiếp: ∑nSO42– trong muối = nSO2 + nO trong oxit = 0,34 mol.
⇒ a + b + 3c = 0,34 và có 0,34 mol BaSO4 trong chất rắn cuối cùng.
103,22 gam gồm 0,34 mol BaSO4 + (½a + c) mol Fe2O3 + b mol CuO.
⇒ 160 × (½a + c) + 80c + 0,34 × 233 = 103,22 ⇒ a + b + 2c = 0,3.
Vậy giải ra (a + b) = 0,22 và c = 0,04 mol.
Quay lại với yêu cầu ở dung dịch Y: gồm x mol FeCl2 + y mol CuCl2 + z mol FeCl3.
Bảo toàn nguyên tố Cl: ∑nCl– trong muối = 2x + 2y + 3z = 0,62.
Mà ∑nnguyên tố kim loại trong muối Y = ∑nnguyên tố kim loại trong muối Z
⇄ x + y + z = a + b + 2c = 0,3 ⇒ giải (x + y) = 0,28 và z = 0,02 mol.
► Đề cũng chỉ yêu cầu liên quan đến FeCl3 thôi (vì có hỏi FeCl2 hay CuCl2 thì cũng chưa đủ giả thiết để giải)
⇒ Yêu cầu C%mFeCl3 = 0,02 × 162,5 ÷ 250 × 100% = 1,30% ⇝ Chọn đáp án A. ♥
Câu 40 [982009]: Cho các phát biểu sau:
(a) Nước có chứa nhiều ion Mg2+ và Ca2+ được gọi là nước cứng.
(b) Để bảo vệ vỏ tàu biển bằng thép, người ta gắn các tấm kẽm vào vỏ tàu.
(c) Kim loại Cu và Ag đều tan được trong dung dịch HNO3 loãng, dư.
(d) Bột nhôm tự bốc cháy khi tiếp xúc với khí clo.
Số phát biểu đúng là
(a) Nước có chứa nhiều ion Mg2+ và Ca2+ được gọi là nước cứng.
(b) Để bảo vệ vỏ tàu biển bằng thép, người ta gắn các tấm kẽm vào vỏ tàu.
(c) Kim loại Cu và Ag đều tan được trong dung dịch HNO3 loãng, dư.
(d) Bột nhôm tự bốc cháy khi tiếp xúc với khí clo.
Số phát biểu đúng là
A, 2.
B, 3.
C, 4.
D, 1.
HD: Phân tích các phát biểu:
✔️ (a) đúng theo khái niệm nước cứng:

✔️ (b) đúng theo phương pháp điện hoá bảo vệ kim loại khi Zn-Fe tiếp xúc NaCl sẽ xảy ra ăn mòn, và kim loại bị phá huỷ sẽ là Zn thay vì thép. Chú ý Zn-Fe gần nhau nên tốc độ ăn mòn sẽ chậm, và khi Zn bị phá huỷ hết thì cần thay tấm Zn khác.
✔️ (c) đúng vì HNO3 là chất oxi hoá mạnh, oxi hoá được hầu hết các kim loại (trừ Au, Pt,...)
✔️ (d) đúng, Al tự bốc cháy khi tiếp xúc với clo.
⇝ Tất cả 4/4 phát biểu đều đúng ⇝ Chọn đáp án C. ♣
✔️ (a) đúng theo khái niệm nước cứng:

✔️ (b) đúng theo phương pháp điện hoá bảo vệ kim loại khi Zn-Fe tiếp xúc NaCl sẽ xảy ra ăn mòn, và kim loại bị phá huỷ sẽ là Zn thay vì thép. Chú ý Zn-Fe gần nhau nên tốc độ ăn mòn sẽ chậm, và khi Zn bị phá huỷ hết thì cần thay tấm Zn khác.
✔️ (c) đúng vì HNO3 là chất oxi hoá mạnh, oxi hoá được hầu hết các kim loại (trừ Au, Pt,...)
✔️ (d) đúng, Al tự bốc cháy khi tiếp xúc với clo.
⇝ Tất cả 4/4 phát biểu đều đúng ⇝ Chọn đáp án C. ♣