Đáp án
1A
2C
3B
4B
5B
6A
7D
8D
9B
10D
11A
12D
13C
14D
15D
16C
17A
18A
19B
20B
21D
22C
23B
24C
25C
26C
27A
28D
29A
30A
31C
32C
33A
34A
35B
36A
37A
38D
39D
40C
Đáp án Đề minh họa số 27 thi Tốt Nghiệp Trung học Phổ Thông 2024 môn Hóa học
Câu 1 [911542]: Dung dịch chất nào sau đây hòa tan được Al(OH)3?
A, H2SO4.
B, NaCl.
C, Na2SO4.
D, KCl.
HD: Các muối NaCl, KCl và Na2SO4 đều không có phản ứng với Al(OH)3.
Còn lại chỉ có H2SO4 phản ứng và thoả mãn hoà tan Al(OH)3:
3H2SO4 + 2Al(OH)3 → Al2(SO4)3 + 3H2O.
Còn lại chỉ có H2SO4 phản ứng và thoả mãn hoà tan Al(OH)3:
3H2SO4 + 2Al(OH)3 → Al2(SO4)3 + 3H2O.
Câu 2 [60656]: Trong hợp chất, crom không có số oxi hóa nào sau đây?
A, +2.
B, +3.
C, +8.
D, +6.
Giải: Crom có các số oxi hóa từ +1 đến +6. Thường gặp là +2, +3 và +6 ⇒ chọn C.
Câu 3 [906747]: Kim loại nào sau đây là kim loại kiềm?
A, Mg.
B, Na.
C, Be.
D, Fe.
HD: Mẹo nhớ: Lâu nay không rảnh cà fê.
⇒ Tương ứng các kim loại kiềm: Li Na K Rb Cs Fr.
⇒ Tương ứng các kim loại kiềm: Li Na K Rb Cs Fr.
Câu 4 [679747]: Đun nước cứng lâu ngày trong ấm nước xuất hiện một lớp cặn. Thành phần chính của lớp cặn đó là
A, CaCl2.
B, CaCO3.
C, Na2CO3.
D, CaO.
HD: Thành phần chính của lớp cặn đó là CaCO3. Nguyên nhân:
Ca(HCO3)2 –––to–→ CaCO3↓ + CO2↑ + H2O.
☆ Để làm sạch, có thể sử dụng giấm ăn:
2CH3COOH + CaCO3 → (CH3COO)2Ca + 2H2O.
Ca(HCO3)2 –––to–→ CaCO3↓ + CO2↑ + H2O.
☆ Để làm sạch, có thể sử dụng giấm ăn:
2CH3COOH + CaCO3 → (CH3COO)2Ca + 2H2O.
Câu 5 [39846]: Hợp chất nào sau đây được dùng để làm bột nở cho bánh kẹo, chất tạo khí trong thuốc sủi bọt và thuốc trị chứng thừa axit trong dạ dày?
A, Na2CO3.
B, NaHCO3.
C, NaCl.
D, NaOH.
HD: Ứng dụng làm bột nở do NaHCO3 dễ bị nhiệt phân hủy sinh ra khí CO2 và H2O.
Ứng dụng làm thuốc do NaHCO3 có khả năng phản ứng với axit dư trong dạ dày. ❒
Ứng dụng làm thuốc do NaHCO3 có khả năng phản ứng với axit dư trong dạ dày. ❒
Câu 6 [257715]: Kim loại nào sau đây có tính khử yếu hơn kim loại Zn?
A, Fe.
B, K.
C, Al.
D, Mg.
HD: Theo dãy điện hoá, thứ tự tính khử các kim loại giảm dần: K > Mg > Al > Fe ⇝ Chọn đáp án A. ♥
Câu 7 [331003]: Chất nào dưới đây trong phân tử không có nitơ ?
A, Tơ tằm.
B, Tơ capron.
C, Protein.
D, Tơ visco.
HD: Phân tích các đáp án:
✔️ A. Tơ tằm có thành phần protein ⇒ chứa liên kết peptit CO–NH ⇝ có nguyên tố N.
✔️ B. Tơ capro trùng ngưng từ H2N[CH2]5COOH ⇝ có nguyên tố N.
✔️ C. Tương tự A, protein ⇒ chứa liên kết peptit CO–NH ⇝ có nguyên tố N.
❌ D. Tơ visco có nguồn gốc từ xenlulozơ (C6H10O5)n, không chứa nguyên tố N.
✔️ A. Tơ tằm có thành phần protein ⇒ chứa liên kết peptit CO–NH ⇝ có nguyên tố N.
✔️ B. Tơ capro trùng ngưng từ H2N[CH2]5COOH ⇝ có nguyên tố N.
✔️ C. Tương tự A, protein ⇒ chứa liên kết peptit CO–NH ⇝ có nguyên tố N.
❌ D. Tơ visco có nguồn gốc từ xenlulozơ (C6H10O5)n, không chứa nguyên tố N.
Câu 8 [906820]: Số nhóm amino (NH2) trong phân tử glyxin là
A, 2.
B, 4.
C, 3.
D, 1.
HD: Cấu tạo glyxin: 
⇝ phân tử chứa 1 nhóm amino (NH2).

⇝ phân tử chứa 1 nhóm amino (NH2).
Câu 9 [908864]: Chất nào sau đây có tính lưỡng tính?
A, CaO.
B, Al2O3.
C, NaOH.
D, HCl.
HD: Al2O3 là oxit lưỡng tính:
• vừa có khả năng tác dụng với axit: Al2O3 + 6HCl → 2AlCl3 + 3H2O.
• vừa có khả năng tác dụng với bazơ: Al2O3 + 2NaOH → 2NaAlO2 + H2O.
Còn lại: CaO là oxit bazơ; NaOH là hiđroxit bazơ; HCl là axit.
• vừa có khả năng tác dụng với axit: Al2O3 + 6HCl → 2AlCl3 + 3H2O.
• vừa có khả năng tác dụng với bazơ: Al2O3 + 2NaOH → 2NaAlO2 + H2O.
Còn lại: CaO là oxit bazơ; NaOH là hiđroxit bazơ; HCl là axit.
Câu 10 [20762]: Xà phòng hóa chất nào sau đây thu được glixerol?
A, Benzyl axetat.
B, Metyl axetat.
C, Metyl propionat.
D, Tristearin.
Giải: A. Benzyl axetat: CH3COOCH2C6H5 + NaOH → CH3COONa + C6H5CH2OH.
B. Metyl axetat: CH3COOCH3 + NaOH → CH3COONa + CH3OH.
C. Metyl propionat: C2H5COOCH3 + NaOH → C2H5COONa + CH3OH.
D. Tristearin: (C17H35COO)3C3H5 + 3NaOH → 3C17H35COONa + C3H5(OH)3.
⇒ chọn D.
B. Metyl axetat: CH3COOCH3 + NaOH → CH3COONa + CH3OH.
C. Metyl propionat: C2H5COOCH3 + NaOH → C2H5COONa + CH3OH.
D. Tristearin: (C17H35COO)3C3H5 + 3NaOH → 3C17H35COONa + C3H5(OH)3.
⇒ chọn D.
Câu 11 [679785]: Khí X được tạo ra trong quá trình đốt nhiên liệu hóa thạch, gây hiệu ứng nhà kính. Khí X là
A, CO2.
B, H2.
C, N2.
D, O2.
HD: Hiệu ứng nhà kính là hiện tượng khí quyển (đóng vai trò như tấm lá chắn) ngăn chặn nhiều tia bức xạ nhiệt của Trái Đất, không cho chúng thoát vào vũ trụ, làm khí quyển Trái Đất nóng lên.

Tác nhân đóng vai trò quan trọng nhất gây “hiệu ứng nhà kính” là CO2 ⇝ Chọn đáp án A. ♥

Tác nhân đóng vai trò quan trọng nhất gây “hiệu ứng nhà kính” là CO2 ⇝ Chọn đáp án A. ♥
Câu 12 [58816]: Hợp kim nào sau đây siêu nhẹ, được dùng trong vật liệu hàng không?
A, Fe – C.
B, Fe – Cr.
C, Cu – Zn.
D, Li – Al.
HD: Al, Li là kim loại nhẹ (Li nhẹ nhất)
⇝ hợp kim của Li – Al siêu nhẹ được dùng trong vật liệu hàng không. ❒
⇝ hợp kim của Li – Al siêu nhẹ được dùng trong vật liệu hàng không. ❒
Câu 13 [21885]: Tên gọi của peptit có cấu tạo HOOCCH2NHCOCH(CH3)NH2 là
A, Val-Ala.
B, Ala-Val.
C, Ala-Gly.
D, Gly-Ala.
Phải đọc từ  -amino axit đầu N nên phải là Ala-Gly chứ không phải Gly-Ala
-amino axit đầu N nên phải là Ala-Gly chứ không phải Gly-Ala
Chọn C
 -amino axit đầu N nên phải là Ala-Gly chứ không phải Gly-Ala
-amino axit đầu N nên phải là Ala-Gly chứ không phải Gly-AlaChọn C
Câu 14 [679546]: Chất nào sau đây thuộc loại polisaccarit?
A, Fructozơ.
B, Glucozơ.
C, Saccarozơ.
D, Tinh bột.
HD: Bài học phân loại hợp chất cacbohiđrat:

⇒ Trong 4 phương án, tinh bột thuộc loại polisaccarit ⇝ Chọn đáp án D. ♠

⇒ Trong 4 phương án, tinh bột thuộc loại polisaccarit ⇝ Chọn đáp án D. ♠
Câu 15 [39798]: Vonfram được dùng để chế tạo dây tóc cho bóng đèn sợi đốt là do kim loại này có
A, độ cứng cao.
B, tính ánh kim.
C, khả năng dẫn điện tốt.
D, nhiệt độ nóng chảy cao.
HD: Đó chính là do vonfram có nhiệt độ nóng chảy cao (khoảng 3400oC)
nên rất khó nóng chảy, đáp ứng được yêu cầu chế tạo dây tóc bóng đèn. Đáp án D.
nên rất khó nóng chảy, đáp ứng được yêu cầu chế tạo dây tóc bóng đèn. Đáp án D.
Câu 16 [906780]: Chất X có công thức FeSO4. Tên gọi của X là
A, sắt(III) sunfua.
B, sắt(II) sunfua.
C, sắt(II) sunfat.
D, sắt(III) sunfat.

Câu 17 [911556]: Este nào sau đây có phản ứng tráng bạc?
A, HCOOCH3.
B, CH3COOCH3.
C, CH3COOC2H5.
D, C2H5COOCH3.
HD: Các este dạng ankyl fomat có cấu tạo đặc biệt:
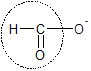
là hình dạng nhóm chức anđehit CHO nên có khả năng tráng bạc.
⇝ trong 4 phương án, thoả mãn là đáp án A. HCOOCH3 (metyl fomat).

là hình dạng nhóm chức anđehit CHO nên có khả năng tráng bạc.
⇝ trong 4 phương án, thoả mãn là đáp án A. HCOOCH3 (metyl fomat).
Câu 18 [982232]: Ở nhiệt độ cao, CO khử được oxit nào sau đây?
A, Fe2O3.
B, Na2O.
C, CaO.
D, K2O.
HD: Bài học điều chế kim loại bằng phương pháp nhiệt luyện:

⇒ dùng CO (nhiệt khí) khử được Fe2O3 thu được kim loại Fe:
3CO + Fe2O3 –––to–→ 2Fe + 3CO2↑.

⇒ dùng CO (nhiệt khí) khử được Fe2O3 thu được kim loại Fe:
3CO + Fe2O3 –––to–→ 2Fe + 3CO2↑.
Câu 19 [906741]: Chất nào sau đây tác dụng với dung dịch HCl sinh ra khí H2?
A, BaO.
B, Mg.
C, Ca(OH)2.
D, Mg(OH)2.
HD: Các phản ứng xảy ra:
❌ A. BaO + 2HCl → BaCl2 + H2O.
✔️ B. Mg + 2HCl → MgCl2 + H2↑.
❌ C. Ca(OH)2 + 2HCl → CaCl2 + 2H2O.
❌ D. Mg(OH)2 + 2HCl → MgCl2 + 2H2O.
❌ A. BaO + 2HCl → BaCl2 + H2O.
✔️ B. Mg + 2HCl → MgCl2 + H2↑.
❌ C. Ca(OH)2 + 2HCl → CaCl2 + 2H2O.
❌ D. Mg(OH)2 + 2HCl → MgCl2 + 2H2O.
Câu 20 [256270]: Công thức phân tử của etilen là
A, C3H4.
B, C2H4.
C, CH4.
D, C4H4.
HD: Công thức cấu tạo của etilen là CH2=CH2
⇝ Công thức phân tử tương ứng: C2H4 ⇝ Chọn đáp án B. ♦
⇝ Công thức phân tử tương ứng: C2H4 ⇝ Chọn đáp án B. ♦
Câu 21 [18195]: Cho 17,64 gam axit glutamic (H2NC3H5(COOH)2) tác dụng hoàn toàn với dung dịch KOH dư, thu được dung dịch chứa m gam muối. Giá trị của m là
A, 20,28.
B, 22,92.
C, 22,20.
D, 26,76.
HD: ☆ Phản ứng: H2NC3H5(COOH)2 + 2KOH → H2NC3H5(COOK)2 + 2H2O.
Giả thiết: naxit glutamic = 17,64 ÷ 147 = 0,12 mol ⇒ nmuối = 0,12 mol.
⇝ Yêu cầu: m = 0,12 × (147 + 2 × 38) = 26,76 gam. ❒
► muối kali, rất nhiều bạn sai cái sai có vẻ ngớ ngẩn nhưng thực sự như vậy:
đó là tính m = 0,12 × (147 + 2 × 22) = 22,92 gam muối natri.!
Giả thiết: naxit glutamic = 17,64 ÷ 147 = 0,12 mol ⇒ nmuối = 0,12 mol.
⇝ Yêu cầu: m = 0,12 × (147 + 2 × 38) = 26,76 gam. ❒
► muối kali, rất nhiều bạn sai cái sai có vẻ ngớ ngẩn nhưng thực sự như vậy:
đó là tính m = 0,12 × (147 + 2 × 22) = 22,92 gam muối natri.!
Câu 22 [908873]: Cho 10 gam CaCO3 tác dụng hết với dung dịch HCl dư, thu được V lít khí CO2. Giá trị của V là
A, 3,36.
B, 4,48.
C, 2,24.
D, 1,12.
HD: Phản ứng: CaCO3 + 2HCl → CaCl2 + CO2↑ + H2O.
Giả thiết: nCaCO3 = 0,1 mol ⇒ nCO2 = 0,1 mol
⇒ Yêu cầu: V = 0,1 × 2,24 lít ⇝ Chọn đáp án C. ♣
Giả thiết: nCaCO3 = 0,1 mol ⇒ nCO2 = 0,1 mol
⇒ Yêu cầu: V = 0,1 × 2,24 lít ⇝ Chọn đáp án C. ♣
Câu 23 [908876]: Thủy phân hoàn toàn m gam tinh bột thành glucozơ. Cho toàn bộ glucozơ tham gia phản ứng tráng bạc (hiệu suất 100%), thu được 21,6 gam Ag. Giá trị của m là
A, 36,0.
B, 16,2.
C, 18,0.
D, 32,4.
HD: Quá trình các phản ứng xảy ra:


Từ tỉ lệ, bấm máy: m = 21,6 ÷ 108 ÷ 2 × 162 = 16,2 gam.


Từ tỉ lệ, bấm máy: m = 21,6 ÷ 108 ÷ 2 × 162 = 16,2 gam.
Câu 24 [906846]: Có bao nhiêu tơ tổng hợp trong các tơ: xenlulozơ axetat, capron, nitron, nilon–6,6?
A, 4.
B, 2.
C, 3.
D, 1.
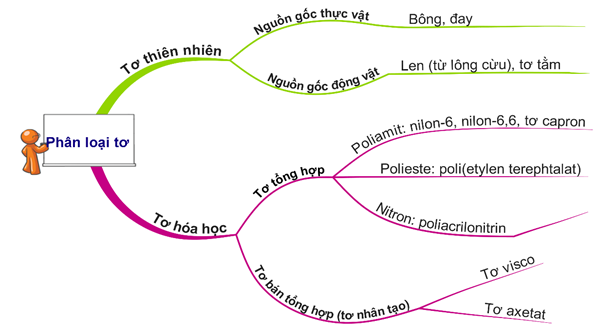
⇝ Có 3 tơ tổng hợp là capron (nilon-6), nitron và nilon-6,6.
Câu 25 [981919]: Phát biểu nào sau đây đúng?
A, Amilozơ và amilopectin đều có cấu trúc mạch phân nhánh.
B, Trong phân tử glucozơ có 4 nhóm ancol (OH).
C, Ở điều kiện thường, saccarozơ là chất rắn kết tinh.
D, Saccarozơ có phản ứng tráng bạc.
HD: Phân tích các phát biểu:
❌ A. sai vì amilozơ có cấu trúc mạch không phân nhánh còn amilopectin có cấu trúc mạch phân nhánh.
❌ B. sai vì phân tử glucozơ có 5 nhóm OH:

✔️ C. đúng theo tính chất vật lý của saccarozơ.
❌ D. sai vì saccarozơ không có phản ứng tráng bạc.
❌ A. sai vì amilozơ có cấu trúc mạch không phân nhánh còn amilopectin có cấu trúc mạch phân nhánh.
❌ B. sai vì phân tử glucozơ có 5 nhóm OH:

✔️ C. đúng theo tính chất vật lý của saccarozơ.
❌ D. sai vì saccarozơ không có phản ứng tráng bạc.
Câu 26 [973552]: Cho 2,7 gam Al phản ứng hoàn toàn với dung dịch HCl dư, thu được V lít khí H2 (đktc). Giá trị của V là
A, 4,48.
B, 2,24.
C, 3,36.
D, 6,72.
HD: Phản ứng xảy ra: 2Al + 6HCl → 2AlCl3 + 3H2↑.
Hay đơn giản là bảo toàn electron ta có: 3nAl = 2nH2
⇒ nH2 = 0,15 mol ⇒ V = 0,15 × 22,4 = 3,36 lít.
Hay đơn giản là bảo toàn electron ta có: 3nAl = 2nH2
⇒ nH2 = 0,15 mol ⇒ V = 0,15 × 22,4 = 3,36 lít.
Câu 27 [982242]: Este X có công thức phân tử C4H8O2. Thủy phân X trong dung dịch H2SO4 loãng, đun nóng, thu được sản phẩm gồm ancol metylic và chất hữu cơ Y. Công thức của Y là
A, C2H5COOH.
B, HCOOH.
C, C2H5OH.
D, CH3COOH.
HD: sản phẩm có ancol metylic: CH3OH ⇒ este có dạng RCOOCH3.
mà công thức phân tử este là C4H8O2 ⇒ cấu tạo tương ứng là C2H5COOCH3 ⇝ Chọn đáp án A. ♥
mà công thức phân tử este là C4H8O2 ⇒ cấu tạo tương ứng là C2H5COOCH3 ⇝ Chọn đáp án A. ♥
Câu 28 [911501]: Nung nóng Fe(OH)3 đến khối lượng không đổi, thu được chất rắn là
A, Fe3O4.
B, Fe.
C, FeO.
D, Fe2O3.
HD: Tổng quát các hiđroxit kim loại (trừ kiềm) dễ bị nhiệt phân:
☆ 2M(OH)n ––to→ M2On + nH2O.
⇒ Với Fe(OH)3 thì tương ứng thu được Fe2O3 và H2O.
☆ 2M(OH)n ––to→ M2On + nH2O.
⇒ Với Fe(OH)3 thì tương ứng thu được Fe2O3 và H2O.
Câu 29 [679623]: Nung nóng 0,1 mol C4H10 có xúc tác thích hợp, thu được hỗn hợp khí gồm H2, CH4, C2H4, C2H6, C3H6, C4H8 và C4H10. Dẫn X qua bình đựng dung dịch Br2 dư, sau khi phản ứng xảy ra hoàn toàn thấy khối lượng bình tăng m gam và có hỗn hợp khí Y thoát ra. Đốt cháy toàn bộ Y cần vừa đủ 6,832 lít khí O2. Giá trị của m là
A, 3,22.
B, 2,80.
C, 3,72.
D, 4,20.
HD: m gam bình brom tăng chính là các anken ⇒ Tinh tế xử lý quy đổi thành a mol cụm CH2.
Giải đốt 0,1 mol C4H10 cần (0,1 × 4 + 0,1 × 10 ÷ 4) = 0,65 mol O2.
Mà 0,1 mol C4H10 cracking tạo a mol CH2 + Y.
Giả thiết đốt Y cần 0,305 mol O2 ⇒ bảo toàn số mol O2 cần đốt:
⇒ đốt a mol CH2 cần 0,345 mol O2 ⇒ a = 0,345 ÷ 1,5 = 0,23 mol.
⇒ Đơn giản yêu cầu m = 14a = 14 × 0,23 = 3,22 gam ⇝ Chọn đáp án A. ♥
Giải đốt 0,1 mol C4H10 cần (0,1 × 4 + 0,1 × 10 ÷ 4) = 0,65 mol O2.
Mà 0,1 mol C4H10 cracking tạo a mol CH2 + Y.
Giả thiết đốt Y cần 0,305 mol O2 ⇒ bảo toàn số mol O2 cần đốt:
⇒ đốt a mol CH2 cần 0,345 mol O2 ⇒ a = 0,345 ÷ 1,5 = 0,23 mol.
⇒ Đơn giản yêu cầu m = 14a = 14 × 0,23 = 3,22 gam ⇝ Chọn đáp án A. ♥
Câu 30 [23850]: Cho kim loại M và các chất X, Y, Z thỏa mãn sơ đồ phản ứng sau:

Các chất X và Z lần lượt là
Các chất X và Z lần lượt là
A, AlCl3 và Al(OH)3.
B, AlCl3 và BaCO3.
C, CrCl3 và BaCO3.
D, FeCl3 và Fe(OH)3.
HD: Kim loại M là Al, các phương trình phản ứng tương ứng xảy ra theo sơ đồ là:
• 2Al + 3Cl2 ––to→ 2AlCl3 (X).
• 2AlCl3 + 4Ba(OH)2 → Ba(AlO2)2 (Y) + 3BaCl2 + 4H2O.
• Ba(AlO2)2 + 2CO2 (dư) + 4H2O → Ba(HCO3)2 + 2Al(OH)3↓ (Z). ❒
• 2Al + 3Cl2 ––to→ 2AlCl3 (X).
• 2AlCl3 + 4Ba(OH)2 → Ba(AlO2)2 (Y) + 3BaCl2 + 4H2O.
• Ba(AlO2)2 + 2CO2 (dư) + 4H2O → Ba(HCO3)2 + 2Al(OH)3↓ (Z). ❒
Câu 31 [633187]: Xà phòng hóa hoàn toàn m gam hỗn hợp X gồm các triglixerit bằng dung dịch NaOH, thu được glixerol và hỗn hợp Y gồm ba muối C17HxCOONa; C17H35COONa; C17HyCOONa. Hiđro hóa hoàn toàn m gam X, thu được 71,2 gam một triglixerit Z. Nếu đốt cháy hoàn toàn m gam X thì cần vừa đủ 6,43 mol O2. Biết m gam X làm mất màu tối đa a mol brom trong dung dịch. Giá trị của a là.
A, 0,06.
B, 0,09.
C, 0,18.
D, 0,12.
HD: Gọi công thức trung bình các triglixerit trong X là (RCOO)3C3H5.
Thuỷ phân: X + NaOH → C17HxCOONa + C17H35COONa + C17HyCOONa + C3H5(OH)3.
Hiđro hoá X: m gam X + a mol H2 → 71,2 gam Z: C57H110O6 (điểm đặc biệt ở số C).
⇒ nX = nZ = 71,2 ÷ 890 = 0,08 mol.
Giải đốt 0,08 mol C57H110O6 cần 6,52 mol O2.
Lại có đốt 0,08 mol X cần 6,43 mol O2 ⇒ đốt a mol H2 cần 0,09 mol O2 ⇒ a = 0,18 mol.
► Chú ý tương quan 1H2 ⇄ 1Br2 để làm no X nhé!.
Thuỷ phân: X + NaOH → C17HxCOONa + C17H35COONa + C17HyCOONa + C3H5(OH)3.
Hiđro hoá X: m gam X + a mol H2 → 71,2 gam Z: C57H110O6 (điểm đặc biệt ở số C).
⇒ nX = nZ = 71,2 ÷ 890 = 0,08 mol.
Giải đốt 0,08 mol C57H110O6 cần 6,52 mol O2.
Lại có đốt 0,08 mol X cần 6,43 mol O2 ⇒ đốt a mol H2 cần 0,09 mol O2 ⇒ a = 0,18 mol.
► Chú ý tương quan 1H2 ⇄ 1Br2 để làm no X nhé!.
Câu 32 [981923]: Hỗn hợp E gồm hai amin X, Y đồng đẳng kế tiếp (MX < MY và phân tử X có số nguyên tử cacbon nhiều hơn số nguyên tử nitơ) và hai ankin đồng đẳng kế tiếp (có số mol bằng nhau). Đốt cháy hoàn toàn 0,07 mol E, thu được 0,025 mol N2, 0,17 mol CO2 và 0,225 mol H2O. Phần trăm khối lượng của X trong E là
A, 28,21%.
B, 55,49%.
C, 42,32%.
D, 36,99%.
HD: ☆ Giải đốt 0,07 mol E + O2 ––to→ 0,17 mol CO2 + 0,225 mol H2O + 0,025 mol N2.
⇒ mE = mC + mH + mN = 3,19 gam.
☆ Nhận xét: ∑nH2O > ∑(nCO2 + nN2) nên amin phải no
⇒ Tương quan đốt: ∑nH2O – ∑(nCO2 + nN2) = namin – nankin = 0,03.
Lại có namin + nankin = nE = 0,07 nên giải ra namin = 0,05 mol và nankin = 0,02.
► CX > NX ≥ 1 nên CX ≥ 2.
Gọi số C trung bình của amin, ankin lần lượt là n, m thì n > 2; m > 2.
Bảo toàn C ta có: 0,05n + 0,02m = 0,17 ⇒ n < (0,17 – 0,02 × 2) ÷ 0,05 = 2,6.
Theo đó 2 < n < 2,6 cho biết hai amin đồng đẳng có 2C và 3C.
X có 2C ⇒ số NX < số CX ⇒ chỉ có 1N
⇒ X là C2H7N và Y tương ứng là C3H9N.
► Chặn: 0,05 × 2 < ∑nC amin < 0,05 × 3 ⇒ 0,02 < 0,02m < 0,07 ⇒ 1 < m < 3,5.
► Hai ankin có số mol bằng nhau, đồng đẳng kế tiếp nên giá trị m chỉ có thể là 2,5; 3,5; 4,5;.... ⇒ m = 2,5 duy nhất thoả mãn.
⇒ Giải ra hỗn hợp ankin là 0,01 mol C2H2 và 0,01 mol C3H4.
⇒ ∑nC amin = 0,12 mol ⇒ giải ra có 0,03 mol C2H7N và 0,02 mol C3H9N.
⇒ Yêu cầu %mX trong E = 0,03 × 45 ÷ 3,19 × 100% ≈ 42,32%.
⇒ mE = mC + mH + mN = 3,19 gam.
☆ Nhận xét: ∑nH2O > ∑(nCO2 + nN2) nên amin phải no
⇒ Tương quan đốt: ∑nH2O – ∑(nCO2 + nN2) = namin – nankin = 0,03.
Lại có namin + nankin = nE = 0,07 nên giải ra namin = 0,05 mol và nankin = 0,02.
► CX > NX ≥ 1 nên CX ≥ 2.
Gọi số C trung bình của amin, ankin lần lượt là n, m thì n > 2; m > 2.
Bảo toàn C ta có: 0,05n + 0,02m = 0,17 ⇒ n < (0,17 – 0,02 × 2) ÷ 0,05 = 2,6.
Theo đó 2 < n < 2,6 cho biết hai amin đồng đẳng có 2C và 3C.
X có 2C ⇒ số NX < số CX ⇒ chỉ có 1N
⇒ X là C2H7N và Y tương ứng là C3H9N.
► Chặn: 0,05 × 2 < ∑nC amin < 0,05 × 3 ⇒ 0,02 < 0,02m < 0,07 ⇒ 1 < m < 3,5.
► Hai ankin có số mol bằng nhau, đồng đẳng kế tiếp nên giá trị m chỉ có thể là 2,5; 3,5; 4,5;.... ⇒ m = 2,5 duy nhất thoả mãn.
⇒ Giải ra hỗn hợp ankin là 0,01 mol C2H2 và 0,01 mol C3H4.
⇒ ∑nC amin = 0,12 mol ⇒ giải ra có 0,03 mol C2H7N và 0,02 mol C3H9N.
⇒ Yêu cầu %mX trong E = 0,03 × 45 ÷ 3,19 × 100% ≈ 42,32%.
Câu 33 [908886]: Tiến hành thí nghiệm theo các bước sau:
Bước 1: Cho 1 ml dung dịch AgNO3 1% vào ống nghiệm sạch.
Bước 2: Thêm từ từ từng giọt dung dịch NH3, lắc đều cho đến khi kết tủa tan hết.
Bước 3: Thêm tiếp khoảng 1 ml dung dịch glucozơ 1% vào ống nghiệm, đun nóng nhẹ.
Phát biểu nào sau đây sai?
Bước 1: Cho 1 ml dung dịch AgNO3 1% vào ống nghiệm sạch.
Bước 2: Thêm từ từ từng giọt dung dịch NH3, lắc đều cho đến khi kết tủa tan hết.
Bước 3: Thêm tiếp khoảng 1 ml dung dịch glucozơ 1% vào ống nghiệm, đun nóng nhẹ.
Phát biểu nào sau đây sai?
A, Sản phẩm hữu cơ thu được sau bước 3 là sobitol.
B, Thí nghiệm trên chứng minh glucozơ có tính chất của anđehit.
C, Sau bước 3, có lớp bạc kim loại bám trên thành ống nghiệm.
D, Ở bước 3, có thể thay thế việc đun nóng nhẹ bằng cách ngâm ống nghiệm trong nước nóng.
HD: Phân tích thí nghiệm:
• Bước 1: chuẩn bị chất tham gia AgNO3.
• Bước 2: xảy ra phản ứng AgNO3 với NH3; mà ở mức độ THPT, ta hiểu đơn giản đó là chuẩn bị hoá chất AgNO3/NH3.
• Bước 3: Tiến hành phản ứng tráng bạc, tráng gương, tráng ruột phích:
glucozơ + 2AgNO3 + 3NH3 + H2O → amoni gluconat + 2Ag↓ + 2NH4NO3.
Nắm rõ ⇒ Phân tích các phát biểu đưa ra:
❌ A. sai vì sản phẩm hữu cơ là muối amoni gluconat chứ không phải sobitol (thu được bằng hiđro hoá glucozơ, xúc tác Ni).
✔️ Còn lại B, C, D đúng theo kiến thức về phản ứng tráng bạc.
• Bước 1: chuẩn bị chất tham gia AgNO3.
• Bước 2: xảy ra phản ứng AgNO3 với NH3; mà ở mức độ THPT, ta hiểu đơn giản đó là chuẩn bị hoá chất AgNO3/NH3.
• Bước 3: Tiến hành phản ứng tráng bạc, tráng gương, tráng ruột phích:
glucozơ + 2AgNO3 + 3NH3 + H2O → amoni gluconat + 2Ag↓ + 2NH4NO3.
Nắm rõ ⇒ Phân tích các phát biểu đưa ra:
❌ A. sai vì sản phẩm hữu cơ là muối amoni gluconat chứ không phải sobitol (thu được bằng hiđro hoá glucozơ, xúc tác Ni).
✔️ Còn lại B, C, D đúng theo kiến thức về phản ứng tráng bạc.
Câu 34 [136854]: Cho 7,36 gam hỗn hợp X gồm Mg và Fe vào dung dịch chứa AgNO3 và Cu(NO3)2, khi phản ứng kết thúc thu được chất rắn Y và dung dịch Z. Hòa tan hết Y bằng dung dịch H2SO4 đặc nóng (dư), thu được 5,04 lít SO2 (đktc, sản phẩm khử duy nhất). Cho NaOH dư vào Z, được kết tủa T. Nung T trong không khí đến khối lượng không đổi được 7,2 gam hỗn hợp rắn. Phần trăm khối lượng của Fe trong X là
A, 60,87%.
B, 38,04%.
C, 83,70%.
D, 49,46%.
HD: Nhận xét: 7,2 gam < 7,36 gam nghĩa sau phản ứng đầu, vẫn còn dư kim loại Fe. Sơ đồ rõ hơn:

Có ngay hệ phương trình:

||→ %mFe trong X = 0,08 × 56 ÷ 7,36 ≈ 60,87%. Chọn đáp án A. ♥.

Có ngay hệ phương trình:

||→ %mFe trong X = 0,08 × 56 ÷ 7,36 ≈ 60,87%. Chọn đáp án A. ♥.
Câu 35 [983270]: Hỗn hợp T gồm ba este mạch hở X (đơn chức), Y (hai chức), Z (ba chức) đều được tạo thành từ axit cacboxylic và ancol. Đốt cháy hoàn toàn m gam T, thu được H2O và 2,0 mol CO2. Xà phòng hóa hoàn toàn m gam T bằng dung dịch NaOH vừa đủ, thu được hỗn hợp E gồm hai ancol (có cùng số nguyên tử cacbon trong phân tử) và 53,85 gam hỗn hợp muối F. Cho E tác dụng hết với kim loại Na dư, thu được 0,4 mol H2. Đốt cháy toàn bộ F, thu được H2O, Na2CO3 và 0,4 mol CO2. Khối lượng của Y trong m gam T là
A, 5,90 gam.
B, 10,95 gam.
C, 8,85 gam.
D, 7,30 gam.
HD: Xâu chuối "chức" phản ứng: este –COO– + NaOH → –COONa (muối) + –OH (ancol).
Sau đó ancol: –OH + Na → –ONa + ½.H2↑.
⇒ Từ nH2↑ = 0,4 mol ⇒ ∑n–OH = 0,8 mol ⇒ nNaOH = 0,8 mol.
Bảo toàn nguyên tố Na ⇒ đốt muối thu được 0,4 mol Na2CO3.
Bảo toàn cacbon từ đốt este, đốt muối ⇒ đốt ancol thu được 2,0 – 0,4 – 0,4 = 1,2 mol CO2.
► "điểm đặc biệt" trong muối số C = số Na, mà Na chỉ ở trong COONa
⇒ Muối chỉ có thể là HCOONa và (COONa)2.
⇒ Giải hệ số mol có 0,25 mol HCOONa và 0,275 mol (COONa)2.
☆ Khó nhất của bài toán chính là việc xác định ancol.!
Có este đơn chức nên chắc chắc có một ancol đơn chức, có este 3 chức nên ancol còn lại là 3 chức, hoặc 2 chức (không thể 4 chức trở lên được).
• TH1: cặp ancol là đơn chức và ba chức ⇒ X là HCOOR; Y là (COOR)2 và Z là (HCOO)3R'.
⇒ nY = ngốc muối hai chức = 0,275 mol; nX + 3nZ = ∑ngốc muối đơn chức= 0,25 mol.
⇒ ∑nancol = nX + 2nY + nZ > (1/3.nX + nZ) + 2nY = 0,633
⇒ số Cancol < 1,2 ÷ 0,633 = 1,89 ⇒ số Cancol = 1→ không có cặp ancol thoả mãn.
• TH2: cặp ancol đơn chức và hai chức: ∑nOH = 0,8 mol; ∑nC = 1,2 mol.
⇒ Chặn khoảng: 1,2 ÷ 0,8 < số C < 1,2 ÷ (0,8 ÷ 2) ⇒ 1,5 < số C < 3 ⇒ số C = 2.
⇒ Giải hệ mol hai ancol tương ứng là 0,4 mol C2H5OH và 0,2 mol C2H4(OH)2.
Ghép tạo este: X chỉ có thể là HCOOC2H5; Z chỉ có thể là HCOOCH2CH2OOC–COOC2H5.
Còn Y có thể là (COOC2H5)2 hoặc (HCOO)2C2H4.
Lập hệ giải số mol X, Y, Z ứng với hai TH của Y thấy ứng với Y là (HCOO)2C2H4 không thoả mãn.
Còn với Y là (COOC2H5)2 thì thấy ngay: nZ = 0,2 mol ⇒ nX = 0,05 mol ⇒ nY = 0,075 mol.
⇝ Yêu cầu mY/T = 0,075 × 146 = 10,95 gam.
Sau đó ancol: –OH + Na → –ONa + ½.H2↑.
⇒ Từ nH2↑ = 0,4 mol ⇒ ∑n–OH = 0,8 mol ⇒ nNaOH = 0,8 mol.
Bảo toàn nguyên tố Na ⇒ đốt muối thu được 0,4 mol Na2CO3.
Bảo toàn cacbon từ đốt este, đốt muối ⇒ đốt ancol thu được 2,0 – 0,4 – 0,4 = 1,2 mol CO2.
► "điểm đặc biệt" trong muối số C = số Na, mà Na chỉ ở trong COONa
⇒ Muối chỉ có thể là HCOONa và (COONa)2.
⇒ Giải hệ số mol có 0,25 mol HCOONa và 0,275 mol (COONa)2.
☆ Khó nhất của bài toán chính là việc xác định ancol.!
Có este đơn chức nên chắc chắc có một ancol đơn chức, có este 3 chức nên ancol còn lại là 3 chức, hoặc 2 chức (không thể 4 chức trở lên được).
• TH1: cặp ancol là đơn chức và ba chức ⇒ X là HCOOR; Y là (COOR)2 và Z là (HCOO)3R'.
⇒ nY = ngốc muối hai chức = 0,275 mol; nX + 3nZ = ∑ngốc muối đơn chức= 0,25 mol.
⇒ ∑nancol = nX + 2nY + nZ > (1/3.nX + nZ) + 2nY = 0,633
⇒ số Cancol < 1,2 ÷ 0,633 = 1,89 ⇒ số Cancol = 1→ không có cặp ancol thoả mãn.
• TH2: cặp ancol đơn chức và hai chức: ∑nOH = 0,8 mol; ∑nC = 1,2 mol.
⇒ Chặn khoảng: 1,2 ÷ 0,8 < số C < 1,2 ÷ (0,8 ÷ 2) ⇒ 1,5 < số C < 3 ⇒ số C = 2.
⇒ Giải hệ mol hai ancol tương ứng là 0,4 mol C2H5OH và 0,2 mol C2H4(OH)2.
Ghép tạo este: X chỉ có thể là HCOOC2H5; Z chỉ có thể là HCOOCH2CH2OOC–COOC2H5.
Còn Y có thể là (COOC2H5)2 hoặc (HCOO)2C2H4.
Lập hệ giải số mol X, Y, Z ứng với hai TH của Y thấy ứng với Y là (HCOO)2C2H4 không thoả mãn.
Còn với Y là (COOC2H5)2 thì thấy ngay: nZ = 0,2 mol ⇒ nX = 0,05 mol ⇒ nY = 0,075 mol.
⇝ Yêu cầu mY/T = 0,075 × 146 = 10,95 gam.
Câu 36 [913166]: Cho 0,2 mol CuO tác dụng vừa đủ với dung dịch H2SO4 20% đun nóng, sau đó làm nguội dung dịch đến 10oC. Biết rằng độ tan của CuSO4 ở 10oC là 17,4 gam, khối lượng CuSO4.5H2O đã tách ra khỏi dung dịch là
A, 30,71 gam.
B, 32,50 gam.
C, 31,25 gam.
D, 29,78 gam.
HD: Phản ứng: CuO + H2SO4 → CuSO4 + H2O.
Vừa đủ nên nH2SO4 = nCuO = 0,2 mol.
⇒ mdung dịch H2SO4 20% = 0,2 × 98 ÷ 0,2 = 98 gam.
Lại có mCuSO4 = 0,2 × 160 = 32 gam
và mdung dịch sau phản ứng = 0,2 × 80 + 98 = 114 gam.
Tương ứng gồm 32 gam chất tan CuSO4 và 82 gam nước.
Ở 10oC, cứ 100 gam H2O hoà tan tối đa 17,4 gam CuSO4 (1).
Giả sử có a mol CuSO4.5H2O tách ra thì dung dịch lúc này:
gồm (32 – 160a) gam CuSO4 và (82 – 90a) gam H2O (2).
Từ (1) và (2) có tỉ lệ: 17,4 × (82 – 90a) = 100 × (32 – 160a) ⇒ a ≈ 0,12285 mol
⇒ Yêu cầu mCuSO4.5H2O tách ra = 250a ≈ 30,71 gam.
Vừa đủ nên nH2SO4 = nCuO = 0,2 mol.
⇒ mdung dịch H2SO4 20% = 0,2 × 98 ÷ 0,2 = 98 gam.
Lại có mCuSO4 = 0,2 × 160 = 32 gam
và mdung dịch sau phản ứng = 0,2 × 80 + 98 = 114 gam.
Tương ứng gồm 32 gam chất tan CuSO4 và 82 gam nước.
Ở 10oC, cứ 100 gam H2O hoà tan tối đa 17,4 gam CuSO4 (1).
Giả sử có a mol CuSO4.5H2O tách ra thì dung dịch lúc này:
gồm (32 – 160a) gam CuSO4 và (82 – 90a) gam H2O (2).
Từ (1) và (2) có tỉ lệ: 17,4 × (82 – 90a) = 100 × (32 – 160a) ⇒ a ≈ 0,12285 mol
⇒ Yêu cầu mCuSO4.5H2O tách ra = 250a ≈ 30,71 gam.
Câu 37 [983271]: Cho các phát biểu sau:
(a) Trong thành phần của xăng sinh học E5 có etanol.
(b) Mỡ lợn có chứa chất béo bão hòa (phân tử có các gốc hiđrocacbon no).
(c) Thành phần chính của sợi bông, sợi đay là tinh bột.
(d) Khi làm đậu phụ từ sữa đậu nành có xảy ra sự đông tụ protein.
(e) Vải lụa tơ tằm sẽ nhanh hỏng nếu ngâm, giặt trong xà phòng có tính kiềm.
Số phát biểu đúng là
(a) Trong thành phần của xăng sinh học E5 có etanol.
(b) Mỡ lợn có chứa chất béo bão hòa (phân tử có các gốc hiđrocacbon no).
(c) Thành phần chính của sợi bông, sợi đay là tinh bột.
(d) Khi làm đậu phụ từ sữa đậu nành có xảy ra sự đông tụ protein.
(e) Vải lụa tơ tằm sẽ nhanh hỏng nếu ngâm, giặt trong xà phòng có tính kiềm.
Số phát biểu đúng là
A, 4.
B, 2.
C, 3.
D, 5.
HD: Phân tích các phát biểu:
✔️ (a) đúng. xăng sinh học gồm 95% RON 92 + 5% Etanol nguyên chất.
✔️ (b) đúng. Mỡ lợn rắn ⇒ các gốc chất béo sẽ là no (bão hoà).
❌ (c) sai vì sợi bông, đay có thành phần chính là xenlulozơ chứ không phải tinh bột.
✔️ (d) đúng. Quá trình sản xuất sẽ đun nóng và sử dụng môi trường chua (axit) để làm đông tụ sữa đậu nành ⇝ tạo thành đậu phụ.
✔️ (e) đúng. Vải lụa tơ tằm bản chất là fibroin (protein) chứa liên kết CO–NH kém bền, sẽ thuỷ phân trong môi trường kiềm ⇝ dẫn đến nhanh hỏng.
⇝ có 4/5 phát biểu đúng ⇝ Chọn đáp án A. ♥
✔️ (a) đúng. xăng sinh học gồm 95% RON 92 + 5% Etanol nguyên chất.
✔️ (b) đúng. Mỡ lợn rắn ⇒ các gốc chất béo sẽ là no (bão hoà).
❌ (c) sai vì sợi bông, đay có thành phần chính là xenlulozơ chứ không phải tinh bột.
✔️ (d) đúng. Quá trình sản xuất sẽ đun nóng và sử dụng môi trường chua (axit) để làm đông tụ sữa đậu nành ⇝ tạo thành đậu phụ.
✔️ (e) đúng. Vải lụa tơ tằm bản chất là fibroin (protein) chứa liên kết CO–NH kém bền, sẽ thuỷ phân trong môi trường kiềm ⇝ dẫn đến nhanh hỏng.
⇝ có 4/5 phát biểu đúng ⇝ Chọn đáp án A. ♥
Câu 38 [982010]: Cho sơ đồ phản ứng sau (xảy ra theo đúng tỉ lệ mol):
(1) E 2X + 2CO2;
2X + 2CO2;
(2) X + O2 Y + H2O.
Y + H2O.
(3) F + 2H2O X + Y + T;
X + Y + T;
Biết E là monosaccarit có nhiều trong quả nho chín; F là hợp chất hữu cơ có công thức phân tử là C7H12O4. Cho các phát biểu nào sau:
(a) Chất Y có nhiệt độ sôi cao hơn chất X.
(b) Hợp chất F có 3 công thức cấu tạo phù hợp.
(c) Chất Y và chất T có cùng công thức đơn giản nhất.
(d) Có thể điều chế trực tiếp được chất Y từ ancol metylic.
(e) Chất T có mạch cacbon không phân nhánh.
Số phát biểu đúng là
(1) E
 2X + 2CO2;
2X + 2CO2;
(2) X + O2
 Y + H2O.
Y + H2O.
(3) F + 2H2O
 X + Y + T;
X + Y + T;
Biết E là monosaccarit có nhiều trong quả nho chín; F là hợp chất hữu cơ có công thức phân tử là C7H12O4. Cho các phát biểu nào sau:
(a) Chất Y có nhiệt độ sôi cao hơn chất X.
(b) Hợp chất F có 3 công thức cấu tạo phù hợp.
(c) Chất Y và chất T có cùng công thức đơn giản nhất.
(d) Có thể điều chế trực tiếp được chất Y từ ancol metylic.
(e) Chất T có mạch cacbon không phân nhánh.
Số phát biểu đúng là
A, 2.
B, 3.
C, 1.
D, 4.
HD: E là monosaccarit có nhiều trong quả nho chín → E là glucozơ: CH2OH[CHOH]4CHO.
Các phản ứng xảy ra khi thực hiện sơ đồ chuyển hoá:
(1) Lên men rượu: C6H12O6 –––lên men, 30oC–→ 2C2H5OH (X) + 2CO2↑.
(2) Lên men giấm: C2H5OH + O2 –––xt, to–→ CH3COOH + H2O.
(3) C7H12O4 + 2H2O ⇄ C2H5OH + CH3COOH + T.
⇒ Bảo toàn nguyên tố ⇒ Công thức phân tử của T là C3H6O3.
⇒ Tương ứng cấu tạo: HOC2H4COOH ⇝ E dạng este nối: CH3COOC2H4COOC2H5.
Phân tích các phát biểu:
✔️ (a) đúng vì axit CH3COOH có nhiệt độ sôi cao hơn ancol C2H5OH (cùng số C).
❌ (b) sai vì F chỉ có hai cấu tạo: CH3COOCH2CH2COOC2H5 và CH3COOCH(CH3)COOC2H5.
✔️ (c) đúng vì Y: CH3COOH và T: HOC2H4COOH có cùng CTĐGN là CH2O.
✔️ (d) đúng, pp hiện đại sản xuất: CH3OH + CO –––xt, to–→ CH3COOH.
✔️ (e) đúng vì T có hai cấu tạo: HOCH2CH2COOH và HOCH(CH3)COOH đều không phân nhánh.
⇒ có 4/5 phát biểu đúng ⇝ Chọn đáp án D. ♠
Các phản ứng xảy ra khi thực hiện sơ đồ chuyển hoá:
(1) Lên men rượu: C6H12O6 –––lên men, 30oC–→ 2C2H5OH (X) + 2CO2↑.
(2) Lên men giấm: C2H5OH + O2 –––xt, to–→ CH3COOH + H2O.
(3) C7H12O4 + 2H2O ⇄ C2H5OH + CH3COOH + T.
⇒ Bảo toàn nguyên tố ⇒ Công thức phân tử của T là C3H6O3.
⇒ Tương ứng cấu tạo: HOC2H4COOH ⇝ E dạng este nối: CH3COOC2H4COOC2H5.
Phân tích các phát biểu:
✔️ (a) đúng vì axit CH3COOH có nhiệt độ sôi cao hơn ancol C2H5OH (cùng số C).
❌ (b) sai vì F chỉ có hai cấu tạo: CH3COOCH2CH2COOC2H5 và CH3COOCH(CH3)COOC2H5.
✔️ (c) đúng vì Y: CH3COOH và T: HOC2H4COOH có cùng CTĐGN là CH2O.
✔️ (d) đúng, pp hiện đại sản xuất: CH3OH + CO –––xt, to–→ CH3COOH.
✔️ (e) đúng vì T có hai cấu tạo: HOCH2CH2COOH và HOCH(CH3)COOH đều không phân nhánh.
⇒ có 4/5 phát biểu đúng ⇝ Chọn đáp án D. ♠
Câu 39 [679733]: Hòa tan hết m gam hỗn hợp X gồm Fe, FeO, Fe2O3 và Fe3O4 vào dung dịch HCl dư, thu được a mol H2 và dung dịch chứa 31,19 gam hỗn hợp muối. Mặt khác, hòa tan hoàn toàn m gam X trong dung dịch chứa 0,55 mol H2SO4 (đặc) đun nóng, thu được dung dịch Y và 0,14 mol SO2 (sản phẩm khử duy nhất của S+6). Cho 400 ml dung dịch NaOH 1M vào Y, sau khi phản ứng kết thúc thu được 10,7 gam một chất kết tủa. Giá trị của a là
A, 0,04.
B, 0,06.
C, 0,05.
D, 0,03.
HD: Nhận xét nhanh các bài tập nhỏ:
• 31,19 gam muối là FeCl2 và FeCl3 ⇒ tổng mol nguyên tố Fe > 31,19 ÷ 162,5 > 0,192.
• 10,7 gam một kết tủa là Fe(OH)2 hay Fe(OH)3? Nhưng nếu toàn bộ Fe đi hết về kết tủa này thì như phân tích trên, số mol phải lớn hơn 0,192 ⇒ ít nhất 0,192 × 90 > 10,7 gam.
Có nghĩa là 0,4 mol NaOH vào Y sẽ phản ứng với axit H2SO4 dư trước, sau đó mới tác dụng với một phần muối Fe tạo kết tủa ⇒ là 0,1 mol Fe(OH)3 ⇒ Y còn dư 0,1 mol H+.
⇒ nH2SO4 phản ứng = 0,55 – 0,1 ÷ 2 = 0,5 mol ⇒ nFe2(SO4)3 = (0,5 – 0,14) ÷ 3 = 0,12 mol.
Bảo toàn electron trực tiếp: 3nnguyên tố Fe = 2nO trong oxit + 2nSO2 ⇒ nO trong X = 0,22 mol.
☆ Quan sát: X + HCl → 31,19 gam (Fe; Cl) + H2 + H2O.
mmuối = 31,19 = mFe + mCl = 0,24 × 56 + mCl ⇒ nCl = 0,5 mol ⇒ nHCl = 0,5 mol.
Lại có nO trong X = nH2O ⇒ nH2O = 0,22 mol
⇒ a = nH2 = (0,5 ÷ 2 – 0,22) = 0,03 mol theo bảo toàn H.
• 31,19 gam muối là FeCl2 và FeCl3 ⇒ tổng mol nguyên tố Fe > 31,19 ÷ 162,5 > 0,192.
• 10,7 gam một kết tủa là Fe(OH)2 hay Fe(OH)3? Nhưng nếu toàn bộ Fe đi hết về kết tủa này thì như phân tích trên, số mol phải lớn hơn 0,192 ⇒ ít nhất 0,192 × 90 > 10,7 gam.
Có nghĩa là 0,4 mol NaOH vào Y sẽ phản ứng với axit H2SO4 dư trước, sau đó mới tác dụng với một phần muối Fe tạo kết tủa ⇒ là 0,1 mol Fe(OH)3 ⇒ Y còn dư 0,1 mol H+.
⇒ nH2SO4 phản ứng = 0,55 – 0,1 ÷ 2 = 0,5 mol ⇒ nFe2(SO4)3 = (0,5 – 0,14) ÷ 3 = 0,12 mol.
Bảo toàn electron trực tiếp: 3nnguyên tố Fe = 2nO trong oxit + 2nSO2 ⇒ nO trong X = 0,22 mol.
☆ Quan sát: X + HCl → 31,19 gam (Fe; Cl) + H2 + H2O.
mmuối = 31,19 = mFe + mCl = 0,24 × 56 + mCl ⇒ nCl = 0,5 mol ⇒ nHCl = 0,5 mol.
Lại có nO trong X = nH2O ⇒ nH2O = 0,22 mol
⇒ a = nH2 = (0,5 ÷ 2 – 0,22) = 0,03 mol theo bảo toàn H.
Câu 40 [982252]: Cho các phát biểu sau:
(a) Ở nhiệt độ cao, kim loại Al khử được Fe2O3.
(b) Điện phân nóng chảy NaCl, thu được khí Cl2 ở anot.
(c) Thành phần chính của supephotphat kép là Ca(H2PO4)2.
(d) Đốt sợi dây thép trong khí Cl2 xảy ra ăn mòn điện hóa học.
Số phát biểu đúng là
(a) Ở nhiệt độ cao, kim loại Al khử được Fe2O3.
(b) Điện phân nóng chảy NaCl, thu được khí Cl2 ở anot.
(c) Thành phần chính của supephotphat kép là Ca(H2PO4)2.
(d) Đốt sợi dây thép trong khí Cl2 xảy ra ăn mòn điện hóa học.
Số phát biểu đúng là
A, 4.
B, 1.
C, 3.
D, 2.
HD: Phân tích các phát biểu:
✔️ (a) đúng, phản ứng nhiệt nhôm: 2Al + Fe2O3 ––to→ Al2O3 + 2Fe.
✔️ (b) đúng, xảy ra: 2NaCl + H2O ––đpdd→ 2NaOH + H2 (catot) + Cl2 (anot).
✔️ (c) đúng, kép là trải qua 2 quá trình nên supephotphat kép chỉ có Ca(H2PO4)2 thôi.
❌ (d) sai vì thiếu điều kiện tiếp xúc dung dịch chất điện li nên không xảy ra ăn mòn điện hoá.
⇝ có 3/4 phát biểu đúng ⇝ Chọn đáp án C. ♣
✔️ (a) đúng, phản ứng nhiệt nhôm: 2Al + Fe2O3 ––to→ Al2O3 + 2Fe.
✔️ (b) đúng, xảy ra: 2NaCl + H2O ––đpdd→ 2NaOH + H2 (catot) + Cl2 (anot).
✔️ (c) đúng, kép là trải qua 2 quá trình nên supephotphat kép chỉ có Ca(H2PO4)2 thôi.
❌ (d) sai vì thiếu điều kiện tiếp xúc dung dịch chất điện li nên không xảy ra ăn mòn điện hoá.
⇝ có 3/4 phát biểu đúng ⇝ Chọn đáp án C. ♣