Đáp án
1D
2C
3B
4A
5A
6C
7C
8C
9A
10A
11C
12B
13B
14C
15A
16B
17D
18D
19D
20C
21D
22A
23C
24A
25C
26C
27C
28D
29C
30D
31D
32C
33D
34C
35A
36D
37C
38A
39C
40D
Đáp án Đề minh họa số 3 thi Tốt Nghiệp Trung học Phổ Thông 2024 môn Hóa học
Câu 1 [982279]: Chất nào sau đây là este?
A, CH3COOH.
B, CH3COONa.
C, C3H5(OH)3.
D, CH3COOCH3.
HD: Phân tích các đáp án:
| Công thức | A. CH3COOH. | B. CH3COONa. | C. C3H5(OH)3. | D. CH3COOCH3. |
| Loại hợp chất | axit cacboxylic | muối | ancol đa chức | este (✔️) |
Câu 2 [911510]: Tên gọi của hợp chất hữu cơ có cấu tạo CH3-CHO là
A, anđehit fomic.
B, axit axetic.
C, anđehit axetic.
D, etanol.
HD: Phân tích các đáp án:
| Hợp chất | anđehit fomic | axit axetic | anđehit axetic | etanol |
| Cấu tạo | HCHO | CH3COOH | CH3CHO | CH3CH2OH |
| ❌ | ❌ | ✔️ | ❌ |
Câu 3 [982500]: Chất nào sau đây khi cho vào nước không làm thay đổi pH của nước?
A, NH4Cl.
B, KCl.
C, Na2CO3.
D, HCl.
HD: Phân tích các đáp án: (Chú ý pH của nước = 7).
| Hợp chất | NH4Cl | KCl | Na2CO3 | HCl |
| pH dung dịch | < 7 | = 7 | > 7 | < 7 |
| ❌ | ✔️ | ❌ | ❌ |
Câu 4 [679795]: Nước chứa nhiều ion nào sau đây được gọi là nước cứng?
A, Ca2+, Mg2+.
B, Na+, K+.
C, Na+, H+.
D, H+, K+.
HD: Nước cứng là nước có chứa nhiều ion Ca2+ và Mg2+.


Câu 5 [906752]: Canxi hiđroxit được sử dụng rộng rãi trong nhiều ngành công nghiệp. Công thức của canxi hiđroxit là
A, Ca(OH)2.
B, CaO.
C, CaSO4.
D, CaCO3.
HD: Phân tích các đáp án:
| Công thức | A. Ca(OH)2. | B. CaO. | C. CaSO4. | D. CaCO3. |
| Tên gọi | canxi hiđroxit | canxi oxit | canxi sunfat | canxi cacbonat |
| Tên gọi khác | vôi tôi | vôi sống | thạch cao | đá vôi |
Câu 6 [982260]: Khi đốt rơm rạ trên các cánh đồng sau những vụ thu hoạch lúa sinh ra nhiều khói bụi, trong đó có khí X. Khí X nặng hơn không khí và gây hiệu ứng nhà kính. Khí X là
A, N2.
B, O2.
C, CO2.
D, CO.
HD: Đốt rơm rạ xảy ra phản ứng: C + O2 –––to–→ CO2.
Nếu C dư thì C + CO2 –––to–→ 2CO.
► khí X nặng hơn không khí (M = 29) và gây nên hiệu ứng nhà kính nên X là CO2 (M = 44).
Nếu C dư thì C + CO2 –––to–→ 2CO.
► khí X nặng hơn không khí (M = 29) và gây nên hiệu ứng nhà kính nên X là CO2 (M = 44).
Câu 7 [983259]: Cho Fe2O3 phản ứng với dung dịch H2SO4 loãng dư, tạo ra muối nào sau đây?
A, FeSO4.
B, FeS.
C, Fe2(SO4)3.
D, FeSO3.
HD: Phản ứng hoá học xảy ra:
Fe2O3 + 3H2SO4 → Fe2(SO4)3 + 3H2O.
Fe2O3 + 3H2SO4 → Fe2(SO4)3 + 3H2O.
Câu 8 [911547]: Kim loại nào sau đây có độ cứng cao nhất?
A, Ag.
B, Al.
C, Cr.
D, Fe.
HD: Crom là kim loại cứng nhất. Nếu coi độ cứng của kim cương là 10 điểm thì crom là 9.
Câu 9 [973596]: Dung dịch K2Cr2O7 có màu gì?
A, Màu da cam.
B, Màu đỏ thẫm.
C, Màu lục thẫm.
D, Màu vàng.
HD: dung dịch K2Cr2O7: kali đicromat có màu da cam

⇝ Chọn đáp án A. ♥

⇝ Chọn đáp án A. ♥
Câu 10 [679306]: Kim loại nào sau đây có tính khử yếu nhất?
A, Ag.
B, Al.
C, Fe.
D, Cu.
Thứ tự dãy điện hóa các kim loại: Al > Fe > (H) > Cu > Ag.
Câu 11 [60324]: Khi tác dụng với dung dịch HCl, chất nào sau đây thể hiện tính khử?
A, NaAlO2.
B, Al2O3.
C, Al.
D, Al(OH)3.
Giải: Loại A, B và D vì chỉ xảy ra phản ứng trao đổi ⇒ chọn C.
Câu 12 [973594]: Số liên kết peptit trong phân tử Ala-Gly-Ala-Gly là
A, 1.
B, 3.
C, 4.
D, 2.
HD: Trong peptit Ala-Gly-Ala-Gly thì gạch nối – chính là liên kết peptit.
Đếm: 1 - 2 - 3 ⇒ có 3 liên kết peptit ⇝ Chọn đáp án B. ♦
Đếm: 1 - 2 - 3 ⇒ có 3 liên kết peptit ⇝ Chọn đáp án B. ♦
Câu 13 [906750]: Số nguyên tử hiđro trong phân tử fructozơ là
A, 10.
B, 12.
C, 22.
D, 6.
HD: Cấu tạo dạng mạch hở của fructozơ cần nhớ:

⇒ Số nguyên tử hiđro trong phân tử fructozơ là 12.

⇒ Số nguyên tử hiđro trong phân tử fructozơ là 12.
Câu 14 [14904]: Trong lò cao, quá trình khử oxit sắt thành sắt được thực hiện bằng phương pháp
A, thủy luyện.
B, điện phân.
C, nhiệt luyện.
D, nhiệt nhôm.
![608697[LG].png](https://m.moon.vn/Images/Teachers/rongden_167/ProS2018/TAPIII/608697[LG].png)
Câu 15 [312001]: Diêm tiêu kali được dùng chế tạo thuốc nổ đen (làm mìn phá đá), đồng thời được dùng làm phân bón, cung cấp nguyên tố nitơ và kali cho cây trồng. Công thức hóa học của diêm tiêu kali là
A, KNO3.
B, K2CO3.
C, KCl.
D, K2SO4.
HD: "Nhất đồng thán, bán đồng sinh, lục đồng diêm"
Nhất đồng thán (một phần than C); bán đồng sinh (nửa phần S);
lục đồng diêm (6 phần diêm tiêu KNO3) gần đúng
với công thức chế tạo thuốc nổ đen: 15%C : 10%S : 75%KNO3.
☆ Yêu cầu: Công thức hóa học của diêm tiêu kali chính là KNO3. ❒
Nhất đồng thán (một phần than C); bán đồng sinh (nửa phần S);
lục đồng diêm (6 phần diêm tiêu KNO3) gần đúng
với công thức chế tạo thuốc nổ đen: 15%C : 10%S : 75%KNO3.
☆ Yêu cầu: Công thức hóa học của diêm tiêu kali chính là KNO3. ❒
Câu 16 [312100]: Trong các chất dưới đây, chất nào là amin bậc hai?
A, H2N[CH2]6NH2.
B, CH3NHCH3.
C, C6H5NH2.
D, CH3CH(CH3)NH2.
HD: Bài học bậc amin:

⇝ tương ứng CH3NHCH3: đimetylamin là amin bậc hai. ❒

⇝ tương ứng CH3NHCH3: đimetylamin là amin bậc hai. ❒
Câu 17 [906786]: Thủy phân tristearin ((C17H35COO)3C3H5) trong dung dịch NaOH, thu được muối có công thức là
A, CH3COONa.
B, C17H33COONa.
C, C2H5COONa.
D, C17H35COONa.
Phản ứng: (C17H35COO)3C3H5 + 3NaOH → 3C17H35COONa + C3H5(OH)3.
Câu 18 [20445]: Polime nào sau đây chứa nguyên tố nitơ?
A, Sợi bông.
B, Poli(vinyl clorua).
C, Polietilen.
D, Tơ nilon-6.
HD: ☆ Phân tích thành phần nguyên tố của các polime:
☒ A. Sợi bông: thành phần xenlulozơ ⇝ chứa các nguyên tố C, H, O.
☒ B. Poli(vinyl clorua) là chuối mắt xích CH2–CHCl ⇝ chứa các nguyên tố C, H, Cl.
☒ C. Polietilen là chuỗi các mắt xích CH2–CH2 ⇝ chứa các nguyên tố C và H.
☑ D. Tơ nilon-6 là chuỗi các mắt xích HN[CH2]5CO ⇝ chứa các nguyên tố C, H, O, N. ❒
☒ A. Sợi bông: thành phần xenlulozơ ⇝ chứa các nguyên tố C, H, O.
☒ B. Poli(vinyl clorua) là chuối mắt xích CH2–CHCl ⇝ chứa các nguyên tố C, H, Cl.
☒ C. Polietilen là chuỗi các mắt xích CH2–CH2 ⇝ chứa các nguyên tố C và H.
☑ D. Tơ nilon-6 là chuỗi các mắt xích HN[CH2]5CO ⇝ chứa các nguyên tố C, H, O, N. ❒
Câu 19 [60083]: Chất nào sau đây tác dụng với dung dịch BaCl2 sinh ra kết tủa?
A, KHCO3.
B, KOH.
C, NaNO3.
D, Na2SO4.
HD: ❌ KHCO3; KOH và NaNO3 đều không có phản ứng với BaCl2.
✔️ Na2SO4 + BaCl2 → BaSO4↓ + 2NaCl ⇝ Chọn đáp án D. ♠
✔️ Na2SO4 + BaCl2 → BaSO4↓ + 2NaCl ⇝ Chọn đáp án D. ♠
Câu 20 [57798]: Kim loại nào sau đây không phản ứng với dung dịch H2SO4 loãng?
A, Fe.
B, Zn.
C, Cu.
D, Mg.
Giải: + Vì Cu đứng sau H trong dãy hoạt động hóa học.
⇒ Cu không tác dụng với H2SO4 loãng ⇒ Chọn C
⇒ Cu không tác dụng với H2SO4 loãng ⇒ Chọn C
Câu 21 [60593]: Cho Fe3O4 tác dụng với lượng dư dung dịch H2SO4 loãng, thu được dung dịch X. Dung dịch X không tác dụng với dung dịch
A, Cu(NO3)2.
B, BaCl2.
C, K2Cr2O7.
D, NaBr.
HD: ☆ Phản ứng: Fe3O4 + 4H2SO4 → FeSO4 + Fe2(SO4)3 + 4H2O.
Lưu ý, H2SO4 dùng dư nên dung dịch X gồm FeSO4; Fe2(SO4)3 và H2SO4.
► Các dung dịch tác dụng được với dung dịch X là:
☑ A. 3Fe2+ + H+ + NO3– → 3Fe3+ + NO↑ + 2H2O.
☑ B. Ba2+ + SO42– → BaSO4↓.
☑ C. 6FeSO4 + K2Cr2O7 + 7H2SO4 → 3Fe2(SO4)3 + K2SO4 + Cr2(SO4)3 + 7H2O.
Chỉ có dung dịch NaBr không tác dụng được với dung dịch X. ❒
Lưu ý, H2SO4 dùng dư nên dung dịch X gồm FeSO4; Fe2(SO4)3 và H2SO4.
► Các dung dịch tác dụng được với dung dịch X là:
☑ A. 3Fe2+ + H+ + NO3– → 3Fe3+ + NO↑ + 2H2O.
☑ B. Ba2+ + SO42– → BaSO4↓.
☑ C. 6FeSO4 + K2Cr2O7 + 7H2SO4 → 3Fe2(SO4)3 + K2SO4 + Cr2(SO4)3 + 7H2O.
Chỉ có dung dịch NaBr không tác dụng được với dung dịch X. ❒
Câu 22 [8486]: Thủy phân hoàn toàn 8,8 gam etyl axetat trong 100ml dung dịch KOH 1,5M, đun nóng. Sau phản ứng hoàn toàn, cô cạn dung dịch thu được m gam chất rắn khan. Giá trị của m là
A, 12,6.
B, 10,2.
C, 9,8.
D, 17,2.
Giải: + Ta có nCH3COOC2H5 = 0,1 mol < nKOH = 0,15 mol ⇒ nC2H5OH = 0,1 mol
+ BTKL ta có mChất rắn = 8,8 + 0,15×56 - 0,1×46 = 12,6 gam ⇒ Chọn A
+ BTKL ta có mChất rắn = 8,8 + 0,15×56 - 0,1×46 = 12,6 gam ⇒ Chọn A
Câu 23 [973603]: Phát biểu nào sau đây đúng?
A, Phân tử xenlulozơ đuợc cấu tạo từ các gốc fructozơ.
B, Fructozơ không có phản ứng tráng bạc.
C, Amilopectin có cấu trúc mạch phân nhánh.
D, Saccarozơ không tham gia phản ứng thủy phân.
HD: Phân tích các đáp án:
❌ A. sai vì phân tử xenlulozơ đuợc cấu tạo từ các gốc β-glucozơ.
❌ B. sai vì fructozơ có phản ứng tráng gương theo sơ đồ sau:

✔️ C. đúng, amilozơ không phân nhánh, còn amilopectin có cấu trúc mạch phân nhánh.
❌ D. sai vì saccarozơ có tham gia phản ứng thủy phân:
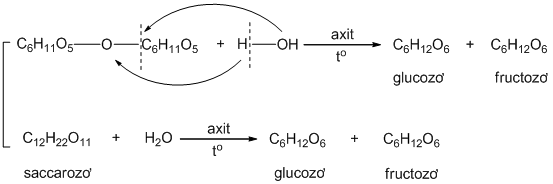
❌ A. sai vì phân tử xenlulozơ đuợc cấu tạo từ các gốc β-glucozơ.
❌ B. sai vì fructozơ có phản ứng tráng gương theo sơ đồ sau:
✔️ C. đúng, amilozơ không phân nhánh, còn amilopectin có cấu trúc mạch phân nhánh.
❌ D. sai vì saccarozơ có tham gia phản ứng thủy phân:

Câu 24 [981940]: Có bao nhiêu polime được điều chế bằng phản ứng trùng hợp trong các polime: polietilen, polibutađien, poliacrilonitrin, poliisopren?
A, 4.
B, 1.
C, 3.
D, 2.
HD: Xem lại bài học về phân loại phương pháp tổng hợp, điều chế polime:
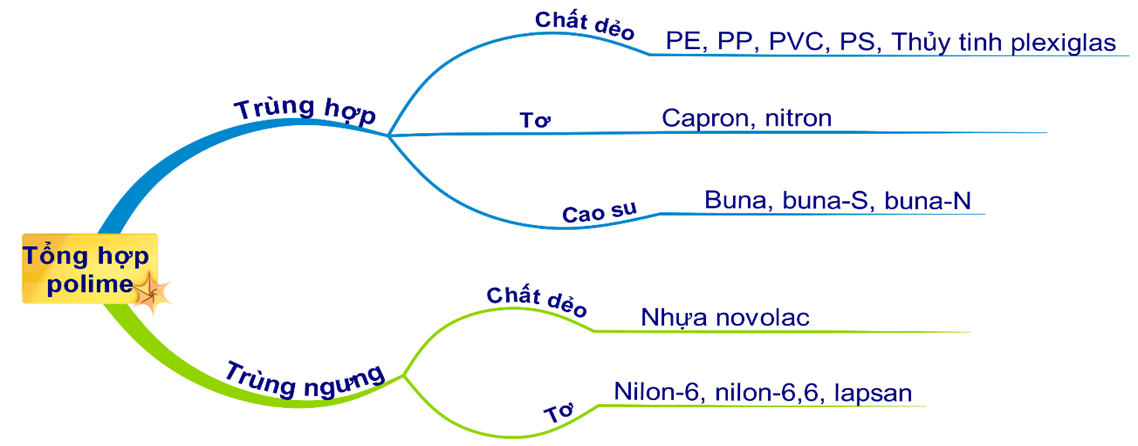
⇒ Tất cả các polime trong dãy: polietilen, polibutađien, poliacrilonitrin, poliisopren đều được tổng hợp từ phản ứng trùng hợp monome tương ứng.

⇒ Tất cả các polime trong dãy: polietilen, polibutađien, poliacrilonitrin, poliisopren đều được tổng hợp từ phản ứng trùng hợp monome tương ứng.
Câu 25 [343778]: Cho glixerol phản ứng với axit cacboxylic đơn chức X thu được hợp chất hữu cơ E có phân tử khối bằng 148. Số đồng phân cấu tạo thỏa mãn E là
A, 2.
B, 3.
C, 4.
D, 6.
Công thức axit cacboxylic: RCOOH.
Đặt công thức của E là: (RCOO)n(HO)3-nC3H5.
Ta có: (R+44)×n + 17×(3-n) + 41 = 148.
+) với n = 1 → R = 29 (C2H5)
→ E: (C2H5COO)(HO)2C3H5 → Có 2 công thức cấu tạo.
+) với n = 2 → R = 1 (H)
→ E: (HCOO)2(HO)C3H5 → Có 2 công thức cấu tạo.
Tổng có 4 công thức cấu tạo phù hợp.
Đặt công thức của E là: (RCOO)n(HO)3-nC3H5.
Ta có: (R+44)×n + 17×(3-n) + 41 = 148.
+) với n = 1 → R = 29 (C2H5)
→ E: (C2H5COO)(HO)2C3H5 → Có 2 công thức cấu tạo.
+) với n = 2 → R = 1 (H)
→ E: (HCOO)2(HO)C3H5 → Có 2 công thức cấu tạo.
Tổng có 4 công thức cấu tạo phù hợp.
Câu 26 [679853]: Cho m gam bột Zn tác dụng hoàn toàn với dung dịch CuSO4 dư, thu được 9,6 gam kim loại Cu. Giá trị của m là
A, 6,50.
B, 3,25.
C, 9,75.
D, 13,00.
HD: Phản ứng: Zn + CuSO4 → ZnSO4 + Cu.
Giả thiết: nCu = 9,6 ÷ 64 = 0,15 mol ⇒ nZn = 0,15 mol
⇒ Yêu cầu: m = mZn = 0,15 × 65 = 9,75 gam.
Giả thiết: nCu = 9,6 ÷ 64 = 0,15 mol ⇒ nZn = 0,15 mol
⇒ Yêu cầu: m = mZn = 0,15 × 65 = 9,75 gam.
Câu 27 [679556]: Đun nóng 100 ml dung dịch glucozơ a (mol/l) với lượng dư dung dịch AgNO3 trong NH3. Sau khi phản ứng xảy ra hoàn toàn, thu được 21,6 gam Ag. Giá trị của a là
A, 0,1.
B, 0,5.
C, 1,0.
D, 0,2.
HD: Tỉ lệ phản ứng tráng bạc:

Giả thiết nAg = 0,2 mol ⇒ nglucozơ = 0,1 mol.
⇒ Yêu cầu a = CM (glucozơ) = 0,1 ÷ 0,1 = 1M ⇝ Chọn đáp án C. ♣

Giả thiết nAg = 0,2 mol ⇒ nglucozơ = 0,1 mol.
⇒ Yêu cầu a = CM (glucozơ) = 0,1 ÷ 0,1 = 1M ⇝ Chọn đáp án C. ♣
Câu 28 [15239]: Đốt cháy hoàn toàn m gam amin X (no, đơn chức, mạch hở), thu được H2O, 1,792 lít khí CO2 (đktc) và 0,28 gam khí N2. Giá trị của m là
A, 1,24.
B, 1,18.
C, 0,90.
D, 1,46.
HD: amin X no, đơn chức, mạch hở → có CTPT dạng CnH2n + 3N.
♦ giải đốt m gam X: CnH2n + 3N + O2 –––to–→ 0,08 mol CO2 + 0,01 mol N2.
⇒ nX = 2nN2 = 0,02 mol ⇒ n = số C = ∑nCO2 ÷ nX = 0,08 ÷ 0,02 = 4.
⇒ m = mX= 0,02 × 73 = 1,46 gam. Chọn đáp án D. ♠.
♦ giải đốt m gam X: CnH2n + 3N + O2 –––to–→ 0,08 mol CO2 + 0,01 mol N2.
⇒ nX = 2nN2 = 0,02 mol ⇒ n = số C = ∑nCO2 ÷ nX = 0,08 ÷ 0,02 = 4.
⇒ m = mX= 0,02 × 73 = 1,46 gam. Chọn đáp án D. ♠.
Câu 29 [352143]: Phát biểu nào sau đây đúng?
A, Điện phân nóng chảy NaCl có màng ngăn thu được khí H2 ở catot.
B, Đun nóng thạch cao sống đến khối lượng không đổi thu được CaO và CO2.
C, Vôi tôi có công thức Ca(OH)2 là chất rắn màu trắng, ít tan trong nước.
D, Al2O3, Al(OH)3 và Na2CO3 là những hợp chất có tính lưỡng tính.
❌ A Sai vì điện phân nóng chảy NaCl. Cực âm (catot) sẽ thu được kim loại Na theo qua trình:
Na+ + 1e → Na.
❌ B Sai vì nung thạch cao sống CaSO4.2H2O đến khối lượng không đổi thu được CaSO4.
✔️ C Đúng.
❌ D. Sai vì Na2CO3 không phải chất có tính lưỡng tính.
Na+ + 1e → Na.
❌ B Sai vì nung thạch cao sống CaSO4.2H2O đến khối lượng không đổi thu được CaSO4.
✔️ C Đúng.
❌ D. Sai vì Na2CO3 không phải chất có tính lưỡng tính.
Câu 30 [911652]: [TN 2017 – L2]: Khử hoàn toàn một lượng Fe3O4 bằng H2 dư, thu được chất rắn X và m gam H2O. Hòa tan hết X trong dung dịch HCl dư, thu được 1,008 lít khí H2 (đktc). Giá trị của m là
A, 0,72.
B, 1,35.
C, 0,81.
D, 1,08.
HD: Khử hoàn toàn oxit sắt: Fe3O4 + 4H2 ––to→ 3Fe + 4H2O.
Tiếp theo: Fe + 2HCl → FeCl2 + H2↑.
Giả thiết nH2 = 0,045 mol ⇒ nFe = 0,045 mol.
Bảo toàn nguyên tố Fe ta có nFe3O4 = 0,045 ÷ 3 = 0,015 mol.
⇒ nH2O = 0,015 × 4 = 0,06 mol (theo tỉ lệ phản ứng).
Vậy yêu cầu m = mH2O = 0,06 × 18 = 1,08 gam ⇝ Chọn đáp án D. ♠
Tiếp theo: Fe + 2HCl → FeCl2 + H2↑.
Giả thiết nH2 = 0,045 mol ⇒ nFe = 0,045 mol.
Bảo toàn nguyên tố Fe ta có nFe3O4 = 0,045 ÷ 3 = 0,015 mol.
⇒ nH2O = 0,015 × 4 = 0,06 mol (theo tỉ lệ phản ứng).
Vậy yêu cầu m = mH2O = 0,06 × 18 = 1,08 gam ⇝ Chọn đáp án D. ♠
Câu 31 [52097]: Cho các phát biểu sau:
(a) Muối NaHCO3 được dùng làm thuốc chữa đau dạ dày do thừa axit.
(b) Ở nhiệt độ thường, tất cả các kim loại kiềm đều tác dụng được với nước.
(c) Công thức hóa học của thạch cao khan là CaSO4.
(d) Các chất Al(OH)3, NaHCO3, Al2O3 đều lưỡng tính.
(e) Có thể dùng dung dịch NaOH để làm mềm nước cứng tạm thời.
Số phát biểu đúng là
(a) Muối NaHCO3 được dùng làm thuốc chữa đau dạ dày do thừa axit.
(b) Ở nhiệt độ thường, tất cả các kim loại kiềm đều tác dụng được với nước.
(c) Công thức hóa học của thạch cao khan là CaSO4.
(d) Các chất Al(OH)3, NaHCO3, Al2O3 đều lưỡng tính.
(e) Có thể dùng dung dịch NaOH để làm mềm nước cứng tạm thời.
Số phát biểu đúng là
A, 2.
B, 3.
C, 4.
D, 5.
Giải: (a) Đúng vì: NaHCO3 + HCl → NaCl + CO2 + H2O
⇒ làm giảm nồng độ HCl trong dạ dày.
(b) Đúng vì có tính khử mạnh.
(c) Đúng, thạch cao sống là CaSO4.2H2O và thạch cao nung là CaSO4.H2O.
(d) Đúng.
(e) Đúng vì nước cứng tạo thời chứa anion HCO3– nên:
HCO3– + OH– → CO32– + H2O
⇒ ion CO32– tạo ↓ với Ca2+ và Mg2+ ⇒ nước mềm.
||⇒ tất cả đều đúng ⇒ chọn D.
⇒ làm giảm nồng độ HCl trong dạ dày.
(b) Đúng vì có tính khử mạnh.
(c) Đúng, thạch cao sống là CaSO4.2H2O và thạch cao nung là CaSO4.H2O.
(d) Đúng.
(e) Đúng vì nước cứng tạo thời chứa anion HCO3– nên:
HCO3– + OH– → CO32– + H2O
⇒ ion CO32– tạo ↓ với Ca2+ và Mg2+ ⇒ nước mềm.
||⇒ tất cả đều đúng ⇒ chọn D.
Câu 32 [184834]: Thực hiện thí nghiệm theo các bước sau:
Bước 1: Cho một đinh sắt đã cạo sạch gỉ vào ống nghiệm.
Bước 2: Thêm tiếp vào ống nghiệm 4-5 ml dung dịch H2SO4 loãng.
Bước 3: Lấy đinh sắt ra rồi nhỏ dần từng giọt dung dịch K2Cr2O7 trong H2SO4 loãng vào ống nghiệm và lắc đều.
Cho các phát biểu sau:
(a) Trong bước 2, không xuất hiện bọt khí.
(b) Trong bước 2, kim loại sắt bị khử thành hợp chất sắt(III).
(c) Trong bước 3, hợp chất sắt(II) bị oxi hóa thành hợp chất sắt(III).
(d) Trong bước 3, hợp chất crom(VI) bị khử thành hợp chất crom(III).
(đ) Ở bước 2, nếu thay dung dịch H2SO4 loãng bằng dung dịch HCl thì có xuất hiện bọt khí.
Số phát biểu đúng là
Bước 1: Cho một đinh sắt đã cạo sạch gỉ vào ống nghiệm.
Bước 2: Thêm tiếp vào ống nghiệm 4-5 ml dung dịch H2SO4 loãng.
Bước 3: Lấy đinh sắt ra rồi nhỏ dần từng giọt dung dịch K2Cr2O7 trong H2SO4 loãng vào ống nghiệm và lắc đều.
Cho các phát biểu sau:
(a) Trong bước 2, không xuất hiện bọt khí.
(b) Trong bước 2, kim loại sắt bị khử thành hợp chất sắt(III).
(c) Trong bước 3, hợp chất sắt(II) bị oxi hóa thành hợp chất sắt(III).
(d) Trong bước 3, hợp chất crom(VI) bị khử thành hợp chất crom(III).
(đ) Ở bước 2, nếu thay dung dịch H2SO4 loãng bằng dung dịch HCl thì có xuất hiện bọt khí.
Số phát biểu đúng là
A, 2.
B, 4.
C, 3.
D, 1.
Bước 1: Làm sạch đinh sắt.
Bước 2: Thêm H2SO4 vào ống nghiệm
Fe + H2SO4 → FeSO4 + H2.
Bước 3: Thêm K2Cr2O7 vào ống nghiệm
6FeSO4 + K2Cr2O7 + 7H2SO4 → 3Fe2(SO4)3 + Cr2(SO4)3 + K2SO4 + 7H2O.
❌ (a) Sai vì có xuất hiện bọt khí H2.
❌ (b) Sai vì phản ứng tạo thành FeSO4 có hóa trị II.
✔️ (c) Đúng vì Fe trong FeSO4 là Fe(II), trong Fe2(SO4)3 là Fe(III).
✔️ (d) Đúng vì Cr trong K2Cr2O7 là Cr(VI) còn trong Cr2(SO4)3 là Cr(III).
✔️ (đ) Đúng vì Fe cũng phản ứng với HCl tạo khí.
Bước 2: Thêm H2SO4 vào ống nghiệm
Fe + H2SO4 → FeSO4 + H2.
Bước 3: Thêm K2Cr2O7 vào ống nghiệm
6FeSO4 + K2Cr2O7 + 7H2SO4 → 3Fe2(SO4)3 + Cr2(SO4)3 + K2SO4 + 7H2O.
❌ (a) Sai vì có xuất hiện bọt khí H2.
❌ (b) Sai vì phản ứng tạo thành FeSO4 có hóa trị II.
✔️ (c) Đúng vì Fe trong FeSO4 là Fe(II), trong Fe2(SO4)3 là Fe(III).
✔️ (d) Đúng vì Cr trong K2Cr2O7 là Cr(VI) còn trong Cr2(SO4)3 là Cr(III).
✔️ (đ) Đúng vì Fe cũng phản ứng với HCl tạo khí.
Fe + 2HCl → FeCl2 + H2.
Câu 33 [906773]: Nhiệt phân hoàn toàn 41,58 gam muối khan X (là muối ở dạng ngậm nước), thu được hỗn hợp Y (gồm khí và hơi) và 11,34 gam chất rắn Z. Hấp thụ toàn bộ Y vào nước thu được dung dịch T. Cho 280 ml dung dịch NaOH 1M vào T, thu được dung dịch chỉ chứa một muối duy nhất, khối lượng muối là 23,8 gam. Phần trăm khối lượng nguyên tố oxi trong X là
A, 48,48%.
B, 53,87%.
C, 59,26%.
D, 64,65%.
HD: 0,28 mol NaOH → một muối duy nhất Na? nặng 23,8 gam.
Thực hiện: 23,8 ÷ 0,28 = 85 = 23 + 62 ⇒ cho biết muối là NaNO3.
Theo đó Y gồm hơi H2O và khí NO2 + O2 với đúng tỉ lệ 4 : 1 để sau đó:
4NO2 + O2 + 2H2O → 4HNO3.
NaOH + HNO3 → NaNO3 + H2O.
► Phân tích: muối dạng M(NO3)n ⇒ oxit dạng M2On: khối lượng 11,34 gam.
Mà nO trong oxit = ½nNO3 = 0,14 mol ⇒ mM = 9,1.
Ta có M ÷ n = 9,1 ÷ (0,14 × 2) = 65/2 cho biết M là kim loại kẽm (Zn); hóa trị II.
⇒ 41,58 gam X dạng Zn(NO3)2.nH2O với số mol 0,28 ⇒ n = 6.
Vậy, X là Zn(NO3)2.6H2O ⇝ yêu cầu %mO trong X ≈ 64,65%.
Thực hiện: 23,8 ÷ 0,28 = 85 = 23 + 62 ⇒ cho biết muối là NaNO3.
Theo đó Y gồm hơi H2O và khí NO2 + O2 với đúng tỉ lệ 4 : 1 để sau đó:
4NO2 + O2 + 2H2O → 4HNO3.
NaOH + HNO3 → NaNO3 + H2O.
► Phân tích: muối dạng M(NO3)n ⇒ oxit dạng M2On: khối lượng 11,34 gam.
Mà nO trong oxit = ½nNO3 = 0,14 mol ⇒ mM = 9,1.
Ta có M ÷ n = 9,1 ÷ (0,14 × 2) = 65/2 cho biết M là kim loại kẽm (Zn); hóa trị II.
⇒ 41,58 gam X dạng Zn(NO3)2.nH2O với số mol 0,28 ⇒ n = 6.
Vậy, X là Zn(NO3)2.6H2O ⇝ yêu cầu %mO trong X ≈ 64,65%.
Câu 34 [136683]: Tại một nhà máy hóa chất, hơi nước được dẫn đi qua cacbon nóng đỏ, thu được hỗn hợp khí than ướt X gồm CO, CO2 và H2. Dẫn V lít X (đktc) vào nước vôi trong dư, thu được 2 gam kết tủa. Cho V lít X (đktc) tác dụng với 6,4 gam bột CuO (dư, nung nóng), thu được chất rắn Y. Cho toàn bộ Y vào dung dịch AgNO3 dư, thu được 14,56 gam chất rắn. Biết các phản ứng xảy ra hoàn toàn. Phần trăm thể tích khí CO trong X là
A, 25,0%.
B, 20,0%.
C, 12,5%.
D, 17,5%.
![635585[LG].png](https://m.moon.vn/Images/Teachers/rongden_167/2019/VDC2018/635585[LG].png)
Câu 35 [352144]: Hỗn hợp E gồm hai hiđrocacbon mạch hở X, Y với MX < MY < 70. Cho 0,1 mol E, có khối lượng 5,75 gam, vào lượng dư dung dịch AgNO3 trong NH3 thu được 19,125 gam hỗn hợp kết tủa. Biết các phản ứng xảy ra hoàn toàn. Phần trăm khối lượng của Y trong E là
A, 88,70%.
B, 50,26%.
C, 65,30%.
D, 78,52%.
* Áp dụng ĐLBTKL và tỉ lệ của AgNO3; NH3 và NH4NO3 đều bằng nhau.
→
Ta có:
→ Trong E chứa 2 ankin: Đặt ankin phản ứng với AgNO3 theo tỉ lệ 1 : 1 là B và ankin phản ứng với AgNO3 theo tỉ lệ 1 : 2 là A.
* Ta có E gồm: A (a mol) và B (b mol).
a + b = 0,1. → a = 0,025.
2a + b = 0,125. → b = 0,075.
Ta có: ME = 5,75 : 0,1 = 57,5.
Suy ra trong E có chứa 1 ankin có M < 57,5.
+) TH1: HC≡CH (0,025 mol) và R-C≡CH (0,075 mol).
mE = 0,025 × 26 + 0,075×(R+25) = 5,75 → R = 43 (C3H7).
%mY = 0,075 × 68 : 5,75 × 100 = 88,70%.
+) TH2: A (0,025 mol) và CH3-C≡CH (0,075 mol).
mE = 0,025 × MA + 0,075×40 = 5,75 → MA = 110 > 70. → Loại.
+) TH3: A (0,025 mol) và C2H5-C≡CH (0,075 mol).
mE = 0,025 × MA + 0,075×54 = 5,75 → MA = 68.
→ Loại vì không có ankin nào M = 68 và phản ứng được với AgNO3 theo tỉ lệ 1 : 2.
→ Chọn đáp án A.
→

Ta có:

→ Trong E chứa 2 ankin: Đặt ankin phản ứng với AgNO3 theo tỉ lệ 1 : 1 là B và ankin phản ứng với AgNO3 theo tỉ lệ 1 : 2 là A.
* Ta có E gồm: A (a mol) và B (b mol).
a + b = 0,1. → a = 0,025.
2a + b = 0,125. → b = 0,075.
Ta có: ME = 5,75 : 0,1 = 57,5.
Suy ra trong E có chứa 1 ankin có M < 57,5.
+) TH1: HC≡CH (0,025 mol) và R-C≡CH (0,075 mol).
mE = 0,025 × 26 + 0,075×(R+25) = 5,75 → R = 43 (C3H7).
%mY = 0,075 × 68 : 5,75 × 100 = 88,70%.
+) TH2: A (0,025 mol) và CH3-C≡CH (0,075 mol).
mE = 0,025 × MA + 0,075×40 = 5,75 → MA = 110 > 70. → Loại.
+) TH3: A (0,025 mol) và C2H5-C≡CH (0,075 mol).
mE = 0,025 × MA + 0,075×54 = 5,75 → MA = 68.
→ Loại vì không có ankin nào M = 68 và phản ứng được với AgNO3 theo tỉ lệ 1 : 2.
→ Chọn đáp án A.
Câu 36 [352145]: Từ hai hợp chất hữu cơ no, mạch hở E và F (đều chỉ chứa nhóm chức este) thực hiện sơ đồ các phản ứng sau theo đúng tỉ lệ mol:
E + NaOH → Y + Z; F + 2NaOH → 2Y + T + X.
Biết khi phân tích phổ khối lượng (phổ MS) cho kết quả chất F có phân tử khối bằng 118. Chất X và Z có cùng số nguyên tử cacbon.
Phát biểu nào sau đây đúng?
E + NaOH → Y + Z; F + 2NaOH → 2Y + T + X.
Biết khi phân tích phổ khối lượng (phổ MS) cho kết quả chất F có phân tử khối bằng 118. Chất X và Z có cùng số nguyên tử cacbon.
Phát biểu nào sau đây đúng?
A, Công thức phân tử của chất E là C4H8O2.
B, Dung dịch chất Y có nồng độ 3-5% dùng gia vị nấu ăn.
C, Chất X thuộc dãy đồng đẳng ancol no, hai chức, mạch hở.
D, Chất Z có thể được điều chế trực tiếp từ chất X.
Vì E và F chỉ chứa chức este (COO)
Mặt khác: F phản ứng NaOH theo tỉ lệ 1:2 → F có 2 nhóm COO → F phải có ít nhất 4O.
Phân tử khối F đều là 118.
Vậy CTPT của E và F là C4H6O4 (k = 2).
F tạo 4 sản phẩm nên CTCT của F phải là:
(HCOO)2-CH-CH3 (F) + 2NaOH → 2HCOONa (Y) + CH3CHO (X) + H2O (T).
E phản ứng với NaOH tạo ra Y và Z (Z có 2C vì Z và X có cùng số C).
HCOOC2H5 (E) + NaOH → HCOONa (Y) + C2H5OH (Z) .
❌ A. Sai vì E (HCOOC2H5) có công thức phân tử C3H6O2.
❌ B. Sai vì Y là dung dịch HCOONa 3-5% không dùng làm gia vị nấu ăn.
❌ C. Sai vì X (CH3CHO) là andehit, không phải ancol.
✔️ D. Đúng vì Z (C2H5OH) có thể điều chế trực tiếp từ X (CH3CHO) khi phản ứng khử với H2, xt Ni.
→ Chọn đáp án D.
Mặt khác: F phản ứng NaOH theo tỉ lệ 1:2 → F có 2 nhóm COO → F phải có ít nhất 4O.
Phân tử khối F đều là 118.
Vậy CTPT của E và F là C4H6O4 (k = 2).
F tạo 4 sản phẩm nên CTCT của F phải là:
(HCOO)2-CH-CH3 (F) + 2NaOH → 2HCOONa (Y) + CH3CHO (X) + H2O (T).
E phản ứng với NaOH tạo ra Y và Z (Z có 2C vì Z và X có cùng số C).
HCOOC2H5 (E) + NaOH → HCOONa (Y) + C2H5OH (Z) .
❌ A. Sai vì E (HCOOC2H5) có công thức phân tử C3H6O2.
❌ B. Sai vì Y là dung dịch HCOONa 3-5% không dùng làm gia vị nấu ăn.
❌ C. Sai vì X (CH3CHO) là andehit, không phải ancol.
✔️ D. Đúng vì Z (C2H5OH) có thể điều chế trực tiếp từ X (CH3CHO) khi phản ứng khử với H2, xt Ni.
→ Chọn đáp án D.
Câu 37 [679401]: Este X hai chức, mạch hở, tạo bởi một ancol no với hai axit cacboxylic no, đơn chức. Este Y ba chức, mạch hở, tạo bởi glixerol với một axit cacboxylic không no, đơn chức (phân tử có hai liên kết pi). Đốt cháy hoàn toàn m gam hỗn hợp E gồm X và Y cần vừa đủ 0,5 mol O2 thu được 0,45 mol CO2. Mặt khác, thủy phân hoàn toàn 0,16 mol E cần vừa đủ 210 ml dung dịch NaOH 2M, thu được hai ancol (có cùng số nguyên tử cacbon trong phân tử) và hỗn hợp ba muối, trong đó tổng khối lượng muối của hai axit no là a gam. Giá trị của a là
A, 13,20.
B, 20,60.
C, 12,36.
D, 10,68.
HD: 0,16 mol E + vừa đủ 0,42 mol NaOH ⇒ giải ra nX = 0,06 mol và nY = 0,1 mol.
☆ Combo giả thiết chữ đầy đủ ⇝ tìm ra CTPT dạng tương ứng:
• Este X hai chức, no, mạch hở ⇝ X dạng: CnH2n – 2O4
• Este Y ba chức, mạch hở, axit tạo Y có 2π ⇒ tổng Y có 6π ⇝ Y dạng CmH2m – 10O6.
Giải đốt (3a mol X + 5a mol Y) + 0,5 mol O2 → 0,45 mol CO2 + b mol H2O.
• Bảo toàn nguyên tố O: (3a × 4 + 5a × 6) + 0,5 × 2 = 0,45 × 2 + b.
• Tương quan đốt: ∑nCO2 – ∑nH2O = nX + 5nY ⇒ 0,45 – b = 3a + 5 × 5a.
⇒ Giải hệ các phương trình ta có: a = 0,005 và b = 0,31.
Đặc trưng nghiệm nguyên: 0,015n + 0,025m = ∑nCO2 = 0,45 ⇒ 3n + 5m = 90.
Do n ≥ 6; m ≥ 12 ⇒ cặp nghiệm duy nhất thoả mãn: n = 10; m = 12.
Thấy ngay Y là (CH2=CHCOO)3C3H5 và X dạng (C2,5H6COO)2C3H6.
⇒ a gam hai muối no là (0,06 × 2) mol C2,5H6COONa ⇒ a = 12,36 gam.
☆ Combo giả thiết chữ đầy đủ ⇝ tìm ra CTPT dạng tương ứng:
• Este X hai chức, no, mạch hở ⇝ X dạng: CnH2n – 2O4
• Este Y ba chức, mạch hở, axit tạo Y có 2π ⇒ tổng Y có 6π ⇝ Y dạng CmH2m – 10O6.
Giải đốt (3a mol X + 5a mol Y) + 0,5 mol O2 → 0,45 mol CO2 + b mol H2O.
• Bảo toàn nguyên tố O: (3a × 4 + 5a × 6) + 0,5 × 2 = 0,45 × 2 + b.
• Tương quan đốt: ∑nCO2 – ∑nH2O = nX + 5nY ⇒ 0,45 – b = 3a + 5 × 5a.
⇒ Giải hệ các phương trình ta có: a = 0,005 và b = 0,31.
Đặc trưng nghiệm nguyên: 0,015n + 0,025m = ∑nCO2 = 0,45 ⇒ 3n + 5m = 90.
Do n ≥ 6; m ≥ 12 ⇒ cặp nghiệm duy nhất thoả mãn: n = 10; m = 12.
Thấy ngay Y là (CH2=CHCOO)3C3H5 và X dạng (C2,5H6COO)2C3H6.
⇒ a gam hai muối no là (0,06 × 2) mol C2,5H6COONa ⇒ a = 12,36 gam.
Câu 38 [24382]: Cho các phát biểu sau:
(a) Tất cả các peptit đều có phản ứng màu biure.
(b) Muối phenylamoni clorua không tan trong nước.
(c) Ở điều kiện thường, metylamin và đimetylamin là những chất khí.
(d) Trong phân tử peptit mạch hở Gly-Ala-Gly có 4 nguyên tử oxi.
(e) Ở điều kiện thường, amino axit là những chất lỏng.
Số phát biểu đúng là
(a) Tất cả các peptit đều có phản ứng màu biure.
(b) Muối phenylamoni clorua không tan trong nước.
(c) Ở điều kiện thường, metylamin và đimetylamin là những chất khí.
(d) Trong phân tử peptit mạch hở Gly-Ala-Gly có 4 nguyên tử oxi.
(e) Ở điều kiện thường, amino axit là những chất lỏng.
Số phát biểu đúng là
A, 2.
B, 4.
C, 5.
D, 3.
HD: Xem xét, phân tích các phát biểu:
(a) sai. TH của đipeptit không có phản ứng màu biure.
(b) sai, muối C6H5NH3Cl tan trong nước (ứng dụng: dùng HCl để rửa anilin).
(c) đúng. 4 amin khí ở điều kiện thường gồm CH3NH2; C2H5NH2 (CH3)2NH và (CH3)3N.
(d) CTTQ của peptit tạo từ các α-amino axit no, mạch hở, chứa 1-NH2; 1-COOH
là CnH2n + 2 – mNmOm + 1. Ở đây m = 3 nên số O là m + 1 = 4.
(e) sai. tính chất vật lí của amino axit. ở điều kiện thường là các chất rắn dạng tinh thể.
||→ chỉ có 2/5 phát biểu đúng. Chọn đáp án A. ♥.
(a) sai. TH của đipeptit không có phản ứng màu biure.
(b) sai, muối C6H5NH3Cl tan trong nước (ứng dụng: dùng HCl để rửa anilin).
(c) đúng. 4 amin khí ở điều kiện thường gồm CH3NH2; C2H5NH2 (CH3)2NH và (CH3)3N.
(d) CTTQ của peptit tạo từ các α-amino axit no, mạch hở, chứa 1-NH2; 1-COOH
là CnH2n + 2 – mNmOm + 1. Ở đây m = 3 nên số O là m + 1 = 4.
(e) sai. tính chất vật lí của amino axit. ở điều kiện thường là các chất rắn dạng tinh thể.
||→ chỉ có 2/5 phát biểu đúng. Chọn đáp án A. ♥.
Câu 39 [679462]: Dẫn từ từ đến dư khí CO2 vào dung dịch Ba(OH)2. Sự phụ thuộc của khối lượng kết tủa (y gam) vào thể tích khí CO2 tham gia phản ứng (x lít) được biểu diễn bằng đồ thị bên. Giá trị của m là


A, 19,70.
B, 39,40.
C, 9,85.
D, 29,55.
HD: Đồ thị biểu diễn quá trình phản ứng:

Phân tích:
• Đoạn OA biểu diễn tỉ lệ phản ứng: 1CO2 + 1Ba(OH)2 → 1BaCO3↓ + 1H2O.
• Đoạn AB biểu diễn tỉ lệ phản ứng: 1CO2 + 1BaCO3 → 1Ba(HCO3)2.
Giả sử: m gam kết tủa tương ứng y mol BaCO3; a lít khí tương ứng x mol (quan sát đồ thị).
Theo đó, ta có: OH = HF → x = 3y || KB = KE = 2y → 2AI = OB = OK + KB.
⇥ có phương trình: 8y = (x + 0,15) + 2y ⇒ 6y = x + 0,15 ⇒ y = 0,05 và x = 0,15.

Phân tích:
• Đoạn OA biểu diễn tỉ lệ phản ứng: 1CO2 + 1Ba(OH)2 → 1BaCO3↓ + 1H2O.
• Đoạn AB biểu diễn tỉ lệ phản ứng: 1CO2 + 1BaCO3 → 1Ba(HCO3)2.
Giả sử: m gam kết tủa tương ứng y mol BaCO3; a lít khí tương ứng x mol (quan sát đồ thị).
Theo đó, ta có: OH = HF → x = 3y || KB = KE = 2y → 2AI = OB = OK + KB.
⇥ có phương trình: 8y = (x + 0,15) + 2y ⇒ 6y = x + 0,15 ⇒ y = 0,05 và x = 0,15.
Vậy, giá trị của m = 197y = 9,85 gam. ⇝ Chọn đáp án C. ♣
Câu 40 [184842]: Poli(etylen terephtalat) (viết tắt là PET) là một polime được điều chế từ axit terephtalic và etylen glicol. PET được sử dụng để sản xuất tơ, chai đựng nước uống, hộp đựng thực phẩm. Để thuận lợi cho việc nhận biết, sử dụng và tái chế thì các đồ nhựa làm từ vật liệu chứa PET thường được in kí hiệu như hình bên.

Cho các phát biểu sau :
(a) PET thuộc loại polieste.
(b) Tơ được chế tạo từ PET thuộc loại tơ tổng hợp.
(c) Trong một mắt xích PET, phần trăm khối lượng cacbon là 62,5%.
(d) Phản ứng tổng hợp PET từ axit terephtalic và etylen glicol thuộc loại phản ứng trùng hợp.
(đ) Trong dung dịch, etylen glicol phản ứng với Cu(OH)2 tạo dung dịch màu xanh lam.
Số phát biểu đúng là

Cho các phát biểu sau :
(a) PET thuộc loại polieste.
(b) Tơ được chế tạo từ PET thuộc loại tơ tổng hợp.
(c) Trong một mắt xích PET, phần trăm khối lượng cacbon là 62,5%.
(d) Phản ứng tổng hợp PET từ axit terephtalic và etylen glicol thuộc loại phản ứng trùng hợp.
(đ) Trong dung dịch, etylen glicol phản ứng với Cu(OH)2 tạo dung dịch màu xanh lam.
Số phát biểu đúng là
A, 2.
B, 3.
C, 5.
D, 4.
PET có công thức: (OC-C6H4-COO-CH2-CH2-O)n
✔️(a) Đúng vì PET có chứa gốc chức este COO.
✔️(b) Đúng
✔️(c) Đúng vì

❌(d) Sai vì phản ứng tổng hợp tách H2O nên thuộc phản ứng trùng ngưng.
✔️(đ) Đúng vì etylen glicol có 2 nhóm OH liền kề nên có thể hòa tan được kết tủa Cu(OH)2 tạo dung dịch xanh lam.
→ Đáp án D đúng.
✔️(a) Đúng vì PET có chứa gốc chức este COO.
✔️(b) Đúng
✔️(c) Đúng vì

❌(d) Sai vì phản ứng tổng hợp tách H2O nên thuộc phản ứng trùng ngưng.
✔️(đ) Đúng vì etylen glicol có 2 nhóm OH liền kề nên có thể hòa tan được kết tủa Cu(OH)2 tạo dung dịch xanh lam.
→ Đáp án D đúng.