Đáp án
1B
2D
3A
4A
5D
6B
7B
8D
9B
10B
11A
12D
13B
14B
15A
16A
17B
18A
19B
20B
21A
22B
23A
24C
25A
26A
27C
28B
29A
30D
31B
32A
33C
34D
35C
36A
37D
38D
39C
40C
Đáp án Đề minh họa số 30 thi Tốt Nghiệp Trung học Phổ Thông 2024 môn Hóa học
Câu 1 [60332]: Oxit nhôm không phản ứng với chất nào sau đây?
A, HCl.
B, H2.
C, Ca(OH)2.
D, NaOH.
HD: ► H2 chỉ khử được oxit của kim loại trung bình và yếu từ Zn trở xuống ⇝ H2 không khử được Al2O3. Còn lại:
✔️ A. 6HCl + Al2O3 → 2AlCl3 + 3H2O.
✔️ C. Ca(OH)2 + Al2O3 → Ca(AlO2)2 + H2O.
✔️ D. 2NaOH + Al2O3 → NaAlO2 + H2O.
✔️ A. 6HCl + Al2O3 → 2AlCl3 + 3H2O.
✔️ C. Ca(OH)2 + Al2O3 → Ca(AlO2)2 + H2O.
✔️ D. 2NaOH + Al2O3 → NaAlO2 + H2O.
Câu 2 [60885]: Đồng (II) hiđroxit có màu
A, lục thẫm.
B, lục xám.
C, trắng.
D, xanh.
HD: Đồng (II) hiđroxit Cu(OH)2 có màu xanh.


Câu 3 [255669]: Kim loại nào sau đây thuộc nhóm IIIA trong bảng tuần hoàn?
A, Al.
B, Fe.
C, Ba.
D, Na.
HD: Nhôm (Al) thuộc nhóm IIIA trong bảng tuần hoàn.
⇝ Chọn đáp án A. ♥
⇝ Chọn đáp án A. ♥
Câu 4 [981934]: Chất nào sau đây tác dụng với NaHCO3 sinh ra khí CO2?
A, HCOOH.
B, CH3CHO.
C, CH3OH.
D, HCOONa.
HD: ► trong chương trình, chỉ có chức axit cacboxylic COOH mới có phản ứng với NaHCO3 tạo khí CO2↑:
Theo đó: HCOOH + NaHCO3 → HCOONa + CO2↑ + H2O.
⇝ Chọn đáp án A. ♥
Theo đó: HCOOH + NaHCO3 → HCOONa + CO2↑ + H2O.
⇝ Chọn đáp án A. ♥
Câu 5 [61712]: Sođa khan (không ngậm nước) là hóa chất quan trọng trong sản xuất thủy tinh, bột giặt, phẩm nhuộm, giấy, sợi. Công thức hóa học của sođa khan là
A, NaCl.
B, Na2SO4.
C, NaNO3.
D, Na2CO3.
HD: Tên gọi các chất tương ứng với công thức:
◈ NaCl: natri clorua ⇝ muối ăn.
◈ Na2SO4: natri sunfat.
◈ NaNO3: natri nitrat.
◈ Na2CO3: natri cacbonat ⇝ sođa khan.
☆ Hóa chất quan trọng hàng đầu trong nhiều ngành sản xuất là H2SO4; sau đó là Na2CO3. ❒
◈ NaCl: natri clorua ⇝ muối ăn.
◈ Na2SO4: natri sunfat.
◈ NaNO3: natri nitrat.
◈ Na2CO3: natri cacbonat ⇝ sođa khan.
☆ Hóa chất quan trọng hàng đầu trong nhiều ngành sản xuất là H2SO4; sau đó là Na2CO3. ❒
Câu 6 [58608]: Cho 4 ion: Al3+, Zn2+, Cu2+, Pt2+. Ion có tính oxi hóa mạnh hơn Pb2+ là
A, Cu2+.
B, Cu2+, Pt2+.
C, Al3+.
D, Al3+, Zn2+.
HD:
Thứ tự tính oxi hóa tăng dần: Al3+, Zn2+, Pb2+, Cu2+, Pt2+.
Thứ tự tính oxi hóa tăng dần: Al3+, Zn2+, Pb2+, Cu2+, Pt2+.
Câu 7 [982268]: Trong mắt xích của polime nào sau đây có nguyên tử clo?
A, Polietilen.
B, Poli(vinyl clorua).
C, Poliacrilonitrin.
D, Polibutađien.
HD: Phân tích các đáp án:
| Polime | Polietilen | Poli(vinyl clorua) | Poliacrilonitrin | Polibutađien |
| Mắt xích | –CH2–CH2– | –CH2–CH(Cl)– | –CH2–CH(CN)– | –CH2–CH=CH–CH2– |
| Thành phần | C, H (❌) | C, H, Cl (✔️) | C, H, N (❌) | C, H (❌) |
Câu 8 [18435]: Hợp chất nào sau đây không có tính chất lưỡng tính?
A, Amoni axetat.
B, Axit glutamic.
C, Alanin.
D, Anilin.
HD: Tất cả các amino axit có tính lưỡng tính nên alanin: H2NCH(CH3)COOH và axit glutamic H2NC3H5(COOH)2 thoả mãn.
► Amoni axetat: CH3COONH4 là muối giữa axit yếu và bazơ yếu nên cũng là một hợp chất lưỡng tính, trong dung dịch CH3COONH4 → CH3COO– + NH4+, trong đó:
• CH3COO– + H2O ⇄ CH3COOH + OH– thể hiện tính bazơ:
• NH4+ + H2O ⇄ NH3 + H3O+ thể hiện tính axit.
► Chỉ có anilin: C6H5NH2 là một amin có tính bazơ rất yếu, không phải là hợp chất lưỡng tính ⇝ Chọn đáp án D. ♠
► Amoni axetat: CH3COONH4 là muối giữa axit yếu và bazơ yếu nên cũng là một hợp chất lưỡng tính, trong dung dịch CH3COONH4 → CH3COO– + NH4+, trong đó:
• CH3COO– + H2O ⇄ CH3COOH + OH– thể hiện tính bazơ:
• NH4+ + H2O ⇄ NH3 + H3O+ thể hiện tính axit.
► Chỉ có anilin: C6H5NH2 là một amin có tính bazơ rất yếu, không phải là hợp chất lưỡng tính ⇝ Chọn đáp án D. ♠
Câu 9 [908854]: Chất nào sau đây là muối axit?
A, NaCl.
B, NaH2PO4.
C, NaOH.
D, NaNO3.
HD: Phân loại muối:
• Muối trung hòa là muối mà anion gốc axit không còn hiđro có khả năng phân li ra H+ (hiđro có tính axit). Ví dụ: NaCl; (CH3COO)2Ca; (NH4)2SO4;...
• Muối axit là muối vẫn còn hiđro có khả năng phân li ra H+. Ví dụ: NaHCO3; KHSO4; NaH2PO4; K2HPO4;...
⇒ NaCl; NaNO3 là các muối trung hoà; NaOH là bazơ, chỉ có NaH2PO4 là muối axit ⇝ Chọn đáp án B. ♦
• Muối trung hòa là muối mà anion gốc axit không còn hiđro có khả năng phân li ra H+ (hiđro có tính axit). Ví dụ: NaCl; (CH3COO)2Ca; (NH4)2SO4;...
• Muối axit là muối vẫn còn hiđro có khả năng phân li ra H+. Ví dụ: NaHCO3; KHSO4; NaH2PO4; K2HPO4;...
⇒ NaCl; NaNO3 là các muối trung hoà; NaOH là bazơ, chỉ có NaH2PO4 là muối axit ⇝ Chọn đáp án B. ♦
Câu 10 [908858]: Số nguyên tử hiđro trong phân tử axit stearic là
A, 33.
B, 36.
C, 34.
D, 31.
HD: Hệ thống 4 axit béo quan trọng cần nhớ:
• C15H31COOH: axit panmitic.
• C17H35COOH: axit stearic.
• C17H33COOH: axit oleic.
• C17H31COOH: axit linoleic.
⇝ Tương ứng số nguyên tử hiđro trong phân tử axit stearic là 36.
• C15H31COOH: axit panmitic.
• C17H35COOH: axit stearic.
• C17H33COOH: axit oleic.
• C17H31COOH: axit linoleic.
⇝ Tương ứng số nguyên tử hiđro trong phân tử axit stearic là 36.
Câu 11 [312029]: Hợp chất CF2Cl2 thuộc nhóm freon được sử dụng là chất làm lạnh trong các máy lạnh, tủ lạnh. Tuy nhiên, đối với môi trường, freon là tác nhân chính gây
A, phá hủy tầng ozon.
B, mưa axit.
C, hiệu ứng nhà kính.
D, hiện tượng El-Nino.
HD: ☆ Các hợp chất dạng CFC dưới tác dụng của tia cực tím UV
⇝ phân rã quang liên kết C-Cl: CCl2F2 –––UV–→ Cl• + CClF2
clo nguyên tử Cl•, hoạt động rất khác với clo phân tử (Cl2).
gốc Cl• tồn tại lâu dài ở tầng thượng khí quyển,
nơi nó xúc tác việc chuyển đổi ozon thành O2.
⇝ mỗi gốc Cl• phá hủy hàng ngìn, chục ngìn O3 → gây thủng tầng ozon. ❒
⇝ phân rã quang liên kết C-Cl: CCl2F2 –––UV–→ Cl• + CClF2
clo nguyên tử Cl•, hoạt động rất khác với clo phân tử (Cl2).
gốc Cl• tồn tại lâu dài ở tầng thượng khí quyển,
nơi nó xúc tác việc chuyển đổi ozon thành O2.
⇝ mỗi gốc Cl• phá hủy hàng ngìn, chục ngìn O3 → gây thủng tầng ozon. ❒
Câu 12 [225753]: Ở nhiệt độ thường, kim loại Al tan hoàn toàn trong lượng dư dung dịch nào sau đây?
A, NaCl.
B, Na2SO4.
C, NaNO3.
D, H2SO4 loãng.
HD: ❌ Al không phản ứng với NaCl, Na2SO4 và NaNO3 ⇝ loại đáp án A, B, C.
✔️ Chọn D. vì 2Al + 3H2SO4 → Al2(SO4)3 + 3H2↑.
✔️ Chọn D. vì 2Al + 3H2SO4 → Al2(SO4)3 + 3H2↑.
Câu 13 [906841]: Nhỏ vài giọt nước brom vào ống nghiệm đựng 2 ml dung dịch chất X, lắc nhẹ thấy có kết tủa trắng. Chất X là
A, etanol.
B, anilin.
C, glixerol.
D, axit axetic.
HD: anilin tạo kết tủa trắng với Br2 tương tự như phenol:


Câu 14 [338844]: Cacbohiđrat chiếm thành phần nhiều nhất trong mật ong là
A, glucozơ.
B, fructozơ.
C, saccarozơ.
D, tinh bột.
HD: Thành phần mật ong:

⇝ đường fructozơ chiếm thành phần nhiều nhất trong mật ong.

⇝ đường fructozơ chiếm thành phần nhiều nhất trong mật ong.
Câu 15 [57671]: Cho dãy các kim loại: Na, Cu, Al, Cr. Kim loại mềm nhất trong dãy là
A, Na.
B, Cr.
C, Cu.
D, Al.
HD:
Các kim loại kiềm có độ cứng thấp nên Na là kim loại mềm nhất trong dãy trên.
Các kim loại kiềm có độ cứng thấp nên Na là kim loại mềm nhất trong dãy trên.
Câu 16 [982773]: Số oxi hóa của sắt trong Fe(NO3)3 là
A, +3.
B, –2.
C, +2.
D, –3.
HD: Số oxi hóa của sắt trong Fe(NO3)3 là +3 ⇝ Chọn đáp án A. ♥
Câu 17 [7605]: Sản phẩm của phản ứng este hóa giữa ancol metylic và axit propionic là
A, propyl propionat.
B, metyl propionat.
C, propyl fomat.
D, metyl axetat.
HD: Ancol metylic là CH3OH || Axit propionic là C2H5COOH.
☆ Phản ứng este hóa: C2H5COOH + CH3OH ⇄ C2H5COOCH3 + H2O.
|⇝ Sản phẩm C2H5COOCH3 có tên gọi là metyl propionat. ❒
☆ Phản ứng este hóa: C2H5COOH + CH3OH ⇄ C2H5COOCH3 + H2O.
|⇝ Sản phẩm C2H5COOCH3 có tên gọi là metyl propionat. ❒
Câu 18 [59313]: Ở nhiệt độ cao, oxit nào sau đây không bị khí H2 khử?
A, Al2O3.
B, CuO.
C, Fe2O3.
D, PbO.
Giải: Oxit của kim loại từ Al trở về trước trong dãy điện hóa không bị H2 khử ⇒ chọn A.
Câu 19 [225762]: Kim loại nào sau đây tác dụng với dung dịch HCl, sinh ra khí H2?
A, Hg.
B, Zn.
C, Cu.
D, Ag.
HD: Dãy điện hoá: 
⇝ trong dãy chỉ có Zn tác dụng axit H+ thu khí H2 mà thôi.
Zn + 2HCl → ZnCl2 + H2↑ ⇝ Chọn đáp án B. ♦

⇝ trong dãy chỉ có Zn tác dụng axit H+ thu khí H2 mà thôi.
Zn + 2HCl → ZnCl2 + H2↑ ⇝ Chọn đáp án B. ♦
Câu 20 [305654]: Ở điều kiện thường, chất nào sau đây tồn tại ở thể rắn?
A, ethyl alcohol.
B, phenol.
C, benzene.
D, styrene.
HD: Ôn lại chút tính chất vật lí của phenol thông qua sơ đồ sau:
![540615[LG].png](https://m.moon.vn/Images/Teachers/rongden_167/ProS2018/BAI%2016/540615[LG].png)
⇒ Ở điều kiện thường, chất tồn tại ở thể rắn chính là phenol. Chọn B. ♦.
![540615[LG].png](https://m.moon.vn/Images/Teachers/rongden_167/ProS2018/BAI%2016/540615[LG].png)
⇒ Ở điều kiện thường, chất tồn tại ở thể rắn chính là phenol. Chọn B. ♦.
Câu 21 [679802]: Cho 0,1 mol Gly-Ala tác dụng với dung dịch KOH dư, đun nóng. Sau khi các phản ứng xảy ra hoàn toàn, số mol KOH đã phản ứng là
A, 0,2.
B, 0,1.
C, 0,3.
D, 0,4.
HD: Phản ứng: Gly-Ala + 2KOH → Gly-K + Ala-K + H2O.
Từ tỉ lệ phản ứng, ta có nKOH = 2nGly-Ala = 0,2 mol.
Từ tỉ lệ phản ứng, ta có nKOH = 2nGly-Ala = 0,2 mol.
Câu 22 [981813]: Hấp thụ hết 0,784 lít khí CO2 (đktc) vào dung dịch Ca(OH)2 dư, thu được m gam kết tủa. Giá trị của m là
A, 1,50.
B, 3,50.
C, 3,94.
D, 7,88.
HD: ► Ca(OH)2 dùng dư nên xảy ra phản ứng:
Ca(OH)2 + CO2 → CaCO3↓ + H2O.
Giả thiết: nCO2 = 0,035 mol ⇒ nCaCO3 = 0,035 mol.
⇝ Yêu cầu m = mkết tủa CaCO3 = 0,035 × 100 = 3,5 gam ⇝ Chọn đáp án B. ♦
Ca(OH)2 + CO2 → CaCO3↓ + H2O.
Giả thiết: nCO2 = 0,035 mol ⇒ nCaCO3 = 0,035 mol.
⇝ Yêu cầu m = mkết tủa CaCO3 = 0,035 × 100 = 3,5 gam ⇝ Chọn đáp án B. ♦
Câu 23 [983209]: Khi lên men m gam glucozơ thì thu được 0,12 mol C2H5OH. Mặt khác, m gam glucozơ tác dụng hết với lượng dư dung dịch AgNO3 trong NH3, thu được 0,2 mol Ag. Hiệu suất a là
A, 60%.
B, 80%.
C, 70%.
D, 75%.
HD: Tỉ lệ phản ứng tráng bạc (hoàn toàn, hiệu suất 100%):

Giả thiết nAg = 0,2 mol ⇒ nglucozơ = 0,1 mol ứng với m gam glucozơ.
☆ Phản ứng lên men: C6H12O6 ––lên men→ 2C2H5OH + 2CO2↑.
Theo lí thiết, nCO2 thu được = 2nglucozơ = 0,2 mol.
Mà thực tế chỉ thu được 0,12 mol CO2
⇒ hiệu suất phản ứng là 0,12 ÷ 0,2 × 100% = 60% ⇝ Chọn đáp án A. ♥

Giả thiết nAg = 0,2 mol ⇒ nglucozơ = 0,1 mol ứng với m gam glucozơ.
☆ Phản ứng lên men: C6H12O6 ––lên men→ 2C2H5OH + 2CO2↑.
Theo lí thiết, nCO2 thu được = 2nglucozơ = 0,2 mol.
Mà thực tế chỉ thu được 0,12 mol CO2
⇒ hiệu suất phản ứng là 0,12 ÷ 0,2 × 100% = 60% ⇝ Chọn đáp án A. ♥
Câu 24 [21674]: Phát biểu nào sau đây là đúng?
A, Trùng hợp stiren thu được poli(phenol-fomanđehit).
B, Trùng ngưng buta-1,3-đien với acrilonitrin có xúc tác Na được cao su buna-N.
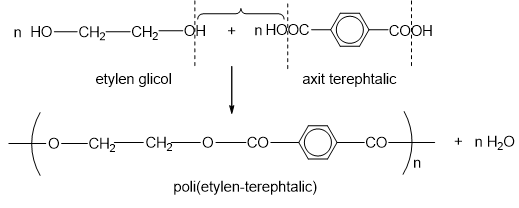
C, Poli(etylen-terephtalat) được điều chế bằng phản ứng trùng ngưng các monome tương ứng.
D, Tơ visco là tơ tổng hợp.
HD: Xem xét - phân tích các phát biểu:
☒ A. sai Trùng hợp stiren thu được polime tương ứng là polistiren.
Còn muốn tổng hợp poli(phenol-fomanđehit) cần trùng ngưng các monome tương ứng:

☒ B. sai vì đó là phản ứng đồng trùng hợp, chứ không phải trùng ngưng:

☑ C. đúng Poli(etylen-terephtalat) được điều chế bằng phản ứng trùng ngưng các monome tương ứng:
☒ D. sai vì tơ visco là tơ bán tổng hợp (tơ nhân tạo) chứ không phải là tơ tổng hợp. ❒
☒ A. sai Trùng hợp stiren thu được polime tương ứng là polistiren.
Còn muốn tổng hợp poli(phenol-fomanđehit) cần trùng ngưng các monome tương ứng:

☒ B. sai vì đó là phản ứng đồng trùng hợp, chứ không phải trùng ngưng:

☑ C. đúng Poli(etylen-terephtalat) được điều chế bằng phản ứng trùng ngưng các monome tương ứng:

☒ D. sai vì tơ visco là tơ bán tổng hợp (tơ nhân tạo) chứ không phải là tơ tổng hợp. ❒
Câu 25 [11183]: Cho các chất: (1) glucozơ, (2) triolein, (3) axit oleic, (4) axetanđehit. Ở điều kiện thích hợp, số chất có khả năng tham gia phản ứng cộng với H2 (xúc tác Ni) là
A, 4.
B, 1.
C, 3.
D, 2.
HD: • (2): triolein (C17H33COO)3C3H5 và (3) axit oleic C17H33COOH còn có
nối đôi C=C trong mạch cacbon ⇒ + H2/xt Ni → gốc hđc no.
• các hợp chất: (1) glucozơ và (4) axetanđehit có nhóm chức anđehit –CHO (πC=O)
⇒ có khả năng + H2/xt Ni → chức ancol –CH2OH.
Theo đó, cả 4 chất đều thỏa mãn → chọn đáp án A. ♥.
nối đôi C=C trong mạch cacbon ⇒ + H2/xt Ni → gốc hđc no.
• các hợp chất: (1) glucozơ và (4) axetanđehit có nhóm chức anđehit –CHO (πC=O)
⇒ có khả năng + H2/xt Ni → chức ancol –CH2OH.
Theo đó, cả 4 chất đều thỏa mãn → chọn đáp án A. ♥.
Câu 26 [679719]: Hòa tan m gam Fe bằng dung dịch H2SO4 loãng, dư thu được 2,24 lít khí H2. Giá trị của m là
A, 5,60.
B, 1,12.
C, 2,24.
D, 2,80.
HD: Phản ứng: Fe + H2SO4 → FeSO4 + H2↑.
Giả thiết nH2 = 0,1 mol ⇒ nFe = 0,1 mol ⇒ m = 0,1 × 56 = 5,6 gam.
Giả thiết nH2 = 0,1 mol ⇒ nFe = 0,1 mol ⇒ m = 0,1 × 56 = 5,6 gam.
Câu 27 [228881]: Khi đun nóng hỗn hợp gồm axit CH3COOH và ancol CH3OH (xúc tác H2SO4 đặc), thu được este X. Số nguyên tử hiđro trong phân tử X là
A, 4.
B, 5.
C, 6.
D, 8.
Đáp án: C
Câu 28 [257381]: Chất nào sau đây tác dụng với dung dịch HCl không thu được sản phẩm khí?
A, FeCO3.
B, Fe(OH)2.
C, FeS
D, Fe.
HD: Các phản ứng xảy ra tương ứng:
✔️ A. FeCO3 + 2HCl → FeCl2 + CO2↑ + H2O.
❌ B. Fe(OH)2 + 2HCl → FeCl2 + 2H2O.
✔️ C. FeS + 2HCl → FeCl2 + H2S↑.
✔️ D. Fe + 2HCl → FeCl2 + H2↑.
⇒ chỉ có phản ứng ở đáp án B không có tạo sản phẩm khí ⇝ Chọn đáp án B. ♦
✔️ A. FeCO3 + 2HCl → FeCl2 + CO2↑ + H2O.
❌ B. Fe(OH)2 + 2HCl → FeCl2 + 2H2O.
✔️ C. FeS + 2HCl → FeCl2 + H2S↑.
✔️ D. Fe + 2HCl → FeCl2 + H2↑.
⇒ chỉ có phản ứng ở đáp án B không có tạo sản phẩm khí ⇝ Chọn đáp án B. ♦
Câu 29 [310781]: Cracking khí butan một thời gian thì thu được hỗn hợp khí X gồm CH4, C3H6, C2H6, C2H4 và C4H10 dư. Cho toàn bộ hỗn hợp X đi qua dung dịch nước Br2 dư thì khối lượng bình brom tăng lên 0,91 gam và có 4 gam Br2 phản ứng, đồng thời có hỗn hợp khí Y thoát ra khỏi bình Br2 (thể tích của Y bằng 54,545% thể tích của X). Để đốt cháy hoàn toàn hỗn hợp Y cần vừa đủ V lít O2 (ở đktc). Giá trị của V là
A, 2,184.
B, 4,368.
C, 2,128.
D, 1,736.
HD: ► Phản ứng cracking: 
Gọi số mol C2H4 và C3H6 lần lượt là a và b ta có hệ:
► Nhận xét: nY = nbutan ban đầu và nX – nbutan ban đầu = a + b = 0,025 mol.
Lại thêm giả thiết: nY = 0,054545nX ⇒ nX = 0,055 mol và nY = 0,03 mol.
Bảo toàn C và H ta có: đốt 0,03 mol Y + ? mol O2 ––to→ 0,055 mol CO2 + 0,085 mol H2O.
Theo đó, bảo toàn nguyên tố O ta có: nO2 = 0,0975 mol ⇒ VO2 = 2,184 lít.

Gọi số mol C2H4 và C3H6 lần lượt là a và b ta có hệ:

► Nhận xét: nY = nbutan ban đầu và nX – nbutan ban đầu = a + b = 0,025 mol.
Lại thêm giả thiết: nY = 0,054545nX ⇒ nX = 0,055 mol và nY = 0,03 mol.
Bảo toàn C và H ta có: đốt 0,03 mol Y + ? mol O2 ––to→ 0,055 mol CO2 + 0,085 mol H2O.
Theo đó, bảo toàn nguyên tố O ta có: nO2 = 0,0975 mol ⇒ VO2 = 2,184 lít.
Câu 30 [255485]: Cho các phản ứng theo sơ đồ sau:
X1 + H2SO4 → X2↑ + X3 + X4;
3X1 + 2Y1 + 3X3 → 3X2↑ + 2Fe(OH)3↓ + 6T;
X1 + CaCl2 → Z↓ + 2T.
Đốt cháy X1 trên ngọn lửa không màu thấy xuất hiện màu tím. X1, Y1 có thể là chất nào sau đây?
X1 + H2SO4 → X2↑ + X3 + X4;
3X1 + 2Y1 + 3X3 → 3X2↑ + 2Fe(OH)3↓ + 6T;
X1 + CaCl2 → Z↓ + 2T.
Đốt cháy X1 trên ngọn lửa không màu thấy xuất hiện màu tím. X1, Y1 có thể là chất nào sau đây?
A, NaHCO3, MgCl2.
B, KHCO3, MgCl2.
C, Na2CO3, FeCl3.
D, K2CO3, FeCl3.
HD: Bài học về màu ngọn lửa các muối kim loại kiềm:

⇝ Loại đáp án A và C vì muối Na cho ngọn lửa màu vàng.
Lại có KHCO3 + CaCl2 không xảy ra phản ứng nên loại đáp án B.
⇝ đáp án D thoả mãn với X1 là K2CO3 và Y1 tương ứng là FeCl3.
✔️ K2CO3 + H2SO4 → CO2↑ (X2) + H2O (X3) + K2SO4 (X4).
✔️ 3K2CO3 + 2FeCl3 + 3H2O → 3CO2↑ + 2Fe(OH)3↓ + 6KCl.
✔️ K2CO3 + CaCl2 → CaCO3↓ + 2KCl.

⇝ Loại đáp án A và C vì muối Na cho ngọn lửa màu vàng.
Lại có KHCO3 + CaCl2 không xảy ra phản ứng nên loại đáp án B.
⇝ đáp án D thoả mãn với X1 là K2CO3 và Y1 tương ứng là FeCl3.
✔️ K2CO3 + H2SO4 → CO2↑ (X2) + H2O (X3) + K2SO4 (X4).
✔️ 3K2CO3 + 2FeCl3 + 3H2O → 3CO2↑ + 2Fe(OH)3↓ + 6KCl.
✔️ K2CO3 + CaCl2 → CaCO3↓ + 2KCl.
Câu 31 [982505]: Đốt cháy hoàn toàn m gam hỗn hợp E gồm triglixerit X và axit béo Y cần vừa đủ 32,592 lít khí O2, sau phản ứng thu được 23,184 lít khí CO2 và 17,1 gam H2O. Mặt khác, thủy phân hoàn toàn 24,12 gam E bằng dung dịch NaOH vừa đủ thu được 25,08 gam một muối natri của axit béo. Các thể tích khí đều đo ở đktc. Phần trăm khối lượng của triglixerit X có trong hỗn hợp E là
A, 83,02%.
B, 82,46%.
C, 78,93%.
D, 81,90%.
HD: ☆ Giải đốt m gam E + 1,455 mol O2 –––to–→ 1,035 mol CO2 + 0,95 mol H2O.
⇒ m gam E gồm: 1,035 mol C + 0,95 mol H2 + 0,055 mol O2.
⇒ m = 16,08 gam và nchức este COO = 0,055 mol.
Đồng nhất số liệu: 24,12 = 16,08 × 1,5 nên thuỷ phân m gam muối thu được 25,08 ÷ 1,5 = 16,72 gam muối.
Ta có 0,055 mol muối dạng RCOONa nặng 16,72 gam ⇒ là C17H33COONa.
m gam E gồm C18H34O2 và C57H104O6
⇒ giải hệ số mol có 0,01 mol C18H34O2 và 0,015 mol C57H104O6.
⇒ Yêu cầu %mX/E = 0,015 × 884 ÷ 16,08 × 100% ≈ 82,46%.
⇒ m gam E gồm: 1,035 mol C + 0,95 mol H2 + 0,055 mol O2.
⇒ m = 16,08 gam và nchức este COO = 0,055 mol.
Đồng nhất số liệu: 24,12 = 16,08 × 1,5 nên thuỷ phân m gam muối thu được 25,08 ÷ 1,5 = 16,72 gam muối.
Ta có 0,055 mol muối dạng RCOONa nặng 16,72 gam ⇒ là C17H33COONa.
m gam E gồm C18H34O2 và C57H104O6
⇒ giải hệ số mol có 0,01 mol C18H34O2 và 0,015 mol C57H104O6.
⇒ Yêu cầu %mX/E = 0,015 × 884 ÷ 16,08 × 100% ≈ 82,46%.
Câu 32 [908887]: Hỗn hợp E gồm hai amin X (CnHmN), Y (CnHm+1N2 với n ≥ 2) và hai anken đồng đẳng kế tiếp. Đốt cháy hoàn toàn 0,11 mol E, thu được 0,05 mol N2, 0,30 mol CO2 và 0,42 mol H2O. Phần trăm khối lượng của X trong E là
A, 40,41%.
B, 38,01%.
C, 70,72%.
D, 30,31%.
Ta thấy:  amin no hoặc có 1 nối đôi trong phân tử.
amin no hoặc có 1 nối đôi trong phân tử.
Xét trường hợp amin có 1 nối đôi, ta có:
0.5nx + ny = = 0,08 => không thỏa mãn do đề cho nx + ny < nE
= 0,08 => không thỏa mãn do đề cho nx + ny < nE
Vậy hai amin cần tìm là amin no.

=> nanken = 0,08 - 0,04 - 0,01 = 0,03 (mol)
BTKL: mE = mC + mH + mN = 4,08 gam
BTNT (C): 0,04n + 0,01n + 0,03. (số Canken) = 0,22
⇒ n = 3; số Canken = 7/3
BTNT H: 0,04.m + 0,01.(m + 1) + 0,03.(2,7/3) = 0,3,2 => vậy m = 9
 57,84%
57,84%
 amin no hoặc có 1 nối đôi trong phân tử.
amin no hoặc có 1 nối đôi trong phân tử.
Xét trường hợp amin có 1 nối đôi, ta có:
0.5nx + ny =
 = 0,08 => không thỏa mãn do đề cho nx + ny < nE
= 0,08 => không thỏa mãn do đề cho nx + ny < nE
Vậy hai amin cần tìm là amin no.

=> nanken = 0,08 - 0,04 - 0,01 = 0,03 (mol)
BTKL: mE = mC + mH + mN = 4,08 gam
BTNT (C): 0,04n + 0,01n + 0,03. (số Canken) = 0,22
⇒ n = 3; số Canken = 7/3
BTNT H: 0,04.m + 0,01.(m + 1) + 0,03.(2,7/3) = 0,3,2 => vậy m = 9
 57,84%
57,84%
Câu 33 [311744]: Cho vào ống nghiệm 1 ml dung dịch lòng trắng trứng 10%, thêm tiếp 1 ml dung dịch NaOH 30% và 1 giọt dung dịch CuSO4 2%. Lắc nhẹ ống nghiệm, hiện tượng quan sát được là
A, xuất hiện kết tủa đỏ gạch, sau đó tan ra tạo dung dịch xanh lam.
B, xuất hiện kết tủa xanh lam, sau đó kết tủa chuyển sang màu đỏ gạch.
C, xuất hiện kết tủa xanh lam, sau đó tan ra tạo dung dịch màu tím.
D, xuất hiện kết tủa đỏ gạch, kết tủa không bị tan ra.
HD: Phân tích thí nghiệm:
☆ đầu tiên tạo thành kết Cu(OH)2 màu xanh do xảy ra phản ứng:
CuSO4 + 2NaOH → Cu(OH)2↓ + Na2SO4.
☆ Sau đó, lòng trắng trứng chứa anbumin (protein) ⇒ có phản ứng màu biure ⇝ kết tủa Cu(OH)2 bị hoà tan thành dung dịch có màu tím.
☆ đầu tiên tạo thành kết Cu(OH)2 màu xanh do xảy ra phản ứng:
CuSO4 + 2NaOH → Cu(OH)2↓ + Na2SO4.
☆ Sau đó, lòng trắng trứng chứa anbumin (protein) ⇒ có phản ứng màu biure ⇝ kết tủa Cu(OH)2 bị hoà tan thành dung dịch có màu tím.
Câu 34 [679464]: Điện phân dung dịch X chứa 3a mol Cu(NO3)2 và a mol KCl (với điện cực trơ, màng ngăn xốp) đến khi khối lượng catot tăng 12,8 gam thì dừng điện phân, thu được dung dịch Y. Cho 22,4 gam bột Fe vào Y, sau khi các phản ứng xảy ra hoàn toàn, thu được khí NO (sản phẩm khử duy nhất của N+5) và 16 gam hỗn hợp kim loại. Giả thiết hiệu suất điện phân là 100%. Giá trị của a là
A, 0,096.
B, 0,128.
C, 0,112.
D, 0,080.
HD: 12,8 gam tương ứng với 0,2 mol Cu. Quan sát 4 đáp án, nhỏ nhất là a = 0,08 ⇒ 3a = 0,24 > 0,2. Dựa vào phân tích này suy ra dung dịch Y chứa (3a – 0,2) mol Cu(NO3)2; 4b mol HNO3 và a mol KNO3.
Bảo toàn số mol anion NO3– ta có: 2 × (3a – 0,2) + 4b + a = 6a ⇒ 4b = 0,4 – a.
Phản ứng:
Ghép cụm hoặc bảo toàn electron có nNO = b mol
⇒ số mol Fe(NO3)2 là (3a + 0,2 + 1,5b) (bảo toàn N).
⇒ BTKL kim loại: 22,4 + 64 × (3a – 0,2) = 56 × (3a + 0,2 + 1,5b) + 16.
Lập hệ các phương trình giải được a = 0,08 mol và b = 0,08 mol ⇝ Chọn đáp án D. ♠
Bảo toàn số mol anion NO3– ta có: 2 × (3a – 0,2) + 4b + a = 6a ⇒ 4b = 0,4 – a.
Phản ứng:

Ghép cụm hoặc bảo toàn electron có nNO = b mol
⇒ số mol Fe(NO3)2 là (3a + 0,2 + 1,5b) (bảo toàn N).
⇒ BTKL kim loại: 22,4 + 64 × (3a – 0,2) = 56 × (3a + 0,2 + 1,5b) + 16.
Lập hệ các phương trình giải được a = 0,08 mol và b = 0,08 mol ⇝ Chọn đáp án D. ♠
Câu 35 [679735]: Hỗn hợp E gồm ba este hở mạch đều tạo bởi axit cacboxylic với ancol: X (no, đơn chức), Y (không no, đơn chức, phân tử có hai liên kết pi) và Z (no, hai chức). Cho 0,58 mol E phản ứng vừa đủ với dung dịch NaOH, thu được 38,34 gam hỗn hợp ba ancol cùng dãy đồng đẳng và 73,22 gam hỗn hợp T gồm ba muối của ba axit cacboxylic. Đốt cháy toàn bộ T cần vừa đủ 0,365 mol O2, thu được Na2CO3, H2O và 0,6 mol CO2. Phần trăm khối lượng của Y trong E có giá trị gần nhất với giá trị nào sau đây?
A, 5.
B, 8.
C, 6.
D, 7.
HD: Đốt T có đủ 3 giả thiết số ⇒ giải được bài toán đốt cháy muối.!
☆ 73,22 gam T + 0,365 mol O2 ––to→ a mol Na2CO3 + 0,6 mol CO2 + b mol H2O.
► Nhận xét: có a mol Na2CO3 ⇄ 2a mol COONa ⇒ nO/T = 4a mol.
⇒ Bảo toàn nguyên tố O: 4a + 0,365 × 2 = 3a + 0,6 × 2 + b.
Lại theo bảo toàn khối lượng: 73,22 + 0,365 × 32 = 106a + 0,6 × 44 + b × 18.
⇒ Giải hệ các phương trình trên ta được a = 0,54 và b = 0,07.
► có 2a = 1,08 mol COONa ⇒ nOH ancol = 1,08 mol.
có este X no, đơn, hở nên ba ancol cùng thuộc dãy đồng đẳng no, đơn, hở.
⇒ 38,34 gam dạng CkH2k + 2O = kCH2.H2O ⇒ nCH2 = (38,34 – 1,08 × 18) ÷ 14 = 1,35 mol.
⇒ Bảo toàn nguyên tố C có ngay ∑nC trong E = ∑nC trong T + ∑nC ancol = 2,49 mol.
Tương tự, bảo toàn nguyên tố H có ∑nH trong E = ∑nH trong T + ∑nH ancol – nH trong NaOH = 3,92 mol.
0,58 mol E gồm x mol X dạng CnH2nO2; y mol Y dạng CmH2m – 2O2 và z mol Z dạng CpH2p – 2O4.
⇒ x + y + z = 0,58; số mol chức este: x + y + 2z = nNaOH = 1,08.
Lại theo tương quan đốt E: ∑nCO2 – ∑nH2O = 2,49 – 3,92 ÷ 2 = y + z.
⇒ Giải hệ các phương trình trên có: x = 0,05; y = 0,03 và z = 0,5 mol.
☆ Phương trình nghiệm nguyên: 0,05n + 0,03m + 0,5p = 2,49 (bảo toàn C).
⇒ 5n + 3m + 50p = 249 với điều kiện n ≥ 2; m ≥ 4; p ≥ 4.
⇒ p ≤ (249 – 5 × 2 – 3 × 4) ÷ 50 = 4,54 ⇒ p = 4 ⇒ 5n + 3m = 49.
Các cặp nghiệm thoả mãn: (n; m) = (2; 13); (5; 8); (8; 3).
► Lại nhận xét, p = 4 thì chỉ có duy nhất cấu tạo (COOCH3)3 thoả mãn ⇒ để thu được 3 ancol thì hai este đơn chức còn lại được tạo từ 2 ancol C2H5OH và C3H7OH ⇒ n ≥ 3; m ≥ 5 ⇒ chỉ có cặp nghiệm n = 5 và m = 8 thoả mãn mà thôi.
mE = mmuối + mancol – mNaOH = 73,22 + 38,34 – 1,08 × 40 = 68,36 gam.
⇒ thông tin về Y: có 0,03 mol C8H14O2 ⇒ %mY/E ≈ 6,23%.
☆ 73,22 gam T + 0,365 mol O2 ––to→ a mol Na2CO3 + 0,6 mol CO2 + b mol H2O.
► Nhận xét: có a mol Na2CO3 ⇄ 2a mol COONa ⇒ nO/T = 4a mol.
⇒ Bảo toàn nguyên tố O: 4a + 0,365 × 2 = 3a + 0,6 × 2 + b.
Lại theo bảo toàn khối lượng: 73,22 + 0,365 × 32 = 106a + 0,6 × 44 + b × 18.
⇒ Giải hệ các phương trình trên ta được a = 0,54 và b = 0,07.
► có 2a = 1,08 mol COONa ⇒ nOH ancol = 1,08 mol.
có este X no, đơn, hở nên ba ancol cùng thuộc dãy đồng đẳng no, đơn, hở.
⇒ 38,34 gam dạng CkH2k + 2O = kCH2.H2O ⇒ nCH2 = (38,34 – 1,08 × 18) ÷ 14 = 1,35 mol.
⇒ Bảo toàn nguyên tố C có ngay ∑nC trong E = ∑nC trong T + ∑nC ancol = 2,49 mol.
Tương tự, bảo toàn nguyên tố H có ∑nH trong E = ∑nH trong T + ∑nH ancol – nH trong NaOH = 3,92 mol.
0,58 mol E gồm x mol X dạng CnH2nO2; y mol Y dạng CmH2m – 2O2 và z mol Z dạng CpH2p – 2O4.
⇒ x + y + z = 0,58; số mol chức este: x + y + 2z = nNaOH = 1,08.
Lại theo tương quan đốt E: ∑nCO2 – ∑nH2O = 2,49 – 3,92 ÷ 2 = y + z.
⇒ Giải hệ các phương trình trên có: x = 0,05; y = 0,03 và z = 0,5 mol.
☆ Phương trình nghiệm nguyên: 0,05n + 0,03m + 0,5p = 2,49 (bảo toàn C).
⇒ 5n + 3m + 50p = 249 với điều kiện n ≥ 2; m ≥ 4; p ≥ 4.
⇒ p ≤ (249 – 5 × 2 – 3 × 4) ÷ 50 = 4,54 ⇒ p = 4 ⇒ 5n + 3m = 49.
Các cặp nghiệm thoả mãn: (n; m) = (2; 13); (5; 8); (8; 3).
► Lại nhận xét, p = 4 thì chỉ có duy nhất cấu tạo (COOCH3)3 thoả mãn ⇒ để thu được 3 ancol thì hai este đơn chức còn lại được tạo từ 2 ancol C2H5OH và C3H7OH ⇒ n ≥ 3; m ≥ 5 ⇒ chỉ có cặp nghiệm n = 5 và m = 8 thoả mãn mà thôi.
mE = mmuối + mancol – mNaOH = 73,22 + 38,34 – 1,08 × 40 = 68,36 gam.
⇒ thông tin về Y: có 0,03 mol C8H14O2 ⇒ %mY/E ≈ 6,23%.
Câu 36 [678631]: Đốt cháy hoàn toàn 4,4 gam sunfua của kim loại M (công thức MS) trong oxi dư. Chất rắn sau phản ứng đem hoà tan trong lượng vừa đủ dung dịch HNO3 37,8%. Nồng độ phần trăm của muối trong dung dịch thu được là 41,72%. Khi làm lạnh dung dịch này thì có 8,08 gam muối rắn X tách ra và nồng độ phần trăm của muối trong dung dịch giảm xuống còn 34,7%. Số nguyên tử oxi có trong công thức phân tử của muối X là
A, 18.
B, 15.
C, 14.
D, 20.
HD: ☆ Toán nồng độ ⇝ ta "tráo giả thiết", tạm thời coi như chưa biết khối lượng MS; lấy 100 gam dung dịch HNO3 37,8% ⇄ 0,6 mol HNO3.
Sơ đồ: MS + O2 (dư) ––to→ M2On + HNO3 → M(NO3)n + H2O.
Bảo toàn H có ngay 0,3 mol H2O. Đặt mM2On = a gam
⇒ BTKL, ta có: mmuối = a + 0,6 × 63 – 0,3 × 18 = (a + 32,4) gam.
mdung dịch sau phản ứng = (100 + a) gam ⇝ C% = (a + 32,4) ÷ (a + 100) × 100% = 41,72%.
⇒ Nhẹ nhàng giải ra a = 16,0 gam ⇒ oxit gồm 11,2 gam M và 0,3 mol O.
Lập tỉ lệ mM ÷ ne trao đổi = 11,2 ÷ (0,3 × 2) = 56/3 ⇝ cho biết là kim loại Fe trong oxit Fe2O3.
Tương ứng có 0,2 mol FeS ⇄ 17,6 gam gấp 4 lần giá trị 4,4 gam MS đề cho.
☆ Đảo lại đúng số liệu: thu được là 29 gam dung dịch chứa 0,05 mol Fe(NO3)3.
Tách 8,08 gam muối Fe(NO3)3.nH2O ⇝ còn lại 20,92 gam dung dịch Fe(NO3)3 nồng độ 34,7% ⇝ tương ứng Fe(NO3)3 có trong dung dịch sau tách là 0,03 mol ⇒ có 0,02 mol Fe(NO3)3 tách ra trong X.
⇒ phần H2O trong X là 3,24 gam tương ứng 0,18 mol ⇝ công thức X: Fe(NO3)3.9H2O.
⇝ Yêu cầu số nguyên tử oxi có trong công thức phân tử của muối X là 18.
Sơ đồ: MS + O2 (dư) ––to→ M2On + HNO3 → M(NO3)n + H2O.
Bảo toàn H có ngay 0,3 mol H2O. Đặt mM2On = a gam
⇒ BTKL, ta có: mmuối = a + 0,6 × 63 – 0,3 × 18 = (a + 32,4) gam.
mdung dịch sau phản ứng = (100 + a) gam ⇝ C% = (a + 32,4) ÷ (a + 100) × 100% = 41,72%.
⇒ Nhẹ nhàng giải ra a = 16,0 gam ⇒ oxit gồm 11,2 gam M và 0,3 mol O.
Lập tỉ lệ mM ÷ ne trao đổi = 11,2 ÷ (0,3 × 2) = 56/3 ⇝ cho biết là kim loại Fe trong oxit Fe2O3.
Tương ứng có 0,2 mol FeS ⇄ 17,6 gam gấp 4 lần giá trị 4,4 gam MS đề cho.
☆ Đảo lại đúng số liệu: thu được là 29 gam dung dịch chứa 0,05 mol Fe(NO3)3.
Tách 8,08 gam muối Fe(NO3)3.nH2O ⇝ còn lại 20,92 gam dung dịch Fe(NO3)3 nồng độ 34,7% ⇝ tương ứng Fe(NO3)3 có trong dung dịch sau tách là 0,03 mol ⇒ có 0,02 mol Fe(NO3)3 tách ra trong X.
⇒ phần H2O trong X là 3,24 gam tương ứng 0,18 mol ⇝ công thức X: Fe(NO3)3.9H2O.
⇝ Yêu cầu số nguyên tử oxi có trong công thức phân tử của muối X là 18.
Câu 37 [982768]: Cho các phát biểu sau:
(a) Trong công nghiệp dược phẩm, saccarozơ được dùng để pha chế thuốc.
(b) Muối đinatri glutamat là thành phần chính của mì chính (bột ngọt).
(c) Tơ nilon-6,6 được dùng dệt vải may mặc, bện dây dù, đan lưới.
(d) Xenlulozơ điaxetat được dùng làm thuốc súng không khói.
(e) Trong cơ thể người, chất béo là nguồn cung cấp và dự trữ năng lượng.
Số phát biểu đúng là
(a) Trong công nghiệp dược phẩm, saccarozơ được dùng để pha chế thuốc.
(b) Muối đinatri glutamat là thành phần chính của mì chính (bột ngọt).
(c) Tơ nilon-6,6 được dùng dệt vải may mặc, bện dây dù, đan lưới.
(d) Xenlulozơ điaxetat được dùng làm thuốc súng không khói.
(e) Trong cơ thể người, chất béo là nguồn cung cấp và dự trữ năng lượng.
Số phát biểu đúng là
A, 4.
B, 2.
C, 5.
D, 3.
HD: Phân tích các đáp án:
✔️ (a) đúng vì saccarozơ được dùng để pha chế thuốc.
❌ (b) sai vì thành phần chính của mì chính (bột ngọt) là muối mononatri glutamat chứ không phải đi-.
✔️ (c) đúng theo ứng dụng của nilon-6,6.
❌ (d) sai vì xenlulozơ điaxetat là thành phân tơ sợi axetat, còn thuốc súng là liên quan đến xenlulozơ trinitrat.
✔️ (e) đúng. Chất béo dự trữ dưới dạng các mô mỡ, khi cần sẽ đốt thành CO2 + H2O + năng lượng.
⇝ có 3/5 phát biểu đúng ⇝ Chọn đáp án D. ♠
✔️ (a) đúng vì saccarozơ được dùng để pha chế thuốc.
❌ (b) sai vì thành phần chính của mì chính (bột ngọt) là muối mononatri glutamat chứ không phải đi-.
✔️ (c) đúng theo ứng dụng của nilon-6,6.
❌ (d) sai vì xenlulozơ điaxetat là thành phân tơ sợi axetat, còn thuốc súng là liên quan đến xenlulozơ trinitrat.
✔️ (e) đúng. Chất béo dự trữ dưới dạng các mô mỡ, khi cần sẽ đốt thành CO2 + H2O + năng lượng.
⇝ có 3/5 phát biểu đúng ⇝ Chọn đáp án D. ♠
Câu 38 [983098]: Este X hai chức mạch hở có công thức phân tử C7H10O4. Thủy phân hoàn toàn X trong dung dịch NaOH đun nóng, thu được ancol Y và hai chất hữu cơ Z và T (MZ < MY < MT). Y tác dụng với Cu(OH)2 ở điều kiện thường, tạo dung dịch màu xanh lam. Cho các phát biểu sau:
(a) Chất Z có phản ứng tráng gương.
(b) Có hai công thức cấu tạo phù hợp với chất X.
(c) Chất T làm mất màu nước brom.
(d) Chất Y là propan-1,2-điol.
(e) Nung chất T với NaOH và CaO ở nhiệt độ cao, thu được khí etilen.
(g) Đốt cháy 0,1 mol Z cần vừa đủ 0,075 mol O2 (hiệu suất phản ứng 100%).
Số phát biểu đúng là
(a) Chất Z có phản ứng tráng gương.
(b) Có hai công thức cấu tạo phù hợp với chất X.
(c) Chất T làm mất màu nước brom.
(d) Chất Y là propan-1,2-điol.
(e) Nung chất T với NaOH và CaO ở nhiệt độ cao, thu được khí etilen.
(g) Đốt cháy 0,1 mol Z cần vừa đủ 0,075 mol O2 (hiệu suất phản ứng 100%).
Số phát biểu đúng là
A, 3.
B, 2.
C, 4.
D, 5.
HD: ancol Y tác dụng được Cu(OH)2 ⇝ Y là ancol hai chức, có 2 nhóm OH liền kề ⇒ X và Y tương ứng là muối.
Mà muối nhỏ nhất là HCOONa ⇒ MX ≥ 68 ⇒ MY > MZ ≥ 68 nên CY ≥ 3.
► Nếu Y có 4C thì MY = 90 ⇒ CZ + CT = 7 – 4 = 3 = 1 + 2
⇒ Z chỉ có thể là HCOONa (68) và T chỉ có thể là CH3COONa (82) ⇝ không thoả mãn.
⇝ CY = 3 ⇝ cấu tạo duy nhất: CH3CHOHCH2OH (propan-1,2-điol).
X có 3π; gồm 2πC=O trong chức este ⇒ còn 1πC=C ⇒ axit T không no ⇒ CT ≥ 3.
Lại có CZ ≥ 1 mà CZ + CT = 4 ⇒ CZ = 1 và CT = 3.
⇒ Cấu tạo Z: HCOONa (68) và T là CH2=CHCOONa (94)
⇝ Có 2 cấu tạo tương ứng của X như sau:

⇝ Phân tích các phát biểu:
✔️ (a) đúng vì cấu tạo Z có hình dạng chức anđehit: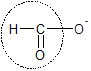
✔️ (b) đúng theo phân tích trên về cấu tạo X.
✔️ (c) đúng vì cấu tạo T là CH2=CHCOONa có nối đôi C=C nên cộng được Br2.
✔️ (d) đúng, Y là CH3CHOHCH2OH: propan-1,2-điol.
✔️ (e) đúng. CH2=CHCOONa + NaOH ––CaO, to→ CH2=CH2↑ + Na2CO3.
❌ (g) sai vì đốt Z: 2HCO2Na + O2 ––to→ Na2CO3 + CO2 + H2O.
Theo phương trình, đốt 0,1 mol Z cần đúng 0,1 mol O2 ≠ 0,075 mol.
⇝ có 5/6 phát biểu đúng ⇝ Chọn đáp án D. ♠
Mà muối nhỏ nhất là HCOONa ⇒ MX ≥ 68 ⇒ MY > MZ ≥ 68 nên CY ≥ 3.
► Nếu Y có 4C thì MY = 90 ⇒ CZ + CT = 7 – 4 = 3 = 1 + 2
⇒ Z chỉ có thể là HCOONa (68) và T chỉ có thể là CH3COONa (82) ⇝ không thoả mãn.
⇝ CY = 3 ⇝ cấu tạo duy nhất: CH3CHOHCH2OH (propan-1,2-điol).
X có 3π; gồm 2πC=O trong chức este ⇒ còn 1πC=C ⇒ axit T không no ⇒ CT ≥ 3.
Lại có CZ ≥ 1 mà CZ + CT = 4 ⇒ CZ = 1 và CT = 3.
⇒ Cấu tạo Z: HCOONa (68) và T là CH2=CHCOONa (94)
⇝ Có 2 cấu tạo tương ứng của X như sau:

⇝ Phân tích các phát biểu:
✔️ (a) đúng vì cấu tạo Z có hình dạng chức anđehit:

✔️ (b) đúng theo phân tích trên về cấu tạo X.
✔️ (c) đúng vì cấu tạo T là CH2=CHCOONa có nối đôi C=C nên cộng được Br2.
✔️ (d) đúng, Y là CH3CHOHCH2OH: propan-1,2-điol.
✔️ (e) đúng. CH2=CHCOONa + NaOH ––CaO, to→ CH2=CH2↑ + Na2CO3.
❌ (g) sai vì đốt Z: 2HCO2Na + O2 ––to→ Na2CO3 + CO2 + H2O.
Theo phương trình, đốt 0,1 mol Z cần đúng 0,1 mol O2 ≠ 0,075 mol.
⇝ có 5/6 phát biểu đúng ⇝ Chọn đáp án D. ♠
Câu 39 [52555]: Để 17,92 gam phôi sắt ngoài không khí một thời gian thu được hỗn hợp X gồm Fe và các oxit Fe. Hòa tan hết X trong dung dịch HCl loãng dư thu được dung dịch Y chứa 44,9 gam muối và 1,792 lít khí H2 (đktc). Mặt khác hòa tan hết X trong 230 gam dung dịch HNO3 31,5% thu được dung dịch Z. Cho 620 ml dung dịch NaOH 1,5M vào dung dịch Z thu được 32,1 gam kết tủa duy nhất. Nồng độ C% của muối sắt có trong dung dịch Z
A, 28,59%.
B, 31,12%
C, 31,36%.
D, 31,74%.
HD: có 0,32 mol Fe → có 0,76 mol Cltrong muối → HCl → H2O → nO trong oxit = 0,3 mol.
NaOH xử lí dung dịch sau phản ứng: tủa duy nhất là 0,3 mol Fe(OH)3 (so với 0,32 mol Fe ban đầu)
||→ nghĩa là 0,93 mol NaOH dùng trước đó đã phản ứng với 0,03 mol HNO3 dư trong Z rồi.
có ∑nHNO3 phản ứng = 1,12 mol → nH2O là 0,56 mol và nN spk = 0,16 mol (bảo toàn N)
→ nO spk = 0,22 mol (theo ghép cụm) → mspk = 5,76 gam.
||→ mdung dịch Z = 246,96 gam → C%Fe(NO3)3 = 0,32 × 242 ÷ Ans ≈ 31,36 %. Chọn C. ♣.
NaOH xử lí dung dịch sau phản ứng: tủa duy nhất là 0,3 mol Fe(OH)3 (so với 0,32 mol Fe ban đầu)
||→ nghĩa là 0,93 mol NaOH dùng trước đó đã phản ứng với 0,03 mol HNO3 dư trong Z rồi.
có ∑nHNO3 phản ứng = 1,12 mol → nH2O là 0,56 mol và nN spk = 0,16 mol (bảo toàn N)
→ nO spk = 0,22 mol (theo ghép cụm) → mspk = 5,76 gam.
||→ mdung dịch Z = 246,96 gam → C%Fe(NO3)3 = 0,32 × 242 ÷ Ans ≈ 31,36 %. Chọn C. ♣.
Câu 40 [982028]: Cho các phát biểu sau:
(a) Để bảo quản natri, người ta ngâm natri trong dầu hỏa.
(b) Hỗn hợp Fe3O4 và Cu (tỉ lệ mol 1 : 1) tan hết trong dung dịch H2SO4 loãng, dư.
(c) Nhỏ từ từ axit HCl vào dung dịch Na2CO3 một lúc sau mới thấy khí thoát ra.
(d) Khi cho Fe(NO3)2 vào dung dịch HCl đặc, có xảy ra phản ứng hóa học.
Số phát biểu đúng là
(a) Để bảo quản natri, người ta ngâm natri trong dầu hỏa.
(b) Hỗn hợp Fe3O4 và Cu (tỉ lệ mol 1 : 1) tan hết trong dung dịch H2SO4 loãng, dư.
(c) Nhỏ từ từ axit HCl vào dung dịch Na2CO3 một lúc sau mới thấy khí thoát ra.
(d) Khi cho Fe(NO3)2 vào dung dịch HCl đặc, có xảy ra phản ứng hóa học.
Số phát biểu đúng là
A, 1.
B, 2.
C, 4.
D, 3.
HD: Phân tích các phát biểu:
✔️ (a) đúng. dầu hoả lỏng là các hiđrocacbon không tác dụng với Na, giúp ngăn cách Na với môi trường xung quanh.
✔️ (b) đúng. Fe3O4 + 4H2SO4 → Fe2(SO4)3 + FeSO4 + 4H2O.
Sau đó Cu + Fe2(SO4)3 → CuSO4 + 2FeSO4 (tỉ lệ cần Cu và Fe3O4 vừa đúng 1 : 1).
✔️ (c) nhỏ từ từ HCl vào Na2CO3 thì đầu tiên: HCl + Na2CO3 → NaCl + NaHCO3; sau đó HCl mới xảy ra tiếp HCl + NaHCO3 → NaCl + CO2↑ + H2O.
✔️ (d) đúng vì xảy ra phản ứng oxi hoá - khử: 3Fe2+ + 4H+ + NO3– → 3Fe3+ + NO + 2H2O.
⇝ Tất cả 4/4 phát biểu đều đúng ⇝ Chọn đáp án C. ♣
✔️ (a) đúng. dầu hoả lỏng là các hiđrocacbon không tác dụng với Na, giúp ngăn cách Na với môi trường xung quanh.
✔️ (b) đúng. Fe3O4 + 4H2SO4 → Fe2(SO4)3 + FeSO4 + 4H2O.
Sau đó Cu + Fe2(SO4)3 → CuSO4 + 2FeSO4 (tỉ lệ cần Cu và Fe3O4 vừa đúng 1 : 1).
✔️ (c) nhỏ từ từ HCl vào Na2CO3 thì đầu tiên: HCl + Na2CO3 → NaCl + NaHCO3; sau đó HCl mới xảy ra tiếp HCl + NaHCO3 → NaCl + CO2↑ + H2O.
✔️ (d) đúng vì xảy ra phản ứng oxi hoá - khử: 3Fe2+ + 4H+ + NO3– → 3Fe3+ + NO + 2H2O.
⇝ Tất cả 4/4 phát biểu đều đúng ⇝ Chọn đáp án C. ♣