Đáp án
1C
2C
3A
4A
5C
6C
7A
8C
9B
10D
11A
12C
13A
14A
15A
16C
17A
18A
19A
20C
21C
22B
23D
24D
25D
26D
27B
28D
29C
30A
31A
32A
33D
34D
35B
36D
37C
38A
39D
40A
Đáp án Đề minh họa số 32 thi Tốt Nghiệp Trung học Phổ Thông 2024 môn Hóa học
Câu 1 [255452]: Kali phản ứng với lượng dư chất nào sau đây tạo thành dung dịch kiềm?
A, HCl.
B, Cl2.
C, H2O.
D, O2.
HD: Phân tích các đáp án:
❌ A. 2K + 2HCl → 2KCl (muối kali clorua) + H2↑.
❌ B. 2K + Cl2 → 2KCl (muối kali clorua).
✔️ C. 2K + 2H2O → 2KOH (kiềm kali hiđroxit) + H2↑.
❌ D. 4K + O2 → 2K2O (oxit bazơ: kali oxit).
❌ A. 2K + 2HCl → 2KCl (muối kali clorua) + H2↑.
❌ B. 2K + Cl2 → 2KCl (muối kali clorua).
✔️ C. 2K + 2H2O → 2KOH (kiềm kali hiđroxit) + H2↑.
❌ D. 4K + O2 → 2K2O (oxit bazơ: kali oxit).
Câu 2 [906737]: Ở điều kiện thường, chất nào sau đây làm mất màu dung dịch Br2?
A, Butan.
B, Metan.
C, Etilen.
D, Propan.
HD: butan: C4H10; metan: CH4 và propan: C3H8 là các ankan, không có khả năng làm mất màu dung dịch Br2 ⇝ đáp án còn lại là C. etilen là CH2=CH2 có khả năng cộng Br2 → làm mất màu:
CH2=CH2 + Br2 → CH2Br–CH2Br.
CH2=CH2 + Br2 → CH2Br–CH2Br.
Câu 3 [679535]: Dung dịch chất nào sau đây hòa tan được Al(OH)3?
A, NaOH.
B, KCl.
C, MgCl2.
D, NaNO3.
HD: Dung dịch NaOH hoà tan được Al(OH)3 tạo muối aluminat:
NaOH + Al(OH)3 → NaAlO2 + 2H2O.
NaOH + Al(OH)3 → NaAlO2 + 2H2O.
Câu 4 [24176]: Chất không phản ứng với dung dịch HCl là
A, phenylclorua.
B, anilin.
C, glyxin.
D, Ala-Gly.
HD: Các hợp chất anilin, glyxin, Ala-Gly chứa nhóm chức amino NH2
⇝ phản ứng được với dung dịch HCl: RNH2 + HCl → RNH3Cl.
Phenyclorua là C6H5Cl không phản ứng được với dung dịch HCl. ❒
⇝ phản ứng được với dung dịch HCl: RNH2 + HCl → RNH3Cl.
Phenyclorua là C6H5Cl không phản ứng được với dung dịch HCl. ❒
Câu 5 [679355]: Cho vài giọt quỳ tím vào dung dịch NH3 thì dung dịch chuyển thành
A, màu đỏ.
B, màu vàng.
C, màu xanh.
D, màu hồng.
HD: Dung dịch amoniac (NH3) có tính bazơ và làm quỳ tím chuyển thành màu xanh.
Câu 6 [679544]: Kim loại nào sau đây tan trong nước ở điều kiện thường?
A, Cu.
B, Fe.
C, Na.
D, Al.
HD: Bài học kim loại phản ứng với nước:

⇝ Na + H2O → NaOH (tan) + H2↑ ||⇒ Na tan được trong nước ở điều kiện thường.

⇝ Na + H2O → NaOH (tan) + H2↑ ||⇒ Na tan được trong nước ở điều kiện thường.
Câu 7 [60414]: Fe có thể tan trong dung dịch chất nào sau đây?
A, FeCl3.
B, MgCl2.
C, AlCl3.
D, FeCl2.
HD:
Fe + 2FeCl3 → 3FeCl2.
Fe + 2FeCl3 → 3FeCl2.
Câu 8 [59573]: Khi điều chế kim loại các ion kim loại đóng vai trò là chất
A, khử.
B, cho proton.
C, bị khử.
D, nhận proton.
HD: ► Ghi nhớ: "khử cho (electron) - o (oxi hóa) nhận (electron)" - "sự gì bị nấy (tương ứng".
☆ Điều chế kim loại: Mn+ + ne → M.
Ion Mn+ nhận electron ⇒ là chất oxi hóa ⇝ Mn+ bị khử
Hay là xảy ra sự khử ion kim loại Mn+ thành kim loại M tương ứng. ❒
☆ Điều chế kim loại: Mn+ + ne → M.
Ion Mn+ nhận electron ⇒ là chất oxi hóa ⇝ Mn+ bị khử
Hay là xảy ra sự khử ion kim loại Mn+ thành kim loại M tương ứng. ❒
Câu 9 [982226]: Polime nào sau đây thuộc loại polime tổng hợp?
A, Xenlulozơ.
B, Poli(vinyl clorua).
C, Tơ visco.
D, Tinh bột.
HD: Bài học phân loại tơ:
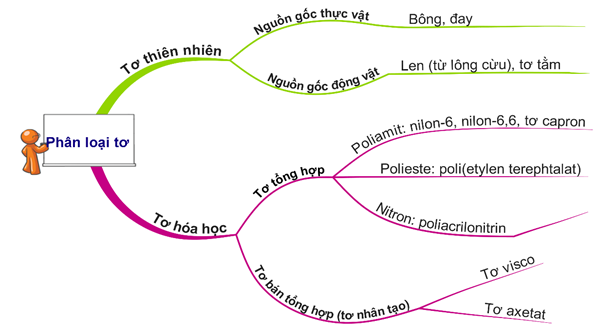
⇝ Poli(vinyl clorua) (PVC) thuộc loại polime tổng hợp ⇝ Chọn đáp án B. ♦

⇝ Poli(vinyl clorua) (PVC) thuộc loại polime tổng hợp ⇝ Chọn đáp án B. ♦
Câu 10 [58609]: Kim loại nào sau đây có tính khử yếu hơn Mg?
A, Na.
B, Ca.
C, K.
D, Fe.
Giải: Dãy hoạt động hóa học được sắp xếp theo chiều tính khử giảm dần ⇒ kim loại có tính khử yếu hơn Mg sẽ đứng sau Mg ⇒ Chọn Fe ⇒ Chọn D.
Câu 11 [906788]: Sắt có số oxi hóa +2 trong hợp chất nào sau đây?
A, FeO.
B, FeCl3.
C, Fe2O3.
D, Fe2(SO4)3.

Câu 12 [311829]: Hóa chất quan trọng đứng hàng thứ hai sau axit sunfuric, được sử dụng để nấu xà phòng, sản xuất chất tẩy rửa, bột giặt, tơ nhân tạo, tinh chế quặng nhôm là
A, NaCl.
B, Na2CO3.
C, NaOH.
D, Na2SO4.
HD: Xem bài các hợp chất quan trọng của kim loại kiềm.!
NaOH là hóa chất quan trọng đứng hàng thứ 2 sau axit sunfuric H2SO4.
ứng dụng: nấu xà phòng, chế phẩm nhuộm, tơ nhân tạo, tinh chất quặng nhôm,... ❒
p/s: quá trình tinh chế quặng nhôm có thể tham khảo ở bookID = 635448
NaOH là hóa chất quan trọng đứng hàng thứ 2 sau axit sunfuric H2SO4.
ứng dụng: nấu xà phòng, chế phẩm nhuộm, tơ nhân tạo, tinh chất quặng nhôm,... ❒
p/s: quá trình tinh chế quặng nhôm có thể tham khảo ở bookID = 635448
Câu 13 [20772]: Muối nào sau đây được dùng làm xà phòng?
A, C17H35COONa.
B, HOOCCH2CH2CH(NH2)COONa.
C, CH2=CHCOONa.
D, CH3CH(NH2)COONa.
Giải: Muối của axit béo được dùng làm xà phòng ⇒ chọn A.
Câu 14 [241217]: Một mẫu khí thải được sục vào dung dịch CuSO4, thấy xuất hiện kết tủa màu đen. Hiện tượng này do chất nào có trong khí thải gây ra?
A, H2S
B, NO2
C, SO2
D, CO2
HD: Hiện tượng do khí H2S (hiđro sunfua) gây ra:
H2S + CuSO4 → CuS↓ + H2SO4.
Rõ hơn, bạn đọc có thể xem video mô tả sau:
H2S + CuSO4 → CuS↓ + H2SO4.
Rõ hơn, bạn đọc có thể xem video mô tả sau:
Câu 15 [11118]: Các chất đồng phân với nhau là
A, glucozơ và fructozơ.
B, tinh bột và xenlulozơ.
C, saccarozơ và glucozơ.
D, saccarozơ và fructozơ.
HD: Glucozơ là fructozơ là hai monosaccarit có cùng công thức phân tử C6H12O6 ⇝ chúng là đồng phân của nhau.
► Tinh bột và xenlulozơ là hai polisaccarit có cùng công thức phân tử dạng (C6H10O5)n nhưng hệ số n (hệ số polime) của chúng khác nhau nên không phải là đồng phân của nhau.! ❒
► Tinh bột và xenlulozơ là hai polisaccarit có cùng công thức phân tử dạng (C6H10O5)n nhưng hệ số n (hệ số polime) của chúng khác nhau nên không phải là đồng phân của nhau.! ❒
Câu 16 [679545]: Công thức hóa học của sắt(III) clorua là
A, FeSO4.
B, FeCl2.
C, FeCl3.
D, Fe2(SO4)3.
HD: Phân tích các đáp án:
| Công thức | A. FeSO4. | B. FeCl2. | C. FeCl3. | D. Fe2(SO4)3. |
| Tên gọi | sắt(II) sunfat | sắt(II) clorua | sắt(III) clorua | sắt(III) sunfat |
Câu 17 [312002]: Trên bề mặt các hố tôi vôi lâu ngày thường có lớp màng chất rắn. Thành phần hóa học của lớp màng này là
A, CaCO3.
B, CaSO4.2H2O.
C, Ca3(PO4)2.
D, Ca(OH)2.
HD: Không khí sẵn có CO2 nên trên bề mặt tiếp xúc không khí
của hố vôi lâu ngày sẽ xảy ra phản ứng hóa học:
CO2 + Ca(OH)2 → CaCO3↓ + H2O.
⇝ lớp màng rắn trên bề mặt chính là CaCO3. ❒
của hố vôi lâu ngày sẽ xảy ra phản ứng hóa học:
CO2 + Ca(OH)2 → CaCO3↓ + H2O.
⇝ lớp màng rắn trên bề mặt chính là CaCO3. ❒
Câu 18 [18096]: Dung dịch của chất nào sau đây không làm đổi màu quỳ tím?
A, Glyxin.
B, Lysin.
C, Axit glutamic.
D, Metylamin.
HD: Metylamin (CH3NH2) có tính bazơ mạnh hơn amoniac (NH3), làm quỳ tím hóa xanh.
Cấu tạo của axit glutamic có 1 nhóm amino –NH2 và 2 nhóm cacboxyl –COOH nên có môi trường axit, làm quỳ tím đổi màu hồng.
Cấu tạo của lysin có 2 nhóm amino –NH2 và 1 nhóm cacboxyl –COOH nên có môi trường bazơ, làm quỳ tím đổi màu xanh.
Glyxin cấu tạo có 1 nhóm NH2; 1 nhóm COOH nên có môi trường trung tính, không làm quỳ tím đổi màu. ❒
Cấu tạo của axit glutamic có 1 nhóm amino –NH2 và 2 nhóm cacboxyl –COOH nên có môi trường axit, làm quỳ tím đổi màu hồng.
Cấu tạo của lysin có 2 nhóm amino –NH2 và 1 nhóm cacboxyl –COOH nên có môi trường bazơ, làm quỳ tím đổi màu xanh.
Glyxin cấu tạo có 1 nhóm NH2; 1 nhóm COOH nên có môi trường trung tính, không làm quỳ tím đổi màu. ❒
Câu 19 [7119]: Thủy phân este nào sau đây thì thu được hỗn hợp CH3OH và CH3COOH?
A, metyl axetat.
B, metyl fomat.
C, metyl propionat.
D, etyl axetat.
Giải: Este đơn chức có dạng RCOOR'.
Từ axit CH3COOH ⇒ R là gốc CH3–.
Từ ancol CH3OH ⇒ R' là gốc CH3–
⇒ Este X có CTCT thu gọn là CH3COOCH3
● Để gọi tên của este (RCOOR') ta đọc theo thứ tự:
Tên R' + Tên RCOO + at
⇒ Tên gọi của CH3COOCH3 là metyl axetat ⇒ Chọn A.
----------------------------------------
● Một số gốc R' thường gặp:
CH3–: Metyl.
C2H5–: Etyl.
CH3CH2CH2–: Propyl.
CH3CH(CH3)–: Iso propyl.
CH2=CH–: Vinyl.
CH2=CH–CH2–: Anlyl.
Vòng thơm C6H5–: Phenyl [Rất hay nhầm với Benzyl ở ngay dưới].
C6H5–CH2–: Benzyl.
----------------------------------------
● Một số gốc RCOO(at) thường gặp:
HCOO–: Fomat.
CH3COO–: Axetat.
C2H5COO–: Propionat.
CH2=CHCOO–: Acrylat
CH2=C(CH3)COO–: Metacrylat.
C6H5COO–: Benzoat.
Từ axit CH3COOH ⇒ R là gốc CH3–.
Từ ancol CH3OH ⇒ R' là gốc CH3–
⇒ Este X có CTCT thu gọn là CH3COOCH3
● Để gọi tên của este (RCOOR') ta đọc theo thứ tự:
Tên R' + Tên RCOO + at
⇒ Tên gọi của CH3COOCH3 là metyl axetat ⇒ Chọn A.
----------------------------------------
● Một số gốc R' thường gặp:
CH3–: Metyl.
C2H5–: Etyl.
CH3CH2CH2–: Propyl.
CH3CH(CH3)–: Iso propyl.
CH2=CH–: Vinyl.
CH2=CH–CH2–: Anlyl.
Vòng thơm C6H5–: Phenyl [Rất hay nhầm với Benzyl ở ngay dưới].
C6H5–CH2–: Benzyl.
----------------------------------------
● Một số gốc RCOO(at) thường gặp:
HCOO–: Fomat.
CH3COO–: Axetat.
C2H5COO–: Propionat.
CH2=CHCOO–: Acrylat
CH2=C(CH3)COO–: Metacrylat.
C6H5COO–: Benzoat.
Câu 20 [14944]: Một mẫu nước tự nhiên có chứa nhiều các ion Ca2+; Mg2+; SO42⁻; Cl⁻, HCO3⁻. Dung dịch chất nào sau đây có khả năng làm mềm mẫu nước trên?
A, HCl.
B, NaOH.
C, Na2CO3.
D, Ca(OH)2.
Giải: Mẫu nước trên là nước cứng toàn phần ⇒ dùng Na2CO3 ⇒ chọn C.
(vì {Ca2+, Mg2+} + CO32– → ↓ {CaCO3, MgCO3}).
(vì {Ca2+, Mg2+} + CO32– → ↓ {CaCO3, MgCO3}).
Câu 21 [24453]: Phát biểu nào sau đây sai?
A, Thủy phân hoàn toàn protein đơn giản thu được các α-amino axit.
B, Dung dịch protein bị đông tụ khi đun nóng.
C, Các peptit đều có phản ứng màu biure trong môi trường kiềm.
D, Các peptit không bền trong môi trường axit hoặc bazơ.
HD: Phân tích - xem xét các phát biểu:
☑ A. đúng vì các protein đơn giản được tạo thành từ các α-amino axit.
☑ B. đúng. Dung dịch protein bị đông tụ khi đun nóng như gạch cua, lòng trắng trứng.
☒ C. sai vì đipeptit không có phản ứng màu biure.
☑ D. đúng vì liên kết peptit CO–NH kém bền trong cả môi trường axit, bazơ. ❒
☑ A. đúng vì các protein đơn giản được tạo thành từ các α-amino axit.
☑ B. đúng. Dung dịch protein bị đông tụ khi đun nóng như gạch cua, lòng trắng trứng.
☒ C. sai vì đipeptit không có phản ứng màu biure.
☑ D. đúng vì liên kết peptit CO–NH kém bền trong cả môi trường axit, bazơ. ❒
Câu 22 [13994]: Cho dãy gồm các polime sau: (1) poli(hexametylen ađipamit), (2) poliacrilonitrin, (3) poli(etylen terephtalat), poli(metyl metacrylat). Số polime có thành phần hóa học chứa nguyên tố nitơ là
A, 1.
B, 2.
C, 3.
D, 4.
HD: Phân tích cấu tạo của các polime trong dãy:
![577750[LG].png](https://m.moon.vn/Images/Teachers/rongden_167/ProS2018/TAP%20II/577750[LG].png)
⇒ có 2 polime thành phân chứa nguyên tố nitơ → chọn đáp án B. ♦.
![577750[LG].png](https://m.moon.vn/Images/Teachers/rongden_167/ProS2018/TAP%20II/577750[LG].png)
⇒ có 2 polime thành phân chứa nguyên tố nitơ → chọn đáp án B. ♦.
Câu 23 [906797]: Cho 2,25 gam H2NCH2COOH tác dụng hết với dung dịch NaOH, thu được dung dịch chứa m gam muối. Giá trị của m là
A, 2,85.
B, 3,39.
C, 3,42.
D, 2,91.
HD: ★ Phản ứng: H2NCH2COOH + NaOH → H2NCH2COONa + H2O.
Giả thiết cho 0,03 mol Gly ⇒ m = 0,03 × 97 = 2,91 gam.
Giả thiết cho 0,03 mol Gly ⇒ m = 0,03 × 97 = 2,91 gam.
Câu 24 [906844]: Thuỷ phân saccarozơ, thu được hai monosaccarit X và Y. Chất X có nhiều trong quả nho chín nên còn được gọi là đường nho. Phát biểu nào sau đây đúng?
A, Y không tan trong nước.
B, X không có phản ứng tráng bạc.
C, Y có phân tử khối bằng 342.
D, X có tính chất của ancol đa chức.
HD: ► X có nhiều trong quả nho chính, còn gọi là đường nho ⇒ X là glucozơ.
⇒ Saccarozơ + H2O ––H+→ glucozơ (X) + fructozơ (Y).
Phân tích các phát biểu:
❌ A. sai vì cả fructozơ, glucozơ hay saccarozơ đều dễ tan trong nước.
❌ B. sai vì glucozơ có khả năng tham gia phản ứng tráng bạc:

❌ C. sai vì Y là fructozơ có công thức phân tử C6H12O6 tương ứng MY = 180 ≠ 342.
✔️ D. đúng vì X cấu tạo của X có nhiều nhóm OH:

⇒ Saccarozơ + H2O ––H+→ glucozơ (X) + fructozơ (Y).
Phân tích các phát biểu:
❌ A. sai vì cả fructozơ, glucozơ hay saccarozơ đều dễ tan trong nước.
❌ B. sai vì glucozơ có khả năng tham gia phản ứng tráng bạc:

❌ C. sai vì Y là fructozơ có công thức phân tử C6H12O6 tương ứng MY = 180 ≠ 342.
✔️ D. đúng vì X cấu tạo của X có nhiều nhóm OH:

Câu 25 [906760]: Nhỏ vài giọt nước brom vào ống nghiệm dựng 2 ml dung dịch chất X, lắc nhẹ thấy có kết tủa trắng. Chất X là
A, glixerol.
B, axit axetic.
C, etanol.
D, phenol.
HD: trong 4 phương án, chỉ có phenol phản ứng với nước brom và thu được kết tủa trắng:

► Chú ý: nếu dùng dư Br2 thì sẽ thu được kết tủa màu vàng:


► Chú ý: nếu dùng dư Br2 thì sẽ thu được kết tủa màu vàng:

Câu 26 [311806]: Phi kim X tác dụng với kim loại M thu được chất rắn Y. Hòa tan Y vào nước được dung dịch Z.
Thêm AgNO3 dư vào dung dịch Z được chất rắn G. Cho G vào dung dịch HNO3 đặc nóng dư thu được khí
màu nâu đỏ và chất rắn F. Kim loại M và chất rắn F lần lượt là
A, Al và AgCl.
B, Fe và AgF.
C, Cu và AgBr.
D, Fe và AgCl.
HD: kim loại M là Fe; phi kim X là Cl2. Quá trình phản ứng:
Fedư + Cl2 → chất rắn Y gồm Fe và FeCl2. Y + H2O → dung dịch Z gồm {FeCl2 + FeCl3}.
AgNO3 + dung dịch Z → chất rắn G gồm {AgCl và Ag}↓
|| khi G + HNO3đặc, nóng, dư thì Ag phản ứng tạo NO2↑; AgCl không phản ứng → chất rắn F.
Theo đó, đáp án đúng cần chọn là D. ♦.
Fedư + Cl2 → chất rắn Y gồm Fe và FeCl2. Y + H2O → dung dịch Z gồm {FeCl2 + FeCl3}.
AgNO3 + dung dịch Z → chất rắn G gồm {AgCl và Ag}↓
|| khi G + HNO3đặc, nóng, dư thì Ag phản ứng tạo NO2↑; AgCl không phản ứng → chất rắn F.
Theo đó, đáp án đúng cần chọn là D. ♦.
Câu 27 [981799]: Cho 0,384 gam kim loại R (hóa trị II) tác dụng hết với dung dịch AgNO3 dư, thu được 1,296 gam Ag. Kim loại R là
A, Zn.
B, Cu.
C, Mg.
D, Fe.
HD: Giả thiết nAg = 1,296 ÷ 108 = 0,012 mol ⇒ nR = nAg ÷ 2 = 0,06 mol.
⇒ MR = m ÷ n = 0,384 ÷ 0,06 = 64 cho biết R là Cu (đồng).
⇒ MR = m ÷ n = 0,384 ÷ 0,06 = 64 cho biết R là Cu (đồng).
Câu 28 [117954]: Hòa tan 0,468 gam K vào trong 200 ml dung dịch NaOH 0,03M thu được 200 ml dung dịch X. Giá trị pH của dung dịch X là
A, 11,34.
B, 11,52.
C, 12,78.
D, 12,95.
HD: Phản ứng: K + H2O → KOH + ½.H2↑.
Giả thiết: nK = 0,468 ÷ 39 = 0,012 mol ⇒ nKOH = 0,012 mol.
Chú ý trong X còn chứa 0,006 mol NaOH ⇒ ∑nOH– trong X = 0,018 mol.
⇒ CM (OH–) = 0,018 ÷ 0,2 = 0,09 M.
⇒ pHdung dịch X = 14 + log 0,09 = 12,95. ❒
Giả thiết: nK = 0,468 ÷ 39 = 0,012 mol ⇒ nKOH = 0,012 mol.
Chú ý trong X còn chứa 0,006 mol NaOH ⇒ ∑nOH– trong X = 0,018 mol.
⇒ CM (OH–) = 0,018 ÷ 0,2 = 0,09 M.
⇒ pHdung dịch X = 14 + log 0,09 = 12,95. ❒
Câu 29 [906842]: Phát biểu nào sau đây đúng?
A, Kim loại Fe dẫn điện tốt hơn kim loại Ag.
B, Ở nhiệt độ thường, H2 khử được MgO.
C, Cho Fe vào dung dịch CuSO4 có xảy ra ăn mòn điện hoá học.
D, Kim loại Al không tác dụng với dung dịch HNO3 đặc nóng.
HD: Phân tích các phát biểu:
❌ A. sai vì thứ tự độ dẫn điện: Ag > Cu > Au > Al > Fe.
❌ B. sai vì H2 không khử được oxit các kim loại từ K → Al.
✔️ C. đúng vì đầu tiên: Fe + CuSO4 → FeSO4 + Cu. Cu sinh ra bám vào sắt tạo thành cặp điện cực, trong dung dịch CuSO4 điện li ⇝ đủ đk xảy ra ăn mòn điện hoá.
❌ D. Al phản ứng mạnh với HNO3 đặc nóng (chú ý nhầm sang bị thụ động hoá trong dung dịch HNO3 đặc nguội).
❌ A. sai vì thứ tự độ dẫn điện: Ag > Cu > Au > Al > Fe.
❌ B. sai vì H2 không khử được oxit các kim loại từ K → Al.
✔️ C. đúng vì đầu tiên: Fe + CuSO4 → FeSO4 + Cu. Cu sinh ra bám vào sắt tạo thành cặp điện cực, trong dung dịch CuSO4 điện li ⇝ đủ đk xảy ra ăn mòn điện hoá.
❌ D. Al phản ứng mạnh với HNO3 đặc nóng (chú ý nhầm sang bị thụ động hoá trong dung dịch HNO3 đặc nguội).
Câu 30 [906801]: Khi đốt cháy hoàn toàn 3,51 gam hỗn hợp glucozơ và saccarozơ cần vừa đủ 0,12 mol O2, thu được CO2 và m gam H2O. Giá trị của m là
A, 2,07.
B, 1,80.
C, 3,60.
D, 2,70.
HD: ★ Phân tích: Glucozơ có công thức phân tử C6H12O6 dạng 6C.6H2O
Saccarozơ có công thức phân tử C12H22O11 dạng 12C.11H2O.
⇝ Quy 3,51 gam hỗn hợp về C và H2O; mà H2O không cần O2 để đốt nên nC = 0,12 mol.
⇒ m = 3,51 – 0,12 × 12 = 2,07 gam.
Saccarozơ có công thức phân tử C12H22O11 dạng 12C.11H2O.
⇝ Quy 3,51 gam hỗn hợp về C và H2O; mà H2O không cần O2 để đốt nên nC = 0,12 mol.
⇒ m = 3,51 – 0,12 × 12 = 2,07 gam.
Câu 31 [117578]: Hỗn hợp X gồm Al, Fe và Mg. Cho 15 gam X tác dụng với oxi, sau một thời gian thu được 18,2 gam chất rắn Y. Hòa tan hoàn toàn Y trong dung dịch HCl dư, thu được 6,72 lít khí H2 (đktc) và dung dịch Z. Cô cạn Z thu được m gam hỗn hợp muối khan. Giá trị của m là
A, 50,5.
B, 39,5.
C, 53,7.
D, 46,6.
Giải: BTKL ta có mO = 18,2 – 15 = 3,2 gam.
⇒ nO = 3,2 ÷ 16 = 0,2 mol || nH2 = 0,3 mol
⇒ ∑nCl– = 2nO + 2nH2 = 1 mol
⇒ mMuối = mKim loại + mCl– = 15 + 35,5 = 50,5 gam ⇒ Chọn A
⇒ nO = 3,2 ÷ 16 = 0,2 mol || nH2 = 0,3 mol
⇒ ∑nCl– = 2nO + 2nH2 = 1 mol
⇒ mMuối = mKim loại + mCl– = 15 + 35,5 = 50,5 gam ⇒ Chọn A
Câu 32 [983208]: Khi thủy phân hoàn toàn 5,88 gam hỗn hợp X gồm hai este đơn chức, mạch hở cần vừa đủ 0,07 mol NaOH, thu được hỗn hợp Y gồm hai muối của hai axit cacboxylic trong cùng dãy đồng đẳng và 2,24 gam một ancol. Đốt cháy hết Y trong O2 dư, thu được Na2CO3, H2O và V lít khí CO2 (đktc). Giá trị của V là
A, 3,472.
B, 2,688.
C, 1,904.
D, 4,256.
HD: hai este đều đơn chức, mạch hở nên không có este của phenol.
Theo đó, nancol = neste = nNaOH phản ứng = 0,07 mol.
⇒ Mancol = 2,24 ÷ 0,07 = 32 cho biết là CH3OH (ancol metylic).
BTKL phản ứng thuỷ phân: 5,88 + 0,07 × 40 = mmuối + 2,24
⇒ mmuối = 6,44 gam ⇒ Mmuối = 92.
► Thật chú ý, muối không no nhỏ nhất là HC≡CCOONa đã có M = 92 rồi.
⇒ Hai muối của hai axit cùng dãy đồng đẳng đều phải no hết.
⇒ Công thức tổng quát 2 muối: CnH2n + 1COONa
⇒ 14n + 68 = 92 ⇒ n = 12/7.
☆ Giải đốt 0,07 mol CnH2n + 1COONa + O2 ––to→ 0,035 mol Na2CO3 + CO2 + H2O.
nC trong muối = 0,07 × (n + 1) = 0,19 mol ⇒ bảo toàn nguyên tố C:
nCO2↑ = 0,19 – 0,035 = 0,155 mol ⇒ V = 3,472 lít ⇝ Chọn đáp án A. ♥
Theo đó, nancol = neste = nNaOH phản ứng = 0,07 mol.
⇒ Mancol = 2,24 ÷ 0,07 = 32 cho biết là CH3OH (ancol metylic).
BTKL phản ứng thuỷ phân: 5,88 + 0,07 × 40 = mmuối + 2,24
⇒ mmuối = 6,44 gam ⇒ Mmuối = 92.
► Thật chú ý, muối không no nhỏ nhất là HC≡CCOONa đã có M = 92 rồi.
⇒ Hai muối của hai axit cùng dãy đồng đẳng đều phải no hết.
⇒ Công thức tổng quát 2 muối: CnH2n + 1COONa
⇒ 14n + 68 = 92 ⇒ n = 12/7.
☆ Giải đốt 0,07 mol CnH2n + 1COONa + O2 ––to→ 0,035 mol Na2CO3 + CO2 + H2O.
nC trong muối = 0,07 × (n + 1) = 0,19 mol ⇒ bảo toàn nguyên tố C:
nCO2↑ = 0,19 – 0,035 = 0,155 mol ⇒ V = 3,472 lít ⇝ Chọn đáp án A. ♥
Câu 33 [981807]: Cho E, Z, F, T đều là các hợp chất hữu cơ no, mạch hở và thỏa mãn sơ đồ các phản ứng:
(1) E + NaOH → X + Y + Z
(2) X + HCl → F + NaCl
(3) Y + HCl → T + NaCl
Biết E chỉ chứa nhóm chức este và trong phân tử có số nguyên tử cacbon bằng số nguyên tử oxi; ME < 168; MZ < MF < MT.
Cho các phát biểu sau:
(a) Có hai công thức cấu tạo của E thỏa mãn sơ đồ trên.
(b) Trong phân tử Z và T đều không có liên kết pi.
(c) Chất F được dùng để điều chế khí CO trong phòng thí nghiệm.
(d) 1 mol chất T phản ứng với kim loại Na dư, thu được tối đa 1 mol H2.
(e) Nhiệt độ sôi của F cao hơn nhiệt độ sôi của Z.
Số phát biểu đúng là
(1) E + NaOH → X + Y + Z
(2) X + HCl → F + NaCl
(3) Y + HCl → T + NaCl
Biết E chỉ chứa nhóm chức este và trong phân tử có số nguyên tử cacbon bằng số nguyên tử oxi; ME < 168; MZ < MF < MT.
Cho các phát biểu sau:
(a) Có hai công thức cấu tạo của E thỏa mãn sơ đồ trên.
(b) Trong phân tử Z và T đều không có liên kết pi.
(c) Chất F được dùng để điều chế khí CO trong phòng thí nghiệm.
(d) 1 mol chất T phản ứng với kim loại Na dư, thu được tối đa 1 mol H2.
(e) Nhiệt độ sôi của F cao hơn nhiệt độ sôi của Z.
Số phát biểu đúng là
A, 1.
B, 2.
C, 4.
D, 3.
HD: Nhận xét: E có số C = số O. mà 6 × (CO) = 6 × 28 = 168 nên số CE = số CO < 6.
Lại có E là este no, mạch hở, E + NaOH → X + Y + Z nên E đa chức.
⇒ E chỉ có thể có công thức là C4H6O4.
Cũng từ E + NaOH → X + Y + Z; và X và Y đều là muối.
⇒ Nếu Z là ancol 2 chức thì CZ ≥ 2; CX ≥ 1 ⇒ từ CY > CX ⇒ CY ≥ 2 ⇒ C E ≥ 2 + 1 + 2 = 5.
Vậy Z là ancol đơn chức ⇝ E chỉ có thể là dạng este nối: HCOOCH2COOCH3.
⇒ Tương ứng: X là HCOONa → F: HCOOH; Y là HOCH2COONa → T: HOCH2COOH; Z là CH3OH. Phân tích các phát biểu:
❌ (a) sai vì như phân tích trên, chỉ có duy nhất một cấu tạo E thoả mãn.
❌ (b) sai vì Z không có liên kết π nhưng trong nhóm COOH của T có nối đôi C=O chứa liên kết π.
✔️ (c) HCOOH = CO.H2O –––H2SO4 đặc to–→ CO + H2O (H2SO4 đặc háo nước).
✔️ (d) đúng vì 1HOCH2COOH (T) + 2Na → NaOCH2COONa + 1H2↑.
✔️ (e) đúng vì nhiệt độ sôi của axit cao hơn ancol có phân tử khối tương đương ⇝ toCH3OH < toHCÔH.
⇝ Số phát biểu đúng là 3/5 ⇝ Chọn đáp án D. ♠
Lại có E là este no, mạch hở, E + NaOH → X + Y + Z nên E đa chức.
⇒ E chỉ có thể có công thức là C4H6O4.
Cũng từ E + NaOH → X + Y + Z; và X và Y đều là muối.
⇒ Nếu Z là ancol 2 chức thì CZ ≥ 2; CX ≥ 1 ⇒ từ CY > CX ⇒ CY ≥ 2 ⇒ C E ≥ 2 + 1 + 2 = 5.
Vậy Z là ancol đơn chức ⇝ E chỉ có thể là dạng este nối: HCOOCH2COOCH3.
⇒ Tương ứng: X là HCOONa → F: HCOOH; Y là HOCH2COONa → T: HOCH2COOH; Z là CH3OH. Phân tích các phát biểu:
❌ (a) sai vì như phân tích trên, chỉ có duy nhất một cấu tạo E thoả mãn.
❌ (b) sai vì Z không có liên kết π nhưng trong nhóm COOH của T có nối đôi C=O chứa liên kết π.
✔️ (c) HCOOH = CO.H2O –––H2SO4 đặc to–→ CO + H2O (H2SO4 đặc háo nước).
✔️ (d) đúng vì 1HOCH2COOH (T) + 2Na → NaOCH2COONa + 1H2↑.
✔️ (e) đúng vì nhiệt độ sôi của axit cao hơn ancol có phân tử khối tương đương ⇝ toCH3OH < toHCÔH.
⇝ Số phát biểu đúng là 3/5 ⇝ Chọn đáp án D. ♠
Câu 34 [52152]: Tiến hành các thí nghiệm sau:
(a) Điện phân dung dịch NaCl với điện cực trơ, màng ngăn xốp.
(b) Cho lá Cu vào dung dịch HNO3 đặc, nguội.
(c) Điện phân dung dịch gồm HCl và CuSO4 với điện cực trơ.
(d) Cho mẩu Na vào lượng dư dung dịch CuSO4.
(e) Cho lá Al vào dung dịch H2SO4 loãng, nguội.
Sau khi phản ứng hoàn toàn, số thí nghiệm có tạo ra chất khí là
(a) Điện phân dung dịch NaCl với điện cực trơ, màng ngăn xốp.
(b) Cho lá Cu vào dung dịch HNO3 đặc, nguội.
(c) Điện phân dung dịch gồm HCl và CuSO4 với điện cực trơ.
(d) Cho mẩu Na vào lượng dư dung dịch CuSO4.
(e) Cho lá Al vào dung dịch H2SO4 loãng, nguội.
Sau khi phản ứng hoàn toàn, số thí nghiệm có tạo ra chất khí là
A, 4.
B, 3.
C, 2.
D, 5.
HD: Các phản ứng xảy ra khi tiến hành các thí nghiệm:
(a) 2NaCl + 2H2O ––ddiepddd, có màng ngăn→ 2NaOH + Cl2↑ + H2↑.
(b) Cu + 4HNO3 → Cu(NO3)2 + 2NO2↑ + 2H2O.
(c) CuSO4 + 2HCl ––điện phân dung dịch→ Cu + Cl2↑ + H2SO4.
(d) 2Na + 2H2O → 2NaOH + H2↑ || CuSO4 + 2NaOH → Cu(OH)2↓ + Na2SO4.
(e) 2Al + 3H2SO4 → Al2(SO4)3 + 3H2↑.
► Thật chú ý: Cu có phản ứng với HNO3 đặc nguội; Al thụ động trong HNO3; H2SO4 đặc nguội; còn loãng thì vẫn phản ứng bình thường; đừng để chữ nguội đánh lừa các bạn ở 2 thí nghiệm trên nhé
|⇝ cả 5 thí nghiệm đều có tạo thành chất khí. ❒
(a) 2NaCl + 2H2O ––ddiepddd, có màng ngăn→ 2NaOH + Cl2↑ + H2↑.
(b) Cu + 4HNO3 → Cu(NO3)2 + 2NO2↑ + 2H2O.
(c) CuSO4 + 2HCl ––điện phân dung dịch→ Cu + Cl2↑ + H2SO4.
(d) 2Na + 2H2O → 2NaOH + H2↑ || CuSO4 + 2NaOH → Cu(OH)2↓ + Na2SO4.
(e) 2Al + 3H2SO4 → Al2(SO4)3 + 3H2↑.
► Thật chú ý: Cu có phản ứng với HNO3 đặc nguội; Al thụ động trong HNO3; H2SO4 đặc nguội; còn loãng thì vẫn phản ứng bình thường; đừng để chữ nguội đánh lừa các bạn ở 2 thí nghiệm trên nhé
|⇝ cả 5 thí nghiệm đều có tạo thành chất khí. ❒
Câu 35 [679772]: Cho các phát biểu sau:
(a) Thủy tinh hữu cơ (plexiglas) được ứng dụng làm cửa kính ô tô.
(b) Quá trình làm rượu vang từ quả nho xảy ra phản ứng lên men rượu của glucozơ.
(c) Khi ngâm trong nước xà phòng có tính kiềm, vải lụa làm bằng tơ tằm sẽ nhanh hỏng.
(d) Khi rớt axit sunfuric đặc vào vải cotton (sợi bông) thì chỗ vải đó sẽ bị đen rồi thủng.
(e) Dầu mỡ động thực vật bị ôi thiu do liên kết C=C của chất béo bị oxi hóa.
Số phát biểu đúng là
(a) Thủy tinh hữu cơ (plexiglas) được ứng dụng làm cửa kính ô tô.
(b) Quá trình làm rượu vang từ quả nho xảy ra phản ứng lên men rượu của glucozơ.
(c) Khi ngâm trong nước xà phòng có tính kiềm, vải lụa làm bằng tơ tằm sẽ nhanh hỏng.
(d) Khi rớt axit sunfuric đặc vào vải cotton (sợi bông) thì chỗ vải đó sẽ bị đen rồi thủng.
(e) Dầu mỡ động thực vật bị ôi thiu do liên kết C=C của chất béo bị oxi hóa.
Số phát biểu đúng là
A, 2.
B, 5.
C, 4.
D, 3.
HD: Phân tích các phát biểu:
✔️ (a) đúng, PMM → thuỷ tinh hữu cơ - vật liệu dẻo ⇒ làm của kính ôtô.
✔️ (b) đúng. Quả nho chính chứa nhiều glucozơ, lên men thì glucozơ ––men rượu→ ancol etylic + CO2↑.
✔️ (c) đúng vì thành phần chính tơ tằm là protein ⇒ các liên kết peptit CO–NH trong đó kém bền trong môi trường kềm, dễ bị thuỷ phân nên vải lụa sẽ nhanh bị hỏng.
✔️ (d) đúng. H2SO4 đặc háo nước, xenlulozơ dạng (6C.5H2O)n sẽ bị mất nước, chỉ còn C - là than có màu đen.
✔️ (e) đúng. Nối đôi C=C dễ bị oxi hoá tạo các anđehit có mùi khó chịu.
⇝ Tất cả có 5/5 phát biểu đúng ⇝ Chọn đáp án B. ♦
✔️ (a) đúng, PMM → thuỷ tinh hữu cơ - vật liệu dẻo ⇒ làm của kính ôtô.
✔️ (b) đúng. Quả nho chính chứa nhiều glucozơ, lên men thì glucozơ ––men rượu→ ancol etylic + CO2↑.
✔️ (c) đúng vì thành phần chính tơ tằm là protein ⇒ các liên kết peptit CO–NH trong đó kém bền trong môi trường kềm, dễ bị thuỷ phân nên vải lụa sẽ nhanh bị hỏng.
✔️ (d) đúng. H2SO4 đặc háo nước, xenlulozơ dạng (6C.5H2O)n sẽ bị mất nước, chỉ còn C - là than có màu đen.
✔️ (e) đúng. Nối đôi C=C dễ bị oxi hoá tạo các anđehit có mùi khó chịu.
⇝ Tất cả có 5/5 phát biểu đúng ⇝ Chọn đáp án B. ♦
Câu 36 [906851]: Cho hỗn hợp E gồm ba chất X, Y và ancol propylic. X, Y là hai amin kế tiếp trong cùng dãy đồng đẳng; phân tử X, Y đều có hai nhóm NH2 và gốc hiđrocacbon không no; MX < MY. Khi đốt cháy hết 0,1 mol E cần vừa đủ 0,551 mol O2, thu được H2O, N2 và 0,354 mol CO2. Phần trăm khối lượng của Y trong E là
A, 52,34%.
B, 30,90%.
C, 49,75%.
D, 19,35%.
HD: ► Tách amin thành dạng CH2 + N + H; C3H8O = 3CH2 + 1H2O.
☆ Quy giải đốt:
► Nhận xét: N và H2O không cần O2 để đốt nên tìm ra số H là 0,08 mol.
Trong đó: ancol propylic: C3H8O = 3CH2 + H2O.
• Amin hai chức, có 1π, ví dụ: H2NCH=CHNH2 ⇄ 2CH2 + NH.
• Amin hai chức, có 2π, ví dụ H2NC≡CNH2 ⇄ 2CH2 + N.
• Amin hai chức, có 3π, ví dụ H2NC≡C-CH=CH2NH2 ⇄ 4CH2 + NH–1…
⇥ Thấy ngay, nếu amin có hơn 1π thì số mol H quy đổi sẽ là 0, hoặc là số âm.
Mà tính toán lại ra là 0,08 nên rõ amin có đúng 1π; cụm NH ⇒ tỉ lệ nN = nH quy đổi = 0,08 mol.
Amin hai chức nên nX + nY = 0,08 ÷ 2 = 0,04 mol ⇒ nancol = 0,1 – 0,04 = 0,06 mol.
⇒ Tương ứng nH2O quy đổi = 0,06 mol ⇒ tính ra khối lượng E là 7,236 gam.
Lại theo bảo toàn C ta có số Ctrung bình X, Y = (0,354 – 0,06 × 3) ÷ 0,04 = 4,35.
⇒ cho biết hai amin tương ứng là 0,026 mol C4H10N2 (X) và 0,014 mol C5H12N2 (Y).
⇒ Yêu cầu: %mY trong E = 0,014 × 100 ÷ 7,236 × 100% ≈ 19,35%.
☆ Quy giải đốt:

► Nhận xét: N và H2O không cần O2 để đốt nên tìm ra số H là 0,08 mol.
Trong đó: ancol propylic: C3H8O = 3CH2 + H2O.
• Amin hai chức, có 1π, ví dụ: H2NCH=CHNH2 ⇄ 2CH2 + NH.
• Amin hai chức, có 2π, ví dụ H2NC≡CNH2 ⇄ 2CH2 + N.
• Amin hai chức, có 3π, ví dụ H2NC≡C-CH=CH2NH2 ⇄ 4CH2 + NH–1…
⇥ Thấy ngay, nếu amin có hơn 1π thì số mol H quy đổi sẽ là 0, hoặc là số âm.
Mà tính toán lại ra là 0,08 nên rõ amin có đúng 1π; cụm NH ⇒ tỉ lệ nN = nH quy đổi = 0,08 mol.
Amin hai chức nên nX + nY = 0,08 ÷ 2 = 0,04 mol ⇒ nancol = 0,1 – 0,04 = 0,06 mol.
⇒ Tương ứng nH2O quy đổi = 0,06 mol ⇒ tính ra khối lượng E là 7,236 gam.
Lại theo bảo toàn C ta có số Ctrung bình X, Y = (0,354 – 0,06 × 3) ÷ 0,04 = 4,35.
⇒ cho biết hai amin tương ứng là 0,026 mol C4H10N2 (X) và 0,014 mol C5H12N2 (Y).
⇒ Yêu cầu: %mY trong E = 0,014 × 100 ÷ 7,236 × 100% ≈ 19,35%.
Câu 37 [332868]: Hỗn hợp E gồm axit oleic, axit linoleic và chất béo X cấu tạo từ hai loại axit béo đó với glixerol. Đốt cháy hoàn toàn m gam E thu được 53,76 lít khí CO2 (đktc). Mặt khác m gam E làm mất màu tối đa 0,18 mol Br2. Thủy phân hoàn toàn m gam E trong NaOH vừa đủ thu được hỗn hợp hai muối natri oleat và natri linoleat có tỉ lệ mol tương ứng là 8 : 5. Giá trị của m gần nhất với
A, 72.
B, 38.
C, 37.
D, 65.
HD: ► Đặc trưng hỗn hợp gồm axit và chất béo ⇒ tư duy quy đổi quen thuộc:
X dạng (RCOO)3C3H5 = 3RCOOH.C3H2
⇒ quy E về gồm 8a mol C17H33COOH + 5a mol C17H31COOH + b mol C3H2.
Ta có nBr2 phản ứng = 8a + 5a × 2 = 0,18 ⇒ a = 0,01 mol.
Lại có đốt E thu được 2,4 mol CO2 ⇒ 0,08 × 18 + 0,05 × 18 + 3b = 2,4 ⇒ b = 0,02 mol.
Theo đó m = mE = 0,08 × 282 + 0,05 × 280 + 0,02 × 38 = 37,32 gam.
X dạng (RCOO)3C3H5 = 3RCOOH.C3H2
⇒ quy E về gồm 8a mol C17H33COOH + 5a mol C17H31COOH + b mol C3H2.
Ta có nBr2 phản ứng = 8a + 5a × 2 = 0,18 ⇒ a = 0,01 mol.
Lại có đốt E thu được 2,4 mol CO2 ⇒ 0,08 × 18 + 0,05 × 18 + 3b = 2,4 ⇒ b = 0,02 mol.
Theo đó m = mE = 0,08 × 282 + 0,05 × 280 + 0,02 × 38 = 37,32 gam.
Câu 38 [678583]: Chia 16 gam oxit kim loại MO thành hai phần bằng nhau:
• Hòa tan phần 1 trong lượng dư dung dịch HCl, xử lý dung dịch thu được ở điều kiện thích hợp thu được 17,1 gam một muối X duy nhất.
• Cho phần 2 tác dụng với dung dịch H2SO4 loãng dư, xử lý dung dịch thu được sau phản ứng ở nhiệt độ dưới 110 độ chỉ thu được 25 gam một muối Y duy nhất.
Biết MX < 180 và MY < 269, giá trị tỉ lệ MY : MX gần nhất với giá trị nào sau đây?
• Hòa tan phần 1 trong lượng dư dung dịch HCl, xử lý dung dịch thu được ở điều kiện thích hợp thu được 17,1 gam một muối X duy nhất.
• Cho phần 2 tác dụng với dung dịch H2SO4 loãng dư, xử lý dung dịch thu được sau phản ứng ở nhiệt độ dưới 110 độ chỉ thu được 25 gam một muối Y duy nhất.
Biết MX < 180 và MY < 269, giá trị tỉ lệ MY : MX gần nhất với giá trị nào sau đây?
A, 1,5.
B, 1,2.
C, 1,3.
D, 1,7.
HD: Phản ứng của 8 gam MO ở mỗi phần:
• MO + 2HCl → MCl2 + H2O, xử lý thu 17,1 gam muối X dạng MCl2.nH2O.
• MO + H2SO4 → MSO4 + H2O; xử lý thu 25 gam Y dạng MSO4.mH2O.
Theo đó: nMO mỗi phần = nMCl2 = nMSO4 ⇝ xây dựng phương trình:

► Lỗi câu hỏi khi MY : MX = 25 : 17,1 ≈ 1,46 ⇝ Chọn đáp án A. ♥ luôn.
► Nếu giải tiếp, ta đi theo cách rất nhanh sau:
MY : MX = 250 ÷ 171; mà MY < 269; MX < 180
⇒ Nghiệm nguyên luôn MY = 250 và MX = 171
⇒ 8 : (M + 16) = 0,1 ⇒ M = 64; từ đó giải n = 2 và m = 5.
Tương ứng X là CuCl2.2H2O và Y là CuSO4.5H2O.
• MO + 2HCl → MCl2 + H2O, xử lý thu 17,1 gam muối X dạng MCl2.nH2O.
• MO + H2SO4 → MSO4 + H2O; xử lý thu 25 gam Y dạng MSO4.mH2O.
Theo đó: nMO mỗi phần = nMCl2 = nMSO4 ⇝ xây dựng phương trình:

► Lỗi câu hỏi khi MY : MX = 25 : 17,1 ≈ 1,46 ⇝ Chọn đáp án A. ♥ luôn.
► Nếu giải tiếp, ta đi theo cách rất nhanh sau:
MY : MX = 250 ÷ 171; mà MY < 269; MX < 180
⇒ Nghiệm nguyên luôn MY = 250 và MX = 171
⇒ 8 : (M + 16) = 0,1 ⇒ M = 64; từ đó giải n = 2 và m = 5.
Tương ứng X là CuCl2.2H2O và Y là CuSO4.5H2O.
Câu 39 [983213]: Hỗn hợp E gồm ba este mạch hở X, Y và Z, trong đó có một este hai chức và hai este đơn chức; MX < MY < MZ. Đốt cháy hết 27,26 gam E cần vừa đủ 1,195 mol O2, thu được H2O và 1,1 mol CO2. Mặt khác, thủy phân hoàn toàn 27,26 gam E trong dung dịch NaOH dư, thu được hỗn hợp các muối của axit cacboxylic no và 14,96 gam hỗn hợp hai ancol kế tiếp nhau trong dãy đồng đẳng. Khối lượng của Y trong 27,26 gam E là
A, 7,88 gam.
B, 3,96 gam.
C, 2,64 gam.
D, 3,06 gam.
HD: ☆ Giải đốt E gồm 1,1 mol C + 0,95 mol H2 + 0,38 mol O2.
có este đơn chức nên ⇒ 2 ancol đồng đẳng đều đơn chức.
mancol = 14,96 gam ⇒ Mancol = 14,96 ÷ 0,38 ≈ 39,37.
⇒ Cho biết hai ancol với số mol là 0,18 mol CH3OH và 0,2 mol C2H5OH.
Bảo toàn C, H, O ⇒ Thành phần muối gồm 0,52 mol C + 0,18 mol H2 + 0,38 mol OONa
Đốt muối ––to→ 0,19 mol Na2CO3 + 0,33 mol CO2 + 0,18 mol H2O.
Hai muối đều no, đốt muối đơn chức cho nCO2 = nH2O còn đốt muối hai chức có nCO2 – nH2O = nmuối hai chức.
⇒ nmuối hai chức = ∑nCO2 – ∑nH2O = 0,33 – 0,18 = 0,15 mol ⇒ nmuối đơn chức = 0,08 mol.
Nếu số C muối hai chức ≥ 3 thì Cmuối đơn chức < (0,52 – 0,15 × 3) ÷ 0,08 = 0,875 không thoả mãn.
⇒ số Cmuối hai chức = 2 tương ứng là (COONa)2.
Vậy, este 2 chức Z chỉ có thể là CH3OOCCOOC2H5: 0,15 mol.
⇒ hai este còn lại là 0,03 mol RCOOCH3 và 0,05 mol R'COOC2H5.
Nghiệm nguyên: 0,03CR + 0,05CR' = 0,14 ⇄ 3CR + 5CR' = 14 ⇒ CR = 3 và CR' = 1.
⇒ Tương ứng có 0,03 mol C3H7COOCH3 (Y) và 0,05 mol CH3COOC2H5 (X).
⇒ Yêu cầu mY trong E = 0,03 × 102 = 3,06 gam ⇝ Chọn đáp án D. ♠
có este đơn chức nên ⇒ 2 ancol đồng đẳng đều đơn chức.
mancol = 14,96 gam ⇒ Mancol = 14,96 ÷ 0,38 ≈ 39,37.
⇒ Cho biết hai ancol với số mol là 0,18 mol CH3OH và 0,2 mol C2H5OH.
Bảo toàn C, H, O ⇒ Thành phần muối gồm 0,52 mol C + 0,18 mol H2 + 0,38 mol OONa
Đốt muối ––to→ 0,19 mol Na2CO3 + 0,33 mol CO2 + 0,18 mol H2O.
Hai muối đều no, đốt muối đơn chức cho nCO2 = nH2O còn đốt muối hai chức có nCO2 – nH2O = nmuối hai chức.
⇒ nmuối hai chức = ∑nCO2 – ∑nH2O = 0,33 – 0,18 = 0,15 mol ⇒ nmuối đơn chức = 0,08 mol.
Nếu số C muối hai chức ≥ 3 thì Cmuối đơn chức < (0,52 – 0,15 × 3) ÷ 0,08 = 0,875 không thoả mãn.
⇒ số Cmuối hai chức = 2 tương ứng là (COONa)2.
Vậy, este 2 chức Z chỉ có thể là CH3OOCCOOC2H5: 0,15 mol.
⇒ hai este còn lại là 0,03 mol RCOOCH3 và 0,05 mol R'COOC2H5.
Nghiệm nguyên: 0,03CR + 0,05CR' = 0,14 ⇄ 3CR + 5CR' = 14 ⇒ CR = 3 và CR' = 1.
⇒ Tương ứng có 0,03 mol C3H7COOCH3 (Y) và 0,05 mol CH3COOC2H5 (X).
⇒ Yêu cầu mY trong E = 0,03 × 102 = 3,06 gam ⇝ Chọn đáp án D. ♠
Câu 40 [906156]: Trong phòng thí nghiệm, khí metan (CH4) được tiến hành điều chế theo các bước sau:
Bước 1: Nghiền nhỏ và trộn đều hỗn hợp gồm natri axetat và vôi tôi xút, sau đó cho vào ống nghiệm khô (ống số 1). Nút kín ống số 1 bằng nút cao su có ống dẫn khí.
Bước 2: Lắp ống số 1 lên giá thí nghiệm rồi nhúng ống dẫn khí vào chậu nước chuẩn bị sẵn.
Bước 3: Dùng đèn cồn đun nóng ống số 1 (lúc đầu đun nhẹ và hơ đều ống nghiệm, sau đó đun tập trung vào phần có hỗn hợp chất rắn).
Bước 4: Từ từ đưa ống dẫn khí vào ống nghiệm (ống số 2) đang ngâm chìm hẳn trong chậu nước để thu khí thoát ra.
Cho các phát biểu sau:
(a) Vôi tôi xút trong hỗn hợp chất rắn ban đầu là Ca(OH)2 và NaOH.
(b) Ở bước 2, lắp ống số 1 sao cho miệng ống hướng lên.
(c) Sau bước 3, cần đợi một thời gian ngắn để khí metan đẩy hết không khí ra khỏi hệ thống trước khi đưa ống dẫn khí vào ống số 2.
(d) Khí metan được thu vào ống số 2 theo phương pháp dời nước.
(e) Kết thúc thí nghiệm: tắt đèn cồn, để ống số 1 nguội hẳn rồi mới đưa ống dẫn khí ra khỏi dung dịch trong ống số 2.
Số phát biểu đúng là
Bước 1: Nghiền nhỏ và trộn đều hỗn hợp gồm natri axetat và vôi tôi xút, sau đó cho vào ống nghiệm khô (ống số 1). Nút kín ống số 1 bằng nút cao su có ống dẫn khí.
Bước 2: Lắp ống số 1 lên giá thí nghiệm rồi nhúng ống dẫn khí vào chậu nước chuẩn bị sẵn.
Bước 3: Dùng đèn cồn đun nóng ống số 1 (lúc đầu đun nhẹ và hơ đều ống nghiệm, sau đó đun tập trung vào phần có hỗn hợp chất rắn).
Bước 4: Từ từ đưa ống dẫn khí vào ống nghiệm (ống số 2) đang ngâm chìm hẳn trong chậu nước để thu khí thoát ra.
Cho các phát biểu sau:
(a) Vôi tôi xút trong hỗn hợp chất rắn ban đầu là Ca(OH)2 và NaOH.
(b) Ở bước 2, lắp ống số 1 sao cho miệng ống hướng lên.
(c) Sau bước 3, cần đợi một thời gian ngắn để khí metan đẩy hết không khí ra khỏi hệ thống trước khi đưa ống dẫn khí vào ống số 2.
(d) Khí metan được thu vào ống số 2 theo phương pháp dời nước.
(e) Kết thúc thí nghiệm: tắt đèn cồn, để ống số 1 nguội hẳn rồi mới đưa ống dẫn khí ra khỏi dung dịch trong ống số 2.
Số phát biểu đúng là
A, 2.
B, 5.
C, 4.
D, 3.
HD: Bố trí thí nghiệm → mô tả lại bằng hình vẽ:
![537483[đề].png](https://m.moon.vn/Images/Teachers/rongden_167/ProS2018/B%C3%80I%204/537483[%C4%91%E1%BB%81].png)
Phản ứng xảy ra: CH3COONa + NaOH ––CaO, to→ CH4↑ + Na2CO3.
☆ Phân tích các phát biểu:
❌ (a) sai, vôi tôi xút trong ống nghiệm (1) là CaO và NaOH.
❌ (b) sai, miệng ống cần lắp hơi chúc xuống như mô tả bởi hoá chất ban đầu thường lẫn hơi nước, khi nung bay hơi, ngưng tụ lại, nếu miệng ống (1) hướng lên thì nước ngưng tụ sẽ chảy ngược lại ống nghiệm, phần chất rắn đang nóng, gặp nước lạnh sẽ dễ dẫn đến vỡ ống nghiệm.
✔️ (c) đúng.
✔️ (d) đúng vì khí metan không tan trong nước nên thu bằng pp đẩy nước.
❌ (e) sai vì nếu tắt đèn cồn mà không tháo ống dẫn khí thì nước sẽ bị hút ngược theo ống dẫn vào ống nghiệm (1) (do áp suất trong ống (1) giảm đột ngột) ⇝ nước lạnh sẽ làm vỡ ống nghiệm (1) đang nóng.
⇝ chỉ có 2/5 phát biểu đúng ⇝ Chọn đáp án A. ♥
Học tập từ thí nghiệm thực tiễn thú vị điều chế CH4 trong PTN:
![537483[đề].png](https://m.moon.vn/Images/Teachers/rongden_167/ProS2018/B%C3%80I%204/537483[%C4%91%E1%BB%81].png)
Phản ứng xảy ra: CH3COONa + NaOH ––CaO, to→ CH4↑ + Na2CO3.
☆ Phân tích các phát biểu:
❌ (a) sai, vôi tôi xút trong ống nghiệm (1) là CaO và NaOH.
❌ (b) sai, miệng ống cần lắp hơi chúc xuống như mô tả bởi hoá chất ban đầu thường lẫn hơi nước, khi nung bay hơi, ngưng tụ lại, nếu miệng ống (1) hướng lên thì nước ngưng tụ sẽ chảy ngược lại ống nghiệm, phần chất rắn đang nóng, gặp nước lạnh sẽ dễ dẫn đến vỡ ống nghiệm.
✔️ (c) đúng.
✔️ (d) đúng vì khí metan không tan trong nước nên thu bằng pp đẩy nước.
❌ (e) sai vì nếu tắt đèn cồn mà không tháo ống dẫn khí thì nước sẽ bị hút ngược theo ống dẫn vào ống nghiệm (1) (do áp suất trong ống (1) giảm đột ngột) ⇝ nước lạnh sẽ làm vỡ ống nghiệm (1) đang nóng.
⇝ chỉ có 2/5 phát biểu đúng ⇝ Chọn đáp án A. ♥
Học tập từ thí nghiệm thực tiễn thú vị điều chế CH4 trong PTN: