Đáp án
1C
2D
3B
4A
5D
6C
7C
8C
9A
10B
11A
12C
13C
14D
15C
16A
17B
18B
19D
20C
21C
22D
23C
24A
25D
26C
27A
28A
29B
30C
31A
32B
33B
34C
35C
36B
37B
38C
39C
40A
Đáp án Đề minh họa số 37 thi Tốt Nghiệp Trung học Phổ Thông 2024 môn Hóa học
Câu 1 [911551]: Các loại phân đạm đều cung cấp cho cây trồng nguyên tố
A, cacbon.
B, kali.
C, nitơ.
D, photpho.
HD: Phân đạm cung cấp nitơ hóa hợp cho cây dưới dạng ion nitrat (NO3–) và ion amoni (NH4+).
► Độ dinh dưỡng phân đạm được đánh giá theo tỉ lệ phần trăm về khối lượng của nguyên tố N ⇝ Chọn đáp án C. ♣
► Độ dinh dưỡng phân đạm được đánh giá theo tỉ lệ phần trăm về khối lượng của nguyên tố N ⇝ Chọn đáp án C. ♣
Câu 2 [14294]: Loại chế phẩm nào sau đây không có saccarozơ?
A, Đường cát.
B, Đường phèn.
C, Mật mía.
D, Nhựa đường (hắc ín).
HD: Nhựa đường là một sản phẩm của quá trình chưng cất dầu mỏ, có thành phần là các hiđrocacbon. ❒


Câu 3 [906751]: Chất X có công thức là FeO. Tên gọi của X là
A, sắt (III) hiđroxit.
B, sắt (II) oxit.
C, sắt (III) hiđroxit.
D, sắt (III) oxit.
HD: Phân tích các đáp án:
| Tên gọi | sắt(III) hiđroxit | sắt(II) oxit | sắt(II) hiđroxit | sắt(III) oxit |
| Cấu tạo | Fe(OH)3 | FeO | Fe(OH)2 | Fe2O3 |
| ❌ | ✔️ | ❌ | ❌ |
Câu 4 [60897]: Kim loại Cu không tan được trong dung dịch nào sau đây?
A, ZnCl2.
B, AgNO3.
C, HNO3.
D, FeCl3.
HD: Thứ tự dãy điện hoá: 
⇒ Cu không phản ứng được với muối ZnCl2 ⇝ Chọn đáp án A. ♥
Còn lại, các phản ứng xảy ra như sau:
✔️ B. 2AgNO3 + Cu → Cu(NO3)2 + 2Ag↓.
✔️ C. 3Cu + 8HNO3 → 3Cu(NO3)2 + 2NO↑ + 4H2O.
✔️ D. Cu + 2FeCl3 → CuCl2 + 2FeCl2.

⇒ Cu không phản ứng được với muối ZnCl2 ⇝ Chọn đáp án A. ♥
Còn lại, các phản ứng xảy ra như sau:
✔️ B. 2AgNO3 + Cu → Cu(NO3)2 + 2Ag↓.
✔️ C. 3Cu + 8HNO3 → 3Cu(NO3)2 + 2NO↑ + 4H2O.
✔️ D. Cu + 2FeCl3 → CuCl2 + 2FeCl2.
Câu 5 [60611]: Kim loại nào sau đây có nhiều hóa trị trong các hợp chất?
A, Al.
B, Zn.
C, Mg.
D, Fe.
HD:
Sắt có thể có hóa trị II, III trong hợp chất.
Sắt có thể có hóa trị II, III trong hợp chất.
Câu 6 [60067]: Kim loại Mg không tác dụng với chất nào dưới đây?
A, Hơi nước nóng.
B, Dung dịch HCl.
C, Dung dịch NaOH.
D, Dung dịch CuSO4.
HD•  ↑
↑
• Mg + 2HCl → MgCl2 + H2↑
• Mg + NaOH →
• Mg + CuSO4 → MgSO4 + Cu
→ Chọn đáp án C.
 ↑
↑• Mg + 2HCl → MgCl2 + H2↑
• Mg + NaOH →
• Mg + CuSO4 → MgSO4 + Cu
→ Chọn đáp án C.
Câu 7 [61015]: Gạch ngói sau khi nung thường có màu đỏ là do có chứa oxit nào sau đây?
A, Al2O3.
B, CaO.
C, Fe2O3.
D, Cr2O3.
HD: Gạch ngói nung từ đất sét có chứa các hợp chất của sắt, khi nung ở nhiệt độ cao trong không khí tạo oxit Fe2O3 có màu đỏ hoặc nâu đỏ ⇝ Chọn đáp án C. ♣
► Cũng sản xuất từ đất sét nhưng gốm sứ lại có màu trắng là do được chọn từ loại đất sét không chứa hoặc chứa rất ít sắt trong đó.!
► Cũng sản xuất từ đất sét nhưng gốm sứ lại có màu trắng là do được chọn từ loại đất sét không chứa hoặc chứa rất ít sắt trong đó.!
Câu 8 [679537]: Dung dịch nào sau đây không làm đổi màu quỳ tím?
A, CH3NH2.
B, NaOH.
C, H2NCH2COOH.
D, HCl.
HD: Phân tích các đáp án:
| Dung dịch | A. CH3NH2. | B. NaOH. | C. H2NCH2COOH. | D. HCl. |
| Quỳ tím | hoá xanh | hoá xanh | không đổi màu (✔️) | hoá đỏ |
Câu 9 [14017]: Dãy nào sau đây sắp xếp các kim loại theo chiều giảm dần tính kim loại?
A, Na, Fe, Cu.
B, Fe, Cu, Na.
C, Cu, Fe, Na.
D, Na, Cu, Fe.
HD: Bài học về sự biến đổi trong bảng tuần hoàn các nguyên tố hóa học:
![591790[LG].png](https://m.moon.vn/Images/Teachers/rongden_167/ProS2018/TAPIII/591790[LG].png)
➤ Xét về tính kim loại giảm dần: Na > Fe > Cu → Chọn đáp án A. ♥.
![591790[LG].png](https://m.moon.vn/Images/Teachers/rongden_167/ProS2018/TAPIII/591790[LG].png)
➤ Xét về tính kim loại giảm dần: Na > Fe > Cu → Chọn đáp án A. ♥.
Câu 10 [13969]: Cho các chất: glixerol, natri panmitat, axit panmitic, tripanmitin. Số chất không tan trong nước ở điều kiện thường là
A, 2.
B, 1.
C, 4.
D, 3.
HD: • các chất glixerol, natri panmitat tan tốt trong nước.
• axit panmitic ít tan còn tripanmitin không tan trong nước ||⇒ chọn B. ♦.
• axit panmitic ít tan còn tripanmitin không tan trong nước ||⇒ chọn B. ♦.
Câu 11 [981933]: Tơ nào sau đây là tơ nhân tạo?
A, Tơ visco.
B, Tơ capron.
C, Tơ nitron.
D, Tơ tằm.
HD: Bài học phân loại tơ:
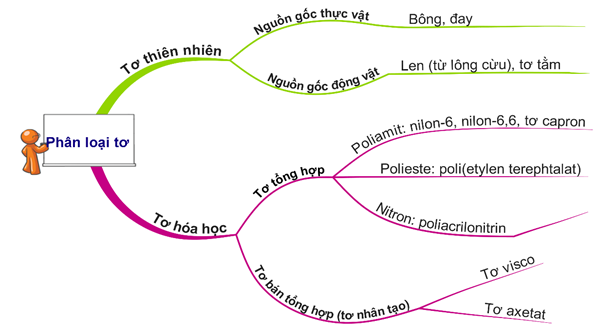
⇝ Tơ visco là tơ nhân tạo ⇝ Chọn đáp án A. ♥

⇝ Tơ visco là tơ nhân tạo ⇝ Chọn đáp án A. ♥
Câu 12 [679794]: Hiđroxit nào sau đây dễ tan trong nước ở điều kiện thường?
A, Al(OH)3.
B, Mg(OH)2.
C, Ba(OH)2.
D, Cu(OH)2.
HD: Các hiđroxit kim loại kiềm, và một số kim loại kiểm thổ như Ba, Sr Ca (Ca(OH)2 ít tan) đều dễ tan trong nước ⇝ Chọn đáp án C. ♣
Câu 13 [679551]: Cặp dung dịch chất nào sau đây phản ứng với nhau tạo ra chất khí?
A, NH4Cl và AgNO3.
B, NaOH và H2SO4.
C, Ba(OH)2 và NH4Cl .
D, Na2CO3 và KOH.
HD: Phân tích các đáp án:
❌ A. NH4Cl + AgNO3 → AgCl↓ + NH4NO3.
❌ B. 2NaOH + H2SO4 → Na2SO4 + 2H2O.
✔️ C. Ba(OH)2 + 2NH4Cl → BaCl2 + 2NH3↑ + 2H2O.
❌ D. Na2CO3 + KOH → không xảy ra phản ứng.
❌ A. NH4Cl + AgNO3 → AgCl↓ + NH4NO3.
❌ B. 2NaOH + H2SO4 → Na2SO4 + 2H2O.
✔️ C. Ba(OH)2 + 2NH4Cl → BaCl2 + 2NH3↑ + 2H2O.
❌ D. Na2CO3 + KOH → không xảy ra phản ứng.
Câu 14 [911599]: Thủy phân este X trong dung dịch NaOH, thu được CH3COONa và C2H5OH. Công thức cấu tạo của X là
A, C2H5COOCH3.
B, C2H5COOC2H5.
C, CH3COOCH3.
D, CH3COOC2H5.
HD: Từ sản phẩm ⇒ cấu tạo của este X là CH3COOC2H5 (etyl axetat).
CH3COOC2H5 + NaOH –––to–→ CH3COONa + C2H5OH.
CH3COOC2H5 + NaOH –––to–→ CH3COONa + C2H5OH.
Câu 15 [311747]: Vàng (Au) tồn tại trong thiên nhiên dưới dạng tự do nhưng quặng vàng thường rất nghèo. Người ta nghiền quặng trộn vào dung dịch KCN và sục khí O2 liên tục, vàng sẽ bị hòa tan thành phức chất, sau đó dùng kim loại X để đẩy vàng (Au) ra khỏi hợp chất. Kim loại X là
A, Ag.
B, Pt.
C, Zn.
D, Be.
HD: Theo quá trình trên:
• 4Au + 8KCN + O2 + 2H2O → 4K[Au(CN)2] + 4KOH.
Sau đó, dùng bột Zn đẩy Au ra khỏi hợp chất:
• Zn + K[Au(CN)2] → K2[Zn(CN)4] + 2Au. ❒
• 4Au + 8KCN + O2 + 2H2O → 4K[Au(CN)2] + 4KOH.
Sau đó, dùng bột Zn đẩy Au ra khỏi hợp chất:
• Zn + K[Au(CN)2] → K2[Zn(CN)4] + 2Au. ❒
Câu 16 [507943]: Nghiền nhỏ 1 gam CH3COONa cùng với 2 gam vôi tôi xút (CaO và NaOH) rồi cho vào đáy ống nghiệm. Đun nóng đều ống nghiệm, sau đó đun tập trung phần có chứa hỗn hợp phản ứng. Hiđrocacbon sinh ra trong thí nghiệm trên là
A, metan.
B, etan.
C, etilen.
D, axetilen.
HD: ► Phản ứng xảy ra gọi là phản ứng vôi tôi xút để điều chế metan (CH4):
CH3COONa + NaOH ––CaO, to→ CH4↑ + Na2CO3.
☆ Tổng quát: RCOONa + NaOH ––CaO, to→ RH↑ + Na2CO3.
Quan sát thí nghiệm trong PTN:
CH3COONa + NaOH ––CaO, to→ CH4↑ + Na2CO3.
☆ Tổng quát: RCOONa + NaOH ––CaO, to→ RH↑ + Na2CO3.
Quan sát thí nghiệm trong PTN:
Câu 17 [911592]: Cho 31,4 gam hỗn hợp gồm glyxin và alanin phản ứng vừa đủ với 400 ml dung dịch NaOH 1M. Cô cạn dung dịch sau phản ứng, thu được m gam muối khan. Giá trị của m là
A, 40,6.
B, 40,2.
C, 42,5.
D, 48,6.
HD: glyxin và alanin đều có dạng H2NRCOOH.
Phản ứng TQ: H2NRCOOH + NaOH → H2NRCOONa + H2O.
Giả thiết nNaOH = 0,4 mol ⇒ nH2O = 0,4 mol.
⇒ BTKL: 31,4 + 0,4 × 40 = m + 0,4 × 18 ⇒ m = 40,2 gam ⇝ Chọn đáp án B. ♦
Phản ứng TQ: H2NRCOOH + NaOH → H2NRCOONa + H2O.
Giả thiết nNaOH = 0,4 mol ⇒ nH2O = 0,4 mol.
⇒ BTKL: 31,4 + 0,4 × 40 = m + 0,4 × 18 ⇒ m = 40,2 gam ⇝ Chọn đáp án B. ♦
Câu 18 [679369]: Cho 0,9 gam glucozơ (C6H12O6) tác dụng hết với lượng dư dung dịch AgNO3 trong NH3, thu được m gam Ag. Giá trị của m là
A, 0,54.
B, 1,08.
C, 2,16.
D, 1,62.
HD: Glucozơ tham gia phản ứng tráng bạc theo tỉ lệ 1 ÷ 2: 1glucozơ  2Ag↓
2Ag↓
→ m = 0,9 ÷ 180 × 2 × 108 = 1,08 gam.
 2Ag↓
2Ag↓→ m = 0,9 ÷ 180 × 2 × 108 = 1,08 gam.
Câu 19 [679558]: Thí nghiệm nào sau đây thu được muối sắt(III) sau khi kết thúc phản ứng?
A, Cho Fe(OH)2 vào dung dịch H2SO4 loãng.
B, Cho Fe vào dung dịch HCl.
C, Cho Fe vào dung dịch CuSO4.
D, Đốt cháy Fe trong bình khí Cl2 dư.
HD: Phân tích các thí nghiệm:
❌ A. Fe(OH)2 + H2SO4 → FeSO4 (sắt(II) sunfat) + 2H2O.
❌ B. Fe + 2HCl → FeCl2 (sắt(II) clorua) + H2↑.
❌ C. Fe + CuSO4 → FeSO4 (sắt(II) sunfat) + Cu.
✔️ D. 2Fe + 3Cl2 ––to→ 2FeCl3 (sắt(III) clorua).
❌ A. Fe(OH)2 + H2SO4 → FeSO4 (sắt(II) sunfat) + 2H2O.
❌ B. Fe + 2HCl → FeCl2 (sắt(II) clorua) + H2↑.
❌ C. Fe + CuSO4 → FeSO4 (sắt(II) sunfat) + Cu.
✔️ D. 2Fe + 3Cl2 ––to→ 2FeCl3 (sắt(III) clorua).
Câu 20 [62593]: Cho dung dịch Na2CO3 vào dung dịch Ca(HCO3)2 thấy
A, có kết tủa trắng và bọt khí.
B, không có hiện tượng gì.
C, có kết tủa trắng.
D, có bọt khí thoát ra.
HD: Phản ứng xảy ra: Na2CO3 + Ca(HCO3)2 → CaCO3↓ + 2NaHCO3.
⇝ Hiện tượng: xuát hiện kết tủa trắng CaCO3↓. ❒
⇝ Hiện tượng: xuát hiện kết tủa trắng CaCO3↓. ❒
Câu 21 [118098]: Cho 0,46 gam kim loại Na tác dụng hết với H2O (dư), thu được x mol khí H2. Giá trị của x là
A, 0,04.
B, 0,02.
C, 0,01.
D, 0,03.
Giải: Ta có nNa = 0,02 mol.
●Cách 1: Truyền thống.
2Na + 2H2O → 2NaOH + H2
⇒ nH2 = 0,02 ÷ 2 = 0,01 mol ⇒ Chọn C
●Cách 2: Bảo toàn e.
1nNa = 2nH2 ⇒ nH2 = 0,02 ÷ 2 = 0,01 ⇒ Chọn C
●Cách 1: Truyền thống.
2Na + 2H2O → 2NaOH + H2
⇒ nH2 = 0,02 ÷ 2 = 0,01 mol ⇒ Chọn C
●Cách 2: Bảo toàn e.
1nNa = 2nH2 ⇒ nH2 = 0,02 ÷ 2 = 0,01 ⇒ Chọn C
Câu 22 [311938]: Thủy tinh hữu cơ plexiglas là loại chất dẻo rất bền, trong suốt, có khả năng cho gần 90% ánh sáng truyền qua nên được sử dụng làm kính ô tô, máy bay, kính xây dựng, kính bảo hiểm,.... Polime dùng để chế tạo thủy tinh hữu cơ là
A, poli(acrilonitrin).
B, poli(hexametylen ađipamit).
C, poli(etylen terephtalat).
D, poli(metyl metacrylat).
HD: Bài học về thủy tinh hữu cơ Plexiglas
![577847[LG].png](https://m.moon.vn/Images/Teachers/rongden_167/ProS2018/TAP%20II/577847[LG].png)
![577847[LG].png](https://m.moon.vn/Images/Teachers/rongden_167/ProS2018/TAP%20II/577847[LG].png)
Câu 23 [312129]: Trong điều kiện thường, X là chất rắn, dạng sợi màu trắng. Phân tử X có cấu trúc mạch không phân nhánh, không xoắn. Thủy phân X trong môi axit, thu được glucozơ. Tên gọi của X là
A, Fructozơ.
B, Amilopectin.
C, Xenlulozơ.
D, Saccarozơ.
HD: Xenlulozơ là chất rắn, dạng sợi màu trắng,
phân tử có cấu trúc mạch không phân nhánh, không xoắn
và thủy phân trong môi trường axit thu được glucozơ:
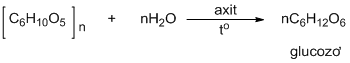
phân tử có cấu trúc mạch không phân nhánh, không xoắn
và thủy phân trong môi trường axit thu được glucozơ:
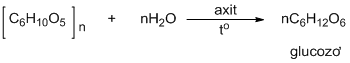
Câu 24 [679762]: Phát biểu nào sau đây đúng?
A, Alanin là hợp chất có tính lưỡng tính.
B, Gly-Ala có phản ứng màu biure.
C, Tripeptit mạch hở có ba liên kết peptit.
D, Đimetylamin là amin bậc ba.
HD: Phân tích các phát biểu:
✔️ A. đúng vì alanin: H2NCH(CH3)COOH là một amino axit ⇝ có tính lưỡng tính.
❌ B. sai vì các đipeptit không có phản ứng màu biure (từ tripeptit trở lên mới có).
❌ C. sai vì tripeptit dạng A–B–C chỉ có 2 liên kết peptit thôi (chính là cái gạch – ở giữa hai amino axit đó).
❌ D. sai vì đimetylamin: CH3NHCH3 là một amin bậc hai.
✔️ A. đúng vì alanin: H2NCH(CH3)COOH là một amino axit ⇝ có tính lưỡng tính.
❌ B. sai vì các đipeptit không có phản ứng màu biure (từ tripeptit trở lên mới có).
❌ C. sai vì tripeptit dạng A–B–C chỉ có 2 liên kết peptit thôi (chính là cái gạch – ở giữa hai amino axit đó).
❌ D. sai vì đimetylamin: CH3NHCH3 là một amin bậc hai.
Câu 25 [973559]: Cho 6,72 lít khí CO (đktc) phàn ứng với CuO nung nóng, thu được hỗn hợp khí có tỉ khối so với H2 bằng 18. Khối lượng CuO đã phản ứng là
A, 24 gam.
B, 8 gam.
C, 16 gam.
D, 12 gam.
HD: Sơ đồ: 
► “Tinh tế” xử lý: nhỗn hợp khí = nCO ban đầu = 0,3 mol
⇒ mO trong oxit = mhỗn hợp khí – mCO ban đầu.
Thay số ta có nO trong oxit = 0,3 × (18 × 2 – 28) ÷ 16 = 0,15 mol.
⇒ Tương ứng có 0,15 mol CuO ⇒ mCuO = 0,15 × 80 = 12 gam. ❒
► Xây công thức: nO trong oxit phản ứng = nCO × (Mhỗn hợp khí – 28) ÷ 16.

► “Tinh tế” xử lý: nhỗn hợp khí = nCO ban đầu = 0,3 mol
⇒ mO trong oxit = mhỗn hợp khí – mCO ban đầu.
Thay số ta có nO trong oxit = 0,3 × (18 × 2 – 28) ÷ 16 = 0,15 mol.
⇒ Tương ứng có 0,15 mol CuO ⇒ mCuO = 0,15 × 80 = 12 gam. ❒
► Xây công thức: nO trong oxit phản ứng = nCO × (Mhỗn hợp khí – 28) ÷ 16.
Câu 26 [679624]: Dẫn a mol hỗn hợp X (gồm hơi nước và khí CO2) qua cacbon nung đỏ, thu được 1,8a mol hỗn hợp khí Y gồm H2, CO và CO2. Cho Y đi qua ống đựng hỗn hợp gồm CuO và Fe2O3 (dư, nung nóng), sau khi các phản ứng xảy ra hoàn toàn, khối lượng chất rắn giảm 1,28 gam. Giá trị của a là
A, 0,10.
B, 0,04.
C, 0,05.
D, 0,08.
HD: Nhắc lại kiến thức và cách xử lý nhanh + tinh tế hệ khí than ướt:

⇒ nC = Δntăng = 1,8a – a = 0,8a mol.
⇒ nO trong oxit bị lấy = 2∑nC = 1,6a mol.
⇒ Δmrắn giảm = 1,28 = nO trong oxit bị lấy = 1,6a × 16 ⇒ a = 0,05 mol.

⇒ nC = Δntăng = 1,8a – a = 0,8a mol.
⇒ nO trong oxit bị lấy = 2∑nC = 1,6a mol.
⇒ Δmrắn giảm = 1,28 = nO trong oxit bị lấy = 1,6a × 16 ⇒ a = 0,05 mol.
Câu 27 [911527]: Cho kim loại M và các hợp chất X, Y, Z thỏa mãn các phương trình hóa học sau:
(a) 2M + 3Cl2 ––to→ 2MCl3;
(b) 2M + 6HCl → 2MCl3 + 3H2↑;
(c) 2M + 2X + 2H2O → 2Y + 3H2↑;
(d) Y + CO2 + 2H2O → Z + KHCO3.
Các chất X, Y, Z lần lượt là
(a) 2M + 3Cl2 ––to→ 2MCl3;
(b) 2M + 6HCl → 2MCl3 + 3H2↑;
(c) 2M + 2X + 2H2O → 2Y + 3H2↑;
(d) Y + CO2 + 2H2O → Z + KHCO3.
Các chất X, Y, Z lần lượt là
A, KOH, KAlO2, Al(OH)3.
B, NaOH, NaCrO2, Cr(OH)3.
C, NaOH, NaAlO2, Al(OH)3.
D, KOH, KCrO2, Cr(OH)3.
HD: Quan sát 4 đáp án và phân tích nhanh.
► Cr + 2HCl → CrCl2 + H2↑ nên M không thể là Cr ⇒ M là Al ⇝ loại đáp án B và D.
(a) 2Al + 3Cl2 ––to→ 2AlCl3.
(b) 2Al + 6HCl → 2AlCl3 + 3H2↑.
► Đơn giản khi thấy ở (d) có muối KHCO3 ⇒ Y là hợp chất của K ⇝ loại C. Theo đó các chất X, Y, Z lần lượt là KOH, KAlO2, Al(OH)3.
(c) 2Al + 2KOH + 2H2O → 2KAlO2 + 3H2↑.
(d) KAlO2 + CO2 + 2H2O → Al(OH)3↓ + KHCO3.
► Cr + 2HCl → CrCl2 + H2↑ nên M không thể là Cr ⇒ M là Al ⇝ loại đáp án B và D.
(a) 2Al + 3Cl2 ––to→ 2AlCl3.
(b) 2Al + 6HCl → 2AlCl3 + 3H2↑.
► Đơn giản khi thấy ở (d) có muối KHCO3 ⇒ Y là hợp chất của K ⇝ loại C. Theo đó các chất X, Y, Z lần lượt là KOH, KAlO2, Al(OH)3.
(c) 2Al + 2KOH + 2H2O → 2KAlO2 + 3H2↑.
(d) KAlO2 + CO2 + 2H2O → Al(OH)3↓ + KHCO3.
Câu 28 [309403]: Hỗn hợp X gồm H2, C2H2 và C2H4 có tỉ khối so với H2 là 3,5. Nung nóng X trong bình kín (với bột Ni xúc tác) một thời gian, thu được hỗn hợp khí Y có tỉ khối so với H2 bằng 5. Dẫn 2,24 lít X (đktc) vào dung dịch Br2 dư, thấy có m gam Br2 đã phản ứng. Biết các phản ứng đều xảy ra hoàn toàn. Giá trị của m là
A, 4,8.
B, 2,4.
C, 8,0.
D, 4,0.
HD: dX/H2 = 3,5 ⇒ MX = 7 ⇝ 0,1 mol X ⇄ 0,7 gam.
Trong bình kín: X → Y nên mY = mX = 0,7 gam.
Lại có dY/H2 = 5 ⇒ MY = 10 ⇝ nY = 0,7 ÷ 10 = 0,07 mol.
⇥ Δsố mol giảm = ∑nH2 phản ứng = nX – nY = 0,03 mol.
☆ Đọc kỹ quá trình và để ý các phản ứng xảy ra hoàn toàn
⇝ ∑nBr2 phản ứng = ∑nH2 phản ứng = 0,03 mol.
⇥ Yêu cầu, giá trị của m là m = 0,03 × 160 = 4,8 gam. ❒
Trong bình kín: X → Y nên mY = mX = 0,7 gam.
Lại có dY/H2 = 5 ⇒ MY = 10 ⇝ nY = 0,7 ÷ 10 = 0,07 mol.
⇥ Δsố mol giảm = ∑nH2 phản ứng = nX – nY = 0,03 mol.
☆ Đọc kỹ quá trình và để ý các phản ứng xảy ra hoàn toàn
⇝ ∑nBr2 phản ứng = ∑nH2 phản ứng = 0,03 mol.
⇥ Yêu cầu, giá trị của m là m = 0,03 × 160 = 4,8 gam. ❒
Câu 29 [167800]: Có hai dung dịch X và Y chứa các ion khác nhau. Mỗi dung dịch chứa đúng hai loại cation và hai loại anion trong số các ion sau:

Biết X hòa tan được Cu(OH)2. Khối lượng chất tan có trong Y gần nhất với giá trị nào sau đây?
Biết X hòa tan được Cu(OH)2. Khối lượng chất tan có trong Y gần nhất với giá trị nào sau đây?
A, 27,50 gam.
B, 30,50 gam.
C, 28,00 gam.
D, 31,00 gam.
+ H+ và Mg2+ cùng phản ứng với CO32- => H+ và Mg2+ không cùng tồn tại trong một dung dịch với CO32- => H+ và Mg2+ sẽ cùng nằm trong một dung dịch với 2 trong 3 anion SO42-, NO3-, Cl-.
+ Vì dung dịch X hoà tan được Cu(OH)2 nên X chứa H+.
+ Tổng điện tích dương của H+ và Mg2+ = 0,30.1 + 0,15.2 = 0,60 mol = 0,10.2 + 0,40.1 => dung dịch X sẽ chứa H+, Mg2+, Cl- và SO42-
+ Dung dịch Y sẽ chứa Na+, NH4+, NO3- và CO32-
Bảo toàn điện tích dung dịch Y: 0,20.1 + 0,25.1 = 0,25.1 + 0,10.2 => thoả mãn.
Vậy dung dịch X: H+, Mg2+, Cl- và SO42-; Dung dịch Y: Na+, NH4+, NO3- và CO32-
Khối lượng chất tan trong dung dịch Y = 0,20.23 + 0,25.18 + 0,25.62 + 0,10.60 = 30,6 gam.
Giá trị gần nhất với 30,6 là 30,5 gam.
+ Vì dung dịch X hoà tan được Cu(OH)2 nên X chứa H+.
+ Tổng điện tích dương của H+ và Mg2+ = 0,30.1 + 0,15.2 = 0,60 mol = 0,10.2 + 0,40.1 => dung dịch X sẽ chứa H+, Mg2+, Cl- và SO42-
+ Dung dịch Y sẽ chứa Na+, NH4+, NO3- và CO32-
Bảo toàn điện tích dung dịch Y: 0,20.1 + 0,25.1 = 0,25.1 + 0,10.2 => thoả mãn.
Vậy dung dịch X: H+, Mg2+, Cl- và SO42-; Dung dịch Y: Na+, NH4+, NO3- và CO32-
Khối lượng chất tan trong dung dịch Y = 0,20.23 + 0,25.18 + 0,25.62 + 0,10.60 = 30,6 gam.
Giá trị gần nhất với 30,6 là 30,5 gam.
Câu 30 [26082]: Cho các phát biểu sau:
(a) Phân tử lysin chứa số nguyên tử oxi bằng số nguyên tử nitơ.
(b) Hiđro hóa hoàn toàn triolein (Ni, to), thu được tristearin.
(c) Glucozơ còn gọi là đường nho do có nhiều trong quả nho chín.
(d) Tơ hóa học gồm hai nhóm: tơ tổng hợp và tơ nhân tạo.
(e) Phản ứng este hóa (H2SO4 đặc, to) xảy ra thuận nghịch.
Số phát biểu đúng là
(a) Phân tử lysin chứa số nguyên tử oxi bằng số nguyên tử nitơ.
(b) Hiđro hóa hoàn toàn triolein (Ni, to), thu được tristearin.
(c) Glucozơ còn gọi là đường nho do có nhiều trong quả nho chín.
(d) Tơ hóa học gồm hai nhóm: tơ tổng hợp và tơ nhân tạo.
(e) Phản ứng este hóa (H2SO4 đặc, to) xảy ra thuận nghịch.
Số phát biểu đúng là
A, 2.
B, 3.
C, 5.
D, 4.
HD: Phân tích các phát biểu:
✔️ (a) đúng vì lysin là (H2N)2C5H9COOH có số O = số N = 2.
✔️ (b) đúng: (C17H33COO)3C3H5 + 3H2 ––Ni, to→ (C17H35COO)3C3H5.
✔️ (c) đúng. glucozơ: đường nho; fructozơ: đường mật ong; saccarozơ: đường mía; mantozơ: đường mạch nha.
✔️ (d) đúng theo bài học phân loại tơ.
✔️ (e) đúng. Phản ứng: RCOOH + R'OH ⇄H2SO4, đặc⇄ RCOOR' + H2O.
⇝ tất cả 5/5 phát biểu đều đúng ⇝ Chọn đáp án C. ♣
✔️ (a) đúng vì lysin là (H2N)2C5H9COOH có số O = số N = 2.
✔️ (b) đúng: (C17H33COO)3C3H5 + 3H2 ––Ni, to→ (C17H35COO)3C3H5.
✔️ (c) đúng. glucozơ: đường nho; fructozơ: đường mật ong; saccarozơ: đường mía; mantozơ: đường mạch nha.
✔️ (d) đúng theo bài học phân loại tơ.
✔️ (e) đúng. Phản ứng: RCOOH + R'OH ⇄H2SO4, đặc⇄ RCOOR' + H2O.
⇝ tất cả 5/5 phát biểu đều đúng ⇝ Chọn đáp án C. ♣
Câu 31 [679727]: Đốt cháy hoàn toàn m gam triglixerit cần vừa đủ 3,08 mol O2, thu được CO2 và 2 mol H2O. Cho m gam X tác dụng với dung dịch NaOH vừa đủ, thu được glixerol và 35,36 gam muối. Mặt khác, m gam X tác dụng được tối đa với a mol Br2 trong dung dịch. Giá trị của a là
A, 0,12.
B, 0,10.
C, 0,04.
D, 0,06.
HD: ► Mẹo: tripanmitin: C51H98O6; tristearin: C57H110O6.
⇒ 98 ≤ số H ≤ 110; có 2,0 mol H2O nên để số mol X tròn đẹp thì số HX = 100 ⇒ nX = 0,04 mol.
☆ Giải thuỷ phân 0,04 mol X + 0,12 mol NaOH → 35,36 gam muối + 0,04 mol C3H5(OH)3.
⇒ mX = 34,24 gam ⇒ MX = 856 ⇝ tương ứng là X là C55H100O6.
X có 3πC=C ⇒ a = nBr2 phản ứng = 3nX = 0,04 × 3 = 0,12 ⇝ Chọn đáp án A. ♥
☆ Cách bình thường: đặt nX = b mol; bảo toàn khối lượng thuỷ phân ta có:
mX = 35,36 + 92b – 120b = (35,36 – 28b) gam.
Giải đốt b mol C?H??O6 + 3,08 gam O2 → ? mol CO2 + 2 mol H2O.
bảo toàn O ta có nCO2 = (3b + 3,08 – 1,0) = (3b + 2,08) mol.
⇒ mX = 12 × (3b + 2,08) + 2,0 × 2 + 16 × 6b = 35,36 – 28b ⇒ b = 0,04 mol.
Giải ra công thức X là C55H100O6 với số mol 0,04 ⇒ a = 0,12 mol tương tự trên.
⇒ 98 ≤ số H ≤ 110; có 2,0 mol H2O nên để số mol X tròn đẹp thì số HX = 100 ⇒ nX = 0,04 mol.
☆ Giải thuỷ phân 0,04 mol X + 0,12 mol NaOH → 35,36 gam muối + 0,04 mol C3H5(OH)3.
⇒ mX = 34,24 gam ⇒ MX = 856 ⇝ tương ứng là X là C55H100O6.
X có 3πC=C ⇒ a = nBr2 phản ứng = 3nX = 0,04 × 3 = 0,12 ⇝ Chọn đáp án A. ♥
☆ Cách bình thường: đặt nX = b mol; bảo toàn khối lượng thuỷ phân ta có:
mX = 35,36 + 92b – 120b = (35,36 – 28b) gam.
Giải đốt b mol C?H??O6 + 3,08 gam O2 → ? mol CO2 + 2 mol H2O.
bảo toàn O ta có nCO2 = (3b + 3,08 – 1,0) = (3b + 2,08) mol.
⇒ mX = 12 × (3b + 2,08) + 2,0 × 2 + 16 × 6b = 35,36 – 28b ⇒ b = 0,04 mol.
Giải ra công thức X là C55H100O6 với số mol 0,04 ⇒ a = 0,12 mol tương tự trên.
Câu 32 [906850]: Thực hiện các thí nghiệm sau:
(a) Cho hỗn hợp Na2O và Al2O3 (tỉ lệ mol 1 : 1) vào nước (dư).
(b) Cho hỗn hợp Cu và Fe3O4 (tỉ lệ mol tương ứng 2 : 1) vào dung dịch HCl (dư).
(c) Cho hỗn hợp Ba và NaHCO3 (tỉ lệ mol 1 : 1) vào nước (dư).
(d) Cho hỗn hợp Cu và NaNO3 (tỉ lệ mol tương ứng 1 : 2) vào dung dịch HCl (dư).
(e) Cho hỗn hợp BaCO3 và KHSO4 vào nước (dư).
Khi phản ứng trong các thí nghiệm trên kết thúc, có bao nhiêu thí nghiệm không thu được chất rắn?
(a) Cho hỗn hợp Na2O và Al2O3 (tỉ lệ mol 1 : 1) vào nước (dư).
(b) Cho hỗn hợp Cu và Fe3O4 (tỉ lệ mol tương ứng 2 : 1) vào dung dịch HCl (dư).
(c) Cho hỗn hợp Ba và NaHCO3 (tỉ lệ mol 1 : 1) vào nước (dư).
(d) Cho hỗn hợp Cu và NaNO3 (tỉ lệ mol tương ứng 1 : 2) vào dung dịch HCl (dư).
(e) Cho hỗn hợp BaCO3 và KHSO4 vào nước (dư).
Khi phản ứng trong các thí nghiệm trên kết thúc, có bao nhiêu thí nghiệm không thu được chất rắn?
A, 1.
B, 2.
C, 3.
D, 4.
(a) 1 mol Na2O tạo thành 2 mol NaOH sau đó hòa tan tối đa 1 mol Al2O3 tạo dung dịch trong suốt.
Na2O + Al2O3 → 2NaAlO2
(b) Cu + Fe3O4 + 8HCl → CuCl2 + 3FeCl2 + 4H2O
Cu vẫn còn dư.
(c) Hòa tan Ba vào dung dịch NaHCO3 thu được kết tủa BaCO3.
Ba + 2H2O → Ba(OH)2 + H2
Ba(OH)2 + NaHCO3 → BaCO3 + NaOH + H2O
(d) 3Cu + 8H+ + 2NO3 → 3Cu2+ + 2NO + 4H2O
(e) Cho hỗn hợp BaCO3 và KHSO4 vào nước thu được kết tủa BaSO4.
BaCO3 + 2KHSO4 → BaSO4 + K2SO4 + CO2 + H2O
Na2O + Al2O3 → 2NaAlO2
(b) Cu + Fe3O4 + 8HCl → CuCl2 + 3FeCl2 + 4H2O
Cu vẫn còn dư.
(c) Hòa tan Ba vào dung dịch NaHCO3 thu được kết tủa BaCO3.
Ba + 2H2O → Ba(OH)2 + H2
Ba(OH)2 + NaHCO3 → BaCO3 + NaOH + H2O
(d) 3Cu + 8H+ + 2NO3 → 3Cu2+ + 2NO + 4H2O
(e) Cho hỗn hợp BaCO3 và KHSO4 vào nước thu được kết tủa BaSO4.
BaCO3 + 2KHSO4 → BaSO4 + K2SO4 + CO2 + H2O
Câu 33 [312119]: Từ hợp chất hữu cơ X (C6H10O4, mạch hở), thực hiện các phản ứng sau (xảy ra theo đúng tỉ lệ số mol):
(a) X + 2NaOH X1 + X2 + X3
X1 + X2 + X3
(b) 2X1 + H2SO4 (loãng, dư) X4 + Na2SO4
X4 + Na2SO4
(c) X4 + 2AgNO3 + 3NH3 + H2O X5 + 2Ag + 2NH4NO3
X5 + 2Ag + 2NH4NO3
(d) 2X2 + Cu(OH)2 X6 + 2H2O
X6 + 2H2O
(e) X3 + NaOH CH4 + Na2CO3
CH4 + Na2CO3
Công thức cấu tạo của X là
(a) X + 2NaOH
 X1 + X2 + X3
X1 + X2 + X3
(b) 2X1 + H2SO4 (loãng, dư)
 X4 + Na2SO4
X4 + Na2SO4
(c) X4 + 2AgNO3 + 3NH3 + H2O
 X5 + 2Ag + 2NH4NO3
X5 + 2Ag + 2NH4NO3
(d) 2X2 + Cu(OH)2
 X6 + 2H2O
X6 + 2H2O
(e) X3 + NaOH
 CH4 + Na2CO3
CH4 + Na2CO3
Công thức cấu tạo của X là
A, HCOOCH2CH2OOCCH2CH3.
B, HCOOCH2CH(CH3)OOCCH3.
C, HCOOCH2CH2CH2OOCCH3.
D, CH3OOCH2CH2OOCCH3.
HD: Các phản ứng xảy ra theo đúng tỉ lệ số mol nên:
Từ (e) ⇝ X3 là CH3COONa; từ (b) ⇝ X1 là muối.
Theo đó, X2 là ancol, từ (d) ⇒ X2 là ancol đa chức.
Lại để ý: X1 → X4 có phản ứng tráng bạc ⇒ X4 là HCOOH.
☆ Phân tích X có 6C; 4O nên ancol có 3C và 2 chức.
để (d) xảy ra thì 2 nhóm chức OH của X2 phải liền kề
⇝ cấu tạo của X2 là CH3CH(OH)CH2OH.
⇥ Cấu tạo của X là HCOOCH2CH(CH3)OOCCH3
và một đồng phân nữa là CH3COOCH2CH(CH3)OOCCH. ❒
Từ (e) ⇝ X3 là CH3COONa; từ (b) ⇝ X1 là muối.
Theo đó, X2 là ancol, từ (d) ⇒ X2 là ancol đa chức.
Lại để ý: X1 → X4 có phản ứng tráng bạc ⇒ X4 là HCOOH.
☆ Phân tích X có 6C; 4O nên ancol có 3C và 2 chức.
để (d) xảy ra thì 2 nhóm chức OH của X2 phải liền kề
⇝ cấu tạo của X2 là CH3CH(OH)CH2OH.
⇥ Cấu tạo của X là HCOOCH2CH(CH3)OOCCH3
và một đồng phân nữa là CH3COOCH2CH(CH3)OOCCH. ❒
Câu 34 [602412]: Tiến hành các bước thí nghiệm như sau:
Bước 1: Cho một nhúm bông vào cốc đựng dung dịch H2SO4 70%, đun nóng đồng thời khuấy đều đến khi thu được dung dịch đồng nhất.
Bước 2: Trung hòa dung dịch thu được bằng dung dịch NaOH 10%.
Bước 3: Lấy dung dịch sau khi trung hòa cho vào ống nghiệm đựng dung dịch AgNO3 trong
NH3 dư, đun nóng trên ngọn lửa đèn cồn.
Cho các phát biểu sau:
(a) Sau bước 1, trong cốc thu được một loại monosaccarit.
(b) Sau bước 3, trên thành ống nghiệm xuất hiện lớp kim loại màu trắng bạc.
(c) Trong bước 2, có thể thay dung dịch NaOH 10% bằng dung dịch KOH 14%.
(d) Trong bước 3, có thể thay việc đun trên ngọn lửa đèn cồn bằng cách ngâm trong cốc nước nóng.
(e) Thí nghiệm trên dùng để chứng minh xenlulozơ có chứa nhiều nhóm -OH.
(g) Dung dịch thu được sau bước 3 có chứa axit gluconic.
Số phát biểu sai là
Bước 1: Cho một nhúm bông vào cốc đựng dung dịch H2SO4 70%, đun nóng đồng thời khuấy đều đến khi thu được dung dịch đồng nhất.
Bước 2: Trung hòa dung dịch thu được bằng dung dịch NaOH 10%.
Bước 3: Lấy dung dịch sau khi trung hòa cho vào ống nghiệm đựng dung dịch AgNO3 trong
NH3 dư, đun nóng trên ngọn lửa đèn cồn.
Cho các phát biểu sau:
(a) Sau bước 1, trong cốc thu được một loại monosaccarit.
(b) Sau bước 3, trên thành ống nghiệm xuất hiện lớp kim loại màu trắng bạc.
(c) Trong bước 2, có thể thay dung dịch NaOH 10% bằng dung dịch KOH 14%.
(d) Trong bước 3, có thể thay việc đun trên ngọn lửa đèn cồn bằng cách ngâm trong cốc nước nóng.
(e) Thí nghiệm trên dùng để chứng minh xenlulozơ có chứa nhiều nhóm -OH.
(g) Dung dịch thu được sau bước 3 có chứa axit gluconic.
Số phát biểu sai là
A, 1.
B, 4.
C, 2.
D, 3.
Hướng dẫn giải
(a) đúng đó là glucozơ
(b) đúng: glucozơ có phản ứng tráng bạc
(c) đúng: chỉ cần trung hòa axit trong dung dịch
(d) đúng
(e) sai: để chứng minh xenlulozơ có phản ứng thủy phân
(f) sai: chứa muối amoni gluconat
(a) đúng đó là glucozơ
(b) đúng: glucozơ có phản ứng tráng bạc
(c) đúng: chỉ cần trung hòa axit trong dung dịch
(d) đúng
(e) sai: để chứng minh xenlulozơ có phản ứng thủy phân
(f) sai: chứa muối amoni gluconat
Câu 35 [679628]: Hòa tan hỗn hợp gồm CuSO4 và NaCl vào nước thu được dung dịch X. Tiến hành điện phân X với điện cực trơ, màng ngăn xốp, dòng điện có cường độ không đổi. Tổng số mol khí thu được ở cả hai điện cực (n) phụ thuộc vào thời gian điện phân (t) được mô tả như đồ thị dưới(đồ thị gấp khúc tại các điểm M, N):

Giả thiết hiệu suất điện phân là 100%, bỏ qua sự bay hơi của nước. Giá trị của m là

Giả thiết hiệu suất điện phân là 100%, bỏ qua sự bay hơi của nước. Giá trị của m là
A, 5,54.
B, 8,74.
C, 11,94.
D, 10,77.
HD: Giải theo hai cách:
☆ Cách 1: Quan sát đồ thị dốc lên – thoải xuống – lại dốc lên nên đồ thị biểu diễn quá trình TH1. Khi đó tại M ứng với a (giây) và khí ra là 0,02 mol Cl2 ⇒ ne trao đổi (M) = 0,02 × 2 = 0,04 mol.
Tại điểm P ứng với thời gian 4a (giây) thì ne trao đổi (P) = 0,04 × 4 = 0,16 mol và khí thoát ra bên anot là 0,02 mol Cl2 + ? mol O2 ⇒ có ngay ? = (0,16 – 0,02 × 2) ÷ 4 = 0,03 mol.
Mà tổng khí thoát ra ở cả 2 điện cực là 0,07 mol ⇒ bên catot thoát ra 0,02 mol H2 nữa.
Cũng từ mol e trao đổi là 0,16 ⇒ tổng số mol Cu là 0,06 mol.
Vậy, m gam hỗn hợp ban đầu gồm 0,06 mol CuSO4 và 0,04 mol NaCl ⇒ m = 11,94 gam.
☆ Cách 2: Sử dụng tỉ lệ đồ thị, chọn I = 96500.

Ta có ngay OH = MH ⇒ a = 0,02. Đặt IN = b, ta có IM = 2IN = 2b. Theo đó :
NK = 4a – IM – OH = 0,06 – 2b và PK = 0,07 – IN – MH = 0,05 – b.
Lại có PK = 1,5NK ⇒ tương ứng: 0,05 – b = 1,5 × (0,06 – 2b) ⇒ b = 0,02.
⇒ Tại N dung dịch ra : 0,02 mol CuCl2 và 0,04 mol CuO ⇒ ∑nCu = 0,06 mol.
Vậy, m gam hỗn hợp ban đầu gồm 0,06 mol CuSO4 và 0,04 mol NaCl ⇒ m = 11,94 gam.
☆ Cách 1: Quan sát đồ thị dốc lên – thoải xuống – lại dốc lên nên đồ thị biểu diễn quá trình TH1. Khi đó tại M ứng với a (giây) và khí ra là 0,02 mol Cl2 ⇒ ne trao đổi (M) = 0,02 × 2 = 0,04 mol.
Tại điểm P ứng với thời gian 4a (giây) thì ne trao đổi (P) = 0,04 × 4 = 0,16 mol và khí thoát ra bên anot là 0,02 mol Cl2 + ? mol O2 ⇒ có ngay ? = (0,16 – 0,02 × 2) ÷ 4 = 0,03 mol.
Mà tổng khí thoát ra ở cả 2 điện cực là 0,07 mol ⇒ bên catot thoát ra 0,02 mol H2 nữa.
Cũng từ mol e trao đổi là 0,16 ⇒ tổng số mol Cu là 0,06 mol.
Vậy, m gam hỗn hợp ban đầu gồm 0,06 mol CuSO4 và 0,04 mol NaCl ⇒ m = 11,94 gam.
☆ Cách 2: Sử dụng tỉ lệ đồ thị, chọn I = 96500.

Ta có ngay OH = MH ⇒ a = 0,02. Đặt IN = b, ta có IM = 2IN = 2b. Theo đó :
NK = 4a – IM – OH = 0,06 – 2b và PK = 0,07 – IN – MH = 0,05 – b.
Lại có PK = 1,5NK ⇒ tương ứng: 0,05 – b = 1,5 × (0,06 – 2b) ⇒ b = 0,02.
⇒ Tại N dung dịch ra : 0,02 mol CuCl2 và 0,04 mol CuO ⇒ ∑nCu = 0,06 mol.
Vậy, m gam hỗn hợp ban đầu gồm 0,06 mol CuSO4 và 0,04 mol NaCl ⇒ m = 11,94 gam.
Câu 36 [120242]: Hấp thụ hoàn toàn 896 mL khí CO2 (đktc) vào dung dịch gồm 0,02 mol Na2CO3 và y mol NaOH, thu được dung dịch T. Cho dung dịch BaCl2 dư vào T, thu được 11,82 gam kết tủa. Nếu cho từ từ dung dịch HCl 2M vào T, đến khi bắt đầu có khí thoát ra thì vừa hết 40 mL. Giá trị của y là
A, 0,12.
B, 0,10.
C, 0,08.
D, 0,14.
HD: 11,82 gam kết tủa là 0,06 mol BaCO3 ⇒ ∑nCO32– trong T = 0,06 mol.
Lại có ∑nC trong T = nCO2 + nNa2CO3 = 0,04 + 0,02 = 0,06 mol.
Nghĩa là T chứa 0,06 mol CO32– và còn lại là OH– còn dư.
chính vì thế mà khi thêm từ từ 0,08 mol HCl vào thì xảy ra:
OH– + H+ → H2O || CO32– + H+ → HCO3–
sau đó, nếu thêm tiếp H+ thì mới xảy ra H+ + HCO3– → CO2↑ + H2O.
⇒ nOH– = 0,08 – 0,06 = 0,02 mol ⇒ ∑nNa+ trong T = 0,02 + 0,06 × 2 = 0,14 mol.
⇒ bảo toàn nguyên tố Na ta có: y = 0,14 – 0,02 × 2 = 0,1 mol ❒.
Lại có ∑nC trong T = nCO2 + nNa2CO3 = 0,04 + 0,02 = 0,06 mol.
Nghĩa là T chứa 0,06 mol CO32– và còn lại là OH– còn dư.
chính vì thế mà khi thêm từ từ 0,08 mol HCl vào thì xảy ra:
OH– + H+ → H2O || CO32– + H+ → HCO3–
sau đó, nếu thêm tiếp H+ thì mới xảy ra H+ + HCO3– → CO2↑ + H2O.
⇒ nOH– = 0,08 – 0,06 = 0,02 mol ⇒ ∑nNa+ trong T = 0,02 + 0,06 × 2 = 0,14 mol.
⇒ bảo toàn nguyên tố Na ta có: y = 0,14 – 0,02 × 2 = 0,1 mol ❒.
Câu 37 [311926]: Hỗn hợp X gồm HCHO; CH3COOH; HCOOCH3 và CH3CH(OH)COOH. Đốt cháy hoàn toàn hỗn hợp X cần dùng V lít O2 (đktc) sau phản ứng thu được H2O và 0,15 mol CO2. Giá trị của V là
A, 3,92.
B, 3,36.
C, 4,20.
D, 2,80.
HD: Bài tập thuần đốt cháy các hợp chất hữu cơ
⇝ Quan sát CTPT các chất trong X ⇥ tìm ra quy luật và giải.
Xem nào: đơn giản nhất là CH2O; phức tạp nhất là C3H6O3 = 3(CH2O).
Hai chất còn lại có cùng CTPT là C2H4O2 cũng cùng dạng 2(CH2O).
⇝ Quy về đốt X có dạng đơn giản nhất là CH2O.
Thấy ngay: nCO2 = nH2O = 0,15 mol ⇒ X: 0,15 mol CH2O.
☆ Đốt 0,15 mol CH2O + ? mol O2 ––to→ CO2 + H2O.
"Tinh ý": O2 dùng để đốt 0,15 mol C ⇒ nO2 = 0,15 mol → V = 3,36 lít. ❒
⇝ Quan sát CTPT các chất trong X ⇥ tìm ra quy luật và giải.
Xem nào: đơn giản nhất là CH2O; phức tạp nhất là C3H6O3 = 3(CH2O).
Hai chất còn lại có cùng CTPT là C2H4O2 cũng cùng dạng 2(CH2O).
⇝ Quy về đốt X có dạng đơn giản nhất là CH2O.
Thấy ngay: nCO2 = nH2O = 0,15 mol ⇒ X: 0,15 mol CH2O.
☆ Đốt 0,15 mol CH2O + ? mol O2 ––to→ CO2 + H2O.
"Tinh ý": O2 dùng để đốt 0,15 mol C ⇒ nO2 = 0,15 mol → V = 3,36 lít. ❒
Câu 38 [133347]: Cho 23,34 gam hỗn hợp gồm Al, Al2O3 và Al(NO3)3 (trong đó oxi chiếm 34,961% về khối lượng) vào dung dịch chứa 1,58 mol NaHSO4 và 0,04 mol NaNO3, khuấy đều cho các phản ứng xảy ra hoàn toàn, thu được dung dịch Y chỉ chứa các muối trung hòa và 0,18 mol hỗn hợp khí Z gồm N2O; N2 và H2. Để tác dụng tối đa các chất tan có trong dung dịch Y cần dùng dung dịch chứa 2,04 mol NaOH. Phần trăm khối lượng của N2 có trong hỗn hợp khí Z là có giá trị gần nhất với
A, 20.
B, 26.
C, 22.
D, 24
HD: Sơ đồ quá trình:

☆ YTHH 02: với 2,04 mol NaOH và 1,62 mol Na sẵn có ⇄ ∑nNa+ = 3,66 mol sẽ đi về đâu?
À, là 1,58 mol Na2SO4 và còn lại là 0,5 mol NaAlO2 ||→ đọc ra có 0,5 mol Al.
Bảo toàn điện tích trong dung dịch Y có nNH4+ = 0,04 mol.
Giả thiết cho %mO ||→ nO trong hh đầu = 0,51 mol ||→ nN trong hh đầu = 0,12 mol.
☆ Đừng vội lao vào đặt hệ x; y; z và giải. Số mol, hỗn hợp → YTHH 01: tinh tế sử dụng:
Xem nào: bảo toàn N có nN2 trong (N2O; N2) = 0,06 mol ||→ nH2 trong Z = 0,12 mol.
⇒ bảo toàn H có nH2O = 0,59 mol ||→ bảo toàn O có nN2O = 0,04 mol
|⇝ quay lại tính được nN2 = 0,02 mol ||→ yêu cầu %mN2 trong Z = 21,875%. ❒

☆ YTHH 02: với 2,04 mol NaOH và 1,62 mol Na sẵn có ⇄ ∑nNa+ = 3,66 mol sẽ đi về đâu?
À, là 1,58 mol Na2SO4 và còn lại là 0,5 mol NaAlO2 ||→ đọc ra có 0,5 mol Al.
Bảo toàn điện tích trong dung dịch Y có nNH4+ = 0,04 mol.
Giả thiết cho %mO ||→ nO trong hh đầu = 0,51 mol ||→ nN trong hh đầu = 0,12 mol.
☆ Đừng vội lao vào đặt hệ x; y; z và giải. Số mol, hỗn hợp → YTHH 01: tinh tế sử dụng:
Xem nào: bảo toàn N có nN2 trong (N2O; N2) = 0,06 mol ||→ nH2 trong Z = 0,12 mol.
⇒ bảo toàn H có nH2O = 0,59 mol ||→ bảo toàn O có nN2O = 0,04 mol
|⇝ quay lại tính được nN2 = 0,02 mol ||→ yêu cầu %mN2 trong Z = 21,875%. ❒
Câu 39 [133774]: Hòa tan hết a gam hỗn hợp X gồm FeO, Fe2O3 và Fe3O4 vào dung dịch HCl dư, thu được dung dịch Y có số mol FeCl2 gấp đôi FeCl3. Cho b gam hỗn hợp Mg và Fe (Mg chiếm 30% khối lượng) tan hoàn toàn vào Y, thu được a mol khí H2. Biết rằng có một phần nguyên tử hiđro vừa sinh ra (chưa kịp kết hợp với nhau thành phân tử) đã khử toàn bộ Fe(III) thành Fe(II) theo phương trình: FeCl3 + H → FeCl2 + HCl. Mặt khác, nếu khử hoàn toàn a gam X cần vừa đủ a mol H2 khi nung nóng. Tỉ lệ a : b tương ứng là
A, 3 : 2.
B, 7 : 3.
C, 7 : 5.
D, 3 : 1.
Đáp án: C
Câu 40 [982258]: Hỗn hợp T gồm ba este mạch hở X (đơn chức), Y (hai chức), Z (ba chức) đều được tạo thành từ axit cacboxylic và ancol. Đốt cháy hoàn toàn m gam T, thu được H2O và 1,0 mol CO2. Xà phòng hóa hoàn toàn m gam T bằng dung dịch NaOH vừa đủ, thu được hỗn hợp E gồm hai ancol (có cùng số nguyên tử cacbon trong phân tử) và 26,96 gam hỗn hợp muối F. Cho E tác dụng hết với kim loại Na dư, thu được 0,2 mol H2. Đốt cháy toàn bộ F, thu được H2O, Na2CO3 và 0,2 mol CO2. Khối lượng của Y trong m gam T là
A, 2,92 gam.
B, 5,92 gam.
C, 2,36 gam.
D, 3,65 gam.
HD: Xâu chuối "chức" phản ứng: este –COO– + NaOH → –COONa (muối) + –OH (ancol).
Sau đó ancol: –OH + Na → –ONa + ½.H2↑.
⇒ Từ nH2↑ = 0,2 mol ⇒ ∑n–OH = 0,4 mol ⇒ nNaOH = 0,4 mol.
Bảo toàn nguyên tố Na ⇒ đốt muối thu được 0,2 mol Na2CO3.
Bảo toàn cacbon từ đốt este, đốt muối ⇒ đốt ancol thu được 1,0 – 0,2 – 0,2 = 0,6 mol CO2.
► "điểm đặc biệt" trong muối số C = số Na, mà Na chỉ ở trong COONa
⇒ Muối chỉ có thể là HCOONa và (COONa)2.
⇒ Giải hệ số mol có 0,16 mol HCOONa và 0,12 mol (COONa)2.
☆ Khó nhất của bài toán chính là việc xác định ancol.!
Có este đơn chức nên chắc chắc có một ancol đơn chức, có este 3 chức nên ancol còn lại là 3 chức, hoặc 2 chức (không thể 4 chức trở lên được).
• TH1: cặp ancol là đơn chức và ba chức ⇒ X là HCOOR; Y là (COOR)2 và Z là (HCOO)3R'.
⇒ nY = 0,16 mol; nX + 3nZ = 0,12 mol.
⇒ ∑nancol = nX + 2nY + nZ > (1/3.nX + nZ) + 2nY = 0,36.
⇒ số Cancol < 0,6 ÷ 0,36 = 1,67 → không có ancol thoả mãn.
• TH2: cặp ancol đơn chức và hai chức: ∑nOH = 0,4 mol; ∑nC = 0,6 mol.
⇒ Chặn khoảng: 0,6 ÷ 0,4 < số C < 0,6 ÷ (0,4 ÷ 2) ⇒ 1,5 < số C < 3 ⇒ số C = 2.
⇒ Giải hệ mol hai ancol tương ứng là 0,2 mol C2H5OH và 0,1 mol C2H4(OH)2.
Ghép tạo este: X chỉ có thể là HCOOC2H5; Z chỉ có thể là HCOOCH2CH2OOC–COOC2H5.
Còn Y có thể là (COOC2H5)2 hoặc (HCOO)2C2H4.
Lập hệ giải số mol X, Y, Z ứng với hai TH của Y thấy ứng với Y là (HCOO)2C2H4 không thoả mãn.
Còn với Y là (COOC2H5)2 thì giải ra: nZ = 0,1 mol; nX = 0,06 mol và nY = 0,02 mol.
⇝ Yêu cầu mY/T = 0,02 × 146 = 2,92 gam.
Sau đó ancol: –OH + Na → –ONa + ½.H2↑.
⇒ Từ nH2↑ = 0,2 mol ⇒ ∑n–OH = 0,4 mol ⇒ nNaOH = 0,4 mol.
Bảo toàn nguyên tố Na ⇒ đốt muối thu được 0,2 mol Na2CO3.
Bảo toàn cacbon từ đốt este, đốt muối ⇒ đốt ancol thu được 1,0 – 0,2 – 0,2 = 0,6 mol CO2.
► "điểm đặc biệt" trong muối số C = số Na, mà Na chỉ ở trong COONa
⇒ Muối chỉ có thể là HCOONa và (COONa)2.
⇒ Giải hệ số mol có 0,16 mol HCOONa và 0,12 mol (COONa)2.
☆ Khó nhất của bài toán chính là việc xác định ancol.!
Có este đơn chức nên chắc chắc có một ancol đơn chức, có este 3 chức nên ancol còn lại là 3 chức, hoặc 2 chức (không thể 4 chức trở lên được).
• TH1: cặp ancol là đơn chức và ba chức ⇒ X là HCOOR; Y là (COOR)2 và Z là (HCOO)3R'.
⇒ nY = 0,16 mol; nX + 3nZ = 0,12 mol.
⇒ ∑nancol = nX + 2nY + nZ > (1/3.nX + nZ) + 2nY = 0,36.
⇒ số Cancol < 0,6 ÷ 0,36 = 1,67 → không có ancol thoả mãn.
• TH2: cặp ancol đơn chức và hai chức: ∑nOH = 0,4 mol; ∑nC = 0,6 mol.
⇒ Chặn khoảng: 0,6 ÷ 0,4 < số C < 0,6 ÷ (0,4 ÷ 2) ⇒ 1,5 < số C < 3 ⇒ số C = 2.
⇒ Giải hệ mol hai ancol tương ứng là 0,2 mol C2H5OH và 0,1 mol C2H4(OH)2.
Ghép tạo este: X chỉ có thể là HCOOC2H5; Z chỉ có thể là HCOOCH2CH2OOC–COOC2H5.
Còn Y có thể là (COOC2H5)2 hoặc (HCOO)2C2H4.
Lập hệ giải số mol X, Y, Z ứng với hai TH của Y thấy ứng với Y là (HCOO)2C2H4 không thoả mãn.
Còn với Y là (COOC2H5)2 thì giải ra: nZ = 0,1 mol; nX = 0,06 mol và nY = 0,02 mol.
⇝ Yêu cầu mY/T = 0,02 × 146 = 2,92 gam.