Đáp án
1B
2B
3D
4C
5C
6B
7A
8A
9B
10D
11C
12B
13D
14D
15B
16D
17C
18C
19B
20C
21D
22B
23D
24A
25D
26A
27A
28C
29C
30B
31D
32B
33A
34C
35B
36D
37B
38D
39D
40A
Đáp án Đề minh họa số 7 thi Tốt Nghiệp Trung học Phổ Thông 2024 môn Hóa học
Câu 1 [982263]: Chất nào sau đây là chất béo?
A, Glixerol.
B, Tripanmitin.
C, Etyl axetat.
D, Tinh bột.
HD: Phân tích các đáp án:
| Hợp chất | Glixerol | Tripanmitin | Etyl axetat | Tinh bột |
| Cấu tạo | C3H5(OH)3 | (C15H31COO)3C3H5 | CH3COOC2H5 | (C6H10O5)n |
| Ancol (❌) | Chất béo (✔️) | Este (❌) | Cacbohiđrat (❌) |
Câu 2 [256260]: Tên gọi ứng với công thức cấu tạo thu gọn CH3CH2CH3 là
A, metan.
B, propan.
C, etan.
D, butan.
HD: Phân tích các đáp án:
| Tên gọi | A. metan. | B. propan. | C. etan. | D. butan. |
| Cấu tạo | CH4 | CH3CH2CH3 | CH3CH3 | CH3CH2CH2CH3 |
Câu 3 [982237]: Chất nào sau đây là muối axit?
A, NaNO3.
B, KCl.
C, K2SO4.
D, NaHSO4.
HD: Khái niệm: muối axit là loại muối có hidro trong gốc axit có khả năng phân tách ra H+.
trong 4 phương án, rõ ràng chỉ có D. NaHSO4 là có H.
Thêm nữa trong dung dịch: NaHSO4 → Na+ + H+ + SO42–.
⇝ Chọn đáp án D. ♠
trong 4 phương án, rõ ràng chỉ có D. NaHSO4 là có H.
Thêm nữa trong dung dịch: NaHSO4 → Na+ + H+ + SO42–.
⇝ Chọn đáp án D. ♠
Câu 4 [60182]: Chất làm mềm nước có tính cứng toàn phần là
A, CaSO4.
B, NaCl.
C, Na2CO3.
D, CaCO3.
HD: Bài học phân loại nước cứng:

⇒ Làm mềm nước cứng vĩnh cửu ta sử dụng Na2CO3 → 2Na+ + CO32–.
☆ Phản ứng tạo kết tủa: Ca2+ + CO32– → CaCO3↓.

⇒ Làm mềm nước cứng vĩnh cửu ta sử dụng Na2CO3 → 2Na+ + CO32–.
☆ Phản ứng tạo kết tủa: Ca2+ + CO32– → CaCO3↓.
Câu 5 [61753]: Công thức của muối có tên gọi magie photphua là
A, Mg3(PO4)2.
B, Mg3(PO3)2.
C, Mg3P2.
D, Mg2P2O7.
HD: Phân tích các đáp án:
| Công thức | Mg3(PO4)2 | Mg3(PO3)2 | Mg3P2 | Mg2P2O7 |
| Tên gọi | magie photphat | magie photphit | magie photphua | magie pyrophotphat |
| ❌ | ❌ | ✔️ | ❌ |
Câu 6 [679361]: Một trong những nguyên nhân gây tử vong trong nhiều vụ cháy là do nhiễm độc khí X. Khi vào cơ thể, khí X kết hợp với hemoglobin, làm giảm khả năng vận chuyển oxi của máu. Khí X là
A, N2.
B, CO.
C, He.
D, H2.
HD: Hemoglobin kết hợp với CO, làm giảm khả năng vận chuyển oxi ⇝ gây ngộ độc khí.


Câu 7 [679846]: Dung dịch KOH tác dụng với chất nào sau đây tạo ra kết tủa Fe(OH)3?
A, FeCl3.
B, FeO.
C, Fe2O3.
D, Fe3O4.
HD: Các oxit FeO; Fe2O3 và Fe3O4 đều không tác dụng với KOH.
Chỉ có FeCl3 phản ứng và tạo thành Fe(OH)3:
FeCl3 + 3KOH → Fe(OH)3↓ + 3NaCl.
Chỉ có FeCl3 phản ứng và tạo thành Fe(OH)3:
FeCl3 + 3KOH → Fe(OH)3↓ + 3NaCl.
Câu 8 [59722]: Kim loại nào sau đây có thể làm dao cắt được kính?
A, Cr.
B, Pb.
C, Cs.
D, Fe.
HD:
Cr là kim loại cứng nhất, có thể dùng làm dao cắt kính.
Cr là kim loại cứng nhất, có thể dùng làm dao cắt kính.
Câu 9 [911590]: Nguyên tố crom có số oxi hóa +6 trong hợp chất nào sau đây?
A, Cr(OH)3.
B, Na2CrO4.
C, Cr2O3.
D, NaCrO2.
HD: Phân tích các đáp án:
| Công thức | A. Cr(OH)3. | B. Na2CrO4. | C. Cr2O3. | D. NaCrO2. |
| Số oxi hoá của crom | +3 | +6 (✔️) | +3 | +3 |
Câu 10 [23913]: Ở cùng điều kiện, ion nào sau đây có tính oxi hóa mạnh nhất?
A, Fe2+.
B, Zn2+.
C, Ca2+.
D, Ag+.
HD: Thứ tự dãy điện hoá: 
☆ Ý nghĩa: tử số là dãy tăng dần tính oxi hoá ⇒ Ag+ là ion có tính oxi hoá mạnh nhất.

☆ Ý nghĩa: tử số là dãy tăng dần tính oxi hoá ⇒ Ag+ là ion có tính oxi hoá mạnh nhất.
Câu 11 [60264]: Hỗn hợp tecmit dùng để hàn đường ray có thành phần gồm bột nhôm và bột
A, natri oxit.
B, magie oxit.
C, sắt oxit.
D, đồng oxit.
HD: Hỗn hợp tecmit có thành phần gồm bột nhôm và bột sắt oxit.

☆ Xảy ra phản ứng: 2Al + Fe2O3 ––to→ Al2O3 + 2Fe.
⇝ Chọn đáp án C. ♣

☆ Xảy ra phản ứng: 2Al + Fe2O3 ––to→ Al2O3 + 2Fe.
⇝ Chọn đáp án C. ♣
Câu 12 [256985]: Chất nào sau đây thuộc loại hợp chất cacbohiđrat?
A, Glyxin.
B, Glucozơ.
C, Etylen glicol.
D, Glyxerin.
HD: Phân tích các đáp án:
| Hợp chất | Glyxin | Glucozơ | Etylen glicol | Glyxerin |
| Thuộc loại | amino axit | cacbohiđrat | ancol | ancol |
| ❌ | ✔️ | ❌ | ❌ |
Câu 13 [24622]: Phân tử khối của peptit Ala-Gly là
A, 164.
B, 160.
C, 132.
D, 146.
Giải: Ala – Gly = Gly + Ala – 1H2O ⇒ M = 75 + 89 – 18 = 146.
Câu 14 [59388]: Kim loại nào sau đây được tạo thành khi điện phân (với điện cực trơ) dung dịch muối sunfat tương ứng?
A, Na.
B, Al.
C, Mg.
D, Cu.
HD: Điện phân dung dịch không điều chế được các kim loại kiềm, kiềm thổ.
☆ Điều chế đồng (Cu): 2CuSO4 + 2H2O → 2Cu + 2H2SO4 + O2. ❒
☆ Điều chế đồng (Cu): 2CuSO4 + 2H2O → 2Cu + 2H2SO4 + O2. ❒
Câu 15 [906794]: Tro thực vật được sử dụng như một loại phân bón cung cấp nguyên tố kali cho cây trồng do chứa muối kali cacbonat. Công thức của kali cacbonat là
A, KCl.
B, K2CO3.
C, NaCl.
D, KOH.

Câu 16 [982277]: Chất nào sau đây là amin bậc ba?
A, C2H5NH2.
B, CH3NH2.
C, CH3NHCH3.
D, (CH3)3N.
HD: Bài học bậc amin:

⇝ tương ứng (CH3)3N: trimetylamin là amin bậc ba. ❒

⇝ tương ứng (CH3)3N: trimetylamin là amin bậc ba. ❒
Câu 17 [5554]: Hợp chất Y có công thức phân tử C4H8O2. Khi cho Y tác dụng với dung dịch NaOH sinh ra chất Z có
công thức C3H5O2Na. Công thức cấu tạo của Y là
A, CH3COOC2H5.
B, HCOOC3H7.
C, C2H5COOCH3.
D, C2H5COOC2H5.
HD: Phản ứng: C4H8O2 + NaOH → C3H5O2Na + ?
bảo toàn nguyên tố C, H, O, Na thấy ngay ? là CH4O là ancol metylic CH3OH.
⇒ cấu tạo của Y là C2H5COOCH3 (metyl propionat) → chọn C. ♣.
bảo toàn nguyên tố C, H, O, Na thấy ngay ? là CH4O là ancol metylic CH3OH.
⇒ cấu tạo của Y là C2H5COOCH3 (metyl propionat) → chọn C. ♣.
Câu 18 [310951]: Loại tơ nào sau đây được điều chế bằng phản ứng trùng ngưng?
A, Tơ visco.
B, Tơ nitron.
C, Tơ nilon–6,6.
D, Tơ xenlulozơ axetat.
HD: ☆ Trùng ngưng hexametylenđiamin với axit ađipic thu được nilon-6,6 là một loại tơ poliamit:

Tơ visco, xenlulozơ axetat là các loại tơ bán tổng hợp từ xenlulozơ.
Còn tơ nitron (tơ olon) là loại tơ được tổng hợp từ acrilonitrin bằng phản ứng trùng hợp. ❒

Tơ visco, xenlulozơ axetat là các loại tơ bán tổng hợp từ xenlulozơ.
Còn tơ nitron (tơ olon) là loại tơ được tổng hợp từ acrilonitrin bằng phản ứng trùng hợp. ❒
Câu 19 [228262]: Chất nào sau đây phản ứng với dung dịch BaCl2 sinh ra kết tủa màu trắng?
A, NaNO3.
B, K2SO4.
C, Al(NO3)3.
D, Ca(OH)2.
HD: ❌ NaNO3; Al(NO3)3 và cả Ca(OH)2 đều không phản ứng với BaCl2.
✔️ Chỉ có K2SO4 phản ứng được với BaCl2, đồng thời thoả mãn thu được kết tủa:
BaCl2 + K2SO4 → BaSO4↓ + 2KCl.
✔️ Chỉ có K2SO4 phản ứng được với BaCl2, đồng thời thoả mãn thu được kết tủa:
BaCl2 + K2SO4 → BaSO4↓ + 2KCl.
Câu 20 [679710]: Kim loại nào sau đây không tan được trong dung dịch H2SO4 loãng?
A, Mg.
B, Al.
C, Cu.
D, Fe.
HD: Thứ tự dãy điện hoá: 
⇒ Cu không tác dụng được với H2SO4 ⇝ không tan ⇝ Chọn đáp án C. ♣

⇒ Cu không tác dụng được với H2SO4 ⇝ không tan ⇝ Chọn đáp án C. ♣
Câu 21 [352160]: Cho kim loại Fe tác dụng với dung dịch HNO3 (loãng, dư) thu được dung dịch X. Thêm tiếp dung dịch NaOH đến dư vào X, thu được kết tủa Y. Tên gọi của Y là
A, sắt(II) oxit.
B, sắt(III) oxit.
C, sắt(II) hiđroxit.
D, sắt(III) hiđroxit.
Đáp án: D
Câu 22 [7506]: Thực hiện phản ứng este hóa 4,6 gam ancol etylic và 12 gam axit axetic với hiệu suất đạt 80% thì khối lượng este thu được là
A, 3,52 gam.
B, 7,04 gam.
C, 14,08 gam.
D, 10,56 gam.
HD: phản ứng: CH3COOH + C2H5OH ⇄ CH3COOC2H5 + H2O.
có nancol etylic = 4,6 ÷ 46 = 0,1 mol; naxit axetic = 12 ÷ 60 = 0,2 mol
⇒ hiệu suất phản ứng 80% tính theo số mol ancol
⇒ neste = 0,1 × 0,8 = 0,08 mol ⇒ meste = 0,08 × 88 = 7,04 gam.
⇒ chọn đáp án B. ♦.
có nancol etylic = 4,6 ÷ 46 = 0,1 mol; naxit axetic = 12 ÷ 60 = 0,2 mol
⇒ hiệu suất phản ứng 80% tính theo số mol ancol
⇒ neste = 0,1 × 0,8 = 0,08 mol ⇒ meste = 0,08 × 88 = 7,04 gam.
⇒ chọn đáp án B. ♦.
Câu 23 [212597]: Phát biểu nào sau đây đúng?
A, Glucozơ bị thủy phân trong môi trường axit.
B, Tinh bột là chất lỏng ở nhiệt độ thường.
C, Xenlulozơ thuộc loại đisaccarit.
D, Dung dịch saccarozơ hòa tan được Cu(OH)2.
HD: ☆ Phân tích các phát biểu:
❌ A. sai vì glucozơ là monosaccarit, không bị thủy phân.
❌ B. sai vì như ta thấy lúa ngô khoai sắn chứa tinh bột là chất rắn ở điều kiện thường đó.
❌ C. sai vì xelulozơ: (C6H10O5)n là polisaccarit.
✔️ D. đúng, cả glucozơ, fructozơ và saccarozơ đều có cấu tạo chứa nhiều nhóm OH liền kề nên có khả năng phản ứng tạo phức tan với Cu(OH)2 màu xanh lam.
❌ A. sai vì glucozơ là monosaccarit, không bị thủy phân.
❌ B. sai vì như ta thấy lúa ngô khoai sắn chứa tinh bột là chất rắn ở điều kiện thường đó.
❌ C. sai vì xelulozơ: (C6H10O5)n là polisaccarit.
✔️ D. đúng, cả glucozơ, fructozơ và saccarozơ đều có cấu tạo chứa nhiều nhóm OH liền kề nên có khả năng phản ứng tạo phức tan với Cu(OH)2 màu xanh lam.
Câu 24 [21802]: Cho dãy gồm các polime: (1) polistiren, (2) poli(phenol-fomanđehit), (3) poli(metyl metacrylat), (4) polietilen. Số polime có chứa vòng benzen là
A, 2.
B, 1.
C, 4.
D, 3.
HD: Phân tích cấu tạo của các polime trong dãy:
![577842[LG].png](https://m.moon.vn/Images/Teachers/rongden_167/ProS2018/TAP%20II/577842[LG].png)
⇒ có 2 polime có chứa vòng benzen → Chọn đáp án A. ♥
![577842[LG].png](https://m.moon.vn/Images/Teachers/rongden_167/ProS2018/TAP%20II/577842[LG].png)
⇒ có 2 polime có chứa vòng benzen → Chọn đáp án A. ♥
Câu 25 [20592]: Phân tử chất béo T được cấu tạo từ một gốc panmitat, một gốc oleat và một gốc stearat liên kết với gốc hiđrocacbon của glixerol. Số đồng phân cấu tạo của T thỏa mãn là
A, 2.
B, 4.
C, 1.
D, 3.
HD: chất béo T được cấu tạo từ một gốc panmitat, một gốc oleat và một gốc stearat
số đồng phân của T là các vị trí tương đối của các gốc trên với gốc hiđrocacbon của glixerol:
![564537[LG].png](https://m.moon.vn/Images/Teachers/rongden_167/ProS2018/TAP%20II/BAI%202/564537[LG].png)
Tổng có 3 đồng phân thỏa mãn. Chọn đáp án D. ♠.
số đồng phân của T là các vị trí tương đối của các gốc trên với gốc hiđrocacbon của glixerol:
![564537[LG].png](https://m.moon.vn/Images/Teachers/rongden_167/ProS2018/TAP%20II/BAI%202/564537[LG].png)
Tổng có 3 đồng phân thỏa mãn. Chọn đáp án D. ♠.
Câu 26 [679797]: Cho khí H2 dư qua ống đựng m gam Fe2O3 nung nóng. Sau khi các phản ứng xảy ra hoàn toàn, thu được 5,6 gam Fe. Giá trị của m là
A, 8,0.
B, 4,0.
C, 16,0.
D, 6,0.
HD: Phản ứng: 3H2 + Fe2O3 ––to→ 2Fe + 3H2O.
Giả thiết: nFe = 0,1 mol ⇒ nFe2O3 = ½.nFe = 0,05 mol.
⇒ Yêu cầu: m = 0,05 × 160 = 8,0 gam ⇝ Chọn đáp án A. ♥
Giả thiết: nFe = 0,1 mol ⇒ nFe2O3 = ½.nFe = 0,05 mol.
⇒ Yêu cầu: m = 0,05 × 160 = 8,0 gam ⇝ Chọn đáp án A. ♥
Câu 27 [12274]: Thủy phân m gam tinh bột một thời gian thu được m gam glucozơ (giả sử chỉ xảy ra phản ứng thủy phân tinh bột thành glucozơ). Phần trăm tinh bột bị thủy phân là
A, 90%.
B, 80%.
C, 75%.
D, 60%.
HD: Lấy m = 180 gam ⇝ thủy phân 180 gam tinh bột thu được 180 gam glucozơ.
☆ Phản ứng: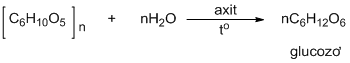
nglucozơ = 1 mol ⇒ mtinh bột bị thủy phân = 1 × 162 = 162 gam
⇝ Phần trăm tinh bột bị thủy phân là 162 ÷ 180 × 100% = 90%. ❒
☆ Phản ứng:
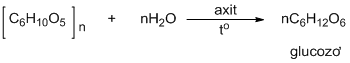
nglucozơ = 1 mol ⇒ mtinh bột bị thủy phân = 1 × 162 = 162 gam
⇝ Phần trăm tinh bột bị thủy phân là 162 ÷ 180 × 100% = 90%. ❒
Câu 28 [679716]: Cho 4,5 gam amin X (no, đơn chức, mạch hở) tác dụng với HCl dư, thu được 8,15 gam muối. Số nguyên tử hiđro trong phân tử X là
A, 9.
B, 5.
C, 7.
D, 11.
HD: Amin X no đơn chức, mạch hở ⇒ có dạng CnH2n + 3N.
Phản ứng: CnH2n + 3N + HCl → CnH2n + 4NCl.
BTKL ta có mHCl = 8,15 – 4,5 = 3,65 gam ⇒ nX = nHCl = 0,1 mol.
⇒ MX = 14n + 17 = 4,5 ÷ 0,1 ⇒ n = 2 cho biết X là C2H7N ⇝ Chọn đáp án C. ♣
Phản ứng: CnH2n + 3N + HCl → CnH2n + 4NCl.
BTKL ta có mHCl = 8,15 – 4,5 = 3,65 gam ⇒ nX = nHCl = 0,1 mol.
⇒ MX = 14n + 17 = 4,5 ÷ 0,1 ⇒ n = 2 cho biết X là C2H7N ⇝ Chọn đáp án C. ♣
Câu 29 [352161]: Phát biểu nào sau đây đúng?
A, Tất cả các hiđroxit của kim loại nhóm IIA đều dễ tan trong nước.
B, Nhôm tồn tại ở cả dạng đơn chất và hợp chất trong tự nhiên.
C, Thạch cao sống dùng để sản xuất xi măng.
D, Trong nhóm IA, tính khử của các kim loại giảm dần từ Li đến Cs.
HD: Phân tích các đáp án:
❌ A. sai vì Mg(OH)2↓ không tan trong nước, Ca(OH)2 ít tan.
❌ B. sai vì ta không tìm thấy Al đơn chất trong tự nhiên.
✔️ C. đúng theo ứng dụng của thạch cao:

❌ D. sai vì như biết "Khi nào may áo giáp" ⇄ K Na Mg Al Zn... thì K có tính khử mạnh hơn Na ⇝ nói tính khử giảm dần từ Li → Cs là sai rồi.
❌ A. sai vì Mg(OH)2↓ không tan trong nước, Ca(OH)2 ít tan.
❌ B. sai vì ta không tìm thấy Al đơn chất trong tự nhiên.
✔️ C. đúng theo ứng dụng của thạch cao:

❌ D. sai vì như biết "Khi nào may áo giáp" ⇄ K Na Mg Al Zn... thì K có tính khử mạnh hơn Na ⇝ nói tính khử giảm dần từ Li → Cs là sai rồi.
Câu 30 [22294]: [THPT QG 2016]: Đốt cháy 2,15 gam hỗn hợp gồm Zn, Al và Mg trong khí oxi dư, thu được 3,43 gam hỗn hợp X. Toàn bộ X phản ứng vừa đủ với V ml dung dịch HCl 0,5M. Biết các phản ứng xảy ra hoàn toàn. Giá trị của V là
A, 160.
B, 320.
C, 240.
D, 480.
HD: 2,15g hh (Zn, Al, Mg) + O2 → 3,43g X (ZnO, Al2O3, MgO).
X (ZnO, Al2O3, MgO) + V ml HCl 0,5M → muối (ZnCl2, AlCl3, MgCl2) + H2O.
nO(X) = = 0,08 mol.
= 0,08 mol.
Nhận thấy O trong X sẽ chuyển hết vào H2O khi X tác dụng với HCl.
Ta có mối quan hệ: nHCl = 2nH2O (bảo toàn H) = 2nO(X) (bảo toàn O) = 0,16 mol.
⇒ VHCl = 0,32 lít = 320 ml.
Vậy V = 320.
Chọn B.
X (ZnO, Al2O3, MgO) + V ml HCl 0,5M → muối (ZnCl2, AlCl3, MgCl2) + H2O.
nO(X) =
 = 0,08 mol.
= 0,08 mol.Nhận thấy O trong X sẽ chuyển hết vào H2O khi X tác dụng với HCl.
Ta có mối quan hệ: nHCl = 2nH2O (bảo toàn H) = 2nO(X) (bảo toàn O) = 0,16 mol.
⇒ VHCl = 0,32 lít = 320 ml.
Vậy V = 320.
Chọn B.
Câu 31 [679293]: Cho các phát biểu sau:
(a) Các kim loại Na, K, Ba đều phản ứng mạnh với nước.
(b) Kim loại Cu tác dụng được với dung dịch hỗn hợp NaNO3 và H2SO4 (loãng).
(c) Crom bền trong không khí và nước do có màng oxit bảo vệ.
(d) Cho bột Cu vào lượng dư dung dịch FeCl3, thu được dung dịch chứa ba muối.
(e) Hỗn hợp Al và BaO (tỉ lệ số mol tương ứng 1 : 1) tan hoàn toàn trong nước dư.
(g) Lưu huỳnh, photpho và ancol etylic đều bốc cháy khi tiếp xúc với CrO3.
Số phát biểu đúng là
(a) Các kim loại Na, K, Ba đều phản ứng mạnh với nước.
(b) Kim loại Cu tác dụng được với dung dịch hỗn hợp NaNO3 và H2SO4 (loãng).
(c) Crom bền trong không khí và nước do có màng oxit bảo vệ.
(d) Cho bột Cu vào lượng dư dung dịch FeCl3, thu được dung dịch chứa ba muối.
(e) Hỗn hợp Al và BaO (tỉ lệ số mol tương ứng 1 : 1) tan hoàn toàn trong nước dư.
(g) Lưu huỳnh, photpho và ancol etylic đều bốc cháy khi tiếp xúc với CrO3.
Số phát biểu đúng là
A, 4.
B, 5.
C, 3.
D, 6.
HD: Chọn đáp án D.
✔️ (a) đúng, các kim loại kiềm và Ca, Ba phản ứng mạnh với H2O tỏa nhiệt và giải phóng H2.
✔️ (b) đúng: 3Cu2+ + 8H+ + 2NO3– → 3Cu2+ + 2NO↑ + 4H2O.
✔️ (c) đúng vì nhôm (Al) và crom (Cr) đều bền trong không khí và nước do có màng oxit bảo vệ.
✔️(d) đúng. Phản ứng Cu + 2FeCl3 → CuCl2 + 2FeCl3 và thêm FeCl3 dư nữa là đúng ba muối.
✔️ (e) đúng. Giả sử có 2 mol BaO thì tạo 2 mol Ba(OH)2; sau đó:
2Al + Ba(OH)2 + 2H2O → Ba(AlO2)2 + 3H2↑. Al tan hết, Ba(OH)2 còn dư.
✔️ (g) đúng. 3S + 4CrO3 → 3SO2 + 2Cr2O3.
⇝ Cả 6/6 phát biểu đều đúng.
✔️ (a) đúng, các kim loại kiềm và Ca, Ba phản ứng mạnh với H2O tỏa nhiệt và giải phóng H2.
✔️ (b) đúng: 3Cu2+ + 8H+ + 2NO3– → 3Cu2+ + 2NO↑ + 4H2O.
✔️ (c) đúng vì nhôm (Al) và crom (Cr) đều bền trong không khí và nước do có màng oxit bảo vệ.
✔️(d) đúng. Phản ứng Cu + 2FeCl3 → CuCl2 + 2FeCl3 và thêm FeCl3 dư nữa là đúng ba muối.
✔️ (e) đúng. Giả sử có 2 mol BaO thì tạo 2 mol Ba(OH)2; sau đó:
2Al + Ba(OH)2 + 2H2O → Ba(AlO2)2 + 3H2↑. Al tan hết, Ba(OH)2 còn dư.
✔️ (g) đúng. 3S + 4CrO3 → 3SO2 + 2Cr2O3.
⇝ Cả 6/6 phát biểu đều đúng.
Câu 32 [311724]: Tiến hành chưng cất thường dung dịch ancol etylic (rượu) như như hình bên.

Có các phát biểu sau:
(a) Vai trò của nhiệt kế là đo nhiệt độ của dung dịch đem chưng cất.
(b) Hơi ancol thoát ra từ bình cầu được ngưng tụ trong ống sinh hàn.
(c) Hàm lượng etanol (nồng độ rượu) trong bình cầu có nhánh tăng dần.
(d) Cần tắt đèn cồn và cách ly với bình hứng sau khi kết thúc quá trình.
(e) Nước trong ống sinh hàn được làm lạnh và thay liên tục.
Số phát biểu đúng là

Có các phát biểu sau:
(a) Vai trò của nhiệt kế là đo nhiệt độ của dung dịch đem chưng cất.
(b) Hơi ancol thoát ra từ bình cầu được ngưng tụ trong ống sinh hàn.
(c) Hàm lượng etanol (nồng độ rượu) trong bình cầu có nhánh tăng dần.
(d) Cần tắt đèn cồn và cách ly với bình hứng sau khi kết thúc quá trình.
(e) Nước trong ống sinh hàn được làm lạnh và thay liên tục.
Số phát biểu đúng là
A, 1.
B, 3.
C, 4.
D, 2.
HD: Xem xét - phân tích các phát biểu:
(a) sai vì quan sát: nhiệt kế đo nhiệt độ phần khí, hơi trong bình cầu có nhánh (nếu muốn đo dung dịch chưng cất thì cần nhúng vào phần dung dịch).
(b) đúng. Nước lạnh ở ống sinh hàn giúp ngưng tụ ancol ⇝ chảy nhỏ giọt vào bình hứng.
(c) sai rất rõ hơi ancol bay ra khỏi bình cầu có nhánh nên hàm lượng ancol sẽ giảm dần.
(d) đúng. bình hứng chứa ancol rất dễ bắt lửa và bốc cháy nên thao tác là cần thiết để đảm bảo an toàn.
(e) đúng. Như phân tích ở ý (b); nước trong ống sinh hàn cần làm lạnh và thay liên tục để ngưng tụ etanol.
⇝ có tất cả 3 phát biểu đúng. ❒
(a) sai vì quan sát: nhiệt kế đo nhiệt độ phần khí, hơi trong bình cầu có nhánh (nếu muốn đo dung dịch chưng cất thì cần nhúng vào phần dung dịch).
(b) đúng. Nước lạnh ở ống sinh hàn giúp ngưng tụ ancol ⇝ chảy nhỏ giọt vào bình hứng.
(c) sai rất rõ hơi ancol bay ra khỏi bình cầu có nhánh nên hàm lượng ancol sẽ giảm dần.
(d) đúng. bình hứng chứa ancol rất dễ bắt lửa và bốc cháy nên thao tác là cần thiết để đảm bảo an toàn.
(e) đúng. Như phân tích ở ý (b); nước trong ống sinh hàn cần làm lạnh và thay liên tục để ngưng tụ etanol.
⇝ có tất cả 3 phát biểu đúng. ❒
Câu 33 [132667]: Hỗn hợp X gồm Fe3O4, Fe2O3, FeS2 và CuO. Cho m gam X vào bình kín chứa 1,875 mol khí O2 (dư) rồi nung nóng bình cho tới khi các phản ứng xảy ra hoàn toàn rồi đưa bình về điều kiện ban đầu thấy áp suất giảm 10% so với lúc trước khi nung. Mặt khác, nếu cho m gam X vào H2SO4 đặc, nóng dư thu được 35,28 lít khí SO2 (đktc, sản phẩm khử duy nhất) và dung dịch Y chứa 155m/69 gam muối. Biết trong X oxi chiếm 19,324% về khối lượng. Giá trị của m gần nhất với giá trị nào sau đây?
A, 82.
B, 66.
C, 74.
D, 91.
HD: ☆☆☆ Sunfua không thuần bởi hỗn hợp và quá trình.!
Tập trung vào S: gọi nS trong X = x mol. Quy X về gồm x mol S và PHẦN CÒN LẠI (gồm Fe, Cu, O).
Quan sát 2 quá trình, bảo toàn electron có:
♦ đốt:

(S chỉ lên S+4)
||→ 4x + ne cho của PHẦN CÒN LẠI = 4nO2 phản ứng = 4 × (0,1875 + x)
♦ + HSO4 đặc nóng (S lên tối đa S+6): 6x + ne cho của PHẦN CÒN LẠI = 2nSO2 = 3,15.
Theo đó, giải ra điều chúng ta đang quan tâm: nS trong X = x = 0,4 mol.
► Đọc yêu cầu: giả thiết có %mO trong X. Quan sát sơ đồ mới và phản xạ bảo toàn O:
Xử lí nhanh trên sơ đồ S + 4H2O và ghép cụm nH2O = 2nSO2 + nO trong oxit.
Và ở trên, kí hiệu nO = nO trong X = 0,19324m ÷ 16.
||→ lập phương trình bảo toàn khối lượng toàn sơ đồ với ẩn duy nhất là m
||→ giải ra m ≈ 82,8 gam. Chọn đáp án A. ♥.
Tập trung vào S: gọi nS trong X = x mol. Quy X về gồm x mol S và PHẦN CÒN LẠI (gồm Fe, Cu, O).
Quan sát 2 quá trình, bảo toàn electron có:
♦ đốt:

(S chỉ lên S+4)
||→ 4x + ne cho của PHẦN CÒN LẠI = 4nO2 phản ứng = 4 × (0,1875 + x)
♦ + HSO4 đặc nóng (S lên tối đa S+6): 6x + ne cho của PHẦN CÒN LẠI = 2nSO2 = 3,15.
Theo đó, giải ra điều chúng ta đang quan tâm: nS trong X = x = 0,4 mol.
► Đọc yêu cầu: giả thiết có %mO trong X. Quan sát sơ đồ mới và phản xạ bảo toàn O:

Xử lí nhanh trên sơ đồ S + 4H2O và ghép cụm nH2O = 2nSO2 + nO trong oxit.
Và ở trên, kí hiệu nO = nO trong X = 0,19324m ÷ 16.
||→ lập phương trình bảo toàn khối lượng toàn sơ đồ với ẩn duy nhất là m
||→ giải ra m ≈ 82,8 gam. Chọn đáp án A. ♥.
Câu 34 [679565]: Dẫn 0,02 mol hỗn hợp X (gồm hơi nước và khí CO2) qua cacbon nung đỏ, thu được 0,035 mol hỗn hợp Y gồm CO, H2 và CO2. Cho Y đi qua ống đựng 10 gam hỗn hợp gồm Fe2O3 và CuO (dư, nung nóng), sau khi các phản ứng xảy ra hoàn toàn, thu được m gam chất rắn. Giá trị của m là
A, 9,76.
B, 9,20.
C, 9,52.
D, 9,28.
HD: Nhắc lại kiến thức và cách xử lý nhanh + tinh tế hệ khí than ướt:

⇒ nC = Δntăng = 0,035 – 0,02 = 0,015 mol.
⇒ nO trong oxit bị lấy = 2∑nC = 0,03 mol.
⇒ m = mrắn sau phản ứng = 10 – 0,03 × 16 = 9,52 gam.

⇒ nC = Δntăng = 0,035 – 0,02 = 0,015 mol.
⇒ nO trong oxit bị lấy = 2∑nC = 0,03 mol.
⇒ m = mrắn sau phản ứng = 10 – 0,03 × 16 = 9,52 gam.
Câu 35 [306157]: Hỗn hợp X gồm 0,15 mol CH4; 0,09 mol C2H2 và 0,2 mol H2. Nung nóng X với xúc tác Ni thu được hỗn hợp Y. Cho Y qua dung dịch Br2 dư thấy khối lượng dung dịch tăng thêm 0,82 gam và thoát ra V lít (đktc) hỗn hợp khí Z có tỉ khối so với H2 là 8. Giá trị của V là
A, 5,600.
B, 6,048.
C, 5,824.
D, 5,376.
HD: Tỉ khối của Z so với H2 là 8 ⇒ MZ = 16 = MCH4 ⇒ số mol C2H6 và H2 trong Z bằng nhau.
Trong Y có x mol C2H2 và y mol C2H4 ||→ trong Z có (0,09 – x – y) mol C2H6 = số mol H2.
||→ số mol H2 đã phản ứng = (x + y + 0,11) mol. Làm no hết X cần 0,09 × 2 = 0,18 mol
||→ có 2x + y + x + y + 0,11 = 0,18; mà 26x + 28y = 0,82 gam ||→ x = 0,01 mol và y = 0,02 mol.
||→ Z có 0,06 mol C2H6; 0,06 mol H2 và 0,15 mol CH4 ||→ VZ = 6,048 lít. Chọn B. ♦.
► Lời giải trên chỉ là "đánh lừa chút thôi".! Chứ với yêu cầu của đề bài thì chỉ cần
một phép tính: mX = 5,15 gam ||→ V = (5,14 – 0,82) ÷ (8 × 2) × 22,4 = 6,048 lít. ❒
⇝ ☆ cùng với cùng một giả thiết, một bài tập, muốn làm khó hay dễ cũng tùy thuộc vào yêu cầu của người ra đề nữa. Ví dụ như trên, yêu cầu V thì đơn giản quá, nhưng nếu hỏi số mol C2H2 + Br2 hay % các khí trong Z thì lại là một vấn đề.!
Trong Y có x mol C2H2 và y mol C2H4 ||→ trong Z có (0,09 – x – y) mol C2H6 = số mol H2.
||→ số mol H2 đã phản ứng = (x + y + 0,11) mol. Làm no hết X cần 0,09 × 2 = 0,18 mol
||→ có 2x + y + x + y + 0,11 = 0,18; mà 26x + 28y = 0,82 gam ||→ x = 0,01 mol và y = 0,02 mol.
||→ Z có 0,06 mol C2H6; 0,06 mol H2 và 0,15 mol CH4 ||→ VZ = 6,048 lít. Chọn B. ♦.
► Lời giải trên chỉ là "đánh lừa chút thôi".! Chứ với yêu cầu của đề bài thì chỉ cần
một phép tính: mX = 5,15 gam ||→ V = (5,14 – 0,82) ÷ (8 × 2) × 22,4 = 6,048 lít. ❒
⇝ ☆ cùng với cùng một giả thiết, một bài tập, muốn làm khó hay dễ cũng tùy thuộc vào yêu cầu của người ra đề nữa. Ví dụ như trên, yêu cầu V thì đơn giản quá, nhưng nếu hỏi số mol C2H2 + Br2 hay % các khí trong Z thì lại là một vấn đề.!
Câu 36 [14867]: X, Y, Z là các hợp chất vô cơ của kali, biết rằng:
+ Điện phân nóng chảy X, thu được kali và clo.
+ Cho KOH vào dung dịch Z, thu được kali sunfat.
+ Cho Cu vào dung dịch gồm Y và Z, có khí NO bay ra.
Phát biểu sai là
+ Điện phân nóng chảy X, thu được kali và clo.
+ Cho KOH vào dung dịch Z, thu được kali sunfat.
+ Cho Cu vào dung dịch gồm Y và Z, có khí NO bay ra.
Phát biểu sai là
A, X được sử dụng làm phân kali.
B, Nung nóng X trên ngọn lửa không màu, thấy có màu tím.
C, Y dễ bị nhiệt phân hủy.
D, Dung dịch Z làm phenolphtalein chuyển màu hồng.
HD: • điện phân nóng chảy X → K + Cl2↑ ⇒ X là KCl.
• KOH + Z → K2SO4 ⇒ Z là KHSO4.
• Cu + KHSO4 + Y → muối đồng + NO↑ + H2O. ⇒ Y là KNO3.
☆ Xem xét các phát biểu:
✔️ A. đúng vì KCl chứa kali được dùng làm phân kali.
✔️ B. đúng vì ngọn lửa kali có màu tím (natri màu vàng).
✔️ C. đúng vì muối KNO3 dễ bị nhiệt phân: KNO3 ––to→ KNO2 + ½.O2↑.
❌ D. sai vì KHSO4 có pH < 7, không làm phenolphtalein đổi màu.
• KOH + Z → K2SO4 ⇒ Z là KHSO4.
• Cu + KHSO4 + Y → muối đồng + NO↑ + H2O. ⇒ Y là KNO3.
☆ Xem xét các phát biểu:
✔️ A. đúng vì KCl chứa kali được dùng làm phân kali.
✔️ B. đúng vì ngọn lửa kali có màu tím (natri màu vàng).
✔️ C. đúng vì muối KNO3 dễ bị nhiệt phân: KNO3 ––to→ KNO2 + ½.O2↑.
❌ D. sai vì KHSO4 có pH < 7, không làm phenolphtalein đổi màu.
Câu 37 [310909]: X, Y là hai axit cacboxylic đều đơn chức, mạch hở (trong phân tử X, Y chứa không quá hai liên kết π và 50 < MX < MY); Z là este được tạo bởi X, Y và etylen glicol. Đốt cháy 13,12 gam hỗn hợp E chứa X, Y, Z cần dùng 0,50 mol O2. Mặt khác 0,36 mol E làm mất màu vừa đủ dung dịch chứa 0,1 mol Br2. Nếu đun nóng 13,12 gam E với 200 ml dung dịch KOH 1M (vừa đủ), cô cạn dung dịch sau phản ứng thu được hỗn hợp F gồm a gam muối A và b gam muối B (MA < MB). Giá trị tỉ lệ của a : b gần nhất với
A, 2,9.
B, 2,7.
C, 2,6.
D, 2,8.
HD: ☆ 13,12 gam E + 0,2 mol KOH (vừa đủ) → …–COOK + … nên ∑nO trong E = 0,4 mol.
Giải đốt 13,12 gam E (gồm C, H, O) cần 0,5 mol O2 thu được x mol CO2 + y mol H2O.
Có hệ:
• Mặt khác, 0,36 mol E phản ứng vừa đủ với 0,1 mol Br2 và kết hợp giả thiết “chữ” về X, Y.
⇝ trong hai axit X và Y thì có một axit no và một axit không no, có đúng một nối đôi C=C.
☆ Phản ứng tạo este: 1X + 1Y + 1C2H4(OH)2 → 1Z + 2H2O.
⇝ Quy đổi E: axit – este về a mol CnH2nO2 + b mol CmH2m – 2O2 + c mol C2H4(OH)2 – 2c mol H2O.
Tương quan đốt: ∑nCO2 – ∑nH2O = b + 2c – c = b + c = 0,49 – 0,42 = 0,07 mol (1).
Bảo toàn nguyên tố oxit có: 2a + 2b = 0,4 mol → a + b = 0,2 mol (2).
☆ Giả sử tỉ lệ 0,36 mol E so với 13,12 gam E là k, ta có: nE = ka + kb + kc – 2kc = 0,36 mol.
Chỉ có kb mol CmH2m – 2O2 phản ứng với Br2 ⇒ kb = 0,1 mol.
Theo đó, rút gọn k có phương trình: a + b – c = 3,6b ⇔ 0,2 – c = 3,6b (3).
Giải hệ (1), (2), (3) được a = 0,15 mol; b = 0,05 mol; c = 0,02 mol.
Thay lại, có số mol CO2: 0,15n + 0,05m + 0,02 × 2 = 0,49 ⇔ 3n + m = 9
Với điều kiện n, m nguyên và yêu cầu n ≥ 1; m ≥ 3 ⇒ cặp (n; m) = (2; 3) duy nhất thỏa mãn.
Vậy hỗn hợp F gồm 0,15 mol CH3COOK (muối A) và 0,05 mol C2H3COOK (muối B).
⇝ Tỉ lệ cần tìm a : b = 0,15 × 98 ÷ (0,05 × 110) ≈ 2,67. ❒
Giải đốt 13,12 gam E (gồm C, H, O) cần 0,5 mol O2 thu được x mol CO2 + y mol H2O.
Có hệ:

• Mặt khác, 0,36 mol E phản ứng vừa đủ với 0,1 mol Br2 và kết hợp giả thiết “chữ” về X, Y.
⇝ trong hai axit X và Y thì có một axit no và một axit không no, có đúng một nối đôi C=C.
☆ Phản ứng tạo este: 1X + 1Y + 1C2H4(OH)2 → 1Z + 2H2O.
⇝ Quy đổi E: axit – este về a mol CnH2nO2 + b mol CmH2m – 2O2 + c mol C2H4(OH)2 – 2c mol H2O.
Tương quan đốt: ∑nCO2 – ∑nH2O = b + 2c – c = b + c = 0,49 – 0,42 = 0,07 mol (1).
Bảo toàn nguyên tố oxit có: 2a + 2b = 0,4 mol → a + b = 0,2 mol (2).
☆ Giả sử tỉ lệ 0,36 mol E so với 13,12 gam E là k, ta có: nE = ka + kb + kc – 2kc = 0,36 mol.
Chỉ có kb mol CmH2m – 2O2 phản ứng với Br2 ⇒ kb = 0,1 mol.
Theo đó, rút gọn k có phương trình: a + b – c = 3,6b ⇔ 0,2 – c = 3,6b (3).
Giải hệ (1), (2), (3) được a = 0,15 mol; b = 0,05 mol; c = 0,02 mol.
Thay lại, có số mol CO2: 0,15n + 0,05m + 0,02 × 2 = 0,49 ⇔ 3n + m = 9
Với điều kiện n, m nguyên và yêu cầu n ≥ 1; m ≥ 3 ⇒ cặp (n; m) = (2; 3) duy nhất thỏa mãn.
Vậy hỗn hợp F gồm 0,15 mol CH3COOK (muối A) và 0,05 mol C2H3COOK (muối B).
⇝ Tỉ lệ cần tìm a : b = 0,15 × 98 ÷ (0,05 × 110) ≈ 2,67. ❒
Câu 38 [352162]: Cho các nhận định sau:
(a) Amino axit là hợp chất hữu cơ tạp chức, phân tử chứa đồng thời nhóm amino và cacboxyl.
(b) Anbumin (lòng trắng trứng) có phản ứng màu biure.
(c) Anilin có tính chất lưỡng tính và không làm đổi màu quỳ tím ẩm.
(d) Axit ađipic và hexametylenđiamin là nguyên liệu để sản xuất tơ nilon-6,6.
(e) Methionin là một α-amino axit dùng làm thuốc bổ gan.
Số nhận định đúng là
(a) Amino axit là hợp chất hữu cơ tạp chức, phân tử chứa đồng thời nhóm amino và cacboxyl.
(b) Anbumin (lòng trắng trứng) có phản ứng màu biure.
(c) Anilin có tính chất lưỡng tính và không làm đổi màu quỳ tím ẩm.
(d) Axit ađipic và hexametylenđiamin là nguyên liệu để sản xuất tơ nilon-6,6.
(e) Methionin là một α-amino axit dùng làm thuốc bổ gan.
Số nhận định đúng là
A, 2.
B, 5.
C, 3.
D, 4.
Đáp án: D
Câu 39 [311721]: Hấp thụ 4,48 lít khí CO2 (đktc) vào 100 ml dung dịch chứa NaOH xM và Na2CO3 yM, kết thúc phản ứng thu được dung dịch X. Cho từ từ dung dịch HCl 2M vào X, kết quả thí nghiệm được ghi lại ở bảng sau:
Tỉ lệ y : x bằng
| Thể tích dung dịch HCl (ml) | 100 | 250 | 350 |
| Số mol khí thoát ra (mol) | 0 | 0,25 | 0,35 |
Tỉ lệ y : x bằng
A, 3 : 5.
B, 2 : 1.
C, 2 : 5.
D, 1 : 2.
HD: Hấp thụ nên 0,2 mol CO2 phản ứng hết với 0,1x mol NaOH và 0,1y mol Na2CO3.
⇝ dung dịch X là NaHCO3 và Na2CO3 hoặc chỉ có Na2CO3 và NaOH còn dư.
► Với TH nào thì khi cho từ từ H+ vào X đều có mối liên hệ như đồ thị sau:
![311721[LG2].png](https://m.moon.vn/Images/Teachers/rongden_167/SACHID/311721[LG2].png)
Nhận xét: • Điểm D(0,3; 0) thuộc đoạn OA: H+ + CO32– → HCO3–
hoặc H+ + OH– → H2O ||⇝ chưa xuất hiện khí.
• Điểm E(0,5; 0,25) thuộc đoạn AB: H+ + HCO3– → CO2↑ + H2O.
Nếu điểm F(0,7; 0,35) cũng thuộc AB thì thêm (0,7 – 0,5) mol H+ đáng nhẽ
phải tạo thêm 0,2 mol CO2. Nhưng, theo kết quả lại chỉ thu (0,35 – 0,25) mol CO2
⇒ không đúng. Vậy điểm F thuộc đoạn BC.
⇒ ∑nCO2↑ = 0,35 mol ⇒ bảo toàn C cả quá trình: 0,2 + 0,1y = 0,35 ⇒ y = 1,5.
Lại có BH = 0,6, tại đó toàn bộ Na đi hết về 0,6 mol NaCl
⇒ 0,1x + 0,1y × 2 = 0,6 ⇒ x = 3. Vậy, yêu cầu y : x = 1 : 2. ❒
⇝ dung dịch X là NaHCO3 và Na2CO3 hoặc chỉ có Na2CO3 và NaOH còn dư.
► Với TH nào thì khi cho từ từ H+ vào X đều có mối liên hệ như đồ thị sau:
![311721[LG2].png](https://m.moon.vn/Images/Teachers/rongden_167/SACHID/311721[LG2].png)
Nhận xét: • Điểm D(0,3; 0) thuộc đoạn OA: H+ + CO32– → HCO3–
hoặc H+ + OH– → H2O ||⇝ chưa xuất hiện khí.
• Điểm E(0,5; 0,25) thuộc đoạn AB: H+ + HCO3– → CO2↑ + H2O.
Nếu điểm F(0,7; 0,35) cũng thuộc AB thì thêm (0,7 – 0,5) mol H+ đáng nhẽ
phải tạo thêm 0,2 mol CO2. Nhưng, theo kết quả lại chỉ thu (0,35 – 0,25) mol CO2
⇒ không đúng. Vậy điểm F thuộc đoạn BC.
⇒ ∑nCO2↑ = 0,35 mol ⇒ bảo toàn C cả quá trình: 0,2 + 0,1y = 0,35 ⇒ y = 1,5.
Lại có BH = 0,6, tại đó toàn bộ Na đi hết về 0,6 mol NaCl
⇒ 0,1x + 0,1y × 2 = 0,6 ⇒ x = 3. Vậy, yêu cầu y : x = 1 : 2. ❒
Câu 40 [352163]: Cao su buna-N là một polime được điều chế từ buta-1,3-dien và acrilonitrin có xúc tác Na. Nó có khả năng chống chịu mạnh mẽ với dầu, xăng, axit, hidrocacbon béo và các hóa chất khác. Nó cũng có phạm vi hoạt động ở nhiệt độ rộng từ -40°C (-40°F) đến 108°C (226°F). Sự kết hợp của hai đặc tính mạnh mẽ này làm cho cao su buna-N trở thành sự lựa chọn hoàn hảo để sử dụng trong ngành công nghiệp ô tô và hàng không vũ trụ. Cao su buna-N còn có khả năng chống nước mạnh cũng như khả năng chống mài mòn và rách tốt. Giả sử trong phần mạch cacbon của polime, các phân tử buta-1,3-dien và acrilonitrin được sắp xếp luân phiên và xen kẽ nhau.
Cho các phát biểu sau:
(a) Cao su buna-N có thành phần nguyên tố hóa học giống với cao su buna.
(b) Nếu một phân tử cao su buna-N có phân tử khối là 26.000 g/mol thì nó chứa khoảng 243 mỗi mắt xích buta-1,3-dien và acrilonitrin.
(c) Trong phân tử cao su buna-N có chứa 1 nguyên tử N.
(d) Cao su buna-N thuộc loại polime tổng hợp.
(e) Cao su buna-N được tổng hợp khi đồng trùng hợp buta-1,3-dien và acrilonitrin.
Số phát biểu đúng là
Cho các phát biểu sau:
(a) Cao su buna-N có thành phần nguyên tố hóa học giống với cao su buna.
(b) Nếu một phân tử cao su buna-N có phân tử khối là 26.000 g/mol thì nó chứa khoảng 243 mỗi mắt xích buta-1,3-dien và acrilonitrin.
(c) Trong phân tử cao su buna-N có chứa 1 nguyên tử N.
(d) Cao su buna-N thuộc loại polime tổng hợp.
(e) Cao su buna-N được tổng hợp khi đồng trùng hợp buta-1,3-dien và acrilonitrin.
Số phát biểu đúng là
A, 3.
B, 2.
C, 4.
D, 1.
HD: Giả sử trong phần mạch cacbon của polime, các phân tử buta-1,3-dien và acrilonitrin được sắp xếp luân phiên và xen kẽ nhau ⇝ cấu tạo mắt một mắt xích của cao su buna-N như sau:

☆ Phân tích các phát biểu:
❌ (a) sai vì thành phần cao su buna không có nguyên tố N như cao su buna-N.
✔️ (b) đúng vì mắt xích của cao su buna-N là C7H9N ⇒ M = 107 ⇒ 243 mắt xích tương ứng với PTK của poilme là 243 × 107 = 26001.
❌ (c) sai vì phân tử polime thì có rất nhiều mắt xích, mà mỗi mắt xích có 1N ⇒ polime thì chắc chắn có nhiều hơn 1 N rồi (rất nhiều bạn nhầm ý này).
✔️ (d) đúng, cao su buna-N được tổng hợp từ các monome ⇝ là polime tổng hợp.
✔️ (e) đúng vì buta-1,3-dien: CH2=CH–CH=CH2 và acrilonitrin: CH2=CH–CN ⇝ đồng trùng hợp thu được cao su buna-N.
⇝ có 3/5 phát biểu đúng ⇝ Chọn đáp án A. ♥

☆ Phân tích các phát biểu:
❌ (a) sai vì thành phần cao su buna không có nguyên tố N như cao su buna-N.
✔️ (b) đúng vì mắt xích của cao su buna-N là C7H9N ⇒ M = 107 ⇒ 243 mắt xích tương ứng với PTK của poilme là 243 × 107 = 26001.
❌ (c) sai vì phân tử polime thì có rất nhiều mắt xích, mà mỗi mắt xích có 1N ⇒ polime thì chắc chắn có nhiều hơn 1 N rồi (rất nhiều bạn nhầm ý này).
✔️ (d) đúng, cao su buna-N được tổng hợp từ các monome ⇝ là polime tổng hợp.
✔️ (e) đúng vì buta-1,3-dien: CH2=CH–CH=CH2 và acrilonitrin: CH2=CH–CN ⇝ đồng trùng hợp thu được cao su buna-N.
⇝ có 3/5 phát biểu đúng ⇝ Chọn đáp án A. ♥