Đáp án
1A
2B
3C
4D
5A
6C
7A
8C
9B
10C
11B
12D
13B
14B
15D
16B
17B
18D
19C
20B
21D
22B
23C
24B
25B
26C
27D
28D
29D
30D
31D
32C
33A
34B
35D
36D
37A
38A
39B
40B
Đáp án Đề minh họa số 8 thi Tốt Nghiệp Trung học Phổ Thông 2024 môn Hóa học
Câu 1 [20917]: Công thức cấu tạo của hợp chất (C17H33COO)3C3H5 có tên gọi là
A, triolein.
B, trilinolein.
C, tristearin.
D, tripanmitin.
HD: C17H33COOH là axit oleic ⇝ tương ứng (C17H33)3C3H5 có tên gọi là triolein.
Một số công thức chất béo khác thường gặp:
• tristearin: (C17H35)3C3H5.
• trilinolein: (C17H31)3C3H5.
• tripanmitin: (C15H31)3C3H5. ❒
Một số công thức chất béo khác thường gặp:
• tristearin: (C17H35)3C3H5.
• trilinolein: (C17H31)3C3H5.
• tripanmitin: (C15H31)3C3H5. ❒
Câu 2 [256264]: Chất nào sau đây không thuộc dãy đồng đẳng ankan
A, CH4.
B, C2H4.
C, C3H8.
D, C4H10.
HD: Dãy đồng đẳng ankan:

⇝ C2H4: etilen không thuộc dãy đồng đẳng ankan.

⇝ C2H4: etilen không thuộc dãy đồng đẳng ankan.
Câu 3 [982219]: Chất nào sau đây là muối trung hòa?
A, NaOH.
B, NaHCO3.
C, Na2SO4.
D, NaHSO4.
HD: NaOH là một hiđroxit bazơ ⇝ loại đáp án A.
Muối gồm muối axit và muối trung hoà; trong đó muối axit là muối có H có khả năng phân li ra H+ ⇒ B. NaHCO3 và D. NaHSO4 là hai muối axit ⇒ còn lại C. Na2SO4 là một muối trung hoà.
Muối gồm muối axit và muối trung hoà; trong đó muối axit là muối có H có khả năng phân li ra H+ ⇒ B. NaHCO3 và D. NaHSO4 là hai muối axit ⇒ còn lại C. Na2SO4 là một muối trung hoà.
Câu 4 [255668]: Anion nào sau đây có nhiều trong nước cứng có tính cứng tạm thời?
A, Cl–.
B, Mg2+, Ca2+.
C, SO42–.
D, HCO3–.
HD: Bài học phân loại nước cứng:

Thật chú ý hỏi anion ⇝ đáp án là HCO3– nhé.! ⇝ Chọn đáp án D. ♠

Thật chú ý hỏi anion ⇝ đáp án là HCO3– nhé.! ⇝ Chọn đáp án D. ♠
Câu 5 [311893]: Khi đun nóng đến 160oC, thạch cao sống mất một phần nước biến thành thạch cao nung, được dùng để nặn tượng, đúc khuôn, bó bột trong y học. Thành phần hóa học của thạch cao nung là
A, CaSO4.H2O.
B, CaSO4.2H2O.
C, CaCO3.
D, CaSO4.
HD: Thạch cao sống có công thức hóa học là CaSO4.2H2O.
Khi nung nóng, CaSO4.2H2O mất một phần nước
⇝ thu được CaSO4.H2O gọi là thạch cao nung.
Nếu nong đến bay hết nước → CaSO4 gọi là thạch cao khan. ❒
Khi nung nóng, CaSO4.2H2O mất một phần nước
⇝ thu được CaSO4.H2O gọi là thạch cao nung.
Nếu nong đến bay hết nước → CaSO4 gọi là thạch cao khan. ❒
Câu 6 [679246]: Ô nhiễm không khí có thể tạo ra mưa axit, gây ra tác hại rất lớn với môi trường. Hai khí nào sau đây đều là nguyên nhân gây ra mưa axit?
A, H2S và N2.
B, CO2 và O2.
C, SO2 và NO2.
D, NH3 và HCl.
HD: SO2, NO2 là hai khí chính gây ra mưa axit. Các khí này hòa tan với hơi nước trong không khí tạo thành các axit. Khi trời mưa, các hạt axit này tan lẫn vào nước mưa, làm độ pH của nước mưa giảm. Nếu nước mưa có độ pH dưới 5,6 được gọi là mưa axit. Do có độ chua khá lớn, nước mưa có thể hoà tan được một số bụi kim loại và oxit kim loại có trong không khí như oxit chì,... làm cho nước mưa trở nên độc hơn nữa đối với cây cối, vật nuôi và con người.


Câu 7 [60552]: Cho FeS tác dụng với dung dịch HCl, chất khí thu được là
A, H2S.
B, Cl2.
C, SO2.
D, H2.
HD: Phản ứng xảy ra:
FeS + 2HCl → FeCl2 + H2S.
FeS + 2HCl → FeCl2 + H2S.
Câu 8 [911505]: Kim loại nào sau đây có nhiệt độ nóng chảy cao nhất?
A, Cr.
B, Ag.
C, W.
D, Fe.
HD: ► Một số cái NHẤT của kim loại:
🥇 Dẻo nhất: vàng (Au).
🥇 Dẫn điện, dẫn nhiệt tốt nhất: Bạc (Ag).
🥇 Kim loại cứng nhất: crom (Cr).
🥇 Kim loại mềm nhất: các kim loại kiềm.
🥇 Nhiệt nóng chảy cao nhất: vonfram (W).
🥇 Nhiệt nóng chảy thấp nhất: thủy ngân (Hg).
🥇 Khối lượng riêng thấp nhất: liti (Li).
🥇 Khối lượng riêng cao nhất: osmi (Os).
🥇 Dẻo nhất: vàng (Au).
🥇 Dẫn điện, dẫn nhiệt tốt nhất: Bạc (Ag).
🥇 Kim loại cứng nhất: crom (Cr).
🥇 Kim loại mềm nhất: các kim loại kiềm.
🥇 Nhiệt nóng chảy cao nhất: vonfram (W).
🥇 Nhiệt nóng chảy thấp nhất: thủy ngân (Hg).
🥇 Khối lượng riêng thấp nhất: liti (Li).
🥇 Khối lượng riêng cao nhất: osmi (Os).
Câu 9 [60699]: Trong các hợp chất sau, hợp chất nào Cr có số oxi hóa thấp nhất?
A, Cr2(SO4)3.
B, CrCl2.
C, K2CrO4.
D, K2Cr2O7.
HD: Phân tích các đáp án:
| Công thức | A. Cr2(SO4)3. | B. CrCl2. | C. K2CrO4. | D. K2Cr2O7. |
| Số oxi hoá của crom | +3 | +2 (✔️) | +6 | +6 |
Câu 10 [224890]: Kim loại Zn có thể khử được ion nào sau đây?
A, Mg2+.
B, Sr2+.
C, H+.
D, Na+.
HD: Dãy điện hoá: 
⇝ Zn có thể khử được ion H+ tạo khí H2.
☆ Phản ứng: Zn + 2H+ → Zn2+ + H2↑.
⇝ Chọn đáp án C. ♣

⇝ Zn có thể khử được ion H+ tạo khí H2.
☆ Phản ứng: Zn + 2H+ → Zn2+ + H2↑.
⇝ Chọn đáp án C. ♣
Câu 11 [973510]: Quặng nào sau đây có thành phần chính là Al2O3?
A, Hematit đỏ.
B, Boxit.
C, Manhetit.
D, Criolit.
HD: Phân tích các đáp án:
| Tên quặng | A. Hemantit đỏ. | B. Boxit. | C. Manhetit. | D. Criolit. |
| Thành phần chính | Fe2O3 | Al2O3.2H2O (✔️) | Fe3O4 | 3NaF.AlF3 |
Câu 12 [679442]: Chất nào sau đây thuộc loại monosaccarit?
A, Saccarozơ.
B, Xenlulozơ.
C, Tinh bột.
D, Glucozơ.
HD: Bài học phân loại hợp chất cacbohiđrat:

⇒ Trong 4 phương án, glucozơ là monosaccarit ⇝ Chọn đáp án D. ♠

⇒ Trong 4 phương án, glucozơ là monosaccarit ⇝ Chọn đáp án D. ♠
Câu 13 [352164]: Trong phân tử Gly-Ala-Val, amino axit đầu N chứa nhóm
A, NO2.
B, NH2.
C, COOH.
D, CHO.
Đáp án: B
Câu 14 [59356]: Để thu được kim loại Cu từ dung dịch CuSO4 bằng phương pháp thủy luyện, ta không thể dùng kim loại nào sau đây?
A, Mg.
B, Ca.
C, Fe.
D, Zn.
HD: Thứ tự dãy điện hóa các kim loại: Ca > Mg > Zn > Fe > Cu.
⇝ các kim loại đều đứng trước Cu trong dãy điện hóa.
Tuy nhiên, trường hợp các kim loại kiềm, kiềm thổ như Na, K, Ca, Ba
phản ứng mãnh liệt với H2O tạo dung dịch bazơ trước:
Ca + 2H2O → Ca(OH)2 + H2↑.
Sau đó: Ca(OH)2 + CuSO4 → Cu(OH)2↓ + CaSO4.
⇒ không dùng được Ca để đẩy Cu2+ ra khỏi dung dịch bằng phương pháp thủy luyện. ❒
⇝ các kim loại đều đứng trước Cu trong dãy điện hóa.
Tuy nhiên, trường hợp các kim loại kiềm, kiềm thổ như Na, K, Ca, Ba
phản ứng mãnh liệt với H2O tạo dung dịch bazơ trước:
Ca + 2H2O → Ca(OH)2 + H2↑.
Sau đó: Ca(OH)2 + CuSO4 → Cu(OH)2↓ + CaSO4.
⇒ không dùng được Ca để đẩy Cu2+ ra khỏi dung dịch bằng phương pháp thủy luyện. ❒
Câu 15 [973592]: Dung dịch Na2CO3 tác dụng được với dung dịch nào sau đây?
A, Na2SO4.
B, KNO3.
C, KOH.
D, CaCl2.
HD: trong dung dịch: Na2CO3 → 2Na+ + CO32–.
Mà Ca2+ + CO32– → CaCO3↓ nên có phản ứng với CaCl2.
Mà Ca2+ + CO32– → CaCO3↓ nên có phản ứng với CaCl2.
Câu 16 [981794]: Chất nào sau đây là amin?
A, CH3COOH.
B, CH3NH2.
C, C2H5OH.
D, CH3COOCH3.
HD: Phân tích các đáp án:
• CH3COOH: axit cacboxylic.
• CH3NH2: amin.
• C2H5OH: ancol.
• CH3COOCH3: este.
• CH3COOH: axit cacboxylic.
• CH3NH2: amin.
• C2H5OH: ancol.
• CH3COOCH3: este.
Câu 17 [983260]: Este X có công thức phân tử C4H8O2. Thủy phân X trong dung dịch H2SO4 loãng, đun nóng, thu được sản phẩm gồm ancol etylic và chất hữu cơ Y. Công thức của Y là
A, CH3OH.
B, CH3COOH.
C, C2H5COOH.
D, HCOOH.
HD: Phản ứng thuỷ phân: C4H8O2 + H2O ⇄H2SO4, to⇄ Y + C2H5OH.
⇒ Bảo toàn thấy ngay Y là CH3COOH và cấu tạo X: CH3COOC2H5 ⇝ Chọn đáp án B. ♦
⇒ Bảo toàn thấy ngay Y là CH3COOH và cấu tạo X: CH3COOC2H5 ⇝ Chọn đáp án B. ♦
Câu 18 [20337]: Polime nào sau đây là polime bán tổng hợp?
A, Tơ olon.
B, Tơ tằm.
C, Tơ nilon-6.
D, Tơ visco.
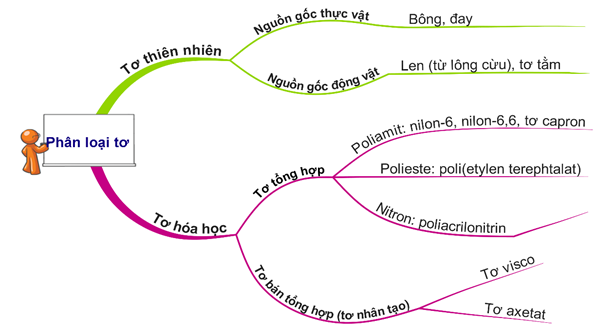
⇝ Tơ visco là tơ bán tổng hợp (hay nhân tạo) ⇝ Chọn đáp án D. ♠ .
Câu 19 [60064]: Cho kim loại X vào dung dịch H2SO4 loãng vừa thấy có khí bay ra vừa thu được chất kết tủa. X là
A, Be.
B, Mg.
C, Ba.
D, Cu.
HD: ☆ Phân tích các đáp án:
☒ A. Be + H2SO4 → BeSO4 + H2↑ (không thu được kết tủa).
☒ B. Mg + H2SO4 → MgSO4 + H2↑ (không thu được kết tủa).
☑ C. Ba + H2SO4 → BaSO4↓ + H2↑ (thỏa mãn thu được kết tủa và khí).
☒ D. Cu + H2SO4 không xảy ra phản ứng. ❒
☒ A. Be + H2SO4 → BeSO4 + H2↑ (không thu được kết tủa).
☒ B. Mg + H2SO4 → MgSO4 + H2↑ (không thu được kết tủa).
☑ C. Ba + H2SO4 → BaSO4↓ + H2↑ (thỏa mãn thu được kết tủa và khí).
☒ D. Cu + H2SO4 không xảy ra phản ứng. ❒
Câu 20 [973509]: Dung dịch nào sau đây tác dụng được với kim loại Cu?
A, HCl.
B, HNO3 loãng.
C, H2SO4 loãng.
D, KOH.
HD: HNO3 loãng phản ứng được với kim loại Cu:
3Cu + 8HNO3 → 3Cu(NO3)2 + 2NO↑ + 4H2O.
3Cu + 8HNO3 → 3Cu(NO3)2 + 2NO↑ + 4H2O.
Câu 21 [352165]: Cho Fe2O3 vào dung dịch H2SO4 (loãng, dư) thu được dung dịch X. Thêm tiếp dung dịch BaCl2 đến dư vào X, thu được kết tủa Y. Công thức của Y là
A, FeCl3.
B, Fe2(SO4)3.
C, Fe(OH)3.
D, BaSO4.
Đáp án: D
Câu 22 [679810]: Thực hiện phản ứng este hóa giữa 4,6 gam ancol etylic với lượng dư axit axetic, thu được 4,4 gam este. Hiệu suất phản ứng este hóa là
A, 30%.
B, 50%.
C, 60%.
D, 25%.
HD: Phản ứng este hoá xảy ra như sau:
CH3COOH + C2H5OH ⇄ CH3COOC2H5 + H2O.
Giả thiết: neste = 4,4 ÷ 88 = 0,05 mol; nancol = 4,6 ÷ 46 = 0,1 mol.
► axit dùng dư nên hiệu suất tính theo lượng ancol.
nancol tính theo este = 0,05 mol ⇒ hiệu suất phản ứng = 0,5 ÷ 0,1 × 100% = 50%.
⇝ Chọn đáp án B. ♦
CH3COOH + C2H5OH ⇄ CH3COOC2H5 + H2O.
Giả thiết: neste = 4,4 ÷ 88 = 0,05 mol; nancol = 4,6 ÷ 46 = 0,1 mol.
► axit dùng dư nên hiệu suất tính theo lượng ancol.
nancol tính theo este = 0,05 mol ⇒ hiệu suất phản ứng = 0,5 ÷ 0,1 × 100% = 50%.
⇝ Chọn đáp án B. ♦
Câu 23 [97304]: Phát biểu nào sau đây đúng?
A, Phân tử xenlulozơ được cấu tạo từ các gốc fructozơ.
B, Fructozơ không có phản ứng tráng bạc.
C, Amilozơ có cấu trúc mạch không phân nhánh.
D, Saccarozơ không tham gia phản ứng thủy phân.
HD: Xem xét các phát biểu:
A. sai vì phân tử xenlulozơ được cấu tạo từ các gốc β–glucozơ:
![567408[LG2].png](https://m.moon.vn/Images/Teachers/rongden_167/ProS2018/TAP%20II/567408[LG2].png)
B. sai vì trong môi trường OH– (do NH3) ở phản ứng tráng bạc, fructozơ ⇄ glucozơ:
![567369[LG].png](https://m.moon.vn/Images/Teachers/rongden_167/ProS2018/TAP%20II/567369[LG].png)
C. đúng.
![567216[LG].png](https://m.moon.vn/Images/Teachers/rongden_167/ProS2018/TAP%20II/567216[LG].png)
D. sai vì saccarozơ là đisaccarit bị thủy phân trong môi trường axit:
![567379[LG2].png](https://m.moon.vn/Images/Teachers/rongden_167/ProS2018/TAP%20II/567379[LG2].png)
⇝ Chọn đáp án C. ♣
A. sai vì phân tử xenlulozơ được cấu tạo từ các gốc β–glucozơ:
![567408[LG2].png](https://m.moon.vn/Images/Teachers/rongden_167/ProS2018/TAP%20II/567408[LG2].png)
B. sai vì trong môi trường OH– (do NH3) ở phản ứng tráng bạc, fructozơ ⇄ glucozơ:
C. đúng.
![567216[LG].png](https://m.moon.vn/Images/Teachers/rongden_167/ProS2018/TAP%20II/567216[LG].png)
D. sai vì saccarozơ là đisaccarit bị thủy phân trong môi trường axit:
![567379[LG2].png](https://m.moon.vn/Images/Teachers/rongden_167/ProS2018/TAP%20II/567379[LG2].png)
⇝ Chọn đáp án C. ♣
Câu 24 [679808]: Cho các polime sau: poli(vinyl clorua), poli(metyl acrylat), poli(etylen terephtalat), nilon-6,6. Số polime được điều chế bằng phản ứng trùng ngưng là
A, 1.
B, 2.
C, 3.
D, 4.
HD: Bài học phân loại tổng hợp este:
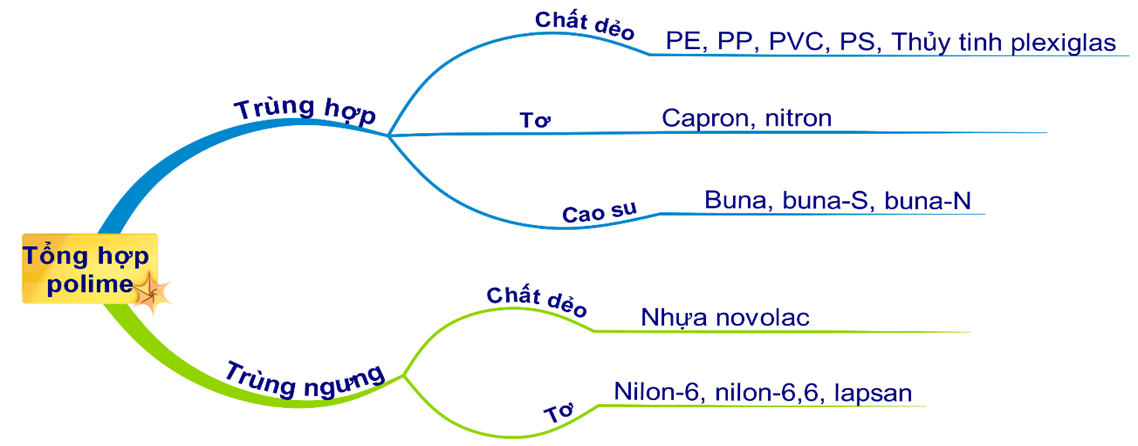
⇝ Trong dãy có poli(etylen terephtalat) và nilon-6,6 được điều chế bằng phản ứng trùng ngưng.

⇝ Trong dãy có poli(etylen terephtalat) và nilon-6,6 được điều chế bằng phản ứng trùng ngưng.
Câu 25 [6913]: Cho 1 mol este X (C9H10O2) tác dụng vừa đủ với 2 mol NaOH, thu được dung dịch không có phản ứng tráng bạc. Số công thức cấu tạo phù hợp của X là
A, 3.
B, 4.
C, 2.
D, 6.
Giải: Các CTCT thỏa mãn là CH3COOC6H4CH3 (o-, m-, p-) và C2H5COOC6H5.
Câu 26 [679761]: Dùng Al khử hoàn toàn 4,8 gam Fe2O3 thành Fe bằng phản ứng nhiệt nhôm. Khối lượng Fe thu được là
A, 1,68 gam.
B, 2,80 gam.
C, 3,36 gam.
D, 0,84 gam.
HD: Phản ứng: 2Al + Fe2O3 ––to→ 2Fe + Al2O3.
Giả thiết: nFe2O3 = 4,8 ÷ 160 = 0,03 mol.
⇒ Yêu cầu mFe thu được = 0,03 × 2 × 56 = 3,36 gam.
Giả thiết: nFe2O3 = 4,8 ÷ 160 = 0,03 mol.
⇒ Yêu cầu mFe thu được = 0,03 × 2 × 56 = 3,36 gam.
Câu 27 [679714]: Cho 54 gam glucozơ lên men rượu với hiệu suất 75%, thu được m gam C2H5OH. Giá trị của m là
A, 36,80.
B, 10,35.
C, 27,60.
D, 20,70.
HD: Tỉ lệ phản ứng lên men rượu: 1glucozơ ––to→ 2C2H5OH + 2CO2↑.
Giả thiết nglucozơ = 54 ÷ 180 = 0,3 mol; chú ý hiệu suất 75%
⇒ nC2H5OH thu được = 0,3 × 2 × 0,75 = 0,45 mol ⇒ m = 0,45 × 46 = 20,7 gam.
Giả thiết nglucozơ = 54 ÷ 180 = 0,3 mol; chú ý hiệu suất 75%
⇒ nC2H5OH thu được = 0,3 × 2 × 0,75 = 0,45 mol ⇒ m = 0,45 × 46 = 20,7 gam.
Câu 28 [679763]: Cho 5,9 gam amin X (no, đơn chức, mạch hở) tác dụng hết với dung dịch HCl dư, thu được 9,55 gam muối. Số nguyên tử H trong phân tử X là
A, 7.
B, 11.
C, 5.
D, 9.
HD: amin no, đơn chức mạch hở có dạng CnH2n + 3N.
☆ Phản ứng với axit: CnH2n + 3N + HCl → CnH2n + 4NCl.
từ giả thiết ta có mHCl = mmuối – mamin = 9,55 – 5,9 = 3,65 gam.
⇒ namin = nHCl = 3,65 ÷ 36,5 = 0,1 mol ⇒ Mamin = 5,9 ÷ 0,1 = 59.
⇒ 14n + 17 = 59 ⇒ n = 3 ⇒ ∑số H = 2n + 3 = 9 ⇝ Chọn đáp án D. ♠
☆ Phản ứng với axit: CnH2n + 3N + HCl → CnH2n + 4NCl.
từ giả thiết ta có mHCl = mmuối – mamin = 9,55 – 5,9 = 3,65 gam.
⇒ namin = nHCl = 3,65 ÷ 36,5 = 0,1 mol ⇒ Mamin = 5,9 ÷ 0,1 = 59.
⇒ 14n + 17 = 59 ⇒ n = 3 ⇒ ∑số H = 2n + 3 = 9 ⇝ Chọn đáp án D. ♠
Câu 29 [352281]: Phát biểu nào sau đây sai?
A, Kim loại xesi dùng để chế tạo tế bào quang điện.
B, Vật dụng bằng nhôm bền trong không khí và nước.
C, Hợp kim liti–nhôm siêu nhẹ, được dùng trong kĩ thuật hàng không.
D, Dây điện làm bằng sắt dẫn điện tốt hơn so với nhôm.
HD: Phân tích các đáp án:
✔️ A. đúng vì 1 electron ngoài cùng của Cs (cấu hình e: [Xe]6s1) xa hạt nhân nên rất dễ bị bứt e ⇝ chế tạo tế bào quang điện.
✔️ B. đúng, bản thân Al bền do lớp oxit Al2O3 rất bền bảo vệ bề mặt cho nhôm.
✔️ C. Li là nguyên tố có khối lượng riêng nhỏ nhất ⇝ hợp kim Li-Al siêu nhẹ và bền ⇝ được dùng trong kĩ thuật hàng không.
❌ D. sai, thứ tự dẫn điện: Ag > Cu > Au > Al > Fe.
✔️ A. đúng vì 1 electron ngoài cùng của Cs (cấu hình e: [Xe]6s1) xa hạt nhân nên rất dễ bị bứt e ⇝ chế tạo tế bào quang điện.
✔️ B. đúng, bản thân Al bền do lớp oxit Al2O3 rất bền bảo vệ bề mặt cho nhôm.
✔️ C. Li là nguyên tố có khối lượng riêng nhỏ nhất ⇝ hợp kim Li-Al siêu nhẹ và bền ⇝ được dùng trong kĩ thuật hàng không.
❌ D. sai, thứ tự dẫn điện: Ag > Cu > Au > Al > Fe.
Câu 30 [118491]: Nung nóng 3,32 gam hỗn hợp gồm Mg, Al, Cu trong bình kín chứa khí O2. Sau một thời gian phản ứng, thu được 4,28 gam chất rắn X. Biết X tác dụng vừa đủ với V lít dung dịch HCl 0,8M, thu được 1,344 lít khí H2 (đktc). Giá trị của V là
A, 0,5.
B, 0,4.
C, 0,2.
D, 0,3.
HD: 3,32 gam (Mg, Al, Cu) + O2 –––to–→ 4,28 gam X.
⇒ BTKL có mO trong X = (4,28 – 3,32) ÷ 16 = 0,06 mol.
phản ứng với HCl, toàn bộ O trong oxit chuyển hết về H2O
⇒ có nH2O = 0,06 mol; đề lại cho nH2↑ = 0,06 mol
⇒ bảo toàn H có ∑nHCl = 2nH2O + 2nH2↑ = 0,24 mol.
⇒ V = n ÷ CM = 0,24 ÷ 0,8 = 0,3 lít. Chọn đáp án D. ♥.
⇒ BTKL có mO trong X = (4,28 – 3,32) ÷ 16 = 0,06 mol.
phản ứng với HCl, toàn bộ O trong oxit chuyển hết về H2O
⇒ có nH2O = 0,06 mol; đề lại cho nH2↑ = 0,06 mol
⇒ bảo toàn H có ∑nHCl = 2nH2O + 2nH2↑ = 0,24 mol.
⇒ V = n ÷ CM = 0,24 ÷ 0,8 = 0,3 lít. Chọn đáp án D. ♥.
Câu 31 [352282]: Cho các phát biểu sau :
(a) Kim loại Al tan được trong dung dịch HNO3 đặc, nguội.
(b) Trong tự nhiên, kim loại Al tồn tại ở cả dạng hợp chất và đơn chất.
(c) Cho dung dịch Ba(OH)2 dư vào dung dịch Al2(SO4)3 không thu được kết tủa.
(d) Al bền trong trong không khí do có màng oxit bảo vệ.
(e) Công thức hóa học của phèn chua là K2SO4.Al2(SO4)3.24H2O.
Số phát biểu đúng là
(a) Kim loại Al tan được trong dung dịch HNO3 đặc, nguội.
(b) Trong tự nhiên, kim loại Al tồn tại ở cả dạng hợp chất và đơn chất.
(c) Cho dung dịch Ba(OH)2 dư vào dung dịch Al2(SO4)3 không thu được kết tủa.
(d) Al bền trong trong không khí do có màng oxit bảo vệ.
(e) Công thức hóa học của phèn chua là K2SO4.Al2(SO4)3.24H2O.
Số phát biểu đúng là
A, 4.
B, 3.
C, 5.
D, 2.
Đáp án: D
Câu 32 [352283]: Tiến hành điều chế Fe(OH)2 theo các bước sau:
Bước 1: Cho đinh sắt đã cạo sạch gỉ vào ống nghiệm (1). Thêm tiếp 3 – 4 ml dung dịch HCl loãng vào (1) và đun nóng nhẹ.
Bước 2: Đun sôi 4 – 5 ml dung dịch NaOH trong ống nghiệm (2).
Bước 3: Rót nhanh 2 – 3 ml dung dịch thu được ở bước 1 vào dung dịch NaOH, ghi nhận ngay màu kết tủa quan sát được.
Bước 4: Ghi nhận màu kết tủa quan sát được ở cuối buổi thí nghiệm. Cho các phát biểu sau:
(a) Sau bước 1, thu được chất khí không màu và dung dịch thu được có màu lục nhạt.
(b) Mục đích chính của bước 2 là đẩy khí O2 hòa tan có trong dung dịch NaOH.
(c) Sau bước 3, thu được kết tủa màu trắng hơi xanh.
(d) Màu kết tủa ghi nhận được ở bước 4 là màu nâu đỏ.
(e) Quan sát phần dung dịch còn lại trong ống nghiệm (1) ở cuối buổi thí nghiệm thấy màu lục nhạt chuyển dần thành xanh lam.
Số phát biểu đúng là
Bước 1: Cho đinh sắt đã cạo sạch gỉ vào ống nghiệm (1). Thêm tiếp 3 – 4 ml dung dịch HCl loãng vào (1) và đun nóng nhẹ.
Bước 2: Đun sôi 4 – 5 ml dung dịch NaOH trong ống nghiệm (2).
Bước 3: Rót nhanh 2 – 3 ml dung dịch thu được ở bước 1 vào dung dịch NaOH, ghi nhận ngay màu kết tủa quan sát được.
Bước 4: Ghi nhận màu kết tủa quan sát được ở cuối buổi thí nghiệm. Cho các phát biểu sau:
(a) Sau bước 1, thu được chất khí không màu và dung dịch thu được có màu lục nhạt.
(b) Mục đích chính của bước 2 là đẩy khí O2 hòa tan có trong dung dịch NaOH.
(c) Sau bước 3, thu được kết tủa màu trắng hơi xanh.
(d) Màu kết tủa ghi nhận được ở bước 4 là màu nâu đỏ.
(e) Quan sát phần dung dịch còn lại trong ống nghiệm (1) ở cuối buổi thí nghiệm thấy màu lục nhạt chuyển dần thành xanh lam.
Số phát biểu đúng là
A, 2.
B, 3.
C, 4.
D, 1.
HD: Phân tích thí nghiệm:
• Bước 1: xảy ra phản ứng Fe + 2HCl → FeCl2 + H2↑.
• Bước 2 + 3: xảy ra phản ứng: FeCl2 + 2NaOH → Fe(OH)2↓ + 2NaCl.
⇒ Hiện tượng quan sát được: kết tủa màu trắng hơi xanh (là Fe(OH)2).
• Bước 4: sau một thời gian (cuối buổi), O2 trong không khí và nước sẽ oxi hóa Fe(OH)2 tạo Fe(OH)3 màu nâu đỏ:
Fe(OH)2 + O2 + H2O → Fe(OH)3.
☆ Phân tích các phát biểu:
✔️ (a) đúng, phản ứng cho thấy có khí H2 không màu thoát ra và dung dịch chứa muối FeCl2 có màu lục nhạt.
✔️ (b) đúng, vì nếu có O2 trong dung dịch sẽ dẫn đến hiện tượng giống như ở bước 4, ảnh hưởng đến mục đích thí nghiệm là điều chế Fe(OH)2.
✔️ (c) đúng theo phân tích bước 3trên.
✔️ (d) đúng theo phân tích bước 4 trên.
❌ (e) sai, màu trắng hơi xanh ⇝ nâu đỏ.
⇝ có 4/5 phát biểu đúng ⇝ Chọn đáp án C. ♣
• Bước 1: xảy ra phản ứng Fe + 2HCl → FeCl2 + H2↑.
• Bước 2 + 3: xảy ra phản ứng: FeCl2 + 2NaOH → Fe(OH)2↓ + 2NaCl.
⇒ Hiện tượng quan sát được: kết tủa màu trắng hơi xanh (là Fe(OH)2).
• Bước 4: sau một thời gian (cuối buổi), O2 trong không khí và nước sẽ oxi hóa Fe(OH)2 tạo Fe(OH)3 màu nâu đỏ:
Fe(OH)2 + O2 + H2O → Fe(OH)3.
☆ Phân tích các phát biểu:
✔️ (a) đúng, phản ứng cho thấy có khí H2 không màu thoát ra và dung dịch chứa muối FeCl2 có màu lục nhạt.
✔️ (b) đúng, vì nếu có O2 trong dung dịch sẽ dẫn đến hiện tượng giống như ở bước 4, ảnh hưởng đến mục đích thí nghiệm là điều chế Fe(OH)2.
✔️ (c) đúng theo phân tích bước 3trên.
✔️ (d) đúng theo phân tích bước 4 trên.
❌ (e) sai, màu trắng hơi xanh ⇝ nâu đỏ.
⇝ có 4/5 phát biểu đúng ⇝ Chọn đáp án C. ♣
Câu 33 [118215]: Cho m gam hỗn hợp X gồm MgO, CuO, Cu2S, MgS (oxi chiếm 30% khối lượng) tan hết trong dung dịch H2SO4 và NaNO3, thu được dung dịch Y chỉ chứa 4m gam muối trung hòa và 0,672 lít(đktc) hỗn hợp khí gồm NO2, SO2 ( không có sản phẩm khử nào khác). Cho Y tác dụng vừa đủ với dung dịch Ba(NO3)2 được dung dịch Z và 9,32 gam kết tủa. Cô cạn dung dịch Z rồi nung đến khối lượng không đổi, thu được 2,688 lít khí (đktc) hỗn hợp khí có tỉ khối so với H2 bằng 19,5. Giá trị của m gần nhất với giá trị nào sau đây?
A, 3,0.
B, 2,5.
C, 3,5.
D, 4,0.
m gam X  +
+  → 0,03 mol
→ 0,03 mol  + H2O + 4m muối
+ H2O + 4m muối
 ↓ 0,04 mol BaSO4 + Z
↓ 0,04 mol BaSO4 + Z  0,12 mol
0,12 mol 
Nhận thấy chất kết tủa là BaSO4 : 0,04 mol → trong muối chứa SO42- : 0,04 mol, và Ba(NO3)2 : 0,04 mol
Gọi số mol của NO2 và O2 lần lượt là x, y mol
Ta có hệ →
→ 
Có nNa+ = 2. ( 0,06 - ) = 0,09 mol ( viết pt nhìn thấy)
) = 0,09 mol ( viết pt nhìn thấy)
Bảo toàn nguyên tố N → nNO3- ( muối) = 2.nNO2 + nNaNO3 - 2nBa(NO3)2 =0,06 + 0,09- 2. 0,04 = 0,07 mol → nNO2 ( khí) = 0,09 - 0,07 = 0,02 mol, nSO2 = 0,01 mol
Ta có hệ →
→ 
→ m = .16 ≈ 2,959 . Đáp án A.
.16 ≈ 2,959 . Đáp án A.
 +
+  → 0,03 mol
→ 0,03 mol  + H2O + 4m muối
+ H2O + 4m muối
 ↓ 0,04 mol BaSO4 + Z
↓ 0,04 mol BaSO4 + Z  0,12 mol
0,12 mol 
Nhận thấy chất kết tủa là BaSO4 : 0,04 mol → trong muối chứa SO42- : 0,04 mol, và Ba(NO3)2 : 0,04 mol
Gọi số mol của NO2 và O2 lần lượt là x, y mol
Ta có hệ
 →
→ 
Có nNa+ = 2. ( 0,06 -
 ) = 0,09 mol ( viết pt nhìn thấy)
) = 0,09 mol ( viết pt nhìn thấy) Bảo toàn nguyên tố N → nNO3- ( muối) = 2.nNO2 + nNaNO3 - 2nBa(NO3)2 =0,06 + 0,09- 2. 0,04 = 0,07 mol → nNO2 ( khí) = 0,09 - 0,07 = 0,02 mol, nSO2 = 0,01 mol
Ta có hệ
 →
→ 
→ m =
 .16 ≈ 2,959 . Đáp án A.
.16 ≈ 2,959 . Đáp án A.
Câu 34 [61906]: Hỗn hợp khí X (đktc) gồm O2 và O3 có tỉ khối so với H2 là 20. Cho 0,896 lít X tác dụng hết với cacbon nóng đỏ, thu được hỗn hợp khí Y có tỉ khối so với X là 0,8. Toàn bộ Y khử được tối đa bao nhiêu gam CuO nung nóng?
A, 1,6 gam.
B, 4,8 gam.
C, 3,2 gam.
D, 5,6 gam.
HD: ☆ xử lí khéo léo chút giả thiết tỉ khối hỗn hợp X:
có MX = 20 × 2 = 40. nX = 0,04 mol → mX = 1,6 gam → ∑nO trong X = 0,1 mol.
Phản ứng: C + O → CO || C + 2O → CO2. ||⇒ Y gồm CO và CO2.
có MY = 40 × 0,8 = 32 → trong Y: nCO : nCO2 = 3 : 1.
lại biết ∑nO = 0,1 mol như tính trên → nCO = 0,06 mol; nCO2 = 0,02 mol.
Phản ứng: CO + CuO → Cu + CO2↑ ||⇒ nCuO = nCO = 0,06 mol
⇒ tối đa lượng CuO bị khử bởi Y là: m = 0,06 × 80 = 4,8 gam. ❒
có MX = 20 × 2 = 40. nX = 0,04 mol → mX = 1,6 gam → ∑nO trong X = 0,1 mol.
Phản ứng: C + O → CO || C + 2O → CO2. ||⇒ Y gồm CO và CO2.
có MY = 40 × 0,8 = 32 → trong Y: nCO : nCO2 = 3 : 1.
lại biết ∑nO = 0,1 mol như tính trên → nCO = 0,06 mol; nCO2 = 0,02 mol.
Phản ứng: CO + CuO → Cu + CO2↑ ||⇒ nCuO = nCO = 0,06 mol
⇒ tối đa lượng CuO bị khử bởi Y là: m = 0,06 × 80 = 4,8 gam. ❒
Câu 35 [911600]: Cho 13,44 lít (đktc) hỗn hợp X gồm C2H2 và H2 qua bình đựng Ni (nung nóng), thu được hỗn hợp Y (chỉ chứa ba hiđrocacbon) có tỉ khối so với H2 là 14,4. Biết Y phản ứng tối đa với a mol Br2 trong dung dịch. Giá trị của a là
A, 0,25.
B, 0,20.
C, 0,10.
D, 0,15.
HD: Gọi số mol C2H2 là b mol. Vì Y chỉ chứa ba hiđrocacbon ⇒ nY = b mol.
Lại có: mX = mY ⇒ 26b + (0,6 – b) × 2 = 14,4 × 2 × b ⇒ b = 0,25.
► Nhận xét: 0,25 mol C2H2 cần 0,35 mol H2 và a mol Br2 để làm no
⇒ 0,25 × 2 = 0,35 + a ⇒ a = 0,15 ⇝ Chọn đáp án D. ♠
Lại có: mX = mY ⇒ 26b + (0,6 – b) × 2 = 14,4 × 2 × b ⇒ b = 0,25.
► Nhận xét: 0,25 mol C2H2 cần 0,35 mol H2 và a mol Br2 để làm no
⇒ 0,25 × 2 = 0,35 + a ⇒ a = 0,15 ⇝ Chọn đáp án D. ♠
Câu 36 [311731]: Cho sơ đồ phản ứng sau (đúng với tỉ lệ mol các chất):
(a) X (C7H10O4) + 2NaOH X2 + X3 + X4.
X2 + X3 + X4.
(b) X2 + H2SO4 X5 + Na2SO4.
X5 + Na2SO4.
(c) 2X3 C2H6O + H2O.
C2H6O + H2O.
(d) X5 + HBr
Biết X4 là hợp chất hữu cơ và X6, X7 là đồng phân của nhau. Phát biểu nào sau đây sai?
(a) X (C7H10O4) + 2NaOH
 X2 + X3 + X4.
X2 + X3 + X4.
(b) X2 + H2SO4
 X5 + Na2SO4.
X5 + Na2SO4.
(c) 2X3
 C2H6O + H2O.
C2H6O + H2O.
(d) X5 + HBr

Biết X4 là hợp chất hữu cơ và X6, X7 là đồng phân của nhau. Phát biểu nào sau đây sai?
A, Trong phân tử chất X chứa 2 nhóm –CH3.
B, Đun nóng chất X4 với H2SO4 đặc ở 170oC thu được một anken duy nhất.
C, Chất X không có đồng phân hình học.
D, Chất X2 có công thức C5H4O4Na2.
HD: ☆ Các phản ứng xảy ra theo sơ đồ và đúng với tỉ lệ mol → suy luận nhanh:
Từ (3) có X3 chỉ chứa 1C ⇒ là CH3OH.
Phản ứng: 2CH3OH ––H2SO4, to→ CH3OCH3 + H2O.
Từ (2) → X5 là axit cacboxylic hai chức, kết hợp (4) và X có 3π (2πC=O và còn 1πC=C nữa) → X5 có 1πC=C ở dạng bất đối xứng ⇒ số C tối thiếu mà X5 có là 4 và dạng CH2=C(COOH)2.
Theo tối thiểu này, C7 = C4 + C1 + C2 cũng là cách phân chia duy nhất.
⇒ X5 đúng là C4 và X3 còn lại là C2 tương ứng với cấu tạo là C2H5OH.
Rõ hơn: (1) C7H10O4 + 2NaOH → CH2=CH(COONa)2 + CH3OH + C2H5OH.
► Xét các phát biểu:
☑ A. đúng. Trong phân tử chất X chứa 2 nhóm CH3 (X: CH2=C(COOCH3)(COOCH2CH3)).
☑ B. đúng. Đun phản ứng: C2H5OH (X4) ––H2SO4, to→ CH2=CH2 + H2O.
☑ C. đúng. Chất X không có đồng phân hình học.
☒ D. sai. Chất X2 là CH2=CH(COONa)2 tương ứng với công thức phân tử C4H3O4Na2. ❒
Từ (3) có X3 chỉ chứa 1C ⇒ là CH3OH.
Phản ứng: 2CH3OH ––H2SO4, to→ CH3OCH3 + H2O.
Từ (2) → X5 là axit cacboxylic hai chức, kết hợp (4) và X có 3π (2πC=O và còn 1πC=C nữa) → X5 có 1πC=C ở dạng bất đối xứng ⇒ số C tối thiếu mà X5 có là 4 và dạng CH2=C(COOH)2.
Theo tối thiểu này, C7 = C4 + C1 + C2 cũng là cách phân chia duy nhất.
⇒ X5 đúng là C4 và X3 còn lại là C2 tương ứng với cấu tạo là C2H5OH.
Rõ hơn: (1) C7H10O4 + 2NaOH → CH2=CH(COONa)2 + CH3OH + C2H5OH.
► Xét các phát biểu:
☑ A. đúng. Trong phân tử chất X chứa 2 nhóm CH3 (X: CH2=C(COOCH3)(COOCH2CH3)).
☑ B. đúng. Đun phản ứng: C2H5OH (X4) ––H2SO4, to→ CH2=CH2 + H2O.
☑ C. đúng. Chất X không có đồng phân hình học.
☒ D. sai. Chất X2 là CH2=CH(COONa)2 tương ứng với công thức phân tử C4H3O4Na2. ❒
Câu 37 [679349]: Cho các chất hữu cơ mạch hở: X là axit không no có hai liên kết π trong phân tử, Y là axit no đơn chức, Z là ancol no hai chức, T là este của X, Y với Z. Đốt cháy hoàn toàn a gam hỗn hợp M gồm X và T, thu được 0,1 mol CO2 và 0,07 mol H2O. Cho 6,9 gam M phản ứng vừa đủ với dung dịch NaOH, cô cạn dung dịch sau phản ứng thu được hỗn hợp muối khan E. Đốt cháy hoàn toàn E, thu được Na2CO3; 0,195 mol CO2 và 0,135 mol H2O. Phần trăm khối lượng của T trong M có giá trị gần nhất với giá trị nào sau đây?
A, 68,7.
B, 68,1.
C, 52,3.
D, 51,3.
HD: Có một chút đặc biệt ở bài tập này do được cài số, rõ hơn ta cùng xem phân tích sau:
Giả thiết chữ ⇝ X dạng CmH2m – 2O2 (m ≥ 3) và T dạng CnH2n – 4O4 (n ≥ 6).
⇒ Phản xạ quy đổi: nhìn thấy M có dạng CH2 và OH–1.
Sử dụng: đốt a gam M thu được 0,1 mol CO2 + 0,07 mol H2O.
⇒ Từ phản xạ trên có M gồm 0,1 mol CH2 và 0,06 mol OH–1 ⇒ a = 2,3 gam.
⇒ Thu hoạch: 6,9 gam M gồm 0,3 mol C + 0,42 mol H và 0,18 mol O. Theo đó:
★ Giải: 6,9 gam M + 0,09 mol NaOH → 0,09 mol muối + x mol ancol + y mol H2O (*)
⇒ Đốt muối E thu được 0,045 mol Na2CO3 + 0,195 mol CO2 + 0,135 mol H2O.
⇒ Trong muối E: số mol C là 0,24, số mol H là 0,27 ⇒ số C trong ancol là 0,06.
Ancol Z no, hai chức, mạch hở dạng CpH2p + 2O2 ⇒ số H trong ancol là (0,12 + 2y)
⇒ Bảo toàn nguyên tố H ở (*): 0,42 + 0,09 = 0,27 + (0,12 + 2y) + 2x ⇒ x + y = 0,06.
Và đừng quên số mol ancol chính là số mol este T và số mol H2O bằng số mol axit X
⇒ bảo toàn nguyên tố O trong M ta có ngay 4x + 2y = 0,18 ⇒ giải: x = y = 0,03.
Thay lại có số mol C trong M là 0,03m + 0,03n = 0,3 ⇒ m + n = 10.
Nhận xét nhanh: nếu m ≥ 4 thì m ≥ 4 + 1 + 2 = 7 ⇒ m + n > 10 không thỏa mãn.
Do đó, chỉ có thể m = 3 ⇒ n = 7 ⇒ công thức phân tử của X là C7H10O4.
⇒ %mT trong M = 0,03 × 158 ÷ 6,9 × 100% ≈ 68,7%.
Giả thiết chữ ⇝ X dạng CmH2m – 2O2 (m ≥ 3) và T dạng CnH2n – 4O4 (n ≥ 6).
⇒ Phản xạ quy đổi: nhìn thấy M có dạng CH2 và OH–1.
Sử dụng: đốt a gam M thu được 0,1 mol CO2 + 0,07 mol H2O.
⇒ Từ phản xạ trên có M gồm 0,1 mol CH2 và 0,06 mol OH–1 ⇒ a = 2,3 gam.
⇒ Thu hoạch: 6,9 gam M gồm 0,3 mol C + 0,42 mol H và 0,18 mol O. Theo đó:
★ Giải: 6,9 gam M + 0,09 mol NaOH → 0,09 mol muối + x mol ancol + y mol H2O (*)
⇒ Đốt muối E thu được 0,045 mol Na2CO3 + 0,195 mol CO2 + 0,135 mol H2O.
⇒ Trong muối E: số mol C là 0,24, số mol H là 0,27 ⇒ số C trong ancol là 0,06.
Ancol Z no, hai chức, mạch hở dạng CpH2p + 2O2 ⇒ số H trong ancol là (0,12 + 2y)
⇒ Bảo toàn nguyên tố H ở (*): 0,42 + 0,09 = 0,27 + (0,12 + 2y) + 2x ⇒ x + y = 0,06.
Và đừng quên số mol ancol chính là số mol este T và số mol H2O bằng số mol axit X
⇒ bảo toàn nguyên tố O trong M ta có ngay 4x + 2y = 0,18 ⇒ giải: x = y = 0,03.
Thay lại có số mol C trong M là 0,03m + 0,03n = 0,3 ⇒ m + n = 10.
Nhận xét nhanh: nếu m ≥ 4 thì m ≥ 4 + 1 + 2 = 7 ⇒ m + n > 10 không thỏa mãn.
Do đó, chỉ có thể m = 3 ⇒ n = 7 ⇒ công thức phân tử của X là C7H10O4.
⇒ %mT trong M = 0,03 × 158 ÷ 6,9 × 100% ≈ 68,7%.
Câu 38 [982256]: Cho các phát biểu sau:
(a) Do có tính sát trùng, fomon được dùng để ngâm mẫu động vật.
(b) Dầu dừa có chứa chất béo chưa bão hòa (phân tử có gốc hiđrocacbon không no).
(c) Quá trình chuyển hóa tinh bột trong cơ thể người có xảy ra phản ứng thủy phân.
(d) Các mảng “riêu cua” xuất hiện khi nấu canh cua là do xảy ra sự đông tụ protein.
(e) Vải lụa tơ tằm sẽ nhanh hỏng nếu ngâm, giặt trong xà phòng có tính kiềm.
Số phát biểu đúng là
(a) Do có tính sát trùng, fomon được dùng để ngâm mẫu động vật.
(b) Dầu dừa có chứa chất béo chưa bão hòa (phân tử có gốc hiđrocacbon không no).
(c) Quá trình chuyển hóa tinh bột trong cơ thể người có xảy ra phản ứng thủy phân.
(d) Các mảng “riêu cua” xuất hiện khi nấu canh cua là do xảy ra sự đông tụ protein.
(e) Vải lụa tơ tằm sẽ nhanh hỏng nếu ngâm, giặt trong xà phòng có tính kiềm.
Số phát biểu đúng là
A, 5.
B, 3.
C, 4.
D, 2.
HD: Phân tích các phát biểu:
(a) đúng. fomon là dung dịch HCHO 37-40%, tác dụng diệt vi khuẩn đặc biệt là vi khuẩn gây thối rữa → thường dùng để ngâm xác động vật.
(b) đúng. Dầu dừa ⇝ chất lỏng ⇒ chứa các gốc axit béo không no (ngược lại, các chất béo rắn thường chứa các gốc axit béo no, đã bão hòa).
(c) đúng. Quá trình: tinh bột → đường đa → đường đôi → đường đơn, đây là các phản ứng thủy phân, chia cắt nhỏ phân tử polime bằng xúc tác enzim đặc trưng.
(d) đúng. Riêu cua là các protein dạng hình cầu, bị đông tụ khi đun nóng.
(e) đúng. Tơ tằm bản chất cũng là protein, các liên kết peptit CONH kém bền trong môi trường axit hay bazơ nên sẽ bị hỏng nếu ngâm giặt bằng xà phòng (môi trường có tính kiềm).
⇝ Tất cả 5 phát biểu đều đúng ⇝ Chọn đáp án A. ♥
(a) đúng. fomon là dung dịch HCHO 37-40%, tác dụng diệt vi khuẩn đặc biệt là vi khuẩn gây thối rữa → thường dùng để ngâm xác động vật.
(b) đúng. Dầu dừa ⇝ chất lỏng ⇒ chứa các gốc axit béo không no (ngược lại, các chất béo rắn thường chứa các gốc axit béo no, đã bão hòa).
(c) đúng. Quá trình: tinh bột → đường đa → đường đôi → đường đơn, đây là các phản ứng thủy phân, chia cắt nhỏ phân tử polime bằng xúc tác enzim đặc trưng.
(d) đúng. Riêu cua là các protein dạng hình cầu, bị đông tụ khi đun nóng.
(e) đúng. Tơ tằm bản chất cũng là protein, các liên kết peptit CONH kém bền trong môi trường axit hay bazơ nên sẽ bị hỏng nếu ngâm giặt bằng xà phòng (môi trường có tính kiềm).
⇝ Tất cả 5 phát biểu đều đúng ⇝ Chọn đáp án A. ♥
Câu 39 [352670]: Cho 5,2 gam hỗn hợp X (gồm Na, Na2O, Ba và BaO) vào H2O dư, thu được dung dịch Y và 0,02 mol H2. Sục từ từ đến hết 0,07 mol CO2 vào Y, thu được dung dịch Z và m gam kết tủa BaCO3. Sự phụ thuộc của số mol kết tủa BaCO3 (a mol) vào số mol CO2 (b mol) được biểu diễn theo đồ thị bên.
Giá trị của m là
A, 1,97.
B, 3,94.
C, 5,91.
D, 7,88.
Đáp án: B
Câu 40 [352284]: Tơ nilon – 6,6 được điều chế từ sự kết hợp giữa axit ađipic và hexametylenđiamin với tỉ lệ mol 1 : 1. Trung bình, phân tử khối của nilon – 6,6 dao động từ 20.000 đến 50.000 g/mol. Tơ nilon – 6,6 được dùng để dệt vải may mặc, vải lót săm lốp xe, dệt bít tất, bện làm dây cáp, …
Cho các phát biểu sau:
(a) Tơ nilon – 6,6 thuộc loại poliamit.
(b) Số lượng mỗi mắt xích axit ađipic và hexametylenđiamin dao động trong khoảng từ 76 đến 191 mắt xích.
(c) Phân tử nilon – 6,6 có chứa liên kết -COO-
(d) Tơ nilon – 6,6 thuộc loại polime tổng hợp.
(e) Đồng trùng hợp axit ađipic và hexametylenđiamin thu được tơ nilon – 6,6.
Số phát biểu đúng là
Cho các phát biểu sau:
(a) Tơ nilon – 6,6 thuộc loại poliamit.
(b) Số lượng mỗi mắt xích axit ađipic và hexametylenđiamin dao động trong khoảng từ 76 đến 191 mắt xích.
(c) Phân tử nilon – 6,6 có chứa liên kết -COO-
(d) Tơ nilon – 6,6 thuộc loại polime tổng hợp.
(e) Đồng trùng hợp axit ađipic và hexametylenđiamin thu được tơ nilon – 6,6.
Số phát biểu đúng là
A, 3.
B, 2.
C, 4.
D, 1.
HD: Điều chế nilon-6,6:

☆ Phân tích các phát biểu:
✔️ (a) đúng theo phản ứng trên, các liên kết CO–NH được hình thành là liên kết amit ⇒ nhiều liên kết vậy gọi là poliamit thôi.
❌ (b) sai vì mỗi mắt xích có CTPT là C12H22N2O2 ứng với PTK = 226 ⇒ số mắt xích dao động từ 20.000 ÷ 226 ≈ 88 đến 50.000 ÷ 226 ≈ 221.
❌ (c) sai vì như phân tích ý (a), poliamid chứa liên kết amit CO–NH chứ không phải este COO của polieste.
✔️ (d) đúng theo phương trình phản ứng trên, đó là quá trình tổng hợp polime.
❌ (e) sai vì phản ứng là trùng ngưng chứ không phải trùng hợp.
⇝ có 2/5 phát biểu đúng ⇝ Chọn đáp án B. ♦

☆ Phân tích các phát biểu:
✔️ (a) đúng theo phản ứng trên, các liên kết CO–NH được hình thành là liên kết amit ⇒ nhiều liên kết vậy gọi là poliamit thôi.
❌ (b) sai vì mỗi mắt xích có CTPT là C12H22N2O2 ứng với PTK = 226 ⇒ số mắt xích dao động từ 20.000 ÷ 226 ≈ 88 đến 50.000 ÷ 226 ≈ 221.
❌ (c) sai vì như phân tích ý (a), poliamid chứa liên kết amit CO–NH chứ không phải este COO của polieste.
✔️ (d) đúng theo phương trình phản ứng trên, đó là quá trình tổng hợp polime.
❌ (e) sai vì phản ứng là trùng ngưng chứ không phải trùng hợp.
⇝ có 2/5 phát biểu đúng ⇝ Chọn đáp án B. ♦