Đáp án [BTTL] Bài học 18: Một số tính chất hóa học cơ bản của kim loại
Câu 1 [560645]: Ở điều kiện thường, chromium tác dụng với phi kim nào sau đây?
A, Fluorine.
B, Lưu huỳnh.
C, Phosphorus.
D, Nitrogen.
Ở điều kiện thường, chromium tác dụng với fluorine:Cr + 2F2 → CrF4.
⟹ Chọn đáp án A Đáp án: A
⟹ Chọn đáp án A Đáp án: A
Câu 2 [57709]: Khi đốt nóng, kim loại nào sau đây không tác dụng với khí O2?
A, Mg.
B, Cu.
C, Au.
D, Fe.
"Lửa thử vàng - gian nan thử sức".
Vàng (Au) có tính khử rất yếu, không bị oxi hóa trong không khí dù ở nhiệt độ nào.
⇒ Chọn đáp án C Đáp án: C
Vàng (Au) có tính khử rất yếu, không bị oxi hóa trong không khí dù ở nhiệt độ nào.
⇒ Chọn đáp án C Đáp án: C
Câu 3 [57710]: Khi đốt nóng, khí clo không tác dụng trực tiếp với
A, khí O2.
B, kim loại Na.
C, kim loại Fe.
D, kim loại Al.
HD: Khí clo (Cl2) không tác dụng trực tiếp với khí O2.
► Cl2 tác dụng được với các kim loại thu được muối clorua tương ứng:
✔️2Na + Cl2 → 2NaCl.
✔️2Fe + 3Cl2 → 2FeCl3.
✔️2Al + 3Cl2 → 2AlCl3 .
⟹ Chọn đáp án A Đáp án: A
► Cl2 tác dụng được với các kim loại thu được muối clorua tương ứng:
✔️2Na + Cl2 → 2NaCl.
✔️2Fe + 3Cl2 → 2FeCl3.
✔️2Al + 3Cl2 → 2AlCl3 .
⟹ Chọn đáp án A Đáp án: A
Câu 4 [57711]: Cho từ từ đến dư một lượng bột sắt vào trong bình đựng một lượng nhỏ khí clo đã được đun nóng. Sau khi các phản ứng xảy ra hoàn toàn, chất rắn thu được trong bình là
A, FeCl2 .
B, FeCl2 và FeCl3.
C, Fe và FeCl2.
D, Fe và FeCl3.
2Fe + 3Cl2 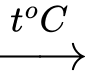 2FeCl3
2FeCl3
Chú ý: Chỉ trong dung dịch thì Fe dư mới có thể phản ứng với FeCl3 để tạo thành FeCl2:
Fe + 2FeCl3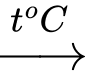 3FeCl2
3FeCl2
Vậy sau phản ứng chất rắn gồm Fe, FeCl3.
⇒ Chọn đáp án D Đáp án: D
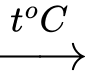 2FeCl3
2FeCl3Chú ý: Chỉ trong dung dịch thì Fe dư mới có thể phản ứng với FeCl3 để tạo thành FeCl2:
Fe + 2FeCl3
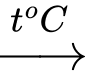 3FeCl2
3FeCl2Vậy sau phản ứng chất rắn gồm Fe, FeCl3.
⇒ Chọn đáp án D Đáp án: D
Câu 5 [237518]: Ở điều kiện thường, kim loại nào sau đây không phản ứng với nước?
A, Ba.
B, Na.
C, K.
D, Be.
HD: các kim loại kiềm (như Na, K,...) và Ca, Ba, Sr phản ứng mãnh liệt với nước. Chỉ có Be không phản ứng với nước dù có đun nóng
⟹ Chọn đáp án D Đáp án: D
⟹ Chọn đáp án D Đáp án: D
Câu 6 [679844]: Ở nhiệt độ thường, kim loại nào sau đây tan hết trong nước dư?
A, Ba.
B, Al.
C, Fe.
D, Cu.
HD: Bài học về kim loại tác dụng với nước:

⟹ Chọn đáp án A Ba: Ba + 2H2O → Ba(OH)2 + H2↑. Đáp án: A

⟹ Chọn đáp án A Ba: Ba + 2H2O → Ba(OH)2 + H2↑. Đáp án: A
Câu 7 [982278]: Kim loại nào sau đây tác dụng với H2O ở nhiệt độ thường?
A, Cu.
B, Au.
C, Ag.
D, Ba.
HD: Bài học về kim loại tác dụng với nước:

⟹ Chọn đáp án D. Ba. Phản ứng: Ba + 2H2O → Ba(OH)2 + H2↑. Đáp án: D

⟹ Chọn đáp án D. Ba. Phản ứng: Ba + 2H2O → Ba(OH)2 + H2↑. Đáp án: D
Câu 8 [233233]: Kim loại nào sau đây không phản ứng được với dung dịch CuSO4?
A, Mg.
B, Fe.
C, Zn.
D, Ag.
HD: Theo dãy điện hóa: 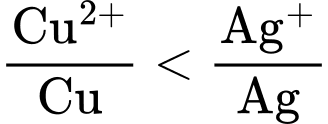 ⇒ Ag không phản ứng được với CuSO4
⇒ Ag không phản ứng được với CuSO4
⟹ Chọn đáp án D Đáp án: D
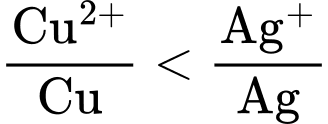 ⇒ Ag không phản ứng được với CuSO4
⇒ Ag không phản ứng được với CuSO4 ⟹ Chọn đáp án D Đáp án: D
Câu 9 [58051]: Cặp chất không xảy ra phản ứng hóa học là
A, Fe và dung dịch FeCl3.
B, Fe và dung dịch HCl.
C, Cu và dung dịch FeCl3.
D, Cu và dung dịch FeCl2.
Giải: Ta có dãy điện hóa:
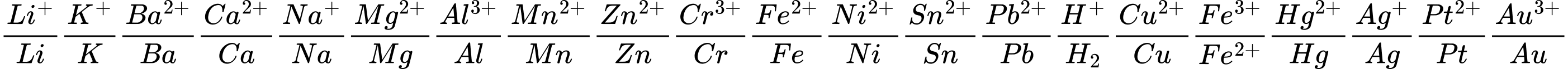
⇒ Cu không tác dụng với dung dịch muối Fe2+
⟹ Chọn đáp án D Đáp án: D
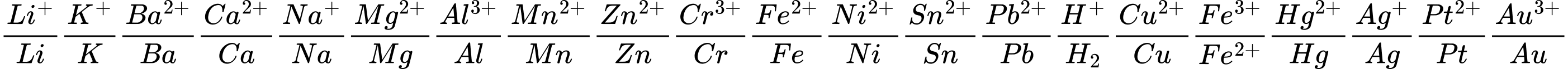
⇒ Cu không tác dụng với dung dịch muối Fe2+
⟹ Chọn đáp án D Đáp án: D
Câu 10 [58059]: Ở nhiệt độ thường, kim loại Al tác dụng được với dung dịch
A, Mg(NO3)2.
B, Ca(NO3)2.
C, KNO3.
D, Cu(NO3)2.
Ở nhiệt độ thường, Al đẩy được Cu ra khỏi dung dịch Cu(NO3)2
Al + Cu(NO3)2 ⟶ Al(NO3)3 + Cu.
⟹ Chọn đáp án D
Đáp án: D
Al + Cu(NO3)2 ⟶ Al(NO3)3 + Cu.
⟹ Chọn đáp án D
Đáp án: D
Câu 11 [39735]: Ở điều kiện thường, Fe không tác dụng với dung dịch (loãng) nào sau đây?
A, Fe2(SO4)3.
B, CuSO4.
C, K2SO4.
D, H2SO4.
Phân tích các đáp án:
✔️A. Fe + Fe2(SO4)3 → 3FeSO4.
✔️B. Fe + CuSO4 → FeSO4 + Cu.
❌C. Fe + K2SO4 → không phản ứng.
✔️D. Fe + H2SO4 → FeSO4 + H2.
⟹ Chọn đáp án C Đáp án: C
✔️A. Fe + Fe2(SO4)3 → 3FeSO4.
✔️B. Fe + CuSO4 → FeSO4 + Cu.
❌C. Fe + K2SO4 → không phản ứng.
✔️D. Fe + H2SO4 → FeSO4 + H2.
⟹ Chọn đáp án C Đáp án: C
Câu 12 [58052]: Ở nhiệt độ thường, dung dịch FeCl2 phản ứng được với kim loại
A, Zn.
B, Ag.
C, Cu.
D, Au.
HD: Thứ tự dãy điện hoá: 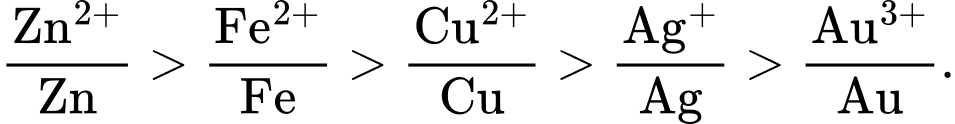
⇒ Theo quy tắc α thì chỉ có Zn tác dụng được với dung dịch FeCl2
Đáp án: A
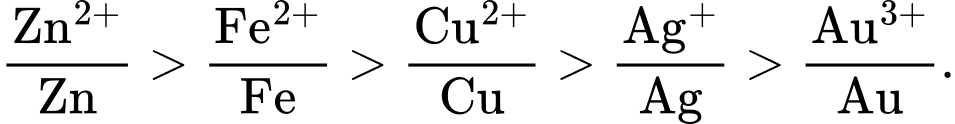
⇒ Theo quy tắc α thì chỉ có Zn tác dụng được với dung dịch FeCl2
⟹ Chọn đáp án A
Câu 13 [58063]: Kim loại nào sau đây không khử được ion Cu2+ trong dung dịch CuSO4 thành Cu?
A, Al.
B, Mg.
C, Fe.
D, K.
Tất cả các kim loại trong 4 đáp án đều có tính khử mạnh hơn Cu. Tuy nhiên, khi cho K vào dd CuSO4 thì:
2K + 2H2O → 2KOH + H2.
Sau đó: Cu2+ + 2OH– → Cu(OH)2.
⟹ Chọn đáp án D Đáp án: D
2K + 2H2O → 2KOH + H2.
Sau đó: Cu2+ + 2OH– → Cu(OH)2.
⟹ Chọn đáp án D Đáp án: D
Câu 14 [58071]: Dung dịch FeSO4 và dung dịch CuSO4 đều tác dụng được với
A, Ag.
B, Fe.
C, Cu.
D, Zn.
Phương trình phản ứng: Dung dịch CuSO4 và FeSO4 đều phản ứng được với Zn:
Zn + FeSO4 → ZnSO4 + Fe
Zn + CuSO4 → ZnSO4 + Cu.
⟹ Chọn đáp án D
Đáp án: D
Zn + FeSO4 → ZnSO4 + Fe
Zn + CuSO4 → ZnSO4 + Cu.
⟹ Chọn đáp án D
Đáp án: D
Câu 15 [62453]: Dung dịch FeSO4 có lẫn tạp chất là CuSO4. Để thu được FeSO4 tinh khiết ta dùng
A, bột Al dư.
B, bột Cu dư.
C, bột Fe dư.
D, bột Zn dư.
Nếu dùng Al hay Zn thì tạp chất CuSO4 mất đi nhưng thay vào đó là tạp chất Al2(SO4)3 hoặc ZnSO4.
+ Không dùng Cu vì Cu không tác dụng được với CuSO4 lẫn FeSO4.
⇒ Dùng Fe vì: Fe + CuSO4 → FeSO4 + Cu
⟹ Chọn đáp án C Đáp án: C
+ Không dùng Cu vì Cu không tác dụng được với CuSO4 lẫn FeSO4.
⇒ Dùng Fe vì: Fe + CuSO4 → FeSO4 + Cu
⟹ Chọn đáp án C Đáp án: C
Câu 16 [29888]: Để làm sạch dung dịch ZnSO4 có lẫn CuSO4, người ta dùng kim loại nào sau đây?
A, Al.
B, Cu.
C, Fe.
D, Zn.
Nhúng thanh kẽm vào hỗn hợp dung dịch chứa ZnSO4 có lẫn CuSO4
Zn+ CuSO4 → ZnSO4 + Cu
Lọc bỏ chất rắn Cu thu được dung dịch chứa ZnSO4
⟹ Chọn đáp án D
Đáp án: D
Zn+ CuSO4 → ZnSO4 + Cu
Lọc bỏ chất rắn Cu thu được dung dịch chứa ZnSO4
⟹ Chọn đáp án D
Đáp án: D
Câu 17 [62462]: Một kim loại dùng để loại bỏ tạp chất Fe2(SO4)3 trong dung dịch FeSO4 là
A, Fe.
B, Ag.
C, Cu.
D, Ba.
Phương trình phản ứng:
Fe + Fe2 (SO4)3 → 3FeSO4
Ag vào dung dịch chứa Fe2(SO4)3 và FeSO4 thì không xảy ra phản ứng → loại B
Cu vào dung dịch chứa Fe2(SO4)3 và FeSO4 thì 2Fe3+ + Cu → 2Fe2+ + Cu2+ vừa thu được FeSO4 và CuSO4 → loại C
Cho Ba vào dung dịch Fe2(SO4)3 và FeSO4 thu được Fe(OH)3 và Fe(OH)2. Loại D
⟹ Chọn đáp án A
Đáp án: A
Fe + Fe2 (SO4)3 → 3FeSO4
Ag vào dung dịch chứa Fe2(SO4)3 và FeSO4 thì không xảy ra phản ứng → loại B
Cu vào dung dịch chứa Fe2(SO4)3 và FeSO4 thì 2Fe3+ + Cu → 2Fe2+ + Cu2+ vừa thu được FeSO4 và CuSO4 → loại C
Cho Ba vào dung dịch Fe2(SO4)3 và FeSO4 thu được Fe(OH)3 và Fe(OH)2. Loại D
⟹ Chọn đáp án A
Đáp án: A
Câu 18 [560649]: Để làm tinh khiết bột đồng có lẫn các kim loại thiếc, kẽm, người ta có thể ngâm hỗn hợp trên vào lượng dư dung dịch nào sau đây?
A, Cu(NO3)2.
B, Zn(NO3)2.
C, Sn(NO3)2.
D, AgNO3.
Zn và Sn bị oxi hóa bởi cation của kim loại đứng sau nó trong dãy điện hóa
⇒ Chọn dung dịch Cu(NO3)2.
Mặc dù dung dịch AgNO3 cũng có thể hòa tan kim loại Zn và Sn lẫn trong bột đồng. Nhưng phản ứng này lại tạo ra kim loại Ag ⇒ không thu được đồng tinh khiết.
⇒ Chọn đáp án A Đáp án: A
⇒ Chọn dung dịch Cu(NO3)2.
Mặc dù dung dịch AgNO3 cũng có thể hòa tan kim loại Zn và Sn lẫn trong bột đồng. Nhưng phản ứng này lại tạo ra kim loại Ag ⇒ không thu được đồng tinh khiết.
⇒ Chọn đáp án A Đáp án: A
Câu 19 [30004]: Để làm sạch dung dịch copper(II) nitrate có lẫn tạp chất silver nitrate, người ta dùng lượng dư kim loại
A, Mg.
B, Cu.
C, Fe.
D, Au.
Đồng nitrat Cu(NO3)2, bạc nitrat AgNO3.
Mg, Fe phản ứng được với Cu(NO3)2 và AgNO3 ⇒ tuy loại được tạp chất AgNO3 nhưng Cu(NO3)2 cũng không còn.
Au không phản ứng với với Cu(NO3)2 và AgNO3.
Cu phản ứng với AgNO3: Cu + 2AgNO3 → Cu(NO3)2 + 2Ag.
Như vậy, dung dịch AgNO3 không còn. Hơn nữa, sản phẩm tạo thành là Cu(NO3)2, không xuất hiện tạp chất mới.
⟹ Chọn đáp án B Đáp án: B
Mg, Fe phản ứng được với Cu(NO3)2 và AgNO3 ⇒ tuy loại được tạp chất AgNO3 nhưng Cu(NO3)2 cũng không còn.
Au không phản ứng với với Cu(NO3)2 và AgNO3.
Cu phản ứng với AgNO3: Cu + 2AgNO3 → Cu(NO3)2 + 2Ag.
Như vậy, dung dịch AgNO3 không còn. Hơn nữa, sản phẩm tạo thành là Cu(NO3)2, không xuất hiện tạp chất mới.
⟹ Chọn đáp án B Đáp án: B
Câu 20 [233242]: Kim loại nào sau đây không phản ứng được với HCl trong dung dịch?
A, Ni.
B, Zn.
C, Fe.
D, Cu.
HD: Kim loại Cu đứng sau (H)axit trong dãy điện hóa nên không phản ứng được với HCl trong dung dịch
⟹ Chọn đáp án D Đáp án: D
⟹ Chọn đáp án D Đáp án: D
Câu 21 [233236]: Kim loại Fe tác dụng với dung dịch H2SO4 loãng sinh ra khí H2 và muối nào sau đây?
A, FeSO4.
B, FeS.
C, FeS2.
D, Fe2(SO4)3.
Kim loại Fe tác dụng với dung dịch H2SO4 loãng sinh ra khí H2 và muối FeSO4.
Phương trình phản ứng:
Fe + H2SO4 → FeSO4 + H2↑.
⟹ Chọn đáp án A Đáp án: A
Phương trình phản ứng:
Fe + H2SO4 → FeSO4 + H2↑.
⟹ Chọn đáp án A Đáp án: A
Câu 22 [57797]: Kim loại nào sau đây khi tác dụng với dung dịch H2SO4 loãng (không có mặt của oxi), khi kim loại tan hết trở thành một dung dịch trong suốt?
A, Mg.
B, Cu.
C, Ba.
D, Ag.
Khi không có mặt O2:
Mg + H2SO4 → MgSO4 + H2.
Ba + H2SO4 → BaSO4↓ + H2 (có kết tủa trắng).
Cu, Ag không tan trong H2SO4 loãng.
⟹ Chọn đáp án A Đáp án: A
Mg + H2SO4 → MgSO4 + H2.
Ba + H2SO4 → BaSO4↓ + H2 (có kết tủa trắng).
Cu, Ag không tan trong H2SO4 loãng.
⟹ Chọn đáp án A Đáp án: A
Câu 23 [57791]: Ở điều kiện thường, kim loại nào sau đây không khử được ion H+ trong dung dịch H2SO4 loãng?
A, Cu.
B, Mg.
C, Fe.
D, Al.
HD: Thứ tự các cặp oxi hoá - khử theo dãy điện hoá: 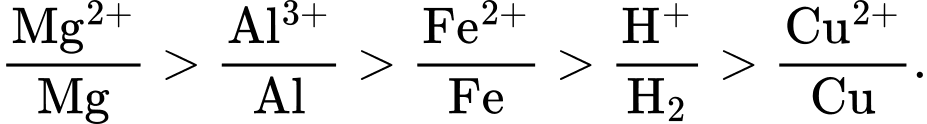
⇒ kim loại Cu không khử được ion H+ trong dung dịch H2SO4 loãng.
⟹ Chọn đáp án A Đáp án: A
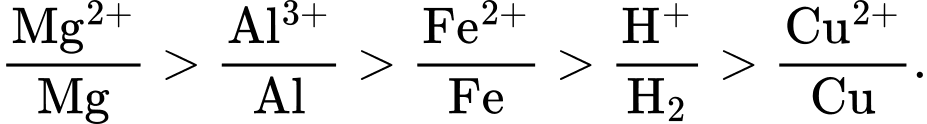
⇒ kim loại Cu không khử được ion H+ trong dung dịch H2SO4 loãng.
⟹ Chọn đáp án A Đáp án: A
Câu 24 [679247]: Cho Fe tác dụng với dung dịch HNO3 đặc, nóng, thu được khí X có màu nâu đỏ. Khí X là
A, N2.
B, N2O.
C, NO.
D, NO2.
Cho Fe tác dụng với dung dịch HNO3 đặc, nóng, thu được khí X có màu nâu đỏ.
Phương trình phản ứng:
Fe + 5HNO3 (đặc, nóng)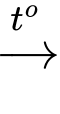 Fe(NO3)3 + 3NO2↑ (khí màu nâu đỏ) + 3H2O.
Fe(NO3)3 + 3NO2↑ (khí màu nâu đỏ) + 3H2O.
Phương trình phản ứng:
Fe + 5HNO3 (đặc, nóng)
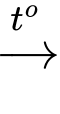 Fe(NO3)3 + 3NO2↑ (khí màu nâu đỏ) + 3H2O.
Fe(NO3)3 + 3NO2↑ (khí màu nâu đỏ) + 3H2O.⟹ Khí X là NO2.
⟹ Chọn đáp án D
Đáp án: D ⟹ Chọn đáp án D
Câu 25 [983253]: Kim loại nào sau đây bị thụ động trong axit sunfuric đặc, nguội?
A, Cu.
B, Al.
C, Ag.
D, Mg.
HD: Các kim loại Al, Cr và Fe bị thụ động hoá trong dung dịch H2SO4 đặc nguội, HNO3 đặc nguội.
⟹ Chọn đáp án B
Đáp án: B