Đáp án [BTTL] Bài học 20: Các thông tin cơ bản về kim loại kiềm – kiềm thổ và chủ đề nước cứng
Câu 1 [680857]: Nguyên tố natri (sodium, Na ) có số hiệu nguyên tử là 11 . Ở trạng thái cơ bản, cấu hình electron của ion Na+ là
A, 1s22s22p63s1.
B, 1s22s22p6.
C, 1s22s22p5.
D, 1s22s22p63s2.
Cấu hình electron của Sodium là: 1s22s22p63s1
⟶ Sodium có 1 electron lớp ngoài cùng cần nhường 1 eletron để tạo thành ion Na+
Na ⟶ Na+ + 1e
Cấu hình electron của ion Na+ là: 1s22s22p6
⟹ Chọn đáp án B Đáp án: B
⟶ Sodium có 1 electron lớp ngoài cùng cần nhường 1 eletron để tạo thành ion Na+
Na ⟶ Na+ + 1e
Cấu hình electron của ion Na+ là: 1s22s22p6
⟹ Chọn đáp án B Đáp án: B
Câu 2 [680853]: Thành phần chính của baking soda là NaHCO3. Tên của hợp chất này là
A, sodium hydrogencarbonate.
B, sodium carbonate.
C, sodium hydrogensulfide.
D, potassium hydrogencarbonate.
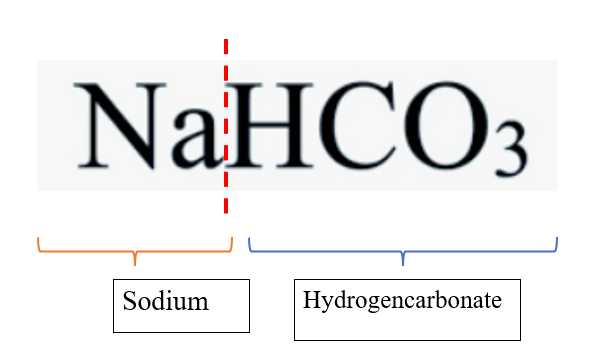
⟹ Chọn đáp án A Đáp án: A
Câu 3 [680858]: Hóa chất nào sau đây không sử dụng để làm mềm nước cứng tạm thời?
A, Na2CO3.
B, Na3PO4.
C, Ca(OH)2.
D, HCl.
Nước cứng tạm thời chứa các muối Ca(HCO3)2 và Mg(HCO3)2. Để làm mềm nước cứng tạm thời, chúng ta cần loại bỏ các ion Ca2+ và Mg2+ ra khỏi dung dịch.
Phân tích các đáp án:
✔️A. Na2CO3 khi thêm vào nước cứng tạm thời có thể phản ứng với ion Ca2+ và Mg2+ để tạo kết tủa. Có thể sử dụng để làm mềm nước cứng tạm thời.
✔️B. Na3PO4 khi thêm vào nước cứng tạm thời có thể phản ứng với ion Ca2+ và Mg2+ để tạo kết tủa. Có thể sử dụng để làm mềm nước cứng tạm thời.
✔️C. Ca(OH)2 khi thêm một lượng vừa đủ Ca(OH)2 vào nước cứng tạm thời có thể phản ứng với ion Ca2+ và Mg2+ để tạo kết tủa. Có thể sử dụng để làm mềm nước cứng tạm thời.
❌D.HCl là một acid mạnh. Khi thêm HCl vào nước cứng tạm thời, nó sẽ phản ứng với các ion bicarbonate, chuyển chúng thành các ion tan . Không thể sử dụng để làm mềm nước cứng.
⟹ Chọn đáp án D Đáp án: D
Phân tích các đáp án:
✔️A. Na2CO3 khi thêm vào nước cứng tạm thời có thể phản ứng với ion Ca2+ và Mg2+ để tạo kết tủa. Có thể sử dụng để làm mềm nước cứng tạm thời.
✔️B. Na3PO4 khi thêm vào nước cứng tạm thời có thể phản ứng với ion Ca2+ và Mg2+ để tạo kết tủa. Có thể sử dụng để làm mềm nước cứng tạm thời.
✔️C. Ca(OH)2 khi thêm một lượng vừa đủ Ca(OH)2 vào nước cứng tạm thời có thể phản ứng với ion Ca2+ và Mg2+ để tạo kết tủa. Có thể sử dụng để làm mềm nước cứng tạm thời.
❌D.HCl là một acid mạnh. Khi thêm HCl vào nước cứng tạm thời, nó sẽ phản ứng với các ion bicarbonate, chuyển chúng thành các ion tan . Không thể sử dụng để làm mềm nước cứng.
⟹ Chọn đáp án D Đáp án: D
Câu 4 [628912]: Kim loại nào sau đây là kim loại kiềm?
A, Al.
B, Mg.
C, K.
D, Ca.
Phân nhóm chính IA (kim loại kiềm) bao gồm các nguyên tố:
Li → Li
Na → Na
K → Kéo
Rb → Rèm
Cs → Xe
Fr → Pháp
⟹ Chọn đáp án C Đáp án: C
Li → Li
Na → Na
K → Kéo
Rb → Rèm
Cs → Xe
Fr → Pháp
⟹ Chọn đáp án C Đáp án: C
Câu 5 [233844]: Kim loại nào sau đây là kim loại kiềm?
A, Mg.
B, Ag.
C, Cu.
D, Na.
Kim loại kiềm là các kim loại thuộc nhóm IA trong BTH: Li, K, Na, Rb, Cs.
⟹ Chọn đáp án D Đáp án: D
⟹ Chọn đáp án D Đáp án: D
Câu 6 [59858]: Công thức chung của oxide kim loại thuộc nhóm IA là
A, R2O3.
B, RO2.
C, R2O.
D, RO.
HD Kim loại thuộc nhóm IA có 1 electron ở lớp ngoài cùng → Oxide kim loại thuộc nhóm IA là R2O
→ Chọn đáp án C
Đáp án: C
→ Chọn đáp án C
Đáp án: C
Câu 7 [824946]: Xu hướng biến đổi nhiệt độ nóng chảy của các kim loại nhóm IA từ Li đến Cs là
A, tăng dần.
B, giảm dần.
C, không đổi.
D, không xác định.
Xu hướng biến đổi nhiệt độ nóng chảy của các kim loại nhóm IA từ Li đến Cs là giảm dần
Giải thích:
Khi đi từ Li đến Cs, bán kính nguyên tử tăng, lực liên kết kim loại giảm vì:
Các nguyên tử lớn hơn → lực hút giữa hạt nhân và "biển electron" yếu hơn.
Cấu trúc mạng tinh thể trở nên kém bền vững hơn.
→ Do đó, nhiệt độ nóng chảy giảm dần.
⟹ Chọn đáp án B
Đáp án: B
Giải thích:
Khi đi từ Li đến Cs, bán kính nguyên tử tăng, lực liên kết kim loại giảm vì:
Các nguyên tử lớn hơn → lực hút giữa hạt nhân và "biển electron" yếu hơn.
Cấu trúc mạng tinh thể trở nên kém bền vững hơn.
→ Do đó, nhiệt độ nóng chảy giảm dần.
⟹ Chọn đáp án B
Đáp án: B
Câu 8 [59789]: Tính chất hoá học chung của kim loại kiềm là
A, tính axít.
B, tính bazơ.
C, tính oxi hoá mạnh.
D, tính khử mạnh.
Tính chất hoá học chung của kim loại kiềm là tính khử mạnh.
⟹ Chọn đáp án D Đáp án: D
⟹ Chọn đáp án D Đáp án: D
Câu 9 [824947]: Cho một mẩu nhỏ postassium vào nước thu được dung dịch. Giá trị pH của dung dịch sau phản ứng có thể nhận giá trị nào dưới đây?
A, pH = 11.
B, pH = 2.
C, pH = 7.
D, pH = 6.
Khi cho một mẩu nhỏ postassium vào nước thu được dung dịch sodium hydroxide. Phương trình phản ứng:
2K + 2H2O ⟶ 2KOH + H2.
⟶ Sản phẩm thu được sau phản ứng là sodium hydroxide và khí hydrogen. Sodium hydroxide (KOH) là một base mạnh khi tan trong nước sẽ tạo thành 1 lượng lớn ion OH- làm tăng nồng độ OH- trong dung dịch . Dung dịch có nồng độ OH- cao sẽ có tính kiềm nên giá trị pH > 7.
⟶ Giá trị pH sau phản ứng có pH = 11.
⟹ Chọn đáp án A Đáp án: A
2K + 2H2O ⟶ 2KOH + H2.
⟶ Sản phẩm thu được sau phản ứng là sodium hydroxide và khí hydrogen. Sodium hydroxide (KOH) là một base mạnh khi tan trong nước sẽ tạo thành 1 lượng lớn ion OH- làm tăng nồng độ OH- trong dung dịch . Dung dịch có nồng độ OH- cao sẽ có tính kiềm nên giá trị pH > 7.
⟶ Giá trị pH sau phản ứng có pH = 11.
⟹ Chọn đáp án A Đáp án: A
Câu 10 [824948]: Để ngăn ngừa sự hình thành các oxide, peroxide và superoxide, kim loại kiềm đôi khi được bảo quản trong môi trường trơ. Khí nào sau đây không nên dùng để bảo quản lithium
A, Ne.
B, Ar.
C, N2.
D, Kr.
Phân tích các đáp án:
✔️A. Ne. Neon là một khí hiếm, rất trơ và không phản ứng với lithium.
✔️B. Ar. Argon cũng là một khí hiếm, trơ và không phản ứng với lithium.
❌C. N2. Nitrogen là một khí tương đối trơ ở nhiệt độ thường. Tuy nhiên, lithium có khả năng phản ứng trực tiếp với nitrogen để tạo thành lithium nitride : 6Li + N2 ⟶ 2Li3N. Do đó, nitrogen không thích hợp để bảo quản lithium.
✔️D. Kr. Krypton là một khí hiếm, trơ và không phản ứng với lithium.
⟹ Chọn đáp án C
Đáp án: C
✔️A. Ne. Neon là một khí hiếm, rất trơ và không phản ứng với lithium.
✔️B. Ar. Argon cũng là một khí hiếm, trơ và không phản ứng với lithium.
❌C. N2. Nitrogen là một khí tương đối trơ ở nhiệt độ thường. Tuy nhiên, lithium có khả năng phản ứng trực tiếp với nitrogen để tạo thành lithium nitride : 6Li + N2 ⟶ 2Li3N. Do đó, nitrogen không thích hợp để bảo quản lithium.
✔️D. Kr. Krypton là một khí hiếm, trơ và không phản ứng với lithium.
⟹ Chọn đáp án C
Đáp án: C
Câu 11 [679749]: Trong phòng thí nghiệm, kim loại Na được bảo quản bằng cách ngâm trong chất lỏng nào sau đây?
A, Nước.
B, Dầu hỏa.
C, Giấm ăn.
D, Ethanol.
HD: Dầu hoả là các hydrocarbon, không có phản ứng với Na, giúp cách li Na với không khí nên dùng bảo quản Na, còn lại:
❌ A. Nước: 2H2O + 2Na → 2NaOH + H2↑.
❌ C. Giấm ăn: 2CH3COOH + 2Na → 2CH3COONa + H2↑.
❌ D. Ethanol: 2C2H5OH + 2Na → 2C2H5ONa + H2↑.
⟹ Chọn đáp án B Đáp án: B
❌ A. Nước: 2H2O + 2Na → 2NaOH + H2↑.
❌ C. Giấm ăn: 2CH3COOH + 2Na → 2CH3COONa + H2↑.
❌ D. Ethanol: 2C2H5OH + 2Na → 2C2H5ONa + H2↑.
⟹ Chọn đáp án B Đáp án: B
Câu 12 [824949]: Trong các kim loại sau, kim loại nào thường được dùng làm tế bào quang điện?
A, Na.
B, K.
C, Rb.
D, Cs.
Trong các kim loại sau, kim loại nào thường được dùng làm tế bào quang điện là Cs.
Giải thích:
- Cs (Cesium) có năng lượng ion hóa thấp nhất. Điều này có nghĩa là nó dễ dàng phát ra electron nhất khi có ánh sáng chiếu vào, kể cả ánh sáng có tần số thấp (ánh sáng nhìn thấy).Do đó, Cesium thường được sử dụng làm tế bào quang điện (hay tế bào quang điện).
- Các kim loại kiềm khác như Na, K, Rb cũng có hiệu ứng quang điện, nhưng chúng cần ánh sáng có tần số cao hơn (năng lượng lớn hơn) để phát ra electron hiệu quả.
⟹ Chọn đáp án D Đáp án: D
Giải thích:
- Cs (Cesium) có năng lượng ion hóa thấp nhất. Điều này có nghĩa là nó dễ dàng phát ra electron nhất khi có ánh sáng chiếu vào, kể cả ánh sáng có tần số thấp (ánh sáng nhìn thấy).Do đó, Cesium thường được sử dụng làm tế bào quang điện (hay tế bào quang điện).
- Các kim loại kiềm khác như Na, K, Rb cũng có hiệu ứng quang điện, nhưng chúng cần ánh sáng có tần số cao hơn (năng lượng lớn hơn) để phát ra electron hiệu quả.
⟹ Chọn đáp án D Đáp án: D
Câu 13 [982756]: Dung dịch nào sau đây làm quỳ tím chuyển sang màu xanh?
A, NaCl.
B, NaOH.
C, KHSO4.
D, KNO3.
Dung dịch NaCl, KNO3 có môi trường trung tính, pH = 7, không làm quỳ tím đổi màu.
Dung dịch NaOH có môi trường bazơ, pH > 7, làm quỳ tím hóa xanh.
Dung dịch KHSO4 có môi trường axit, pH < 7, làm quỳ tím hóa đỏ.
⟹ Chọn đáp án B Đáp án: B
Dung dịch NaOH có môi trường bazơ, pH > 7, làm quỳ tím hóa xanh.
Dung dịch KHSO4 có môi trường axit, pH < 7, làm quỳ tím hóa đỏ.
⟹ Chọn đáp án B Đáp án: B
Câu 14 [911583]: Chất nào sau đây không tác dụng với dung dịch NaOH?
A, FeCl2.
B, CuSO4.
C, MgCl2.
D, KNO3.
Phân tích các đáp án:
✔️ A. FeCl2 + 2NaOH → Fe(OH)2↓ + 2NaCl.
✔️ B. CuSO4 + 2NaOH → Cu(OH)2↓ + Na2SO4.
✔️ C. MgCl2 + 2NaOH → Mg(OH)2↓ + 2NaCl.
❌ D. KNO3 + NaOH ⇝ không xảy ra phản ứng.
⟹ Chọn đáp án D Đáp án: D
✔️ A. FeCl2 + 2NaOH → Fe(OH)2↓ + 2NaCl.
✔️ B. CuSO4 + 2NaOH → Cu(OH)2↓ + Na2SO4.
✔️ C. MgCl2 + 2NaOH → Mg(OH)2↓ + 2NaCl.
❌ D. KNO3 + NaOH ⇝ không xảy ra phản ứng.
⟹ Chọn đáp án D Đáp án: D
Câu 15 [792342]: Chất nào sau đây tác dụng với dung dịch KHCO3 sinh ra khí CO2?
A, HCl.
B, K2SO4.
C, NaCl.
D, Na2SO4.
HD: K2SO4; NaCl và Na2SO4 là các muối trung tính, không phản ứng với KHCO3, chỉ có HCl phản ứng được với KHCO3 và "thật may mắn" khi nó cũng sinh ra khí CO2 thỏa mãn yêu cầu:
• HCl + KHCO3 → KCl + CO2↑ + H2O.
⟹ Chọn đáp án A Đáp án: A
• HCl + KHCO3 → KCl + CO2↑ + H2O.
⟹ Chọn đáp án A Đáp án: A
Câu 16 [39846]: Hợp chất nào sau đây được dùng để làm bột nở cho bánh kẹo, chất tạo khí trong thuốc sủi bọt và thuốc trị chứng thừa axit trong dạ dày?
A, Na2CO3.
B, NaHCO3.
C, NaCl.
D, NaOH.
HD: Ứng dụng làm bột nở do NaHCO3 dễ bị nhiệt phân hủy sinh ra khí CO2 và H2O.
Ứng dụng làm thuốc do NaHCO3 có khả năng phản ứng với acid dư trong dạ dày.
⟹ Chọn đáp án B Đáp án: B
Ứng dụng làm thuốc do NaHCO3 có khả năng phản ứng với acid dư trong dạ dày.
⟹ Chọn đáp án B Đáp án: B
Câu 17 [62466]: Hóa chất NaOH rắn có thể làm khô các khí nào trong số các khí sau
A, H2S.
B, SO2.
C, CO2.
D, NH3.
HD: NaOH rắn hút ẩm, nhưng phản ứng được với H2S, SO2, CO2. Vì vậy NaOH rắn chỉ làm khô được khí NH3 trong các khí trên.
⟹ Chọn đáp án D Đáp án: D
⟹ Chọn đáp án D Đáp án: D
Câu 18 [824950]: Trong quá trình Solvay, X là một trong những sản phẩm được tạo thành khi calcium hydroxide phản ứng với ammonium chloride. X ở trạng thái rắn là một chất màu trắng, nó là sản phẩm cuối của quá trình Solvay và được thải ra đại dương. Chất X là
A, Calcium chloride.
B, Calcium carbonate.
C, Calcium oxide.
D, Calcium hydrogencarbonate.
Trong quá trình Solvay, Calcium chloride là một trong những sản phẩm được tạo thành khi calcium hydroxide phản ứng với ammonium chloride.
Phương trình phản ứng:
2NH4Cl + Ca(OH)2 → CaCl2 + 2NH3 + 2H2O.
Calcium chloride ở trạng thái rắn là một chất màu trắng, nó là sản phẩm cuối của quá trình Solvay và được thải ra đại dương. ⟹ Chọn đáp án A
Các đáp án khác
❌B. Calcium carbonate (CaCO3): Đây là sản phẩm chính của quá trình Solvay, được tạo ra khi sục khí carbon dioxide vào dung dịch sodium bicarbonate.
❌C. Calcium oxide (CaO): Đây là vôi sống, được tạo ra khi nung calcium carbonate.
❌D. Calcium hydrogencarbonate (Ca(HCO3)2 ): Chất này tồn tại chủ yếu trong dung dịch và không phải là sản phẩm cuối được thải ra trực tiếp ở dạng rắn. Đáp án: A
Phương trình phản ứng:
2NH4Cl + Ca(OH)2 → CaCl2 + 2NH3 + 2H2O.
Calcium chloride ở trạng thái rắn là một chất màu trắng, nó là sản phẩm cuối của quá trình Solvay và được thải ra đại dương. ⟹ Chọn đáp án A
Các đáp án khác
❌B. Calcium carbonate (CaCO3): Đây là sản phẩm chính của quá trình Solvay, được tạo ra khi sục khí carbon dioxide vào dung dịch sodium bicarbonate.
❌C. Calcium oxide (CaO): Đây là vôi sống, được tạo ra khi nung calcium carbonate.
❌D. Calcium hydrogencarbonate (Ca(HCO3)2 ): Chất này tồn tại chủ yếu trong dung dịch và không phải là sản phẩm cuối được thải ra trực tiếp ở dạng rắn. Đáp án: A
Câu 19 [824953]: Nguyên liệu thô là bất kỳ nguyên liệu chưa qua chế biến và được sử dụng trong quá trình sản xuất. Xác định ba chất chính đóng vai trò là nguyên liệu thô trong quy trình Solvay.
A, Nước muối, ammonia và đá vôi.
B, Nước, ammonia và carbon dioxide.
C, Nước muối, ammonia và carbon dioxide.
D, Nước, sodium hydrogencarbonate và calcium oxide.
Phân tích các đáp án:
✔️A. Nước muối, ammonia và đá vôi là nguyên liệu thô chưa qua chế biến và được sử dụng trong quá trình Solvay.
❌B. Nước, ammonia và carbon dioxide. Nước là dung môi nhưng không được coi là một trong ba nguyên liệu thô chính.
❌C. Nước muối, ammonia và carbon dioxide. Carbon dioxide là một nguyên liệu quan trọng, nhưng nó được tạo ra từ đá vôi, do đó đá vôi mới là nguyên liệu thô ban đầu.
❌D. Nước, sodium hydrogencarbonate và calcium oxide. Sodium hydrogencarbonate là một sản phẩm trung gian, và calcium oxide là sản phẩm phụ dùng để tái tạo ammonia, không phải là nguyên liệu thô ban đầu.
⟹ Chọn đáp án A Đáp án: A
✔️A. Nước muối, ammonia và đá vôi là nguyên liệu thô chưa qua chế biến và được sử dụng trong quá trình Solvay.
❌B. Nước, ammonia và carbon dioxide. Nước là dung môi nhưng không được coi là một trong ba nguyên liệu thô chính.
❌C. Nước muối, ammonia và carbon dioxide. Carbon dioxide là một nguyên liệu quan trọng, nhưng nó được tạo ra từ đá vôi, do đó đá vôi mới là nguyên liệu thô ban đầu.
❌D. Nước, sodium hydrogencarbonate và calcium oxide. Sodium hydrogencarbonate là một sản phẩm trung gian, và calcium oxide là sản phẩm phụ dùng để tái tạo ammonia, không phải là nguyên liệu thô ban đầu.
⟹ Chọn đáp án A Đáp án: A
Câu 20 [560820]: Nhúng đầu dây platinum vào dung dịch sodium chlorine. Sau đó, đưa đầu dây platinum vào ngọn lửa đèn khí thì xuất hiện ngọn lửa màu
A, vàng.
B, tím.
C, xanh.
D, đỏ.
Khi sodium chloride bị đốt nóng, các ion sodium (Na+) phát ra ánh sáng vàng đặc trưng.
⟹ Chọn đáp án A Đáp án: A
⟹ Chọn đáp án A Đáp án: A
Câu 21 [560821]: Nhúng đầu dây platinum vào dung dịch potassium nitrate. Sau đó, đưa đầu dây platinum vào ngọn lửa đèn khí thì xuất hiện ngọn lửa màu
A, vàng.
B, tím.
C, xanh.
D, đỏ.
Khi potassium (K+) bị đốt nóng, các ion potassium phát ra ánh sáng màu tím đặc trưng.
⟹ Chọn đáp án B Đáp án: B
⟹ Chọn đáp án B Đáp án: B
Câu 22 [233243]: Kim loại nào sau đây là kim loại kiềm thổ?
A, Ag.
B, Cu.
C, Ca.
D, Na.
Mẹo: "Bé Mang Cá Sang Bà Rán" ⇄ Be Mg Ca Sr Ba Rn.
⇒ Kim loại kiềm thổ xuất hiện trong 4 phương án là Ca (canxi).
⟹ Chọn đáp án C Đáp án: C
⇒ Kim loại kiềm thổ xuất hiện trong 4 phương án là Ca (canxi).
⟹ Chọn đáp án C Đáp án: C
Câu 23 [60057]: Hai kim loại đều thuộc nhóm IIA trong bảng tuần hoàn là
A, Sr, K.
B, Be, Al.
C, Ca, Ba.
D, Na, Ba.
Phân tích các đáp án:
❌A. Sr, K: Sr thuộc nhóm IIA, K thuộc nhóm IA.
❌B. Be, Al: Be thuộc nhóm IIA, Al thuộc nhóm IIIA.
✔️C. Ca, Ba đều thuộc nhóm IIA.
❌D. Na, Ba: Na thuộc nhóm IA, Ba thuộc nhóm IIA.
⟹ Chọn đáp án C Đáp án: C
❌A. Sr, K: Sr thuộc nhóm IIA, K thuộc nhóm IA.
❌B. Be, Al: Be thuộc nhóm IIA, Al thuộc nhóm IIIA.
✔️C. Ca, Ba đều thuộc nhóm IIA.
❌D. Na, Ba: Na thuộc nhóm IA, Ba thuộc nhóm IIA.
⟹ Chọn đáp án C Đáp án: C
Câu 24 [61786]: Quặng dolomite bao gồm các chất
A, CaO và BaO.
B, CaCO3 và BaCO3.
C, MgCO3 và CaCO3.
D, BaCO3 và MgCO3.
HD: Quặng dolomite bao gồm MgCO3 và CaCO3.
⟹ Chọn đáp án C
Đáp án: C
⟹ Chọn đáp án C
Đáp án: C
Câu 25 [61754]: Trong các khoáng vật dưới đây, khoáng vật nào không chứa CaCO3?
A, Calcite.
B, Dolomite.
C, Đá hoa.
D, Magnesite.
HD: Thành phần chính của các khoảng vật:
✔️ A. Calcite: CaCO3.
✔️ B. Dolomite: CaCO3.MgCO3.
✔️ C. Đá hoa: CaCO3.
❌ D. Magnesite: MgCO3.
⇒ Chọn đáp án D Đáp án: D
✔️ A. Calcite: CaCO3.
✔️ B. Dolomite: CaCO3.MgCO3.
✔️ C. Đá hoa: CaCO3.
❌ D. Magnesite: MgCO3.
⇒ Chọn đáp án D Đáp án: D
Câu 26 [560891]: Nhiệt độ nóng chảy của các kim loại nhóm IIA từ Be đến Ba có xu hướng biến đổi như thế nào?
A, Tăng dần.
B, Giảm dần.
C, Không đổi.
D, Không xác định.
Các kim loại nhóm IIA có nhiệt độ nóng chảy cao hơn so với kim loại nhóm IA, nhưng tươngđối thấp so với các kim loại khác.
⟶ Tuy nhiên, nhiệt độ nóng chảy của kim loại trong cùng nhóm IIA biến đổi không theo xuhướng rõ rệt. Ví dụ từ Be đến Mg có nhiệt độ nóng chảy giảm nhưng Mg đến Ca nhiệt độ nóng chảy lại tăng. Sau đó từ Ca đến Sr, Ba thì nhiệt độ nóng chảy giảm.
⟹ Chọn đáp án D Đáp án: D
⟶ Tuy nhiên, nhiệt độ nóng chảy của kim loại trong cùng nhóm IIA biến đổi không theo xuhướng rõ rệt. Ví dụ từ Be đến Mg có nhiệt độ nóng chảy giảm nhưng Mg đến Ca nhiệt độ nóng chảy lại tăng. Sau đó từ Ca đến Sr, Ba thì nhiệt độ nóng chảy giảm.
⟹ Chọn đáp án D Đáp án: D
Câu 27 [560895]: Tính chất hoá học đặc trưng của kim loại nhóm IIA là
A, Tính oxi hóa.
B, Tính khử.
C, Tính acid.
D, Tính base.
Các kim loại nhóm IIA như Be, Mg, Ca, Sr, Ba có xu hướng nhường 2 electron ở lớp ngoài cùng để đạt cấu hình bền vững của khí hiếm:
M ⟶ M2+ + 2e
⇒ Đóng vai trò chất khử trong phản ứng.
⇒ Chọn đáp án B Đáp án: B
M ⟶ M2+ + 2e
⇒ Đóng vai trò chất khử trong phản ứng.
⇒ Chọn đáp án B Đáp án: B
Câu 28 [619770]: Trong tự nhiên, calcium sulfate tồn tại dưới dạng muối ngậm nước (CaSO4, 2H2O) được gọi là
A, bauxite.
B, đá vôi.
C, thạch cao nung.
D, thạch cao sống.
Phân tích các đáp án:
❌A. Bauxite là Al2O3.2H2O.
❌B. Đá vôi là CaCO3.
❌C. Thạch cao nung là CaSO4.H2O.
✔️D. Thạch cao sống là CaSO4.2H2O.
⇒ Chọn đáp án D.
Đáp án: D
❌A. Bauxite là Al2O3.2H2O.
❌B. Đá vôi là CaCO3.
❌C. Thạch cao nung là CaSO4.H2O.
✔️D. Thạch cao sống là CaSO4.2H2O.
⇒ Chọn đáp án D.
Đáp án: D
Câu 29 [679540]: Chất nào sau đây được dùng để khử chua đất trong nông nghiệp?
A, CaO.
B, CaSO4.
C, CaCl2.
D, Ca(NO3)2.
Đất chua (pH < 6,5) do đất bị rửa trôi bởi nước mưa, nước tưới dư thừa. Nước mang đi chất dinh dưỡng hòa tan, trong đó có chứa nhiều chất kiềm xuống tầng đất sâu, sông suối, ao hồ ⇝ làm đất mất chất kiềm ⇝ trở nên chua.
⇒ Biện pháp khắc phục là bón vôi tôi (CaO) bởi CaO + H2O → Ca(OH)2 có tính base ⇝ tăng tính kiềm cho đất cũng như giúp khử chua (loại bỏ các acid trong đất).
⇒ Chọn đáp án A Đáp án: A
⇒ Biện pháp khắc phục là bón vôi tôi (CaO) bởi CaO + H2O → Ca(OH)2 có tính base ⇝ tăng tính kiềm cho đất cũng như giúp khử chua (loại bỏ các acid trong đất).
⇒ Chọn đáp án A Đáp án: A
Câu 30 [39828]: Hydroxide nào sau đây có giá thành rẻ, được sử dụng rộng rãi trong nhiều ngành công nghiệp như sản xuất amoniac, chloride vôi (CaOCl2), vật liệu xây dựng, sản xuất mía đường?
A, NaOH.
B, KOH.
C, Ca(OH)2.
D, Ba(OH)2.
Calcium hydroxide có giá thành rẻ, được sử dụng rộng rãi trong nhiều ngành công nghiệp như sản xuất amoniac, clorua vôi (CaOCl2), vật liệu xây dựng, sản xuất mía đường.
Các hydroxide khác:
NaOH (sodium hydroxide) và KOH (potassium hydroxide): Mặc dù cũng là các base mạnh và có nhiều ứng dụng, nhưng thường có giá thành cao hơn Ca(OH)2 .
Ba(OH)2 (barium hydroxide): Có tính base mạnh nhưng độc hại và ít được sử dụng rộng rãi hơn Ca(OH)2 .
⟹ Chọn đáp án C Đáp án: C
Các hydroxide khác:
NaOH (sodium hydroxide) và KOH (potassium hydroxide): Mặc dù cũng là các base mạnh và có nhiều ứng dụng, nhưng thường có giá thành cao hơn Ca(OH)2 .
Ba(OH)2 (barium hydroxide): Có tính base mạnh nhưng độc hại và ít được sử dụng rộng rãi hơn Ca(OH)2 .
⟹ Chọn đáp án C Đáp án: C
Câu 31 [61732]: Trước khi đi thi đấu các môn thể thao, các vận động viên thường xoa một ít chất X dưới dạng bột mịn màu trắng làm tăng ma sát và hút ẩm. Chất X là
A, MgCO3.
B, CaOCl2.
C, CaO.
D, Tinh bột.
Chất X chính là MgCO3 (magnesium carbonate).
► Các chất như CaO, CaOCl2 không được sử dụng do khi hút ẩm sẽ gây ảnh hưởng đến da tay.
⇒ Chọn đáp án A Đáp án: A
► Các chất như CaO, CaOCl2 không được sử dụng do khi hút ẩm sẽ gây ảnh hưởng đến da tay.
⇒ Chọn đáp án A Đáp án: A
Câu 32 [56044]: Trong cơ thể người, sự thiếu hụt nguyên tố nào sau đây có thể gây ra bệnh loãng xương?
A, Ba.
B, Mg.
C, Be.
D, Ca.
Trong cơ thể người, sự thiếu hụt nguyên tố Ca có thể gây ra bệnh loãng xương.
⇒ Chọn đáp án D Đáp án: D
⇒ Chọn đáp án D Đáp án: D
Câu 33 [560906]: Một số hợp chất nhóm 2 có thể được sử dụng để điều trị chứng khó tiêu do acid hoặc để trung hòa đất chua. Hợp chất nhóm 2 nào sẽ không phù hợp cho cả hai mục đích sử dụng?
A, Ca(OH)2.
B, BaSO4.
C, Mg(OH)2.
D, CaCO3.
- Ca(OH)2, Mg(OH)2, CaCO3 có khả năng tác dụng với acid, nên có thể sử dụng để trung hòa acid trong dạ dày, hoặc trung hòa đất chua.
- BaSO4 là muối ít tan và không có tính kiềm mạnh, nên không có tác dụng với việc trung hòa acid trong dạ dày.
⟹ Chọn đáp án B Đáp án: B
- BaSO4 là muối ít tan và không có tính kiềm mạnh, nên không có tác dụng với việc trung hòa acid trong dạ dày.
⟹ Chọn đáp án B Đáp án: B
Câu 34 [560907]: Thuốc diệt chuột cân phải không tan trong nước mưa nhưng hòa tan ở độ pH thấp của chất chứa trong dạ dày. Hợp chất barium nào thích hợp để dùng làm thuộc diệt chuột?
A, Barium carbonate.
B, Barium chloride.
C, Barium hydroxide.
D, Barium sulfate.
Barium carbonate BaCO3 không tan trong nước mưa (pH trung tính) nhưng sẽ hòa tan trong môi trường có độ pH thấp, như trong dạ dày, tạo ra barium ion (Ba2+) có tính độc hại. Khi chuột nuốt phải barium carbonate, nó sẽ bị hòa tan trong dạ dày, giải phóng barium ion gây độc cho cơ thể.
❌ B. Barium chloride (BaCl2): Là một muối tan trong nước, không có đặc tính phù hợp với yêu cầu của thuốc diệt chuột.
❌ C. Barium hydroxide (Ba(OH)2): Là một base mạnh, tan trong nước và có tính kiềm cao, không phù hợp để làm thuốc diệt chuột.
❌ D. Barium sulfate (BaSO4): Là một muối không tan trong nước và cũng không có tính độc hại ở nồng độ bình thường, không phù hợp với mục đích diệt chuột.
⟹ Chọn đáp án A. Đáp án: A
❌ B. Barium chloride (BaCl2): Là một muối tan trong nước, không có đặc tính phù hợp với yêu cầu của thuốc diệt chuột.
❌ C. Barium hydroxide (Ba(OH)2): Là một base mạnh, tan trong nước và có tính kiềm cao, không phù hợp để làm thuốc diệt chuột.
❌ D. Barium sulfate (BaSO4): Là một muối không tan trong nước và cũng không có tính độc hại ở nồng độ bình thường, không phù hợp với mục đích diệt chuột.
⟹ Chọn đáp án A. Đáp án: A
Câu 35 [60115]: Dung dịch chất phản ứng với đá vôi giải phóng khí carbon dioxide là
A, rượu uống.
B, bột ngọt (mì chính).
C, giấm.
D, đường ăn.
Rượu uống, bột ngọt và đường ăn không phản ứng với CaCO3.
Giấm có tính acid của CH3COOH nên phản ứng với CaCO3 giải phóng khí carbon dioxide (CO2).
PTHH:
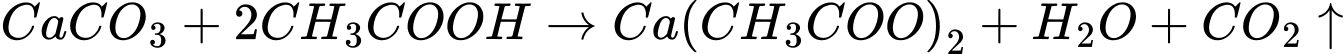
Chọn đáp án C Đáp án: C
Giấm có tính acid của CH3COOH nên phản ứng với CaCO3 giải phóng khí carbon dioxide (CO2).
PTHH:
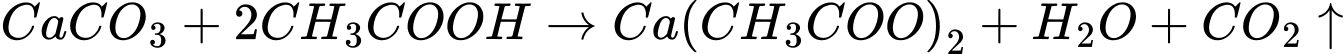
Chọn đáp án C Đáp án: C
Câu 36 [973546]: Dung dịch nào sau đây tác dụng với dung dịch Ba(HCO3)2, vừa thu được kểt tủa, vừa có khí thoát ra?
A, NaOH.
B, HCl.
C, Ca(OH)2.
D, H2SO4.
HD: Các phản ứng xảy ra khi cho Ba(HCO3)2 lần lượt phản ứng:
❌ A. NaOH + Ba(HCO3)2 → NaOH + BaCO3↓ + H2O.
❌ B. 2HCl + Ba(HCO3)2 → BaCl2 + 2CO2↑ + 2H2O.
❌ C. Ca(OH)2 + Ba(HCO3)2 → BaCO3↓ + CaCO3↓ + 2H2O.
✔️ D. H2SO4 + Ba(HCO3)2 → BaSO4↓ + 2CO2↑ + 2H2O.
⟹ Chọn đáp án D Đáp án: D
❌ A. NaOH + Ba(HCO3)2 → NaOH + BaCO3↓ + H2O.
❌ B. 2HCl + Ba(HCO3)2 → BaCl2 + 2CO2↑ + 2H2O.
❌ C. Ca(OH)2 + Ba(HCO3)2 → BaCO3↓ + CaCO3↓ + 2H2O.
✔️ D. H2SO4 + Ba(HCO3)2 → BaSO4↓ + 2CO2↑ + 2H2O.
⟹ Chọn đáp án D Đáp án: D
Câu 37 [982764]: Khi phân hủy calcium carbonatet ở nhiệt độ khoảng 1000oC thì thu được sản phẩm gồm CO2 và chất nào sau đây?
A, Ca(OH)2.
B, Ca.
C, O2.
D, CaO.
HD: Phản ứng nhiệt phân: CaCO3 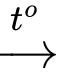 CaO + CO2↑.
CaO + CO2↑.
⟶ Ngoài CO2, chất còn lại là CaO.
⟹ Chọn đáp án D Đáp án: D
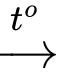 CaO + CO2↑.
CaO + CO2↑.⟶ Ngoài CO2, chất còn lại là CaO.
⟹ Chọn đáp án D Đáp án: D
Câu 38 [60086]: Calcium oxide có tính hút ẩm mạnh nên được sử dụng để làm khô nhiều chất. Khí nào sau đây không làm khô bằng CaO do có phản ứng với chất này?
A, O2.
B, CO.
C, CO2.
D, N2.
HD: Có phản ứng xảy ra: CaO + CO2 → CaCO3.
Hoặc khi CaO hút ẩm: CaO + H2O → Ca(OH)2
|⇝ Sau đó: Ca(OH)2 + CO2 → CaCO3 + H2O.
⟹ Chọn đáp án C Đáp án: C
Hoặc khi CaO hút ẩm: CaO + H2O → Ca(OH)2
|⇝ Sau đó: Ca(OH)2 + CO2 → CaCO3 + H2O.
⟹ Chọn đáp án C Đáp án: C
Câu 39 [560912]: Trên bề mặt các hố vôi tôi lâu ngày thường có màng chất rắn do tạo thành hợp chất X không tan màu trắng. Công thức hóa học của X là
A, Ca(NO3)2.
B, CaSO4.
C, CaCO3.
D, CaCrO4.
Trên bề mặt các hố vôi tôi lâu ngày thường có màng chất rắn do tạo thành hợp chất X không tan màu trắng. Phản ứng hóa học xảy ra như sau:
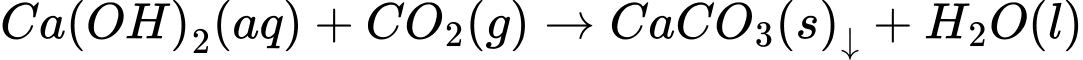
→ Chất X là CaCO3.
⟹ Chọn đáp án C Đáp án: C
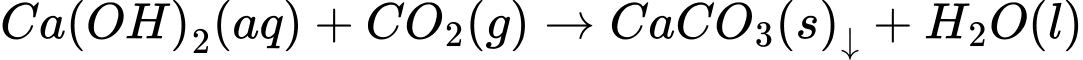
→ Chất X là CaCO3.
⟹ Chọn đáp án C Đáp án: C
Câu 40 [233830]: Nước tự nhiên chứa nhiều những cation nào sau đây được gọi là nước cứng?
A, Na+, Al3+.
B, Na+, K+.
C, Al3+, K+.
D, Ca2+, Mg2+.
HD: Nước cứng là nước có chứa nhiều ion Ca2+ và Mg2+.
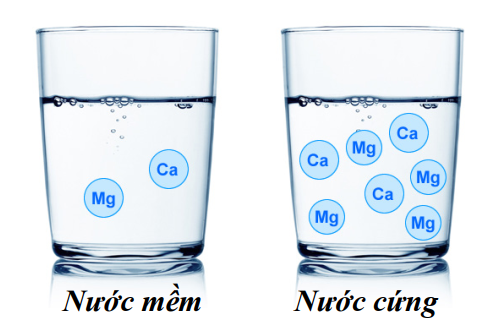
⇝ Chọn đáp án D. Đáp án: D

⇝ Chọn đáp án D. Đáp án: D
Câu 41 [982224]: Cặp chất nào sau đây gây nên tính cứng tạm thời của nước?
A, Na2SO4, KCl.
B, Mg(HCO3)2, Ca(HCO3)2.
C, NaCl, KCl.
D, Na2SO4, K2SO4.
HD: Bài học phân loại nước cứng:
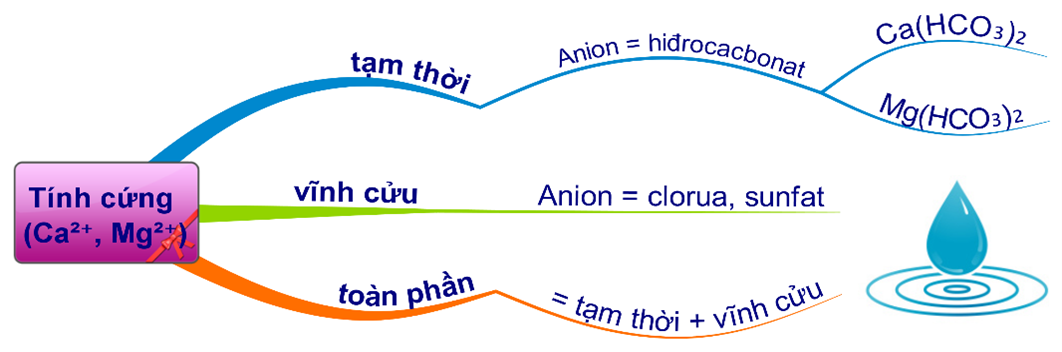
Mg(HCO3)2, Ca(HCO3)2 gây nên tính cứng tạm thời của nước.
⇝ Chọn đáp án B Đáp án: B

Mg(HCO3)2, Ca(HCO3)2 gây nên tính cứng tạm thời của nước.
⇝ Chọn đáp án B Đáp án: B
Câu 42 [983247]: Cặp chất nào sau đây gây nên tính cũng vĩnh cửu của nước?
A, NaNO3, KNO3.
B, NaNO3, KHCO3.
C, MgCl2, CaSO4.
D, NaHCO3, KNO3.
HD: Phân loại nước cứng:

⇝ Cặp chất gây nên tính cũng vĩnh cửu của nước là: MgCl2 và CaSO4
⟹ Chọn đáp án C Đáp án: C

⇝ Cặp chất gây nên tính cũng vĩnh cửu của nước là: MgCl2 và CaSO4
⟹ Chọn đáp án C Đáp án: C
Câu 43 [679747]: Đun nước cứng lâu ngày trong ấm nước xuất hiện một lớp cặn. Thành phần chính của lớp cặn đó là
A, CaCl2.
B, CaCO3.
C, Na2CO3.
D, CaO.
HD: Thành phần chính của lớp cặn đó là CaCO3. Nguyên nhân:
Ca(HCO3)2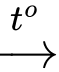 CaCO3↓ + CO2↑ + H2O.
CaCO3↓ + CO2↑ + H2O.
☆ Để làm sạch, có thể sử dụng giấm ăn:
2CH3COOH + CaCO3 → (CH3COO)2Ca + 2H2O.
⇒ Chọn đáp án B Đáp án: B
Ca(HCO3)2
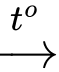 CaCO3↓ + CO2↑ + H2O.
CaCO3↓ + CO2↑ + H2O.☆ Để làm sạch, có thể sử dụng giấm ăn:
2CH3COOH + CaCO3 → (CH3COO)2Ca + 2H2O.
⇒ Chọn đáp án B Đáp án: B
Câu 44 [679600]: Dung dịch nào sau đây được dùng để xử lí lớp cặn CaCO3 bám vào ấm đun nước?
A, Muối ăn.
B, Cồn.
C, Nước vôi trong.
D, Giấm ăn.
HD: Giấm ăn chứa acetic acid: CH3COOH có khả năng hoà tan CaCO3 (thêm nữa là ấm nước dùng để sinh hoạt ăn uống nên cần hoá chất an toàn với sức khoẻ chúng ta, dùng giấm ăn hoặc chanh,... là hợp lý nhất).
Phản ứng xảy ra: 2CH3COOH + CaCO3 → (CH3COO)2Ca + CO2↑ + H2O.
⇒ Chọn đáp án D Đáp án: D
Phản ứng xảy ra: 2CH3COOH + CaCO3 → (CH3COO)2Ca + CO2↑ + H2O.
⇒ Chọn đáp án D Đáp án: D
Câu 45 [60172]: Sử dụng nước cứng không gây ra tác hại nào sau đây?
A, Đóng cặn nồi hơi gây nguy hiểm.
B, Tốn nhiên liệu, làm giảm hương vị thức ăn.
C, Hao tổn chất giặt rửa tổng hợp.
D, Tắc ống dẫn nước nóng trong nồi hơi.
Nước cứng chỉ gây ra kết tủa với xà phòng, còn với chất giặt rửa tổng hợp thì vẫn bình thường nên không gây hao tổn
⟹ Chọn đáp án C Đáp án: C
⟹ Chọn đáp án C Đáp án: C
Câu 46 [233868]: Chất nào sau đây có khả năng làm mềm được nước cứng vĩnh cửu?
A, NaCl.
B, CaCl2.
C, Na2SO4.
D, Na2CO3.
Dung dịch Na2CO3, Na3PO4 làm mềm nước cứng vĩnh cửu.
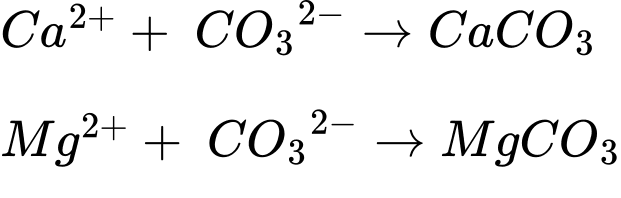
⇒ Chọn đáp án D Đáp án: D
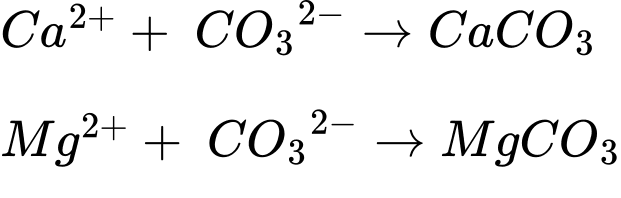
⇒ Chọn đáp án D Đáp án: D
Câu 47 [679845]: Chất nào sau đây được dùng để làm mềm nước có tính cứng tạm thời?
A, CaCO3.
B, MgCl2.
C, NaOH.
D, Fe(OH)2.
Nước cứng tạm thời chứa Ca(HCO3)2 và Mg(HCO3)2, khi sử dụng NaOH:
• 2NaOH + Ca(HCO3)2 → CaCO3↓ + Na2CO3 + 2H2O.
• 2NaOH + Mg(HCO3)2 → MgCO3↓ + Na2CO3 + 2H2O.
Kết tủa các cation Mg2+ và Ca2+ ⇝ làm mềm nước.
⇒ Chọn đáp án C Đáp án: C
• 2NaOH + Ca(HCO3)2 → CaCO3↓ + Na2CO3 + 2H2O.
• 2NaOH + Mg(HCO3)2 → MgCO3↓ + Na2CO3 + 2H2O.
Kết tủa các cation Mg2+ và Ca2+ ⇝ làm mềm nước.
⇒ Chọn đáp án C Đáp án: C
Câu 48 [39681]: Cho mẫu nước cứng chứa các ion: Ca2+, Mg2+ và HCO3–. Hoá chất được dùng để làm mềm mẫu nước cứng trên là
A, HCl.
B, Na2CO3.
C, H2SO4.
D, NaCl.
Mẫu nước cứng chứa các ion: Ca2+, Mg2+ và HCO3-. Hóa chất được dùng để làm mềm nước cứng Na2CO3.
Phương trình phản ứng:
Ca(HCO3)2 + Na2CO3 ⟶ CaCO3 ↓ + 2NaHCO3.
Mg(HCO3)2 + Na2CO3 ⟶ MgCO3 ↓ + 2NaHCO3.
⟹ Chọn đáp án B
Đáp án: B
Phương trình phản ứng:
Ca(HCO3)2 + Na2CO3 ⟶ CaCO3 ↓ + 2NaHCO3.
Mg(HCO3)2 + Na2CO3 ⟶ MgCO3 ↓ + 2NaHCO3.
⟹ Chọn đáp án B
Câu 49 [60186]: Để làm mềm một loại nước cứng có thành phần : Ca2+, Mg2+, Cl-, SO42- nên dùng
A, dung dịch soda.
B, dung dịch nước vôi trong.
C, nước Javel.
D, dung dịch xút ăn da.
Nước cứng là nước chứa các ion Ca2+, Mg2+ (thường kết hợp với các anion như Cl−, SO42−).
Muốn làm mềm nước cứng thường cần loại bỏ hoặc giảm nồng độ Ca2+ và Mg2++ bằng cách kết tủa chúng dưới dạng muối không tan (như CaCO3, Mg(OH)2)
Phân tích các chất:
✔️ A. Dung dịch soda (Na2CO3)
Soda phản ứng với Ca2+ và Mg2+, tạo kết tủa không tan CaCO3 và MgCO3:
Ca2+ + CO32− → CaCO3↓
Mg2+ + CO32− → MgCO3↓
❌ B. Dung dịch nước vôi trong (Ca(OH)2)
Nước vôi trong có thể làm mềm nước cứng tạm thời (nước cứng chứa HCO3−) bằng cách tạo kết tủa CaCO3. Tuy nhiên, với nước cứng chứa Cl− và SO42−, nó không hiệu quả.
❌ C. Nước Javel (NaClO)
Nước Javel là chất oxi hóa, không làm mềm nước cứng vì nó không phản ứng với Ca2+ hoặc Mg2+.
❌ D. Dung dịch xút ăn da (NaOH)
NaOH có thể phản ứng với Mg2+ tạo Mg(OH)2 kết tủa, nhưng không hiệu quả với Ca2+. Hơn nữa, việc sử dụng NaOH có thể làm tăng pH quá cao, gây bất lợi.
⇒ Chọn đáp án A Đáp án: A
Muốn làm mềm nước cứng thường cần loại bỏ hoặc giảm nồng độ Ca2+ và Mg2++ bằng cách kết tủa chúng dưới dạng muối không tan (như CaCO3, Mg(OH)2)
Phân tích các chất:
✔️ A. Dung dịch soda (Na2CO3)
Soda phản ứng với Ca2+ và Mg2+, tạo kết tủa không tan CaCO3 và MgCO3:
Ca2+ + CO32− → CaCO3↓
Mg2+ + CO32− → MgCO3↓
❌ B. Dung dịch nước vôi trong (Ca(OH)2)
Nước vôi trong có thể làm mềm nước cứng tạm thời (nước cứng chứa HCO3−) bằng cách tạo kết tủa CaCO3. Tuy nhiên, với nước cứng chứa Cl− và SO42−, nó không hiệu quả.
❌ C. Nước Javel (NaClO)
Nước Javel là chất oxi hóa, không làm mềm nước cứng vì nó không phản ứng với Ca2+ hoặc Mg2+.
❌ D. Dung dịch xút ăn da (NaOH)
NaOH có thể phản ứng với Mg2+ tạo Mg(OH)2 kết tủa, nhưng không hiệu quả với Ca2+. Hơn nữa, việc sử dụng NaOH có thể làm tăng pH quá cao, gây bất lợi.
⇒ Chọn đáp án A Đáp án: A
Câu 50 [706082]: Nước cứng là kết quả tự nhiên tạo ra từ các khoáng chất (calcium và magnesium) tích tụ trong chu trình của nước, chứa một hàm Ca2+ và Mg2+ cao vượt mức tiêu chuẩn. Sử dụng nước cứng lâu ngày sẽ dễ dẫn đến sỏi thận, sỏi tiết niệu hoặc làm tắc thành trọng của động mạch, tĩnh mạch do đóng cặn vôi gây nguy hiểm đến sức khỏe. Tóc khô xơ, mất độ mềm mại.
(a) Nước có chứa nhiều ion HCO3– được gọi là nước có tính cứng tạm thời.
(b) Có thể làm mềm nước có tính cứng tạm thời bằng cách đun sôi nước.
(c) Có thể loại bỏ một phần tính cứng của nước có tính cứng vĩnh cửu bằng cách dùng một lượng vừa đủ Ca(OH)2.
(d) Không thể dùng cách đun sôi để loại bỏ hoàn toàn tính cứng của nước có chứa nhiều các ion sau: Mg2+, Ca2+, Cl–, HCO3–, SO42–.
(e) Nước cứng có thể là nguyên nhân gây nổ nồi hơi.Số phát biểu đúng là
(a) Nước có chứa nhiều ion HCO3– được gọi là nước có tính cứng tạm thời.
(b) Có thể làm mềm nước có tính cứng tạm thời bằng cách đun sôi nước.
(c) Có thể loại bỏ một phần tính cứng của nước có tính cứng vĩnh cửu bằng cách dùng một lượng vừa đủ Ca(OH)2.
(d) Không thể dùng cách đun sôi để loại bỏ hoàn toàn tính cứng của nước có chứa nhiều các ion sau: Mg2+, Ca2+, Cl–, HCO3–, SO42–.
(e) Nước cứng có thể là nguyên nhân gây nổ nồi hơi.Số phát biểu đúng là
A, 1.
B, 2.
C, 3.
D, 4.
Phân tích các phát biểu :
❌(a) – Sai. Nước có chứa nhiều ion Mg2+, Ca2+, HCO3- được gọi là -nước có tính cứng tạm thời.
✔️(b) – Đúng. Có thể làm mềm nước có tính cứng tạm thời bằng cách đun sôi nước.
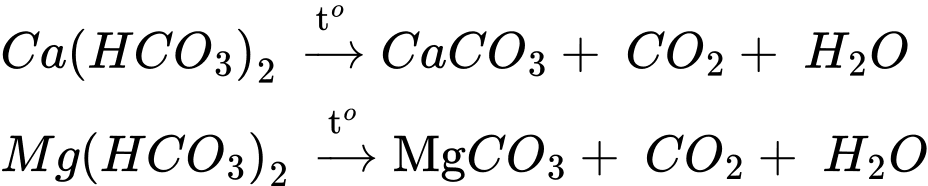
❌(c) – Sai. Không thể loại bỏ tính cứng của nước có tính cứng tạm thời bằng cách dùng một lượng vừa đủ Ca(OH)2.
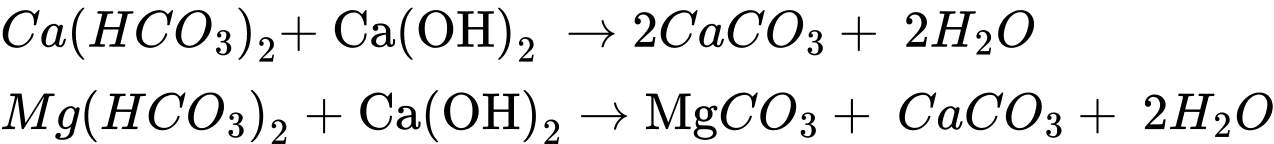
✔️(d) – Đúng. Không thể dùng cách đun sôi để loại bỏ hoàn toàn tính cứng của nước có chứa nhiều các ion sau: Mg2+, Ca2+, Сl-, НСО3- , SO42-. Chỉ loại bỏ được 1 phần Ca2+ và Mg2+ thông qua phản ứng phân hủy Ca(HCO3)2 và Mg(HCO3)2 làm nước cứng chuyển từ nước cứng toàn phần sang nước cứng vĩnh cữu.
✔️(e) – Đúng. nước cứng có thể gây đóng cặn CaCO3, MgCO3 trong nồi hơi tạo thành lớp cách nhiệt ngay dưới đáy nồi, làm cản trở quá trình dẫn nhiệt từ đó có thể gây hiện tượng nổ nồi hơi.
Có 3 phát biểu đúng.
⟹Chọn đáp án C Đáp án: C
❌(a) – Sai. Nước có chứa nhiều ion Mg2+, Ca2+, HCO3- được gọi là -nước có tính cứng tạm thời.
✔️(b) – Đúng. Có thể làm mềm nước có tính cứng tạm thời bằng cách đun sôi nước.
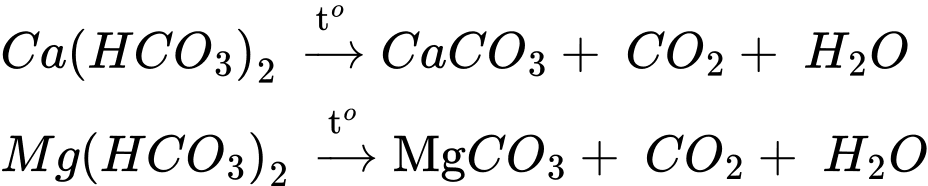
❌(c) – Sai. Không thể loại bỏ tính cứng của nước có tính cứng tạm thời bằng cách dùng một lượng vừa đủ Ca(OH)2.
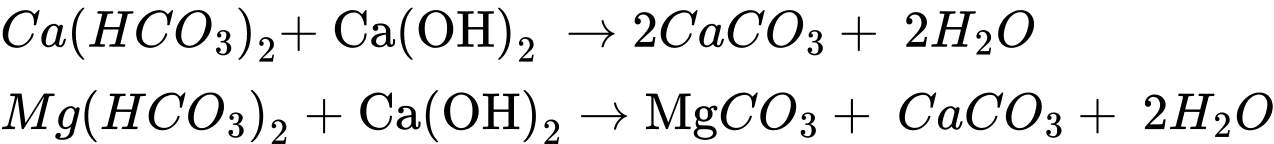
✔️(d) – Đúng. Không thể dùng cách đun sôi để loại bỏ hoàn toàn tính cứng của nước có chứa nhiều các ion sau: Mg2+, Ca2+, Сl-, НСО3- , SO42-. Chỉ loại bỏ được 1 phần Ca2+ và Mg2+ thông qua phản ứng phân hủy Ca(HCO3)2 và Mg(HCO3)2 làm nước cứng chuyển từ nước cứng toàn phần sang nước cứng vĩnh cữu.
✔️(e) – Đúng. nước cứng có thể gây đóng cặn CaCO3, MgCO3 trong nồi hơi tạo thành lớp cách nhiệt ngay dưới đáy nồi, làm cản trở quá trình dẫn nhiệt từ đó có thể gây hiện tượng nổ nồi hơi.
Có 3 phát biểu đúng.
⟹Chọn đáp án C Đáp án: C