Đáp án [BTTL] Bài học 21: Sơ lược về một số kim loại chuyển tiếp và phức chất
Câu 1 [561008]: Kim loại nào sau đây thuộc dãy kim loại chuyển tiếp thứ nhất?
A, Ti.
B, Al.
C, Ba.
D, Na.
Trong bảng tuần hoàn các nguyên tố hóa học, kim loại chuyển tiếp dãy thứ nhất gồm các nguyên tố có số hiệu nguyên tử từ 21 (Sc) đến 29 (Cu), thuộc chu kì 4.

⇒ Chọn đáp án A Đáp án: A

⇒ Chọn đáp án A Đáp án: A
Câu 2 [561010]: Trong bảng tuần hoàn các nguyên tố hoá học, nguyên tố chuyển tiếp dãy thứ nhất được xếp ở
A, chu kì 3.
B, chu kì 4.
C, chu kì 5.
D, chu kì 3 và chu kì 4.
Trong bảng tuần hoàn các nguyên tố hóa học, kim loại chuyển tiếp dãy thứ nhất gồm các nguyên tố có số hiệu nguyên tử từ 21 (Sc) đến 29 (Cu), thuộc chu kì 4.

⇒ Chọn đáp án B Đáp án: B

⇒ Chọn đáp án B Đáp án: B
Câu 3 [561013]: Nguyên tố nào sau đây thuộc nhóm B?
A, [Ar]3d34s2.
B, [Ar]3d104s24p3.
C, [Ar] 3d104s24p5.
D, [Ne]3s23p5.
Các nguyên tố nhóm B đều thuộc chu kì lớn(4,5,6,7). Chúng là các nguyên tố d và nguyên tố f, còn được gọi là các kim loại chuyển tiếp.
Các nguyên tố nhóm B có cấu hình e nguyên tử tận cùng là (n-1)dxnsy
Cấu hình các nguyên tố chu kì 4 : [Ar]3dx4sy
Cấu hình các nguyên tố chu kì 5: [Kr]3dx4sy
⇒ Chọn đáp án A Đáp án: A
Các nguyên tố nhóm B có cấu hình e nguyên tử tận cùng là (n-1)dxnsy
Cấu hình các nguyên tố chu kì 4 : [Ar]3dx4sy
Cấu hình các nguyên tố chu kì 5: [Kr]3dx4sy
⇒ Chọn đáp án A Đáp án: A
Câu 4 [561018]: Xác định số oxi hoá của sắt trong FeO
A, +2.
B, +3.
C, +4.
D, +6.
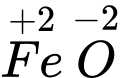
⇒ Chọn đáp án A Đáp án: A
Câu 5 [561019]: Xác định số oxi hoá của sắt trong Fe2O3
A, +2.
B, +3.
C, +4.
D, +6.
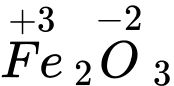
⇒ Chọn đáp án B Đáp án: B
Câu 6 [561020]: Xác định số oxi hoá của sắt trong Fe3O4 (hay FeO – Fe2O3)
A, +4.
B, +1 và +3.
C, +2 và +3.
D, +6.
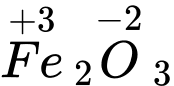
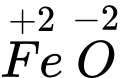
⇒ Chọn đáp án C Đáp án: C
Câu 7 [561021]: Nguyên tử manganese có số oxi hoá +6 trong hợp chất nào sau đây?
A, KMnO4.
B, K2MnO4.
C, MnO2.
D, MnSO4.
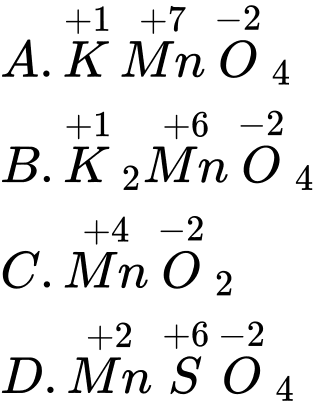
⟹ Chọn đáp án B Đáp án: B
Câu 8 [561024]: Dung dịch có chứa ion Fe3+ có màu
A, đỏ.
B, tím.
C, vàng nâu.
D, xanh lam.

⟹ Dung dịch chứa ion Fe3+ có màu vàng nâu.
⇒ Chọn đáp án C
Câu 9 [561025]: Dung dịch có chứa ion Cu2+ có màu
A, đỏ.
B, tím.
C, vàng nâu.
D, xanh lam.

⟹ Dung dịch Cu2+ có màu xanh lam.
⇒ Chọn đáp án D
Câu 10 [561026]: Dung dịch KMnO4 có chứa nguyên tử Mn với mức oxi hóa +7. Dung dịch KMnO4 có màu
A, vàng.
B, hồng.
C, đỏ.
D, tím.

Dung dịch KMnO4 có chứa nguyên tử Mn với mức oxi hóa +7 có màu tím.
⇒ Chọn đáp án D
Câu 11 [561027]: Trong dãy nguyên tử Sc (Z = 21), Ti (Z = 22), V (Z = 23), Cr (Z = 24), bán kính nguyên tử biến đổi như thế nào?
A, Tăng dần.
B, Không đổi.
C, Giảm dần.
D, Không xác định.
Khi đi từ Sc đến Cr, số proton trong hạt nhân tăng lên, làm tăng điện tích hạt nhân. Điều này làm lực hút giữa hạt nhân và các electron lớp vỏ ngoài tăng lên, dẫn đến bán kính nguyên tử giảm dần.
⇒ Chọn đáp án C Đáp án: C
⇒ Chọn đáp án C Đáp án: C
Câu 12 [561030]: Không nên sử dụng các kim loại chuyển tiếp dãy thứ nhất làm dây chảy trong các cầu chì là vì các kim loại chuyển tiếp dãy thứ nhất có
A, độ cứng cao.
B, nhiệt độ nóng chảy cao.
C, bán kính nguyên tử lớn.
D, cấu trúc tinh thể phức tạp.
❌A. Độ cứng cao: Mặc dù độ cứng có thể là một yếu tố trong một số ứng dụng, nhưng đó không phải là lý do chính để không sử dụng những kim loại này trong cầu chì.
✔️B. Kim loại chuyển tiếp hàng đầu có điểm nóng chảy tương đối cao. Điều này có nghĩa là chúng sẽ không dễ nóng chảy khi có dòng điện tăng đột biến, khiến chúng không phù hợp để sử dụng trong cầu chì.
❌C. Bán kính nguyên tử lớn: Bán kính nguyên tử không ảnh hưởng trực tiếp đến chức năng của cầu chì.
❌D. Cấu trúc tinh thể phức tạp: Cấu trúc tinh thể liên quan nhiều hơn đến các đặc tính tổng thể của vật liệu như độ bền và độ dẫn điện, không phải là lý do khiến vật liệu không phù hợp để làm cầu chì.
⇒ Chọn đáp án B Đáp án: B
✔️B. Kim loại chuyển tiếp hàng đầu có điểm nóng chảy tương đối cao. Điều này có nghĩa là chúng sẽ không dễ nóng chảy khi có dòng điện tăng đột biến, khiến chúng không phù hợp để sử dụng trong cầu chì.
❌C. Bán kính nguyên tử lớn: Bán kính nguyên tử không ảnh hưởng trực tiếp đến chức năng của cầu chì.
❌D. Cấu trúc tinh thể phức tạp: Cấu trúc tinh thể liên quan nhiều hơn đến các đặc tính tổng thể của vật liệu như độ bền và độ dẫn điện, không phải là lý do khiến vật liệu không phù hợp để làm cầu chì.
⇒ Chọn đáp án B Đáp án: B
Câu 13 [561032]: Kim loại được mạ lên sắt để bảo vệ sắt và dùng để chế tạo thép không gỉ (dùng làm thìa, dao, dụng cụ y tế,...) là
A, Al.
B, Mg.
C, Cr.
D, Ca.
Mạ chromium: chromium được mạ lên bề mặt sắt để tạo lớp bảo vệ chống ăn mòn và tăng độ bền.
Thép không gỉ: Thép không gỉ là hợp kim của sắt chứa ít nhất 10,5% chromium. Crom tạo ra một lớp oxide chromium mỏng trên bề mặt, giúp thép chống ăn mòn và gỉ sét, được sử dụng trong các sản phẩm như dao, thìa, dụng cụ y tế, và thiết bị công nghiệp.
⇒ Chọn đáp án C Đáp án: C
Thép không gỉ: Thép không gỉ là hợp kim của sắt chứa ít nhất 10,5% chromium. Crom tạo ra một lớp oxide chromium mỏng trên bề mặt, giúp thép chống ăn mòn và gỉ sét, được sử dụng trong các sản phẩm như dao, thìa, dụng cụ y tế, và thiết bị công nghiệp.
⇒ Chọn đáp án C Đáp án: C
Câu 14 [824954]: Nguyên tố nào sau đây không thể hiện xu hướng có nhiều số oxi hóa trong hợp chất?
A, Cr.
B, Mn.
C, Fe.
D, Al.
Al (Nhôm) là một kim loại thuộc nhóm IIIA và có cấu hình electron lớp ngoài là 3s23p1. Nhôm có xu hướng nhường 3 electron này để đạt cấu hình bền vững của khí hiếm, do đó số oxi hóa phổ biến và gần như duy nhất của nhôm trong các hợp chất là +3. Mặc dù trong một số hợp chất trung gian hoặc phức chất có thể tồn tại các số oxi hóa khác, nhưng chúng rất kém bền.
⇒ Chọn đáp án D Đáp án: D
⇒ Chọn đáp án D Đáp án: D
Câu 15 [824955]: Nguyên tố kim loại có trong hemoglobin làm nhiệm vụ vận chuyển oxygen, duy trì sự sống là
A, sodium.
B, magnesium.
C, iron.
D, aluminium.
Nguyên tố kim loại có trong hemoglobin và đóng vai trò quan trọng trong việc vận chuyển oxygen, duy trì sự sống là iron (Fe).
Ion sắt (Fe2+) ở trung tâm của phân tử heme (một thành phần của hemoglobin) có khả năng liên kết thuận nghịch với phân tử oxygen (O2). Khi máu đi qua phổi, oxygen khuếch tán vào hồng cầu và liên kết với sắt trong hemoglobin. Sau đó, hemoglobin vận chuyển oxygen đến các mô và cơ quan trong cơ thể, nơi oxygen được giải phóng để phục vụ cho các quá trình trao đổi chất.
⇒ Chọn đáp án C Đáp án: C
Ion sắt (Fe2+) ở trung tâm của phân tử heme (một thành phần của hemoglobin) có khả năng liên kết thuận nghịch với phân tử oxygen (O2). Khi máu đi qua phổi, oxygen khuếch tán vào hồng cầu và liên kết với sắt trong hemoglobin. Sau đó, hemoglobin vận chuyển oxygen đến các mô và cơ quan trong cơ thể, nơi oxygen được giải phóng để phục vụ cho các quá trình trao đổi chất.
⇒ Chọn đáp án C Đáp án: C
Câu 16 [824956]: Muối nào sau đây có khả năng làm mất màu thuốc tím trong môi trường sulfuric acid loãng?
A, BaSO4.
B, Na2SO4.
C, FeSO4.
D, ZnSO4.
Thuốc tím là một chất oxy hóa mạnh trong môi trường acid. Muối làm mất màu thuốc tím phải chứa ion kim loại có thể bị oxy hóa lên trạng thái oxy hóa cao hơn.
BaSO4 , Na2SO4 , ZnSO4 có trạng thái ổn định, do đó không có khả năng bị oxy hóa thêm. Trong FeSO4, Fe có số oxi hóa +2 có khả năng bị oxy hóa bởi thuốc tím.
FeSO4 + H2SO4 + KMnO4 ⟶ Fe2(SO4)3 + K2SO4 + MnSO4 + H2O
⇒ Chọn đáp án C Đáp án: C
BaSO4 , Na2SO4 , ZnSO4 có trạng thái ổn định, do đó không có khả năng bị oxy hóa thêm. Trong FeSO4, Fe có số oxi hóa +2 có khả năng bị oxy hóa bởi thuốc tím.
FeSO4 + H2SO4 + KMnO4 ⟶ Fe2(SO4)3 + K2SO4 + MnSO4 + H2O
⇒ Chọn đáp án C Đáp án: C
Câu 17 [824958]: Nguyên tố nào sau đây được mệnh danh là “nguyên tố của màu sắc” do có khả năng thể hiện màu sắc phong phí trong các hợp chất của nó?
A, Iron.
B, Copper.
C, Nickel.
D, Chromium.
Nguyên tố được mệnh danh là chromium (Cr) là "nguyên tố của màu sắc" do khả năng thể hiện vô số màu sắc khác nhau trong các hợp chất của nó vì:
- Chromium có thể tồn tại ở nhiều trạng thái oxy hóa khác nhau, phổ biến nhất là +2, +3 và +6. Mỗi trạng thái oxy hóa này thường tạo ra các ion hoặc hợp chất có màu sắc đặc trưng.
- Các ion chromium có electron ở lớp d. Sự chuyển dời electron giữa các orbital d khác nhau khi hấp thụ ánh sáng trong vùng khả kiến sẽ tạo ra các màu sắc khác nhau.
⇒ Chọn đáp án D Đáp án: D
- Chromium có thể tồn tại ở nhiều trạng thái oxy hóa khác nhau, phổ biến nhất là +2, +3 và +6. Mỗi trạng thái oxy hóa này thường tạo ra các ion hoặc hợp chất có màu sắc đặc trưng.
- Các ion chromium có electron ở lớp d. Sự chuyển dời electron giữa các orbital d khác nhau khi hấp thụ ánh sáng trong vùng khả kiến sẽ tạo ra các màu sắc khác nhau.
⇒ Chọn đáp án D Đáp án: D
Câu 18 [834290]: Thiết bị cảm biến độ ẩm trong công nghiệp thường là giấy hoặc màng polymer chứa 5 – 10% CoCl2 được đặt trong kho hàng, nhà máy. Khi độ ẩm tăng, màu sắc của CoCl2 thay đổi, giúp giám sát môi trường. Điều này quan trọng trong công nghiệp sản xuất, lưu trữ và vận chuyển hàng hóa nhạy cảm với hơi nước.
Cơ chế hoạt động của thiết bị cảm biến dựa trên cân bằng sau:
CoCl2(s) + 6H2O(g)
CoCl2.6H2O(s)
(màu xanh) (không máu) (màu hồng)
Hãy cho biết màu nào cho phép ta dự đoán môi trường đang có xu hướng bị ẩm và cần kiểm soát độ ẩm?
Cơ chế hoạt động của thiết bị cảm biến dựa trên cân bằng sau:
CoCl2(s) + 6H2O(g)
CoCl2.6H2O(s)
(màu xanh) (không máu) (màu hồng)
Hãy cho biết màu nào cho phép ta dự đoán môi trường đang có xu hướng bị ẩm và cần kiểm soát độ ẩm?
A, Màu xanh.
B, Màu đỏ.
C, Không màu.
D, Màu hồng.
* Khi độ ẩm trong không khí tăng, lượng hơi nước (H2O(g)) tăng → phản ứng chuyển dịch theo chiều thuận → tạo CoCl2·6H2O (màu hồng).
* Ngược lại, khi không khí khô hơn, phản ứng chuyển dịch theo chiều nghịch → tạo CoCl2 khan (màu xanh).
→ Màu hồng cho biết môi trường đang ẩm, và đây là dấu hiệu cảnh báo rằng cần kiểm soát lại độ ẩm.
→ Chọn đáp án D Đáp án: D
* Ngược lại, khi không khí khô hơn, phản ứng chuyển dịch theo chiều nghịch → tạo CoCl2 khan (màu xanh).
→ Màu hồng cho biết môi trường đang ẩm, và đây là dấu hiệu cảnh báo rằng cần kiểm soát lại độ ẩm.
→ Chọn đáp án D Đáp án: D
Câu 19 [561071]: Phân tử hay ion nào sau đây không phải là phức chất?
A, [Cu(NH3)4](OH)2.
B, [PtCl4]2–.
C, KMnO4.
D, [PtBr4]2–.
Đặc điểm nổi bật của phức chất:
-Ion kim loại trung tâm: Thường là các kim loại chuyển tiếp, có khả năng tạo liên kết với nhiều loại phối tử khác nhau.
-Phối tử: Có thể là các phân tử hoặc ion mang điện tích âm hoặc trung hòa, có khả năng cung cấp cặp electron cho ion kim loại trung tâm để tạo liên kết.
-Liên kết phối trí: Liên kết giữa ion kim loại trung tâm và phối tử là liên kết đặc biệt, trong đó cặp electron liên kết được cung cấp bởi phối tử.
A.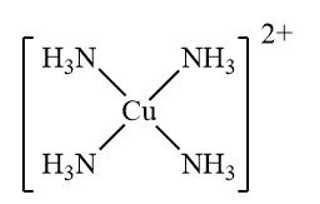
B.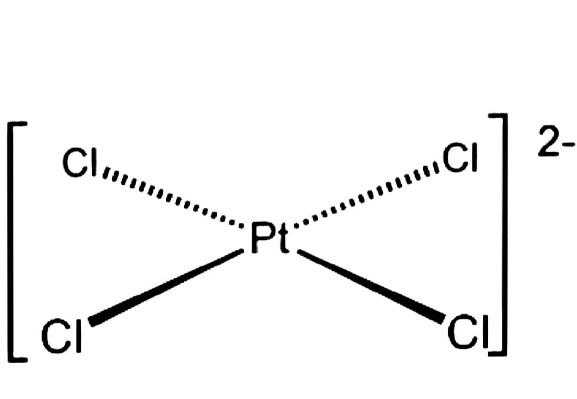
C.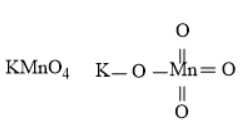
D.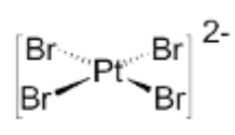
⇒ Chọn đáp án C Đáp án: C
-Ion kim loại trung tâm: Thường là các kim loại chuyển tiếp, có khả năng tạo liên kết với nhiều loại phối tử khác nhau.
-Phối tử: Có thể là các phân tử hoặc ion mang điện tích âm hoặc trung hòa, có khả năng cung cấp cặp electron cho ion kim loại trung tâm để tạo liên kết.
-Liên kết phối trí: Liên kết giữa ion kim loại trung tâm và phối tử là liên kết đặc biệt, trong đó cặp electron liên kết được cung cấp bởi phối tử.
A.

B.

C.
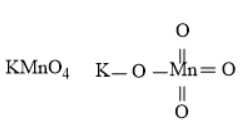
D.

⇒ Chọn đáp án C Đáp án: C
Câu 20 [824961]: Phối tử trong phức chất [PtCl4]2– và [Fe(CO)5] lần lượt là
A, Cl và CO.
B, Pt và Fe.
C, Cl và O.
D, Cl– và CO.
Với [PtCl4]2-: phối tử là Cl-
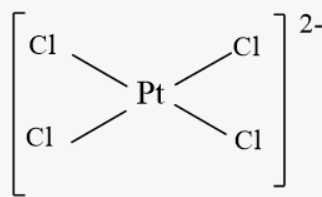
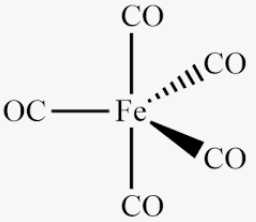
Với [Fe(CO)5] : phối tử là CO
⇒ Chọn đáp án D
Đáp án: D

Với [Fe(CO)5] : phối tử là CO

⇒ Chọn đáp án D
Đáp án: D
Câu 21 [824962]: Số lượng phối tử có trong mỗi phức chất [PtCl4]2– và [Fe(CO)5] lần lượt là
A, 4 và 5.
B, 5 và 6.
C, 2 và 5.
D, 1 và 1.
Trong [PtCl4]2- có 4 phối tử Cl-
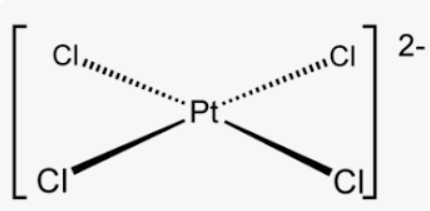
Trong [Fe(CO)5] có 5 phối tử CO
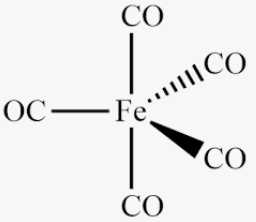
⇒ Chọn đáp án A Đáp án: A

Trong [Fe(CO)5] có 5 phối tử CO

⇒ Chọn đáp án A Đáp án: A
Câu 22 [824963]: Nguyên tử trung tâm của phức chất [PtCl4]2– và [Fe(CO)5] lần lượt là
A, Pt4+ và Fe2+.
B, Pt2+ và Fe2+.
C, Cl và Co.
D, Pt2+ và Fe.
Phức chất [PtCl4]2– có ion trung tâm là Pt2+
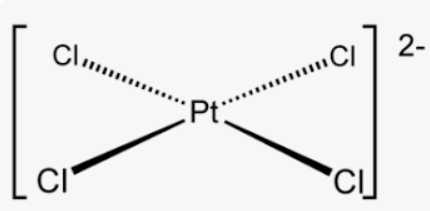
Phức chất [Fe(CO)5] có nguyên tử trung tâm là Fe
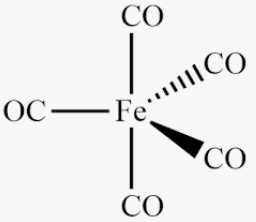
⇒ Chọn đáp án D Đáp án: D

Phức chất [Fe(CO)5] có nguyên tử trung tâm là Fe

⇒ Chọn đáp án D Đáp án: D
Câu 23 [824964]: Điện tích của phức chất [PtCl4]2– và [Fe(CO)5] lần lượt là
A, +2 và +5.
B, +2 và 0.
C, –1 và 0.
D, –2 và 0.
Điện tích của phức chất [PtCl4]2- là 2-. Ký hiệu này thường được viết là -2.
Điện tích của phức chất [Fe(CO)5] là 0. Đây là một phức chất trung hòa, không mang điện tích.
Vậy, điện tích của [PtCl4]2- và [Fe(CO)5] lần lượt là -2 và 0.
⇒ Chọn đáp án D Đáp án: D
Điện tích của phức chất [Fe(CO)5] là 0. Đây là một phức chất trung hòa, không mang điện tích.
Vậy, điện tích của [PtCl4]2- và [Fe(CO)5] lần lượt là -2 và 0.
⇒ Chọn đáp án D Đáp án: D
Câu 24 [561072]: Phối tử trong phức chất sau đây là
A, Cl–.
B, NH3.
C, Cl– và NH3.
D, Pt2+ và Cl–.
Phức chất bao gồm:
- Nguyên tử hoặc ion kim loại trung tâm: Là ion kim loại có khả năng nhận cặp electron từ phối tử.Thường là các kim loại chuyển tiếp như Fe, Cu, Co, Ni, Zn, Pt, Ag...
- Phối tử: Là các phân tử hoặc ion có chứa cặp electron chưa sử dụng, có thể cho cặp electron này để tạo liên kết với ion kim loại trung tâm. Phối tử có thể là trung hòa (H2O, NH3, CO) hoặc mang điện tích (Cl- , CN- ,…)
Có 2 loại phối tử trong phức chất trên là Cl- và NH3
⇒ Chọn đáp án C Đáp án: C
- Nguyên tử hoặc ion kim loại trung tâm: Là ion kim loại có khả năng nhận cặp electron từ phối tử.Thường là các kim loại chuyển tiếp như Fe, Cu, Co, Ni, Zn, Pt, Ag...
- Phối tử: Là các phân tử hoặc ion có chứa cặp electron chưa sử dụng, có thể cho cặp electron này để tạo liên kết với ion kim loại trung tâm. Phối tử có thể là trung hòa (H2O, NH3, CO) hoặc mang điện tích (Cl- , CN- ,…)
Có 2 loại phối tử trong phức chất trên là Cl- và NH3
⇒ Chọn đáp án C Đáp án: C
Câu 25 [561073]: Phối tử trong phức chất [Co(NH3)6]Cl3 là
A, Co3+.
B, NH3.
C, Cl–.
D, NH3 và Cl–.
Phức chất bao gồm:
- Nguyên tử hoặc ion kim loại trung tâm: Là ion kim loại có khả năng nhận cặp electron từ phối tử.Thường là các kim loại chuyển tiếp như Fe, Cu, Co, Ni, Zn, Pt, Ag...
- Phối tử: Là các phân tử hoặc ion có chứa cặp electron chưa sử dụng, có thể cho cặp electron này để tạo liên kết với ion kim loại trung tâm. Phối tử có thể là trung hòa (H2O, NH3, CO) hoặc mang điện tích (Cl- , CN- ,…)
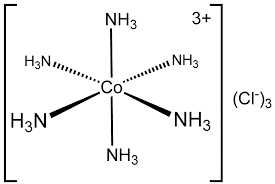
⟹ Phối tử trong phức chất [Co(NH3)6]Cl3 là NH3
⇒ Chọn đáp án B Đáp án: B
- Nguyên tử hoặc ion kim loại trung tâm: Là ion kim loại có khả năng nhận cặp electron từ phối tử.Thường là các kim loại chuyển tiếp như Fe, Cu, Co, Ni, Zn, Pt, Ag...
- Phối tử: Là các phân tử hoặc ion có chứa cặp electron chưa sử dụng, có thể cho cặp electron này để tạo liên kết với ion kim loại trung tâm. Phối tử có thể là trung hòa (H2O, NH3, CO) hoặc mang điện tích (Cl- , CN- ,…)

⟹ Phối tử trong phức chất [Co(NH3)6]Cl3 là NH3
⇒ Chọn đáp án B Đáp án: B
Câu 26 [824966]: Số lượng phối tử có trong phức chất [PtCl4(NH3)2] là
A, 6.
B, 2.
C, 4.
D, 7.
Số lượng phối tử có trong phức chất [PtCl4(NH3)2] là 6.
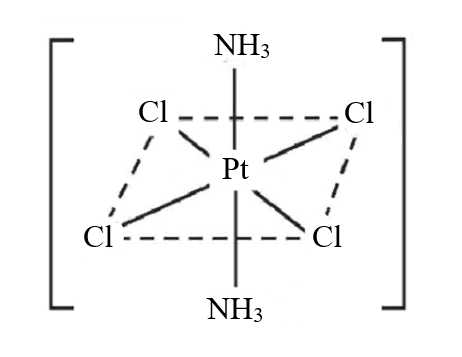
⇒ Chọn đáp án A Đáp án: A

⇒ Chọn đáp án A Đáp án: A
Câu 27 [561076]: Nguyên tử trung tâm trong phức chất sau đây là
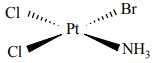

A, Cl–.
B, Br–.
C, Pt2+.
D, NH3.
Nguyên tử trung tâm trong phức chất thường là ion kim loại có khả năng tạo liên kết phối trí với các phối tử xung quanh. Ở đây, Pt 2+ tạo liên kết với 4 phối tử: Cl-, Br-, NH3
⇒ Chọn đáp án C Đáp án: C
⇒ Chọn đáp án C Đáp án: C
Câu 28 [561077]: Nguyên tử trung tâm trong phức chất [Co(en)2Br2]+ là
A, Co+.
B, CO2+.
C, CO3+.
D, CO6+.
Giả sử điện tích của Co trong phức là x
Tổng hợp điện tích trong phức [Co(en)2Br2]+ ta có:
x + 0.2 + (-1).2 = +1
⟹ x = +3
Vậy nguyên tử trung tâm trong phức [Co(en)2Br2]+ là Co3+
⟹ Chọn đáp án C Đáp án: C
Tổng hợp điện tích trong phức [Co(en)2Br2]+ ta có:
x + 0.2 + (-1).2 = +1
⟹ x = +3
Vậy nguyên tử trung tâm trong phức [Co(en)2Br2]+ là Co3+
⟹ Chọn đáp án C Đáp án: C
Câu 29 [561082]: Phức chất sau đây có điện tích bằng bao nhiêu?
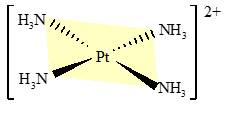

A, 1+.
B, 2+.
C, 3+.
D, 4+.
Phức chất [Pt(NH3)4]2+ gồm ion trung tâm Pt2+ và 4 phối tử trung hòa NH3 nên phức chất [Pt(NH3)4]2+ có điện tích là 2+.
⟹ Chọn đáp án B Đáp án: B
⟹ Chọn đáp án B Đáp án: B
Câu 30 [824967]: Phức chất của Cr(0) có dạng hình học bát diện chỉ chứa phối tử CO có công thức hóa học là
A, [Cr(CO)4].
B, [Cr(CO)6].
C, [Cr(CO)4]2+.
D, [Cr(CO)6]2+.
Phức chất Cr(0) gồm nguyên tử trung tâm Cr(0) và 6 phối tử CO( do có dạng bát diện ) trung hòa nên phức chất có điện tích = 0.
Công thức của phức là [Cr(CO)6].
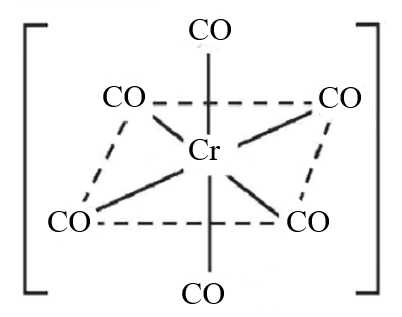
⟹ Chọn đáp án B Đáp án: B
Công thức của phức là [Cr(CO)6].

⟹ Chọn đáp án B Đáp án: B
Câu 31 [561083]: Cho các phức chất sau: [Cu(OH2)6]2+, [CoF6]3–, [Ni(CO)4], [PtCl2(NH3)2]. Hãy cho biết điện tích của các phức chất trên lần lượt là
A, 1+, 3–, 0, 0.
B, 2+, 3–, 0, 0.
C, 2+, 1–, 2+, 0.
D, 3+, 1–, +2, +2.
Điện tích của các phức là chỉ số bên ngoài dấu [...].
Điện tích của các phức [Cu(OH2)6]2+, [CoF6]3–, [Ni(CO)4], [PtCl2(NH3)2] lần lượt là 2+, 3+, 0, 0
⇒ Chọn đáp án B Đáp án: B
Điện tích của các phức [Cu(OH2)6]2+, [CoF6]3–, [Ni(CO)4], [PtCl2(NH3)2] lần lượt là 2+, 3+, 0, 0
⇒ Chọn đáp án B Đáp án: B
Câu 32 [561084]: Khi cho copper(II) sulfate vào nước thì hình thành phức chất bát diện với các phối tử là 6 phân tử H2O. Công thức của phức chất là
A, [Cu(OH2)6]3+.
B, [Cu(OH2)6]2+.
C, [Cu(OH2)4]3+.
D, [Cu(OH2)4]2+.
Khi cho copper(II) sulfate vào nước thì hình thành phức chất bát diện với các phối tử là 6 phân tử H2O. Công thức của phức chất là
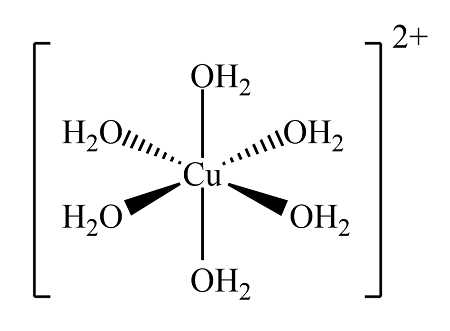
⇒ Chọn đáp án B Đáp án: B

⇒ Chọn đáp án B Đáp án: B
Câu 33 [824968]: Công thức tổng quát của phức chất (với nguyên tử trung tâm M và phối tử L) có dạng tứ diện và bát diện lần lượt là
A, [ML2] và [ML4].
B, [ML4] và [ML6].
C, [ML6] và [ML2].
D, [ML6] và [ML4].
Công thức tổng quát của phức chất (với nguyên tử trung tâm M và phối tử L) có dạng tứ diện và bát diện lần lượt là [ML4] và [ML6].
⇒ Chọn đáp án B Đáp án: B
⇒ Chọn đáp án B Đáp án: B
Câu 34 [824969]: Dạng hình học nào sau đây là đúng nhất có thể có của phức chất có công thức tổng quát [ML4] (với nguyên tử trung tâm M và phối tử L)?
A, Tứ diện.
B, Vuông phẳng.
C, Bát diện.
D, Tứ diện hoặc vuông phẳng.
Phức chất [ML4] có 4 phối tử L nên có dạng tứ diện hoặc dạng vuông phẳng.
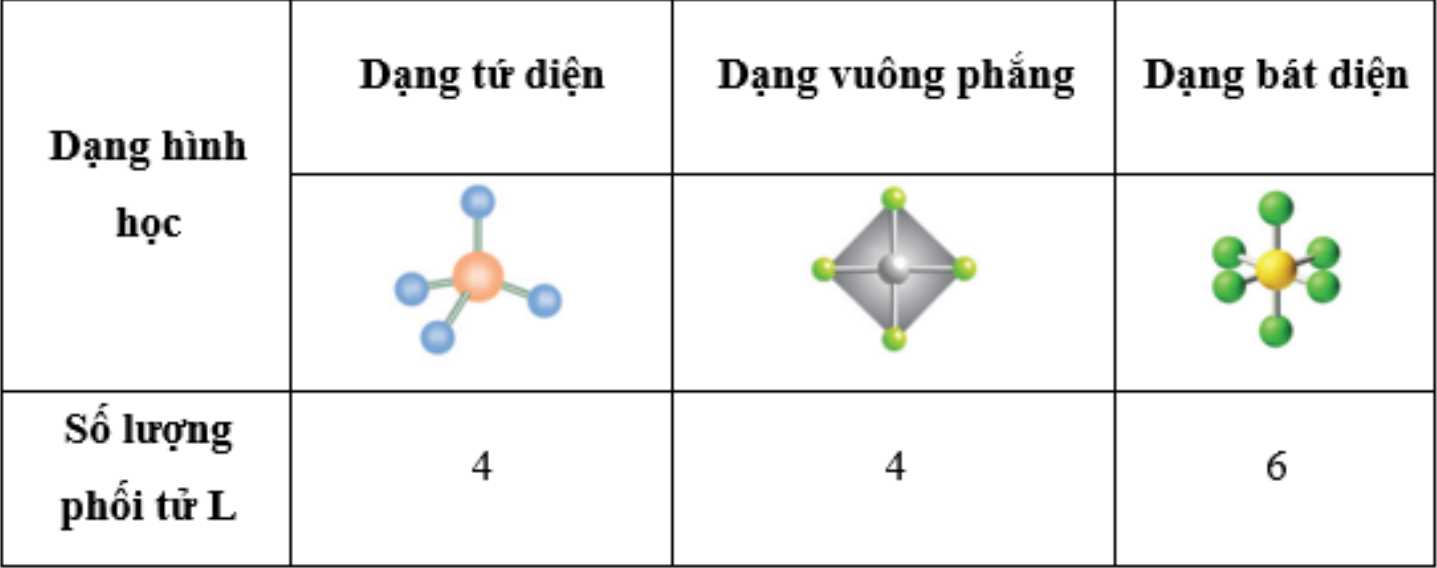
⇒ Chọn đáp án D Đáp án: D

⇒ Chọn đáp án D Đáp án: D
Câu 35 [824974]: Dạng hình học có thể có của phức chất [FeF6]3– là
A, tứ diện.
B, bát diện.
C, vuông phẳng.
D, tứ diện hoặc vuông phẳng.
Phức chất [FeF6]3− có dạng [ML6] nên dạng hình học là bát diện.
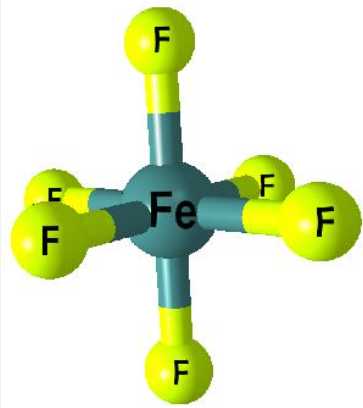
⇒ Chọn đáp án B
Đáp án: B

⇒ Chọn đáp án B
Đáp án: B
Câu 36 [561090]: Phức chất nào sau đây không có dạng hình học bát diện?
A, [Cu(EDTA)]3–.
B, [Cu(en)3]2+.
C, [Co(C2O4)3]3–.
D, [PtCl2(NH3)2].
Phân tích các đáp án:
A. EDTA là phối tử đa càng => dạng bát diện
B.en là phối tử hai càng, có 3 en nên ở dạng ML6 => dạng bát diện.
C. C2O4 2- là phối tử hai càng, có 3 C2O4 2- nên ở dạng ML6 => dạng bát diện.
⇒ Chọn đáp án D
Đáp án: D
A. EDTA là phối tử đa càng => dạng bát diện
B.en là phối tử hai càng, có 3 en nên ở dạng ML6 => dạng bát diện.
C. C2O4 2- là phối tử hai càng, có 3 C2O4 2- nên ở dạng ML6 => dạng bát diện.
⇒ Chọn đáp án D
Đáp án: D
Câu 37 [561111]: Biết rằng phức chất aqua của ion Mn2+ có dạng hình học bát diện. Công thức hoá học các phức chất là
A, [Mn(OH2)6]2+.
B, [Mn(OH2)6]3+.
C, [Mn(OH2)4]2+.
D, [Mn(OH2)4]3+.
Mn2+ là ion trung tâm.
H2O là phối tử trung tính.
Số phối trí là 6, tạo cấu trúc bát diện.
Công thức của phức là: [Mn(OH2)6]2+.
⇒ Chọn đáp án A Đáp án: A
H2O là phối tử trung tính.
Số phối trí là 6, tạo cấu trúc bát diện.
Công thức của phức là: [Mn(OH2)6]2+.
⇒ Chọn đáp án A Đáp án: A
Câu 38 [561112]: Biết rằng phức chất aqua của ion Co2+ có dạng hình học bát diện. Công thức hoá học các phức chất là
A, [Co(OH2)6]2+.
B, [Co(OH2)6]3+.
C, [Co(OH2)4]2+.
D, [Co(OH2)4]3+.
Co2+ là ion trung tâm.
H2O là phối tử trung tính.
Số phối trí là 6, tạo cấu trúc bát diện.
Công thức của phức là: [Co(OH2)6]2+.
⇒ Chọn đáp án A Đáp án: A
H2O là phối tử trung tính.
Số phối trí là 6, tạo cấu trúc bát diện.
Công thức của phức là: [Co(OH2)6]2+.
⇒ Chọn đáp án A Đáp án: A
Câu 39 [561117]: Phối tử thay thế và phối tử bị thay thế trong phương trình sau lần lượt là
[Ni(OH2)6]2+(aq) + 6NH3(aq) [Ni(NH3)6]2+(aq) + 6H2O(l)
[Ni(NH3)6]2+(aq) + 6H2O(l)
[Ni(OH2)6]2+(aq) + 6NH3(aq)
 [Ni(NH3)6]2+(aq) + 6H2O(l)
[Ni(NH3)6]2+(aq) + 6H2O(l) A, H2O và NH3.
B, NH3 và H2O.
C, [Ni(OH2)6]2+ và [Ni(NH3)6]2+.
D, [Ni(OH2)6]2+ và NH3.
[Ni(OH2)6]2+(aq) + 6NH3(aq) ⟶ [Ni(NH3)6]2+(aq) + 6H2O(l)
Ở Pt trên, H2O trong [Ni(OH2)6]2+ đã bị thay thế bởi NH3 để tạo thành phức [Ni(NH3)6]2+ Vây phối tử thay thế là NH3 và phối tử bị thay thế là H2O.
⇒ Chọn đáp án B Đáp án: B
Ở Pt trên, H2O trong [Ni(OH2)6]2+ đã bị thay thế bởi NH3 để tạo thành phức [Ni(NH3)6]2+ Vây phối tử thay thế là NH3 và phối tử bị thay thế là H2O.
⇒ Chọn đáp án B Đáp án: B
Câu 40 [561118]: Phối tử thay thế và phối tử bị thay thế trong phương trình sau lần lượt là
[PtCl4]2–(aq) + 2NH3(aq) [PtCl2(NH3)2](s) + 2Cl–(aq)
[PtCl2(NH3)2](s) + 2Cl–(aq)
[PtCl4]2–(aq) + 2NH3(aq)
 [PtCl2(NH3)2](s) + 2Cl–(aq)
[PtCl2(NH3)2](s) + 2Cl–(aq) A, Cl– và NH3.
B, NH3 và Cl–.
C, [PtCl4]2– và [PtCl2(NH3)2].
D, [PtCl4]2– và NH3.
[PtCl4]2–(aq) + 2NH3(aq) ⟶ [PtCl2(NH3)2](s) + 2Cl–(aq)
Ở Pt trên, Cl - trong [PtCl4]2– đã bị thay thế bởi NH3 để tạo thành phức [PtCl2(NH3)2]
Vây phối tử thay thế là NH3 và phối tử bị thay thế là Cl -
⇒ Chọn đáp án B Đáp án: B
Ở Pt trên, Cl - trong [PtCl4]2– đã bị thay thế bởi NH3 để tạo thành phức [PtCl2(NH3)2]
Vây phối tử thay thế là NH3 và phối tử bị thay thế là Cl -
⇒ Chọn đáp án B Đáp án: B
Câu 41 [561119]: Cho phản ứng dưới đây:
NiCl2(s) + X(l) [Ni(OH2)6]2+(aq) + Y(aq)
[Ni(OH2)6]2+(aq) + Y(aq)
Phối tử thay thế X có thể là
NiCl2(s) + X(l)
 [Ni(OH2)6]2+(aq) + Y(aq)
[Ni(OH2)6]2+(aq) + Y(aq)Phối tử thay thế X có thể là
A, H2O.
B, NH3.
C, Cl–.
D, O2.
Chất tạo thành là [Ni(OH2)6]2+, tức là ion Ni2+ trong dung dịch đã tạo phức với phối tử H2O (aqua).Điều này cho thấy NiCl2 đã hòa tan và các ion Cl- bị thay thế bởi H2O để tạo thành phức.
NiCl2 + 6H2O ⟶ [Ni(OH2)6]2+ + 2Cl-
⇒ Chọn đáp án A Đáp án: A
NiCl2 + 6H2O ⟶ [Ni(OH2)6]2+ + 2Cl-
⇒ Chọn đáp án A Đáp án: A