Đáp án [BTTL] Bài học 22: Đặc trưng – Điền vào chỗ trống các chủ đề vô cơ 12
Câu 1 [705396]: Thế điện cực chuẩn của cặp oxi hóa – khử càng lớn thì tính oxi hóa của dạng oxi hóa càng …(1)… và tính khử của dạng khử càng …(2)… Nội dung phù hợp trong ô trống (1), (2) lần lượt là
A, mạnh, yếu.
B, yếu, mạnh.
C, mạnh, mạnh.
D, yếu, yếu.
Thế điện cực chuẩn của cặp oxi hóa – khử càng lớn thì tính oxi hóa của dạng oxi hóa càng mạnh và tính khử của dạng khử càng yếu.
Giải thích:
Dựa vào đặc điểm của thế điện cực chuẩn, thế điện cực chuẩn càng lớn:
+) Dạng oxi hóa (chất nhận electron) có tính oxi hóa mạnh hơn, vì dễ dàng nhận electron.
+) Dạng khử (chất cho electron) có tính khử yếu hơn, vì khó nhường electron.
⇒ Chọn đáp án A Đáp án: A
Giải thích:
Dựa vào đặc điểm của thế điện cực chuẩn, thế điện cực chuẩn càng lớn:
+) Dạng oxi hóa (chất nhận electron) có tính oxi hóa mạnh hơn, vì dễ dàng nhận electron.
+) Dạng khử (chất cho electron) có tính khử yếu hơn, vì khó nhường electron.
⇒ Chọn đáp án A Đáp án: A
Câu 2 [704019]: “Trong pin điện hoá, điện năng được sinh ra từ phản ứng ..(1).. là một quá trình ..(2)..”. Nội dung phù hợp trong ô trống (1), (2) lần lượt là
A, oxi hoá, không tự diễn biến.
B, oxi hoá - khử, tự diễn biến.
C, khử, tự diễn biến.
D, trao đổi, oxi hóa - khử.
- Trong pin điện hóa, điện năng được sinh ra nhờ vào sự chuyển đổi năng lượng hóa học thành năng lượng điện. Phản ứng xảy ra trong pin là một phản ứng oxi hóa - khử do có sự chuyển electron từ chất khử (bị oxi hóa) sang chất oxi hóa (bị khử).
- Phản ứng trong pin điện hóa là một phản ứng tự diễn biến, tức là nó có thể diễn ra mà không cần cung cấp năng lượng từ bên ngoài.
⇒ Trong pin điện hoá, điện năng được sinh ra từ phản ứng oxi hoá - khử là một quá trình tự diễn biến.
⇒ Chọn đáp án B Đáp án: B
- Phản ứng trong pin điện hóa là một phản ứng tự diễn biến, tức là nó có thể diễn ra mà không cần cung cấp năng lượng từ bên ngoài.
⇒ Trong pin điện hoá, điện năng được sinh ra từ phản ứng oxi hoá - khử là một quá trình tự diễn biến.
⇒ Chọn đáp án B Đáp án: B
Câu 3 [705439]: Sức điện động chuẩn của ...(1)... được tính bằng ...(2)... của thế điện cực chuẩn tương ứng của điện cực dương và điện cực âm. Nội dung phù hợp trong ô trống (1), (2) lần lượt là
A, pin Galvani, hiệu.
B, pin Galvani, tổng.
C, acquy, hiệu.
D, acquy, tổng.
Sức điện động chuẩn của pin Galvani được tính bằng hiệu của thế điện cực chuẩn tương ứng của điện cực dương và điện cực âm.
Công thức:
Eopin = Eocathode − Eoanode
Trong đó:
Eocathode là thế điện cực chuẩn của điện cực dương (nơi xảy ra quá trình khử).
Eoanode là thế điện cực chuẩn của điện cực âm (nơi xảy ra quá trình oxi hóa).
⇒ Chọn đáp án: A Đáp án: A
Công thức:
Eopin = Eocathode − Eoanode
Trong đó:
Eocathode là thế điện cực chuẩn của điện cực dương (nơi xảy ra quá trình khử).
Eoanode là thế điện cực chuẩn của điện cực âm (nơi xảy ra quá trình oxi hóa).
⇒ Chọn đáp án: A Đáp án: A
Câu 4 [705703]: Nguồn điện ...(1)... là một loại nguồn điện được tạo ra bằng cách sử dụng các phản ứng hoá học để tạo ra ...(2)... Nội dung phù hợp trong ô trống (1), (2) lần lượt là
A, cơ học, dòng điện.
B, pin, nhiệt năng.
C, hoá học, điện năng.
D, acquy, điện năng.
Nguồn điện hoá học là một loại nguồn điện được tạo ra bằng cách sử dụng các phản ứng hoá học để tạo ra điện năng.
Giải thích:
Nguồn điện hóa học là loại nguồn điện được tạo ra nhờ các phản ứng hóa học xảy ra bên trong pin hoặc ắc quy. Khi các chất tham gia phản ứng, chúng chuyển hóa năng lượng hóa học thành năng lượng điện, tạo ra dòng electron dịch chuyển trong mạch ngoài, tức là tạo ra dòng điện.
Ví dụ:
⭐ Pin điện hóa (pin khô, pin kiềm, pin lithium, v.v.): Trong pin, các phản ứng oxi hóa – khử xảy ra giữa hai điện cực (cực dương và cực âm) với dung dịch điện phân giúp tạo ra dòng điện.
⭐ Ắc quy chì - acid: Khi hoạt động, ắc quy sử dụng phản ứng hóa học giữa chì (Pb), lead dioxide (PbO2) và dung dịch sulfuric acid (H2SO4) để tạo ra điện.
⇒ Chọn đáp án C Đáp án: C
Giải thích:
Nguồn điện hóa học là loại nguồn điện được tạo ra nhờ các phản ứng hóa học xảy ra bên trong pin hoặc ắc quy. Khi các chất tham gia phản ứng, chúng chuyển hóa năng lượng hóa học thành năng lượng điện, tạo ra dòng electron dịch chuyển trong mạch ngoài, tức là tạo ra dòng điện.
Ví dụ:
⭐ Pin điện hóa (pin khô, pin kiềm, pin lithium, v.v.): Trong pin, các phản ứng oxi hóa – khử xảy ra giữa hai điện cực (cực dương và cực âm) với dung dịch điện phân giúp tạo ra dòng điện.
⭐ Ắc quy chì - acid: Khi hoạt động, ắc quy sử dụng phản ứng hóa học giữa chì (Pb), lead dioxide (PbO2) và dung dịch sulfuric acid (H2SO4) để tạo ra điện.
⇒ Chọn đáp án C Đáp án: C
Câu 5 [703920]: “Điện phân là quá trình ...(1)... xảy ra trên bề mặt các điện cực khi có dòng điện ...(2)... đi qua chất điện li nóng chảy hoặc dung dịch chất điện li”. Nội dung phù hợp trong ô trống (1), (2) lần lượt là
A, khử, một chiều.
B, oxi hoá, một chiều.
C, oxi hoá – khử, xoay chiều.
D, oxi hoá – khử, một chiều.
- Điện phân là một quá trình hóa học trong đó xảy ra sự oxi hóa (mất electron) tại anode (cực dương) và khử (nhận electron) tại cathode (cực âm).
- Để xảy ra điện phân, cần có dòng điện một chiều làm cho các ion dương (cation) di chuyển về cathode và các ion âm (anion) di chuyển về anode.
⇒ Điện phân là quá trình oxi hoá – khử xảy ra trên bề mặt các điện cực khi có dòng điện một chiều đi qua chất điện li nóng chảy hoặc dung dịch chất điện li.
⇒ Chọn đáp án D Đáp án: D
- Để xảy ra điện phân, cần có dòng điện một chiều làm cho các ion dương (cation) di chuyển về cathode và các ion âm (anion) di chuyển về anode.
⇒ Điện phân là quá trình oxi hoá – khử xảy ra trên bề mặt các điện cực khi có dòng điện một chiều đi qua chất điện li nóng chảy hoặc dung dịch chất điện li.
⇒ Chọn đáp án D Đáp án: D
Câu 6 [705569]: Ion kim loại ứng với thế điện cực chuẩn …(1)… hơn sẽ được điện phân trước ở …(2)… Nội dung phù hợp trong ô trống (1), (2) lần lượt là
A, dương, cực dương.
B, dương, cực âm.
C, âm, cực âm.
D, âm, cực dương.
Ion kim loại ứng với thế điện cực chuẩn dương hơn sẽ được điện phân trước ở cực âm.
Giải thích:
- Thế điện cực chuẩn của một cặp oxi hoá - khử thể hiện khả năng nhận electron (bị khử) nên:
+ Ion có thế điện cực chuẩn (Eo) dương hơn sẽ dễ bị khử (dễ nhận e hơn) để hình thành kim loại tự do.
+ Ion có thế điện cực chuẩn (Eo) âm hơn sẽ khó bị khử hơn (thường ít tham gia vào quá trình điện phân nếu có mặt của các ion có Eo dương hơn)
⟶ Ưu tiên điện phân ion có thế điện cực chuẩn dương hơn trước.
- Quá trình nhận electron là quá trình khử, xảy ra ở cathode (cực âm).
⇒ Chọn đáp án B Đáp án: B
Giải thích:
- Thế điện cực chuẩn của một cặp oxi hoá - khử thể hiện khả năng nhận electron (bị khử) nên:
+ Ion có thế điện cực chuẩn (Eo) dương hơn sẽ dễ bị khử (dễ nhận e hơn) để hình thành kim loại tự do.
+ Ion có thế điện cực chuẩn (Eo) âm hơn sẽ khó bị khử hơn (thường ít tham gia vào quá trình điện phân nếu có mặt của các ion có Eo dương hơn)
⟶ Ưu tiên điện phân ion có thế điện cực chuẩn dương hơn trước.
- Quá trình nhận electron là quá trình khử, xảy ra ở cathode (cực âm).
⇒ Chọn đáp án B Đáp án: B
Câu 7 [825027]: “Trong dung dịch điện phân, cathode là cực …(1)… xảy ra quá trình …(2)…”. Nội dung phù hợp trong các ô trống (1), (2) lần lượt là
A, dương, oxi hóa.
B, âm, oxi hóa.
C, dương, khử.
D, âm, khử.
- Điện phân là một quá trình hóa học trong đó xảy ra sự oxi hóa (mất electron) tại anode (cực dương) và khử (nhận electron) tại cathode (cực âm).
⟹ Trong dung dịch điện phân, cathode là cực âm xảy ra quá trình khử.
⟹ Chọn đáp án D Đáp án: D
⟹ Trong dung dịch điện phân, cathode là cực âm xảy ra quá trình khử.
⟹ Chọn đáp án D Đáp án: D
Câu 8 [825028]: “Ion Na+ không bị khử trong điện phân dung dịch NaCl vì thế …(1)… bị khử tạo thành …(2)….”. Nội dung phù hợp trong các ô trống (1), (2) lần lượt là
A, nước, khí H2.
B, nước, khí O2.
C, ion Cl-, khí Cl2.
D, ion Na+, kim loại Na.
Điện phân dung dịch NaCl chính là việc cho dòng điện một chiều chạy qua dung dịch NaCl. Trong quá trình này, dung dịch muối NaCl sẽ được tách ra thành Na+ và Cl–. Trong đó các ion Na+ sẽ di chuyển về hướng cực âm (cathode) và Cl– sẽ di chuyển về cực dương (anode). Phương pháp này được ứng dụng rất rộng rãi trong đời sống.
Cực dương (Anode): Xảy ra sự oxi hóa
2Cl ⟶ Cl2 + 2e
Cực âm (Cathode): Xảy ra sự khử
2H2O + 2e → H2 + 2OH-
Quá trình điện phân:
2NaCl + 2H2O 2NaOH + H2 + Cl2.
2NaOH + H2 + Cl2.
⟹ Ion Na+ không bị khử trong điện phân dung dịch NaCl vì thế nước bị khử tạo thành khí H2.
⟹ Chọn đáp án A Đáp án: A
Cực dương (Anode): Xảy ra sự oxi hóa
2Cl ⟶ Cl2 + 2e
Cực âm (Cathode): Xảy ra sự khử
2H2O + 2e → H2 + 2OH-
Quá trình điện phân:
2NaCl + 2H2O
 2NaOH + H2 + Cl2.
2NaOH + H2 + Cl2.
⟹ Ion Na+ không bị khử trong điện phân dung dịch NaCl vì thế nước bị khử tạo thành khí H2.
⟹ Chọn đáp án A Đáp án: A
Câu 9 [705687]: Trong vỏ Trái Đất, các kim loại …(1)… tồn tại chủ yếu dưới dạng …(2)... Nội dung phù hợp trong ô trống (1), (2) lần lượt là
A, Fe và Na, đơn chất.
B, Ag và Cu, hợp chất.
C, K và Li, hợp chất.
D, Au và Ag, đơn chất.
Trong vỏ Trái Đất, các kim loại Au và Ag tồn tại chủ yếu dưới dạng đơn chất.
Phân tích:
Kim loại trong vỏ Trái Đất thường tồn tại dưới dạng hợp chất, trừ một số loại kim có tính khử yếu như vàng (Au), bạc (Ag), bạch kim (Pt),... có thể tồn tại ở dạng đơn chất.
⭐ Fe và Na: Là các loại kim loại hoạt động mạnh, thường tồn tại trong tự nhiên dưới dạng hợp chất chứ không phải chất đơn.
⭐ Ag và Cu: Đồng tồn tại ở dạng hợp chất, nhưng bạc có thể được tìm thấy ở dạng đơn chất trong tự nhiên.
⭐ K và Li: Là loại kim loại kiềm, có tính khử mạnh nên chỉ tồn tại dưới dạng hợp chất .
⭐ Au và Ag: Là những loại kim loại có tính khử yếu, có thể tồn tại ở dạng đơn chất trong tự nhiên.
⇒ Chọn đáp án D Đáp án: D
Phân tích:
Kim loại trong vỏ Trái Đất thường tồn tại dưới dạng hợp chất, trừ một số loại kim có tính khử yếu như vàng (Au), bạc (Ag), bạch kim (Pt),... có thể tồn tại ở dạng đơn chất.
⭐ Fe và Na: Là các loại kim loại hoạt động mạnh, thường tồn tại trong tự nhiên dưới dạng hợp chất chứ không phải chất đơn.
⭐ Ag và Cu: Đồng tồn tại ở dạng hợp chất, nhưng bạc có thể được tìm thấy ở dạng đơn chất trong tự nhiên.
⭐ K và Li: Là loại kim loại kiềm, có tính khử mạnh nên chỉ tồn tại dưới dạng hợp chất .
⭐ Au và Ag: Là những loại kim loại có tính khử yếu, có thể tồn tại ở dạng đơn chất trong tự nhiên.
⇒ Chọn đáp án D Đáp án: D
Câu 10 [702828]: Tinh thể kim loại chứa các …(1)… sắp xếp theo trật tự nhất định cùng với các …(2)… chuyển động tự do. Nội dung phù hợp trong các ô trống (1), (2) lần lượt là
A, hạt kim loại, hạt nhân nguyên tử.
B, hạt nhân nguyên tử, hạt kim loại.
C, electron tự do, cation kim loại.
D, cation kim loại, electron tự do.
- Trong kim loại, khi các nguyên tử mất đi electron ở lớp vỏ ngoài cùng sẽ trở thành các ion dương (cation). Những ion này chiếm các vị trí cố định trong mạng tinh thể kim loại, tạo nên cấu trúc trật tự.
- Các electron bị mất không bị giữ cố định bởi bất kỳ ion dương nào mà chuyển động tự do trong tinh thể kim loại.
⇒ Tinh thể kim loại chứa các cation kim loại sắp xếp theo trật tự nhất định cùng với các electron tự do chuyển động tự do.
Chọn đáp án D Đáp án: D
- Các electron bị mất không bị giữ cố định bởi bất kỳ ion dương nào mà chuyển động tự do trong tinh thể kim loại.
⇒ Tinh thể kim loại chứa các cation kim loại sắp xếp theo trật tự nhất định cùng với các electron tự do chuyển động tự do.
Chọn đáp án D Đáp án: D
Câu 11 [704176]: “Kim loại có vẻ sáng lấp lánh (tính ánh kim) là do các ...(1)... trong tinh thể ...(2)... hầu hết những tia sáng mà mắt còn người nhìn thấy được." Nội dung phù hợp trong ô trống (1), (2) lần lượt là
A, cation, phản xạ.
B, electron tự do, phản xạ.
C, cation, hấp thụ.
D, electron tự do, hấp thụ.
Trong tinh thể kim loại, các nguyên tử kim loại sắp xếp theo một mạng tinh thể chặt chẽ. Các electron ở lớp ngoài cùng (electron hóa trị) không bị giữ chặt bởi hạt nhân mà di chuyển tự do trong mạng tinh thể, tạo thành "đám mây electron". Những electron tự do này có khả năng dao động và tương tác với ánh sáng khi nó chiếu vào bề mặt kim loại.
→ Kim loại có vẻ sáng lấp lánh (tính ánh kim) là do các electron tự do trong tinh thể phản xạ hầu hết những tia sáng mà mắt còn người nhìn thấy được.
⇒ Chọn đáp án B Đáp án: B
→ Kim loại có vẻ sáng lấp lánh (tính ánh kim) là do các electron tự do trong tinh thể phản xạ hầu hết những tia sáng mà mắt còn người nhìn thấy được.
⇒ Chọn đáp án B Đáp án: B
Câu 12 [704365]: Do có …(1)… vừa phải và dẫn điện tốt nên đồng được sử dụng làm …(2)… trong các thiết bị và mạng lưới điện gia dụng. Nội dung phù hợp trong ô trống (1), (2) lần lượt là
A, độ bền, dây dẫn.
B, độ cứng, dây dẫn.
C, tính dẻo, điện trở.
D, tính đàn hồi, dây truyền.
Do có độ cứng vừa phải và dẫn điện tốt nên đồng được sử dụng làm dây dẫn trong các thiết bị và mạng lưới điện gia dụng.
Giải thích:
- Đồng có độ dẫn điện rất cao, chỉ đứng sau bạc. Điều này giúp giảm tổn thất năng lượng khi truyền tải điện.
- Đồng không quá cứng nhưng cũng không quá mềm, vừa đủ để giữ được hình dạng ổn định trong quá trình sử dụng mà vẫn có thể dễ dàng chế tạo, uốn nắn.
⇒ Chọn đáp án B Đáp án: B
Giải thích:
- Đồng có độ dẫn điện rất cao, chỉ đứng sau bạc. Điều này giúp giảm tổn thất năng lượng khi truyền tải điện.
- Đồng không quá cứng nhưng cũng không quá mềm, vừa đủ để giữ được hình dạng ổn định trong quá trình sử dụng mà vẫn có thể dễ dàng chế tạo, uốn nắn.
⇒ Chọn đáp án B Đáp án: B
Câu 13 [706030]: “Khi đốt nóng một đầu dây kim loại, các ..(1).. tự do ở vùng nhiệt độ cao có động năng lớn hơn di chuyển đến vùng có nhiệt độ thấp hơn trong tinh thể kim loại và truyền năng lượng cho các ..(2).. ở đây”. Nội dung phù hợp trong các ô trống (1), (2) lần lượt là
A, proton hoá trị, anion phi kim.
B, electron hoá trị, anion gốc acid.
C, electron hoá trị, cation kim loại.
D, neutron hoá trị, cation ammonium.
- Khi đốt nóng một đầu dây kim loại, các hạt mang điện tích trong kim loại sẽ tham gia vào quá trình truyền nhiệt. Trong kim loại, các electron hóa trị là các hạt có thể di chuyển tự do và đóng vai trò quan trọng trong việc dẫn nhiệt.
- Các electron tự do này sẽ di chuyển từ vùng có nhiệt độ cao đến vùng có nhiệt độ thấp hơn, giúp truyền năng lượng cho các ion kim loại trong mạng tinh thể.
⟹Chọn đáp án C Đáp án: C
- Các electron tự do này sẽ di chuyển từ vùng có nhiệt độ cao đến vùng có nhiệt độ thấp hơn, giúp truyền năng lượng cho các ion kim loại trong mạng tinh thể.
⟹Chọn đáp án C Đáp án: C
Câu 14 [705417]: Nhờ có …(1)… cao, đồng thời bền trước tác động của các tác nhân …(2)… nên chromium được dùng làm lớp bảo vệ chống ăn mòn cho các dụng cụ, máy móc, thiết bị, đồ gia dụng,... Nội dung phù hợp trong ô trống (1), (2) lần lượt là
A, độ cứng, ăn mòn.
B, tính dẻo, oxi hóa.
C, độ bền, hóa học.
D, khả năng chịu nhiệt, vật lý.
Nhờ có độ cứng cao, đồng thời bền trước tác động của các tác nhân ăn mòn nên chromium được dùng làm lớp bảo vệ chống ăn mòn cho các dụng cụ, máy móc, thiết bị, đồ gia dụng,...
Giải thích:
- Chromium là một trong những kim loại cứng nhất nên giúp nó chống lại sự ăn mòn cơ học khi sử dụng trong các thiết bị hoặc đồ gia dụng, nơi thường xuyên chịu va chạm hoặc ma sát.
- Chromium có tính kháng hóa chất rất tốt. Khi tiếp xúc với không khí, một lớp màng mỏng Cr2O3 (chromium oxide) hình thành trên bề mặt. Lớp oxide này bền vững, không bị phá hủy bởi oxygen hay nước, ngăn cản sự tiếp xúc trực tiếp giữa kim loại bên trong và các tác nhân gây ăn mòn như O2, H2O, HCl, SO2,...
⇒ Chọn đáp án A Đáp án: A
Giải thích:
- Chromium là một trong những kim loại cứng nhất nên giúp nó chống lại sự ăn mòn cơ học khi sử dụng trong các thiết bị hoặc đồ gia dụng, nơi thường xuyên chịu va chạm hoặc ma sát.
- Chromium có tính kháng hóa chất rất tốt. Khi tiếp xúc với không khí, một lớp màng mỏng Cr2O3 (chromium oxide) hình thành trên bề mặt. Lớp oxide này bền vững, không bị phá hủy bởi oxygen hay nước, ngăn cản sự tiếp xúc trực tiếp giữa kim loại bên trong và các tác nhân gây ăn mòn như O2, H2O, HCl, SO2,...
⇒ Chọn đáp án A Đáp án: A
Câu 15 [702801]: Trong các phản ứng hóa học, nguyên tử kim loại dễ …(1)… hóa trị để tạo thành …(2)… kim loại. Nội dung phù hợp trong các ô trống (1), (2) lần lượt là
A, nhường electron, cation.
B, nhường electron, anion.
C, nhận electron, cation.
D, nhận electron, anion.
Trong các phản ứng hóa học, nguyên tử kim loại có tính khử nên dễ nhường electron hóa trị để tạo thành cation kim loại.
⇒ Chọn đáp án A Đáp án: A
⇒ Chọn đáp án A Đáp án: A
Câu 16 [705760]: Nguyên tắc tách kim loại ra khỏi hợp chất của chúng là khử ...(1)... trong hợp chất thành ...(2)... Nội dung phù hợp trong ô trống (1), (2) lần lượt là
A, ion kim loại, ion dương.
B, nguyên tử, ion kim loại.
C, ion kim loại, nguyên tử.
D, nguyên tử, nguyên tố.
Nguyên tắc tách kim loại ra khỏi hợp chất của chúng là khử ion kim loại trong hợp chất thành nguyên tử.
Giải thích:
- Trong hợp chất, kim loại thường tồn tại dưới dạng ion dương (Mn+). Để tách kim loại ra, ta cần khử ion Mn+ thành kim loại M bằng cách cung cấp electron. Phương trình tổng quát:
Giải thích:
- Trong hợp chất, kim loại thường tồn tại dưới dạng ion dương (Mn+). Để tách kim loại ra, ta cần khử ion Mn+ thành kim loại M bằng cách cung cấp electron. Phương trình tổng quát:
Mn+ + ne → M
Đáp án: C - Phương pháp thực hiện:
+ Dùng chất khử mạnh (C, CO, Al, H2,...): thường áp dụng cho các kim loại trung bình và yếu.
+ Điện phân (đối với kim loại hoạt động mạnh như Na, K, Al).
⇒ Chọn đáp án C
+ Dùng chất khử mạnh (C, CO, Al, H2,...): thường áp dụng cho các kim loại trung bình và yếu.
+ Điện phân (đối với kim loại hoạt động mạnh như Na, K, Al).
⇒ Chọn đáp án C
Câu 17 [825030]: “Điện phân các hợp chất điện li nóng chảy của kim loại (muối, oxide,...) để ...(1)... những kim loại có độ hoạt động ...(2)... như Li, Na, K, Mg, Al,...”. Nội dung phù hợp trong ô trống (1), (2) lần lượt là
A, trộn, trung bình.
B, tách, mạnh.
C, phá vỡ, yếu.
D, phân biệt, trung bình.
- Các kim loại Li, Na, K, Mg, là các kim loại kiềm, kiềm thổ và Al đều là các kim loại hoạt động hóa học mạnh. Các kim loại hoạt động hóa học mạnh rất khó bị khử . Vì vậy phương pháp điện phân nóng chảy dùng để tách các kim loại này ra khỏi hợp chất của chúng.
⟹ Điện phân các hợp chất điện li nóng chảy của kim loại (muối,oxide...) để tách những kim loại có độ hoạt động mạnh như Li, Na, K, Mg, Al.
⟹ Chọn đáp án B Đáp án: B
⟹ Điện phân các hợp chất điện li nóng chảy của kim loại (muối,oxide...) để tách những kim loại có độ hoạt động mạnh như Li, Na, K, Mg, Al.
⟹ Chọn đáp án B Đáp án: B
Câu 18 [825031]: “Để điều chế nhôm từ quặng bauxite, người ta sử dụng phương pháp ...(1)... bằng cách điện phân ...(2)... nóng chảy”. Nội dung phù hợp trong ô trống (1), (2) lần lượt là
A, thuỷ luyện, aluminium oxide.
B, nhiệt luyện, aluminium oxide.
C, điện phân, aluminium oxide.
D, điện phân, aluminium hydroxide.
Để điều chế nhôm từ quặng bauxite, người ta sử dụng phương pháp điện phân bằng cách điện phân aluminium oxide nóng chảy.
Giải thích:
Điện phân aluminium oxide nóng chảy:
+ Ở cathode (cực âm): Al3+ + 3e ⟶ Al
+ Ở anode (cực dương): 2O2- ⟶ O2 + 4e
Phương trình điện phân: 2Al2O3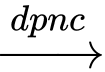 4Al + 3O2.
4Al + 3O2.
⟹ Chọn đáp án C Đáp án: C
Giải thích:
Điện phân aluminium oxide nóng chảy:
+ Ở cathode (cực âm): Al3+ + 3e ⟶ Al
+ Ở anode (cực dương): 2O2- ⟶ O2 + 4e
Phương trình điện phân: 2Al2O3
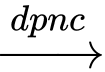 4Al + 3O2.
4Al + 3O2. ⟹ Chọn đáp án C Đáp án: C
Câu 19 [705955]: “ Phương pháp nhiệt luyện thường được dùng để tách các kim loại hoạt động hoá học trung bình ra khỏi các ..(1).. bằng các chất khử như C, CO,... ở ..(2)..”. Nội dung phù hợp trong các ô trống (1), (2) lần lượt là
A, base, môi trường chân không.
B, oxide, nhiệt độ cao.
C, muối, môi trường khí trơ.
D, acid, nhiệt độ thấp.
Phương pháp nhiệt luyện là phương pháp dùng chất khử như C, CO để tách kim loại khỏi hợp chất oxide của chúng ở nhiệt độ cao.
- Ô trống (1) là oxide.
- Ô trống (2) là nhiệt độ cao vì nhiệt luyện diễn ra ở nhiệt độ cao để phản ứng khử xảy ra.
⟹Chọn đáp án B Đáp án: B
- Ô trống (1) là oxide.
- Ô trống (2) là nhiệt độ cao vì nhiệt luyện diễn ra ở nhiệt độ cao để phản ứng khử xảy ra.
⟹Chọn đáp án B Đáp án: B
Câu 20 [705981]: “ Phương pháp thủy luyện thường được dùng để tách những kim loại hoạt động hoá học ..(1).. ra khỏi dung dịch ..(2).. của chúng bằng các kim loại có tính khử mạnh hơn. Nội dung phù hợp trong các ô trống (1), (2) lần lượt là
A, mạnh, muối.
B, yếu, acid.
C, trung bình, base.
D, yếu, muối.
Kim loại có hoạt động hóa học yếu thường được tách ra khỏi dung dịch.
Dung dịch chứa kim loại thường là muối của kim loại đó.
“ Phương pháp thủy luyện thường được dùng để tách những kim loại hoạt động hoá học yếu ra khỏi dung dịch muối của chúng bằng các kim loại có tính khử mạnh hơn.
⟹Chọn đáp án D Đáp án: D
Dung dịch chứa kim loại thường là muối của kim loại đó.
“ Phương pháp thủy luyện thường được dùng để tách những kim loại hoạt động hoá học yếu ra khỏi dung dịch muối của chúng bằng các kim loại có tính khử mạnh hơn.
⟹Chọn đáp án D Đáp án: D
Câu 21 [680852]: "Ăn mòn hóa học là quá trình ...(1)..., trong đó các electron của ...(2)... chuyển trực tiếp đến các chất trong môi trường". Nội dung phù hợp trong các ô trống (1), (2) lần lượt là
A, oxi hóa - khử, kim loại.
B, khử, kim loại.
C, oxi hoá, ion kim loại.
D, oxi hóa - khử, ion kim loại.
Ăn mòn hóa học là quá trình oxi hóa trong đó các electron của ion kim loại chuyển trực tiếp đến các chất trong môi trường.
Giải thích:
- Trong quá trình ăn mòn hóa học, kim loại (M) bị oxi hóa, mất electron để trở thành ion kim loại (Mn+):
M ⟶ Mn+ + ne.
- Trong quá trình này, kim loại sẽ nhường electron (bị oxi hóa) cho các chất oxi hóa trong môi trường.
⟹ Chọn đáp án A Đáp án: A
Giải thích:
- Trong quá trình ăn mòn hóa học, kim loại (M) bị oxi hóa, mất electron để trở thành ion kim loại (Mn+):
M ⟶ Mn+ + ne.
- Trong quá trình này, kim loại sẽ nhường electron (bị oxi hóa) cho các chất oxi hóa trong môi trường.
⟹ Chọn đáp án A Đáp án: A
Câu 22 [702605]: Một vật làm bằng sắt tây (sắt tráng thiếc) có một vết cắt sâu đến lớp sắt. Khi để vật này tiếp xúc với không khí ẩm thì xảy ra ăn mòn …(1)…, trong đó …(2)… bị oxi hóa. Nội dung phù hợp trong các ô trống (1), (2) lần lượt là
A, hóa học, sắt.
B, điện hóa, thiếc.
C, hóa học, thiếc.
D, điện hóa, sắt.
Một vật làm bằng sắt tây (sắt tráng thiếc) có một vết cắt sâu đến lớp sắt. Khi để vật này tiếp xúc với không khí ẩm (tạo ra môi trường điện li, điều kiện để xảy ra ăn mòn điện hoá) sẽ xuất hiện 2 điện cực là sắt và thiếc.
Dựa vào dãy hoạt động hoá học của kim loại, sắt (Fe) đứng trước thiếc (Sn) nên sắt hoạt động hoá học mạnh hơn , dễ nhường electron hơn ⇒ Sắt đóng vai trò là chất khử (hay chất bị oxi hoá)
⇒ Chọn đáp án D. Đáp án: D
Dựa vào dãy hoạt động hoá học của kim loại, sắt (Fe) đứng trước thiếc (Sn) nên sắt hoạt động hoá học mạnh hơn , dễ nhường electron hơn ⇒ Sắt đóng vai trò là chất khử (hay chất bị oxi hoá)
⇒ Chọn đáp án D. Đáp án: D
Câu 23 [705902]: “Trong phương pháp điện hoá, để bảo vệ ...(1)..., người ta nối kim loại cần bảo vệ với một kim loại hoạt động hoá học ...(2)...”. Nội dung phù hợp trong các ô trống (1), (2) lần lượt là
A, phi kim, yếu hơn.
B, hợp chất, mạnh hơn.
C, đơn chất, yếu hơn.
D, kim loại, mạnh hơn.
Phương pháp điện hoá: gắn kim loại có tính khử mạnh hơn vào vật cần bảo vệ, kim loại sẽ bị ăn mòn vật được bảo vệ.
“Trong phương pháp điện hoá, để bảo vệ kim loại, người ta nối kim loại cần bảo vệ với một kim loại hoạt động hoá học mạnh hơn”.
⟹ Chọn đáp án D Đáp án: D
“Trong phương pháp điện hoá, để bảo vệ kim loại, người ta nối kim loại cần bảo vệ với một kim loại hoạt động hoá học mạnh hơn”.
⟹ Chọn đáp án D Đáp án: D
Câu 24 [825032]: “Kim loại kiềm là những kim loại hoạt động hoá học ...(1)..., có tính khử mạnh và tính khử ...(2)... từ Li đến Cs”. Nội dung phù hợp trong ô trống (1), (2) lần lượt là
A, mạnh, giảm dần.
B, mạnh, tăng dần.
C, trung bình, tăng dần.
D, yếu, giảm dần.
Kim loại kiềm là những kim loại hoạt động hóa học mạnh có tính khử mạnh và tính khử tăng dần từ Li đến Cs.
Giải thích:
- Kim loại kiềm (nhóm IA trong bảng tuần hoàn) là những kim loại có độ hoạt động hóa học mạnh. Chúng dễ dàng nhường electron để đạt cấu hình electron bền vững của khí hiếm.
- Trong nhóm kim loại kiềm, khi đi từ trên xuống dưới (từ Li đến Cs), bán kính nguyên tử tăng lên và năng lượng ion hóa giảm xuống. Điều này làm cho các electron hóa trị dễ bị mất đi hơn. Do đó, tính khử của các kim loại kiềm tăng dần từ Li đến Cs. Cs là kim loại kiềm có tính khử mạnh nhất.
⟹ Chọn đáp án B Đáp án: B
Giải thích:
- Kim loại kiềm (nhóm IA trong bảng tuần hoàn) là những kim loại có độ hoạt động hóa học mạnh. Chúng dễ dàng nhường electron để đạt cấu hình electron bền vững của khí hiếm.
- Trong nhóm kim loại kiềm, khi đi từ trên xuống dưới (từ Li đến Cs), bán kính nguyên tử tăng lên và năng lượng ion hóa giảm xuống. Điều này làm cho các electron hóa trị dễ bị mất đi hơn. Do đó, tính khử của các kim loại kiềm tăng dần từ Li đến Cs. Cs là kim loại kiềm có tính khử mạnh nhất.
⟹ Chọn đáp án B Đáp án: B
Câu 25 [825033]: “Kim loại nhóm IA có tính …(1)…, mức độ phản ứng với nước, chlorine và oxygen …(2)… trong dãy lithium, sodium, potassium”. Nội dung phù hợp trong các ô trống (1), (2) lần lượt là
A, oxi hóa mạnh, giảm dần.
B, khử mạnh, tăng dần.
C, lưỡng tính, tăng dần.
D, base mạnh, giảm dần.
Kim loại nhóm IA có tính khử mạnh, mức độ phản ứng với nước, chlorine và oxygen tăng dần trong dãy lithium, sodium, potassium.
Giải thích:
- Kim loại nhóm IA (kim loại kiềm) có cấu hình electron lớp ngoài cùng là ns1, chúng dễ dàng nhường 1 electron để đạt cấu hình bền vững của khí hiếm. Do đó, chúng có tính khử mạnh.
- Trong dãy lithium (Li), sodium (Na), potassium (K), khi đi từ Li đến K, bán kính nguyên tử tăng lên và năng lượng ion hóa giảm xuống. Do đó, mức độ phản ứng của chúng với các chất oxi hóa như nước, chlorine và oxygen cũng tăng dần theo thứ tự Li < Na < K.
⟹ Chọn đáp án B Đáp án: B
Giải thích:
- Kim loại nhóm IA (kim loại kiềm) có cấu hình electron lớp ngoài cùng là ns1, chúng dễ dàng nhường 1 electron để đạt cấu hình bền vững của khí hiếm. Do đó, chúng có tính khử mạnh.
- Trong dãy lithium (Li), sodium (Na), potassium (K), khi đi từ Li đến K, bán kính nguyên tử tăng lên và năng lượng ion hóa giảm xuống. Do đó, mức độ phản ứng của chúng với các chất oxi hóa như nước, chlorine và oxygen cũng tăng dần theo thứ tự Li < Na < K.
⟹ Chọn đáp án B Đáp án: B
Câu 26 [825034]: “Kim loại kiềm có cấu hình electron lớp ngoài cùng là …(1)…, do đó dễ dàng …(2)… để tạo ion dương”. Nội dung phù hợp trong các ô trống (1), (2) lần lượt là
A, ns1, nhường 1 electron.
B, ns2, nhận 2 electron.
C, np1, nhường 1 electron.
D, ns2np2, nhận 2 electron.
Kim loại kiềm (nhóm IA) có cấu hình electron lớp ngoài cùng là ns1, chúng dễ dàng nhường 1 electron để đạt cấu hình bền vững của khí hiếm. Do đó, chúng có tính khử mạnh.
⟹ Kim loại kiềm có cấu hình electron lớp ngoài cùng là ns1 do đó dễ dàng nhường 1 electron để tạo ion dương.
⟹ Chọn đáp án A Đáp án: A
⟹ Kim loại kiềm có cấu hình electron lớp ngoài cùng là ns1 do đó dễ dàng nhường 1 electron để tạo ion dương.
⟹ Chọn đáp án A Đáp án: A
Câu 27 [825037]: “Các kim loại kiềm thổ có độ cứng lớn hơn kim loại kiềm nhưng mềm hơn …(1)…, do có …(2)…”. Nội dung phù hợp trong các ô trống (1), (2) lần lượt là
A, phi kim, khối lượng riêng nhỏ hơn.
B, kim loại chuyển tiếp, liên kết kim loại yếu hơn.
C, khí hiếm, cấu trúc mạng tinh thể khác.
D, hợp kim, nhiệt độ nóng chảy cao.
Các kim loại kiềm thổ có độ cứng lớn hơn kim loại kiềm nhưng mềm hơn kim loại chuyển tiếp, do có liên kết kim loại yếu hơn.
Giải thích:
- Các kim loại kiềm thổ có 2 electron hóa trị nên tạo liên kết kim loại bền vững hơn. Nhiệt độ nóng chảy, nhiệt độ sôi cao hơn các kim loại kiềm. Kim loại kiềm thổ có khối lượng riêng lớn.
- Kim loại chuyển tiếp: Thường có độ cứng cao hơn nhiều so với kim loại kiềm thổ do có nhiều electron tham gia liên kết kim loại (bao gồm cả electron ở lớp d).
Giải thích:
- Các kim loại kiềm thổ có 2 electron hóa trị nên tạo liên kết kim loại bền vững hơn. Nhiệt độ nóng chảy, nhiệt độ sôi cao hơn các kim loại kiềm. Kim loại kiềm thổ có khối lượng riêng lớn.
- Kim loại chuyển tiếp: Thường có độ cứng cao hơn nhiều so với kim loại kiềm thổ do có nhiều electron tham gia liên kết kim loại (bao gồm cả electron ở lớp d).
⟹ Chọn đáp án B
Câu 28 [705456]: Trong tự nhiên, các nguyên tố ...(1)... chỉ tồn tại ở dạng hợp chất do đều là những kim loại hoạt động hóa học ...(2)... nên không tồn tại dạng đơn chất. Nội dung phù hợp trong ô trống (1), (2) lần lượt là
A, nhóm IIA, yếu.
B, nhóm IA, yếu.
C, Nhóm VIIA, mạnh.
D, nhóm IA, mạnh.
Trong tự nhiên, các nguyên tố nhóm IA chỉ tồn tại ở dạng hợp chất do đều là những kim loại hoạt động hóa học mạnh nên không tồn tại dạng đơn chất.
Giải thích:
– Kim loại kiềm (Nhóm IA) gồm Li, Na, K, Rb, Cs, Fr và kim loại kiềm thổ (Nhóm IIA): Gồm Be, Mg, Ca, Sr, Ba, Ra có 1 hoặc 2 electron hóa trị, rất dễ mất electron để tạo ion dương (M+ hay M2+), nên có tính khử rất mạnh.
– Do phản ứng quá mạnh với các chất trong môi trường tự nhiên (oxygen, nước, CO2...), các kim loại này không thể tồn tại lâu dưới dạng đơn chất mà luôn tồn tại dưới dạng hợp chất (oxide, muối, silicate...).
⇒ Chọn đáp án D Đáp án: D
Giải thích:
– Kim loại kiềm (Nhóm IA) gồm Li, Na, K, Rb, Cs, Fr và kim loại kiềm thổ (Nhóm IIA): Gồm Be, Mg, Ca, Sr, Ba, Ra có 1 hoặc 2 electron hóa trị, rất dễ mất electron để tạo ion dương (M+ hay M2+), nên có tính khử rất mạnh.
– Do phản ứng quá mạnh với các chất trong môi trường tự nhiên (oxygen, nước, CO2...), các kim loại này không thể tồn tại lâu dưới dạng đơn chất mà luôn tồn tại dưới dạng hợp chất (oxide, muối, silicate...).
⇒ Chọn đáp án D Đáp án: D
Câu 29 [705492]: “Các kim loại kiềm có thế điện cực chuẩn …(1)…, do đó chúng đều phản ứng với nước ở điều kiện thường với mức độ …(2)… từ Li đến Cs”. Nội dung phù hợp trong ô trống (1), (2) lần lượt là
A, rất âm, giảm dần.
B, rất dương, giảm dần.
C, rất dương, tăng dần.
D, rất âm, tăng dần.
Các kim loại kiềm có thế điện cực chuẩn rất âm, do đó chúng đều phản ứng với nước ở điều kiện thường với mức độ tăng dần từ Li đến Cs.
Giải thích:
- Thế điện cực chuẩn (Eo) của kim loại kiềm so với cặp M+/M đều có giá trị rất âm, chứng tỏ chúng dễ bị oxi hóa để tạo ion dương, tức kim loại kiềm có tính khử rất mạnh, dễ dàng nhường electron để phản ứng với các chất như nước.
- Bán kính nguyên tử của các kim loại kiềm lớn nên lực liên kết giữa hạt nhân và electron hóa trị nhỏ ⟶ khả năng nhường electron dễ dàng hơn. Vì thế, tính khử mạnh, dẫn đến phản ứng với nước diễn ra mạnh.
⇒ Chọn đáp án D Đáp án: D
Giải thích:
- Thế điện cực chuẩn (Eo) của kim loại kiềm so với cặp M+/M đều có giá trị rất âm, chứng tỏ chúng dễ bị oxi hóa để tạo ion dương, tức kim loại kiềm có tính khử rất mạnh, dễ dàng nhường electron để phản ứng với các chất như nước.
- Bán kính nguyên tử của các kim loại kiềm lớn nên lực liên kết giữa hạt nhân và electron hóa trị nhỏ ⟶ khả năng nhường electron dễ dàng hơn. Vì thế, tính khử mạnh, dẫn đến phản ứng với nước diễn ra mạnh.
⇒ Chọn đáp án D Đáp án: D
Câu 30 [705781]: "Phương pháp Solvay dùng để sản xuất soda và baking soda sử dụng nguồn nguyên liệu dễ tìm trong tự nhiên là ..(1)..., đá vôi và ...(2)...”. Nội dung phù hợp trong ô trống (1), (2) lần lượt là
A, muối ăn, ammonia.
B, muối ăn, carbon dioxide.
C, cát, ammonia.
D, cát, carbon dioxide.
"Phương pháp Solvay dùng để sản xuất soda và baking soda sử dụng nguồn nguyên liệu dễ tìm trong tự nhiên là muối ăn, đá vôi và ammonia”
Giải thích:
Phương pháp Solvay là một quy trình công nghiệp quan trọng để sản xuất soda (Na2CO3) và baking soda (NaHCO3). Phương pháp này sử dụng nguyên liệu rẻ, dễ tìm trong tự nhiên gồm:
- Nước muối (NaCl) – nguồn cung cấp ion Na+.
- Đá vôi (CaCO3) – dùng để tạo CO2 và CaO.
- Ammonia (NH3) – giúp kết tủa NaHCO3 từ dung dịch.
⇒ Chọn đáp án A Đáp án: A
Giải thích:
Phương pháp Solvay là một quy trình công nghiệp quan trọng để sản xuất soda (Na2CO3) và baking soda (NaHCO3). Phương pháp này sử dụng nguyên liệu rẻ, dễ tìm trong tự nhiên gồm:
- Nước muối (NaCl) – nguồn cung cấp ion Na+.
- Đá vôi (CaCO3) – dùng để tạo CO2 và CaO.
- Ammonia (NH3) – giúp kết tủa NaHCO3 từ dung dịch.
⇒ Chọn đáp án A Đáp án: A
Câu 31 [825038]: “Nước cứng là loại nước chứa nhiều ion ...(1)... với hàm lượng ...(2)... mức cho phép”. Nội dung phù hợp trong ô trống (1), (2) lần lượt là
A, SO42- và Cl-, vượt mức cho phép.
B, Ca2+ và Mg2+, vượt mức cho phép.
C, HCO3- và SO42-, đạt mức cho phép.
D, Ca2+ và Mg2+, đạt mức cho phép.
Nước cứng là loại nước chứa nhiều ion Ca2+ và Mg2 với hàm lượng vượt mức cho phép.
Giải thích:
- Nước chứa nhiều ion Ca2+ và Mg2+ sẽ gây nên tính cứng cho nước. Hàm lượng các ion này vượt mức cho phép sẽ gây ra các tác động không mong muốn trong quá trình sinh hoạt và đời sống hằng ngày như không tạo bọt với xà phòng, đóng cặn ở bình đun nước rất có hại.
⟹ Chọn đáp án B Đáp án: B
Giải thích:
- Nước chứa nhiều ion Ca2+ và Mg2+ sẽ gây nên tính cứng cho nước. Hàm lượng các ion này vượt mức cho phép sẽ gây ra các tác động không mong muốn trong quá trình sinh hoạt và đời sống hằng ngày như không tạo bọt với xà phòng, đóng cặn ở bình đun nước rất có hại.
⟹ Chọn đáp án B Đáp án: B
Câu 32 [825039]: “Kim loại chuyển tiếp thuộc các nhóm …(1)… trong bảng tuần hoàn, có đặc điểm chung là …(2)….”. Nội dung phù hợp trong các ô trống (1), (2) lần lượt là
A, IA - IIA, có bán kính nguyên tử lớn.
B, IIIA - VIIA, có độ âm điện cao.
C, IIIB - IIB, có nhiều trạng thái oxi hóa.
D, IIIB - VIIIB, chỉ có một số oxi hóa.
Kim loại chuyển tiếp thuộc các nhóm IIIB - IIB trong bảng tuần hoàn, có đặc điểm chung là có nhiều trạng thái oxi hóa.
Giải thích:
- Kim loại chuyển tiếp là các kim loại thuộc phân lớp d chưa bão hòa thuộc các kim loại khối d thuộc nhóm B.
- Các kim loại chuyển tiếp thuộc phần lớp d nên chúng có nhiều trạng thái oxi hóa.
Ví dụ : Fe có số oxi hóa là Fe2+, Fe3+.
⟹ Chọn đáp án C Đáp án: C
Giải thích:
- Kim loại chuyển tiếp là các kim loại thuộc phân lớp d chưa bão hòa thuộc các kim loại khối d thuộc nhóm B.
- Các kim loại chuyển tiếp thuộc phần lớp d nên chúng có nhiều trạng thái oxi hóa.
Ví dụ : Fe có số oxi hóa là Fe2+, Fe3+.
⟹ Chọn đáp án C Đáp án: C
Câu 33 [704386]: Theo IUPAC, nguyên tố chuyển tiếp là những nguyên tố có …(1)… chưa được xếp (hoặc điền) đầy …(2)… ở trạng thái nguyên tử hoặc ở trạng thái ion. Nội dung phù hợp trong ô trống (1), (2) lần lượt là
A, lớp, điện tích hạt nhân.
B, phân lớp, electron.
C, phân lớp, điện tích hạt nhân.
D, lớp, electron.
Theo IUPAC, nguyên tố chuyển tiếp là những nguyên tố có phân lớp chưa được xếp (hoặc điền) đầy electron.
Giải thích:
- Theo IUPAC, một nguyên tố được gọi là nguyên tố chuyển tiếp nếu trong trạng thái nguyên tử hoặc trạng thái ion, nguyên tố đó có phân lớp d chưa được điền đầy hoàn toàn (chưa chứa đủ 10 electron). Điều này có nghĩa là số electron trong phân lớp d phải nằm trong khoảng từ 1 đến 9.
- Ví dụ:
Nguyên tố Fe (Z = 26): Cấu hình electron: Ar]3d6 4s2.
Phân lớp 3d có 6 electron → chưa đầy → Fe là nguyên tố chuyển tiếp.
⇒ Chọn đáp án B Đáp án: B
Giải thích:
- Theo IUPAC, một nguyên tố được gọi là nguyên tố chuyển tiếp nếu trong trạng thái nguyên tử hoặc trạng thái ion, nguyên tố đó có phân lớp d chưa được điền đầy hoàn toàn (chưa chứa đủ 10 electron). Điều này có nghĩa là số electron trong phân lớp d phải nằm trong khoảng từ 1 đến 9.
- Ví dụ:
Nguyên tố Fe (Z = 26): Cấu hình electron: Ar]3d6 4s2.
Phân lớp 3d có 6 electron → chưa đầy → Fe là nguyên tố chuyển tiếp.
⇒ Chọn đáp án B Đáp án: B
Câu 34 [825041]: “Chromium là kim loại có độ cứng rất cao do có cấu trúc mạng tinh thể …(1)… và thường được dùng để …(2)….”. Nội dung phù hợp trong các ô trống (1), (2) lần lượt là
A, lập phương tâm diện, sản xuất kính.
B, lập phương tâm diện, chế tạo thuốc súng.
C, lập phương tâm khối, sản xuất phân bón.
D, lập phương tâm khối, mạ kim loại.
- Chromium là kim loại có độ cứng lớn nhất . Vì là kim loại có độ cứng rất cao nên có cấu trúc mạng tinh thể lập phương tâm khối. Mạng tinh thể lập phương tâm khối thường tạo các kim loại có độ cứng lớn và nhiệt độ nóng chảy cao.
- Chromium có độ cứng cao, khả năng chống ăn mòn tốt, có độ sáng bóng nên thường được sử dụng để mạ kim loại đặc biệt là mạ trang trí hoặc bảo vệ bề mặt . Ngoài ra còn được sử dụng để sản xuất thép không gỉ và hợp kim.
⟹ Chromium là kim loại có độ cứng rất cao do có cấu trúc mạng tinh thể lập phương tâm khối và thường được dùng để mạ kim loại.
⟹ Chọn đáp án D Đáp án: D
- Chromium có độ cứng cao, khả năng chống ăn mòn tốt, có độ sáng bóng nên thường được sử dụng để mạ kim loại đặc biệt là mạ trang trí hoặc bảo vệ bề mặt . Ngoài ra còn được sử dụng để sản xuất thép không gỉ và hợp kim.
⟹ Chromium là kim loại có độ cứng rất cao do có cấu trúc mạng tinh thể lập phương tâm khối và thường được dùng để mạ kim loại.
⟹ Chọn đáp án D Đáp án: D
Câu 35 [703962]: “...(1)... là vật liệu kim loại chứa một kim loại cơ bản và một số kim loại khác hoặc …(2)…”. Nội dung phù hợp trong ô trống (1), (2) lần lượt là
A, vật liệu tổng hợp, polymer.
B, hợp kim, khí hiếm.
C, hợp kim, phi kim.
D, chất dẻo, khí hiếm.
Để tăng độ cứng, chống ăn mòn hoặc tăng cường khả năng chịu nhiệt hoặc điện của vật liệu, người ta thường trộn một kim loại cơ bản (như sắt, đồng, hoặc nhôm) với một hoặc nhiều nguyên tố khác. Các nguyên tố bổ sung có thể là kim loại (như chromium, nickel) hoặc phi kim (như carbon, silicon)... được gọi là họp kim.
⇒ Hợp kim là vật liệu kim loại chứa một kim loại cơ bản và một số kim loại khác hoặc phi kim.
⇒ Chọn đáp án C Đáp án: C
⇒ Hợp kim là vật liệu kim loại chứa một kim loại cơ bản và một số kim loại khác hoặc phi kim.
⇒ Chọn đáp án C Đáp án: C
Câu 36 [825042]: “Gang là hợp kim chứa khoảng 95% ...(1)..., 2% đến 5% ...(2)... và một số nguyên tố khác như manganese, silicon, phosphorus, sulfur,...”. Nội dung phù hợp trong ô trống (1), (2) lần lượt là
A, sắt, đồng.
B, nhôm, chromium.
C, đồng, nhôm.
D, sắt, carbon.
Gang là hợp kim chứa khoảng 95% sắt 2% đến 5% carbon và một số nguyên tố khác như manganese, silicon, phosphorus, sulfur,....
Giải thích:
- Gang là hợp kim chứa khoảng 95% sắt 2% đến 5% carbon và một số nguyên tố khác. Carbon là yếu tố giúp phân biệt gang và thép. Thép cũng là hợp kim chứa sắt và thép tuy nhiên thép chỉ chứa dưới 2% carbon.
⟹ Chọn đáp án D Đáp án: D
Giải thích:
- Gang là hợp kim chứa khoảng 95% sắt 2% đến 5% carbon và một số nguyên tố khác. Carbon là yếu tố giúp phân biệt gang và thép. Thép cũng là hợp kim chứa sắt và thép tuy nhiên thép chỉ chứa dưới 2% carbon.
⟹ Chọn đáp án D Đáp án: D
Câu 37 [825045]: “Thép là hợp kim của ...(1)... chứa ít hơn 2,0% carbon và một số nguyên tố như chromium, manganese, silicon,... tạo cho thép tính ...(2)..., tính chịu nhiệt và các tính chất quý khác”. Nội dung phù hợp trong ô trống (1), (2) lần lượt là
A, nhôm, nhẹ.
B, đồng, dẫn điện.
C, sắt, cứng.
D, chromium, cứng.
“Thép là hợp kim của sắt chứa ít hơn 2,0% carbon và một số nguyên tố như chromium, manganese, silicon,... tạo cho thép tính cứng, tính chịu nhiệt và các tính chất quý khác”.
Giải thích :
- Tương tự như gang, thép cũng là hợp kim của sắt và carbon tuy nhiên chỉ chứa dưới 2% carbon. Các nguyên tố khác được thêm vào giúp cải thiện tính chất làm cho thép có tính cứng hơn, chịu nhiệt tốt và các tính chất quý khác.
⟹ Chọn đáp án C
Đáp án: C
Giải thích :
- Tương tự như gang, thép cũng là hợp kim của sắt và carbon tuy nhiên chỉ chứa dưới 2% carbon. Các nguyên tố khác được thêm vào giúp cải thiện tính chất làm cho thép có tính cứng hơn, chịu nhiệt tốt và các tính chất quý khác.
⟹ Chọn đáp án C
Đáp án: C
Câu 38 [704002]: “Phức chất là hợp chất có chứa ...(1)... và các ...(2)..., nó có thể mang điện tích hoặc không mang điện tích”. Nội dung phù hợp trong ô trống (1), (2) lần lượt là
A, ion kim loại, phân tử nước.
B, kim loại kiềm, ion âm.
C, nguyên tử trung tâm, phân tử liên kết.
D, nguyên tử trung tâm, phối tử.
Phức chất là hợp chất có chứa nguyên tử trung tâm (có thể là kim loại hoặc cation kim loại) và các phối tử liên kết với nguyên tử trung tâm bằng liên kết phối trí, nó có thể mang điện tích hoặc không mang điện tích.
⇒ Chọn đáp án D Đáp án: D
⇒ Chọn đáp án D Đáp án: D
Câu 39 [825046]: “Liên kết giữa nguyên tử trung tâm và phối tử là liên kết ...(1)... được hình thành nhờ sự cho ...(2)... của phối tử vào orbital trống của nguyên tử trung tâm”. Nội dung phù hợp trong ô trống (1), (2) lần lượt là
A, cộng hoá trị, ion âm.
B, ion, cặp electron chưa liên kết.
C, cho – nhận, cặp electron chưa liên kết.
D, kim loại, ion dương.
- Một phân tử phức chất sẽ bao gồm hai phần là : nguyên tử trung tâm và phối tử. Nguyên tử trung tâm sẽ có các obital trống để nhận electron chưa tham gia liên kết từ phối tử. Phối tử sẽ có các cặp electron chưa tham gia liên kết để cho nguyên tử trung tâm.
⟹ Liên kết giữa nguyên tử trung tâm và phối tử là liên kết cho - nhận được hình thành nhờ sự cho cặp electron chưa liên kết của phối tử vào orbital trống của nguyên tử trung tâm.
⟹ Chọn đáp án C
Đáp án: C
⟹ Liên kết giữa nguyên tử trung tâm và phối tử là liên kết cho - nhận được hình thành nhờ sự cho cặp electron chưa liên kết của phối tử vào orbital trống của nguyên tử trung tâm.
⟹ Chọn đáp án C
Đáp án: C
Câu 40 [705359]: Khi tan trong nước, muối của các kim loại chuyển tiếp …(1)… thành các ion. Sau đó, cation kim loại chuyển tiếp (Mn+) thường nhận các cặp electron hoá trị riêng từ các phân tử H2O để hình thành các liên kêt cho - nhận, tạo ra phức chất aqua có dạng tổng quát là ...(2)... Nội dung phù hợp trong ô trống (1), (2) lần lượt là
A, điện li, [M(OH2)m]n+.
B, điện li, [M(OH2)n]+.
C, phân li, [M(OH2)n]+.
D, phân li, [M(OH2)m]n+.
Khi tan trong nước, muối của các kim loại chuyển tiếp phân li thành các ion. Sau đó, cation kim loại chuyển tiếp (Mn+) thường nhận các cặp electron hoá trị riêng từ các phân tử H2O để hình thành các liên kêt cho - nhận, tạo ra phức chất aqua có dạng tổng quát là [M(OH2)m]n+.
- Khi tan trong nước, muối của các kim loại chuyển tiếp phân li thành các ion. Sau đó, cation kim loại chuyển tiếp (Mn+) thường nhận các cặp electron hóa trị riêng từ các phân tử H2O để hình thành các liên kết cho – nhận, tạo ra phức chất aqua theo phương trình hóa học tổng quát sau:
Mn+(aq) + mH2O(l) →[M(OH2)m]n+(aq)
- Trong đó:
+ n là giá trị điện tích của cation kim loại M
+ m là số phối tử H2O
+ [M(OH2)m]n+ là công thức tổng quát của phức chất aqua của Mn+.
⇒ Chọn đáp án D Đáp án: D
- Khi tan trong nước, muối của các kim loại chuyển tiếp phân li thành các ion. Sau đó, cation kim loại chuyển tiếp (Mn+) thường nhận các cặp electron hóa trị riêng từ các phân tử H2O để hình thành các liên kết cho – nhận, tạo ra phức chất aqua theo phương trình hóa học tổng quát sau:
Mn+(aq) + mH2O(l) →[M(OH2)m]n+(aq)
- Trong đó:
+ n là giá trị điện tích của cation kim loại M
+ m là số phối tử H2O
+ [M(OH2)m]n+ là công thức tổng quát của phức chất aqua của Mn+.
⇒ Chọn đáp án D Đáp án: D