Đáp án [BTTL] Bài học 02. Dạng điền từ - Tổng ôn các chủ đề lý thuyết lớp 10
Câu 1 [823581]: “Nguyên tử gồm …(1)… được tạo nên bởi các hạt electron và …(2)… được tạo nên bởi các hạt proton và neutron”. Nội dung phù hợp trong ô trống (1), (2) lần lượt là
A, bán kính, trung tâm.
B, lớp vỏ, hạt nhân.
C, đám mây, hạt nhân.
D, AO, lớp nhân.
“Nguyên tử gồm lớp vỏ được tạo nên bởi các hạt electron và hạt nhân được tạo nên bởi các hạt proton và neutron”.
Chọn đáp án B Đáp án: B
Chọn đáp án B Đáp án: B
Câu 2 [823584]: “Do khối lượng của các electron …(1)… so với khối lượng của proton hay neutron nên khối lượng nguyên tử tập trung chủ yếu ở …(2)…”. Nội dung phù hợp trong các ô trống (1), (2) lần lượt là
A, rất lớn, lớp vỏ.
B, rất nhỏ, hạt nhân.
C, không đáng kể, lớp vỏ.
D, lớn hơn nhiều, hạt nhân.
“Do khối lượng của các electron rất nhỏ so với khối lượng của proton hay neutron nên khối lượng nguyên tử tập trung chủ yếu ở hạt nhân”.
Chọn đáp án B Đáp án: B
Chọn đáp án B Đáp án: B
Câu 3 [823586]: “Nguyên tử trung hòa về điện vì có tổng số hạt …(1)… bằng tổng số hạt …(2)…”. Nội dung phù hợp trong các ô trống (1), (2) lần lượt là
A, electron, neutron.
B, proton, neutron.
C, electron, proton.
D, trong hạt nhân, electron.
“Nguyên tử trung hòa về điện vì có tổng số hạt electron bằng tổng số hạt proton”.
Chọn đáp án C Đáp án: C
Chọn đáp án C Đáp án: C
Câu 4 [823587]: “Nguyên tố hóa học là tập hợp các …(1)… có cùng số hạt …(2)…”. Nội dung phù hợp trong các ô trống (1), (2) lần lượt là
A, nguyên tử, proton.
B, phân tử, neutron.
C, phân tử, proton.
D, nguyên tử, electron.
“Nguyên tố hóa học là tập hợp các nguyên tử có cùng số hạt proton”.
Chọn đáp án A Đáp án: A
Chọn đáp án A Đáp án: A
Câu 5 [823589]: “Số proton trong một hạt nhân nguyên tử được gọi là …(1)…, kí hiệu là …(2)…”. Nội dung phù hợp trong các ô trống (1), (2) lần lượt là
A, khối lượng nguyên tử, Z.
B, số hiệu nguyên tử, Z.
C, số khối, A.
D, điện tích hạt nhân, A.
“Số proton trong một hạt nhân nguyên tử được gọi là số hiệu nguyên tử, kí hiệu là Z ”.
Chọn đáp án B Đáp án: B
Chọn đáp án B Đáp án: B
Câu 6 [823590]: “Số proton (Z) và neutron (N) trong một hạt nhân nguyên tử được gọi là …(1)…, kí hiệu là …(2)…”. Nội dung phù hợp trong các ô trống (1), (2) lần lượt là
A, khối lượng nguyên tử, Z.
B, số hiệu nguyên tử, Z.
C, số khối, A.
D, điện tích hạt nhân, A.
“Số proton (Z) và neutron (N) trong một hạt nhân nguyên tử được gọi là số khối, kí hiệu là A ”.
Chọn đáp án C Đáp án: C
Chọn đáp án C Đáp án: C
Câu 7 [823591]: “Kí hiệu nguyên tử 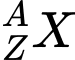 cho biết kí hiệu hóa học của nguyên tố (X), …(1)… (Z) và …(2)… (A)”. Nội dung phù hợp trong các ô trống (1), (2) lần lượt là
cho biết kí hiệu hóa học của nguyên tố (X), …(1)… (Z) và …(2)… (A)”. Nội dung phù hợp trong các ô trống (1), (2) lần lượt là
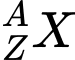 cho biết kí hiệu hóa học của nguyên tố (X), …(1)… (Z) và …(2)… (A)”. Nội dung phù hợp trong các ô trống (1), (2) lần lượt là
cho biết kí hiệu hóa học của nguyên tố (X), …(1)… (Z) và …(2)… (A)”. Nội dung phù hợp trong các ô trống (1), (2) lần lượt là A, số khối, số hiệu nguyên tử.
B, số hiệu nguyên tử, điện tích hạt nhân.
C, số khối, điện tích hạt nhân.
D, số hiệu nguyên tử, số khối.
“Kí hiệu nguyên tử 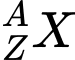 cho biết kí hiệu hóa học của nguyên tố (X), số hiệu nguyên tử (Z) và số khối (A)”.
cho biết kí hiệu hóa học của nguyên tố (X), số hiệu nguyên tử (Z) và số khối (A)”.
Chọn đáp án D Đáp án: D
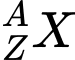 cho biết kí hiệu hóa học của nguyên tố (X), số hiệu nguyên tử (Z) và số khối (A)”.
cho biết kí hiệu hóa học của nguyên tố (X), số hiệu nguyên tử (Z) và số khối (A)”.Chọn đáp án D Đáp án: D
Câu 8 [823593]: “Các đồng vị của một nguyên tố hóa học là những nguyên tử có cùng …(1)… nhưng khác nhau về …(2)…”. Nội dung phù hợp trong các ô trống (1), (2) lần lượt là
A, số proton, số neutron.
B, số neutron, số electron.
C, số khối, số proton.
D, số proton, số electron.
“Các đồng vị của một nguyên tố hóa học là những nguyên tử có cùng số proton nhưng khác nhau về số neutron”.
Chọn đáp án A Đáp án: A
Chọn đáp án A Đáp án: A
Câu 9 [823595]: “Phổ khối lượng chủ yếu được sử dụng để xác định …(1)… của các chất và hàm lượng …(2)… của một nguyên tố”. Nội dung phù hợp trong các ô trống (1), (2) lần lượt là
A, nguyên tử khối, phân tử khối; số proton.
B, cấu trúc phân tử; số electron.
C, công thức cấu tạo; đồng vị bền.
D, nguyên tử khối, phân tử khối; đồng vị bền.
“Phổ khối lượng chủ yếu được sử dụng để xác định nguyên tử khối, phân tử khối của các chất và hàm lượng đồng vị bền của một nguyên tố”.
Chọn đáp án D Đáp án: D
Chọn đáp án D Đáp án: D
Câu 10 [823600]: “Orbital nguyên tử (kí hiệu AO) là khu vực không gian xung quanh …(1)… mà xác suất tìm thấy …(2)… trong khu vực đó là lớn nhất (khoảng 90%)”. Nội dung phù hợp trong các ô trống (1), (2) lần lượt là
A, lớp vỏ nguyên tử, electron.
B, hạt nhân nguyên tử, electron.
C, hạt nhân nguyên tử, proton.
D, lớp vỏ nguyên tử, proton.
“Orbital nguyên tử (kí hiệu AO) là khu vực không gian xung quanh hạt nhân nguyên tử mà xác suất tìm thấy electron trong khu vực đó là lớn nhất (khoảng 90%)”.
Chọn đáp án B Đáp án: B
Chọn đáp án B Đáp án: B
Câu 11 [823601]: “Các AO (orbital nguyên tử) có hình dạng khác nhau: AO s có dạng …(1)…, AO p có dạng …(2)…, AO d và AO f có hình dạng phức tạp”. Nội dung phù hợp trong các ô trống (1), (2) lần lượt là
A, hình elip, hình tròn.
B, hình số tám nổi, hình tròn.
C, hình cầu, hình số tám nổi.
D, hình cầu, hình elip.
“Các AO (orbital nguyên tử) có hình dạng khác nhau: AO s có dạng hình cầu, AO p có dạng hình số tám nổi, AO d và AO f có hình dạng phức tạp”.
Chọn đáp án C Đáp án: C
Chọn đáp án C Đáp án: C
Câu 12 [823602]: “Để biểu diễn orbital nguyên tử, người ta sử dụng các ô vuông, gọi là …(1)… (ứng với một AO). Mỗi AO chứa tối đa …(2)… electron”. Nội dung phù hợp trong các ô trống (1), (2) lần lượt là
A, ô nguyên tử, hai.
B, ô orbital, một.
C, ô năng lượng, ba.
D, ô lượng tử, hai.
“Để biểu diễn orbital nguyên tử, người ta sử dụng các ô vuông, gọi là ô lượng tử (ứng với một AO). Mỗi AO chứa tối đa hai electron”.
Chọn đáp án D Đáp án: D
Chọn đáp án D Đáp án: D
Câu 13 [823605]: “Sự khác biệt cơ bản giữa mô hình Rutherford – Borh và mô hình hiện đại về nguyên tử là: Electron chuyển động …(1)… (mô hình Rutherford – Borh) và electron chuyển động …(2)… (mô hình hiện đại)”. Nội dung phù hợp trong các ô trống (1), (2) lần lượt là
A, trong đám mây electron, trên quỹ đạo xác định.
B, theo quỹ đạo giống như các hành tinh xoay quanh Mặt Trời, không theo quỹ đạo xác định.
C, theo đường xoắn ốc, theo quỹ đạo giống như các hành tinh xoay quanh Mặt Trời.
D, tự do trong không gian, không theo quỹ đạo xác định trong vùng quanh lớp vỏ nguyên tử.
“Sự khác biệt cơ bản giữa mô hình Rutherford – Borh và mô hình hiện đại về nguyên tử là: Electron chuyển động theo quỹ đạo giống như các hành tinh xoay quanh Mặt Trời (mô hình Rutherford – Borh) và electron chuyển động không theo quỹ đạo xác định (mô hình hiện đại)”.
Chọn đáp án B Đáp án: B
Chọn đáp án B Đáp án: B
Câu 14 [823609]: “Chu kì là tập hợp các nguyên tố hoá học mà nguyên tử của chúng có cùng …(1)…, được xếp thành …(2)… theo chiều tăng dần điện tích hạt nhân”. Nội dung phù hợp trong các ô trống (1), (2) lần lượt là
A, số electron lớp ngoài cùng, cột.
B, số lớp electron, cột.
C, số lớp electron, hàng.
D, số electron hoá trị, hàng.
“Chu kì là tập hợp các nguyên tố hoá học mà nguyên tử của chúng có cùng số lớp electron, được xếp thành hàng theo chiều tăng dần điện tích hạt nhân”.
Chọn đáp án C Đáp án: C
Chọn đáp án C Đáp án: C
Câu 15 [823610]: “Trong một chu kì, theo chiều …(1)… điện tích hạt nhân, độ âm điện của các nguyên tố có xu hướng tăng dần, tính base của các hydroxide của các nguyên tố có xu hướng …(2)… dần”. Nội dung phù hợp trong các ô trống (1), (2) lần lượt là
A, tăng, giảm.
B, tăng, tăng.
C, giảm, tăng.
D, giảm, giảm.
“Trong một chu kì, theo chiều tăng điện tích hạt nhân, độ âm điện của các nguyên tố có xu hướng tăng dần, tính base của các hydroxide của các nguyên tố có xu hướng giảm dần”.
Chọn đáp án A Đáp án: A
Chọn đáp án A Đáp án: A
Câu 16 [823612]: “Nhóm ...(1)... là nhóm chứa các nguyên tố đứng đầu mỗi chu kì trong bảng tuần hoàn. Trong nhóm này, nguyên tử nguyên tố Francium (Fr) có bán kính lớn nhất. Số lượng các nguyên tố là kim loại của nhóm này là ...(2)...”. Nội dung phù hợp trong các ô trống (1), (2) lần lượt là
A, kim loại kiềm thổ, 7.
B, kim loại kiềm, 6.
C, kim loại chuyển tiếp, 8.
D, kim loại kiềm thổ, 5.
“Nhóm kim loại kiềm là nhóm chứa các nguyên tố đứng đầu mỗi chu kì trong bảng tuần hoàn. Trong nhóm này, nguyên tử nguyên tố Francium (Fr) có bán kính lớn nhất. Số lượng các nguyên tố là kim loại của nhóm này là 6 ”.
Chọn đáp án B Đáp án: B
Chọn đáp án B Đáp án: B
Câu 17 [702828]: Tinh thể kim loại chứa các …(1)… sắp xếp theo trật tự nhất định cùng với các …(2)… chuyển động tự do. Nội dung phù hợp trong các ô trống (1), (2) lần lượt là
A, hạt kim loại, hạt nhân nguyên tử.
B, hạt nhân nguyên tử, hạt kim loại.
C, electron tự do, cation kim loại.
D, cation kim loại, electron tự do.
- Trong kim loại, khi các nguyên tử mất đi electron ở lớp vỏ ngoài cùng sẽ trở thành các ion dương (cation). Những ion này chiếm các vị trí cố định trong mạng tinh thể kim loại, tạo nên cấu trúc trật tự.
- Các electron bị mất không bị giữ cố định bởi bất kỳ ion dương nào mà chuyển động tự do trong tinh thể kim loại.
⇒ Tinh thể kim loại chứa các cation kim loại sắp xếp theo trật tự nhất định cùng với các electron tự do chuyển động tự do.
Chọn đáp án D Đáp án: D
- Các electron bị mất không bị giữ cố định bởi bất kỳ ion dương nào mà chuyển động tự do trong tinh thể kim loại.
⇒ Tinh thể kim loại chứa các cation kim loại sắp xếp theo trật tự nhất định cùng với các electron tự do chuyển động tự do.
Chọn đáp án D Đáp án: D
Câu 18 [823613]: “Liên kết ion là liên kết được hình thành bởi …(1)… giữa các ion …(2)…”. Nội dung phù hợp trong các ô trống (1), (2) lần lượt là
A, lực hấp dẫn, mang điện tích trái dấu.
B, lực hút tĩnh điện, mang điện tích dương.
C, lực đẩy tĩnh điện, mang điện tích âm.
D, lực hút tĩnh điện, mang điện tích trái dấu.
“Liên kết ion là liên kết được hình thành bởi lực hút tĩnh điện giữa các ion mang điện tích trái dấu”.
Chọn đáp án D Đáp án: D
Chọn đáp án D Đáp án: D
Câu 19 [823614]: “Liên kết cộng hoá trị …(1)… là liên kết cộng hoá trị trong đó cặp electron chung lệch về phía nguyên tử có độ âm điện …(2)…”. Nội dung phù hợp trong các ô trống (1), (2) lần lượt là
A, phân cực, lớn hơn.
B, không phân cực, nhỏ hơn.
C, không phân cực, lớn hơn.
D, phân cực, nhỏ hơn.
“Liên kết cộng hoá trị phân cực là liên kết cộng hoá trị trong đó cặp electron chung lệch về phía nguyên tử có độ âm điện lớn hơn ”.
Chọn đáp án A Đáp án: A
Chọn đáp án A Đáp án: A
Câu 20 [703815]: “Trong tinh thể kim loại, liên kết kim loại được hình thành do ...(1)... giữa các electron hoá trị tự do với các ...(2)... kim loại ở các nút mạng”. Nội dung phù hợp trong ô trống (1), (2) lần lượt là
A, lực hút tĩnh điện, ion dương.
B, lực hút tĩnh điện, ion âm.
C, lực hạt nhân, ion dương.
D, lực đẩy tĩnh điện, ion âm.
Trong tinh thể kim loại, các nguyên tử kim loại giải phóng electron hóa trị (electron ở lớp ngoài cùng) để trở thành ion dương. Lực hút tĩnh điện giữa các electron tự do và ion dương kim loại là yếu tố chính giữ các ion dương ở vị trí cố định trong mạng tinh thể. Do đó, lực hút tĩnh điện là đặc trưng cơ bản của liên kết kim loại.
⇒ Trong tinh thể kim loại, liên kết kim loại được hình thành do lực hút tĩnh điện giữa các electron hoá trị tự do với các ion dương kim loại ở các nút mạng.
Chọn đáp án A Đáp án: A
⇒ Trong tinh thể kim loại, liên kết kim loại được hình thành do lực hút tĩnh điện giữa các electron hoá trị tự do với các ion dương kim loại ở các nút mạng.
Chọn đáp án A Đáp án: A
Câu 21 [823617]: “Mỗi hàng trong bảng tuần hoàn được gọi là một ...(2)... Mỗi cột trong bảng tuần hoàn được gọi là một ...(3)...”. Nội dung phù hợp trong các ô trống (1), (2) lần lượt là
A, chu kì, ô.
B, chu kì, nhóm.
C, họ, nhóm.
D, chu kì, nhóm chính.
“Mỗi hàng trong bảng tuần hoàn được gọi là một chu kì. Mỗi cột trong bảng tuần hoàn được gọi là một nhóm ”.
Chọn đáp án B Đáp án: B
Chọn đáp án B Đáp án: B
Câu 22 [823619]: “Trong bảng tuần hoàn các nguyên tố hoá học do Mendeleev đề xuất, các nguyên tố được sắp xếp theo chiều tăng dần của ...(1).... Trong bảng tuần hoàn các nguyên tố hoá học hiện đại, các nguyên tố được sắp xếp theo chiều tăng dần của ...(2)....”. Nội dung phù hợp trong các ô trống (1), (2) lần lượt là
A, số electron hoá trị, khối lượng nguyên tử.
B, số hiệu nguyên tử, khối lượng nguyên tử.
C, khối lượng nguyên tử, số hiệu nguyên tử.
D, số electron hóa trị, số hiệu nguyên tử.
“Trong bảng tuần hoàn các nguyên tố hoá học do Mendeleev đề xuất, các nguyên tố được sắp xếp theo chiều tăng dần của khối lượng nguyên tử. Trong bảng tuần hoàn các nguyên tố hoá học hiện đại, các nguyên tố được sắp xếp theo chiều tăng dần của số hiệu nguyên tử ”.
Chọn đáp án C Đáp án: C
Chọn đáp án C Đáp án: C
Câu 23 [823620]: “Phản ứng giải phóng năng lượng dưới dạng nhiệt gọi là phản ứng …(1)… Phản ứng hấp thụ năng lượng dưới dạng nhiệt gọi là phản ứng …(2)…”. Nội dung phù hợp trong các ô trống (1), (2) lần lượt là
A, toả nhiệt, thu nhiệt.
B, oxi hoá, khử.
C, phân huỷ, hoá hợp.
D, thu nhiệt, oxi hoá.
Phản ứng giải phóng năng lượng dưới dạng nhiệt gọi là phản ứng tỏa nhiệt. Phản ứng hấp thụ năng lượng dưới dạng nhiệt gọi là phản ứng thu nhiệt.
Các đáp án khác :
- Phản ứng oxi hóa - khử là phản ứng hoá học trong đó có sự thay đổi số oxi hoá của một số nguyên tố hay là phản ứng trong đó có sự chuyến electron giữa các chất phản ứng.
Phản ứng phân huỷ là phản ứng hóa học trong đó một chất sinh ra hai hay nhiều chất mới.
Phản ứng hóa hợp là phản ứng hóa học trong đó chỉ có một chất mới (sản phẩm) được tạo thành từ hai hay nhiều chất ban đầu.
Chọn đáp án A Đáp án: A
Các đáp án khác :
- Phản ứng oxi hóa - khử là phản ứng hoá học trong đó có sự thay đổi số oxi hoá của một số nguyên tố hay là phản ứng trong đó có sự chuyến electron giữa các chất phản ứng.
Phản ứng phân huỷ là phản ứng hóa học trong đó một chất sinh ra hai hay nhiều chất mới.
Phản ứng hóa hợp là phản ứng hóa học trong đó chỉ có một chất mới (sản phẩm) được tạo thành từ hai hay nhiều chất ban đầu.
Chọn đáp án A Đáp án: A
Câu 24 [823624]: “Phản ứng toả nhiệt: biến thiên enthalpy của phản ứng có giá trị âm. Biến thiên enthalpy …(1)…, phản ứng toả ra …(2)…”. Nội dung phù hợp trong các ô trống (1), (2) lần lượt là
A, càng dương, càng nhiều nhiệt.
B, càng âm, càng ít nhiệt.
C, càng dương, càng mãnh liệt.
D, càng âm, càng nhiều nhiệt.
“Phản ứng toả nhiệt: biến thiên enthalpy của phản ứng có giá trị âm. Biến thiên enthalpy càng âm, phản ứng toả ra càng nhiều nhiệt.
Chọn đáp án D Đáp án: D
Chọn đáp án D Đáp án: D
Câu 25 [823625]: “Phản ứng thu nhiệt: biến thiên enthalpy của phản ứng có giá trị dương. Biến thiên enthalpy …(1)…, phản ứng thu vào …(2)…”. Nội dung phù hợp trong các ô trống (1), (2) lần lượt là
A, càng dương, càng nhiều nhiệt.
B, càng âm, càng ít nhiệt.
C, càng dương, càng mãnh liệt.
D, càng âm, càng nhiều nhiệt.
“Phản ứng thu nhiệt: biến thiên enthalpy của phản ứng có giá trị dương. Biến thiên enthalpy càng dương, phản ứng thu vào càng nhiều nhiệt.
Chọn đáp án A Đáp án: A
Chọn đáp án A Đáp án: A
Câu 26 [823626]: Điều kiện chuẩn là điều kiện ứng với áp suất …(1)… (đối với chất khí), nồng độ …(2)… (đối với chất tan trong dung dịch) và nhiệt độ thường được chọn là 298K (25oC). Nội dung phù hợp trong các ô trống (1) và (2) lần lượt là
A, 1 bar, 1 M.
B, 2 bar, 1 M.
C, 1 bar, 2 M.
D, 2 bar, 2 M.
Điều kiện chuẩn là điều kiện ứng với áp suất 1 bar (đối với chất khí), nồng độ 1M (đối với chất tan trong dung dịch) và nhiệt độ thường được chọn là 298K (25oC).
Chọn đáp án A Đáp án: A
Chọn đáp án A Đáp án: A
Câu 27 [823627]: “Tốc độ phản ứng của một phản ứng hoá học là đại lượng đặc trưng cho sự thay đổi …(1)… của chất phản ứng hoặc sản phẩm phản ứng trong một đơn vị …(2)…”. Nội dung phù hợp trong các ô trống (1), (2) lần lượt là
A, khối lượng, nhiệt độ.
B, nồng độ, thời gian.
C, nhiệt độ, thể tích.
D, khối lượng, thời gian.
“Tốc độ phản ứng của một phản ứng hoá học là đại lượng đặc trưng cho sự thay đổi nồng độ của chất phản ứng hoặc sản phẩm phản ứng trong một đơn vị thời gian.
Chọn đáp án B Đáp án: B
Chọn đáp án B Đáp án: B
Câu 28 [823628]: “Tốc độ của phản ứng phụ thuộc vào các yếu tố: nồng độ, …(1)…, diện tích bề mặt, nhiệt độ, …(2)…”. Nội dung phù hợp trong các ô trống (1), (2) lần lượt là
A, khối lượng, thể tích.
B, điện tích, áp suất.
C, độ ẩm, chất xúc tác.
D, áp suất, chất xúc tác.
Tốc độ của phản ứng phụ thuộc vào các yếu tố: nồng độ, áp suất, diện tích bề mặt, nhiệt độ, chất xúc tác.
Chọn đáp án D Đáp án: D
Chọn đáp án D Đáp án: D
Câu 29 [823630]: “Đơn chất halogen tồn tại ở dạng phân tử …(1)…, liên kết trong phân tử là liên kết …(2)…”. Nội dung phù hợp trong các ô trống (1), (2) lần lượt là
A, X3, ion.
B, X2, cộng hoá trị phân cực.
C, X2, cộng hoá trị không phân cực.
D, X3, cộng hoá trị không phân cực.
Đơn chất halogen tồn tại ở dạng phân tử X2, liên kết trong phân tử là liên kết cộng hóa trị không phân cực.
Các đáp án khác:
- Liên kết cộng hóa trị phân cực (có cực) là liên kết giữa hai nguyên tử khác nhau có hiệu độ âm điện từ 0,4 đến < 1,7 ; các cặp electron phân bỏ lệch về phía nguyên tử có độ âm điện lớn.
Chọn đáp án C Đáp án: C
Các đáp án khác:
- Liên kết cộng hóa trị phân cực (có cực) là liên kết giữa hai nguyên tử khác nhau có hiệu độ âm điện từ 0,4 đến < 1,7 ; các cặp electron phân bỏ lệch về phía nguyên tử có độ âm điện lớn.
Chọn đáp án C Đáp án: C
Câu 30 [823631]: “Halogen có …(1)… ở lớp ngoài cùng nên nguyên tử halogen có xu hướng …(2)… 1 electron để tạo hợp chất ion hoặc dùng chung electron để tạo hợp chất cộng hoá trị”. Nội dung phù hợp trong các ô trống (1), (2) lần lượt là
A, 2 electron, nhận thêm.
B, 1 electron, nhường đi.
C, 7 electron, nhận thêm.
D, 6 electron, nhường đi.
Halogen có 7 electron ở lớp ngoài cùng nên nguyên tử halogen có xu hướng nhận thêm 1 electron để tạo hợp chất ion hoặc dùng chung electron để tạo hợp chất cộng hoá trị.
Chọn đáp án C Đáp án: C
Chọn đáp án C Đáp án: C
Câu 31 [823634]: “Tốc độ phản ứng tăng khi …(1)… của chất phản ứng tăng lên hoặc khi …(2)… được sử dụng”. Nội dung phù hợp trong các ô trống (1), (2) lần lượt là
A, áp suất, nhiệt độ.
B, nồng độ, chất xúc tác.
C, nhiệt độ, khối lượng.
D, diện tích bề mặt, thể tích.
- Tốc độ của phản ứng phụ thuộc vào các yếu tố: nồng độ, áp suất, diện tích bề mặt, nhiệt độ, chất xúc tác.
- Khối lượng và thể tích không ảnh hưởng tới tốc độ phản ứng.
⟹ Tốc độ phản ứng tăng khi nồng độ của chất phản ứng tăng lên hoặc khi chất xúc tác được sử dụng.
Chọn đáp án B
Đáp án: B
- Khối lượng và thể tích không ảnh hưởng tới tốc độ phản ứng.
⟹ Tốc độ phản ứng tăng khi nồng độ của chất phản ứng tăng lên hoặc khi chất xúc tác được sử dụng.
Chọn đáp án B
Đáp án: B
Câu 32 [823635]: “Các nguyên tố trong nhóm VIIA có tính chất hoá học đặc trưng là …(1)… một electron để tạo thành ion âm có điện tích …(2)….”. Nội dung phù hợp trong các ô trống (1), (2) lần lượt là
A, nhường, –1.
B, nhận, –1.
C, nhường, –2.
D, nhận, +1.
Các nguyên tố nhóm VIIA có cấu hình electron lớp ngoài cùng là ns2np5, thiếu 1 electron để đạt cấu hình bền vững của khí hiếm. Do đó, chúng có xu hướng nhận 1 electron để tạo thành ion âm.
⟹ Các nguyên tố trong nhóm VIIA có tính chất hoá học đặc trưng là nhận một electron để tạo thành ion âm có điện tích –1.
Chọn đáp án B Đáp án: B
⟹ Các nguyên tố trong nhóm VIIA có tính chất hoá học đặc trưng là nhận một electron để tạo thành ion âm có điện tích –1.
Chọn đáp án B Đáp án: B
Câu 33 [823636]: “Phản ứng oxi hoá – khử là phản ứng trong đó có sự thay đổi về …(1)… và …(2)… của các chất tham gia phản ứng”. Nội dung phù hợp trong các ô trống (1), (2) lần lượt là
A, số electron, nhiệt độ.
B, số proton, số electron.
C, số electron, điện tích.
D, số neutron, số proton.
Phản ứng oxi hoá – khử là phản ứng trong đó có sự thay đổi về số electron và điện tích của các chất tham gia phản ứng.
Chọn đáp án C Đáp án: C
Chọn đáp án C Đáp án: C
Câu 34 [823637]: “Nhiệt độ sôi của các hydrogen halide …(1)… từ HCl đến HI. Nguyên nhân là do khối lượng phân tử tăng, làm …(2)… năng lượng cần thiết cho quá trình sôi”. Nội dung phù hợp trong các ô trống (1), (2) lần lượt là
A, giảm dần, tăng.
B, tăng dần, giảm.
C, giảm dần, giảm.
D, tăng dần, tăng.
Nhiệt độ sôi của các hydrogen halide tăng dần từ HCl đến HI. Nguyên nhân là do khối lượng phân tử tăng, làm tăng năng lượng cần thiết cho quá trình sôi.
Chọn đáp án D Đáp án: D
Chọn đáp án D Đáp án: D
Câu 35 [823638]: “Trong cùng chu kì, nguyên tử của nguyên tố kim loại có bán kính …(1)… và điện tích hạt nhân …(2)… so với nguyên tử của nguyên tố phi kim”. Nội dung phù hợp trong ô trống (1), (2) lần lượt là
A, lớn hơn, sấp xỉ.
B, lớn hơn, nhỏ hơn.
C, sấp xỉ, nhỏ hơn.
D, nhỏ hơn, lớn hơn.
Trong cùng chu kì, nguyên tử của nguyên tố kim loại có bán kính lớn hơn và điện tích hạt nhân nhỏ hơn so với nguyên tử của nguyên tố phi kim.
Chọn đáp án B
Đáp án: B