PHẦN I. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
Câu 1 [702605]: Một vật làm bằng sắt tây (sắt tráng thiếc) có một vết cắt sâu đến lớp sắt. Khi để vật này tiếp xúc với không khí ẩm thì xảy ra ăn mòn …(1)…, trong đó …(2)… bị oxi hóa. Nội dung phù hợp trong các ô trống (1), (2) lần lượt là
A, hóa học, sắt.
B, điện hóa, thiếc.
C, hóa học, thiếc.
D, điện hóa, sắt.
Một vật làm bằng sắt tây (sắt tráng thiếc) có một vết cắt sâu đến lớp sắt. Khi để vật này tiếp xúc với không khí ẩm (tạo ra môi trường điện li, điều kiện để xảy ra ăn mòn điện hoá) sẽ xuất hiện 2 điện cực là sắt và thiếc.
Dựa vào dãy hoạt động hoá học của kim loại, sắt (Fe) đứng trước thiếc (Sn) nên sắt hoạt động hoá học mạnh hơn , dễ nhường electron hơn ⇒ Sắt đóng vai trò là chất khử (hay chất bị oxi hoá)
⇒ Chọn đáp án D. Đáp án: D
Dựa vào dãy hoạt động hoá học của kim loại, sắt (Fe) đứng trước thiếc (Sn) nên sắt hoạt động hoá học mạnh hơn , dễ nhường electron hơn ⇒ Sắt đóng vai trò là chất khử (hay chất bị oxi hoá)
⇒ Chọn đáp án D. Đáp án: D
Câu 2 [702606]: Vôi tôi là tên gọi thông thường của Ca(OH)2. Vôi tôi có giá thành rẻ, được sử dụng rộng rãi trong nhiều ngành công nghiệp như sản xuất ammonia, chloride vôi (CaOCl2), vật liệu xây dựng, sản xuất mía đường. Tên thay thế (IUPAC) của vôi tôi là
A, calcium oxide.
B, calcium carbonate.
C, calcium hydroxide.
D, calcium chloride.
Tên thay thế (IUPAC) của vôi tôi Ca(OH)2 là calcium hydroxide.
❌ A. calcium oxide có công thức là CaO
❌ B. calcium carbonate có công thức là CaCO3
❌ D. calcium chloride có công thức là CaCl2
⇒ Chọn đáp án C Đáp án: C
❌ A. calcium oxide có công thức là CaO
❌ B. calcium carbonate có công thức là CaCO3
❌ D. calcium chloride có công thức là CaCl2
⇒ Chọn đáp án C Đáp án: C
Câu 3 [702607]: Một polymer có cấu tạo một đoạn ngắn như sau:
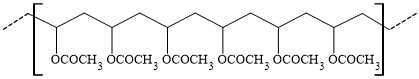
Monomer nào sau đây tạo nên polymer trên?

Monomer nào sau đây tạo nên polymer trên?
A, 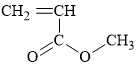

B, 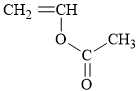

C, 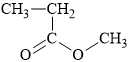

D, 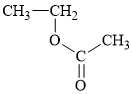

Dựa vào cấu tạo của polymer để dự đoán được monomer tạo nên là CH2=CH‒O‒C(=O)‒CH3.
⇒ Chọn đáp án B Đáp án: B
⇒ Chọn đáp án B Đáp án: B
Câu 4 [560616]: Vì sao người ta thường buộc một mẩu chì vào dây của cần câu mà không phải một mẩu nhôm?
A, Chì có khối lượng riêng lớn nên dễ chìm xuống nước.
B, Chì có giá thành rẻ hơn nhôm.
C, Chì nhẹ hơn hơn nên có thể nổi trên mặt nước.
D, Chì có màu gần như trong suốt nên cá sẽ không phát hiện ra.
Vì chì là kim loại có khối lượng riêng lớn làm dây cần câu chìm sâu xuống nước. Trong khi đó, nhôm là kim loại nhẹ (có khối lượng riêng nhỏ) nên dây cần câu không chìm được sâu dưới nước.
⇒ Chọn đáp án A Đáp án: A
⇒ Chọn đáp án A Đáp án: A
Câu 5 [702608]: 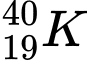 là một đồng vị phóng xạ của nguyên tố potassium có mặt trong cơ thể con người. Tổng số các loại hạt (proton, neutron và electron) trong đồng vị này là
là một đồng vị phóng xạ của nguyên tố potassium có mặt trong cơ thể con người. Tổng số các loại hạt (proton, neutron và electron) trong đồng vị này là
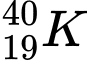 là một đồng vị phóng xạ của nguyên tố potassium có mặt trong cơ thể con người. Tổng số các loại hạt (proton, neutron và electron) trong đồng vị này là
là một đồng vị phóng xạ của nguyên tố potassium có mặt trong cơ thể con người. Tổng số các loại hạt (proton, neutron và electron) trong đồng vị này là A, 40.
B, 59.
C, 21.
D, 61.
Đồng vị potassium này có số hạt proton = số hạt electron = 19 hạt.
Số khối: A = Z + N ⇔ 40 = 19 + N ⇔ N = 21 hạt.
Tổng số các loại hạt trong đồng vị này là: 19 + 19 + 21 = 59 hạt.
⇒ Chọn đáp án B Đáp án: B
Số khối: A = Z + N ⇔ 40 = 19 + N ⇔ N = 21 hạt.
Tổng số các loại hạt trong đồng vị này là: 19 + 19 + 21 = 59 hạt.
⇒ Chọn đáp án B Đáp án: B
Câu 6 [233830]: Nước tự nhiên chứa nhiều những cation nào sau đây được gọi là nước cứng?
A, Na+, Al3+.
B, Na+, K+.
C, Al3+, K+.
D, Ca2+, Mg2+.
HD: Nước cứng là nước có chứa nhiều ion Ca2+ và Mg2+.
⇝ Chọn đáp án D. Đáp án: D

⇝ Chọn đáp án D. Đáp án: D
Câu 7 [702609]: Năm 1785, một vụ nổ xảy ra tại nhà kho nhà Giacomelli (Roma, Italia) làm nghề nghiền bột mì. Sau khi điều tra, nguyên nhân ban đầu dẫn đến vụ nổ là do bột mì khô. Sự cố xảy ra khi bột mì bay trong không khí, chạm tới nguồn lửa của chiếc đèn, đây là vụ “nổ bụi” đầu tiên trong lịch sử. Sau đó là các vụ nổ bụi trong hầm than, xưởng sản xuất sữa bột, dược phẩm, kim loại, … Vụ nổ bụi có thể xảy ra nếu hội tụ đủ 5 điều kiện: Nhiên liệu dạng bụi mịn, bụi nhiên liệu phân tán trong không khí, có oxygen, nguồn nhiệt gây kích nổ, không gian kín. Cho các phát biểu sau:
(a) Nếu không có nguồn oxygen thì vụ nổ bụi sẽ không thể xảy ra.
(b) Các hạt bụi mịn như bụi than, bụi kim loại,… có thể dẫn đến nổ bụi.
(c) Khi ở dạng bột hay dạng bụi, diện tích tiếp xúc sẽ rất lớn khiến cho phản ứng xảy ra nhanh hơn và sẽ gây nổ.
(d) Bụi càng mịn, khả năng gây nổ càng cao do phát tán nhanh và dễ lơ lửng trong không khí.
Các phát biểu đúng là
(a) Nếu không có nguồn oxygen thì vụ nổ bụi sẽ không thể xảy ra.
(b) Các hạt bụi mịn như bụi than, bụi kim loại,… có thể dẫn đến nổ bụi.
(c) Khi ở dạng bột hay dạng bụi, diện tích tiếp xúc sẽ rất lớn khiến cho phản ứng xảy ra nhanh hơn và sẽ gây nổ.
(d) Bụi càng mịn, khả năng gây nổ càng cao do phát tán nhanh và dễ lơ lửng trong không khí.
Các phát biểu đúng là
A, (a), (b).
B, (a), (b), (d).
C, (b), (c), (d).
D, (a), (b), (c), (d).
Vụ nổ bụi có thể xảy ra nếu hội tụ đủ 5 điều kiện:
💥 Nhiên liệu dạng bụi mịn.
💥 Bụi nhiên liệu phân tán trong không khí.
💥 Có oxygen.
💥 Nguồn nhiệt gây kích nổ.
💥 Không gian kín.
Phân tích các phát biểu:
✔️ (a) Đúng. Nếu không có nguồn oxygen thì vụ nổ bụi sẽ không thể xảy ra do nổ bụi là một phản ứng cháy xảy ra khi bụi mịn tiếp xúc với oxygen và có nguồn năng lượng kích hoạt. Không có oxygen, quá trình cháy không xảy ra.
✔️ (b) Đúng. Đúng. Các hạt bụi mịn của các chất dễ cháy (như than, kim loại) có khả năng dẫn đến nổ bụi nếu có điều kiện thích hợp (hàm lượng bụi, nguồn oxygen, nguồn kích hoạt).
✔️ (c) Đúng. Khi ở dạng bột hoặc bụi, diện tích tiếp xúc với oxygen lớn hơn rất nhiều, làm cho phản ứng xảy ra nhanh gây thay đổi áp suất đột ngột và dễ dẫn đến nổ.
✔️ (d) Đúng. Bụi càng mịn thì khả năng phát tán trong không khí càng cao, dễ tạo hỗn hợp cháy với oxygen, làm tăng nguy cơ gây nổ.
▷ Cả 4 phát biểu đều đúng
⇒ Chọn đáp án D Đáp án: D
💥 Nhiên liệu dạng bụi mịn.
💥 Bụi nhiên liệu phân tán trong không khí.
💥 Có oxygen.
💥 Nguồn nhiệt gây kích nổ.
💥 Không gian kín.
Phân tích các phát biểu:
✔️ (a) Đúng. Nếu không có nguồn oxygen thì vụ nổ bụi sẽ không thể xảy ra do nổ bụi là một phản ứng cháy xảy ra khi bụi mịn tiếp xúc với oxygen và có nguồn năng lượng kích hoạt. Không có oxygen, quá trình cháy không xảy ra.
✔️ (b) Đúng. Đúng. Các hạt bụi mịn của các chất dễ cháy (như than, kim loại) có khả năng dẫn đến nổ bụi nếu có điều kiện thích hợp (hàm lượng bụi, nguồn oxygen, nguồn kích hoạt).
✔️ (c) Đúng. Khi ở dạng bột hoặc bụi, diện tích tiếp xúc với oxygen lớn hơn rất nhiều, làm cho phản ứng xảy ra nhanh gây thay đổi áp suất đột ngột và dễ dẫn đến nổ.
✔️ (d) Đúng. Bụi càng mịn thì khả năng phát tán trong không khí càng cao, dễ tạo hỗn hợp cháy với oxygen, làm tăng nguy cơ gây nổ.
▷ Cả 4 phát biểu đều đúng
⇒ Chọn đáp án D Đáp án: D
Câu 8 [702610]: Nguyên liệu nitrogen được sử dụng trong các nhà máy sản xuất phân bón được lấy từ
A, không khí.
B, ammonia.
C, khí lò cốc.
D, oxide của nitrogen.
Ammonia (NH3) là nguyên liệu ban đầu của tất cả các quá trình sản xuất phân đạm. “Cuộc cách mạng xanh" giúp loài người thoát khỏi tình trạng thiếu lương thực bắt đầu từ việc sản xuất ammonia theo quy trình Haber-Bosch.
⇒ Chọn đáp án B Đáp án: B
⇒ Chọn đáp án B Đáp án: B
Câu 9 [702611]: Phổ khối lượng (MS) là phương pháp hiện đại để xác định phân tử khối của các hợp chất hữu cơ. Kết quả phân tích phổ khối lượng cho thấy phân tử khối của hợp chất hữu cơ X là 60. Chất X không phải là chất nào sau đây?
A, Acetic acid.
B, Methyl formate.
C, Acetone.
D, Propan-2-ol.
Acetic acid (CH3COOH); Methyl formate (HCOOCH3); Propan-2-ol (CH3CH(OH)CH3) đều có phân tử khối bằng 60.
Acetone (CH3COCH3) có phân tử khối là 58.
⇒ Chọn đáp án C Đáp án: C
Acetone (CH3COCH3) có phân tử khối là 58.
⇒ Chọn đáp án C Đáp án: C
Câu 10 [702612]: 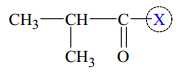
Nhóm được gắn vào vị trí X được khoanh tròn trên là
Danh pháp IUPAC của hợp chất dưới đây là methyl isobutyrate.

Nhóm được gắn vào vị trí X được khoanh tròn trên là
A, CH3.
B, C2H5.
C, OCH3.
D, CH(CH3)2.
Methyl isobutyrate là tên gọi của một ester (RCOOR'). Từ công thức cấu tạo thấy phần X chính là OR', mà tên gọi của gốc R' là methyl
⇒ X chính là OCH3.
⇒ Chọn đáp án C Đáp án: C
⇒ X chính là OCH3.
⇒ Chọn đáp án C Đáp án: C
Câu 11 [308668]: Nhóm chức -NH2 có tên gọi là
A, Amino.
B, Nitro.
C, Amine.
D, Nitrile.
Nhóm chức -NH2 có tên gọi là amine.
⇒ Chọn đáp án C Đáp án: C
⇒ Chọn đáp án C Đáp án: C
Câu 12 [702613]: Carbohydrate nào sau đây có kích thước phân tử lớn nhất?
A, Maltose.
B, Saccharose.
C, Glucose.
D, Cellulose.
Carbohydrate có kích thước phân tử lớn nhất là cellulose vì nó là một polysaccharide.
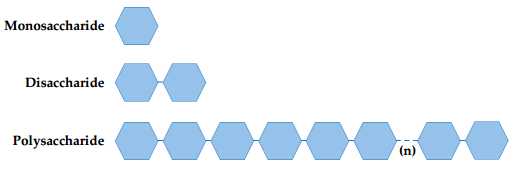
⇒ Chọn đáp án D Đáp án: D

⇒ Chọn đáp án D Đáp án: D
Câu 13 [702614]: Phương trình hóa học của phản ứng halogeno hóa methane để điều chế dùng để điều chế chloromethane như sau:
CH4 + Cl2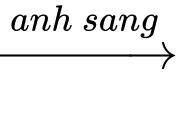 HCl + CH3Cl.
HCl + CH3Cl.
Cơ chế của phản ứng trên xảy ra theo các giai đoạn:
❶ Giai đoạn khơi mào: Cl–Cl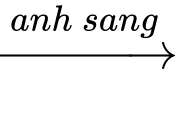 Cl• + Cl•.
Cl• + Cl•.
❷ Giai đoạn phát triển: CH4 + Cl• CH3• + HCl;
CH3• + HCl;
Cl2 + CH3• CH3Cl + Cl•.
CH3Cl + Cl•.
❸ Giai đoạn kết thúc: Cl• + CH3• CH3Cl;
CH3Cl;
Cl• + Cl• Cl2.
Cl2.
Các chất Cl• và CH3• được gọi là gốc tự do. Nhận định nào sau đây là đúng?
CH4 + Cl2
 HCl + CH3Cl.
HCl + CH3Cl.Cơ chế của phản ứng trên xảy ra theo các giai đoạn:
❶ Giai đoạn khơi mào: Cl–Cl
 Cl• + Cl•.
Cl• + Cl•.❷ Giai đoạn phát triển: CH4 + Cl•
 CH3• + HCl;
CH3• + HCl;Cl2 + CH3•
 CH3Cl + Cl•.
CH3Cl + Cl•.❸ Giai đoạn kết thúc: Cl• + CH3•
 CH3Cl;
CH3Cl;Cl• + Cl•
 Cl2.
Cl2.Các chất Cl• và CH3• được gọi là gốc tự do. Nhận định nào sau đây là đúng?
A, Trong cấu tạo Lewis của gốc tự do Cl• có chứa 8 electron.
B, Phản ứng trên giúp điều chế dẫn xuất dichloro.
C, Trong giai đoạn khơi mào, liên kết π trong phân tử Cl2 bị phá vỡ.
D, Trong giai đoạn phát triển, tổng số liên kết σ trước và sau phản ứng bằng nhau.
Phân tích các nhận định:
❌ A. Sai. Trong cấu tạo Lewis của gốc tự do Cl• có chứa 7 electron:
❌ B. Sai. Phản ứng trên giúp điều chế chloromethane (CH3Cl) (chỉ 1 Cl bị thay thế) chứ không phải dichloro (Trường hợp 2 nguyên tử Cl bị thay thế sẽ tạo thành chloromethane CH2Cl2).
❌ C. Sai. Phân tử Cl2 gồm hai nguyên tử chlorine liên kết với nhau bằng một liên kết đơn (liên kết đơn là liên kết σ), không phải liên kết π.
✔️ D. Đúng. Trong giai đoạn phát triển, phân tử CH4 có 4 liên kết σ và trong phân tử CH3Cl cũng có 4 liên kết σ → Do đó tổng số liên kết σ trước và sau phản ứng bằng nhau.
⇒ Chọn đáp án D Đáp án: D
❌ A. Sai. Trong cấu tạo Lewis của gốc tự do Cl• có chứa 7 electron:

❌ B. Sai. Phản ứng trên giúp điều chế chloromethane (CH3Cl) (chỉ 1 Cl bị thay thế) chứ không phải dichloro (Trường hợp 2 nguyên tử Cl bị thay thế sẽ tạo thành chloromethane CH2Cl2).
❌ C. Sai. Phân tử Cl2 gồm hai nguyên tử chlorine liên kết với nhau bằng một liên kết đơn (liên kết đơn là liên kết σ), không phải liên kết π.
✔️ D. Đúng. Trong giai đoạn phát triển, phân tử CH4 có 4 liên kết σ và trong phân tử CH3Cl cũng có 4 liên kết σ → Do đó tổng số liên kết σ trước và sau phản ứng bằng nhau.
⇒ Chọn đáp án D Đáp án: D
Câu 14 [702615]: Ester X có công thức cấu tạo CH3COOCH(CH3)CH2CH3. X có thể được điều chế bằng cách đun hồi lưu alcohol Y với ethanoic acid trong xúc tác H+. Tên gọi của Y là
A, butan-1-ol.
B, butan-2-ol.
C, butan-3-ol.
D, methylpropan-2-ol.
CH3COOH + CH3CH(OH)CH2CH3 (Y) -(H+)→ CH3COOCH(CH3)CH2CH3 (X) + H2O
⇒ Chọn đáp án B Đáp án: B
⇒ Chọn đáp án B Đáp án: B
Câu 15 [702616]: Hiện nay, hàng trăm amino acid khác nhau đã được tìm ra, cả tổng hợp và tự nhiên, nhưng trong số này chỉ có 20 loại …(1)… xây dựng nên tất cả các …(2)… trong cơ thể con người. Nội dung phù hợp trong các ô trống (1), (2) lần lượt là
A, β-amino acid, enzyme.
B, amide, peptide.
C, α-amino acid, protein.
D, peptide, nucleotide.
Hiện nay, hàng trăm amino acid khác nhau đã được tìm ra, cả tổng hợp và tự nhiên, nhưng trong số này chỉ có 20 loại α-amino acid xây dựng nên tất cả các protein trong cơ thể con người.
⇒ Chọn đáp án C Đáp án: C
⇒ Chọn đáp án C Đáp án: C
Câu 16 [702617]: Ở độ pH = 7, các amino acid: lysine (Lys), glycine (Gly) và glutamic acid (Glu) tồn tại ở các dạng như sau:
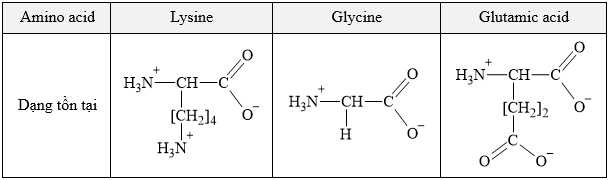
Kết quả khi tiến hành điện di hỗn hợp của ba amino acid được thể hiện trong hình dưới đây:
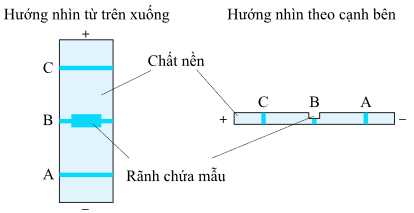
Cho các nhận định sau về quá trình điện di:
(a) Tại môi trường pH = 7 thì tất cả các nhóm NH2 của lysine sẽ chuyển thành nhóm NH3+.
(b) Chất B là glycine có phân tử khối nhỏ nhất nên sẽ không di chuyển.
(c) Chất C là glutamic acid sẽ di chuyển về phía cực dương.
(d) Theo thí nghiệm trên, có thể tách riêng các amino acid trong hỗn hợp của chúng.
Các nhận định đúng là

Kết quả khi tiến hành điện di hỗn hợp của ba amino acid được thể hiện trong hình dưới đây:

Cho các nhận định sau về quá trình điện di:
(a) Tại môi trường pH = 7 thì tất cả các nhóm NH2 của lysine sẽ chuyển thành nhóm NH3+.
(b) Chất B là glycine có phân tử khối nhỏ nhất nên sẽ không di chuyển.
(c) Chất C là glutamic acid sẽ di chuyển về phía cực dương.
(d) Theo thí nghiệm trên, có thể tách riêng các amino acid trong hỗn hợp của chúng.
Các nhận định đúng là
A, (a), (b).
B, (a), (c).
C, (a), (c), (d).
D, (b), (c), (d).
Phân tích các nhận định:
✔️ (a) Đúng. Tại môi trường pH = 7 (môi trường trung tính) thì amino acid tồn tại ở dạng ion lưỡng cực nên tất cả các nhóm NH2 của lysine sẽ chuyển thành nhóm NH3+ và nhóm COOH sẽ chuyển thành nhóm COO‒.
❌ (b) Sai. Chất B là glycine không di chuyển do có tổng điện tích bằng 0 ở pH = 7 chứ không ảnh hưởng bởi phân tử khối.
✔️ (c) Chất C là glutamic acid sẽ di chuyển về phía cực dương do có tổng điện tích ‒1 ở pH = 7.
✔️ (d) Theo thí nghiệm trên, có thể tách riêng các amino acid trong hỗn hợp của chúng vì lysine với điện tích +1 sẽ di chuyển về phía cực âm, glutamic acid di chuyển về phía cực dương với điện tích là -1 và glycine không di chuyển trong môi trường trung tính.
Các nhận định đúng là (a) (c) (d)
⇒ Chọn đáp án C Đáp án: C
✔️ (a) Đúng. Tại môi trường pH = 7 (môi trường trung tính) thì amino acid tồn tại ở dạng ion lưỡng cực nên tất cả các nhóm NH2 của lysine sẽ chuyển thành nhóm NH3+ và nhóm COOH sẽ chuyển thành nhóm COO‒.
❌ (b) Sai. Chất B là glycine không di chuyển do có tổng điện tích bằng 0 ở pH = 7 chứ không ảnh hưởng bởi phân tử khối.
✔️ (c) Chất C là glutamic acid sẽ di chuyển về phía cực dương do có tổng điện tích ‒1 ở pH = 7.
✔️ (d) Theo thí nghiệm trên, có thể tách riêng các amino acid trong hỗn hợp của chúng vì lysine với điện tích +1 sẽ di chuyển về phía cực âm, glutamic acid di chuyển về phía cực dương với điện tích là -1 và glycine không di chuyển trong môi trường trung tính.
Các nhận định đúng là (a) (c) (d)
⇒ Chọn đáp án C Đáp án: C
Sử dụng đoạn thông tin dưới đây để trả lời câu 17 và câu 18
Cho bảng thế điện cực chuẩn của các cặp oxi hóa – khử như sau:
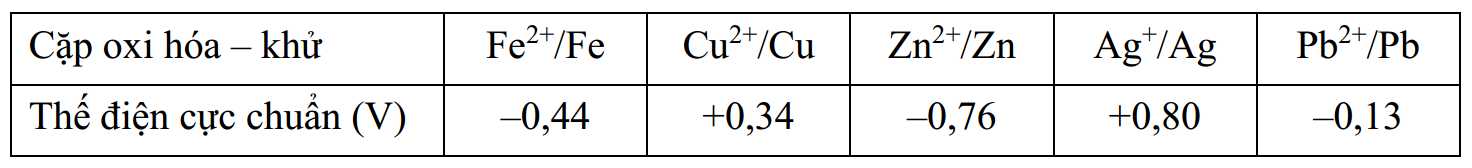
Thiết lập một pin Galvani nối với bòng đèn như sơ đồ hình vẽ bên. Trong đó 2 dung dịch A và B sử dụng các cặp trên. Giả sử một bóng đèn cần tối thiểu 1,5 V để hoạt động.
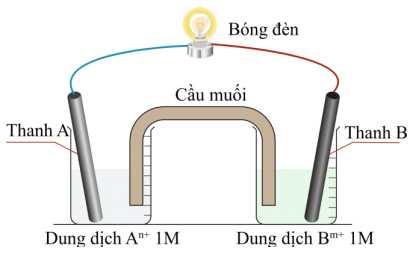
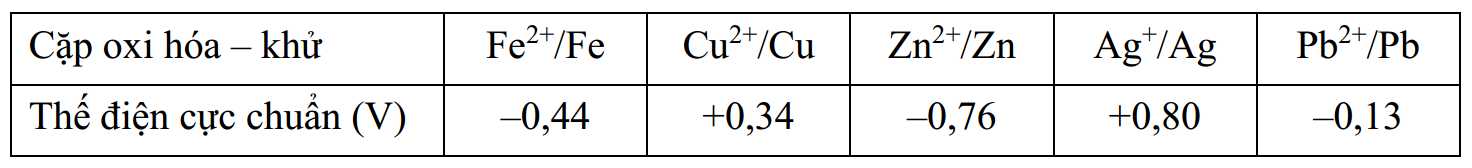
Thiết lập một pin Galvani nối với bòng đèn như sơ đồ hình vẽ bên. Trong đó 2 dung dịch A và B sử dụng các cặp trên. Giả sử một bóng đèn cần tối thiểu 1,5 V để hoạt động.

Câu 17 [702618]: Nếu dung dịch A và B được thiết lập từ các cặp oxi hoá khử là Fe2+/Fe và Ag+/Ag ở điều kiện chuẩn thì quá trình xảy ra ở cực âm là
A, Fe(s)  Fe2+(aq) +2e.
Fe2+(aq) +2e.
 Fe2+(aq) +2e.
Fe2+(aq) +2e.B, Fe2+(aq) + 2e  Fe(s).
Fe(s).
 Fe(s).
Fe(s).C, Ag+(aq) + 1e  Ag(s).
Ag(s).
 Ag(s).
Ag(s).D, Ag(s)  Ag+(aq) + 1e.
Ag+(aq) + 1e.
 Ag+(aq) + 1e.
Ag+(aq) + 1e.
Pin Galvani gồm hai điện cực được nối với nhau bằng cầu muối. Khi pin hoạt động, ở điện cực âm (anode) xảy ra quá trình oxi hoá kim loại và ở điện cực dương (cathode) xảy ra quá trình khử cation.
Cực dương là kim loại có thế điện cực lớn hơn, cực âm là kim loại có thế điện cực nhỏ hơn.
Vì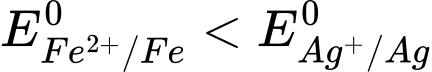 nên cực âm là Fe.
nên cực âm là Fe.
Cực dương là kim loại có thế điện cực lớn hơn, cực âm là kim loại có thế điện cực nhỏ hơn.
Vì
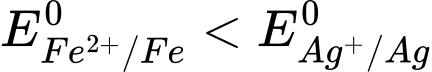 nên cực âm là Fe.
nên cực âm là Fe.Khi pin hoạt động, ở điện cực âm (anode) xảy ra quá trình oxi hoá kim loại: Fe(s) → Fe2+(aq)+ 2e.
⇒ Chọn đáp án A
⇒ Chọn đáp án A
Câu 18 [702619]: Có bao nhiêu cách tạo ra pin Galvani được thiết lập từ hai cặp oxi hóa – khử trong số các cặp trong bảng trên để bóng đèn hoạt động?
A, 1.
B, 2.
C, 3.
D, 4.
Để bóng đèn hoạt động thì cần tối thiểu 1,5 V. Ta xét bảng hiệu điện thế của các cặp oxi hoá - khử như sau:
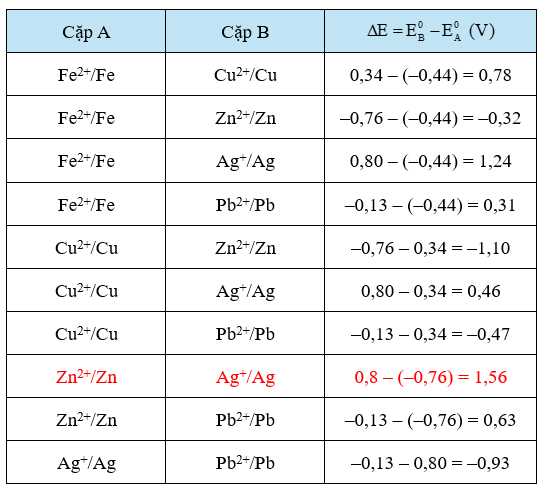
Vậy chỉ có 1 cặp oxi hóa – khử có hiệu điện thế lớn hơn 1,5: Ag được tạo ra ở cực dương, Zn2+ được tạo ra ở cực âm.
⇒ Chọn đáp án A Đáp án: A

Vậy chỉ có 1 cặp oxi hóa – khử có hiệu điện thế lớn hơn 1,5: Ag được tạo ra ở cực dương, Zn2+ được tạo ra ở cực âm.
⇒ Chọn đáp án A Đáp án: A
PHẦN II. Thí sinh trả lời từ câu 1 đến câu 4. Trong mỗi ý a), b), c), d) ở mỗi câu, thí sinh chọn đúng hoặc sai
Câu 19 [702620]: Gỉ đồng được hình thành do sự ăn mòn kim loại đồng, nó có màu xanh lục chứa cả đồng(II) carbonate, CuCO3 và đồng(II) hydroxide, Cu(OH)2, với hàm lượng khác nhau. Cả hai hợp chất đồng đều phản ứng với hydrochloric acid loãng.
CuCO3(s) + 2HCl (aq) CuCl2(aq) + CO2(g) + H2O(l)
CuCl2(aq) + CO2(g) + H2O(l)
Cu(OH)2(s) + 2HCl (aq) CuCl2(aq) + 2H2O(l)
CuCl2(aq) + 2H2O(l)
Một bạn học sinh lập kế hoạch thực hiện một thí nghiệm để xác định phần trăm đồng(II) carbonate trong một mẫu gỉ đồng. Giả thuyết được học sinh đưa ra: “Tìm thể tích hydrochloric acid loãng cần thiết để phản ứng vừa đủ với khối lượng gỉ đồng sẽ là phương pháp phù hợp để xác định hàm lượng đồng(II) carbonate trong mẫu gỉ đồng”. Các hóa chất cần chuẩn bị gồm:
▪ Một mẫu gỉ đồng.
▪ dung dịch hydrochloric acid, HCl 1 M .
▪ Thuốc thử và thiết bị phòng thí nghiệm thông thường.
Giả sử các chất khác có trong gỉ đồng đều không bị ảnh hưởng bởi nhiệt và trơ.
CuCO3(s) + 2HCl (aq)
 CuCl2(aq) + CO2(g) + H2O(l)
CuCl2(aq) + CO2(g) + H2O(l)Cu(OH)2(s) + 2HCl (aq)
 CuCl2(aq) + 2H2O(l)
CuCl2(aq) + 2H2O(l)Một bạn học sinh lập kế hoạch thực hiện một thí nghiệm để xác định phần trăm đồng(II) carbonate trong một mẫu gỉ đồng. Giả thuyết được học sinh đưa ra: “Tìm thể tích hydrochloric acid loãng cần thiết để phản ứng vừa đủ với khối lượng gỉ đồng sẽ là phương pháp phù hợp để xác định hàm lượng đồng(II) carbonate trong mẫu gỉ đồng”. Các hóa chất cần chuẩn bị gồm:
▪ Một mẫu gỉ đồng.
▪ dung dịch hydrochloric acid, HCl 1 M .
▪ Thuốc thử và thiết bị phòng thí nghiệm thông thường.
Giả sử các chất khác có trong gỉ đồng đều không bị ảnh hưởng bởi nhiệt và trơ.
Phân tích các phát biểu:
✔️ a) Đúng. HCl có nhiệm vụ cung cấp H+ cho phản ứng, H2SO4 và HNO3 hoàn toàn có thể thay HCl để tạo ra H+ tương tự. Do H2SO4 và HNO3 trong phản ứng này không thể hiện tính oxi hoá mạnh (Cu2+ đã không còn tính khử)
✔️ b) Đúng. Ta cần một lượng mol HCl nhất định để phản ứng vừa đủ, mà nHCl = CM HCl . VHCl nên nếu nồng độ HCl giảm thì thể tích HCl cần dùng phải tăng để phản ứng hoàn toàn.
✔️ c) Đúng. Giả thuyết là sai vì cả CuCO3 và Cu(OH)2 đều phản ứng với HCl nên không thể dựa vào thể tích acid HCl loãng để xác định hàm lượng đồng(II) carbonate trong mẫu gỉ đồng.
✔️ d) Đúng. Dựa vào 2 phản ứng xảy ra thì chỉ có phản ứng của đồng(II) carbonate với acid là sinh ra khí nên dựa vào thể tích khí sinh ra trong quá trình phản ứng có thể xác định được hàm lượng đồng(II) carbonate.
✔️ a) Đúng. HCl có nhiệm vụ cung cấp H+ cho phản ứng, H2SO4 và HNO3 hoàn toàn có thể thay HCl để tạo ra H+ tương tự. Do H2SO4 và HNO3 trong phản ứng này không thể hiện tính oxi hoá mạnh (Cu2+ đã không còn tính khử)
✔️ b) Đúng. Ta cần một lượng mol HCl nhất định để phản ứng vừa đủ, mà nHCl = CM HCl . VHCl nên nếu nồng độ HCl giảm thì thể tích HCl cần dùng phải tăng để phản ứng hoàn toàn.
✔️ c) Đúng. Giả thuyết là sai vì cả CuCO3 và Cu(OH)2 đều phản ứng với HCl nên không thể dựa vào thể tích acid HCl loãng để xác định hàm lượng đồng(II) carbonate trong mẫu gỉ đồng.
✔️ d) Đúng. Dựa vào 2 phản ứng xảy ra thì chỉ có phản ứng của đồng(II) carbonate với acid là sinh ra khí nên dựa vào thể tích khí sinh ra trong quá trình phản ứng có thể xác định được hàm lượng đồng(II) carbonate.
Câu 20 [702621]: Cấu trúc dày đặc của cellulose làm giảm khả năng phản ứng và cản trở các ứng dụng của nó. Sulfuric acid đậm đặc là dung môi lý tưởng để hòa tan cellulose và do đó đã được sử dụng rộng rãi để xử lý cellulose.
Chuẩn bị:
Mẫu cellulose thô và các mẫu cellulose được xử lí với sulfuric acid đậm đặc 70 % theo tỉ lệ 1 : 2,5 trong các khoảng thời gian khác nhau. Ký hiệu “cellulose – 30'” có nghĩa là mẫu cellulose được xử lí với sulfuric acid đậm đặc 70 % theo tỉ lệ 1 : 2,5 trong 30 phút. Tương tự với các mẫu cellulose được xử lí với sulfuric acid theo tỉ lệ 1 : 2,5 lần lượt trong 20 phút; 15 phút; 10 phút; 5 phút, ký hiệu lần lượt là: cellulose – 20'; cellulose – 15'; cellulose – 10'; cellulose – 5'.
Tiến hành thí nghiệm:
Cho mẫu cellulose thô và các mẫu cellulose được xử lí với sulfuric acid đậm đặc 70 % cùng với một lượng enzyme. Hỗn hợp được thêm vào máy khuấy (tốc độ 150 vòng/phút và 50oC).
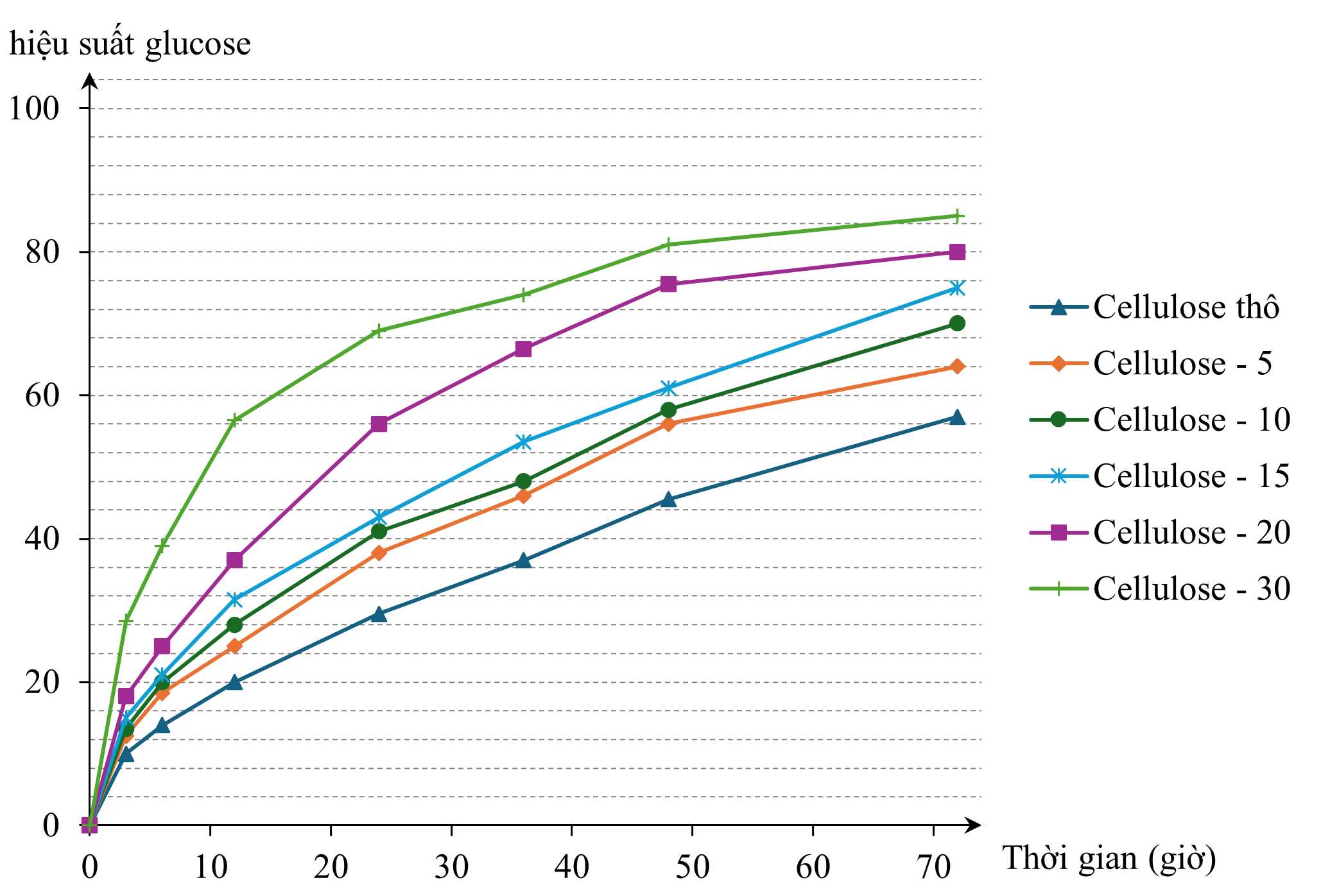
Kết quả của quá trình thủy phân được thể hiện trong biểu đồ sau:
Chuẩn bị:
Mẫu cellulose thô và các mẫu cellulose được xử lí với sulfuric acid đậm đặc 70 % theo tỉ lệ 1 : 2,5 trong các khoảng thời gian khác nhau. Ký hiệu “cellulose – 30'” có nghĩa là mẫu cellulose được xử lí với sulfuric acid đậm đặc 70 % theo tỉ lệ 1 : 2,5 trong 30 phút. Tương tự với các mẫu cellulose được xử lí với sulfuric acid theo tỉ lệ 1 : 2,5 lần lượt trong 20 phút; 15 phút; 10 phút; 5 phút, ký hiệu lần lượt là: cellulose – 20'; cellulose – 15'; cellulose – 10'; cellulose – 5'.
Tiến hành thí nghiệm:
Cho mẫu cellulose thô và các mẫu cellulose được xử lí với sulfuric acid đậm đặc 70 % cùng với một lượng enzyme. Hỗn hợp được thêm vào máy khuấy (tốc độ 150 vòng/phút và 50oC).
Kết quả của quá trình thủy phân được thể hiện trong biểu đồ sau:

Phân tích các phát biểu:
❌ a) Sai. Phát biểu đưa ra là xét "đối với cellulose thô" chứ không phải so sánh cellulose thô với các mẫu khác nên đối với cellulose thô, ta quan sát trong biểu đồ thấy hiệu suất của quá trình thủy phân sau 72 giờ là cao nhất.
✔️ b) Đúng. Tại mọi thời điểm, mẫu cellulose được xử lí trong 20 phút sẽ giúp hiệu suất của quá trình thủy phân tốt hơn mẫu được xử lí trong 15 phút.
✔️ c) Đúng. Quan sát thấy đường biểu diễn mẫu cellulose được xử lí trong 30 phút luôn có giá trị hiệu suất lớn nhất nên xử lí mẫu với sulfuric acid đậm đặc 70 % trong 30 phút sẽ giúp hiệu suất của quá trình thủy phân là lớn nhất.
✔️ d) Đúng. Từ kết quả của thí nghiệm có thể đứa ra kết luận là thời gian xử lí cellulose với sulfuric acid đậm đặc 70 % càng lâu thì hiệu suất của quá trình thủy phân càng lớn.
❌ a) Sai. Phát biểu đưa ra là xét "đối với cellulose thô" chứ không phải so sánh cellulose thô với các mẫu khác nên đối với cellulose thô, ta quan sát trong biểu đồ thấy hiệu suất của quá trình thủy phân sau 72 giờ là cao nhất.
✔️ b) Đúng. Tại mọi thời điểm, mẫu cellulose được xử lí trong 20 phút sẽ giúp hiệu suất của quá trình thủy phân tốt hơn mẫu được xử lí trong 15 phút.
✔️ c) Đúng. Quan sát thấy đường biểu diễn mẫu cellulose được xử lí trong 30 phút luôn có giá trị hiệu suất lớn nhất nên xử lí mẫu với sulfuric acid đậm đặc 70 % trong 30 phút sẽ giúp hiệu suất của quá trình thủy phân là lớn nhất.
✔️ d) Đúng. Từ kết quả của thí nghiệm có thể đứa ra kết luận là thời gian xử lí cellulose với sulfuric acid đậm đặc 70 % càng lâu thì hiệu suất của quá trình thủy phân càng lớn.
Câu 21 [702622]: Một học sinh đưa ra giả thuyết rằng có thể oxi hóa pentan-2-ol để tạo thành pentan-2-one như sau:
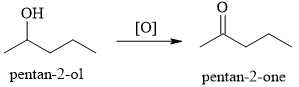
Tiến hành thực hiện phản ứng oxi hóa, để kiểm tra phản ứng oxi hóa có xảy ra hay không thì học sinh tách riêng từng chất trong hỗn hợp sản phẩm và tiến hành đo phổ hồng ngoại. Phổ hồng ngoại của một chất X được cho như sau:
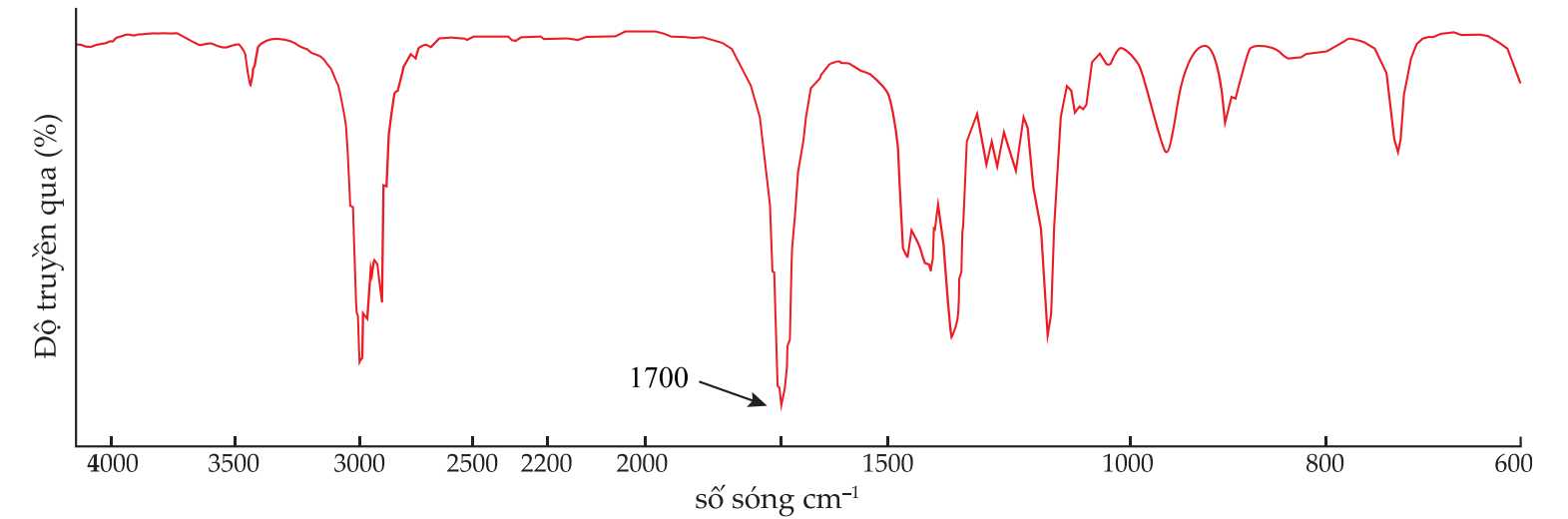

Tiến hành thực hiện phản ứng oxi hóa, để kiểm tra phản ứng oxi hóa có xảy ra hay không thì học sinh tách riêng từng chất trong hỗn hợp sản phẩm và tiến hành đo phổ hồng ngoại. Phổ hồng ngoại của một chất X được cho như sau:

Phân tích các phát biểu:
❌ a) Sai. Tín hiệu đặc trưng cho liên kết O-H (alcohol) là 3600 – 3200 cm-1; O-H trong carboxylic acid là 3300-2500 cm-1. Còn tín hiệu 1700 cm-1 là của liên kết C=O.
❌ b) Sai. Phổ hồng ngoại dùng để xác định các nhóm chức có thể có trong phân tử hợp chất hữu cơ.
✔️ c) Đúng. Tín hiệu đặc trưng cho liên kết O-H (alcohol) trong pentan-2-ol xuất hiện ở số sóng 3600 – 3200 cm-1.
✔️ d) Đúng. Dựa vào phổ hồng ngoại có thể thấy sự xuất hiện của tín hiệu nhóm C=O của sản phẩm chứng tỏ phản ứng oxi hoá đã xảy ra.
❌ a) Sai. Tín hiệu đặc trưng cho liên kết O-H (alcohol) là 3600 – 3200 cm-1; O-H trong carboxylic acid là 3300-2500 cm-1. Còn tín hiệu 1700 cm-1 là của liên kết C=O.
❌ b) Sai. Phổ hồng ngoại dùng để xác định các nhóm chức có thể có trong phân tử hợp chất hữu cơ.
✔️ c) Đúng. Tín hiệu đặc trưng cho liên kết O-H (alcohol) trong pentan-2-ol xuất hiện ở số sóng 3600 – 3200 cm-1.
✔️ d) Đúng. Dựa vào phổ hồng ngoại có thể thấy sự xuất hiện của tín hiệu nhóm C=O của sản phẩm chứng tỏ phản ứng oxi hoá đã xảy ra.
Câu 22 [702623]: Muối Fe(III) chloride có màu nâu - đen. Khi hoà tan trong nước thu được dung dịch có màu vàng và môi trường acid. Màu sắc và môi trường được giải thích do sự tạo thành phức chất và sự thuỷ phân của phức chất trong nước. Một trong những lí giải được đưa ra là
FeCl3 + 6H2O(l)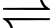 [Fe(OH2)6]3+(aq) + 3Cl–(aq) (1)
[Fe(OH2)6]3+(aq) + 3Cl–(aq) (1)
[Fe(H2O)6]3+(aq)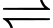 [Fe(OH2)5(OH)]2+(aq) + H+(aq) (2)
[Fe(OH2)5(OH)]2+(aq) + H+(aq) (2)
FeCl3 + 6H2O(l)
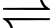 [Fe(OH2)6]3+(aq) + 3Cl–(aq) (1)
[Fe(OH2)6]3+(aq) + 3Cl–(aq) (1)[Fe(H2O)6]3+(aq)
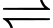 [Fe(OH2)5(OH)]2+(aq) + H+(aq) (2)
[Fe(OH2)5(OH)]2+(aq) + H+(aq) (2)
Phân tích các phát biểu:
- Trong phức chất [Fe(OH2)6]3+ ngoài liên kết cộng hoá trị phân cực giữa H và O giống nước thì còn có liên kết cho - nhận (liên kết phối trí) giữa ion trung tâm Fe3+ và phối tử H2O, mà cặp electron dùng chung bị lệch về phía Fe (biểu diễn như hình dưới). Vì thế nên lực hút electron của O với H sẽ mạnh hơn để nhường electron cho Fe.
⇒ Liên kết O-H trong phức chất [Fe(OH2)6]3+ phân cực hơn liên kết O-H trong phân tử H2O.
✔️ a) Đúng. Các phức chất [Fe(OH2)6]3+ và [Fe(OH2)5(OH)]2+ đều có 6 phối tử nên đều tạo thành các phức bát diện (8 mặt) như sau:
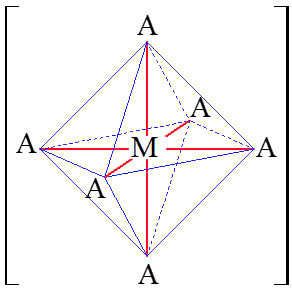
✔️ b) Đúng.
- Trong phân tử H2O chỉ có liên kết cộng hoá trị phân cực giữa H và O mà nguyên tố O có độ âm điện lớn nên sẽ hút cặp electron dùng chung về phía nó.
✔️ b) Đúng.
- Trong phức chất [Fe(OH2)6]3+ ngoài liên kết cộng hoá trị phân cực giữa H và O giống nước thì còn có liên kết cho - nhận (liên kết phối trí) giữa ion trung tâm Fe3+ và phối tử H2O, mà cặp electron dùng chung bị lệch về phía Fe (biểu diễn như hình dưới). Vì thế nên lực hút electron của O với H sẽ mạnh hơn để nhường electron cho Fe.
⇒ Liên kết O-H trong phức chất [Fe(OH2)6]3+ phân cực hơn liên kết O-H trong phân tử H2O.
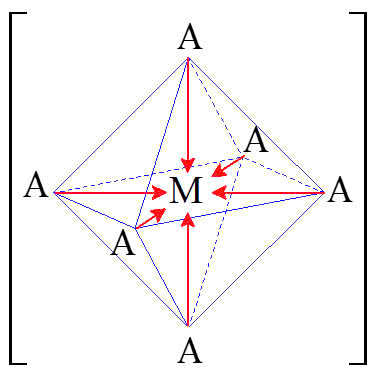
❌ c) Sai. Số oxi hoá của OH2 bằng 0 (phân tử nước trung hoà về điện) và số oxi hoá của OH là (-1)
Số oxi hoá của Fe trong phức [Fe(OH2)6]3+ là x: +3 = x + 0.6 ⇒ x = +3
Số oxi hoá của Fe trong phức [Fe(OH2)5(OH)]2+ là y: +2 = y + 0.5 + (-1) ⇒ y = +3
⟿ Trạng thái oxi hoá của Fe trong phức [Fe(OH2)6]3+ và [Fe(OH2)5(OH)]2+ là giống nhau.
✔️ d) Đúng. Khi thêm dung dịch HCl (H+) vào, cân bằng (2) chuyển dịch theo chiều làm giảm H+ là chiều nghịch.
PHẦN III. Thí sinh trả lời từ câu 1 đến câu 6.
Câu 23 [702624]: Để sản xuất được 1 triệu chiếc chảo gang có hàm lượng sắt là 95% thì cần dùng tối thiểu x tấn quặng magnetite chứa 80% Fe3O4. Giả sử mỗi chiếc chảo gang nặng 3,2 kg và trong quá trình sản xuất lượng sắt bị hao hụt là 8%. Giá trị của x là bao nhiêu? (làm tròn đến số nguyên)
Khối lượng sắt có trong 1 triệu chảo gang là: 1000000.3,2.95% = 3040000 kg = 3040 tấn
Lượng Fe thực tế là: mFe = 100% - 8% hao hụt = 92%
Sơ đồ phản ứng:
→ Khối lượng Fe3O4 trong quặng magnetite là: (tấn)
→ Khối lượng quặng magnetite là: (tấn)
⇒ Điền đáp án: 5704
Lượng Fe thực tế là: mFe = 100% - 8% hao hụt = 92%
Sơ đồ phản ứng:
→ Khối lượng Fe3O4 trong quặng magnetite là: (tấn)
→ Khối lượng quặng magnetite là: (tấn)
⇒ Điền đáp án: 5704
Câu 24 [702625]: Thủy phân hoàn toàn 1 mol chất béo X trong dung dịch NaOH dư, thu được 1 mol glycerol, 1 mol sodium stearate và 2 mol sodium oleate. Có bao nhiêu đồng phân cấu tạo chất béo X thỏa mãn?
Bộ khung gốc hydrocarbon của glycerol:
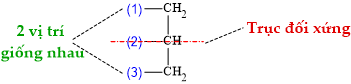
Quan sát ⇝ đính một gốc stearate và hai gốc oleate ta có 2 đồng phân sau:
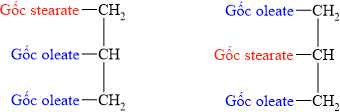
⇒ Điền đáp án: 2
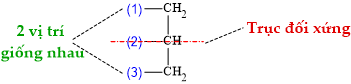
Quan sát ⇝ đính một gốc stearate và hai gốc oleate ta có 2 đồng phân sau:
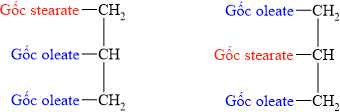
⇒ Điền đáp án: 2
Câu 25 [702626]: Để chứng minh cấu tạo saccharose chứa nhiều nhóm OH liền kề, có thể cho dung dịch saccharose phản ứng với kết tủa Cu(OH)2. Các bước tiến hành thí nghiệm như sau:
(1) Thêm vào ống nghiệm chứa kết tủa dung dịch saccharose 3%, lắc đều đến khi thu được dung dịch đồng nhất.
(2) Lọc lấy kết tủa Cu(OH)2 màu xanh rồi cho vào ống nghiệm.
(3) Đun nóng dung dịch chứa phức chất xanh thẫm trong ống nghiệm.
(4) Cho vào ống nghiệm khoảng dung dịch NaOH 10% và dung dịch CuSO4 5%, lắc đều.
Hãy sắp xếp các bước trên với trình tự dãy bốn số theo đúng thứ tự các bước cần tiến hành (ví dụ: 1234, 4213, ...).
(1) Thêm vào ống nghiệm chứa kết tủa dung dịch saccharose 3%, lắc đều đến khi thu được dung dịch đồng nhất.
(2) Lọc lấy kết tủa Cu(OH)2 màu xanh rồi cho vào ống nghiệm.
(3) Đun nóng dung dịch chứa phức chất xanh thẫm trong ống nghiệm.
(4) Cho vào ống nghiệm khoảng dung dịch NaOH 10% và dung dịch CuSO4 5%, lắc đều.
Hãy sắp xếp các bước trên với trình tự dãy bốn số theo đúng thứ tự các bước cần tiến hành (ví dụ: 1234, 4213, ...).
Thí nghiệm: Chứng minh cấu tạo của sacchorose chứa nhiều nhóm OH liền kề bằng cách cho dung dịch saccharose phản ứng với kết tủa Cu(OH)2. Các bước thực hiện như sau:
Bước 1: Cho vào ống nghiệm khoảng 2 ml dung dịch NaOH 10% và 0,5 ml dung dịch CuSO4 5%, lắc đều → ứng với (4).
Bước 2: Lọc lấy kết tủa Cu(OH)2 màu xanh rồi cho vào ống nghiệm → ứng với (2).
Bước 3: Thêm vào ống nghiệm chứa kết tủa dung dịch saccharose 3%, lắc đều đến khi thu được dung dịch đồng nhất → ứng với (1).
Bước 4: Đun nóng dung dịch chứa phức chất xanh thẫm trong ống nghiệm → ứng với (1)
⇒ Điền đáp án: 4213
Bước 1: Cho vào ống nghiệm khoảng 2 ml dung dịch NaOH 10% và 0,5 ml dung dịch CuSO4 5%, lắc đều → ứng với (4).
Bước 2: Lọc lấy kết tủa Cu(OH)2 màu xanh rồi cho vào ống nghiệm → ứng với (2).
Bước 3: Thêm vào ống nghiệm chứa kết tủa dung dịch saccharose 3%, lắc đều đến khi thu được dung dịch đồng nhất → ứng với (1).
Bước 4: Đun nóng dung dịch chứa phức chất xanh thẫm trong ống nghiệm → ứng với (1)
⇒ Điền đáp án: 4213
Câu 26 [702627]: Hồng cầu là một loại protein trong máu, có chức năng vận chuyển oxygen từ phổi đến các mô trong cơ thể. Biết hồng cầu chứa 0,33% iron (Fe) theo khối lượng, phân tử khối của hồng cầu là 67 878 g/mol. Có bao nhiêu nguyên tử iron trong một phân tử hồng cầu? (làm tròn đến chữ số nguyên)
Tổng phân tử khối của Fe có trong hồng cầu là: 67878 x 0,33% = 224 (gam.mol-1)
Số nguyên tử Fe có trong 1 phân tử hồng cầu là: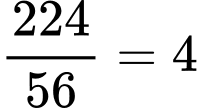 (nguyên tử)
(nguyên tử)
⇒ Điền đáp án: 4
Số nguyên tử Fe có trong 1 phân tử hồng cầu là:
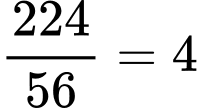 (nguyên tử)
(nguyên tử)⇒ Điền đáp án: 4
Câu 27 [702628]: Nescafe đã sản xuất thành công lon cafe tự làm nóng. Để làm nóng cafe, chỉ cần ấn nút (trên lon) để trộn nguyên liệu gồm một dung dịch KOH hoặc NaOH rất loãng và CaO; 210 mL cafe trong lon sẽ được hâm nóng đến khoảng 40°C. Giả sử nhiệt dung riêng của cafe là 4,2 J/g.K (nhiệt dung riêng là nhiệt lượng cần cung cấp để 1 gam chất tăng lên 1oC). Biết enthalpy tiêu chuẩn của các chất được cho trong bảng sau:
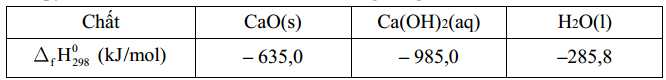
Nhiệt tỏa ra từ phản ứng thất thoát vào sản phẩm, vỏ hộp và môi trường là 20%. Cần cung cấp bao nhiêu gam CaO để làm nóng 210 mL cafe từ 25oC đến 40oC (d = 1,0 g/ml) (làm tròn đến phần hàng phần mười)?

Nhiệt tỏa ra từ phản ứng thất thoát vào sản phẩm, vỏ hộp và môi trường là 20%. Cần cung cấp bao nhiêu gam CaO để làm nóng 210 mL cafe từ 25oC đến 40oC (d = 1,0 g/ml) (làm tròn đến phần hàng phần mười)?
CaO(s) + H2O(l) ⟶ Ca(OH)2(aq)
Biến thiên enthalpy của phản ứng trên là 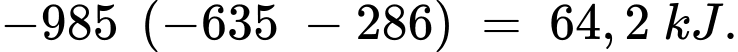
Nhiệt cà phê hấp thụ để tăng từ 25oC lên 40oC cần 4,2.210.(40 – 25) = 13230 J = 13,23 kJ
Vậy khối lượng CaO cần cung cấp là
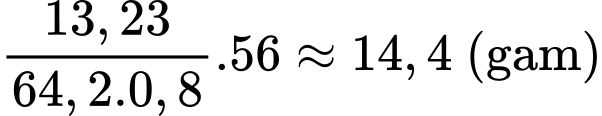
⇒ Điền đáp án: 14,4
Câu 28 [702629]: Viên nén chứa potassium permanganate KMnO4, được hòa tan trong nước tạo thành dung dịch sát trùng để điều trị các bệnh về da. Để kiểm tra hàm lượng KMnO4 có trong một viên thuốc, tiến hành quy trình như sau: Hòa tan năm viên thuốc trong nước cất để tạo thành 100,0 mL dung dịch, thêm dung dịch KMnO4 vào burete. Thêm 25,0 mL dung dịch Na2C2O4 0,200 M vào bình nón và làm ấm, thêm tiếp dung dịch H2SO4 2 M vào bình. Phương trình phản ứng trong phép chuẩn độ như sau:
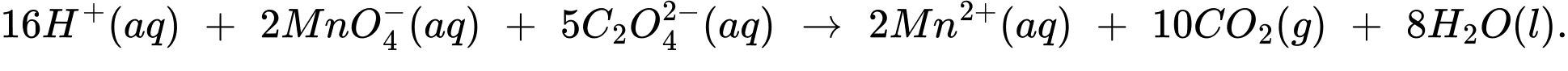
Kết quả trung bình của quá trình chuẩn độ thấy tiêu tốn 16,85 mL dung dịch KMnO4. Tính khối lượng của KMnO4 có trong một viên thuốc (làm tròn kết quả thu được đến phần trăm).
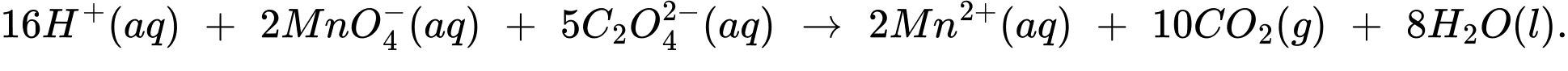
Kết quả trung bình của quá trình chuẩn độ thấy tiêu tốn 16,85 mL dung dịch KMnO4. Tính khối lượng của KMnO4 có trong một viên thuốc (làm tròn kết quả thu được đến phần trăm).
Đổi 25ml = 0,025 L; 16,85 ml = 0,01685 L; 100 ml = 0,1 L
16H+(aq) + 2MnO4-(aq) + 5C2O42-(aq) ⟶ 2Mn2+(aq) + 10CO2(g) + 8H2O(l)
Số mol của dung dịch Na2C2O4 phản ứng là: 0,025 . 0,2 = 0,005 (mol)
Từ PTHH số mol KMnO4 phản ứng là: 0,002 mol
Nồng độ của KMnO4 là: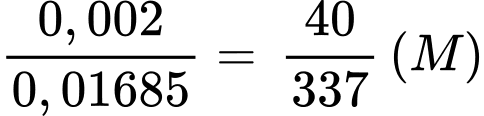
Khối lượng của KMnO4 trong 100ml dung dịch là: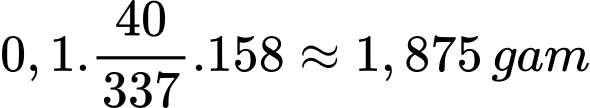
Khối lượng của KMnO4 trong 1 viên thuốc là: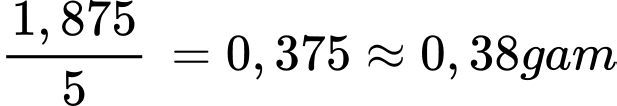
⇒ Điền đáp án: 0,38
16H+(aq) + 2MnO4-(aq) + 5C2O42-(aq) ⟶ 2Mn2+(aq) + 10CO2(g) + 8H2O(l)
Số mol của dung dịch Na2C2O4 phản ứng là: 0,025 . 0,2 = 0,005 (mol)
Từ PTHH số mol KMnO4 phản ứng là: 0,002 mol
Nồng độ của KMnO4 là:
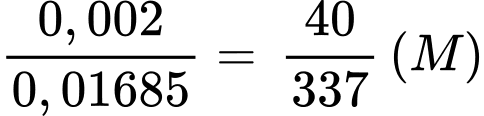
Khối lượng của KMnO4 trong 100ml dung dịch là:
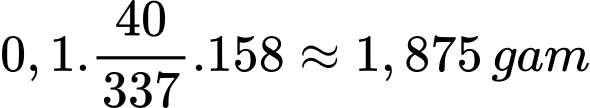
Khối lượng của KMnO4 trong 1 viên thuốc là:
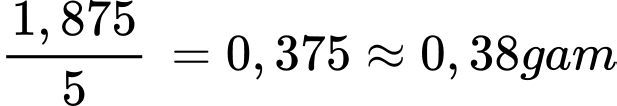
⇒ Điền đáp án: 0,38