PHẦN I. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
Câu 1 [705569]: Ion kim loại ứng với thế điện cực chuẩn …(1)… hơn sẽ được điện phân trước ở …(2)… Nội dung phù hợp trong ô trống (1), (2) lần lượt là
A, dương, cực dương.
B, dương, cực âm.
C, âm, cực âm.
D, âm, cực dương.
Ion kim loại ứng với thế điện cực chuẩn dương hơn sẽ được điện phân trước ở cực âm.
Giải thích:
- Thế điện cực chuẩn của một cặp oxi hoá - khử thể hiện khả năng nhận electron (bị khử) nên:
+ Ion có thế điện cực chuẩn (Eo) dương hơn sẽ dễ bị khử (dễ nhận e hơn) để hình thành kim loại tự do.
+ Ion có thế điện cực chuẩn (Eo) âm hơn sẽ khó bị khử hơn (thường ít tham gia vào quá trình điện phân nếu có mặt của các ion có Eo dương hơn)
⟶ Ưu tiên điện phân ion có thế điện cực chuẩn dương hơn trước.
- Quá trình nhận electron là quá trình khử, xảy ra ở cathode (cực âm).
⇒ Chọn đáp án B Đáp án: B
Giải thích:
- Thế điện cực chuẩn của một cặp oxi hoá - khử thể hiện khả năng nhận electron (bị khử) nên:
+ Ion có thế điện cực chuẩn (Eo) dương hơn sẽ dễ bị khử (dễ nhận e hơn) để hình thành kim loại tự do.
+ Ion có thế điện cực chuẩn (Eo) âm hơn sẽ khó bị khử hơn (thường ít tham gia vào quá trình điện phân nếu có mặt của các ion có Eo dương hơn)
⟶ Ưu tiên điện phân ion có thế điện cực chuẩn dương hơn trước.
- Quá trình nhận electron là quá trình khử, xảy ra ở cathode (cực âm).
⇒ Chọn đáp án B Đáp án: B
Câu 2 [59275]: Trong thực tế, cách nào sau đây không được dùng để bảo vệ kim loại sắt khỏi bị ăn mòn?
A, Gắn kim loại đồng với sắt.
B, Tráng kẽm lên bề mặt sắt.
C, Phủ một lớp sơn lên bề mặt sắt.
D, Tráng thiếc lên bề mặt sắt.
HD: ☆ Phương pháp bảo vệ bề mặt
Nguyên tắc: Cách li kim loại với môi trường bằng một lớp phân cách mỏng, bền vững.
Biện pháp: ta có thể: Bôi dầu mỡ, sơn, mạ, tráng men,...
Sắt tây là sắt được tráng thiếc (Sn), được sử dụng làm vỏ hộp trong ngành thực phẩm.
Tôn là sắt được tráng kẽm, được sử dụng trong ngành vật liệu xây dựng.
Các đồ vật bằng sắt thường được mạ bằng niken hay crom.
☆ Phương pháp điện hóa
Nguyên tắc: Trong quá trình ăn mòn điện hóa, kim loại mạnh hơn bị ăn mòn.
Biện pháp: Nối kim loại cần bảo vệ với kim loại hoạt động mạnh hơn để kim loại đó bị ăn mòn thay.
Để bảo vệ vỏ tàu biển bằng thép, những tấm kẽm đã được gắn vào mặt ngoài vỏ tàu (phần chìm dưới nước) để Zn bị ăn mòn, còn thép được bảo vệ.
⇒ Chọn đáp án A Đáp án: A
Nguyên tắc: Cách li kim loại với môi trường bằng một lớp phân cách mỏng, bền vững.
Biện pháp: ta có thể: Bôi dầu mỡ, sơn, mạ, tráng men,...
Sắt tây là sắt được tráng thiếc (Sn), được sử dụng làm vỏ hộp trong ngành thực phẩm.
Tôn là sắt được tráng kẽm, được sử dụng trong ngành vật liệu xây dựng.
Các đồ vật bằng sắt thường được mạ bằng niken hay crom.
☆ Phương pháp điện hóa
Nguyên tắc: Trong quá trình ăn mòn điện hóa, kim loại mạnh hơn bị ăn mòn.
Biện pháp: Nối kim loại cần bảo vệ với kim loại hoạt động mạnh hơn để kim loại đó bị ăn mòn thay.
Để bảo vệ vỏ tàu biển bằng thép, những tấm kẽm đã được gắn vào mặt ngoài vỏ tàu (phần chìm dưới nước) để Zn bị ăn mòn, còn thép được bảo vệ.
⇒ Chọn đáp án A Đáp án: A
Câu 3 [310503]: Vật liệu polymer nào sau đây có cấu trúc mạng lưới không gian?
A, Cao su thiên nhiên.
B, Cao su lưu hóa.
C, Cao su buna-S.
D, Cao su buna-N.
Phân tích các đáp án:
❌ A. Cao su thiên nhiên: Là polyisopren, có cấu trúc mạch thẳng hoặc mạch nhánh, không phải mạng lưới không gian.
✔️ B. Cao su lưu hóa: Là cao su thiên nhiên được lưu hóa bằng lưu huỳnh (S), tạo cầu nối -S-S- giữa các mạch polymer, hình thành cấu trúc mạng lưới không gian.
❌ C,D. Cao su buna-S (C) và Cao su buna-N: Là các cao su tổng hợp có cấu trúc mạch thẳng, không phải mạng lưới không gian.
⇒ Chọn đáp án B Đáp án: B
❌ A. Cao su thiên nhiên: Là polyisopren, có cấu trúc mạch thẳng hoặc mạch nhánh, không phải mạng lưới không gian.
✔️ B. Cao su lưu hóa: Là cao su thiên nhiên được lưu hóa bằng lưu huỳnh (S), tạo cầu nối -S-S- giữa các mạch polymer, hình thành cấu trúc mạng lưới không gian.
❌ C,D. Cao su buna-S (C) và Cao su buna-N: Là các cao su tổng hợp có cấu trúc mạch thẳng, không phải mạng lưới không gian.
⇒ Chọn đáp án B Đáp án: B
Câu 4 [906850]: Thực hiện các thí nghiệm sau:
(a) Cho hỗn hợp Na2O và Al2O3 (tỉ lệ mol 1 : 1) vào nước (dư).
(b) Cho hỗn hợp Cu và Fe3O4 (tỉ lệ mol tương ứng 2 : 1) vào dung dịch HCl (dư).
(c) Cho hỗn hợp Ba và NaHCO3 (tỉ lệ mol 1 : 1) vào nước (dư).
(d) Cho hỗn hợp Cu và NaNO3 (tỉ lệ mol tương ứng 1 : 2) vào dung dịch HCl (dư).
(e) Cho hỗn hợp BaCO3 và KHSO4 vào nước (dư).
Khi phản ứng trong các thí nghiệm trên kết thúc, có bao nhiêu thí nghiệm không thu được chất rắn?
(a) Cho hỗn hợp Na2O và Al2O3 (tỉ lệ mol 1 : 1) vào nước (dư).
(b) Cho hỗn hợp Cu và Fe3O4 (tỉ lệ mol tương ứng 2 : 1) vào dung dịch HCl (dư).
(c) Cho hỗn hợp Ba và NaHCO3 (tỉ lệ mol 1 : 1) vào nước (dư).
(d) Cho hỗn hợp Cu và NaNO3 (tỉ lệ mol tương ứng 1 : 2) vào dung dịch HCl (dư).
(e) Cho hỗn hợp BaCO3 và KHSO4 vào nước (dư).
Khi phản ứng trong các thí nghiệm trên kết thúc, có bao nhiêu thí nghiệm không thu được chất rắn?
A, 1.
B, 2.
C, 3.
D, 4.
Các thí nghiệm xảy ra như sau:
❌ (a) 1 mol Na2O tạo thành 2 mol NaOH sau đó hòa tan tối đa 1 mol Al2O3 tạo dung dịch trong suốt.
Na2O + Al2O3 → 2NaAlO2
✔️ (b) Cu + Fe3O4 + 8HCl → CuCl2 + 3FeCl2 + 4H2O
Cu vẫn còn dư.
✔️ (c) Hòa tan Ba vào dung dịch NaHCO3 thu được kết tủa BaCO3.
Ba + 2H2O → Ba(OH)2 + H2
Ba(OH)2 + NaHCO3 → BaCO3 + NaOH + H2O
❌ (d) Sản phẩm thu được gồm dung dịch muối, khí NO và nước.
3Cu + 8H+ + 2NO3 → 3Cu2+ + 2NO + 4H2O
✔️ (e) Cho hỗn hợp BaCO3 và KHSO4 vào nước thu được kết tủa BaSO4.
BaCO3 + 2KHSO4 → BaSO4 + K2SO4 + CO2 + H2O
Vậy các thí nghiệm không thu được chất rắn là (a) và (d).
⇒ Chọn đáp án B Đáp án: B
❌ (a) 1 mol Na2O tạo thành 2 mol NaOH sau đó hòa tan tối đa 1 mol Al2O3 tạo dung dịch trong suốt.
Na2O + Al2O3 → 2NaAlO2
✔️ (b) Cu + Fe3O4 + 8HCl → CuCl2 + 3FeCl2 + 4H2O
Cu vẫn còn dư.
✔️ (c) Hòa tan Ba vào dung dịch NaHCO3 thu được kết tủa BaCO3.
Ba + 2H2O → Ba(OH)2 + H2
Ba(OH)2 + NaHCO3 → BaCO3 + NaOH + H2O
❌ (d) Sản phẩm thu được gồm dung dịch muối, khí NO và nước.
3Cu + 8H+ + 2NO3 → 3Cu2+ + 2NO + 4H2O
✔️ (e) Cho hỗn hợp BaCO3 và KHSO4 vào nước thu được kết tủa BaSO4.
BaCO3 + 2KHSO4 → BaSO4 + K2SO4 + CO2 + H2O
Vậy các thí nghiệm không thu được chất rắn là (a) và (d).
⇒ Chọn đáp án B Đáp án: B
Câu 5 [705570]: Số oxi hóa trung bình của nguyên tố được đánh dấu (in đậm) trong ion nào sau đây có giá trị lớn nhất?
A, 

B, 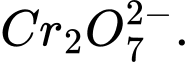
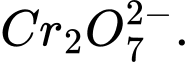
C, 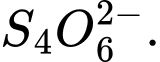
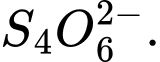
D, 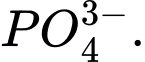
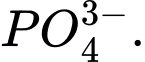
Gọi số oxi hoá của các nguyên tố được in đậm ở từng ion là a, b, c, d. Tổng số oxi hoá của các ion phải bằng điện tích của ion đó nên ta có:
✔️Đúng.A.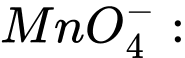 a + 4 × (−2) = −1 ⇔ a − 8 = −1 ⇔ a = +7 ⟶ Số oxi hóa trung bình của Mn là +7.
a + 4 × (−2) = −1 ⇔ a − 8 = −1 ⇔ a = +7 ⟶ Số oxi hóa trung bình của Mn là +7.
❌Sai.B.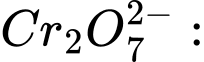 2b + 7 × (−2) = −2 ⇔ 2b − 14 = −2 ⇔ 2b = 12 ⇔ b = +6 ⟶ Số oxi hóa trung bình của Cr là +6.
2b + 7 × (−2) = −2 ⇔ 2b − 14 = −2 ⇔ 2b = 12 ⇔ b = +6 ⟶ Số oxi hóa trung bình của Cr là +6.
❌Sai.C.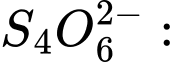 c = [(2×5) + (2×0)] ÷ 4 = 10 ÷ 4 = +2,5 ⟶ Số oxi hóa trung bình của S là +2,5.
c = [(2×5) + (2×0)] ÷ 4 = 10 ÷ 4 = +2,5 ⟶ Số oxi hóa trung bình của S là +2,5.
❌Sai.D.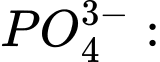 d + 4 × (−2) = −3 ⇔ d − 8 = −3 ⇔ d = +5 ⟶ Số oxi hóa trung bình của P là +5.
d + 4 × (−2) = −3 ⇔ d − 8 = −3 ⇔ d = +5 ⟶ Số oxi hóa trung bình của P là +5.
Vậy số oxi hóa trung bình của nguyên tố được đánh dấu (in đậm) trong ion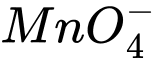 có giá trị lớn nhất.
có giá trị lớn nhất.
⇒ Chọn đáp án A Đáp án: A
✔️Đúng.A.
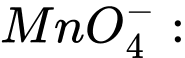 a + 4 × (−2) = −1 ⇔ a − 8 = −1 ⇔ a = +7 ⟶ Số oxi hóa trung bình của Mn là +7.
a + 4 × (−2) = −1 ⇔ a − 8 = −1 ⇔ a = +7 ⟶ Số oxi hóa trung bình của Mn là +7.❌Sai.B.
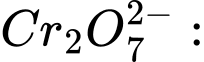 2b + 7 × (−2) = −2 ⇔ 2b − 14 = −2 ⇔ 2b = 12 ⇔ b = +6 ⟶ Số oxi hóa trung bình của Cr là +6.
2b + 7 × (−2) = −2 ⇔ 2b − 14 = −2 ⇔ 2b = 12 ⇔ b = +6 ⟶ Số oxi hóa trung bình của Cr là +6.❌Sai.C.
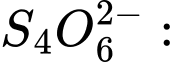 c = [(2×5) + (2×0)] ÷ 4 = 10 ÷ 4 = +2,5 ⟶ Số oxi hóa trung bình của S là +2,5.
c = [(2×5) + (2×0)] ÷ 4 = 10 ÷ 4 = +2,5 ⟶ Số oxi hóa trung bình của S là +2,5.❌Sai.D.
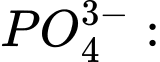 d + 4 × (−2) = −3 ⇔ d − 8 = −3 ⇔ d = +5 ⟶ Số oxi hóa trung bình của P là +5.
d + 4 × (−2) = −3 ⇔ d − 8 = −3 ⇔ d = +5 ⟶ Số oxi hóa trung bình của P là +5.Vậy số oxi hóa trung bình của nguyên tố được đánh dấu (in đậm) trong ion
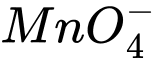 có giá trị lớn nhất.
có giá trị lớn nhất.⇒ Chọn đáp án A Đáp án: A
Câu 6 [560615]: Kim loại nào sau đây có khối lượng riêng nhỏ nhất?
A, Fe.
B, Al.
C, Li.
D, Mg.
Khối lượng riêng nhỏ nhất: Lithium (Li).
⇒ Chọn đáp án C Đáp án: C
⇒ Chọn đáp án C Đáp án: C
Câu 7 [792356]: Cho mẩu sodium vào ống nghiệm đựng 3 mL chất lỏng X, thấy sodium tan dần và có khí thoát ra. Chất X là
A, pentane.
B, ethanol.
C, hexane.
D, benzene.
2CH3CH2OH + 2Na → 2CH3CH2ONa + H2
Đáp án B Đáp án: B
Đáp án B Đáp án: B
Câu 8 [308715]: Dung dịch chất nào sau đây làm quỳ tím chuyển màu xanh?
A, Aniline.
B, Glycine.
C, Valine.
D, Methylamine.
+) 3 dung dịch Aniline, Glycine, Valine là các amino acid mà trong phân tử có 1 nhóm amino và 1 nhóm carboxyl nên không làm chuyển màu quỳ tím.
+) Methylamine(CH3NH2) mang tính chất của một base yếu nên sẽ làm quỳ tím chuyển màu xanh.
⇒ Chọn đáp án D Đáp án: D
+) Methylamine(CH3NH2) mang tính chất của một base yếu nên sẽ làm quỳ tím chuyển màu xanh.
⇒ Chọn đáp án D Đáp án: D
Câu 9 [705571]: Khi một chất lỏng dễ cháy (ví dụ: xăng) bốc cháy, chất thực sự bốc cháy là phần hơi được tạo ra từ phần chất lỏng. Nếu nồng độ hơi trong không khí phía trên chất lỏng vượt quá một mức nhất định, hơi sẽ bốc cháy nếu tiếp xúc với tia lửa hoặc nguồn đánh lửa khác. Sau khi bốc cháy, nhiệt giải phóng có khả năng gây ra sự bốc hơi thêm của chất lỏng và đám cháy kết quả có thể tiếp tục cho đến khi tất cả các vật liệu dễ cháy đã được tiêu thụ. Cách nào sau đây không thể được sử dụng để đảm bảo an toàn khu vực cất trữ xăng?
A, Không để tia lửa hoặc nguồn đánh lửa ở gần khu vực cất trữ xăng.
B, Cất trữ trong không gian kín, cô lập với không khí bên ngoài.
C, Làm mát bằng nước ở các khu vực xung quanh cất trữ xăng.
D, Cất trữ xăng với các chất hữu cơ khác để hạn chế sự bay hơi của xăng.
✔️A. Không để tia lửa hoặc nguồn đánh lửa gần khu vực cất trữ xăng là một biện pháp an toàn quan trọng. Hơi xăng dễ cháy khi tiếp xúc với nguồn lửa, nên cần tránh xa để ngăn ngừa nguy cơ cháy nổ.
✔️B. Cất trữ trong không gian kín, cô lập với không khí bên ngoài giúp giảm thiểu sự bay hơi của xăng, tránh tạo môi trường dễ cháy trong khu vực cất trữ
✔️C. Làm mát bằng nước ở các khu vực xung quanh giúp giảm nhiệt độ, ngăn hơi xăng đạt đến giới hạn nồng độ cháy và hạn chế nguy cơ bốc cháy.
❌D. Cất trữ xăng với các chất hữu cơ khác là không an toàn vì có thể tạo phản ứng hóa học nguy hiểm hoặc làm tăng nguy cơ cháy nổ. Xăng nên được cất trữ riêng biệt trong thùng chứa chuyên dụng.
Chọn đáp án D Đáp án: D
✔️B. Cất trữ trong không gian kín, cô lập với không khí bên ngoài giúp giảm thiểu sự bay hơi của xăng, tránh tạo môi trường dễ cháy trong khu vực cất trữ
✔️C. Làm mát bằng nước ở các khu vực xung quanh giúp giảm nhiệt độ, ngăn hơi xăng đạt đến giới hạn nồng độ cháy và hạn chế nguy cơ bốc cháy.
❌D. Cất trữ xăng với các chất hữu cơ khác là không an toàn vì có thể tạo phản ứng hóa học nguy hiểm hoặc làm tăng nguy cơ cháy nổ. Xăng nên được cất trữ riêng biệt trong thùng chứa chuyên dụng.
Chọn đáp án D Đáp án: D
Câu 10 [705572]: Phát biểu nào sau đây là không đúng khi nói về ammonia?
A, Trong công nghiệp, ammonia thường được sử dụng với vai trò chất làm lạnh (chất sinh hàn).
B, Do có hàm lượng nitrogen cao (82,35% theo khối lượng) nên ammonia được sử dụng làm phân đạm rất hiệu quả.
C, Phần lớn ammonia được dùng phản ứng với acid để sản xuất các loại phân đạm.
D, Quá trình tổng hợp ammonia từ nitrogen và hydrogen là quá trình thuận nghịch nên không thể đạt hiệu suất 100%.
✔️A.NH3 được sử dụng làm môi chất lạnh trong hệ thống làm lạnh công nghiệp (đặc biệt trong các kho lạnh, nhà máy chế biến thực phẩm).
❌B. Phân đạm được cung cấp ion NH4+ và NO3-, không cung cấp trực tiếp NH3
✔️C.Ammonia không phải là phân bón trực tiếp, nhưng nó là nguyên liệu quan trọng để sản xuất các loại phân đạm.
✔️D.Do phản ứng thuận nghịch, không thể đạt hiệu suất 100% vì luôn có một phần NH3 bị phân hủy ngược.
Chọn đáp án B Đáp án: B
❌B. Phân đạm được cung cấp ion NH4+ và NO3-, không cung cấp trực tiếp NH3
✔️C.Ammonia không phải là phân bón trực tiếp, nhưng nó là nguyên liệu quan trọng để sản xuất các loại phân đạm.
✔️D.Do phản ứng thuận nghịch, không thể đạt hiệu suất 100% vì luôn có một phần NH3 bị phân hủy ngược.
Chọn đáp án B Đáp án: B
Câu 11 [308763]: Đốt cháy hoàn toàn chất hữu cơ nào sau đây thu được sản phẩm có chứa N2?
A, Cellulose.
B, Tinh bột.
C, Protein.
D, Chất béo.
- Cellulose và tinh bột (C6H10O5)n và chất béo (RCOO)3C3H5 với R là các acid béo đều chỉ được tạo thành từ C, H và O nên khi đốt cháy sản phẩm sẽ không chứa N2.
- Protein là đại phân tử polypeptide nên có liên kết CO-NH => Đốt cháy tạo N2.
⟹ Chọn đáp án C Đáp án: C
- Protein là đại phân tử polypeptide nên có liên kết CO-NH => Đốt cháy tạo N2.
⟹ Chọn đáp án C Đáp án: C
Câu 12 [308344]: Saccharose là một loại carbohydrate có trong đường mía. Saccharose thuộc loại
A, monosaccharide.
B, polysaccharide.
C, disaccharide.
D, lipid.
HD: Xem lại bài học về phân loại hợp chất carbohydrate trong chương trình:
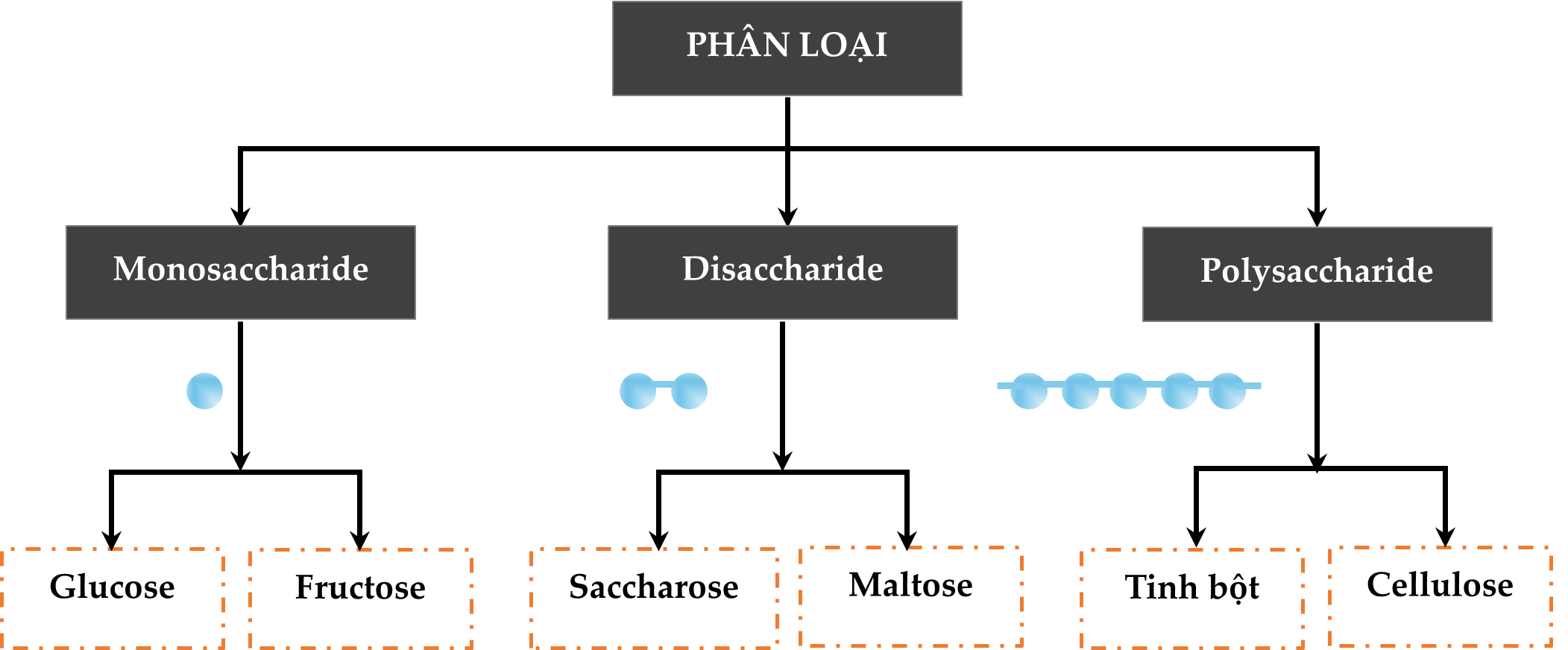
⇒ Saccharose thuộc loại disaccharide. Đáp án: C

⇒ Saccharose thuộc loại disaccharide. Đáp án: C
Câu 13 [705573]: Alkene propane CH2=CHCH3 và HBr đều có cấu tạo bất đối xứng nên phản ứng xảy ra tạo hai sản phẩm khác nhau:
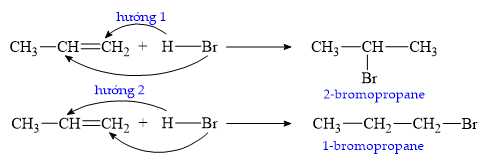
Trong cơ chế của phản ứng, sản phẩm 2-bromopropane (hướng 1) được tạo ra do hình thành carbocation nào sau đây?

Trong cơ chế của phản ứng, sản phẩm 2-bromopropane (hướng 1) được tạo ra do hình thành carbocation nào sau đây?
A, 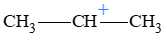
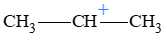
B, 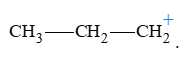
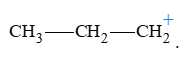
C, 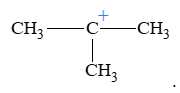

D, 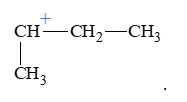
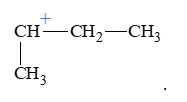
Sản phẩm 2-bromopropane (hướng 1) được tạo ra do hình thành carbocation bậc 2 theo quy tắc Markovnikov: Nguyên tử H+ của HBr sẽ ưu tiên cộng vào carbon có nhiều hydrogen hơn và Br - sẽ tấn công vào vị trí còn lại.
✔️A.CH3-CH+-CH3 → Đây là carbocation bậc 2, phù hợp với cơ chế phản ứng
❌B.CH3-CH2-CH2+ → Đây là carbocation bậc 1, kém ổn định hơn
❌C và D. Đây là các carbocation bậc 3 hoặc có cấu trúc khác, không phù hợp với propene.
Chọn đáp án A Đáp án: A
✔️A.CH3-CH+-CH3 → Đây là carbocation bậc 2, phù hợp với cơ chế phản ứng
❌B.CH3-CH2-CH2+ → Đây là carbocation bậc 1, kém ổn định hơn
❌C và D. Đây là các carbocation bậc 3 hoặc có cấu trúc khác, không phù hợp với propene.
Chọn đáp án A Đáp án: A
Câu 14 [304843]: Khi đun nóng chất X có công thức phân tử C3H6O2 với dung dịch NaOH thu được CH3COONa. Công thức cấu tạo của X là
A, C2H5COOH.
B, CH3COOCH3.
C, CH3COOC2H5.
D, HCOOC2H5.
Từ giả thiết ta có sơ đồ phản ứng sau:
X (C3H6O2) + NaOH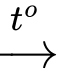 CH3COONa + Y.
CH3COONa + Y.
Bảo toàn nguyên tố suy ra công thức phân tử Y là CH4OH.
⇒ Cấu tạo Y là CH3OH (methyl alcohol) ⇒ X là Ester CH3COOCH3.
⟹ Tên gọi methyl acetate
⟹ Chọn đáp án B. Đáp án: B
X (C3H6O2) + NaOH
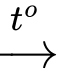 CH3COONa + Y.
CH3COONa + Y.Bảo toàn nguyên tố suy ra công thức phân tử Y là CH4OH.
⇒ Cấu tạo Y là CH3OH (methyl alcohol) ⇒ X là Ester CH3COOCH3.
⟹ Tên gọi methyl acetate
⟹ Chọn đáp án B. Đáp án: B
Câu 15 [705574]: Chất giặt rửa có thành phần không phải muối của …(1)…, nhưng có tính chất …(2)… như xà phòng. Nội dung phù hợp trong ô trống (1), (2) lần lượt là
A, hydrocarbon, không tan trong nước.
B, ester, bay hơi nhanh.
C, acid béo, giặt rửa.
D, alcohol, giặt rửa.
Xà phòng là muối của acid béo (thường là muối Na hoặc K của acid béo).
Các chất giặt rửa tổng hợp có thể không phải là muối của acid béo, nhưng chúng vẫn có tính chất giặt rửa giống như xà phòng.
⟹ Chất giặt rửa có thành phần không phải muối của acid béo , nhưng có tính chất giặt rửa như xà phòng.
⟹Chọn đáp án C Đáp án: C
Các chất giặt rửa tổng hợp có thể không phải là muối của acid béo, nhưng chúng vẫn có tính chất giặt rửa giống như xà phòng.
⟹ Chất giặt rửa có thành phần không phải muối của acid béo , nhưng có tính chất giặt rửa như xà phòng.
⟹Chọn đáp án C Đáp án: C
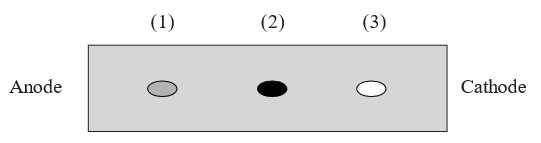
Câu 16 [705575]: Kết quả phân tích nguyên tố của một α-amino acid X như sau: % C = 46,60%; % H = 8,74%; % N = 13,59% (về khối lượng); còn lại là oxygen. Bằng phổ khối lượng (MS), xác định được phân tử khối của X bằng 103. Tính chất điện di của amino acid X được nghiên cứu và amino acid X được đặt ở vị trí trung tâm của điện trường.
Cho các phát biểu sau:
(a) Công thức phân tử của X là C4H9O2N.
(b) Có 2 đồng phân cấu tạo ứng với công thức phân tử của X.
(c) Amino acid X thể hiện tính base trong môi trường dung dịch CH3COOH.
(d) pH được điều chỉnh để X tồn tại dạng ion lưỡng cực, vị trí (3) phù hợp với sự di chuyển của X trong điện trường.
Các phát biểu đúng là

Cho các phát biểu sau:
(a) Công thức phân tử của X là C4H9O2N.
(b) Có 2 đồng phân cấu tạo ứng với công thức phân tử của X.
(c) Amino acid X thể hiện tính base trong môi trường dung dịch CH3COOH.
(d) pH được điều chỉnh để X tồn tại dạng ion lưỡng cực, vị trí (3) phù hợp với sự di chuyển của X trong điện trường.
Các phát biểu đúng là
A, (a), (b).
B, (a), (c).
C, (a), (b), (c).
D, (a), (c), (d).
Gọi công thức phân tử của X là CxHyOzNt
Ta có :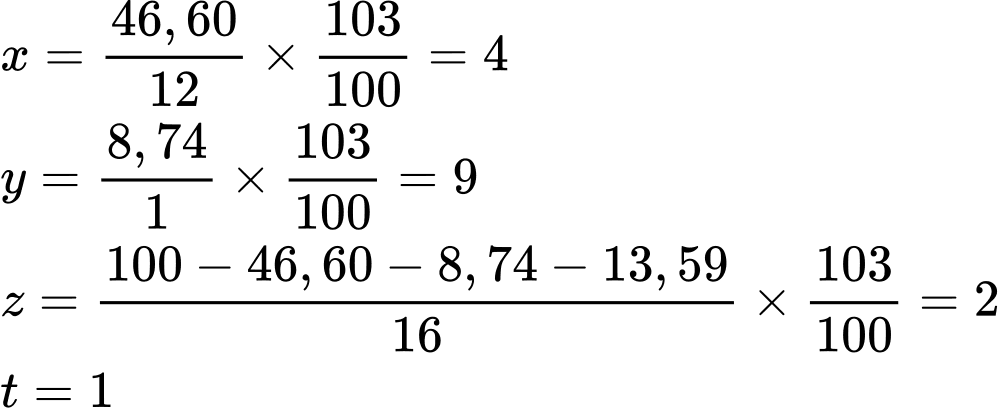
Công thức của X là C4H9O2N.
Phân tích các đáp án:
✔️(a). Đúng. Công thức của X là C4H9O2N.
✔️(b). Đúng. X có 2 đồng phân cấu tạo
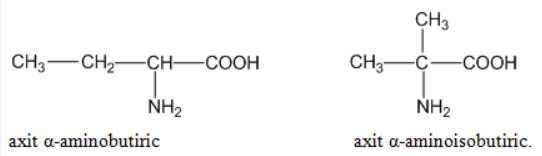
✔️(c). Đúng. Amino acid có tính lưỡng tính, khi trong môi trường có CH3COOH ( acid ) thì X đóng vai trò base.
❌(d). pH được điều chỉnh để X tồn tại dạng ion lưỡng cực nên không có sự di chuyển.
Các đáp án đúng: a,b,c
Chọn đáp án C Đáp án: C
Ta có :
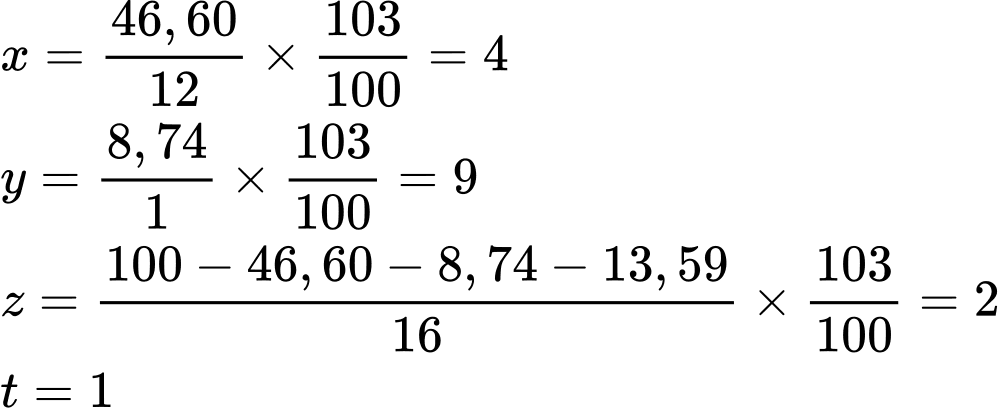
Công thức của X là C4H9O2N.
Phân tích các đáp án:
✔️(a). Đúng. Công thức của X là C4H9O2N.
✔️(b). Đúng. X có 2 đồng phân cấu tạo
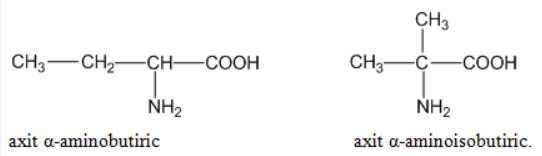
✔️(c). Đúng. Amino acid có tính lưỡng tính, khi trong môi trường có CH3COOH ( acid ) thì X đóng vai trò base.
❌(d). pH được điều chỉnh để X tồn tại dạng ion lưỡng cực nên không có sự di chuyển.
Các đáp án đúng: a,b,c
Chọn đáp án C Đáp án: C
Sử dụng thông tin ở bảng dưới đây để trả lời các câu 17 – 18:
Một mẫu nước cứng có nồng độ các ion Na+; Ca2+; Mg2+, Cl–; SO42– và HCO3– tương ứng là 1,2 mM; 3,0 mM; 1,0 mM; 0,6 mM; 0,01 mM và x mM (1 mM = 1 mmol/L), ngoài ra không chứa ion nào khác.
Câu 17 [705576]: Cách nào sau đây không thể làm mất tính cứng của loại nước nào?
A, Sử dụng Na3PO4.
B, Đun sôi.
C, Sử dụng Ca(OH)2.
D, Sử dụng Na2CO3.
Nước cứng tạm thời (do Ca(HCO3)2 và Mg(HCO3)2): có thể khử bằng cách đun sôi.
Nước cứng vĩnh cửu ( do MgSO4, CaCl2, MgCl2): không thể khử bằng đun sôi, cần dùng hóa chất.
⟹ Chọn đáp án B Đáp án: B
Nước cứng vĩnh cửu ( do MgSO4, CaCl2, MgCl2): không thể khử bằng đun sôi, cần dùng hóa chất.
⟹ Chọn đáp án B Đáp án: B
Câu 18 [705577]: Tổng khối lượng chất tan còn lại sau khi đun sôi kỹ 2 lít mẫu nước cứng trên là bao nhiêu? Giả sử các muối MgCO3, CaCO3 hầu như không tan trong nước.
A, 134,52
B, 123,6.
C, 142,2.
D, 141,0 mg.
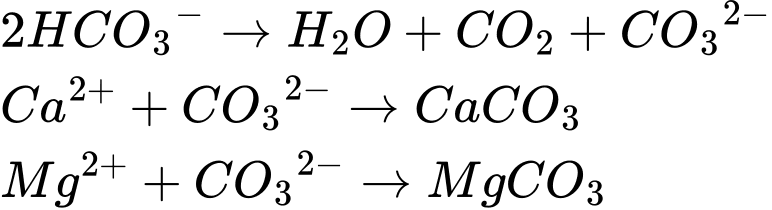
Trong 2L có: Na+ : 2,4mM; Ca2+ : 6,0mM; Mg2+ : 2,0mM; Cl- : 1,2mM; SO42-: 0,02mM; HCO3- : 2x
Bảo toàn điện tích:
1nNa+ + 2nCa2+ + 2nMg2+ = 1nCl- + 2nSO42- + 1nHCO3-
2,4 + 2. 6,0 + 2. 2,0 = 1. 1,2 + 2. 0,02 + 2x
⟹ x = 8,58mM
⟹ Dung dịch sau phản ứng còn:
Na+ : 2,4mM ; Cl- : 1,2mM ; SO42- : 0,02mM ; CO32-: 0,58mM
Khối lượng chất rắn:
m = mNa+ + mCl- + mSO42- + mCO32-
= 2,4 × 23 + 1,2 × 35,5 + 96 × 0,02 + 0,58 × 60
= 134,52
⟹ Chọn đáp án A Đáp án: A
PHẦN II. Thí sinh trả lời từ câu 1 đến câu 4. Trong mỗi ý a), b), c), d) ở mỗi câu, thí sinh chọn đúng hoặc sai
Câu 19 [705578]: Tiến hành thí nghiệm xác định hai chất chưa biết X và Y theo các bước sau:
∎ Bước 1: Trộn dung dịch của hai chất X và Y theo tỉ lệ hợp thức thì có 1,25 g kết tủa được tạo thành, chứa một muối của kim loại M (hóa trị II).
∎ Bước 2: Lọc, tách riêng phần kết tủa và phần dịch lọc.
∎ Bước 3: Nung nóng kết tủa đến 1100 oC thì kết tủa bị phân hủy thành 0,70 g oxide kim loại rắn MO và một oxide khí.
∎ Bước 4: Làm bay hơi phần dịch lọc, còn lại một chất rắn D nặng 2,0 g, chất này tạo thành hai sản phẩm khi phân hủy nhiệt ở 215 oC gồm một oxide khí và 0,90 g hơi nước. Tổng thể tích hỗn hợp khí và hơi là 1,86 L (đkc).
∎ Bước 1: Trộn dung dịch của hai chất X và Y theo tỉ lệ hợp thức thì có 1,25 g kết tủa được tạo thành, chứa một muối của kim loại M (hóa trị II).
∎ Bước 2: Lọc, tách riêng phần kết tủa và phần dịch lọc.
∎ Bước 3: Nung nóng kết tủa đến 1100 oC thì kết tủa bị phân hủy thành 0,70 g oxide kim loại rắn MO và một oxide khí.
∎ Bước 4: Làm bay hơi phần dịch lọc, còn lại một chất rắn D nặng 2,0 g, chất này tạo thành hai sản phẩm khi phân hủy nhiệt ở 215 oC gồm một oxide khí và 0,90 g hơi nước. Tổng thể tích hỗn hợp khí và hơi là 1,86 L (đkc).
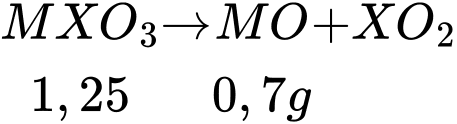
mXO2 = 0,55g.
Giả sử XO2 là CO2 ⟹ nXO2 = m : M = 0,0125mol = nMO
⟹ MMO = m : n = 0,7 : 0,0125 = 56
⟹ M là Ca
Phân tích các đáp án:
❌A. Sai. Hợp chất X là CaCO3
✔️B. Đúng. Phương trình phản ứng:
CaCO3 + 2HCl ⟶CaCl2 + CO2 + H2O
❌C. Sai.
Gọi số mol oxide là x mol , H2O = 0,05 mol.
⟶ x + 0,05 = 1,86 : 24,79
⟶ x = 0,025 mol
Chất D ⟶ H2O + oxide
⟶ M oxide = 1,1 : 0,025 = 44
⟶ CO2 hoặc N2O
Khi nhiệt phân D tạo 2 sản phẩm khí ⟶ D là NH4NO3 không chứa C
❌D.Sai. X là Ca(NO3)2 có 9 nguyên tử; Y là (NH4)2CO3 có 14 nguyên tử ⟶ X ít hơn Y.
Câu 20 [705579]: Tiến hành thí nghiệm như sau: Cho từ từ vào bình cầu dung tích 250 mL, thêm khoảng 30 mL H2SO4 đặc, làm lạnh trong chậu nước đá rồi thêm từ từ khoảng 30 mL HNO3, sau đó thêm tiếp khoảng 10 mL benzene và lắp sinh hàn hồi lưu. Đun cách thuỷ hỗn hợp phản ứng trên bếp từ đến 80 °C trong khoảng 60 phút. Để nguội rồi cho hỗn hợp vào phễu chiết.
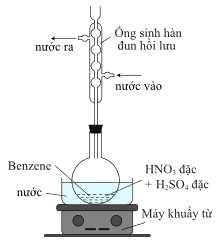

C6H6 + HNO3 ⟶C6H5NO2 + H2O
Phân tích các phát biểu:
✔️A. Đúng. Sản phẩm thu được là nitrobenzene C6H5NO2.
❌B.Sai. HNO3 là chất dễ bay hơi, việc đặt trong chậu nước đá sẽ làm HNO3 bay hơi đi.
✔️C.Đúng. Sản phẩm thu được nằm ở phía dưới ống nghiệm.
❌D.Sai. Sản phẩm là nitrobenzene là chất lỏng màu vàng ở phía trên.
Phân tích các phát biểu:
✔️A. Đúng. Sản phẩm thu được là nitrobenzene C6H5NO2.
❌B.Sai. HNO3 là chất dễ bay hơi, việc đặt trong chậu nước đá sẽ làm HNO3 bay hơi đi.
✔️C.Đúng. Sản phẩm thu được nằm ở phía dưới ống nghiệm.
❌D.Sai. Sản phẩm là nitrobenzene là chất lỏng màu vàng ở phía trên.
Câu 21 [705580]: Tính chất cụ thể của triolein, một triglyceride phổ biến trong dầu thực vật, có thể được xác định thông qua phân tích phố Mass Spectrometry (MS) và phổ Infrared (IR). Phổ MS có thể cung cấp thông tin về khối lượng phân từ của triolein bằng cách xác định các ion phân tử và các ion mảnh vỡ, từ đó giúp xác định cấu trúc và thành phần phân tử của nó. Mặt khác, phổ IR có thể tiết lộ các nhóm chức như cacbonyl, hydroxyl và các nhóm chức khác có mặt trong triolein, giúp xác định cấu trúc hóa học tổng thể của nó.
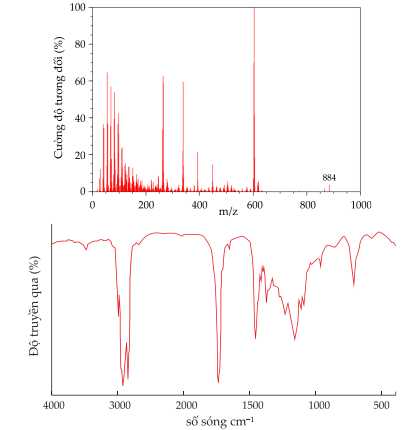
Bằng cách kết hợp thông tin từ cả hai phổ, chúng ta có thể hiểu rõ hơn về cấu trúc và tính chất hóa học của triolein, từ đó cung cấp một cách tiếp cận toàn diện trong việc nghiên cứu và ứng dụng của chất này trong lĩnh vực thực phẩm, y học và công nghiệp. Xét tính đúng - sai của các phát biểu sau:

Bằng cách kết hợp thông tin từ cả hai phổ, chúng ta có thể hiểu rõ hơn về cấu trúc và tính chất hóa học của triolein, từ đó cung cấp một cách tiếp cận toàn diện trong việc nghiên cứu và ứng dụng của chất này trong lĩnh vực thực phẩm, y học và công nghiệp. Xét tính đúng - sai của các phát biểu sau:
Phân tích các phát biểu:
❌A. Sai. Dựa vào phổ MS, mảnh ion phân tử lớn nhất của triolein có m/z = 884.
✔️B. Đúng. Trên phổ IR có bước sóng hấp thụ khoảng 1740cm-1 là đặc trưng của C=O nhóm ester.
❌C. Sai. Liên kết C=C không phải nhóm chức.
✔️D. Đúng. Nhóm chức ester và liên kết C=C là cơ sở ứng dụng của chất này trong thực phẩm, y học và công nghiệp.
❌A. Sai. Dựa vào phổ MS, mảnh ion phân tử lớn nhất của triolein có m/z = 884.
✔️B. Đúng. Trên phổ IR có bước sóng hấp thụ khoảng 1740cm-1 là đặc trưng của C=O nhóm ester.
❌C. Sai. Liên kết C=C không phải nhóm chức.
✔️D. Đúng. Nhóm chức ester và liên kết C=C là cơ sở ứng dụng của chất này trong thực phẩm, y học và công nghiệp.
Câu 22 [705581]: Một miếng kim loại nickel rắn được thêm vào dung dịch potassium dichromate (K2Cr2O7), phương trình ion rút gọn được biểu diễn như dưới đây:
14H+(aq) + Cr2O72–(aq) + 3Ni(s) ⟶ 2Cr3+(aq) + 3Ni2+(aq) + 7H2O(l)
14H+(aq) + Cr2O72–(aq) + 3Ni(s) ⟶ 2Cr3+(aq) + 3Ni2+(aq) + 7H2O(l)
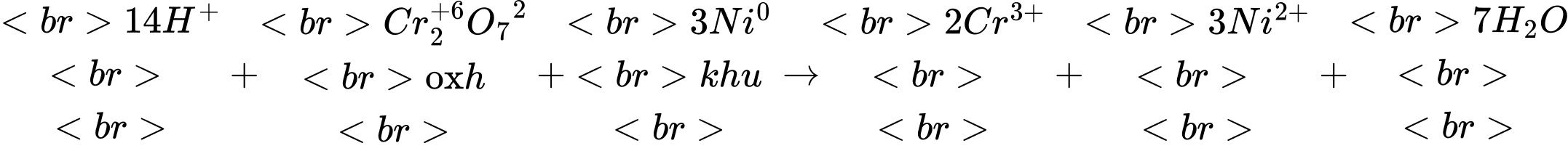
Phân tích các phát biểu:
✔️A.Đúng. Ni có số oxi hóa từ 0 lên +2 ⟹ Chất khử.
✔️B. Đúng. Nồng độ H+ giảm ⟹ pH tăng.
❌C. Sai. Ni ⟶ Ni2+ +2e. Vậy 1 mol K2Cr2O7 phản ứng với 3 mol Ni thì số mol electron trao đổi là 6e
❌D. Sai. Khi các chất phản ứng vừa đủ thì toàn bộ H+ chuyển hóa thành nước ⟹ môi trường trung tính.
PHẦN III. Thí sinh trả lời từ câu 1 đến câu 6.
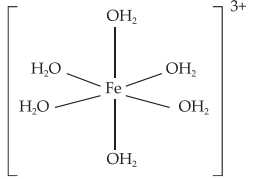
Câu 23 [705582]: Phức chất  có cấu tạo như hình bên dưới.
có cấu tạo như hình bên dưới.
Có bao nhiêu liên kết cho nhận có trong phức chất trên?
 có cấu tạo như hình bên dưới.
có cấu tạo như hình bên dưới.
Có bao nhiêu liên kết cho nhận có trong phức chất trên?
Phức chất [Fe(OH2)6]3+ có cấu trúc bát diện, mỗi phân tử H2O có một cặp electron không chia, đóng vai trò là phối tử và cung cấp electron để tạo liên kết với ion Fe3+.
Trong đó ion Fe3+ liên kết với 6 phân tử nước thông qua liên kết cho nhận.
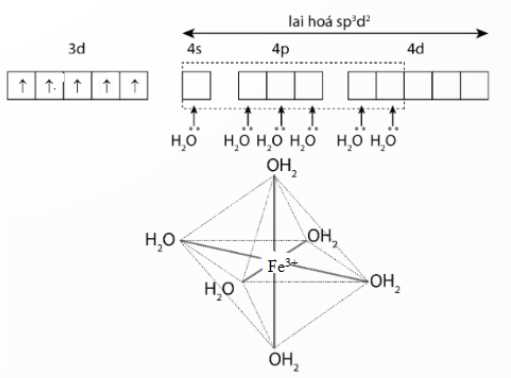
Vậy có 6 liên kết cho nhận.
Trong đó ion Fe3+ liên kết với 6 phân tử nước thông qua liên kết cho nhận.

Vậy có 6 liên kết cho nhận.
Điền đáp án: 6
Câu 24 [684323]: Cho sơ đồ phản ứng hóa học sau:
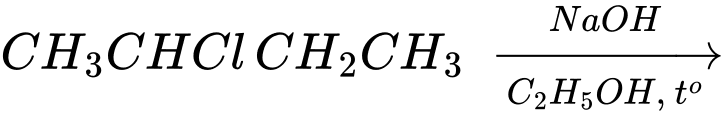
Sản phẩm chính theo quy tắc Zaitsev của phản ứng trên sẽ có liên kết đôi ở vị trí carbon số mấy?
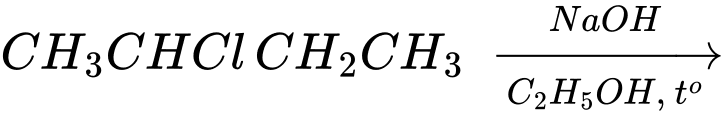
Sản phẩm chính theo quy tắc Zaitsev của phản ứng trên sẽ có liên kết đôi ở vị trí carbon số mấy?
Phản ứng xảy ra ở đây là phản ứng tách HCl trong môi trường NaOH/ethanol. Theo quy tắc Zaitsev, sản phẩm chính sẽ là alkene có liên kết đôi ở vị trí tạo ra alkene bền nhất, nghĩa là liên kết đôi sẽ hình thành ở vị trí có số lượng nhóm thế nhiều nhất (alkyl hóa nhiều nhất).
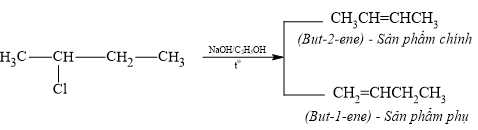
But-2-ene bền hơn vì liên kết đôi nằm giữa hai carbon bậc 2 (có nhiều nhóm thế hơn). Trong khi dó but-1-ene kém bền hơn vì vì liên kết đôi nằm ở đầu mạch (có ít nhóm thế hơn).
⇒ Theo quy tắc Zaitsev, sản phẩm chính sẽ là but-2-ene, với liên kết đôi nằm ở vị trí carbon số 2 và carbon số 3.
⇒ Điền đáp án: 2

But-2-ene bền hơn vì liên kết đôi nằm giữa hai carbon bậc 2 (có nhiều nhóm thế hơn). Trong khi dó but-1-ene kém bền hơn vì vì liên kết đôi nằm ở đầu mạch (có ít nhóm thế hơn).
⇒ Theo quy tắc Zaitsev, sản phẩm chính sẽ là but-2-ene, với liên kết đôi nằm ở vị trí carbon số 2 và carbon số 3.
⇒ Điền đáp án: 2
Câu 25 [705583]: Khí Biogas còn gọi là khí sinh học. Thành phần chính của khí sinh học Biogas có khí methane chiếm 60% thể tích còn lại là carbon dioxide và các khí khác. Một bình gas (khí hóa lỏng) chứa hỗn hợp propane và butane với tỉ lệ mol 1 : 2. Trung bình 60 ngày một hộ gia đình cần dùng hết một bình “ga” loại 12 kg (giả thiết hiệu suất hấp thụ nhiệt các chất bằng nhau). Thể tích khí Biogas tối thiểu cần dùng để tạo ra lượng nhiệt tương đương khi đốt cháy 1 bình “ga” loại 12 kg là bao nhiêu m3 (đkc)? (Làm tròn đến hàng phần mười)
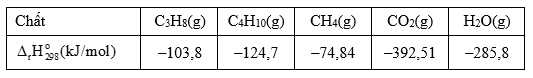

Trong 12kg có : C3H8: x mol ; C4H10 : 2x mol
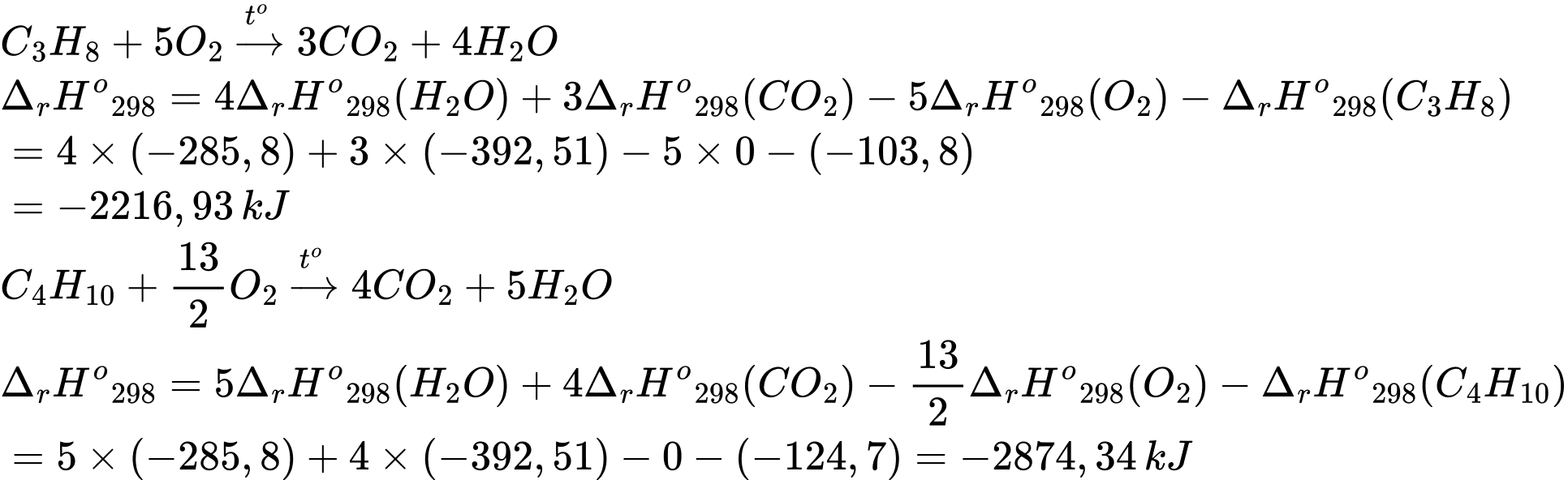
Nhiệt tỏa ra khi đốt bình ga : Q tỏa = x.(2216,93) + 2x.(2874,34) = 597420,75 kJ
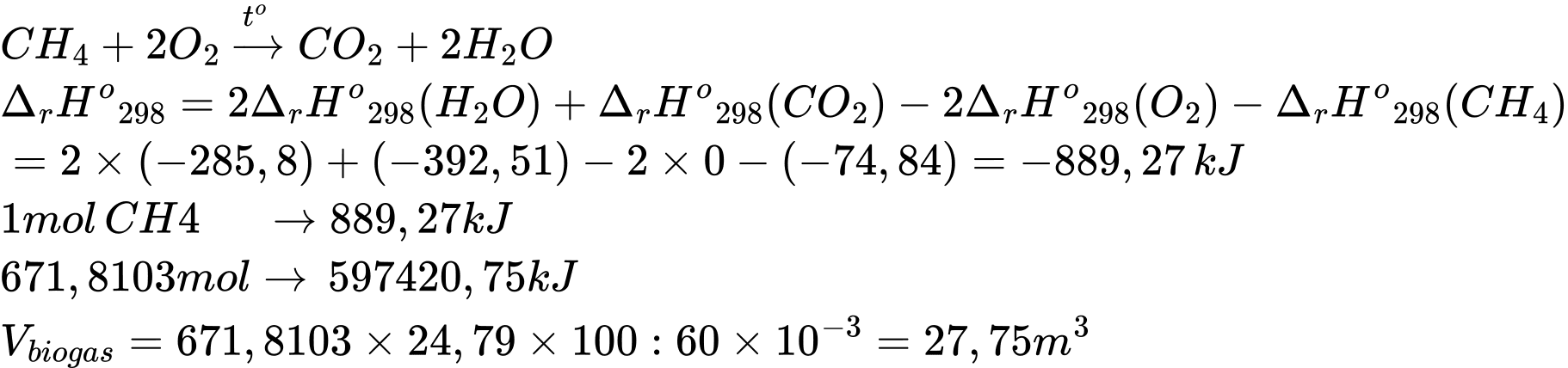
⇒ Điền đáp án: 27,8
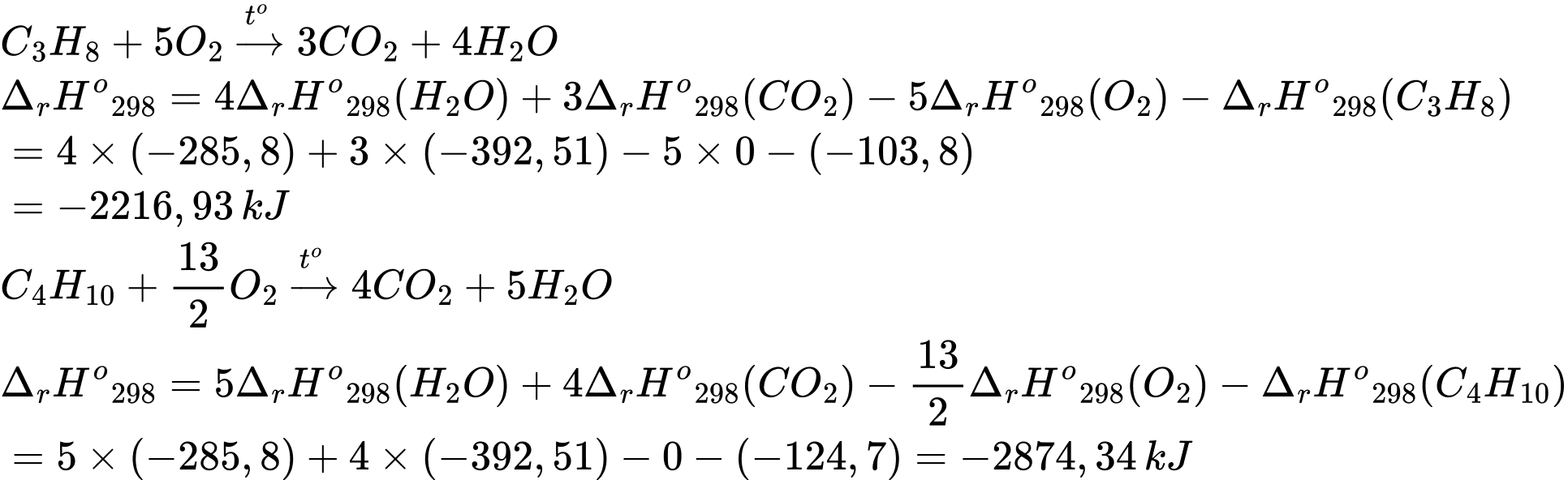
Nhiệt tỏa ra khi đốt bình ga : Q tỏa = x.(2216,93) + 2x.(2874,34) = 597420,75 kJ
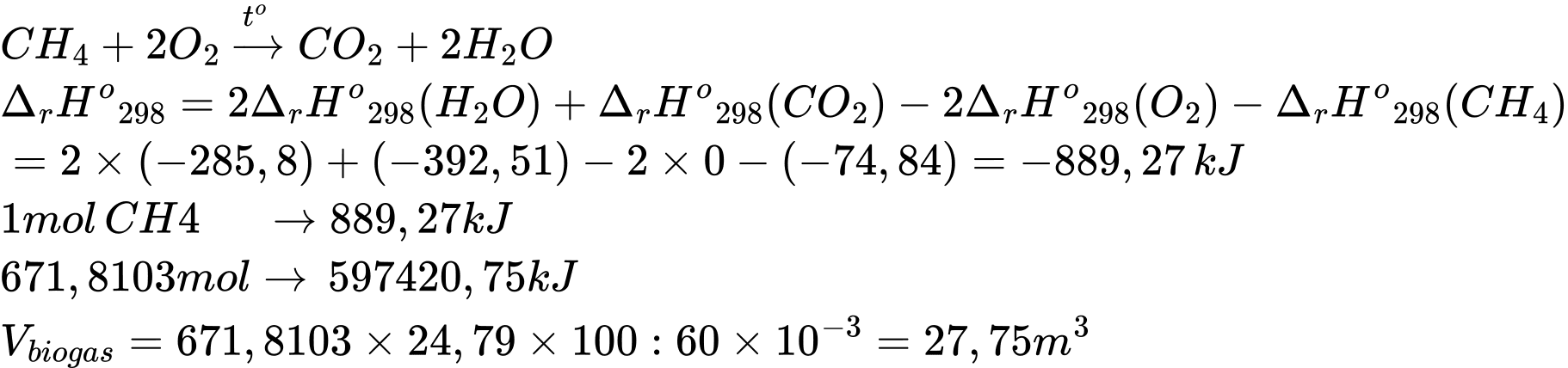
⇒ Điền đáp án: 27,8
Câu 26 [705584]: Cho các polymer sau: (1) polyacrylonitrile; (2) polycaproamide; (3) poly(ethylene terephthalate); (4) poly(hexamethylene adipamide); (5) tơ cellulose acetate. Có bao nhiêu polymer có thể dùng làm tơ hóa học?
Một polymer có thể dùng làm tơ hóa học khi nó có tính bền cơ học, có thể kéo thành sợi dài và bền với nhiệt độ. Các loại polymer thường dùng làm tơ gồm: tơ tổng hợp và tơ bán tổng hợp.
✔️(1) Polyacrylonitrile: (-CH2-CH(CN)- )n thành phần chính của tơ olon.
✔️(2) Polycaproamide (Nylon-6) là một loại tơ polyamide (tơ tổng hợp – Nylon-6).
✔️(3) Poly(ethylene terephthalate) là thành phần chính của tơ polyester.
✔️(4)Poly(hexamethylene adipamide) (Nylon-6,6) là một loại tơ polyamide (tơ tổng hợp – Nylon-6,6)
✔️(5)Tơ cellulose acetate loại tơ bán tổng hợp từ cellulose, được dùng làm tơ nhân tạo.
Điền đáp án: 5
✔️(1) Polyacrylonitrile: (-CH2-CH(CN)- )n thành phần chính của tơ olon.
✔️(2) Polycaproamide (Nylon-6) là một loại tơ polyamide (tơ tổng hợp – Nylon-6).
✔️(3) Poly(ethylene terephthalate) là thành phần chính của tơ polyester.
✔️(4)Poly(hexamethylene adipamide) (Nylon-6,6) là một loại tơ polyamide (tơ tổng hợp – Nylon-6,6)
✔️(5)Tơ cellulose acetate loại tơ bán tổng hợp từ cellulose, được dùng làm tơ nhân tạo.
Điền đáp án: 5
Câu 27 [705585]: Dưới đây là phổ khối lượng của một chất hữu cơ có nguyên tố C, 10 nguyên tố H và 1 nguyên tố O. Có bao nhiêu nguyên tố C trong phân tử chất hữu cơ trên?
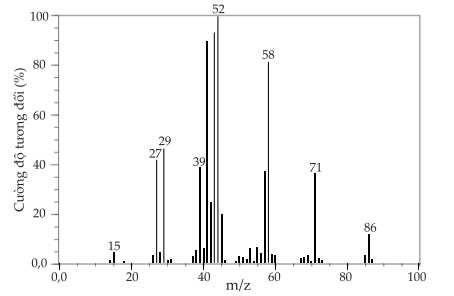

Gọi công thức phân tử của hợp chất là CxH10O
Khối lượng phân tử của hợp chất là 86 nên:
12x + 10 + 16 = 86
⟹ x = 5
⟹ Công thức phân tử của hợp chất là C5H10O
Điền đáp án: 5
Khối lượng phân tử của hợp chất là 86 nên:
12x + 10 + 16 = 86
⟹ x = 5
⟹ Công thức phân tử của hợp chất là C5H10O
Điền đáp án: 5
Câu 28 [705586]: Sulphur dioxide (SO2) và sulfite (SO32–) thường được sử dụng làm chất bảo quản và chất chống oxy hóa trong ngành công nghiệp thực phẩm. Sulfur dioxide đặc biệt thường được sử dụng trong trái cây sấy khô, nước ép trái cây, mứt, rượu vang. Nó ức chế sự phát triển của nấm và vi khuẩn và do đó kéo dài thời hạn sử dụng của thực phẩm. Tuy nhiên, do tác dụng độc hại của sulfur dioxide nên việc sử dụng nó cũng gây ra các tác hại.
Bước 1: Cân chính xác 15,65 (gam) mẫu, cho mẫu vào 100 mL nước cất, tiến hành chưng cất hỗn hợp, trong quá trình chưng cất thêm từ từ phosphoric acid 1M với mục đích tách SO2 từ mẫu.
Bước 2: Dẫn toàn bộ SO2 sinh ra qua 25 mL dung dịch H2O2 (lấy dư), khuấy đều dung dịch thu được dung dịch A: H2O2(aq) + SO2(g)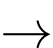 H2SO4(aq)
H2SO4(aq)
Bước 3: Đun nhẹ dung dịch A với mục đích phân hủy hết H2O2 thu được dung dịch B.
Bước 4: Thêm vào dung dịch B vài giọt phenolphthalein, tiến hành chuẩn độ dung dịch B với NaOH 0,01 M. Chuẩn độ đến khi dung dịch chuyển sang màu hồng nhạt bền trong 30s thì dung hết 1,4 mL dung dịch NaOH.
Tính hàm lượng SO2 trong thực phẩm trên theo mg trong 1 kg mẫu (làm tròn đến hàng phần mười).
Bước 1: Cân chính xác 15,65 (gam) mẫu, cho mẫu vào 100 mL nước cất, tiến hành chưng cất hỗn hợp, trong quá trình chưng cất thêm từ từ phosphoric acid 1M với mục đích tách SO2 từ mẫu.
Bước 2: Dẫn toàn bộ SO2 sinh ra qua 25 mL dung dịch H2O2 (lấy dư), khuấy đều dung dịch thu được dung dịch A: H2O2(aq) + SO2(g)
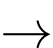 H2SO4(aq)
H2SO4(aq)Bước 3: Đun nhẹ dung dịch A với mục đích phân hủy hết H2O2 thu được dung dịch B.
Bước 4: Thêm vào dung dịch B vài giọt phenolphthalein, tiến hành chuẩn độ dung dịch B với NaOH 0,01 M. Chuẩn độ đến khi dung dịch chuyển sang màu hồng nhạt bền trong 30s thì dung hết 1,4 mL dung dịch NaOH.
Tính hàm lượng SO2 trong thực phẩm trên theo mg trong 1 kg mẫu (làm tròn đến hàng phần mười).
H2O2 + SO2 ⟶ H2SO4
H2SO4 + 2NaOH ⟶ Na2SO4 + H2O
nNaOH = 1,4.10-5 mol ⟶ nH2SO4 = 7.10-6 mol
MSO2 = 4,48 .10-4 = 0,448mg
Có: 0,01565 kg ⟶0,448mg SO2
1kg ⟶ 28,62 mg
Điền đáp án: 28,6
H2SO4 + 2NaOH ⟶ Na2SO4 + H2O
nNaOH = 1,4.10-5 mol ⟶ nH2SO4 = 7.10-6 mol
MSO2 = 4,48 .10-4 = 0,448mg
Có: 0,01565 kg ⟶0,448mg SO2
1kg ⟶ 28,62 mg
Điền đáp án: 28,6