PHẦN I. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
Câu 1 [705798]: “Khi đốt đơn chất hay hợp chất của Ca, Ba trên ngọn lửa đèn khí thì ngọn lửa có màu ..(1).. với Ca và ..(2).. của Ca có ngọn lửa màu đỏ cam; Ba và ..(2).. của Ba có ngọn lửa màu lục. Nội dung phù hợp trong các ô trống (1), (2) lần lượt là
A, giống nhau, đơn chất.
B, khác nhau, hợp chất.
C, không xác định, hợp chất.
D, khác nhau, nguyên tố.
(Ca) cháy có ngọn lửa đỏ cam, (Ba) cháy có ngọn lửa màu lục.
⟹ Màu sắc ngọn lửa khác nhau → (1) là "khác nhau".
Một số hợp chất của Ca (ví dụ: CaCl2) và Ba (ví dụ: BaCl2) khi đốt cũng có màu lửa đặc trưng.
⟹ (2) điền "hợp chất"
Chọn đáp án B Đáp án: B
⟹ Màu sắc ngọn lửa khác nhau → (1) là "khác nhau".
Một số hợp chất của Ca (ví dụ: CaCl2) và Ba (ví dụ: BaCl2) khi đốt cũng có màu lửa đặc trưng.
⟹ (2) điền "hợp chất"
Chọn đáp án B Đáp án: B
Câu 2 [705799]: Thuốc súng bao gồm potassium nitrate, than củi và lưu huỳnh theo tỉ lệ khối lượng xấp xỉ 6 : 1 : 1. Công thức hóa học của potassium nitrate là
A, KNO2.
B, KNO3.
C, K3N.
D, KNSC.
Phân tích các đáp án:
❌A. KNO2 là potassium nitrite.
✔️B. KNO3 là potassium nitrate.
❌C. K3N là potassium nitride.
❌D. KNSC là potassium thiocyanate Đáp án: B
❌A. KNO2 là potassium nitrite.
✔️B. KNO3 là potassium nitrate.
❌C. K3N là potassium nitride.
❌D. KNSC là potassium thiocyanate Đáp án: B
Câu 3 [705800]: Trong các hợp chất cho dưới đây, hợp chất nào chứa mắt xích fructose trong phân tử?
A, Saccharose.
B, Maltose.
C, Tinh bột.
D, Cellulose.
Phân tích các đáp án:
✔️A. Saccharose : Là đisaccharide gồm glucose và fructose
❌B. Maltose: Gồm hai phân tử glucose → Không chứa fructose
❌C. Tinh bột: Là polysaccharide chỉ gồm nhiều mắt xích glucose
❌D. Cellulose: Cũng là polysaccharide, chỉ chứa glucose Đáp án: A
✔️A. Saccharose : Là đisaccharide gồm glucose và fructose
❌B. Maltose: Gồm hai phân tử glucose → Không chứa fructose
❌C. Tinh bột: Là polysaccharide chỉ gồm nhiều mắt xích glucose
❌D. Cellulose: Cũng là polysaccharide, chỉ chứa glucose Đáp án: A
Câu 4 [705801]: Một loại polymer thiên nhiên có trong thực phẩm, hỗ trợ kiểm soát lượng đường trong máu, có lợi cho những người đang kiểm soát bệnh tiểu đường. Polymer nào sau đây là polymer thiên nhiên?
A, Amylose.
B, Nylon-6,6.
C, Nylon-7.
D, PVC.
Phân tích các đáp án:
✔️A. Amylose là thành phần của tinh bột (cùng với amylopectin) có nguồn gốc thiên nhiên, giúp kiểm soát lượng đường trong máu.
❌B. Nylon-6,6 là polymer tổng hợp, không liên quan đến thực phẩm.
❌C. Nylon-7 là polymer tổng hợp, không có trong thực phẩm.
❌D. PVC là polymer nhân tạo dùng trong công nghiệp nhựa. Đáp án: A
✔️A. Amylose là thành phần của tinh bột (cùng với amylopectin) có nguồn gốc thiên nhiên, giúp kiểm soát lượng đường trong máu.
❌B. Nylon-6,6 là polymer tổng hợp, không liên quan đến thực phẩm.
❌C. Nylon-7 là polymer tổng hợp, không có trong thực phẩm.
❌D. PVC là polymer nhân tạo dùng trong công nghiệp nhựa. Đáp án: A
Câu 5 [705802]: Khi một đinh sắt được cắm vào củ khoai tây tươi, hiện tượng ăn mòn nào có thể xảy ra ngay tại thời điểm đó?
A, Ăn mòn hóa học.
B, Ăn mòn điện hóa.
C, Không có hiện tượng ăn mòn.
D, Cả ăn mòn hóa học và điện hóa.
Ăn mòn xảy ra là ăn mòn hóa học, do sắt phản ứng trực tiếp với các acid hữu cơ và oxygen trong khoai tây.
Ở đây, chỉ có một kim loại (Fe) phản ứng với môi trường, không có sự di chuyển điện tích giữa hai điện cực khác nhau, nên không thể coi là ăn mòn điện hóa.
Chọn đáp án A Đáp án: A
Ở đây, chỉ có một kim loại (Fe) phản ứng với môi trường, không có sự di chuyển điện tích giữa hai điện cực khác nhau, nên không thể coi là ăn mòn điện hóa.
Chọn đáp án A Đáp án: A
Câu 6 [705803]: Để tẩy lớp cặn bám dưới đáy dụng cụ đun, đựng nước nóng trong gia đình, người ta có thể sử dụng dung dịch nào sau đây?
A, Ethyl alcohol.
B, Muối ăn.
C, Giấm ăn.
D, Đường kính.
Lớp cặn bám dưới đáy dụng cụ đun nước nóng trong gia đình chủ yếu là các muối không tan, đặc biệt là CaCO3 và MgCO3. Để tẩy lớp cặn này, ta cần dùng acid để hòa tan chúng.
Phân tích các đáp án:
❌A. Ethyl alcohol là alcohol, không phải acid.
❌B. Muối ăn là hợp chất NaCl, không phải acid.
✔️C. Giấm ăn thành phần chính là CH3COOH là acid hữu cơ.
❌D. Đường kính là hợp chất hữu cơ, không phải acid.
Chọn đáp án C Đáp án: C
Phân tích các đáp án:
❌A. Ethyl alcohol là alcohol, không phải acid.
❌B. Muối ăn là hợp chất NaCl, không phải acid.
✔️C. Giấm ăn thành phần chính là CH3COOH là acid hữu cơ.
❌D. Đường kính là hợp chất hữu cơ, không phải acid.
Chọn đáp án C Đáp án: C
Câu 7 [705804]: Cho phản ứng thuận nghịch sau là một phản ứng đơn giản:
4NO(g) + 2O2(g) ⇌ 4NO2(g)
Biểu thức tốc độ phản ứng thuận được viết dưới dạng: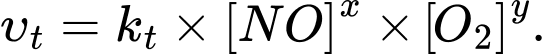 Giá trị của x, y lần lượt là
Giá trị của x, y lần lượt là
4NO(g) + 2O2(g) ⇌ 4NO2(g)
Biểu thức tốc độ phản ứng thuận được viết dưới dạng:
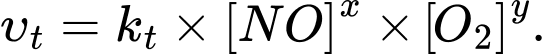 Giá trị của x, y lần lượt là
Giá trị của x, y lần lượt là A, 2, 1.
B, 4, 2.
C, 4, 4.
D, 1, 4.
x và y là hệ số cân bằng của NO và O2.
vt = kt × [NO]4 × [O2]2
x = 4 , y = 2
Chọn đáp án B Đáp án: B
vt = kt × [NO]4 × [O2]2
x = 4 , y = 2
Chọn đáp án B Đáp án: B
Câu 8 [705805]: Số liên kết sigma (σ) trong phân tử pentane CH3CH2CH2CH2CH3 là
A, 10.
B, 12.
C, 15.
D, 16.
Số liên kết sigma = số H + số liên kết C - C
Phân tử CH3CH2CH2CH2CH3 có 12 H và 4 liên kết C - C.
⟹ Số liên kết sigma = 12 + 4 = 16
Chọn đáp án D Đáp án: D
Phân tử CH3CH2CH2CH2CH3 có 12 H và 4 liên kết C - C.
⟹ Số liên kết sigma = 12 + 4 = 16
Chọn đáp án D Đáp án: D
Câu 9 [705806]: Khi sử dụng bếp than, cần lưu ý thông gió tốt để tránh bị ngộ độc khí CO. Phản ứng cháy của than xảy ra theo phương trình hoá học sau:
C(s) + O2(g) ⇌ CO2(g)
Trong các cách thực hiện sau:
(a) Tăng cường thông gió khu vực bếp.
(b) Sử dụng bếp than có ống khói.
(c) Sử dụng bếp than có quạt thổi không khí vào lò.
(d) Giảm lượng than sử dụng.
Có bao nhiêu phát biểu dưới đây là đúng về biện pháp làm giảm nguy cơ ngộ độc khí CO?
C(s) + O2(g) ⇌ CO2(g)
Trong các cách thực hiện sau:
(a) Tăng cường thông gió khu vực bếp.
(b) Sử dụng bếp than có ống khói.
(c) Sử dụng bếp than có quạt thổi không khí vào lò.
(d) Giảm lượng than sử dụng.
Có bao nhiêu phát biểu dưới đây là đúng về biện pháp làm giảm nguy cơ ngộ độc khí CO?
A, 1.
B, 2.
C, 3.
D, 4.
Phân tích các đáp án:
✔️(a) Tăng cường thông gió khu vực bếp : Cung cấp thêm oxygen, giúp than cháy hoàn toàn thành CO2 thay vì CO.
✔️(b) Sử dụng bếp than có ống khói: Giúp khí CO thoát ra ngoài, tránh tích tụ trong phòng.
✔️(c) Sử dụng bếp than có quạt thổi không khí vào lò: Tăng lượng oxygen, giúp than cháy hoàn toàn thành CO2
❌(d) Giảm lượng than sử dụng: Không trực tiếp làm tăng lượng oxygen. Nếu vẫn dùng bếp trong không gian kín, khí CO vẫn có thể sinh ra do thiếu oxygen.
Có 3 đáp án đúng.
Chọn đáp án C Đáp án: C
✔️(a) Tăng cường thông gió khu vực bếp : Cung cấp thêm oxygen, giúp than cháy hoàn toàn thành CO2 thay vì CO.
✔️(b) Sử dụng bếp than có ống khói: Giúp khí CO thoát ra ngoài, tránh tích tụ trong phòng.
✔️(c) Sử dụng bếp than có quạt thổi không khí vào lò: Tăng lượng oxygen, giúp than cháy hoàn toàn thành CO2
❌(d) Giảm lượng than sử dụng: Không trực tiếp làm tăng lượng oxygen. Nếu vẫn dùng bếp trong không gian kín, khí CO vẫn có thể sinh ra do thiếu oxygen.
Có 3 đáp án đúng.
Chọn đáp án C Đáp án: C
Câu 10 [575313]: Hình ảnh dưới đây mô phỏng các hạt bắn vào một điện trường:
Hạt nào sau đây có thể là hạt electron?
Hạt nào sau đây có thể là hạt electron?
A, Hạt A.
B, Hạt B.
C, Hạt C.
D, Cả 3 hạt A, B, C.
A có thể là electron do chùm các hạt A bị lệch về phía cực dương của điện trường nên các hạt này mang điện tích âm.
Chọn đáp án A Đáp án: A
Chọn đáp án A Đáp án: A
Câu 11 [705807]: Hiện tượng xảy ra khi cho một lượng nhỏ bột đồng vào ống nghiệm chứa dung dịch MgCl2 là gì?
A, Dung dịch chuyển sang màu xanh.
B, Xuất hiện kết tủa Mg màu đen.
C, Cu tan vào trong dung dịch.
D, Không quan sát được hiện tượng gì.
Cu không phản ứng với MgCl2 nên không có hiện tượng trong ống nghiệm.
Chọn đáp án D Đáp án: D
Chọn đáp án D Đáp án: D
Câu 12 [705808]: Dung dịch nitric acid đặc có thể hòa tan copper (II) sulfide theo phương trình chưa cân bằng như sau:
CuS + HNO3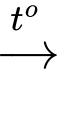 CuSO4 + NO + H2O.
CuSO4 + NO + H2O.
Để hòa tan 28,8 gam CuS thì thể tích (mL) dung dịch HNO3 16 M cần dùng là
CuS + HNO3
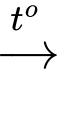 CuSO4 + NO + H2O.
CuSO4 + NO + H2O.Để hòa tan 28,8 gam CuS thì thể tích (mL) dung dịch HNO3 16 M cần dùng là
A, 80.
B, 800.
C, 50.
D, 500.
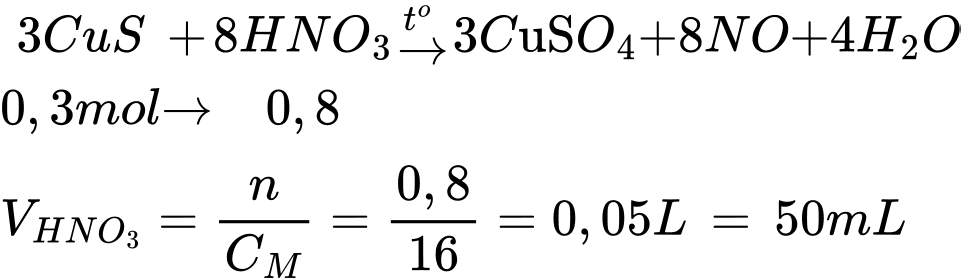
Chọn đáp án C Đáp án: C
Câu 13 [705809]: Methanoic acid phản ứng với propanol khi có mặt một lượng nhỏ sulfuric acid đặc. Tên gọi của ester được tạo thành là
A, Methyl propyl sulfate.
B, Methyl propanoate.
C, Propyl ethanoate.
D, Propyl methanoate.
Methanoic acid : HCOOH và propanol C3H7OH.
HCOOH + C3H7OH ⟶ HCOOC3H7 + H2O
Ester tạo thành là HCOOC3H7 có tên là propyl methanoate.
Phân tích các đáp án:
❌A. Methyl propyl sulfate : CH3OSO2OCH2CH2CH3
❌B.Methyl propanoate : CH3CH2COOCH3
❌C.Propyl ethanoate : CH3COOC3H7
Chọn đáp án D.
HCOOH + C3H7OH ⟶ HCOOC3H7 + H2O
Ester tạo thành là HCOOC3H7 có tên là propyl methanoate.
Phân tích các đáp án:
❌A. Methyl propyl sulfate : CH3OSO2OCH2CH2CH3
❌B.Methyl propanoate : CH3CH2COOCH3
❌C.Propyl ethanoate : CH3COOC3H7
Chọn đáp án D.
Câu 14 [705810]: “Amino acid có nhiệt độ nóng chảy ..(1).. do tồn tại ở trạng thái ..(2)..”. Nội dung phù hợp trong ô trống (1), (2) lần lượt là
A, thấp, ion lưỡng cực.
B, cao, ion lưỡng cực.
C, thấp, cation.
D, cao, anion.
- Amino acid có liên kết ion mạnh giữa các ion lưỡng cực trong mạng tinh thể, đòi hỏi nhiệt độ cao để phá vỡ. Do đó, amino acid thường có nhiệt độ nóng chảy cao hơn so với các hợp chất hữu cơ có khối lượng phân tử tương tự.
⟹ (1) Nhiệt độ nóng chảy cao.
- Ở điều kiện thường, amino acid tồn tại chủ yếu dưới dạng ion lưỡng cực.
⟹ (2) ion lưỡng cực.
Chọn đáp án B
Đáp án: B
⟹ (1) Nhiệt độ nóng chảy cao.
- Ở điều kiện thường, amino acid tồn tại chủ yếu dưới dạng ion lưỡng cực.
⟹ (2) ion lưỡng cực.
Chọn đáp án B
Đáp án: B
Câu 15 [705811]: Gói làm nóng thức ăn trong lầu tự sôi có thành phần theo khối lượng là Mg (90%), Fe (4%), NaCl (6%). Khi thêm vào một ít nước, phản ứng hoá học:
Mg + H2O → Mg(OH)2 + H2
Phản ứng xảy ra mãnh liệt kèm theo lượng nhiệt toả ra lớn, giúp làm nóng thức ăn.
Cho các phát biểu sau:
(a) Magnesium có thể khử được nước ở nhiệt độ thường.
(b) Có thể dùng bột chứa 100% Fe để tăng hiệu quả làm nóng thức ăn.
(c) Nếu thêm nước quá nhiều, khả năng làm nóng thức ăn của hỗn hợp giảm.
(d) Khi thay NaCl bằng KCl, khả năng làm nóng của hỗn hợp không đổi.
Số phát biểu đúng là
Mg + H2O → Mg(OH)2 + H2
Phản ứng xảy ra mãnh liệt kèm theo lượng nhiệt toả ra lớn, giúp làm nóng thức ăn.
Cho các phát biểu sau:
(a) Magnesium có thể khử được nước ở nhiệt độ thường.
(b) Có thể dùng bột chứa 100% Fe để tăng hiệu quả làm nóng thức ăn.
(c) Nếu thêm nước quá nhiều, khả năng làm nóng thức ăn của hỗn hợp giảm.
(d) Khi thay NaCl bằng KCl, khả năng làm nóng của hỗn hợp không đổi.
Số phát biểu đúng là
A, 1.
B, 2.
C, 3.
D, 4.
Phân tích các phát biểu:
✔️(a) Đúng, vì Mg có thể phản ứng với nước tạo ra Mg(OH)2 và khí H2 ngay ở nhiệt độ thường
❌(b) Sai, vì Fe không phản ứng với nước ở nhiệt độ thường để tạo nhiệt. Nếu dùng 100% Fe, hỗn hợp không sinh nhiệt, làm giảm hiệu quả làm nóng thức ăn.
✔️(c) Đúng, vì quá nhiều nước sẽ hấp thụ nhiệt, làm giảm nhiệt độ tổng thể của hệ thống, khiến thức ăn không nóng hiệu quả.
✔️(d) Đúng, vì NaCl và KCl đều là muối tan tốt trong nước, giúp tạo môi trường điện ly hỗ trợ phản ứng, nhưng không trực tiếp sinh nhiệt. Do đó, thay NaCl bằng KCl không ảnh hưởng đáng kể đến quá trình làm nóng.
Có 3 phát biểu đúng là : a, c, d
Chọn đáp án C Đáp án: C
✔️(a) Đúng, vì Mg có thể phản ứng với nước tạo ra Mg(OH)2 và khí H2 ngay ở nhiệt độ thường
❌(b) Sai, vì Fe không phản ứng với nước ở nhiệt độ thường để tạo nhiệt. Nếu dùng 100% Fe, hỗn hợp không sinh nhiệt, làm giảm hiệu quả làm nóng thức ăn.
✔️(c) Đúng, vì quá nhiều nước sẽ hấp thụ nhiệt, làm giảm nhiệt độ tổng thể của hệ thống, khiến thức ăn không nóng hiệu quả.
✔️(d) Đúng, vì NaCl và KCl đều là muối tan tốt trong nước, giúp tạo môi trường điện ly hỗ trợ phản ứng, nhưng không trực tiếp sinh nhiệt. Do đó, thay NaCl bằng KCl không ảnh hưởng đáng kể đến quá trình làm nóng.
Có 3 phát biểu đúng là : a, c, d
Chọn đáp án C Đáp án: C
Câu 16 [705812]: Cho hai phức chất A và B có công thức lần lượt sau:
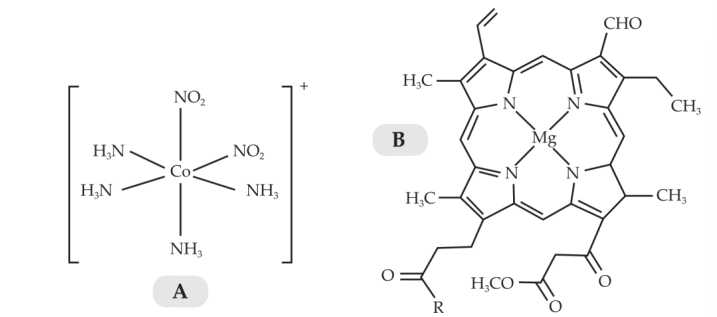
Phát biểu nào sau đây đúng?

Phát biểu nào sau đây đúng?
A, Trong phức chất B có 4 phối tử.
B, Hai phức chất A và B có dạng hình học khác nhau.
C, Trong A và trong B đều có hai loại phối tử.
D, Nguyên tử trung tâm của hai phức chất đều là nguyên tố kim loại chuyển tiếp.
Phân tích các phát biểu:
❌A. Trong phức chất B có 1 phối tử.
✔️B. A có dạng bát diện, B là phức có phối tử đa càng ⟹ Hai phức chất A và B có dạng hình học khác nhau.
❌C. Trong A có 2 loại phối tử là NO2 và NH3, trong B đều có 1 phối tử đa càng.
❌D. Co là kim loại chuyển tiếp, Mg không phải kim loại chuyển tiếp.
⟹ Chọn đáp án B
Đáp án: B
❌A. Trong phức chất B có 1 phối tử.
✔️B. A có dạng bát diện, B là phức có phối tử đa càng ⟹ Hai phức chất A và B có dạng hình học khác nhau.
❌C. Trong A có 2 loại phối tử là NO2 và NH3, trong B đều có 1 phối tử đa càng.
❌D. Co là kim loại chuyển tiếp, Mg không phải kim loại chuyển tiếp.
⟹ Chọn đáp án B
Đáp án: B
Sử dụng thông tin dưới đây, trả lời câu hỏi số 17, 18
Serotonin là một neurotransmitter quan trọng, ảnh hưởng đến tâm trạng, hành vi, ăn uống, giấc ngủ và nhiều chức năng cơ thể khác. Sự thiếu hụt serotonin có thể gây ra tình trạng trầm cảm.
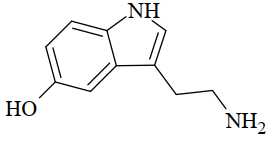

Câu 17 [705813]: Số nguyên tử hydrogen trong phân tử serotonin là
A, 10.
B, 12.
C, 14.
D, 16.
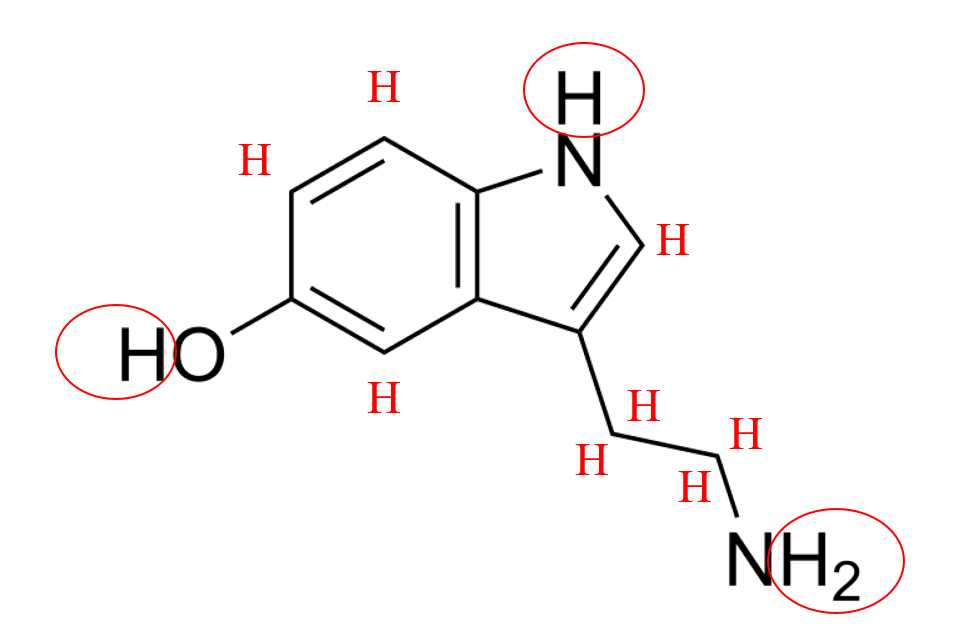
Tổng số hydrogen có trong Serotonin là 12
⟹ Chọn đáp án B
Câu 18 [705814]: 26,4 gam serotonin phản ứng vừa đủ với x mol NaOH. Giá trị của x là bao nhiêu?
A, 0,15 mol.
B, 0,3 mol.
C, 0,1 mol.
D, 0,2 mol.
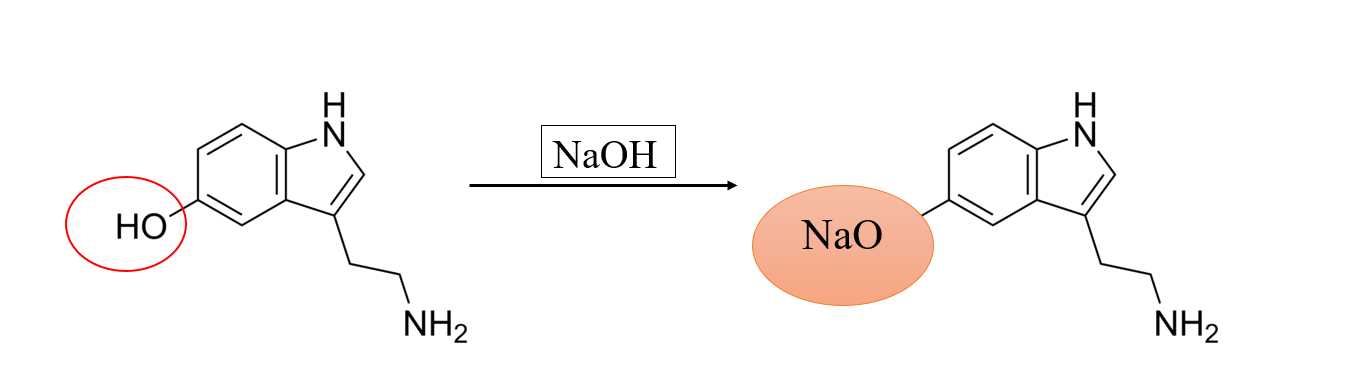
Phản ứng với NaOH vào nhóm OH của Serotonin. Serotonin có 1 nhóm OH => phản ứng với 1 NaOH
Số mol serotonin = m : M = 0,15 mol = n NaOH
⟹Chọn đáp án A
Đáp án: A
PHẦN II. Thí sinh trả lời từ câu 1 đến câu 4. Trong mỗi ý a), b), c), d) ở mỗi câu, thí sinh chọn đúng hoặc sai
Câu 19 [705815]: Sự hình thành nước thải acid mỏ (Acid mine drainage – AMD) được công nhận rộng rãi là một trong những vấn đề môi trường chính do khai thác mỏ trên toàn thế giới gây ra. Khoáng chất chịu trách nhiệm tạo ra AMD là sắt sulphide (pyrite), ổn định và không hòa tan khi không tiếp xúc với nước và oxygen trong khí quyển. Khi các loại quặng thải giàu pyrite được khai thác và được tiếp xúc với oxygen, nước khi có vi khuẩn Thiobacillus ferrooxidans, AMD được tạo ra do quá trình oxi hóa pyrite theo phương trình sau:
4FeS2(s) + 15O2(g) + 14H2O(1) → 4Fe(OH)3(s) + 8H2SO4(aq)
Một nhà máy khai thác mỏ copper – nickel, sản xuất 450 tấn quặng/ngày, thành phần quặng rắn chứa 5,00 % khối lượng pyrite và gặp phải vấn đề AMD. Sự rò rỉ acid ra ngoài môi trường đã dẫn đến sự xuống cấp của đất xung quanh mỏ. Để giải quyết vấn đề này, nhà máy đã sử dụng đá vôi để xử lý AMD theo phương trình như sau:
CaCO3(s) + H2SO4(aq) → CaSO4(s) + CO2(g) + H2O(l)
Một dòng sông bị xả thải nước acid mỏ, sau khi được xử lí thì tính acid của nước thải giảm, giá trị pH tăng từ 1,9 lên 6,0.
4FeS2(s) + 15O2(g) + 14H2O(1) → 4Fe(OH)3(s) + 8H2SO4(aq)
Một nhà máy khai thác mỏ copper – nickel, sản xuất 450 tấn quặng/ngày, thành phần quặng rắn chứa 5,00 % khối lượng pyrite và gặp phải vấn đề AMD. Sự rò rỉ acid ra ngoài môi trường đã dẫn đến sự xuống cấp của đất xung quanh mỏ. Để giải quyết vấn đề này, nhà máy đã sử dụng đá vôi để xử lý AMD theo phương trình như sau:
CaCO3(s) + H2SO4(aq) → CaSO4(s) + CO2(g) + H2O(l)
Một dòng sông bị xả thải nước acid mỏ, sau khi được xử lí thì tính acid của nước thải giảm, giá trị pH tăng từ 1,9 lên 6,0.
Phân tích các đáp án:
✔️A. Đúng. Có thể thay Ca(OH)2 cho đá vôi nhưng cần kiểm soát tốt hàm lượng Ca(OH)2 vì nếu dư thì sẽ làm đất có tính base.
Ca(OH)2 + H2SO4 ⟶ CaSO4 + H2O
✔️B. Đúng.
mFeS2 = 450 × 5% = 22,5 tấn ⟹ nFeS2 = m : M = 22,5 : 120 = 0,1875 mol
nH2SO4 = 4 × n = 0,375 mol ⟹ mH2SO4 = n × M = 36,75 tấn
❌C. Sai. Đất xung quanh mỏ AMD bị rò rỉ acid ⟹ H+ > OH-
✔️D. Đúng.
Tại pH = 1,9 => Nồng độ [H+] = 10-1,9 M
Tại pH = 6 => Nồng độ [H+] = 10-6 M
Lượng H+ đã mất đi là 10-1,9 - 10-6 M
Số mol của H+ cần cho mỗi lít dung dịch là nH+= 10-1,9 - 10-6 = 1,26.10-2 mol
Câu 20 [305834]: Tiến hành thí nghiệm theo các bước sau:
Bước 1: Cho vào cốc thủy tinh chịu nhiệt khoảng 5 gam mỡ lợn và 10 ml dung dịch NaOH 40%.
Bước 2: Đun sôi nhẹ hỗn hợp, liên tục khuấy đều bằng đũa thủy tinh khoảng 30 phút và thỉnh thoảng thêm nước cất để giữ cho thể tích hỗn hợp không đổi. Để nguội hỗn hợp.
Bước 3: Thêm vào hỗn hợp 15 – 20 ml dung dịch NaCl bão hòa nóng, khuấy nhẹ. Để yên hỗn hợp.
Bước 1: Cho vào cốc thủy tinh chịu nhiệt khoảng 5 gam mỡ lợn và 10 ml dung dịch NaOH 40%.
Bước 2: Đun sôi nhẹ hỗn hợp, liên tục khuấy đều bằng đũa thủy tinh khoảng 30 phút và thỉnh thoảng thêm nước cất để giữ cho thể tích hỗn hợp không đổi. Để nguội hỗn hợp.
Bước 3: Thêm vào hỗn hợp 15 – 20 ml dung dịch NaCl bão hòa nóng, khuấy nhẹ. Để yên hỗn hợp.
HD: Mỡ lợn chứa các chất béo no như tristearin, tripanmitin, khi đun sôi với dung dịch NaOH xảy ra phản ứng xà phòng hóa (thủy phân chất béo): (RCOO)3C3H5 + 3NaOH ––to→ 3RCOONa + C3H5(OH)3.
Sản phẩm thu được gồm muối và glixerol dễ tan trong dung dịch nên sau bước 2 ⇝ chất lỏng đồng nhất.
Ở bước 3: để nguội và hòa tan thêm NaCl (muối ăn) vào → làm giảm độ tan của muối natri stearat, thêm nữa khối lượng riêng của dung dịch lúc này cũng tăng lên → các muối hữu cơ (muối natri của các axit béo) bị tách ra khỏi dung dịch, nhẹ hơn dung dịch ⇝ tạo chất rắn màu trắng nổi lên trên dung dịch.
Xem xét các phát biểu:
✔️ a. đúng. Như phân tích, chất rắn nổi lên là muối acid béo, cũng chính là xà phòng.
✔️ b. đúng. Phản ứng tiến hành trong thời gian dài (30 phút) sẽ làm bay hơi nước, mà phản ứng thủy phân, không có nước thì phản ứng sao có thể xảy ra ⇝ cần bổ sung nước để đảm bảo phản ứng. Ở đây, việc giữ thể tích không đổi thực chất là 1 phép đo áng chứng để kiểm soát; bởi dung dịch chứa nhiều chất, không biết bao giờ là nước cạn hết,...
✔️ c. đúng. Đây là thí nghiệm về phản ứng xà phòng hóa, dầu thực vật hay dầu mỡ đều là chất béo nên đều được.
✔️ d. đúng. Phản ứng thủy phân thu được glycerol và muối acid béo chính là xà phòng ⇝ ứng dụng thực tiễn sản xuất trong công nghiệp.
Sản phẩm thu được gồm muối và glixerol dễ tan trong dung dịch nên sau bước 2 ⇝ chất lỏng đồng nhất.
Ở bước 3: để nguội và hòa tan thêm NaCl (muối ăn) vào → làm giảm độ tan của muối natri stearat, thêm nữa khối lượng riêng của dung dịch lúc này cũng tăng lên → các muối hữu cơ (muối natri của các axit béo) bị tách ra khỏi dung dịch, nhẹ hơn dung dịch ⇝ tạo chất rắn màu trắng nổi lên trên dung dịch.
Xem xét các phát biểu:
✔️ a. đúng. Như phân tích, chất rắn nổi lên là muối acid béo, cũng chính là xà phòng.
✔️ b. đúng. Phản ứng tiến hành trong thời gian dài (30 phút) sẽ làm bay hơi nước, mà phản ứng thủy phân, không có nước thì phản ứng sao có thể xảy ra ⇝ cần bổ sung nước để đảm bảo phản ứng. Ở đây, việc giữ thể tích không đổi thực chất là 1 phép đo áng chứng để kiểm soát; bởi dung dịch chứa nhiều chất, không biết bao giờ là nước cạn hết,...
✔️ c. đúng. Đây là thí nghiệm về phản ứng xà phòng hóa, dầu thực vật hay dầu mỡ đều là chất béo nên đều được.
✔️ d. đúng. Phản ứng thủy phân thu được glycerol và muối acid béo chính là xà phòng ⇝ ứng dụng thực tiễn sản xuất trong công nghiệp.
Câu 21 [705816]: Phương pháp kết tinh được sử dụng trong phòng thí nghiệm hóa học như một kỹ thuật tinh chế chất rắn. Một chất rắn không tinh khiết được hòa tan hoàn toàn trong một lượng nhỏ dung môi sôi nóng và dung dịch nóng được để nguội từ từ.
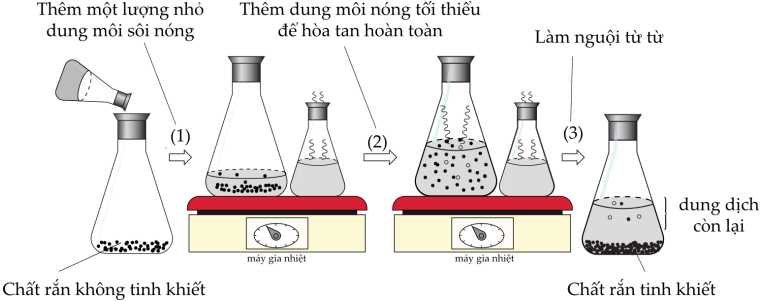

Phân tích các phát biểu:
✔️A. Đúng. Khi dung dịch nguội dần, các tinh thể của chất rắn kết tinh lại với độ tinh khiết cao vì tạp chất vẫn hòa tan trong dung dịch và không kết tinh theo.
✔️B. Đúng. Các tạp chất không kết tinh mà nằm lại trong dung dịch,do đó chúng không bị lẫn vào tinh thể sản phẩm.
❌C. Sai.Chất kết tinh có độ tan cao hơn khi tăng nhiệt độ.
✔️D. Đúng. Dung dịch sau kết tinh (phần dung dịch còn lại sau khi chất kết tinh đã tách ra) là dung dịch bão hòa của chất cần kết tinh tại nhiệt độ đó.
✔️A. Đúng. Khi dung dịch nguội dần, các tinh thể của chất rắn kết tinh lại với độ tinh khiết cao vì tạp chất vẫn hòa tan trong dung dịch và không kết tinh theo.
✔️B. Đúng. Các tạp chất không kết tinh mà nằm lại trong dung dịch,do đó chúng không bị lẫn vào tinh thể sản phẩm.
❌C. Sai.Chất kết tinh có độ tan cao hơn khi tăng nhiệt độ.
✔️D. Đúng. Dung dịch sau kết tinh (phần dung dịch còn lại sau khi chất kết tinh đã tách ra) là dung dịch bão hòa của chất cần kết tinh tại nhiệt độ đó.
Câu 22 [705817]: Rất nhiều tính chất vật lí của kim loại có thể được giải thích thông qua mô hình mô tả khái quát cation kim loại và các electron hoá trị tự do trong tinh thể kim loại dưới đây:
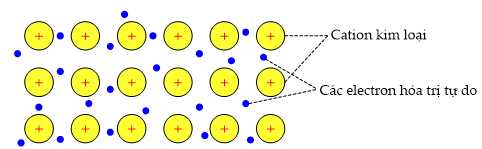

Phân tích các phát biểu:
✔️ A. Đúng. Tinh thể kim loại bao gồm các cation kim loại (ion dương) sắp xếp theo mạng tinh thể và các electron hóa trị tự do di chuyển giữa chúng.
✔️ B. Đúng. Trong tinh thể kim loại, các cation kim loại được sắp xếp theo trật tự xác định, tạo thành mạng lưới tinh thể. Điều này giúp kim loại có tính chất cơ học bền vững.
✔️ C. Đúng. Khi có điện trường tác động, các electron hóa trị tự do có thể di chuyển theo hướng ngược với điện trường, tạo nên dòng điện. Đây là lý do kim loại có tính dẫn điện cao.
❌ D. Sai. Liên kết kim loại không phải là liên kết ion (giữa cation kim loại và anion gốc axit). Thay vào đó, nó hình thành nhờ lực hút tĩnh điện giữa các cation kim loại và "biển electron" tự do. Điều này giúp kim loại có độ dẻo và tính dẫn điện cao hơn so với tinh thể ion.
✔️ A. Đúng. Tinh thể kim loại bao gồm các cation kim loại (ion dương) sắp xếp theo mạng tinh thể và các electron hóa trị tự do di chuyển giữa chúng.
✔️ B. Đúng. Trong tinh thể kim loại, các cation kim loại được sắp xếp theo trật tự xác định, tạo thành mạng lưới tinh thể. Điều này giúp kim loại có tính chất cơ học bền vững.
✔️ C. Đúng. Khi có điện trường tác động, các electron hóa trị tự do có thể di chuyển theo hướng ngược với điện trường, tạo nên dòng điện. Đây là lý do kim loại có tính dẫn điện cao.
❌ D. Sai. Liên kết kim loại không phải là liên kết ion (giữa cation kim loại và anion gốc axit). Thay vào đó, nó hình thành nhờ lực hút tĩnh điện giữa các cation kim loại và "biển electron" tự do. Điều này giúp kim loại có độ dẻo và tính dẫn điện cao hơn so với tinh thể ion.
PHẦN III. Thí sinh trả lời từ câu 1 đến câu 6.
Câu 23 [705818]: Khi làm lạnh dung dịch FeCl3 thu được tinh thể FeCl3.6H2O. Cho độ tan của FeCl3.6H2O trong nước ở một số nhiệt độ như sau:
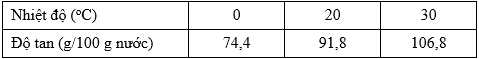
Để tạo ra dung dịch bão hoà của FeCl3 ở 20oC từ 50 g nước thì cần bao nhiêu gam FeCl3.6H2O?

Để tạo ra dung dịch bão hoà của FeCl3 ở 20oC từ 50 g nước thì cần bao nhiêu gam FeCl3.6H2O?
Trong 100g nước độ tan của FeCl3.6H2O là 91,8 g
Trong 50g nước độ tan của FeCl3.6H2O là :
91,8 : 2 = 45,9 (g)
Điền đáp án: 45,9
Trong 50g nước độ tan của FeCl3.6H2O là :
91,8 : 2 = 45,9 (g)
Điền đáp án: 45,9
Câu 24 [705819]: Cho 4 dung dịch riêng biệt sau: (a) Fe2(SO4)3; (b) H2SO4 loãng; (c) CuSO4; (d) H2SO4 loãng có lẫn CuSO4. Nhúng vào mỗi dung dịch thanh Zn nguyên chất. Số trường hợp xuất hiện ăn mòn điện hóa là
Ăn mòn điện hóa xảy ra khi có các điều kiện sau:
- Có hai chất dẫn điện khác nhau (kim loại hoặc phi kim) tiếp xúc trực tiếp hoặc gián tiếp qua dung dịch điện ly.
- Có môi trường điện ly (dung dịch chứa ion).
- Có sự chênh lệch điện thế giữa hai chất dẫn điện, dẫn đến dòng electron di chuyển.
Phân tích các trường hợp:
(a) Fe2(SO4)3 : có phản ứng:
Zn + 2Fe3+ ⟶ Zn2+ + 2Fe2+
Fe2+ tiếp tục bị khử thành Fe kim loại bám lên Zn, sẽ tạo thành cặp điện cực Zn - Fe trong dung dịch điện ly → Xảy ra ăn mòn điện hóa.
(b) H2SO4 loãng : Chỉ có một kim loại tham gia, không hình thành cặp điện cực → Không có ăn mòn điện hóa.
Zn + H2SO4 ⟶ ZnSO4 + H2
(c) CuSO4: (Cu) bám lên Zn, tạo thành cặp điện cực Zn - Cu → Xảy ra ăn mòn điện hóa.
Zn + Cu2+ ⟶ Zn2+ + Cu
(d) H2SO4 loãng lẫn CuSO4 : Cu kết tủa trên bề mặt Zn, tạo thành cặp điện cực Zn - Cu trong môi trường điện ly → Xảy ra ăn mòn điện hóa.
Có 3 trường hợp xảy ra ăn mòn điện hóa là : a, c, d
Điền đáp án: 3
- Có hai chất dẫn điện khác nhau (kim loại hoặc phi kim) tiếp xúc trực tiếp hoặc gián tiếp qua dung dịch điện ly.
- Có môi trường điện ly (dung dịch chứa ion).
- Có sự chênh lệch điện thế giữa hai chất dẫn điện, dẫn đến dòng electron di chuyển.
Phân tích các trường hợp:
(a) Fe2(SO4)3 : có phản ứng:
Zn + 2Fe3+ ⟶ Zn2+ + 2Fe2+
Fe2+ tiếp tục bị khử thành Fe kim loại bám lên Zn, sẽ tạo thành cặp điện cực Zn - Fe trong dung dịch điện ly → Xảy ra ăn mòn điện hóa.
(b) H2SO4 loãng : Chỉ có một kim loại tham gia, không hình thành cặp điện cực → Không có ăn mòn điện hóa.
Zn + H2SO4 ⟶ ZnSO4 + H2
(c) CuSO4: (Cu) bám lên Zn, tạo thành cặp điện cực Zn - Cu → Xảy ra ăn mòn điện hóa.
Zn + Cu2+ ⟶ Zn2+ + Cu
(d) H2SO4 loãng lẫn CuSO4 : Cu kết tủa trên bề mặt Zn, tạo thành cặp điện cực Zn - Cu trong môi trường điện ly → Xảy ra ăn mòn điện hóa.
Có 3 trường hợp xảy ra ăn mòn điện hóa là : a, c, d
Điền đáp án: 3
Câu 25 [705820]: Khi đun nóng X với hỗn hợp HNO3 đặc và H2SO4 đặc có thể thu được cellulose trinitrate, là chất dễ cháy và nổ mạnh, dùng để chế tạo thuốc súng không khói. Từ 4 lít dung dịch HNO3 63% (khối lượng riêng 1,5 g/mL) có thể điều chế m kg cellulose trinitrate với hiệu suất phản ứng đạt 70%. Xác định giá trị của m.
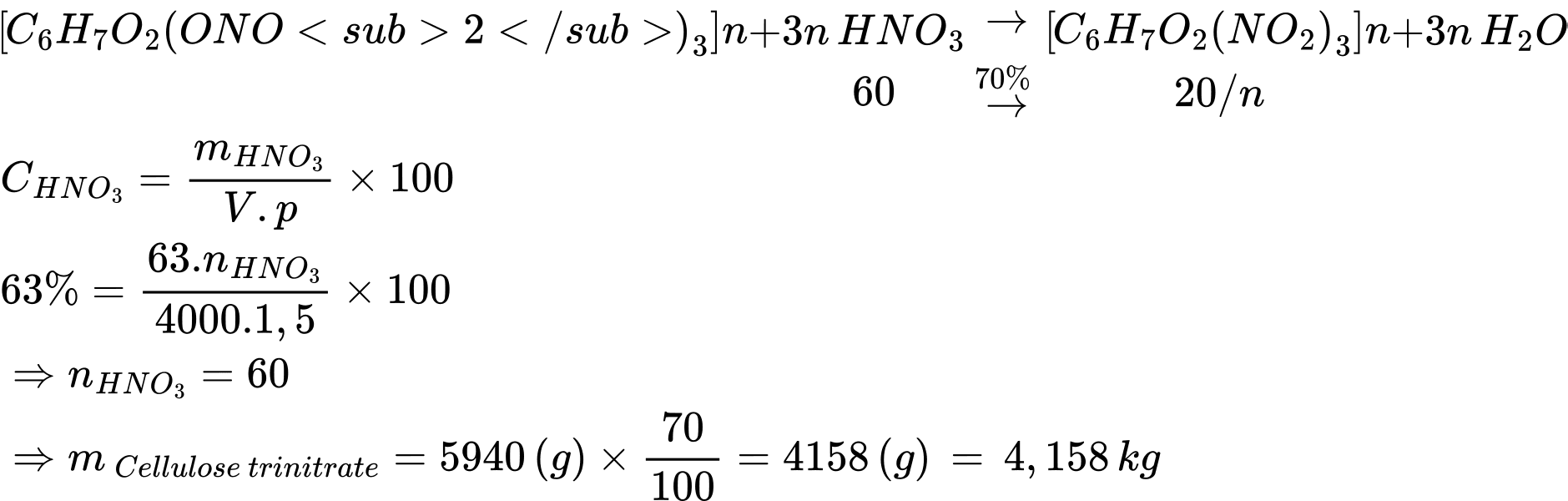
Điền đáp án: 4,16
Câu 26 [705821]: Cấu trúc của một peptide được đưa ra dưới đây:
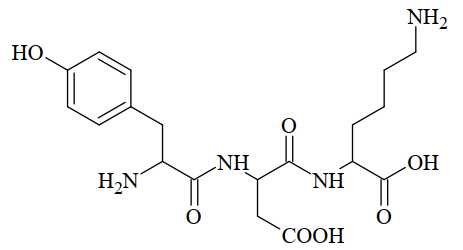
Nếu giá trị tuyệt đối của điện tích ứng với dạng tồn tại chủ yếu của peptide ở pH = 2, pH = 6 và pH = 11 lần lượt là |z1 |, |z2 | và |z3 | thì |𝑧1 | + |𝑧2 | + |𝑧3 | bằng bao nhiêu?

Nếu giá trị tuyệt đối của điện tích ứng với dạng tồn tại chủ yếu của peptide ở pH = 2, pH = 6 và pH = 11 lần lượt là |z1 |, |z2 | và |z3 | thì |𝑧1 | + |𝑧2 | + |𝑧3 | bằng bao nhiêu?
- Tại pH = 2 : cung cấp môi trường H+
2 nhóm NH2 ⟹ NH3+
2 nhóm COOH điện tích = 0
⟹ |z1| = 2
- Tại pH = 6 : tồn tại dạng ion lưỡng cực
2 nhóm NH2 ⟹ NH3+
2 nhóm COOH ⟹ COO-
⟹ |z2| = 0
- Tại pH = 11: cung cấp ion OH-
2 nhóm COOH ⟹ COO-
⟹ |z3| = 2
⟹ |z1| + |z2| + |z3| = 2 + 0 + 2 = 4
Điền đáp án: 4
2 nhóm NH2 ⟹ NH3+
2 nhóm COOH điện tích = 0
⟹ |z1| = 2
- Tại pH = 6 : tồn tại dạng ion lưỡng cực
2 nhóm NH2 ⟹ NH3+
2 nhóm COOH ⟹ COO-
⟹ |z2| = 0
- Tại pH = 11: cung cấp ion OH-
2 nhóm COOH ⟹ COO-
⟹ |z3| = 2
⟹ |z1| + |z2| + |z3| = 2 + 0 + 2 = 4
Điền đáp án: 4
Câu 27 [705822]: Hàm lượng vitamin C (ascorbic acid, C6H8O6) có trong các loại đồ uống thể thao có thể được bằng cách chuẩn độ với dung dịch iodine.
I2(aq) + C6H8O6(aq) 2I−(aq) + C6H6O6(aq) + 2H+(aq)
Lấy 25,0 mL một mẫu đồ uống thể thao, tiến hành chuẩn độ thì thấy cần dùng 29,25 mL dung dịch I2 1,25×10–3 M để đạt đến điểm tương đương. Khối lượng vitamin C (tính bằng mg) chứa trong chai 350 mL dung dịch đồ uống thể thao đó là bao nhiêu (Làm tròn đến số nguyên)?
I2(aq) + C6H8O6(aq) 2I−(aq) + C6H6O6(aq) + 2H+(aq)
Lấy 25,0 mL một mẫu đồ uống thể thao, tiến hành chuẩn độ thì thấy cần dùng 29,25 mL dung dịch I2 1,25×10–3 M để đạt đến điểm tương đương. Khối lượng vitamin C (tính bằng mg) chứa trong chai 350 mL dung dịch đồ uống thể thao đó là bao nhiêu (Làm tròn đến số nguyên)?
Số mol I2 : nI2 = CM . V = 1,25.10-3 . 29,25 . 10-3 = 3,65625.10-5 mol
Ta có phương trình: I2 + C6H8O6 ⟶ 2I- + C6H6O6 + 2H+
nI2 = nC6H8O6 = 3,65625 . 10-5 ⟶ 25mL
5,11875 . 10-4 ⟵ 350mL
m vitamin = 0,09009 = 90,09 mg
Điền đáp án: 90
Ta có phương trình: I2 + C6H8O6 ⟶ 2I- + C6H6O6 + 2H+
nI2 = nC6H8O6 = 3,65625 . 10-5 ⟶ 25mL
5,11875 . 10-4 ⟵ 350mL
m vitamin = 0,09009 = 90,09 mg
Điền đáp án: 90
Câu 28 [705823]: Phân tích nhiệt trọng là kỹ thuật phân tích để xác định thành phần các chất rắn bị phân hủy khi đun nóng. Sự thay đổi khối lượng được đo trong quá trình đun nóng sẽ cung cấp các thông tin về thành phần của chất ban đầu. Đun nóng 4,96 gam hỗn hợp CaC2O4 và MgC2O4 đến 1200°C, trong quá trình này khối lượng hỗn hợp chất rắn được đo liên tục. Biết rằng có 2 phản ứng phân hủy xảy ra ở khoảng 400°C:
MgC2O4(s) → MgO(s) + CO(g) + CO2(g)
CaC2O4(s) → CaCO3(s) + CO(g)
Ở 900°C quan sát được phản ứng phân hủy thứ 3. Khi các phản ứng xảy ra hoàn toàn thu được 2,008 gam chất rắn. Tính phần trăm khối lượng của CaC2O4 trong 4,96 gam hỗn hợp ban đầu (Làm tròn đến hàng phần mười).
MgC2O4(s) → MgO(s) + CO(g) + CO2(g)
CaC2O4(s) → CaCO3(s) + CO(g)
Ở 900°C quan sát được phản ứng phân hủy thứ 3. Khi các phản ứng xảy ra hoàn toàn thu được 2,008 gam chất rắn. Tính phần trăm khối lượng của CaC2O4 trong 4,96 gam hỗn hợp ban đầu (Làm tròn đến hàng phần mười).
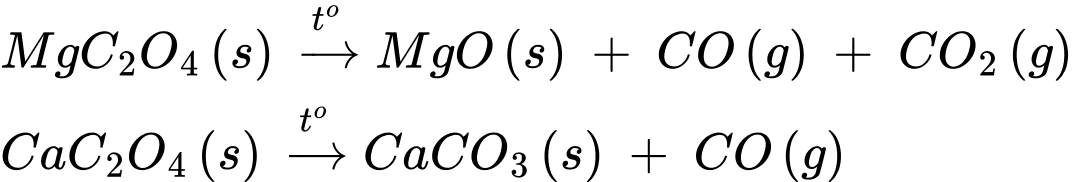
Ở 900 oC quan sát được phản ứng phân hủy thứ 3 là phân hủy CaCO3
 .
.
Gọi: nMgC2O4 = a (mol); nCaC2O4 = b (mol)
Khối lượng hỗn hợp là: mMgC2O4 + mCaC2O4 = 112a + 128b = 4,96 (gam) (1)
Từ PTHH số mol của MgO và CaO lần lượt là a và b mol
Khối lượng chất rắn sau nung là: mMgO + mCaO = 40a + 56b = 2,008 (gam) (2)
Từ phương trình (1) và (2) → a = 0,018 mol; b = 0,023 mol
Phần trăm khối lượng của CaC2O4 trong 4,96 gam hỗn hợp ban đầu là:
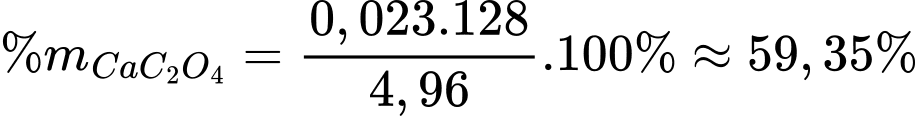
⇒ Điền đáp án: 59,4