PHẦN I. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
Câu 1 [705902]: “Trong phương pháp điện hoá, để bảo vệ ...(1)..., người ta nối kim loại cần bảo vệ với một kim loại hoạt động hoá học ...(2)...”. Nội dung phù hợp trong các ô trống (1), (2) lần lượt là
A, phi kim, yếu hơn.
B, hợp chất, mạnh hơn.
C, đơn chất, yếu hơn.
D, kim loại, mạnh hơn.
Phương pháp điện hoá: gắn kim loại có tính khử mạnh hơn vào vật cần bảo vệ, kim loại sẽ bị ăn mòn vật được bảo vệ.
“Trong phương pháp điện hoá, để bảo vệ kim loại, người ta nối kim loại cần bảo vệ với một kim loại hoạt động hoá học mạnh hơn”.
⟹ Chọn đáp án D Đáp án: D
“Trong phương pháp điện hoá, để bảo vệ kim loại, người ta nối kim loại cần bảo vệ với một kim loại hoạt động hoá học mạnh hơn”.
⟹ Chọn đáp án D Đáp án: D
Câu 2 [705903]: Phèn nhôm – kali là muối sulfate kép của potassium và nhôm. Công thức hóa học của phèn nhôm – kali là
A, KAl(SO4)2.
B, NaAl(SO4)2.
C, (NH4)Al(SO4)2.
D, KAl(SO4)2.12H2O.
Kali alum là muối sulfate kép của potasium và aluminium. Tên tiếng Việt phổ biến là phèn chua. Công thức hóa học là KAl(SO4)2 và thông thường được thấy ở dạng ngậm nước là KAl(SO4)2.12H2O. Chất này được sử dụng rộng rãi để làm trong nước đục, thuộc da, sản xuất vải chống cháy và bột nở.
Phèn chua là loại muối có tinh thể to nhỏ không đều, không màu hoặc trắng, cũng có thể trong hoặc hơi đục. Phèn chua tan trong nước nhưng không tan trong cồn.
Chọn đáp án D Đáp án: D
Phèn chua là loại muối có tinh thể to nhỏ không đều, không màu hoặc trắng, cũng có thể trong hoặc hơi đục. Phèn chua tan trong nước nhưng không tan trong cồn.
Chọn đáp án D Đáp án: D
Câu 3 [705904]: Glucose là đường monosaccharide phổ biến và có nhiều ứng dụng trong đời sống. Trong phân tử glucose ở dạng mạch hở có bao nhiêu nhóm –OH?
A, 5.
B, 4.
C, 6.
D, 3.
-Dạng mạch hở (ít)
+ Glucose: CH2OH-[CHOH]4-CHO có 5 nhóm hydroxy (OH) + 1 nhóm aldehyde (CHO).
- Dạng mạch vòng chủ yếu và luôn chuyển hoá lẫn nhau theo một cân bằng qua dạng mạch hở.
+ Glucose vòng 6 cạnh alpha - glucose và beta -glucose.
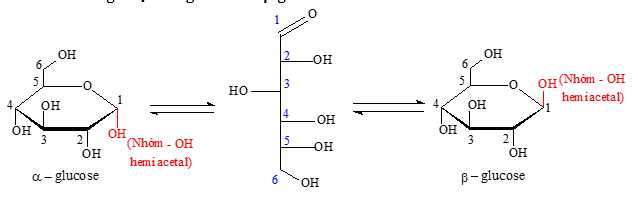
Chọn đáp án A Đáp án: A
+ Glucose: CH2OH-[CHOH]4-CHO có 5 nhóm hydroxy (OH) + 1 nhóm aldehyde (CHO).
- Dạng mạch vòng chủ yếu và luôn chuyển hoá lẫn nhau theo một cân bằng qua dạng mạch hở.
+ Glucose vòng 6 cạnh alpha - glucose và beta -glucose.

Chọn đáp án A Đáp án: A
Câu 4 [705905]: Tơ nhân tạo hay tơ bán tổng hợp xuất phát từ polymer thiên nhiên nhưng được chế biến thêm bằng phương pháp hóa học. Tơ nào sau đây là tơ nhân tạo?
A, Tơ visco.
B, Tơ nylon-6,6.
C, Tơ nitron.
D, Tơ tằm.
Tơ bán tổng hợp: Đây là những loại tơ nhân tạo xuất phát từ polymer thiên nhiên nhưng được chế biến thêm bằng phương pháp hoá học.
Tơ visco: Thành phần chính là cellulose đã được xử lí hoá chất.
Chọn đáp án A Đáp án: A
Tơ visco: Thành phần chính là cellulose đã được xử lí hoá chất.
Chọn đáp án A Đáp án: A
Câu 5 [705906]: Vì sao không nên sử dụng vật dụng bằng nhôm để đựng thức ăn chua (như canh chua, nước mắm) trong thời gian dài?
A, Thức ăn chua làm hòa tan lớp oxide nhôm bảo vệ, gây ăn mòn nhôm.
B, Thức ăn chua làm nhôm bị nóng chảy nhanh hơn.
C, Nhôm phản ứng với thức ăn tạo khí độc.
D, Thức ăn chua làm nhôm bị đen và kém thẩm mỹ.
Khi độ chua của thức ăn làm ăn mòn đồ vật bằng nhôm, hòa tan lớp Al2O3 của đồ vật bằng nhôm
Al2O3 + 6H+ → 2Al3+ + 3H2O
2Al + 6H+ → 2Al3+ + 3H2
Chọn đáp án A Đáp án: A
Al2O3 + 6H+ → 2Al3+ + 3H2O
2Al + 6H+ → 2Al3+ + 3H2
Chọn đáp án A Đáp án: A
Câu 6 [705907]: Kim loại kiềm thổ nào thường được sử dụng làm chất chống tia phóng xạ?
A, Be.
B, Mg.
C, Ca.
D, Ba.
Hợp chất BaSO4 được sử dụng làm chất cản quang phóng xạ trong chụp X-quang. BaCO3 sử dụng trong sản xuất thủy tinh. BaNO3 sử dụng trong chế tạo pháo hoa…
Chọn đáp án D Đáp án: D
Chọn đáp án D Đáp án: D
Câu 7 [705908]: Đất sét polymer là một loại đất sét làm mô hình có độ cứng, dựa trên poly(vinyl chloride) (PVC). Đất sét polymer không chứa khoáng chất đất sét, nhưng khi PVC được trộn với một chất lỏng sẽ thu được vật liệu giống như đất sét; do đó, thường được gọi là đất sét và được dùng để làm đồ chơi, đồ thủ công, đồ trang trí. Các ứng dụng này dựa trên tính chất nào của PVC?
A, Tính đàn hồi.
B, Tính cứng.
C, Tính không độc hại.
D, Tính dẻo.
Tính dẻo của vật liệu là tính bị biến dạng khi chịu tác dụng của nhiệt, của áp lực bên ngoài và vẫn giữ được sự biến dạng đó khi thôi tác dụng.
Chọn đáp án D Đáp án: D
Chọn đáp án D Đáp án: D
Câu 8 [705909]: Dung dịch chứa chất nào sau đây sẽ có khả năng dẫn điện tốt nhất?
A, NH3.
B, HClO4.
C, K2SO4.
D, KMnO4.
1 mol NH3 trong dung dịch phân li không hoàn toàn thành 1 mol NH4+ và 1 mol OH-
1 mol HClO4 trong dung dịch phân li hòa toàn thành 1 mol H+ và 1 mol ClO4-
1 mol K2SO4 trong dung dịch phân li hòa toàn thành 2 mol K+ và 1 mol SO42-
1 mol KMnO4 trong dung dịch phân li hòa toàn thành 1 mol K+ và 1 mol MnO4-
→ Dung dịch K2SO4 có độ dẫn điện tốt nhất.
Chọn đáp án C Đáp án: C
1 mol HClO4 trong dung dịch phân li hòa toàn thành 1 mol H+ và 1 mol ClO4-
1 mol K2SO4 trong dung dịch phân li hòa toàn thành 2 mol K+ và 1 mol SO42-
1 mol KMnO4 trong dung dịch phân li hòa toàn thành 1 mol K+ và 1 mol MnO4-
→ Dung dịch K2SO4 có độ dẫn điện tốt nhất.
Chọn đáp án C Đáp án: C
Câu 9 [524953]: Cho dãy các chất: trans-but-2-ene, buta-1,3-diene (CH2=CH–CH=CH2), dimethylacetylene, vinylacetylene. Số chất trong dãy tham khi phản ứng hoàn toàn với khí H2 dư (xúc tác Ni, to) tạo ra butane là
A, 2.
B, 4.
C, 1.
D, 3.
Số chất trong dãy tham khi phản ứng hoàn toàn với khí H2 dư (xúc tác Ni, t0) tạo ra butane là: trans-but-2-ene, buta-1,3-diene, dimethylacetylene, vinylacetylene
(1) CH3-CH=CH-CH3 + H2 ⟶ CH3-CH2-CH2-CH3
(2) CH2=CH-CH=CH2 + 2H2 ⟶ CH3-CH2-CH2-CH3
(3) CH3-C≡C-CH3 + 2H2 ⟶ CH3-CH2-CH2-CH3
(4) CH2=CH-C≡CH + 3H2 ⟶ CH3-CH2-CH2-CH3
Chọn đáp án B
Đáp án: B
(1) CH3-CH=CH-CH3 + H2 ⟶ CH3-CH2-CH2-CH3
(2) CH2=CH-CH=CH2 + 2H2 ⟶ CH3-CH2-CH2-CH3
(3) CH3-C≡C-CH3 + 2H2 ⟶ CH3-CH2-CH2-CH3
(4) CH2=CH-C≡CH + 3H2 ⟶ CH3-CH2-CH2-CH3
Chọn đáp án B
Đáp án: B
Câu 10 [247235]: Mỗi orbital nguyên tử chứa tối đa
A, 1 electron.
B, 2 electron.
C, 3 electron.
D, 4 electron.
Mỗi orbital nguyên tử chứa tối đa 2 electron. Đáp án: B
Câu 11 [705910]: Trong pin Galvani, nếu rút cầu muối ra thì hiệu điện thế giữa hai điện cựccủa pin sẽ
A, bằng 0.
B, không thay đổi.
C, tăng từ từ.
D, giảm từ từ.
Dựa vào lí thuyết về pin điện hoá. Trong pin Galvani, nếu rút cầu muối ra thì hiệu điện thế giữa hai điện cực của pin sẽ bằng 0 vì mạch điện không khép kín, nên sẽ không có dòng điện chạy qua hai điện cực.
⟹ Chọn đáp án A Đáp án: A
⟹ Chọn đáp án A Đáp án: A
Câu 12 [252437]: Nung 8,1 gam bột aluminum với 38,1 gam iodine, biết hiệu suất phản ứng là 80%. Khối lượng (g) aluminum iodide thu được là
A, 32,64.
B, 46,2.
C, 36,96.
D, 97,92.
số mol của Al = 0,3 mol; số mol của I2 = 0,15 mol
2Al + 3I2 2AlI3
2AlI3
Ban đầu 0,3 0,15
Phản ứng0,1 0,15 0,1
Khối lượng AlI3 = 0,1 (27+ 127.3). 80% = 32,64 gam
Chọn đáp án A Đáp án: A
2Al + 3I2
Ban đầu 0,3 0,15
Phản ứng0,1 0,15 0,1
Khối lượng AlI3 = 0,1 (27+ 127.3). 80% = 32,64 gam
Chọn đáp án A Đáp án: A
Câu 13 [705911]: Để điều chế một lượng nhỏ khí chlorine trong phòng thí nghiệm, người ta cho dung dịch HCl đặc phản ứng với MnO2 rắn theo sơ đồ thí nghiệm như hình dưới đây:
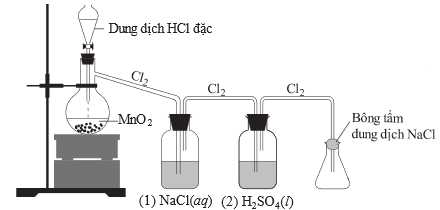
Trong đó: Bình (1) chứa NaCl(aq) giúp giữ khí HCl, bình (2) chứa H2SO4(l) đặc giúp hút ẩm, làm khô khí, bảo đảm chất lượng chlorine. Cho các phát biểu sau:
(a) Dung dịch HCl đặc đóng vai trò là chất oxi hoá trong phản ứng điều chế chlorine.
(b) Bông tẩm dung dịch NaOH giúp ngăn khí chlorine rò rỉ ra ngoài.
(c) Khi thay MnO2 bằng KMnO4 cùng khối lượng, lượng Cl2 thu được sẽ nhiều hơn, biết HCl đặc dùng dư.
(d) Nếu hoán đổi vị trí bình (1) và bình (2), chất lượng khí chlorine thu được sẽ không đổi.
Các phát biểu đúng là

Trong đó: Bình (1) chứa NaCl(aq) giúp giữ khí HCl, bình (2) chứa H2SO4(l) đặc giúp hút ẩm, làm khô khí, bảo đảm chất lượng chlorine. Cho các phát biểu sau:
(a) Dung dịch HCl đặc đóng vai trò là chất oxi hoá trong phản ứng điều chế chlorine.
(b) Bông tẩm dung dịch NaOH giúp ngăn khí chlorine rò rỉ ra ngoài.
(c) Khi thay MnO2 bằng KMnO4 cùng khối lượng, lượng Cl2 thu được sẽ nhiều hơn, biết HCl đặc dùng dư.
(d) Nếu hoán đổi vị trí bình (1) và bình (2), chất lượng khí chlorine thu được sẽ không đổi.
Các phát biểu đúng là
A, (a), (c).
B, (b), (c).
C, (a), (b), (c).
D, (b), (c), (d).
❌ (a) – Sai. Dung dịch HCl đặc đóng vai trò là chất khử trong phản ứng điều chế chlorine.
MnO2 + 4HCl → MnCl2 + Cl2 + 2H2O
Quá trình oxi hóa: 2Cl- ⟶ Cl2 + 2e
Quá trình khử: Mn4+ + 2e ⟶ Mn2+
✔️ (b) – Đúng. Bông tẩm dung dịch NaOH giúp ngăn khí chlorine rò rỉ ra ngoài.
2NaOH + 2Cl2 → 2NaCl + NaClO + H2O
✔️(c) – Đúng. Khi thay MnO2 bằng KMnO4 cùng khối lượng, lượng Cl2 thu được sẽ nhiều hơn, biết HCI đặc dùng dư.
MnO2 + 4HCl → MnCl2 + Cl2 + 2H2O
2KMnO4 + 16HCl → 2KCl + 2MnCl2 + 5Cl2 + 8H2O
1 mol MnO2 tạo ra 1 mol Cl2
1 mol KMnO4 tạo ra 2,5 mol Cl2
❌ (d) – Sai. Không thể hoán đổi bình (1) và (2), giai đoạn làm khô phải ở sau cùng. Nếu làm khô trước rồi lại dẫn qua dung dịch thì Cl2 sẽ bị ẩm.
Chọn đáp án B Đáp án: B
MnO2 + 4HCl → MnCl2 + Cl2 + 2H2O
Quá trình oxi hóa: 2Cl- ⟶ Cl2 + 2e
Quá trình khử: Mn4+ + 2e ⟶ Mn2+
✔️ (b) – Đúng. Bông tẩm dung dịch NaOH giúp ngăn khí chlorine rò rỉ ra ngoài.
2NaOH + 2Cl2 → 2NaCl + NaClO + H2O
✔️(c) – Đúng. Khi thay MnO2 bằng KMnO4 cùng khối lượng, lượng Cl2 thu được sẽ nhiều hơn, biết HCI đặc dùng dư.
MnO2 + 4HCl → MnCl2 + Cl2 + 2H2O
2KMnO4 + 16HCl → 2KCl + 2MnCl2 + 5Cl2 + 8H2O
1 mol MnO2 tạo ra 1 mol Cl2
1 mol KMnO4 tạo ra 2,5 mol Cl2
❌ (d) – Sai. Không thể hoán đổi bình (1) và (2), giai đoạn làm khô phải ở sau cùng. Nếu làm khô trước rồi lại dẫn qua dung dịch thì Cl2 sẽ bị ẩm.
Chọn đáp án B Đáp án: B
Câu 14 [305726]: Chất nào sau chỉ tác dụng với NaOH dư trong dung dịch theo tỉ lệ số mol 1 : 1?
A, Phenyl acetate.
B, Triolein.
C, Tristearin.
D, Methyl acrylate.
Phân tích các chất:
❌ A. Phenyl acetae: CH3COOC6H5: ester của phenol nên tác dụng NaOH tỉ lệ 1 : 2:
CH3COOC6H5 + 2NaOH ⟶ CH3COONa + C6H5ONa + H2O.
❌ B. Triolein: (C17H33COO)3C3H5: chất béo ⟶ tác dụng NaOH tỉ lệ 1 : 3:
(C17H33COO)3C3H5 + 3NaOH ⟶3C17H33COONa + C3H5(OH)3.
❌ C. Tristearin: (C17H35COO)3C3H5: chất béo ⟶ tác dụng NaOH tỉ lệ 1 : 3:
(C17H35COO)3C3H5 + 3NaOH ⟶ 3C17H35COONa + C3H5(OH)3.
✔️ D. Methyl acrylate: CH2=CHCOOCH3: ester đơn chức thường ⟶ tác dụng NaOH tỉ lệ 1 : 1:
CH2=CHCOOCH3 + NaOH ⟶ CH2=CHCOONa + CH3OH.
⟹Chọn đáp án D Đáp án: D
❌ A. Phenyl acetae: CH3COOC6H5: ester của phenol nên tác dụng NaOH tỉ lệ 1 : 2:
CH3COOC6H5 + 2NaOH ⟶ CH3COONa + C6H5ONa + H2O.
❌ B. Triolein: (C17H33COO)3C3H5: chất béo ⟶ tác dụng NaOH tỉ lệ 1 : 3:
(C17H33COO)3C3H5 + 3NaOH ⟶3C17H33COONa + C3H5(OH)3.
❌ C. Tristearin: (C17H35COO)3C3H5: chất béo ⟶ tác dụng NaOH tỉ lệ 1 : 3:
(C17H35COO)3C3H5 + 3NaOH ⟶ 3C17H35COONa + C3H5(OH)3.
✔️ D. Methyl acrylate: CH2=CHCOOCH3: ester đơn chức thường ⟶ tác dụng NaOH tỉ lệ 1 : 1:
CH2=CHCOOCH3 + NaOH ⟶ CH2=CHCOONa + CH3OH.
⟹Chọn đáp án D Đáp án: D
Câu 15 [705912]: “Acid béo omega-3, omega-6 là một trong những thành phần quan trọng giúp cơ thể đủ năng lượng để hoạt động tốt, cân bằng việc hấp thu thức ăn. Trong acid béo omega-3, liên kết đôi C=C ở vị trí nguyên tử carbon thứ ...(1)... tính từ nhóm ...(2)...” . Nội dung phù hợp trong ô trống (1), (2) lần lượt là
A, ba, carboxylic (–COOH)
B, ba, methylene (–CH2)
C, ba, methyl (–CH3).
D, ba, ethyl (–C2H5).
“Acid béo omega-3, omega-6 là một trong những thành phần quan trọng giúp cơ thể đủ năng lượng để hoạt động tốt, cân bằng việc hấp thu thức ăn. Trong acid béo omega-3, liên kết đôi C=C ở vị trí nguyên tử carbon thứ ba tính từ nhóm methyl”.
Chọn đáp án C Đáp án: C
Chọn đáp án C Đáp án: C
Câu 16 [705913]: Dạng hình học của phức chất được xác nhận bằng thực nghiệm. Phức chất mà xung quanh nguyên tử trung tâm có 4 liên kết σ thường có dạng hình học là tứ diện hoặc vuông phẳng và được gọi là phức chất tứ diện hoặc phức chất vuông phẳng. Phức chất mà xung quanh nguyên tử trung tâm có 6 liên kết σ có dạng hình học là bát diện và được gọi là phức chất bát diện. Cấu trúc của phức chất [PtCl4]2– được cho dưới đây:
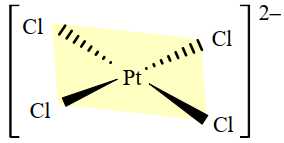
Cho các phát biểu sau:
(a) Phức chất có 4 liên kết xung quanh nguyên tử trung tâm.
(b) Phức chất có dạng hình học là tứ diện.
(c) Hai liên kết Pt–Cl kế cận nhau trong phức chất tạo thành một góc 90o.
(d) Phức chất có thể kết hợp với hai cation K+ để tạo thành hợp chất trung hòa điện.
Số phát biểu đúng là

Cho các phát biểu sau:
(a) Phức chất có 4 liên kết xung quanh nguyên tử trung tâm.
(b) Phức chất có dạng hình học là tứ diện.
(c) Hai liên kết Pt–Cl kế cận nhau trong phức chất tạo thành một góc 90o.
(d) Phức chất có thể kết hợp với hai cation K+ để tạo thành hợp chất trung hòa điện.
Số phát biểu đúng là
A, 1.
B, 2.
C, 3.
D, 4.
Phân tích các phát biểu:
✔️ (a) – Đúng. Phức chất [PtCl4]2- có ion nguyên tử trung tâm là Pt2+ và 4 phối tử Cl- liên kết với nguyên tử trung tâm.
❌ (b) – Sai. Từ cấu tạo, phức chất [PtCl4]2- có dạng vuông phẳng.
✔️(c) – Đúng. [PtCl4]2- là phức chất vuông phẳng. Hai liên kết Pt-Cl kế cận nhau trong anion [PtCl4]2- tạo thành một góc liên kết. Thực nghiệm xác nhận trong anion [PtCl4]- có bốn góc liên kết đều có giá trị xấp xỉ 90°.
✔️ (d) – Đúng. Phức chất [PtCl4]2- là phức chất anion có điện tích 2- nên cần 2 cation K+ để trung hòa về điện.
Có 3 phát biểu đúng.
⟹ Chọn đáp án C Đáp án: C
✔️ (a) – Đúng. Phức chất [PtCl4]2- có ion nguyên tử trung tâm là Pt2+ và 4 phối tử Cl- liên kết với nguyên tử trung tâm.
❌ (b) – Sai. Từ cấu tạo, phức chất [PtCl4]2- có dạng vuông phẳng.
✔️(c) – Đúng. [PtCl4]2- là phức chất vuông phẳng. Hai liên kết Pt-Cl kế cận nhau trong anion [PtCl4]2- tạo thành một góc liên kết. Thực nghiệm xác nhận trong anion [PtCl4]- có bốn góc liên kết đều có giá trị xấp xỉ 90°.
✔️ (d) – Đúng. Phức chất [PtCl4]2- là phức chất anion có điện tích 2- nên cần 2 cation K+ để trung hòa về điện.
Có 3 phát biểu đúng.
⟹ Chọn đáp án C Đáp án: C
Sử dụng thông tin dưới đây, trả lời câu hỏi số 17, 18
Methyl cinnmate có mùi thơm của dâu tây (strawberry) được sử dụng trong ngành công nghiệp hương liệu và nước hoa có công thức phân tử C10H10O2.
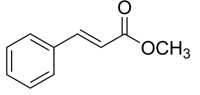

Câu 17 [705914]: Methyl cinnamate không tham gia phản ứng với chất nào dưới đây?
A, dung dịch NaOH.
B, nước bromine.
C, kim loại Na.
D, dung dịch KMnO4.
Hợp chất methyl cinnamate có nhóm chức ester nên có khả năng tham gia phản ứng với dung dịch NaOH
Trong hợp chất, mạch carbon có liên kết C=C không no, nên có khả năng tham gia phản ứng cộng Br2 và có khả năng làm mất màu dung dịch thuốc tím KMnO4.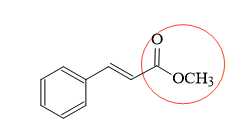
Chọn đáp án C Đáp án: C
Trong hợp chất, mạch carbon có liên kết C=C không no, nên có khả năng tham gia phản ứng cộng Br2 và có khả năng làm mất màu dung dịch thuốc tím KMnO4.

Chọn đáp án C Đáp án: C
Câu 18 [705915]: Để điều chế 16,2 gam ester X người ta cho 29,6 gam cinnamic acid (C6H5CH=CH–COOH) phản ứng với lượng dư methyl alcohol (CH3OH). Hiệu suất phản ứng ester hóa là bao nhiêu?
A, 60%.
B, 62,5%.
C, 50%.
D, 55%.
Số mol của cinnamic acid là C6H5CH=CHCOOH là
nCinnamic acid = 29,6:148 = 0,2 mol
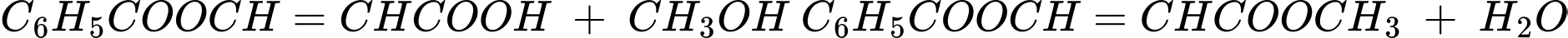
Từ PTHH hóa số mol ester thu được theo lí thuyết là nester = nCinnamic acid = 0,2 mol
Hiệu suất của phản ứng là :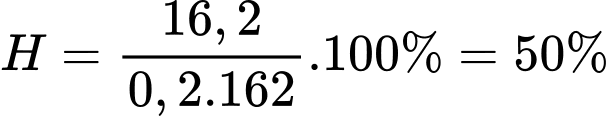
Chọn đáp án C Đáp án: C
nCinnamic acid = 29,6:148 = 0,2 mol
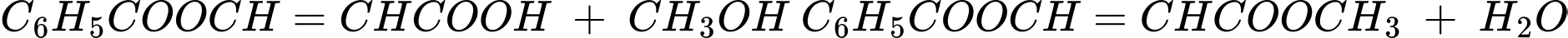
Từ PTHH hóa số mol ester thu được theo lí thuyết là nester = nCinnamic acid = 0,2 mol
Hiệu suất của phản ứng là :
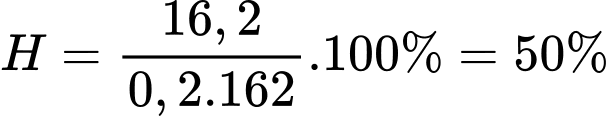
Chọn đáp án C Đáp án: C
PHẦN II. Thí sinh trả lời từ câu 1 đến câu 4. Trong mỗi ý a), b), c), d) ở mỗi câu, thí sinh chọn đúng hoặc sai
Câu 19 [705916]: Tiến hành thí nghiệm theo bước sau:
∎ Bước 1: Cho vào ống nghiệm 1 mL dung dịch hồ tinh bột, thêm vài giọt dung dịch I2 trong dung dịch KI. Lắc đều ống nghiệm.
∎ Bước 2: Đun nóng dung dịch trong ống nghiệm.
∎ Bước 3: Sau đó để nguội dung dịch trong ống nghiệm.
∎ Bước 1: Cho vào ống nghiệm 1 mL dung dịch hồ tinh bột, thêm vài giọt dung dịch I2 trong dung dịch KI. Lắc đều ống nghiệm.
∎ Bước 2: Đun nóng dung dịch trong ống nghiệm.
∎ Bước 3: Sau đó để nguội dung dịch trong ống nghiệm.
Phản ứng giữa hồ tinh bột với dung dịch iod tạo màu xanh tím đặc trưng (còn được gọi là phản ứng màu của iodine với hồ tinh bột). Đây là phản ứng dùng để nhận biết tinh bột. Phân tử tinh bột hấp phụ iodine tạo ra dung dịch có màu xanh tím. Khi đun nóng, iodine bị giải phóng ra khỏi phân tử tinh bột làm mất màu xanh tím.
Phân tích các phát biểu:
✔️A – Đúng. I2 tan kém trong nước nên phải dùng dung dịch KI, tạo dung dịch KI3 theo phương trình:
I2 + KI → KI3
✔️B – Đúng. Hồ tinh bột chứa amylose, một loại polysaccharid có cấu trúc xoắn. I2 bị giữ trong cấu trúc xoắn này, tạo thành phức chất màu xanh tím đặc trưng.
✔️C – Đúng. Khi đun nóng, các liên kết hydro trong cấu trúc xoắn của amylose bị phá vỡ, làm mạch amylose duỗi thẳng. I2 được giải phóng khỏi cấu trúc xoắn, dẫn đến mất màu xanh tím.
✔️D – Đúng. Khi để nguội, các liên kết hydro trong amylose hình thành trở lại, làm mạch amylose xoắn lại. I2 lại bị giữ trong cấu trúc xoắn, màu xanh tím xuất hiện trở lại.
Phân tích các phát biểu:
✔️A – Đúng. I2 tan kém trong nước nên phải dùng dung dịch KI, tạo dung dịch KI3 theo phương trình:
I2 + KI → KI3
✔️B – Đúng. Hồ tinh bột chứa amylose, một loại polysaccharid có cấu trúc xoắn. I2 bị giữ trong cấu trúc xoắn này, tạo thành phức chất màu xanh tím đặc trưng.
✔️C – Đúng. Khi đun nóng, các liên kết hydro trong cấu trúc xoắn của amylose bị phá vỡ, làm mạch amylose duỗi thẳng. I2 được giải phóng khỏi cấu trúc xoắn, dẫn đến mất màu xanh tím.
✔️D – Đúng. Khi để nguội, các liên kết hydro trong amylose hình thành trở lại, làm mạch amylose xoắn lại. I2 lại bị giữ trong cấu trúc xoắn, màu xanh tím xuất hiện trở lại.
Câu 20 [705919]: Cho 2,15 gam magnesium bromide rắn, MgBr2, được hòa tan hoàn toàn trong nước để tạo thành 500 mL dung dịch từ 3 thiết bị đo thể tích dưới đây:
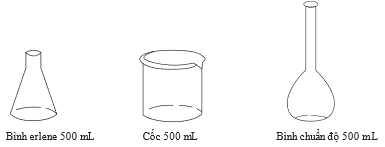
Sau đó, cho dung dịch MgBr2 tác dụng với dung dịch Na3PO4 dư để tạo thành kết tủa. Lọc kết tủa ra khỏi dung dịch trước khi định lượng. Kết tủa thu được lại có giá trị lớn hơn so với tính toán lí thuyết. Có hai cách giải thích lỗi này được đưa ra như sau:
(i) Các hạt kết tủa nhỏ hơn các lỗ trên giấy lọc.
(ii) Kết tủa không được sấy khô hoàn toàn trước khi cân.

Sau đó, cho dung dịch MgBr2 tác dụng với dung dịch Na3PO4 dư để tạo thành kết tủa. Lọc kết tủa ra khỏi dung dịch trước khi định lượng. Kết tủa thu được lại có giá trị lớn hơn so với tính toán lí thuyết. Có hai cách giải thích lỗi này được đưa ra như sau:
(i) Các hạt kết tủa nhỏ hơn các lỗ trên giấy lọc.
(ii) Kết tủa không được sấy khô hoàn toàn trước khi cân.
Phân tích các phát biểu:
❌A. Sai. Do không thể biết số ion NO3- trong hai cốc có bằng nhau hay không.
- Cốc một là bình erlen, thường dùng để pha chế dung dịch không yêu cầu độ chính xác cao về thể tích.
- Cốc ba là bình định mức, dùng để pha chế dung dịch với độ chính xác cao về thể tích.
❌B. Sai. Trong dung dịch có MgBr2 có 1 cation Mg2+ và 2 anion Br-.
✔️C. Đúng. Tổng điện tích dương của các cation phải bằng tổng điện tích âm của các anion để dung dịch giữ trạng thái trung hòa.
✔️D. Đúng. Vì
- Cốc thứ ba là bình định mức, dùng để pha chế dung dịch với độ chính xác cao.
- Bình định mức có cổ hẹp và một vạch mức duy nhất, đảm bảo thể tích dung dịch được pha chính xác.
❌A. Sai. Do không thể biết số ion NO3- trong hai cốc có bằng nhau hay không.
- Cốc một là bình erlen, thường dùng để pha chế dung dịch không yêu cầu độ chính xác cao về thể tích.
- Cốc ba là bình định mức, dùng để pha chế dung dịch với độ chính xác cao về thể tích.
❌B. Sai. Trong dung dịch có MgBr2 có 1 cation Mg2+ và 2 anion Br-.
✔️C. Đúng. Tổng điện tích dương của các cation phải bằng tổng điện tích âm của các anion để dung dịch giữ trạng thái trung hòa.
✔️D. Đúng. Vì
- Cốc thứ ba là bình định mức, dùng để pha chế dung dịch với độ chính xác cao.
- Bình định mức có cổ hẹp và một vạch mức duy nhất, đảm bảo thể tích dung dịch được pha chính xác.
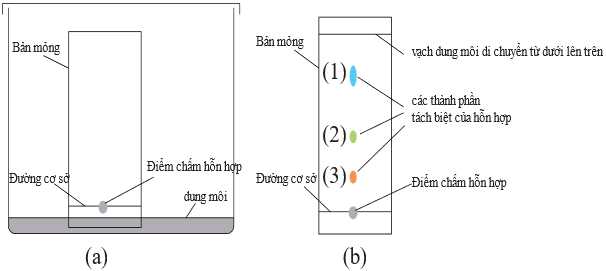
Câu 21 [705917]: Trong sắc ký bản mỏng silica gel, hỗn hợp các chất được chấm lên “đường cơ sở” cách cạnh dưới một khoảng 1 – 1,5 cm. Bản mỏng được đặt trong một lọ và thêm một lượng dung môi đã chọn thích hợp vào (hình a). Đậy nắp lọ và dung môi sẽ chạy ngược từ dưới lên trên, các chất trong hỗn hợp có thể tách ra khỏi nhau trên bản mỏng (hình b).

Phân tích các phát biểu:
✔️A.Đúng. Các chất có độ phân cực khác nhau thì sẽ có sự di chuyển khác nhau. Sắc kí cột được tiến hành dựa trên nguyên tắc tính phân cực. Phân chia hỗn hợp các chất thành 2 pha là pha động và pha tĩnh để sắc ký. Sắc ký hấp thụ là một ống thẳng đứng được làm bằng thủy tinh. Pha tĩnh là chất hấp thụ – các chất phổ biến sử dụng làm pha tĩnh là oxit nhôm, silicagel, CaCO3,…Được tiêu chuẩn hóa có sẵn trên thị trường, Pha động là dung môi rửa cột, chảy qua chất hấp thụ.
✔️B. Đúng. Hình b cho thấy có 3 vệt màu riêng biệt, mỗi vệt tương ứng với một chất trong hỗn hợp ban đầu.
❌C. Sai. Nếu dung môi cao hơn đường cơ sở, các chất sẽ tan vào dung môi trước khi sắc ký diễn ra, làm thí nghiệm thất bại.
❌D. Sai. Chất (1) di chuyển xa nhất, tức là nó tương tác yếu nhất với pha tĩnh (silica gel, phân cực). Do đó, chất (1) có độ phân cực thấp nhất, bất kể dung môi phân cực hay không phân cực.
✔️A.Đúng. Các chất có độ phân cực khác nhau thì sẽ có sự di chuyển khác nhau. Sắc kí cột được tiến hành dựa trên nguyên tắc tính phân cực. Phân chia hỗn hợp các chất thành 2 pha là pha động và pha tĩnh để sắc ký. Sắc ký hấp thụ là một ống thẳng đứng được làm bằng thủy tinh. Pha tĩnh là chất hấp thụ – các chất phổ biến sử dụng làm pha tĩnh là oxit nhôm, silicagel, CaCO3,…Được tiêu chuẩn hóa có sẵn trên thị trường, Pha động là dung môi rửa cột, chảy qua chất hấp thụ.
✔️B. Đúng. Hình b cho thấy có 3 vệt màu riêng biệt, mỗi vệt tương ứng với một chất trong hỗn hợp ban đầu.
❌C. Sai. Nếu dung môi cao hơn đường cơ sở, các chất sẽ tan vào dung môi trước khi sắc ký diễn ra, làm thí nghiệm thất bại.
❌D. Sai. Chất (1) di chuyển xa nhất, tức là nó tương tác yếu nhất với pha tĩnh (silica gel, phân cực). Do đó, chất (1) có độ phân cực thấp nhất, bất kể dung môi phân cực hay không phân cực.
Câu 22 [705918]: Độ dẫn điện của một dung dịch phụ thuộc vào số lượng ion tự do cũng như bản chất của các ion tồn tại trong dung dịch đó. Biểu đồ trong bảng dưới đây biểu diễn phép chuẩn độ, đồng thời đo độ dẫn điện. Trong đó:
∎ X là thể tích dung dịch thêm vào từ burette; Y là độ dẫn điện.
∎ Thí nghiệm 1: Acetic acid với ammonia (trên burette).
∎ Thí nghiệm 2: Silver nitrate với potassium chloride (trên burette).
∎ Thí nghiệm 3: Nitric acid với ammonia (trên burette).
∎ Thí nghiệm 4: Magnesium sulphate với barium hydroxide (trên burette).
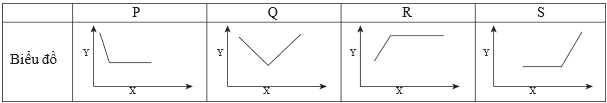
∎ X là thể tích dung dịch thêm vào từ burette; Y là độ dẫn điện.
∎ Thí nghiệm 1: Acetic acid với ammonia (trên burette).
∎ Thí nghiệm 2: Silver nitrate với potassium chloride (trên burette).
∎ Thí nghiệm 3: Nitric acid với ammonia (trên burette).
∎ Thí nghiệm 4: Magnesium sulphate với barium hydroxide (trên burette).

Phân tích các phát biểu:
✔️A. Đúng. (CH3COOH) là một acid yếu, chỉ phân li một phần trong dung dịch tạo ra ion H+ và CH3COO-. Do đó, dung dịch CH3COOH có độ dẫn điện thấp hơn so với các axit mạnh ở cùng nồng độ.
❌B. Sai. Ion H+ có độ linh động cao hơn nhiều so với ion NH4+ trong dung dịch. Do đó, độ dẫn điện của ion H+ lớn hơn ion NH4+.
✔️C. Đúng. Khi tạo thành kết tủa, các ion trong dung dịch bị loại bỏ khỏi dung dịch, làm giảm số lượng ion tự do và do đó làm giảm độ dẫn điện.
❌D. Sai. Vì:
- TN1: Độ dẫn điện thấp do CH3COOH là axit yếu, phân li kém.
- TN2: Độ dẫn điện cao do có nhiều ion Ag+ và NO3-, K+ và Cl-.
- TN3 : Độ dẫn điện cao do HNO3 là axit mạnh, phân li hoàn toàn.
- TN4 : Độ dẫn điện cao do có nhiều ion Mg2+, SO42-, Ba2+ và OH-.
✔️A. Đúng. (CH3COOH) là một acid yếu, chỉ phân li một phần trong dung dịch tạo ra ion H+ và CH3COO-. Do đó, dung dịch CH3COOH có độ dẫn điện thấp hơn so với các axit mạnh ở cùng nồng độ.
❌B. Sai. Ion H+ có độ linh động cao hơn nhiều so với ion NH4+ trong dung dịch. Do đó, độ dẫn điện của ion H+ lớn hơn ion NH4+.
✔️C. Đúng. Khi tạo thành kết tủa, các ion trong dung dịch bị loại bỏ khỏi dung dịch, làm giảm số lượng ion tự do và do đó làm giảm độ dẫn điện.
❌D. Sai. Vì:
- TN1: Độ dẫn điện thấp do CH3COOH là axit yếu, phân li kém.
- TN2: Độ dẫn điện cao do có nhiều ion Ag+ và NO3-, K+ và Cl-.
- TN3 : Độ dẫn điện cao do HNO3 là axit mạnh, phân li hoàn toàn.
- TN4 : Độ dẫn điện cao do có nhiều ion Mg2+, SO42-, Ba2+ và OH-.
PHẦN III. Thí sinh trả lời từ câu 1 đến câu 6.
Câu 23 [705920]: Một mẫu nước thải của nhà máy sản xuất dây lưới thép có pH = 4,0. Để thải được ra môi trường, nhà máy đó cần phải tăng pH trong nước thải lên tới 5,8 – 8,6 (theo tiêu chuẩn quy định). Tính lượng vôi sống (g) cần dùng để tăng pH trong 100 m3 nước thải từ 4,0 lên 7,0. Giả thiết thể tích nước thải thay đổi không đáng kể (Kết quả làm tròn đến số nguyên).
Đổi 100 m3 = 100000 L
Ta có của nước thải pH = 4 → [H+] = 10-4 M
Số mol của H+ là nH+ = 10-4.100000 = 10 mol
H+ + OH- → H2O
CaO + H2O → Ca(OH)2
Để pH của nước thải từ pH = 4 đến pH = 7 cần số mol OH- là nH+ = nOH- = 10 mol
2nOH- = nCa(OH)2 = 10 mol → nCa(OH)2 = 5 mol
Từ PTHH số mol của CaO là 5 mol
Khối lượng của CaO là mCaO = 5.56 = 280 gam
Điền đáp án : 280
Ta có của nước thải pH = 4 → [H+] = 10-4 M
Số mol của H+ là nH+ = 10-4.100000 = 10 mol
H+ + OH- → H2O
CaO + H2O → Ca(OH)2
Để pH của nước thải từ pH = 4 đến pH = 7 cần số mol OH- là nH+ = nOH- = 10 mol
2nOH- = nCa(OH)2 = 10 mol → nCa(OH)2 = 5 mol
Từ PTHH số mol của CaO là 5 mol
Khối lượng của CaO là mCaO = 5.56 = 280 gam
Điền đáp án : 280
Câu 24 [59367]: Trong các kim loại Cu; Ag; Na; K và Ba, số kim loại điều chế được bằng phương pháp thủy luyện là
- Phương pháp thủy luyện áp dụng điều chế các kim loại có mức độ hoạt động thấp như Cu, Hg, Au, Ag...
- Điều chế kim loại bằng phương pháp thủy luyện thường được sử dụng trong phòng thí nghiệm với mục đích điều chế những kim loại yếu đứng sau Mg.
Kim loại được điều chế bằng phương pháp thủy luyện gồm Cu và Ag
⇒ Có 2 kim loại.
Điền đáp án : 2
- Điều chế kim loại bằng phương pháp thủy luyện thường được sử dụng trong phòng thí nghiệm với mục đích điều chế những kim loại yếu đứng sau Mg.
Kim loại được điều chế bằng phương pháp thủy luyện gồm Cu và Ag
⇒ Có 2 kim loại.
Điền đáp án : 2
Câu 25 [705921]: Sắn khô chứa 38% khối lượng là tinh bột, còn lại là các chất không có khả năng lên men thành ethanol. Lên men 2 tấn sắn khô với hiệu suất cả quá trình là 74%. Toàn bộ lượng ethanol sinh ra để điều chế xăng E5 (có chứa 5% thể tích ethanol). Biết khối lượng riêng của ethyl alcohol là 0,8 g/mL, thể tích xăng E5 thu được là bao nhiêu lít?
Đổi 2 tấn = 2000 kg; 0,8 g/mL = 0,8 kg/L
Khối lượng của tinh bột trong sắn khô là 2000.38% = 760 kg
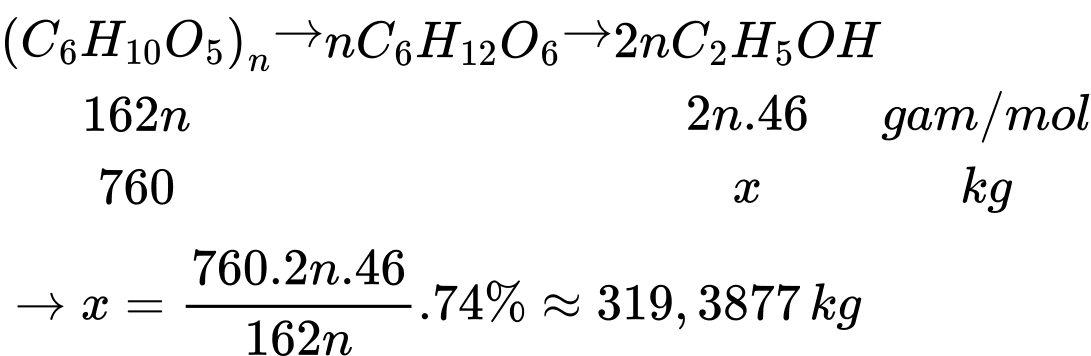
Thể tích alcohol là VC2H5OH = 318,2877:0,8 = 399,2346 L
Thể tích xăng E5 là VE5 = 399,2346:5% ≈ 7985 L
Điền đáp án : 7985
Khối lượng của tinh bột trong sắn khô là 2000.38% = 760 kg
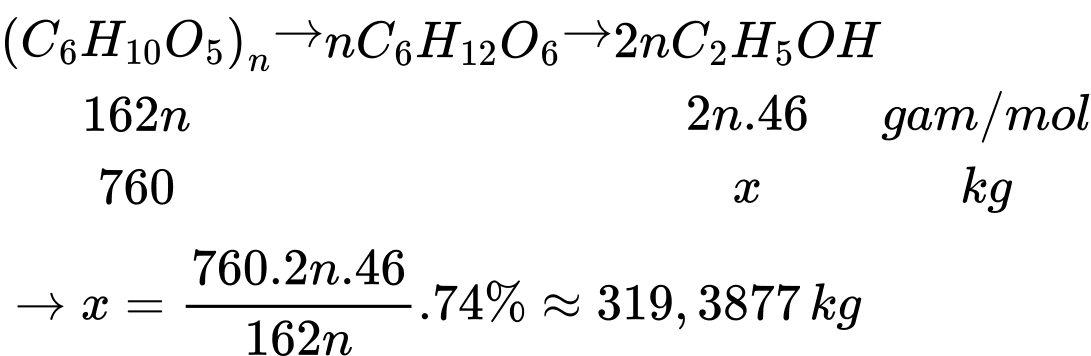
Thể tích alcohol là VC2H5OH = 318,2877:0,8 = 399,2346 L
Thể tích xăng E5 là VE5 = 399,2346:5% ≈ 7985 L
Điền đáp án : 7985
Câu 26 [310456]: Cho dãy polymer: polyethylene, poly(vinyl chloride), cao su buna, polystyrene, amylose, amylopectin, cellulose, nhựa novolac, tơ nylon-6. Số polymer có cấu tạo mạch không phân nhánh là
Điền đáp án: [..........]
Điền đáp án: [..........]
- Polymer có cấu trúc không phân nhánh là: polyethylene (PE), poly(vinyl chloride) (PVC), cao su buna, polystyrene, amylose, cellulose, nhựa novolac, tơ nylon-6.
- Polymer có cấu trúc phân nhánh: amylopectin.
→ Số polymer có cấu tạo mạch không phân nhánh là 8.
⇒ Điền đáp án: 8
- Polymer có cấu trúc phân nhánh: amylopectin.
→ Số polymer có cấu tạo mạch không phân nhánh là 8.
⇒ Điền đáp án: 8
Câu 27 [705922]: Sulfuric acid là một trong những hoá chất quan trọng nhất được sử dụng trong công nghiệp; được sản xuất hàng trăm triệu tấn mỗi năm, chiếm nhiều nhất trong ngành công nghiệp hoá chất. Phương pháp sản xuất sulfuric acid phổ biến nhất là phương pháp tiếp xúc, theo đó acid có thể được điều chế qua các giai đoạn sau:
(1) 4FeS2(s) + 11O2(g) → 2Fe2O3(s) + 8SO2(g)
(2) 2SO2(g) + O2(g) ⇌ 2SO3(g)
(3) H2SO4(aq) + nSO3(g) → H2SO4.nSO3(l)
(4) H2SO4.nSO3(l) + H2O(l) → H2SO4(aq)
Dùng sulfuric acid 98% hấp thụ SO3(g) trong giai đoạn (3), quá trình này được thực hiện trong tháp tiếp xúc. Để xác định công thức của oleum thu được, người ta pha loãng 8,36 gam oleum vào nước thành 1,0 L dung dịch sulfuric acid, sau đó tiến hành chuẩn độ 10,00 mL dung dịch acid này bằng dung dịch chuẩn NaOH 0,10 M. Thể tích NaOH trung bình cần sử dụng để chuẩn độ là 20,01 mL. Công thức của oleum trên có dạng H2SO4.nSO3. Xác định giá trị của n (Làm tròn đến số nguyên).
(1) 4FeS2(s) + 11O2(g) → 2Fe2O3(s) + 8SO2(g)
(2) 2SO2(g) + O2(g) ⇌ 2SO3(g)
(3) H2SO4(aq) + nSO3(g) → H2SO4.nSO3(l)
(4) H2SO4.nSO3(l) + H2O(l) → H2SO4(aq)
Dùng sulfuric acid 98% hấp thụ SO3(g) trong giai đoạn (3), quá trình này được thực hiện trong tháp tiếp xúc. Để xác định công thức của oleum thu được, người ta pha loãng 8,36 gam oleum vào nước thành 1,0 L dung dịch sulfuric acid, sau đó tiến hành chuẩn độ 10,00 mL dung dịch acid này bằng dung dịch chuẩn NaOH 0,10 M. Thể tích NaOH trung bình cần sử dụng để chuẩn độ là 20,01 mL. Công thức của oleum trên có dạng H2SO4.nSO3. Xác định giá trị của n (Làm tròn đến số nguyên).
H2SO4.nSO3 + nH2O → (n+1)H2SO4
2NaOH + H2SO4 → Na2SO4 + 2H2O
Đổi 20,01 mL = 0,02001 L; 1 L = 1000 mL
Số mol của NaOH là nNaOH = 0,02001.0,1 = 0,002001 mol
Từ phương trình hóa học số mol của H2SO4 là nH2SO4 = 0,0010005 mol
Số mol của oleum trong 10 mL là
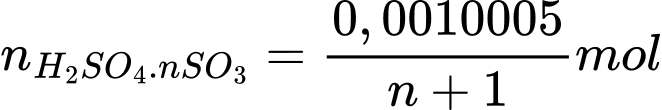
Khối lượng của oleum là
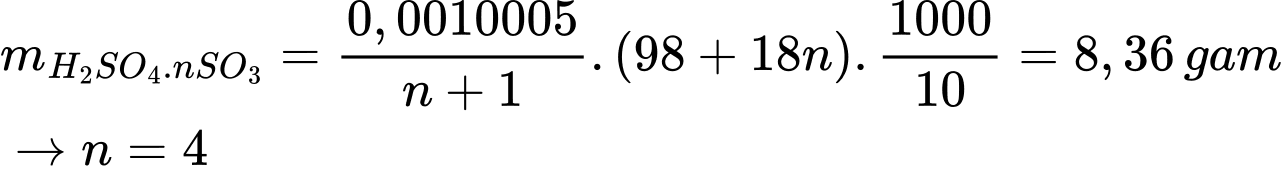
⟹Điền đáp án : 4
2NaOH + H2SO4 → Na2SO4 + 2H2O
Đổi 20,01 mL = 0,02001 L; 1 L = 1000 mL
Số mol của NaOH là nNaOH = 0,02001.0,1 = 0,002001 mol
Từ phương trình hóa học số mol của H2SO4 là nH2SO4 = 0,0010005 mol
Số mol của oleum trong 10 mL là
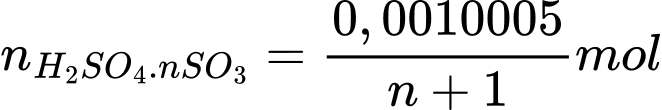
Khối lượng của oleum là
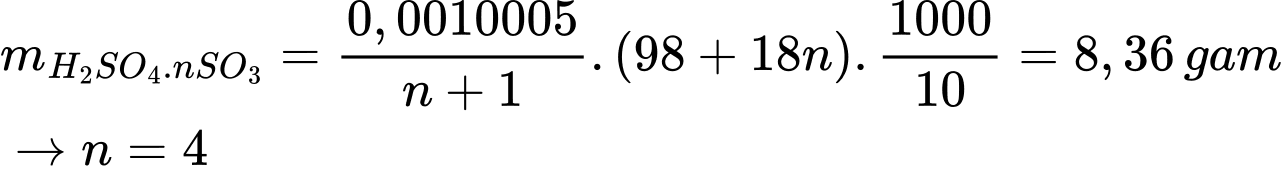
⟹Điền đáp án : 4
Câu 28 [705923]: Aspirin (hay acetylsalicylic acid), là một dẫn xuất của salicylic acid được sử dụng để hạ sốt và giảm đau nhẹ đến trung bình do tình trạng đau nhức cơ, răng, cảm lạnh đau đầu và sưng tấy do viêm khớp. Cho quy trình tổng hợp Aspirin trong phòng thí nghiệm như sau:
Bước 1: Cho 50,0 gam salicylic acid khan và 70,0 mL acetic anhydrid (d = 1,08 g/mL) vào bình cầu 250 mL; thêm 3,0 ml sulfuric acid đặc vào và lắc kĩ. Sau đó, khuấy khối phản ứng ở 50-60 °C trong khoảng 45 phút cho đến khi tan hết phần chất rắn.
Bước 2: Dùng nước đá để làm lạnh hỗn hợp phản ứng đến nhiệt độ nhỏ hơn 10 °C. Thêm từ từ 750 ml nước cất và khuấy kỹ, aspirin sẽ kết tủa. Lọc lấy sản phẩm bằng phễu lọc Buchner.
Bước 3: Hòa tan aspirin thô trong 150 mL ethanol 90 ° (cần đun nóng để tan hoàn toàn), sau đó đổ dung dịch này từ từ vào 375 mL nước nóng khoảng 50 °C. Nếu aspirin kết tủa lại thì cần đun nóng cho tan hết. Để nguội dung dịch thu được đến nhiệt độ phòng. Aspirin sẽ kết tinh dưới dạng tinh thể. Lọc và hút kiệt rồi sấy khô ở 50 °C.
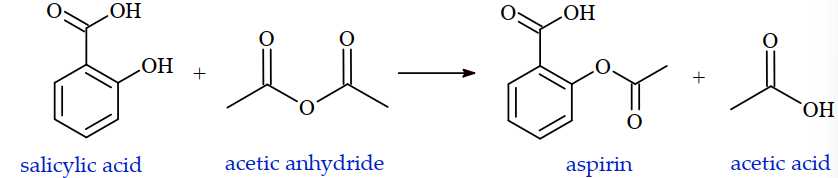
Bước 4: Cân sản phẩm thu được 55,4 gam aspirin.Cho biết phương trình hóa học điều chế aspirin từ salicylic acid được biểu diễn như sau:
Hiệu suất của phản ứng tổng hợp aspirin ở thí nghiệm trên là bao nhiêu (làm tròn kết quả đến phần chục)?
Bước 1: Cho 50,0 gam salicylic acid khan và 70,0 mL acetic anhydrid (d = 1,08 g/mL) vào bình cầu 250 mL; thêm 3,0 ml sulfuric acid đặc vào và lắc kĩ. Sau đó, khuấy khối phản ứng ở 50-60 °C trong khoảng 45 phút cho đến khi tan hết phần chất rắn.
Bước 2: Dùng nước đá để làm lạnh hỗn hợp phản ứng đến nhiệt độ nhỏ hơn 10 °C. Thêm từ từ 750 ml nước cất và khuấy kỹ, aspirin sẽ kết tủa. Lọc lấy sản phẩm bằng phễu lọc Buchner.
Bước 3: Hòa tan aspirin thô trong 150 mL ethanol 90 ° (cần đun nóng để tan hoàn toàn), sau đó đổ dung dịch này từ từ vào 375 mL nước nóng khoảng 50 °C. Nếu aspirin kết tủa lại thì cần đun nóng cho tan hết. Để nguội dung dịch thu được đến nhiệt độ phòng. Aspirin sẽ kết tinh dưới dạng tinh thể. Lọc và hút kiệt rồi sấy khô ở 50 °C.
Bước 4: Cân sản phẩm thu được 55,4 gam aspirin.Cho biết phương trình hóa học điều chế aspirin từ salicylic acid được biểu diễn như sau:

Hiệu suất của phản ứng tổng hợp aspirin ở thí nghiệm trên là bao nhiêu (làm tròn kết quả đến phần chục)?
HOC6H4COOH + (CH3CO)2O → HOOCC6H4OOCCH3 + CH3COOH
Khối lượng của acetic anhydride là m(CH3CO)2O = 70.1,08 = 75,6 gam
Số mol của acetic anhydride là n(CH3CO)2O = 75,6:102 = 0,7412 mol
Số mol của salicylic acid là nsalicylic acid = 50:138 = 0,3623 mol
Số mol của aspirin theo lí thuyết là naspirin = 0,3623 mol
Hiệu suất của phản ứng là :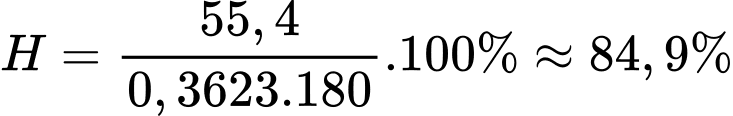
Điền đáp án : 84,9
Khối lượng của acetic anhydride là m(CH3CO)2O = 70.1,08 = 75,6 gam
Số mol của acetic anhydride là n(CH3CO)2O = 75,6:102 = 0,7412 mol
Số mol của salicylic acid là nsalicylic acid = 50:138 = 0,3623 mol
Số mol của aspirin theo lí thuyết là naspirin = 0,3623 mol
Hiệu suất của phản ứng là :
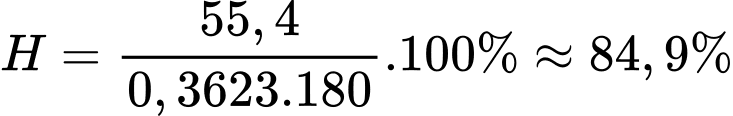
Điền đáp án : 84,9