PHẦN I. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
Câu 1 [705924]: “Tính chất hoá học của ..(1).. thường tương tự tính chất hoá học của các ..(2).. thành phần tham gia tạo hợp kim”. Nội dung phù hợp trong các ô trống (1), (2) lần lượt là
A, phi kim, đơn chất.
B, kim loại, hợp chất.
C, hợp kim, đơn chất.
D, khí hiếm, phi kim.
Hợp kim là vật liệu được tạo từ kim loại và một số nguyên tố khác.
Tính chất hóa học của hợp kim thường tương tự với các đơn chất kim loại vì hợp kim chủ yếu được tạo từ kim loại.
“Tính chất hoá học của hợp kim thường tương tự tính chất hoá học của các đơn chất thành phần tham gia tạo hợp kim”.
Chọn đáp án C Đáp án: C
Tính chất hóa học của hợp kim thường tương tự với các đơn chất kim loại vì hợp kim chủ yếu được tạo từ kim loại.
“Tính chất hoá học của hợp kim thường tương tự tính chất hoá học của các đơn chất thành phần tham gia tạo hợp kim”.
Chọn đáp án C Đáp án: C
Câu 2 [705925]: Khoáng chất sylvite có chứa muối KCl. Tên gọi của muối này là
A, potassium chloride.
B, potassium chlorate.
C, potassium chlorite.
D, potassium hypochlorite.
Phân tích các đáp án:
✔️A. potassium chloride - KCl
❌B.potassium chlorate - KClO3
❌C.potassium chlorite - KClO2
❌D.potassium hypochlorite - KClO
Chọn đáp án A Đáp án: A
✔️A. potassium chloride - KCl
❌B.potassium chlorate - KClO3
❌C.potassium chlorite - KClO2
❌D.potassium hypochlorite - KClO
Chọn đáp án A Đáp án: A
Câu 3 [705926]: Dãy sắp xếp theo chiều tăng dần độ ngọt của các carbohydrate là
A, glucose < tinh bột < fructose.
B, glucose < saccharose < cellulose.
C, glucose < saccharose < fructose.
D, saccharose < glucose < fructose.
Độ ngọt của các carbohydrate :

Chọn đáp án C Đáp án: C

Chọn đáp án C Đáp án: C
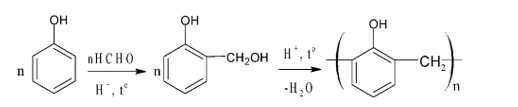
Câu 4 [705927]: Nhựa Phenol formaldehyde (PF) là một loại nhựa tổng hợp có ứng dụng rộng rãi trong ngành công nghiệp như lĩnh vực như ngành điện tử, sản xuất gỗ công nghiệp và xây dựng do khả năng chịu nhiệt và kháng cháy,... Nhựa PF được tổng hợp bằng phương pháp đun nóng phenol với
A, CH3COOH trong môi trường acid.
B, HCHO trong môi trường acid.
C, HCOOH trong môi trường acid.
D, CH3CHO trong môi trường acid.
Đun hỗn hợp phenol (lấy dư) và formaldehyde trong môi trường acid.
Chọn đáp án B Đáp án: B

Chọn đáp án B Đáp án: B
Câu 5 [705928]: Tại sao ở các vùng ven biển, vật liệu xây dựng làm bằng sắt thường bị ăn mòn nhanh hơn vì
A, sắt dễ bị oxi hóa bởi oxygen có mặt trong không khí.
B, dễ tiếp xúc với nước muối, hình thành môi trường điện li.
C, chi phí bảo trì sắt cao hơn các kim loại khác.
D, nhiệt độ tăng cao nên sắt dễ bị nóng trong thời tiết nắng.
Muối trong không khí đại dương ở các vùng ven biển gây ra các vấn đề lo ngại cho thép và gỗ. Đối với thép, nước là tác nhân chính dẫn đến rỉ sét. Nhưng cuộc sống ven biển đưa muối vào quá trình này, và muối được thêm vào sẽ gây ra các phản ứng hóa học làm tăng tốc độ ăn mòn một cách đáng kể.
Chọn đáp án B Đáp án: B
Chọn đáp án B Đáp án: B
Câu 6 [705930]: Một người ngủ quên trong ô tô tắt máy, đóng kín cửa. Sau một thời gian, khi hàm lượng oxygen trong xe giảm xuống còn 16% thể tích không khí thì có người kịp thời phát hiện, phá vỡ kính xe để đưa đi cấp cứu. Tại thời điểm được cứu, tốc độ “phản ứng hô hấp" (υhô hấp = k×CO2) của người trong xe giảm bao nhiêu lần so với bình thường? Biết ban đầu oxygen chiếm 21% thể tích không khí.
A, 1,2500.
B, 1,3125.
C, 1,1125.
D, 1,4325.
Tốc độ hô hấp ban đầu 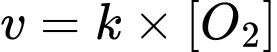
Tốc độ khi oxygen giảm xuống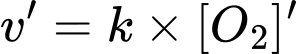
Tại thời điểm cấp cứu tốc độ của phản ứng hô hấp giảm xuống là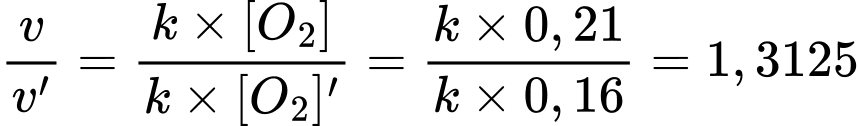
Chọn đáp án B Đáp án: B
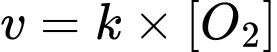
Tốc độ khi oxygen giảm xuống
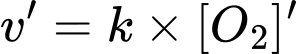
Tại thời điểm cấp cứu tốc độ của phản ứng hô hấp giảm xuống là
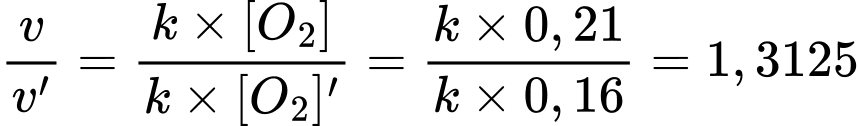
Chọn đáp án B Đáp án: B
Câu 7 [705929]: Magnesium hydroxide (Mg(OH)2) là một trong những hợp chất quan trọng được sử dụng rộng rãi trong y học. Vai trò chính của Mg(OH)2 trong ứng dụng này là
A, Thuốc kháng acid dạ dày.
B, Thuốc tẩy rửa.
C, Chất khử trùng.
D, Thuốc giảm đau.
✔️A. Thuốc kháng acid dạ dày: Mg(OH)2 là một loại thuốc kháng acid phổ biến, được sử dụng rộng rãi trong điều trị các chứng ợ nóng, khó tiêu, đau dạ dày, táo bón và ngăn ngừa loét dạ dày.
❌B. Thuốc tẩy rửa : (NaOH) hoặc (KOH) thường được sử dụng làm chất tẩy rửa mạnh vì chúng có tính kiềm cao, giúp phân hủy dầu mỡ và chất bẩn.
❌C. Thường là các hợp chất như (H2O2), Ethanol (C2H5OH) hoặc (Cl2) có khả năng diệt khuẩn.
❌D. Thuốc giảm đau: Paracetamol (C8H9NO2) hoặc Aspirin (C9H8O4) là các chất phổ biến dùng để giảm đau và hạ sốt.
Chọn đáp án A Đáp án: A
❌B. Thuốc tẩy rửa : (NaOH) hoặc (KOH) thường được sử dụng làm chất tẩy rửa mạnh vì chúng có tính kiềm cao, giúp phân hủy dầu mỡ và chất bẩn.
❌C. Thường là các hợp chất như (H2O2), Ethanol (C2H5OH) hoặc (Cl2) có khả năng diệt khuẩn.
❌D. Thuốc giảm đau: Paracetamol (C8H9NO2) hoặc Aspirin (C9H8O4) là các chất phổ biến dùng để giảm đau và hạ sốt.
Chọn đáp án A Đáp án: A
Câu 8 [705931]: Dung dịch X có chứa a mol Na+; b mol Mg2+; c mol NO3– và d mol 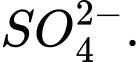 Biểu thức liên hệ giữa a, b, c, d là
Biểu thức liên hệ giữa a, b, c, d là
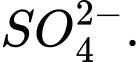 Biểu thức liên hệ giữa a, b, c, d là
Biểu thức liên hệ giữa a, b, c, d là A, a + 2b = c + 2d.
B, a + 2b = c + d.
C, a + b = c + d.
D, 2a + b = 2c + d.
Bảo toàn điện tích:
Số điện tích dương = số điện tích âm
⟶ 1×a + 2×b = 1×c + 2×d
⟶ a + 2b = c + 2d
Chọn đáp án A Đáp án: A
Số điện tích dương = số điện tích âm
⟶ 1×a + 2×b = 1×c + 2×d
⟶ a + 2b = c + 2d
Chọn đáp án A Đáp án: A
Câu 9 [13992]: Phân biệt được các chất lỏng: hex-1-ene, hexane, hex-1-yne bằng cách sử dụng hai dung dịch chứa thuốc thử là
A, silver nitrate trong ammoniac, bromine.
B, thuốc tím, bromine.
C, bromine, nước vôi trong.
D, thuốc tím, nước vôi trong.
HD: ► để phân biệt hex-1-ene, hexane, hex-1-yne người ta dùng cặp thuốc thử AgNO3/NH3 và Br2.
♦ chỉ ank-1-yne dạng RC≡CH + AgNO3 + NH3 → RC≡CAg↓ (tủa màu vàng) + NH4NO3.
⇒ biết được hex-1-yne dựa vào kết tủa vàng khi phản ứng với AgNO3/NH3.
còn lại hex-1-ene và hexane ta dùng Br2, chất nào làm mất màu dung dịch Br2 là alkene → chọn A. ♥.
p/s: các đáp án khác: B sai vì thuốc tím KMnO4 giúp biết được hexane (không phản ứng)
còn hex-1-yne và hex-1-ene đều làm mất màu và tạo ↓MnO2 màu đen
NHƯNG brom không giúp ta phân biệt được hex-1-yne và hex-1-ene.
đáp án C, D tương tự khi không thể dùng thuốc tím hay Br2 hay nước vôi trong
để phân biệt được cặp alkyne (hex-1-yne) và anken (hex-1-ene) ⇒ tự tin chọn A..!
Đáp án: A
♦ chỉ ank-1-yne dạng RC≡CH + AgNO3 + NH3 → RC≡CAg↓ (tủa màu vàng) + NH4NO3.
⇒ biết được hex-1-yne dựa vào kết tủa vàng khi phản ứng với AgNO3/NH3.
còn lại hex-1-ene và hexane ta dùng Br2, chất nào làm mất màu dung dịch Br2 là alkene → chọn A. ♥.
p/s: các đáp án khác: B sai vì thuốc tím KMnO4 giúp biết được hexane (không phản ứng)
còn hex-1-yne và hex-1-ene đều làm mất màu và tạo ↓MnO2 màu đen
NHƯNG brom không giúp ta phân biệt được hex-1-yne và hex-1-ene.
đáp án C, D tương tự khi không thể dùng thuốc tím hay Br2 hay nước vôi trong
để phân biệt được cặp alkyne (hex-1-yne) và anken (hex-1-ene) ⇒ tự tin chọn A..!
Đáp án: A
Câu 10 [247258]: Trong các AO sau, AO nào là AOpx?
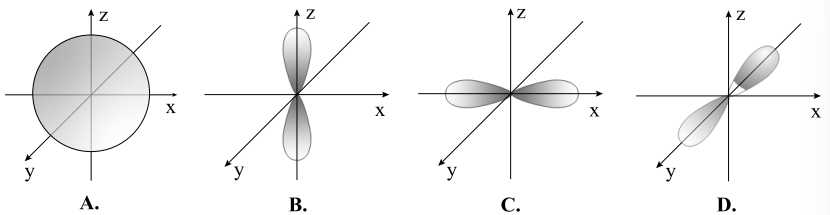

A, Chỉ có (1).
B, Chỉ có (2).
C, Chỉ có (3).
D, Chỉ có (4).
AOpx có dạng hình số 8 nổi và định hướng theo trục x.
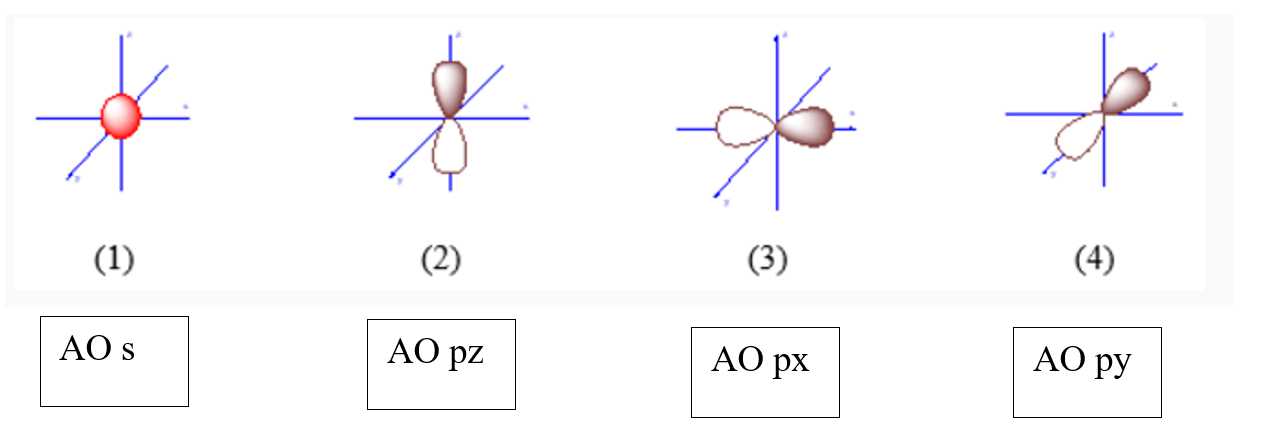
Chọn đáp án C Đáp án: C

Chọn đáp án C Đáp án: C
Câu 11 [705932]: Điện phân dung dịch nước của hỗn hợp các chất Cu(NO3)2, AgNO3, Hg2(NO3)2 và Mg(NO3)2 với điện cực trơ. Các chất đều có nồng độ 1 M. Thứ tự các kim loại được giải phóng ở cathode là:
A, Ag, Hg, Cu.
B, Cu, Hg, Ag.
C, Ag, Hg, Cu, Mg.
D, Mg, Cu, Hg, Ag.

Hg đứng trước Ag trong dãy điện hóa.
Dựa vào thế điện cực chuẩn, Ion có thế điện cực chuẩn lớn hơn sẽ nhận electron và bị khử trước.
Dựa vào thế khử chuẩn, thứ tự các kim loại bị khử tại cathode là
Thứ tự điện phân :
1.Ag → Bị khử trước.
2.Hg
3.Cu
4.Mg không bị khử, vì nước bị khử trước tạo H2.
Chọn đáp án A Đáp án: A
Câu 12 [252458]: Sục khí chlorine dư vào dung dịch chứa muối sodium bromide và potassium bromide thu được hỗn hợp muối, đồng thời thấy khối lượng muối giảm 4,45 gam. Lượng chlorine đã tham gia phản ứng là
A, 0,1 mol.
B, 0,05 mol.
C, 0,02 mol.
D, 0,01 mol.
Cl2 + 2NaBr → 2NaCl + Br2
a 2a 2a a mol
Cl2 + 2KBr → 2KCl + Br2
b 2b 2b b mol
Khối lượng muối giảm = KL NaBr + KL KBr – KL NaCl – KL KCl
103.2a + 119.2b – 58,5.2a – 74,5.2b = 4,45
=> 89a + 89b = 4,45 => a+b = 0,05
Lượng Cl2 phản ứng = a+ b = 0,05
Chọn đáp án B
Đáp án: B Chọn đáp án B
Câu 13 [705934]: Formic acid (HCOOH) có trong nọc kiến, nọc ong, sâu róm. Chất nào sau đây là ester của formic acid?
A, CH3COOCH3.
B, HCOOCH3.
C, CH3CH2COOCH3.
D, C6H5COOCH3.
Ester của formic acid (HCOOH) có công thức chung là HCOOR, trong đó R là nhóm alkyl hoặc aryl.
Phân tích các đáp án:
❌A. CH3COOCH3 → Đây là methyl acetate, ester của acetic acid (CH3COOH), không phải của formic acid.
✔️B. HCOOCH3 → Đây là methyl formate, ester của formic acid.
❌C. CH3CH2COOCH3 → Đây là methyl propionate, ester của propionic acid (CH3CH2COOH).
❌D. C6H5COOCH3 → Đây là methyl benzoate, ester của benzoic acid (C6H5COOH)
Chọn đáp án B Đáp án: B
Phân tích các đáp án:
❌A. CH3COOCH3 → Đây là methyl acetate, ester của acetic acid (CH3COOH), không phải của formic acid.
✔️B. HCOOCH3 → Đây là methyl formate, ester của formic acid.
❌C. CH3CH2COOCH3 → Đây là methyl propionate, ester của propionic acid (CH3CH2COOH).
❌D. C6H5COOCH3 → Đây là methyl benzoate, ester của benzoic acid (C6H5COOH)
Chọn đáp án B Đáp án: B
Câu 14 [705935]: “Ở dạng mạch vòng, saccharose và maltose là các disaccharide được tạo bởi lần lượt các loại liên kết ...(1)... và ...(2)...” . Nội dung phù hợp trong ô trống (1), (2) lần lượt là
A, α-1,2-glycoside, α-1,2-glycoside.
B, β-1,4-glycoside, β-1,2-glycoside.
C, α-1,2-glycoside, α-1,4-glycoside.
D, α-1,4-glycoside, β-1,4-glycoside.
Cấu trúc phân tử :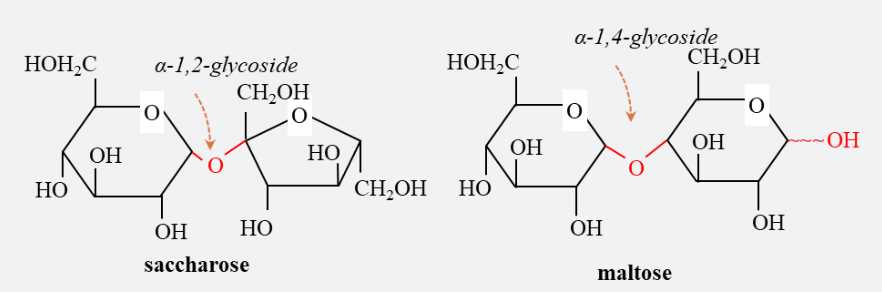
“Ở dạng mạch vòng, saccharose và maltose là các disaccharide được tạo bởi lần lượt các loại liên kết α-1,2-glycoside, α-1,4-glycoside ” .
Chọn đáp án C
Câu 15 [705933]: Chanh là một loài thực vật cho quả nhỏ, thuộc chỉ cam chanh (citrus). Quả chanh được sử dụng làm thực phẩm. Nước ép chanh chứa khoảng 5% citric acid nên chanh có vị chua và độ pH khoảng 2 – 3. Công thức (X) được cho ở hình bên.
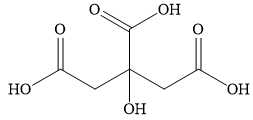
Chọn phát biểu đúng về citric acid

Chọn phát biểu đúng về citric acid
A, Công thức phân tử của citric acid là C4H6O7.
B, 1 mol citric acid tác dụng với Na tạo ra 2 mol H2.
C, Citric acid thuộc loại hợp chất đa chức.
D, Citric acid tác dụng với NaOH theo tỉ lệ mol 1 : 4.
Phân tích các phát biểu:
❌A – Sai. Công thức phân tử của citric acid là C6H8O7.
✔️B – Đúng. Citric acid có 1 nhóm OH (alcohol) và 3 nhóm (carboxylic acid) nên tác dụng với Na theo tỉ lệ 1:4
HOC3H4(COOH)3 + 4Na → NaOC3H4(COONa)3 + 2H2
❌C – Sai. Citric acid thuộc loại hợp chất tạp chức, citric acid có 1 nhóm OH (alcohol) và 3 nhóm (carboxylic acid)
❌D – Sai. Citric acid có 1 nhóm OH (alcohol) và 3 nhóm (carboxylic acid) nên tác dụng với NaOH theo tỉ lệ 1:3
Chọn đáp án B Đáp án: B
❌A – Sai. Công thức phân tử của citric acid là C6H8O7.
✔️B – Đúng. Citric acid có 1 nhóm OH (alcohol) và 3 nhóm (carboxylic acid) nên tác dụng với Na theo tỉ lệ 1:4
HOC3H4(COOH)3 + 4Na → NaOC3H4(COONa)3 + 2H2
❌C – Sai. Citric acid thuộc loại hợp chất tạp chức, citric acid có 1 nhóm OH (alcohol) và 3 nhóm (carboxylic acid)
❌D – Sai. Citric acid có 1 nhóm OH (alcohol) và 3 nhóm (carboxylic acid) nên tác dụng với NaOH theo tỉ lệ 1:3
Chọn đáp án B Đáp án: B
Câu 16 [705936]: Một mẫu nước có chứa các ion Ca2+, [Cu(OH2)6]2+, [Fe(OH2)6]2+, Na+, Cl–, SO42–. Sau một thời gian tiếp xúc với không khí, mẫu nước này chuyển sang màu vàng và nổi váng màu nâu do quá trình:
[M(OH2)6]n+(aq) + mH2O(l) ⇌ [M(OH)m(OH2)6–m](n–m)+(aq hoặc s) + mH3O+(aq) (3)
Cho các phát biểu sau:
(a) Mẫu nước trên có pH lớn hơn 7.
(b) Ion bị oxi hoá và gây nên hiện tượng trên là [Fe(OH2)6]2+.
(c) Trong nước, ion H+ nhận cặp electron từ H2O để tạo thành ion H3O+.
(d) Chất màu nâu sinh trong mô tả trên là phức chất có công thức là [Fe(OH)2(OH2)4].
Các phát biểu đúng là
[M(OH2)6]n+(aq) + mH2O(l) ⇌ [M(OH)m(OH2)6–m](n–m)+(aq hoặc s) + mH3O+(aq) (3)
Cho các phát biểu sau:
(a) Mẫu nước trên có pH lớn hơn 7.
(b) Ion bị oxi hoá và gây nên hiện tượng trên là [Fe(OH2)6]2+.
(c) Trong nước, ion H+ nhận cặp electron từ H2O để tạo thành ion H3O+.
(d) Chất màu nâu sinh trong mô tả trên là phức chất có công thức là [Fe(OH)2(OH2)4].
Các phát biểu đúng là
A, (a), (b).
B, (b), (c).
C, (a), (b), (c).
D, (b), (c), (d).
Phân tích các phát biểu:
❌(a) – Sai. Mẫu nước trên có pH nhỏ hơn 7. Trong quá trình phức chất phân li trong nước sinh ra H3O+ có tính acid nên tạo môi trường acid có pH nhỏ hơn 7.
✔️(b) – Đúng. Sau một thời gian tiếp xúc với không khí, mẫu nước này chuyển sang màu vàng và nổi váng màu nâu do quá trình lon bị oxi hoá và gây nên hiện tượng trên chất phù hợp là [Fe(OH2)6]2+.
✔️(c) – Đúng. Thuyết bronsted – Lowry: Acid là chất cho proton (H+), base là chất nhận proton. Acid và base có thể là phân tử hoặc ion.H+ + H2O → H3O+
❌(d) – Sai. Chất trong mô tả trên là phức chất có công thức là [Fe(OH)2(OH2)4] có màu trắng xanh, sau khi tiếp xúc với không khí chuyển sang màu vàng và nổi váng màu nâu.
Các phát biểu đúng là (b), (c)
⟹ Chọn đáp án B Đáp án: B
❌(a) – Sai. Mẫu nước trên có pH nhỏ hơn 7. Trong quá trình phức chất phân li trong nước sinh ra H3O+ có tính acid nên tạo môi trường acid có pH nhỏ hơn 7.
✔️(b) – Đúng. Sau một thời gian tiếp xúc với không khí, mẫu nước này chuyển sang màu vàng và nổi váng màu nâu do quá trình lon bị oxi hoá và gây nên hiện tượng trên chất phù hợp là [Fe(OH2)6]2+.
✔️(c) – Đúng. Thuyết bronsted – Lowry: Acid là chất cho proton (H+), base là chất nhận proton. Acid và base có thể là phân tử hoặc ion.H+ + H2O → H3O+
❌(d) – Sai. Chất trong mô tả trên là phức chất có công thức là [Fe(OH)2(OH2)4] có màu trắng xanh, sau khi tiếp xúc với không khí chuyển sang màu vàng và nổi váng màu nâu.
Các phát biểu đúng là (b), (c)
⟹ Chọn đáp án B Đáp án: B
Sử dụng thông tin dưới đây, trả lời câu hỏi số 17, 18
Tiến hành đun nóng 100 kg một loại chất béo chứa 80% tristearin, còn lại là các tạp chất không phản ứng với dung dịch NaOH theo phương trình sau:
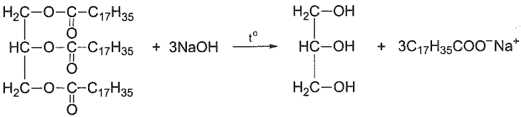

Câu 17 [705937]: Phản ứng trên thuộc loại phản ứng nào?
A, trung hòa.
B, xà phòng hóa.
C, ester hóa.
D, lên men.
Trong công nghiệp, để sản xuất xà phòng, người ta thường đun chất béo (mỡ động vật, dầu thực vật) với dung dịch kiềm đặc ở nhiệt độ cao (phản ứng xà phòng hóa). Sau phản ứng, hỗn hợp muối của acid béo được tách ra bằng cách cho dung dịch muối ăn bảo hoà và hỗn hợp sản phẩm. các muối của acid béo nổi lên, được lấy ra sau đó được trọn với chất phụ gia để làm xà phòng. Phần dung dịch còn lại đem tách và thu hồi glycerol.
(C17H35COO)3C3H5 + 3NaOH → 3C17H35COONa + C3H5(OH)3
⟹ Chọn đáp án B Đáp án: B
(C17H35COO)3C3H5 + 3NaOH → 3C17H35COONa + C3H5(OH)3
⟹ Chọn đáp án B Đáp án: B
Câu 18 [705938]: Sau khi thực hiện phản ứng trên thu được bao nhiêu kilogam sodium stearate? (Biết hiệu suất phản ứng là 90%.)
A, 91,684.
B, 82,515.
C, 74,264.
D, 24,754.
Phương trình phản ứng:
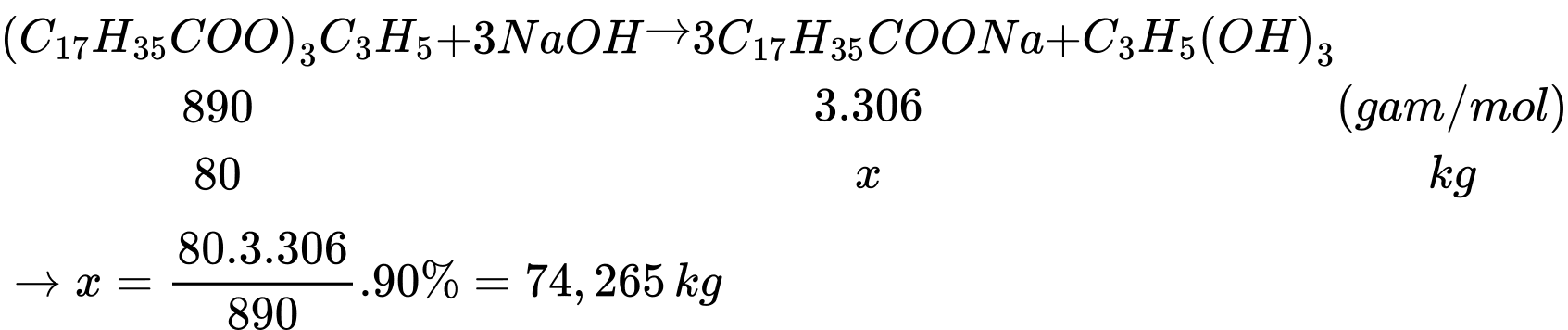
⟹ Chọn đáp án C Đáp án: C
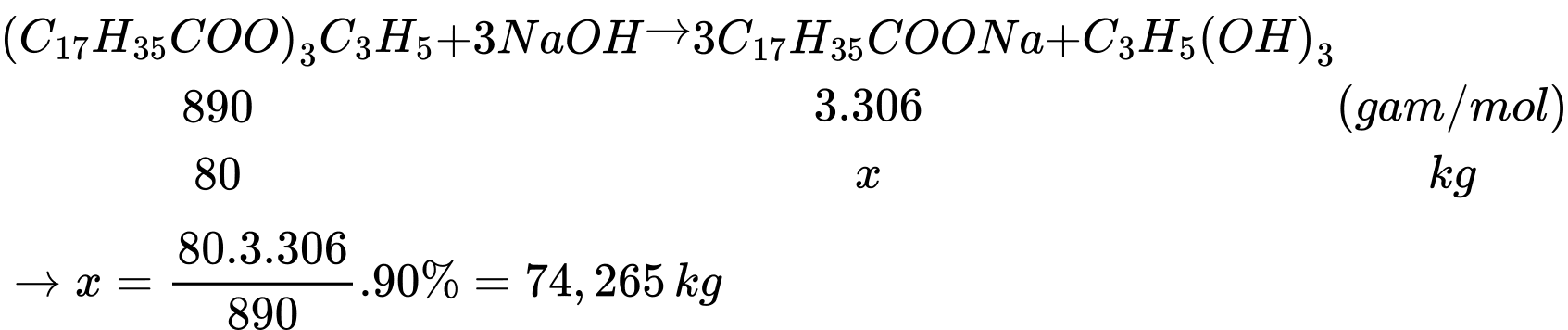
⟹ Chọn đáp án C Đáp án: C
PHẦN II. Thí sinh trả lời từ câu 1 đến câu 4. Trong mỗi ý a), b), c), d) ở mỗi câu, thí sinh chọn đúng hoặc sai
Câu 19 [705939]: Một học sinh tiến hành chuẩn bị hai cốc với các thành phần tương ứng như sau:
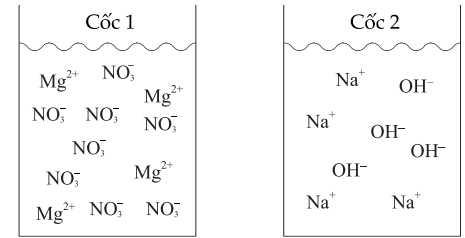
Trộn hai cốc trên vào cốc thứ ba và tạo thành kết tủa Mg(OH)2. Bạn học sinh đưa ra 4 khả năng có thể có về thành phần của cốc thứ ba dưới đây:
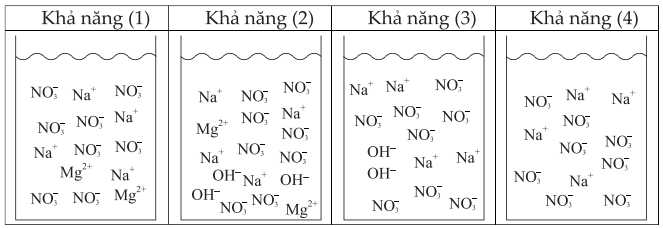

Trộn hai cốc trên vào cốc thứ ba và tạo thành kết tủa Mg(OH)2. Bạn học sinh đưa ra 4 khả năng có thể có về thành phần của cốc thứ ba dưới đây:

Phân tích các phát biểu
✔️A. Đúng. Trộn hai cốc trên vào cốc thứ ba và tạo thành kết tủa Mg(OH)2.
Mg(NO3)2 + 2NaOH → Mg(OH)2 + 2NaNO3
Khi hình thành kết tủa Mg(OH)2 thì ion Mg2+ và OH- mất đi các ion Na+ và NO3- không đổi
✔️B. Đúng. Trộn hai cốc trên vào cốc thứ ba và tạo thành kết tủa Mg(OH)2 tách ra khỏi dung dịch.
❌C. Sai. Số điện tích âm = số điện tích dương, không phải "ion".
❌D. Sai. Từ hình vẽ cốc (1) chứa 4 mol Mg(NO3)2 và cốc (2) chứa 4 mol NaOH
Mg(NO3)2 + 2NaOH → Mg(OH)2 + 2NaNO3
Từ PTHH sau phản ứng NaOH hết, Mg(NO3)2 dư
Dung dịch sau phản ứng gồm: 2 mol Mg(NO3)2 ; 4 mol NaNO3
✔️A. Đúng. Trộn hai cốc trên vào cốc thứ ba và tạo thành kết tủa Mg(OH)2.
Mg(NO3)2 + 2NaOH → Mg(OH)2 + 2NaNO3
Khi hình thành kết tủa Mg(OH)2 thì ion Mg2+ và OH- mất đi các ion Na+ và NO3- không đổi
✔️B. Đúng. Trộn hai cốc trên vào cốc thứ ba và tạo thành kết tủa Mg(OH)2 tách ra khỏi dung dịch.
❌C. Sai. Số điện tích âm = số điện tích dương, không phải "ion".
❌D. Sai. Từ hình vẽ cốc (1) chứa 4 mol Mg(NO3)2 và cốc (2) chứa 4 mol NaOH
Mg(NO3)2 + 2NaOH → Mg(OH)2 + 2NaNO3
Từ PTHH sau phản ứng NaOH hết, Mg(NO3)2 dư
Dung dịch sau phản ứng gồm: 2 mol Mg(NO3)2 ; 4 mol NaNO3
Câu 20 [705940]: Nghiên cứu phản ứng giữa glucose với nước bromine được tiến hành theo bước sau:
∎ Bước 1: Cho vào ống nghiệm khoảng 1 mL nước bromine 1 M.
∎ Bước 2: Thêm tiếp vào ống nghiệm 2 mL dung dịch glucose 2 %. Lắc đều.
∎ Bước 1: Cho vào ống nghiệm khoảng 1 mL nước bromine 1 M.
∎ Bước 2: Thêm tiếp vào ống nghiệm 2 mL dung dịch glucose 2 %. Lắc đều.
Phân tích các đáp án:
❌A – Sai. Tính chất của aldehyde: glucose bị oxi hóa tác dụng với nước bromine làm nước bromine bị mất màu.
✔️B – Đúng. Tính chất của aldehyde: glucose bị oxi hóa tác dụng với nước bromine làm nước bromine bị mất màu.
✔️C – Đúng. Nếu bromine dùng dư thì hỗn hợp sau phản ứng vẫn có màu vàng nâu nguyên do Br2 tan trong nước tạo dung dịch màu vàng nâu.
✔️D – Đúng. Tính chất của aldehyde: glucose tác dụng với nước bromine làm nước bromine bị mất màu. Fructose không làm mất màu nước bromine. Trong glucose có nhóm CHO (Aldehyde) và trong fructose có nhóm C=O (ketone)
❌A – Sai. Tính chất của aldehyde: glucose bị oxi hóa tác dụng với nước bromine làm nước bromine bị mất màu.
✔️B – Đúng. Tính chất của aldehyde: glucose bị oxi hóa tác dụng với nước bromine làm nước bromine bị mất màu.
✔️C – Đúng. Nếu bromine dùng dư thì hỗn hợp sau phản ứng vẫn có màu vàng nâu nguyên do Br2 tan trong nước tạo dung dịch màu vàng nâu.
✔️D – Đúng. Tính chất của aldehyde: glucose tác dụng với nước bromine làm nước bromine bị mất màu. Fructose không làm mất màu nước bromine. Trong glucose có nhóm CHO (Aldehyde) và trong fructose có nhóm C=O (ketone)
Câu 21 [705941]: Trong thực tế, sắc ký bản mỏng silica gel thường được thực hiện đối với hỗn hợp chất sản phẩm và các chất đã biết tham gia ban đầu trong cùng một thí nghiệm để có thể so sánh. Hỗn hợp sản phẩm thường được kí hiệu là Rf. Các chất dùng để so sánh kí hiệu lần lượt từ trái sang phải là (1), (2), (3), (4). Dung môi sẽ chạy ngược từ dưới lên trên, các chất trong hỗn hợp có thể tách ra khỏi nhau trên bản mỏng.
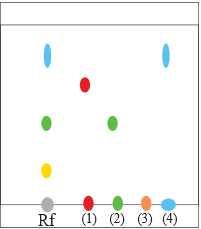

Phân tích các phát biểu:
✔️A – Đúng. Hỗn hợp sản phẩm không chứa chất (1), từ hình vẽ hỗn hợp Rf không chứa chất so sánh (1).
✔️B – Đúng. Có thể kết luận hỗn hợp ban đầu không chứa chất (3) nguyên do không có chất nào phù hợp với chất so sánh (3)
✔️C – Đúng. Từ chất so sánh, hỗn hợp sản phẩm có thể chứa chất (2), (4).
✔️D – Đúng. Liên kết hydrogen và tương tác lưỡng cực – lưỡng cực giữa các phân tử làm cho các hợp chất hữu cơ phân cực bị giữ bởi silica gel mạnh hơn các hợp chất hữu cơ không phân cực, dung môi pha động kéo các hợp chất phân cực đi chậm hơn so với các chất không phân cực.
✔️A – Đúng. Hỗn hợp sản phẩm không chứa chất (1), từ hình vẽ hỗn hợp Rf không chứa chất so sánh (1).
✔️B – Đúng. Có thể kết luận hỗn hợp ban đầu không chứa chất (3) nguyên do không có chất nào phù hợp với chất so sánh (3)
✔️C – Đúng. Từ chất so sánh, hỗn hợp sản phẩm có thể chứa chất (2), (4).
✔️D – Đúng. Liên kết hydrogen và tương tác lưỡng cực – lưỡng cực giữa các phân tử làm cho các hợp chất hữu cơ phân cực bị giữ bởi silica gel mạnh hơn các hợp chất hữu cơ không phân cực, dung môi pha động kéo các hợp chất phân cực đi chậm hơn so với các chất không phân cực.
Câu 22 [560700]: Iron được chiết xuất từ quặng hematite (thành phần chính là Fe2O3, ngoài ra còn có sillic dioxide). Nguyên liệu ban đầu gồm có quặng hematite, than cốc và chất phụ gia như đá vôi sẽ sản xuất được hợp kim quan trọng của iron là gang. Quá trình luyện gang trong lò cao với 3 phản ứng chính:
- Phản ứng tạo chất khử CO (1).
- Phản ứng CO khử iron oxide thành iron (2).
- Phản ứng tạo thành xỉ giữa calcium oxide và sillic dioxide (3).
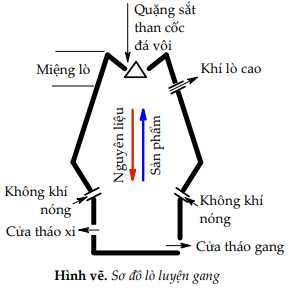
a. Phản ứng xảy ra ở (2) là Fe2O3 + 3CO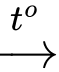 2Fe + 3CO2.
2Fe + 3CO2.
b. Trong các phản ứng ở (1), carbon là chất nhận electron.
c. Phản ứng tạo thành xỉ là CaO + SiO2 → CaSiO3.
d. Vai trò của đá vôi trong là loại bỏ tạp chất sillic dioxide có trong quặng
- Phản ứng tạo chất khử CO (1).
- Phản ứng CO khử iron oxide thành iron (2).
- Phản ứng tạo thành xỉ giữa calcium oxide và sillic dioxide (3).

a. Phản ứng xảy ra ở (2) là Fe2O3 + 3CO
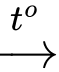 2Fe + 3CO2.
2Fe + 3CO2.b. Trong các phản ứng ở (1), carbon là chất nhận electron.
c. Phản ứng tạo thành xỉ là CaO + SiO2 → CaSiO3.
d. Vai trò của đá vôi trong là loại bỏ tạp chất sillic dioxide có trong quặng
Giai đoạn 1:
C + O2 ⟶ CO2
C + O2 ⟶ CO
Giai đoạn 2 :
3CO + Fe2O3 ⟶ 2Fe + 3CO2
C tăng số oxi hóa trong các giai đoạn ⟶ nhường e
Phân tích các đáp án:
✔️A – Đúng. Phản ứng xảy ra ở (2) là
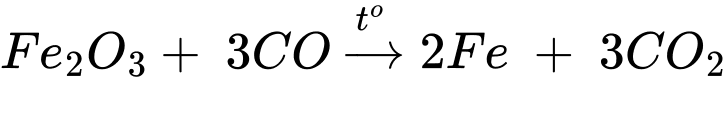
❌B – Sai. Carbon đóng vai trò là chất nhường electron do là chất khử.
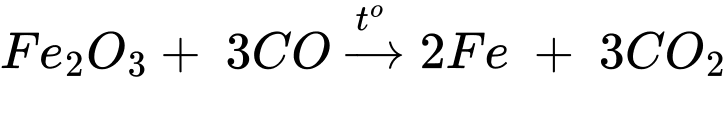
Quá trình oxi hóa: C2+ → C4+ + 2e
Quá trình khử: Fe3+ + 3e → Fe
✔️C – Đúng. Phản ứng tạo thành xỉ là CaO + SiO2 → CaSiO3
✔️D – Đúng. Vai trò của đá vôi là loại bỏ tạp chất sillic dioxide (SiO2) có trong quặng theo quá trình:
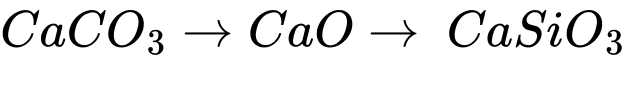
C + O2 ⟶ CO2
C + O2 ⟶ CO
Giai đoạn 2 :
3CO + Fe2O3 ⟶ 2Fe + 3CO2
C tăng số oxi hóa trong các giai đoạn ⟶ nhường e
Phân tích các đáp án:
✔️A – Đúng. Phản ứng xảy ra ở (2) là
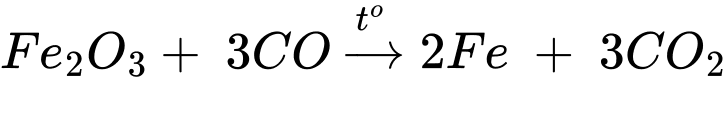
❌B – Sai. Carbon đóng vai trò là chất nhường electron do là chất khử.
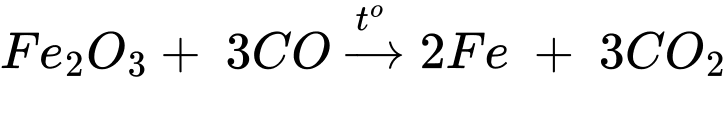
Quá trình oxi hóa: C2+ → C4+ + 2e
Quá trình khử: Fe3+ + 3e → Fe
✔️C – Đúng. Phản ứng tạo thành xỉ là CaO + SiO2 → CaSiO3
✔️D – Đúng. Vai trò của đá vôi là loại bỏ tạp chất sillic dioxide (SiO2) có trong quặng theo quá trình:
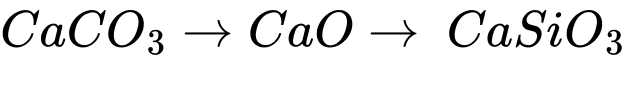
PHẦN III. Thí sinh trả lời từ câu 1 đến câu 6.
Câu 23 [705942]: Khi nung nóng, CuSO4.5H2O sẽ bắt đầu mất dần khối lượng. Đồ thị sau đây biểu diễn sự phụ thuộc của khối lượng chất rắn vào nhiệt độ.
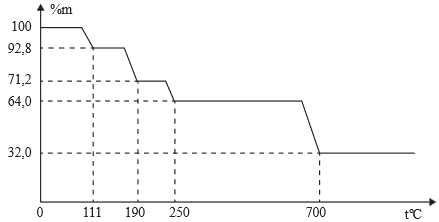
Tại nhiệt độ đạt đến 190 oC, thành phần gần nhất của chất rắn là CuSO4.nH2O. Giá trị của n là bao nhiêu (Làm tròn đến số nguyên)?

Tại nhiệt độ đạt đến 190 oC, thành phần gần nhất của chất rắn là CuSO4.nH2O. Giá trị của n là bao nhiêu (Làm tròn đến số nguyên)?
Tại 190 oC hàm lượng chất rắn còn lại là : 71,2%
CuSO4.nH2O ⟶ CuSO4.xH2O + H2O
m mất đi = m H2O

Điền đáp án : 1
CuSO4.nH2O ⟶ CuSO4.xH2O + H2O
m mất đi = m H2O

Điền đáp án : 1
Câu 24 [705943]: Dẫn khí CO dư qua hỗn hợp bột gồm MgO, CuO, Al2O3 và FeO, nung nóng. Sau khi các phản ứng xảy ra hoàn toàn, thu được hỗn hợp rắn Y. Số oxide kim loại trong Y là
Các oxide bị khử bởi CO là oxide kim loại đứng sau Al : FeO và CuO
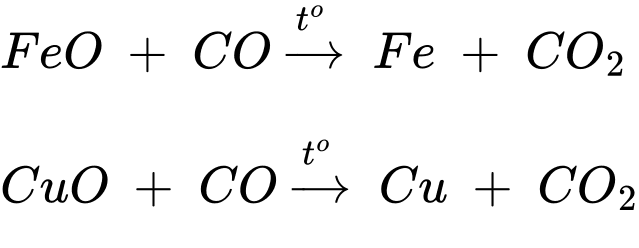
Các oxide trong hỗn hợp Y là MgO và Al2O3
Điền đáp án : 2
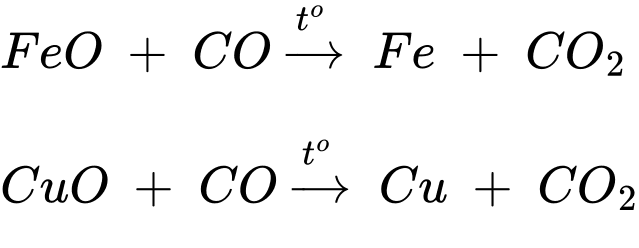
Các oxide trong hỗn hợp Y là MgO và Al2O3
Điền đáp án : 2
Câu 25 [705944]: Tiến hành sản xuất rượu vang bằng phương pháp lên men rượu với nguyên liệu là 16 kg quả nho tươi (chứa 15% glucose về khối lượng), thu được V lít rượu vang 12o. Biết khối lượng riêng của ethyl alcohol nguyên chất là 0,8 g/mL. Giả thiết trong thành phần quả nho tươi chỉ có glucose bị lên men rượu, hiệu suất toàn bộ quá trình sản xuất là 72%. Xác định giá trị của V.
Đổi 16 kg = 16000 gam
Hàm lượng glucose có trong 16 kg nho là mGlucose = 16000.15% = 2400 gam
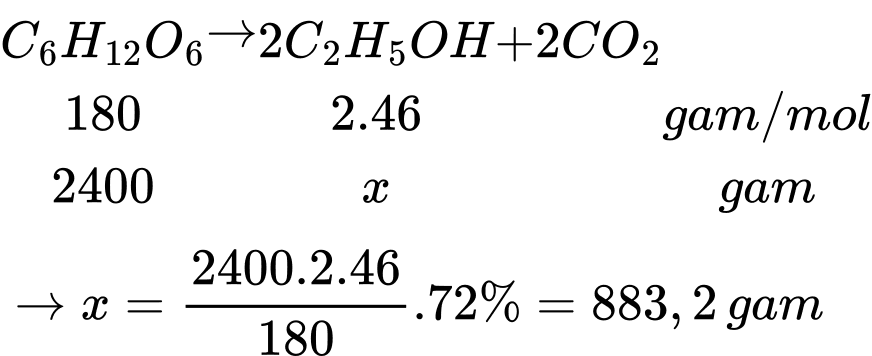
Thể tích ethyl alcohol là VC2H5OH = 883,2 : 0,8 = 1104 mL
Thể tích rượu vang 12o là:
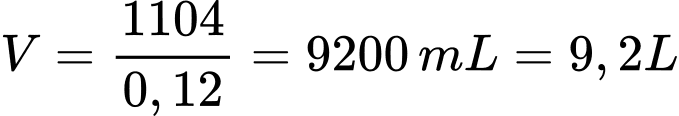
Điền đáp án : 9,2
Hàm lượng glucose có trong 16 kg nho là mGlucose = 16000.15% = 2400 gam
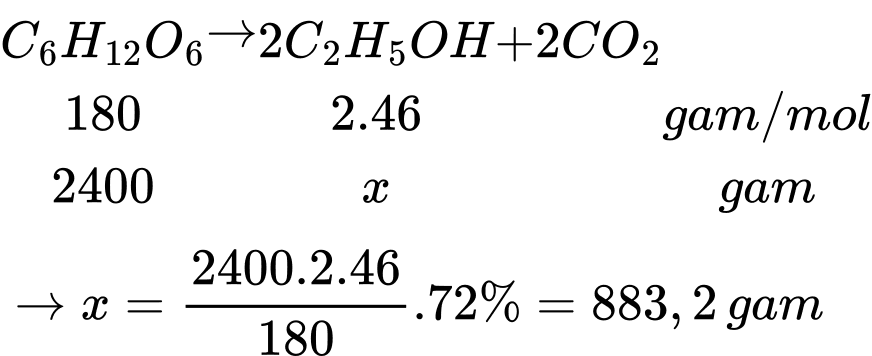
Thể tích ethyl alcohol là VC2H5OH = 883,2 : 0,8 = 1104 mL
Thể tích rượu vang 12o là:
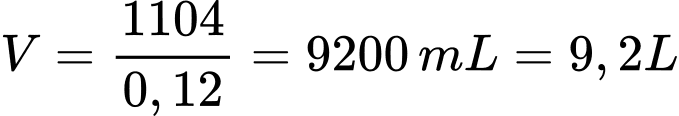
Điền đáp án : 9,2
Câu 26 [705945]: Tartaric acid HOOC–CH(OH)–CH(OH)–COOH có trong nho nhưng cũng có trong me, chuối, bơ. Tiến hành cho 1 mol tartaric acid phản ứng tối đa với a mol NaOH. Giá trị của a là bao nhiêu?
Tartaric acid có 2 nhóm COOH (carboxylic acid) nên 1 mol tartaric acid nên sẽ phản ứng với 2 mol NaOH.
Phương trình :
HOOC–CH(OH)–CH(OH)–COOH + 2NaOH ⟶ NaOOC–CH(OH)–CH(OH)–COONa
Điền đáp án : 2
Phương trình :
HOOC–CH(OH)–CH(OH)–COOH + 2NaOH ⟶ NaOOC–CH(OH)–CH(OH)–COONa
Điền đáp án : 2
Câu 27 [705946]: Nồng độ pyridin trong dung dịch có thể được chuẩn độ bằng dung dịch HCl đã chuẩn hóa. Nếu cần 37,0 mL dung dịch HCl 0,475 M để chuẩn độ 50,0 mL dung dịch pyridin:
C5H5N(aq) + HCl(aq) → C5H5NH+(aq) + Cl–(aq)
Nồng độ pyridin trong dung dịch trước chẩn độ là bao nhiêu (Làm tròn đến hàng phần trăm)?
C5H5N(aq) + HCl(aq) → C5H5NH+(aq) + Cl–(aq)
Nồng độ pyridin trong dung dịch trước chẩn độ là bao nhiêu (Làm tròn đến hàng phần trăm)?
Đổi 37,0 mL = 0,037 L; 50 mL = 0,05 L
Số mol của HCl là nHCl = 0,037.0,475 = 0,017575 mol
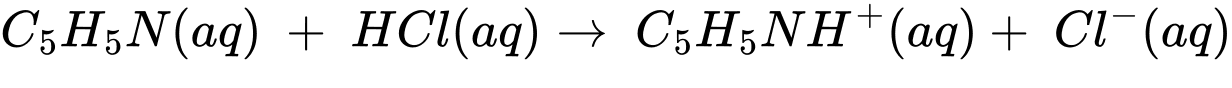
Từ PTHH số mol của pyridin là npyridin = 0,017575 mol
Nồng độ của dung dịch pyridin là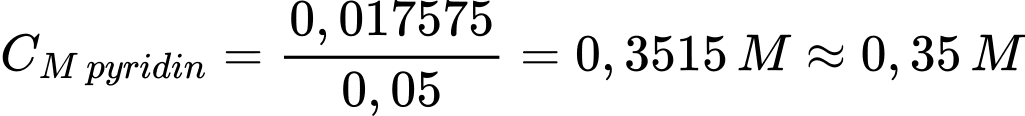
Điền đáp án : 0,35
Số mol của HCl là nHCl = 0,037.0,475 = 0,017575 mol
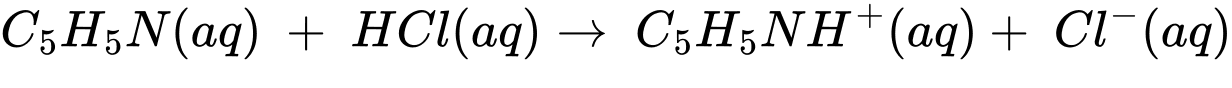
Từ PTHH số mol của pyridin là npyridin = 0,017575 mol
Nồng độ của dung dịch pyridin là
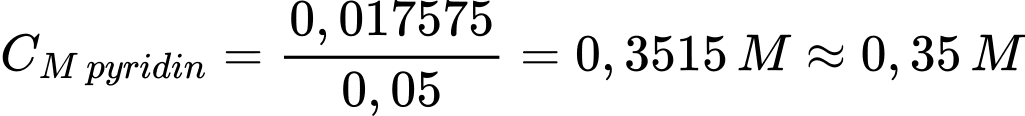
Điền đáp án : 0,35
Câu 28 [705947]: Nước cứng là loại nước chứa hàm lượng chất khoáng cao, chủ yếu là hai ion calcium (Ca2+) và magnesium (Mg2+). Nước cứng là nguyên nhân gây ra nhiều vấn đề nghiêm trọng trong các ngành công nghiệp do đó cần phải được loại bỏ. Phương pháp trao đổi ion để làm mềm nước cứng dựa trên sự thay thế các ion Mg2+ và Ca2+ trong nước cứng (kí hiệu chung là M2+) bằng các cation Na+, H+ có trong các gốc –SO3Na hoặc –SO3H được gắn vào trong nhựa trao đổi ion. Khi nước cứng đi qua nhựa, các ion Ca2+, Mg2+ sẽ được giữ lại và các ion H+, Na+ từ nhựa sẽ đi vào nước theo phản ứng:
M2+ + 2 –SO3X → (–SO3)2M + 2X+ (với X+ là H⁺ hoặc Na+).
Một loại nhựa cationite có phần trăm khối lượng lượng nguyên tố sulfur là 7,94% được sử dụng để loại bỏ các ion Mg2+, Ca2+ trong nước cứng và giả sử nguyên tố sulfur chỉ nằm trong các gốc –SO3X. Nếu khối lượng nhựa cationite đó là 500 gam thì tổng số mol Mg2+, Ca2+ tối đa có thể được loại bỏ là x mol. Giá trị của x là bao nhiêu? (Làm tròn kết quả đến số nguyên)
M2+ + 2 –SO3X → (–SO3)2M + 2X+ (với X+ là H⁺ hoặc Na+).
Một loại nhựa cationite có phần trăm khối lượng lượng nguyên tố sulfur là 7,94% được sử dụng để loại bỏ các ion Mg2+, Ca2+ trong nước cứng và giả sử nguyên tố sulfur chỉ nằm trong các gốc –SO3X. Nếu khối lượng nhựa cationite đó là 500 gam thì tổng số mol Mg2+, Ca2+ tối đa có thể được loại bỏ là x mol. Giá trị của x là bao nhiêu? (Làm tròn kết quả đến số nguyên)
Khối lượng của Sulfur trong nhựa cationite là mS = 500 . 7,94% = 39,7 gam
Số mol của sulfur là nS = 39,7 : 32 = 1,240625 mol
Bảo toàn nguyên tố S: nS = n-SO3X = 1,240625 mol
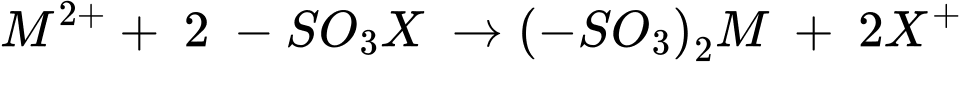
Từ phương trình hóa học tổng số mol của Ca2+ và Mg2+ là nM2+ = 1,240625:2 ≈ 1 mol
Điền đáp án : 1
Số mol của sulfur là nS = 39,7 : 32 = 1,240625 mol
Bảo toàn nguyên tố S: nS = n-SO3X = 1,240625 mol
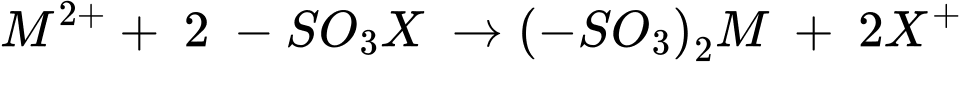
Từ phương trình hóa học tổng số mol của Ca2+ và Mg2+ là nM2+ = 1,240625:2 ≈ 1 mol
Điền đáp án : 1