PHẦN I. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
Câu 1 [703004]: “Ăn mòn kim loại là sự phá huỷ kim loại hoặc …(1)… dưới tác dụng của các chất trong môi trường, trong đó kim loại bị …(2)…”. Nội dung phù hợp trong ô trống (1), (2) lần lượt là
A, hợp kim, oxi hoá.
B, ion kim loại, khử.
C, hợp kim, khử.
D, á kim, oxi hoá.
- Ăn mòn kim loại là quá trình phá hủy kim loại hoặc hỗn hợp kim loại (hợp kim) do các phản ứng hóa học hoặc điện hóa với các chất trong môi trường như không khí, nước, dung dịch acid, base, hoặc muối. Kết quả của quá trình này thường làm hư hỏng cấu trúc kim loại.
- Trong đó kim loại có xu hướng nhường electron thể hiện tính khử (bị oxi hoá)
⇒ Ăn mòn kim loại là sự phá huỷ kim loại hoặc hợp kim dưới tác dụng của các chất trong môi trường, trong đó kim loại bị oxi hoá.
⇒ Chọn đáp án A Đáp án: A
- Trong đó kim loại có xu hướng nhường electron thể hiện tính khử (bị oxi hoá)
⇒ Ăn mòn kim loại là sự phá huỷ kim loại hoặc hợp kim dưới tác dụng của các chất trong môi trường, trong đó kim loại bị oxi hoá.
⇒ Chọn đáp án A Đáp án: A
Câu 2 [792330]: Calcium carbonate được dùng sản xuất vôi, thủy tinh, xi măng. Công thức của Calcium carbonate là
A, CaCO3.
B, Ca(OH)2.
C, CaO.
D, CaCl2.
HD: Calcium: Ca và carbonate: CO3 ⇒ ghép tên: Calcium carbonate là CaCO3
⇝ Chọn đáp án A. Đáp án: A
⇝ Chọn đáp án A. Đáp án: A
Câu 3 [309448]: Polymer X có công thức
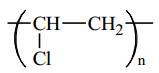
Tên của X là
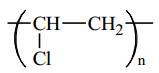
Tên của X là
A, Polyisoprene.
B, Polyethylene.
C, Poly(vinyl chloride).
D, Polychloroethane.
Polymer X được tạo bởi monomer Vinyl chloride (CH2=CHCl) nên Polymer X −(CH2−CHCl)n− có tên gọi là poly(vinyl chloride) hay còn gọi là nhựa PVC.
⇒ Chọn đáp án C Đáp án: C
⇒ Chọn đáp án C Đáp án: C
Câu 4 [703005]: Kim loại nào sau đây dẫn điện tốt nhất?
A, Silver (Ag).
B, Aluminium (Al).
C, Copper (Cu).
D, Mercury (Hg).
Trong số các kim loại, bạc (Ag) có độ dẫn điện cao nhất, tiếp theo là đồng (Cu) và vàng (Au). Tuy nhiên, do giá thành cao và dễ bị oxi hóa, bạc ít được sử dụng trong các ứng dụng thực tế cần dây dẫn lớn mà thay vào đó người ta thường sử dụng đồng.
⇒ Chọn đáp án A Đáp án: A
⇒ Chọn đáp án A Đáp án: A
Câu 5 [575853]: Nguyên tử nguyên tố X có số hiệu nguyên tử là 16, khi tham gia hình thành liên kết hóa học, X tạo thành ion có chứa bao nhiêu electron?
A, 14.
B, 15.
C, 17.
D, 18.
Nguyên tử nguyên tố X có số hiệu nguyên tử là 16, khi tham gia hình thành liên kết hóa học, X có xu hướng nhận thêm 2 electron để tạo thành ion chứa 18 electron có cấu hình giống khí hiếm gần nhất Argon (Z = 18).
⇒ Chọn đáp án D Đáp án: D
⇒ Chọn đáp án D Đáp án: D
Câu 6 [560791]: Tính chất hóa học chung của kim loại kiềm là
A, tính acid.
B, tính base.
C, tính oxi hóa mạnh.
D, tính khử mạnh.
Tính chất hóa học chung của kim loại kiềm là tính khử mạnh.
⇒ Chọn đáp án D Đáp án: D
⇒ Chọn đáp án D Đáp án: D
Câu 7 [703006]: “Trong phương pháp phổ khối lượng, đối với các hợp chất đơn giản, thường mảnh có giá trị m/z lớn nhất ứng với mảnh ion phân tử [M+] và giá trị này bằng giá trị …… của chất nghiên cứu”. Nội dung phù hợp điền vào chỗ trống là
A, nguyên tử khối.
B, phân tử khối.
C, điện tích cation.
D, khối lượng riêng.
Trong phương pháp phổ khối lượng, đối với các hợp chất đơn giản, mảnh có giá trị m/z lớn nhất thường ứng với mảnh ion phân tử [M+], và giá trị này bằng khối lượng phân tử (M) của chất nghiên cứu.
Điều này xảy ra vì ion phân tử [M+] là kết quả của việc chất nghiên cứu mất một electron mà không bị phá vỡ cấu trúc, do đó giá trị m/z của nó phản ánh trực tiếp khối lượng phân tử.
⇒ Chọn đáp án B Đáp án: B
Điều này xảy ra vì ion phân tử [M+] là kết quả của việc chất nghiên cứu mất một electron mà không bị phá vỡ cấu trúc, do đó giá trị m/z của nó phản ánh trực tiếp khối lượng phân tử.
⇒ Chọn đáp án B Đáp án: B
Câu 8 [703007]: Chất Y phản ứng với dung dịch sodium hydroxide tạo thành methanol và sodium ethanoate. Công thức của Y là
A, CH3COOCH3.
B, HCOOC2H5.
C, HOOCCH2CHO.
D, HOCH2CH2COOH.
Phản ứng tổng quát khi thủy phân ester trong môi trường kiềm:
RCOOR' + NaOH ⟶ RCOONa + R'OH
⤑ RCOONa = CH3COONa (sodium ethanote)
⤑ R'OH = CH3OH (methanol)
Ester có công thức là: CH3COOCH3
⇒ Chọn đáp án A
Đáp án: A
RCOOR' + NaOH ⟶ RCOONa + R'OH
⤑ RCOONa = CH3COONa (sodium ethanote)
⤑ R'OH = CH3OH (methanol)
Ester có công thức là: CH3COOCH3
⇒ Chọn đáp án A
Đáp án: A
Câu 9 [304089]: Có bao nhiêu đồng phân cấu tạo của ester ứng với công thức C3H6O2?
A, 2.
B, 3.
C, 4.
D, 5.
HD: ứng với công thức C3H6O2 chỉ có 2 cấu tạo ester như sau:
(1) HCOOCH2CH3 và (2) CH3COOCH3.
⇝ Chọn đáp án A Đáp án: A
(1) HCOOCH2CH3 và (2) CH3COOCH3.
⇝ Chọn đáp án A Đáp án: A
Câu 10 [703008]: Tại các quốc gia hàn đới, khi đến mùa đông, việc di chuyển trên các con đường trở nên khó khăn. Nước bị đóng băng khiến đường trơn trượt và dễ xảy ra tai nạn. Để khắc khục điều này, có thể dùng muối ăn để làm tan băng tuyết. Điều này được giải thích là vì các phân tử nước tạo thành tinh thể khi chúng đóng băng. Nhưng khi có muối trong nước, các ion Na+ và Cl– sẽ cản trở các phân tử nước sắp xếp lại thành tinh thể hơn trong quá trình thay đổi pha từ lỏng sang rắn. Cho các phát biểu sau:
(a) Nước muối NaCl có nhiệt độ nóng chảy thấp hơn nước tinh khiết.
(b) Nguyên tử H của phân tử H2O sẽ hướng về phía các ion dương Na+.
(c) Phân tử nước trong dung dịch muối ăn khó sắp xếp lại thành tinh thể hơn nước tinh khiết.
(d) Khi hòa tan muối ăn vào nước sẽ làm khối lượng riêng của dung dịch giảm.
Các phát biểu đúng là
(a) Nước muối NaCl có nhiệt độ nóng chảy thấp hơn nước tinh khiết.
(b) Nguyên tử H của phân tử H2O sẽ hướng về phía các ion dương Na+.
(c) Phân tử nước trong dung dịch muối ăn khó sắp xếp lại thành tinh thể hơn nước tinh khiết.
(d) Khi hòa tan muối ăn vào nước sẽ làm khối lượng riêng của dung dịch giảm.
Các phát biểu đúng là
A, (a), (c).
B, (c), (d).
C, (a), (b), (c).
D, (a), (c), (d).
Phân tích các phát biểu:
✔️ (a) Đúng. Nước muối NaCl có nhiệt độ nóng chảy thấp hơn nước tinh khiết vì muối hòa tan trong nước làm giảm nhiệt độ đông đặc (hiện tượng hạ nhiệt độ đông đặc).
❌ (b) Sai. Ion Na+ mang điện tích dương nên để tạo liên kết tĩnh điện thì nguyên tử O trong phân tử H2O mang điện tích âm (do phân cực) phải hướng về ion Na+.
✔️ (c) Đúng. Các ion Na+ và Cl- trong nước muối cản trở sự sắp xếp trật tự của các phân tử nước thành tinh thể, khiến nước khó đông đặc hơn.
❌ (d) Sai. Khi hòa tan muối vào nước, khối lượng của dung dịch tăng nhưng thể tích chỉ tăng rất ít, dẫn đến khối lượng riêng của dung dịch tăng chứ không giảm.
Các phát biểu đúng là (a) (c)
⇒ Chọn đáp án A Đáp án: A
✔️ (a) Đúng. Nước muối NaCl có nhiệt độ nóng chảy thấp hơn nước tinh khiết vì muối hòa tan trong nước làm giảm nhiệt độ đông đặc (hiện tượng hạ nhiệt độ đông đặc).
❌ (b) Sai. Ion Na+ mang điện tích dương nên để tạo liên kết tĩnh điện thì nguyên tử O trong phân tử H2O mang điện tích âm (do phân cực) phải hướng về ion Na+.
✔️ (c) Đúng. Các ion Na+ và Cl- trong nước muối cản trở sự sắp xếp trật tự của các phân tử nước thành tinh thể, khiến nước khó đông đặc hơn.
❌ (d) Sai. Khi hòa tan muối vào nước, khối lượng của dung dịch tăng nhưng thể tích chỉ tăng rất ít, dẫn đến khối lượng riêng của dung dịch tăng chứ không giảm.
Các phát biểu đúng là (a) (c)
⇒ Chọn đáp án A Đáp án: A
Câu 11 [703009]: Nguyên tố nào sau đây không phải là nguyên tố dinh dưỡng thiết yếu cho cây trồng?
A, Nitrogen.
B, Platinum.
C, Phosphorus.
D, Potassium.
Nhóm nguyên tố đa lượng thiết yếu của cây trồng là nitrogen (N), potassium (K), phosphorous (P)
⤑ Platinum không phải là nguyên tố dinh dưỡng thiết yếu cho cây trồng.
⇒ Chọn đáp án B Đáp án: B
⤑ Platinum không phải là nguyên tố dinh dưỡng thiết yếu cho cây trồng.
⇒ Chọn đáp án B Đáp án: B
Câu 12 [308506]: Trong phân tử chất nào sau đây có chứa nguyên tố nitrogen?
A, Glucose.
B, Ethyl acetate.
C, Methylamine.
D, Saccharose.
Công thức phân tử của:
❌A. Glucose: C6H12O6
❌B. Ethyl acetate: C4H8O
✔️C. Methylamine: CH5N
❌D. Saccharose:C12H22O11
⇒ Phân tử của Methylamine chứa nguyên tố nitrogen.
⇒ Chọn đáp án C Đáp án: C
❌A. Glucose: C6H12O6
❌B. Ethyl acetate: C4H8O
✔️C. Methylamine: CH5N
❌D. Saccharose:C12H22O11
⇒ Phân tử của Methylamine chứa nguyên tố nitrogen.
⇒ Chọn đáp án C Đáp án: C
Câu 13 [308240]: Carbohydrate có cấu tạo như hình bên thuộc vào nhóm chất nào sau đây?
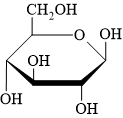

A, Monosaccharide.
B, Disaccharide.
C, Polysaccharide.
D, Carboxylic acid.
HD: Đây là dạng mạch vòng của hợp chất carbohydrate. Một cách trực quan: 1 vòng ⇄ monosaccharide; 2 vòng ⇄ disaccharide và nhiều vòng ⇄ polysaccharide.
Theo đó, ở câu hỏi này quan sát thấy 1 vòng nên hợp chất thuộc loại monosaccharide
⇝ Chọn đáp án A. ♥
p/s: Cụ thể, cấu tạo được cho tương ứng là β-glucose:
 Đáp án: A
Đáp án: A
Theo đó, ở câu hỏi này quan sát thấy 1 vòng nên hợp chất thuộc loại monosaccharide
⇝ Chọn đáp án A. ♥
p/s: Cụ thể, cấu tạo được cho tương ứng là β-glucose:
 Đáp án: A
Đáp án: A
Câu 14 [703010]: Phương trình tổng quát cho sự đốt cháy alkane có công thức phân tử C5H12 là
C5H12 + 8O2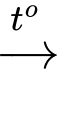 5CO2 + 6H2O
5CO2 + 6H2O
Các giá trị ∆Ho cho sự đốt cháy ba đồng phân pentane là
CH3CH2CH2CH2CH3 = –3536 kJ/mol
(CH3)2CHCH2CH3 = –3529 kJ/mol
(CH3)4C = –3515 kJ/mol
Trong các phát biểu sau, phát biểu nào không đúng?
C5H12 + 8O2
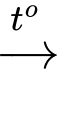 5CO2 + 6H2O
5CO2 + 6H2OCác giá trị ∆Ho cho sự đốt cháy ba đồng phân pentane là
CH3CH2CH2CH2CH3 = –3536 kJ/mol
(CH3)2CHCH2CH3 = –3529 kJ/mol
(CH3)4C = –3515 kJ/mol
Trong các phát biểu sau, phát biểu nào không đúng?
A, Quá trình đốt cháy cả ba đồng phân pentane đều tỏa nhiệt.
B, Cùng khối lượng đốt cháy, 2-methylbutane tỏa nhiệt nhiều hơn n-pentane.
C, Giá trị ∆Ho càng âm thì quá trình đốt cháy tỏa nhiệt càng mạnh.
D, Sự phân nhánh của cấu tạo sẽ làm hợp chất trở nên ổn định hơn.
Phân tích các phát biểu:
✔️ A. Đúng. Tất cả các giá trị ốt cháy của các đồng phân đều âm, cho thấy quá trình đốt cháy đều tỏa nhiệt.
❌ B. Sai. 2-methylbutane và n-pentane là đồng phân cấu tạo, nhiệt lượng tỏa ra khi đốt 2-methylbutane là 3529 kJ.mol-1 và n-pentane là -3536kJ.mol-1 nên pentane tỏa nhiều nhiệt hơn do giá trị ∆Ho càng âm thì quá trình đốt cháy tỏa nhiệt càng mạnh.
✔️ C. Đúng.Giá trị ∆Ho âm biểu thị năng lượng tỏa ra trong quá trình đốt cháy. Giá trị càng âm thì năng lượng tỏa ra càng lớn.
✔️ D. Đúng. Đồng phân càng phân nhánh (như neopentane) thì càng bền nhiệt hơn, dẫn đến
⇒ Chọn đáp án B
Đáp án: B
✔️ A. Đúng. Tất cả các giá trị ốt cháy của các đồng phân đều âm, cho thấy quá trình đốt cháy đều tỏa nhiệt.
❌ B. Sai. 2-methylbutane và n-pentane là đồng phân cấu tạo, nhiệt lượng tỏa ra khi đốt 2-methylbutane là 3529 kJ.mol-1 và n-pentane là -3536kJ.mol-1 nên pentane tỏa nhiều nhiệt hơn do giá trị ∆Ho càng âm thì quá trình đốt cháy tỏa nhiệt càng mạnh.
✔️ C. Đúng.Giá trị ∆Ho âm biểu thị năng lượng tỏa ra trong quá trình đốt cháy. Giá trị càng âm thì năng lượng tỏa ra càng lớn.
✔️ D. Đúng. Đồng phân càng phân nhánh (như neopentane) thì càng bền nhiệt hơn, dẫn đến
⇒ Chọn đáp án B
Đáp án: B
Câu 15 [703011]: “Ở điều kiện thường, amino acid là chất …(1)…, khi ở dạng kết tinh, chúng …(2)…, có nhiệt độ nóng chảy cao và thường tan tốt trong nước”. Nội dung phù hợp trong ô trống (1), (2) lần lượt là
A, rắn, màu trắng.
B, rắn, không màu.
C, khí, không màu.
D, khí, màu vàng.
- Amino acid tồn tại ở dạng tinh thể rắn trong điều kiện thường.
- Phần lớn amino acid ở dạng kết tinh là chất không màu, trừ một số amino acid đặc biệt như tyrosine, có thể hơi vàng nhạt.
- Chúng có nhiệt độ nóng chảy cao do lực tương tác mạnh giữa các ion lưỡng cực.
⇒ Ở điều kiện thường, amino acid là chất rắn, khi ở dạng kết tinh, chúng không màu, có nhiệt độ nóng chảy cao và thường tan tốt trong nước
⇒ Chọn đáp án B Đáp án: B
- Phần lớn amino acid ở dạng kết tinh là chất không màu, trừ một số amino acid đặc biệt như tyrosine, có thể hơi vàng nhạt.
- Chúng có nhiệt độ nóng chảy cao do lực tương tác mạnh giữa các ion lưỡng cực.
⇒ Ở điều kiện thường, amino acid là chất rắn, khi ở dạng kết tinh, chúng không màu, có nhiệt độ nóng chảy cao và thường tan tốt trong nước
⇒ Chọn đáp án B Đáp án: B
Câu 16 [703012]: Một thí nghiệm điện di được tiến hành ở độ pH là 6,0 để tách hỗn hợp gồm ba amino acid arginine, glycine, glutamic acid. Biết tại giá trị pH này, các dạng tồn tại của ba amino acid như sau:
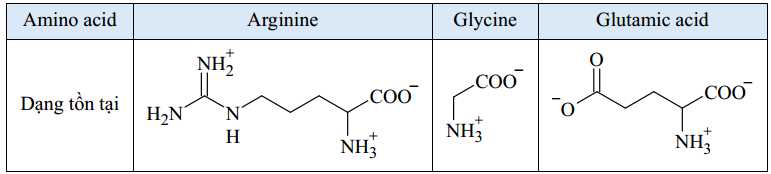
Sau quá trình điện di, kết quả thu được như sau:
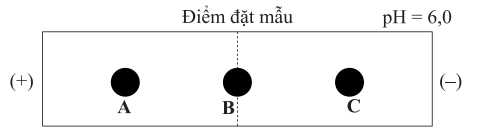
Cho các nhận định sau về quá trình điện di:
(a) Chất B không bị ảnh hưởng điện trường nên không di chuyển.
(b) Nếu đảo chiều điện cực thì vị trí của A và C cũng sẽ bị đảo tương ứng.
(c) Tại môi trường pH = 6 chất C là arginine mang điện tích dương di chuyển về phía cực âm.
(d) Ngoài phương pháp điện di để tách 3 amino acid thì có thể sử dụng phương pháp kết tinh để tách.
Các nhận định đúng là

Sau quá trình điện di, kết quả thu được như sau:

Cho các nhận định sau về quá trình điện di:
(a) Chất B không bị ảnh hưởng điện trường nên không di chuyển.
(b) Nếu đảo chiều điện cực thì vị trí của A và C cũng sẽ bị đảo tương ứng.
(c) Tại môi trường pH = 6 chất C là arginine mang điện tích dương di chuyển về phía cực âm.
(d) Ngoài phương pháp điện di để tách 3 amino acid thì có thể sử dụng phương pháp kết tinh để tách.
Các nhận định đúng là
A, (a), (b).
B, (a), (c).
C, (a), (b), (c).
D, (b), (c), (d).
Ở pH = 6, Arginine có điện tích +1; Glycine trung hoà về điện và Glutamic acid có điện tích là -1.
⇾ Trong quá trình điện di:
- Arginine mang điện dương sẽ di chuyển về cực âm ⤏ Arginine là chất C
- Glycine trung hoà về điện nên gần như không di chuyển trong điện trường ⤏ Glycine là chất B
- Glutamic acid mang điện âm sẽ di chuyển về cực dương ⤏ Glutamic là chất A.
Phân tích các nhận định:
✔️ (a) Đúng. Chất B không bị ảnh hưởng điện trường nên gần như không di chuyển.
✔️ (b) Đúng. Nếu đảo chiều điện cực thì vị trí của A và C cũng sẽ bị đảo tương ứng vì A bị hút về cực dương, C bị hút về cực âm.
✔️ (c) Đúng. Tại môi trường pH = 6 chất C là arginine mang điện tích dương di chuyển về phía cực âm.
❌ (d) Sai. Arginine, glycine và glutamic acid đều có khả năng hòa tan trong nước. Điểm nóng chảy của chúng cũng rất cao (hàng trăm độ C) nên việc kết tinh tách riêng chúng là không khả thi.
⇾ Các phát biểu đúng là (a) (b) (c)
⇒ Chọn đáp án: C Đáp án: C
⇾ Trong quá trình điện di:
- Arginine mang điện dương sẽ di chuyển về cực âm ⤏ Arginine là chất C
- Glycine trung hoà về điện nên gần như không di chuyển trong điện trường ⤏ Glycine là chất B
- Glutamic acid mang điện âm sẽ di chuyển về cực dương ⤏ Glutamic là chất A.
Phân tích các nhận định:
✔️ (a) Đúng. Chất B không bị ảnh hưởng điện trường nên gần như không di chuyển.
✔️ (b) Đúng. Nếu đảo chiều điện cực thì vị trí của A và C cũng sẽ bị đảo tương ứng vì A bị hút về cực dương, C bị hút về cực âm.
✔️ (c) Đúng. Tại môi trường pH = 6 chất C là arginine mang điện tích dương di chuyển về phía cực âm.
❌ (d) Sai. Arginine, glycine và glutamic acid đều có khả năng hòa tan trong nước. Điểm nóng chảy của chúng cũng rất cao (hàng trăm độ C) nên việc kết tinh tách riêng chúng là không khả thi.
⇾ Các phát biểu đúng là (a) (b) (c)
⇒ Chọn đáp án: C Đáp án: C
Sử dụng đoạn thông tin dưới đây để trả lời câu 17 và câu 18:
MgCl2 nóng chảy có thể bị phân hủy thành các nguyên tố nếu như đặt một điện áp đủ lớn vào hai điện cực trơ. Sản phẩm của phản ứng là Mg nóng chảy (ở cực âm) và khí Cl2 (ở cực dương). Cho bảng thế điện cực chuẩn của các bán phản ứng như sau:


Câu 17 [703013]: Giả sử các chất ở điều kiện chuẩn. Hiệu điện thế tối thiểu cần đặt vào để phản ứng điện phân xảy ra là
A, 3,73 V.
B, 1,01 V.
C, 2,16 V.
D, 3,43 V.
MgCl2 –(đpnc)→ Mg + Cl2
Cathode (–): Mg2+ + 2e → Mg
Anode (+): 2Cl– → Cl2 + 2e
→ E = –2,37 – 1,26 = –3,73 V
→ Hiệu điện thế tối thiểu cần đặt vào để phản ứng điện phân là 3,73 V
⇒ Chọn đáp án A Đáp án: A
Cathode (–): Mg2+ + 2e → Mg
Anode (+): 2Cl– → Cl2 + 2e
→ E = –2,37 – 1,26 = –3,73 V
→ Hiệu điện thế tối thiểu cần đặt vào để phản ứng điện phân là 3,73 V
⇒ Chọn đáp án A Đáp án: A
Câu 18 [703014]: Nếu dòng điện trong bình được giữ ở mức không đổi 5 A, giả sử hằng số Faraday bằng 96485 C thì mất bao nhiêu giây để tạo ra 2,00 gam Mg(l) ở cực âm?
A, 2160.
B, 4190.
C, 3180.
D, 3216.
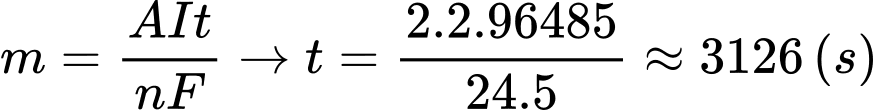
⇒ Chọn đáp án D Đáp án: D
Thí sinh trả lời từ câu 1 đến câu 4. Trong mỗi ý a), b), c), d) ở mỗi câu, thí sinh chọn đúng hoặc sai
Câu 19 [703015]: Phân tử khối tương đối của muối X2CO3 có thể được xác định, từ đó dự đoán được kim loại X bằng thí nghiệm đơn giản sau:
▪ Bước 1: Đo khối lượng của bình cân rỗng.
▪ Bước 2: Đo khối lượng của một bình cân chứa X2CO3.
▪ Bước 3: Chuyển 50,0 mL hydrochloric acid 2 M (dư) vào bình hình nón dung tích 250 mL.
▪ Bước 4: Thêm sodium carbonate vào trong bình nón chứa acid để làm bão hòa carbon dioxide tan trong dung dịch.
▪ Bước 5: Đặt một nút bông gòn vào cổ bình nón và cân bình nón (chứa acid).
▪ Bước 6: Thêm X2CO3 vào bình nón chứa acid và nhanh chóng đậy nút bông gòn vào cổ bình.
▪ Bước 7: Khi phản ứng trong bình dừng lại, để bình trong 10 phút để carbon dioxide khuếch tán ra khỏi bình. Đo khối lượng của bình nón chứa hỗn hợp sau phản ứng.

Các kết quả cân khối lượng được cho trong bảng sau:

▪ Bước 1: Đo khối lượng của bình cân rỗng.
▪ Bước 2: Đo khối lượng của một bình cân chứa X2CO3.
▪ Bước 3: Chuyển 50,0 mL hydrochloric acid 2 M (dư) vào bình hình nón dung tích 250 mL.
▪ Bước 4: Thêm sodium carbonate vào trong bình nón chứa acid để làm bão hòa carbon dioxide tan trong dung dịch.
▪ Bước 5: Đặt một nút bông gòn vào cổ bình nón và cân bình nón (chứa acid).
▪ Bước 6: Thêm X2CO3 vào bình nón chứa acid và nhanh chóng đậy nút bông gòn vào cổ bình.
▪ Bước 7: Khi phản ứng trong bình dừng lại, để bình trong 10 phút để carbon dioxide khuếch tán ra khỏi bình. Đo khối lượng của bình nón chứa hỗn hợp sau phản ứng.

Các kết quả cân khối lượng được cho trong bảng sau:

X2CO3 + 2HCl → 2XCl + CO2↑ + H2O
Khối lượng muối là:
mbình cân + X2CO3 – mbình rỗng = 14,29 – 11,48 = 2,81 (gam)
Gọi khối lượng khí thoát ra là x (gam)
Áp dụng định luật bảo toàn khối lượng:
mbình nón + mdd acid + mmuối = mbình nón + mdd sau phản ứng + mCO2
⇔ 221,35 + 2,81 = 223,21 + x
→ x = 0,95 (gam)
Từ PTHH:
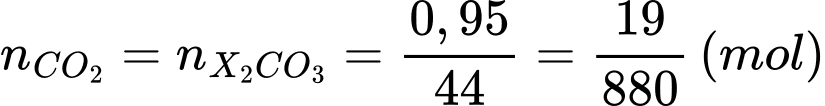
→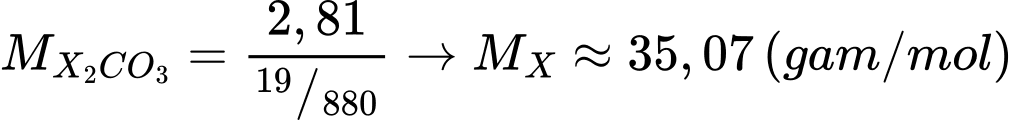
Phân tích các phát biểu:
✔️ a) Đúng. Phân tử khối của X (35,07) gần nhất với potassium (39) nên X có khả năng là potassium.
✔️ b) Đúng. Khi tăng nồng độ acid, số ion H+ tham gia phản ứng tăng lên, làm tăng tốc độ phản ứng giữa acid và muối nên khí CO2 được giải phóng nhanh hơn, dẫn đến tốc độ thoát khí CO2 tăng.
❌ c) Sai. Nếu CO2 khuếch tán trong dung dịch thì lượng CO2 thu được đã hao hụt và ít hơn so với thực tế.
✔️ d) Đúng. Từ phương trình phản ứng, ta thấy số mol CO2 sinh ra tỷ lệ với số mol muối carbonate được sử dụng. Mà acid dư nên lượng CO2 sinh ra phụ thuộc vào muối carbonate → Lượng carbon dioxide thoát ra tỉ lệ thuận với khối lượng muối carbonate được sử dụng khi acid dư.
Khối lượng muối là:
mbình cân + X2CO3 – mbình rỗng = 14,29 – 11,48 = 2,81 (gam)
Gọi khối lượng khí thoát ra là x (gam)
Áp dụng định luật bảo toàn khối lượng:
mbình nón + mdd acid + mmuối = mbình nón + mdd sau phản ứng + mCO2
⇔ 221,35 + 2,81 = 223,21 + x
→ x = 0,95 (gam)
Từ PTHH:
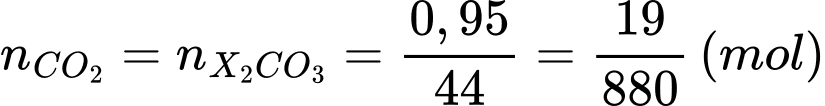
→
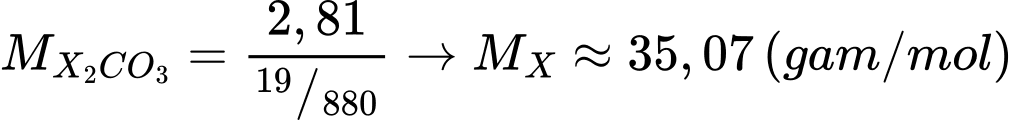
Phân tích các phát biểu:
✔️ a) Đúng. Phân tử khối của X (35,07) gần nhất với potassium (39) nên X có khả năng là potassium.
✔️ b) Đúng. Khi tăng nồng độ acid, số ion H+ tham gia phản ứng tăng lên, làm tăng tốc độ phản ứng giữa acid và muối nên khí CO2 được giải phóng nhanh hơn, dẫn đến tốc độ thoát khí CO2 tăng.
❌ c) Sai. Nếu CO2 khuếch tán trong dung dịch thì lượng CO2 thu được đã hao hụt và ít hơn so với thực tế.
✔️ d) Đúng. Từ phương trình phản ứng, ta thấy số mol CO2 sinh ra tỷ lệ với số mol muối carbonate được sử dụng. Mà acid dư nên lượng CO2 sinh ra phụ thuộc vào muối carbonate → Lượng carbon dioxide thoát ra tỉ lệ thuận với khối lượng muối carbonate được sử dụng khi acid dư.
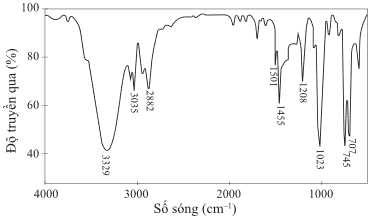
Câu 20 [703016]: Ba hợp chất thơm A, B, C đều có ứng dụng trong thực tiễn: A có tác dụng chống sinh vật kí sinh (chấy, rận); B làm chất tạo mùi hạnh nhân; C là chất bảo quản thực phẩm do có tác dụng kháng nấm, diệt khuẩn. A có công thức phân tử là C7H8O, phố IR của A được thể hiện như sau:

Cho sơ đồ chuyển hoá: A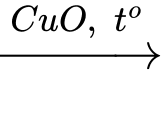 B
B 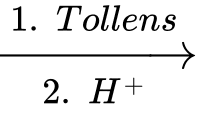 C.
C.


Cho sơ đồ chuyển hoá: A
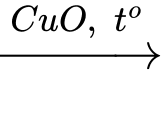 B
B 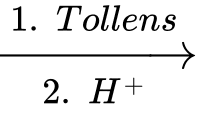 C.
C.
Sơ đồ chuyển hóa xảy ra như sau:
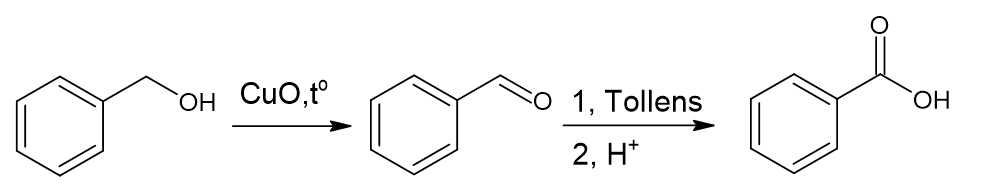
Phân tích các phát biểu:
✔️ a) Đúng. B là Benzaldehyde, có nhóm C=O, nên có peak hấp thụ đặc trung ở khoảng 1700 cm-1.
❌ b) Sai. C là benzoic acid nên có nhiệt độ sôi cao hơn alcohol và ester.
Thứ tự nhiệt độ sôi giảm tăng dần là: CH3CHO < C6H5COOCH3 < C2H5OH < C.
❌ c) Sai. A có công thức cấu tạo là C6H5CH2OH.
✔️ d) Đúng. Dựa vào phổ hồng ngoại, phân biệt được 3 hợp chất A, B, C do có số sóng hấp thụ đặc trưng riêng.

Phân tích các phát biểu:
✔️ a) Đúng. B là Benzaldehyde, có nhóm C=O, nên có peak hấp thụ đặc trung ở khoảng 1700 cm-1.
❌ b) Sai. C là benzoic acid nên có nhiệt độ sôi cao hơn alcohol và ester.
Thứ tự nhiệt độ sôi giảm tăng dần là: CH3CHO < C6H5COOCH3 < C2H5OH < C.
❌ c) Sai. A có công thức cấu tạo là C6H5CH2OH.
✔️ d) Đúng. Dựa vào phổ hồng ngoại, phân biệt được 3 hợp chất A, B, C do có số sóng hấp thụ đặc trưng riêng.
Câu 21 [703017]: Đồng phân là những hợp chất khác nhau nhưng có cùng công thức phân tử, chúng có cùng số lượng và loại nguyên tử nhưng được sắp xếp khác nhau. Phức chất tồn tại một loại đồng phân gọi là đồng phân ion hóa. Chúng sẽ khác nhau về vị trí của phối tử ion có mặt trong cầu nội hoặc cầu ngoại. Cùng xem xét hai đồng phân ion hóa sau:
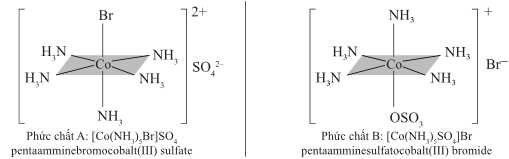
▪ Phức chất A: [Co(NH3)5Br]SO4 màu đỏ tím với phối tử Br– ở cầu nội và SO42– ở cầu ngoại.
▪ Phức chất B: [Co(NH3)5SO4]Br màu đỏ với phối tử SO42– ở cầu nội và Br– ở cầu ngoại.
Các phối tử ở cầu ngoại dễ dàng phân li trong dung dịch, đồng nghĩa với tính chất hóa học và khả năng dẫn điện của các đồng phân ion hóa cũng sẽ khác nhau.

▪ Phức chất A: [Co(NH3)5Br]SO4 màu đỏ tím với phối tử Br– ở cầu nội và SO42– ở cầu ngoại.
▪ Phức chất B: [Co(NH3)5SO4]Br màu đỏ với phối tử SO42– ở cầu nội và Br– ở cầu ngoại.
Các phối tử ở cầu ngoại dễ dàng phân li trong dung dịch, đồng nghĩa với tính chất hóa học và khả năng dẫn điện của các đồng phân ion hóa cũng sẽ khác nhau.
Phân tích các phát biểu:
✔️ a) Đúng. Cả hai phức chất A và B đều có 6 đỉnh tạo thành dạng hình học bát diện (8 mặt).
✔️ b) Đúng. Cho BaCl2 vào dung dịch phức chất A, thấy xuất hiện kết tủa trắng:
Ba2+ + SO42- → BaSO4↓ (màu trắng)
✔️ c) Đúng. Khi cùng nồng độ, dung dịch phức chất A phân li được ra ion có điện tích lớn hơn phức chất B nên độ dẫn điện của A tốt hơn B.
✔️ d) Đúng. Có thể dùng các dung dịch thuốc thử chứa ion Ba2+ hoặc ion Ag+ để phân biệt được hai dung dịch phức chất A và B do có tạo kết tủa có màu sắc khác nhau như sau:
Ba2+ + SO42- → BaSO4↓ (màu trắng) → nhận biết được phức chất A.
Ag+ + Br- → AgBr↓ (màu vàng nhạt) → nhận biết được phức chất B.
✔️ a) Đúng. Cả hai phức chất A và B đều có 6 đỉnh tạo thành dạng hình học bát diện (8 mặt).
✔️ b) Đúng. Cho BaCl2 vào dung dịch phức chất A, thấy xuất hiện kết tủa trắng:
Ba2+ + SO42- → BaSO4↓ (màu trắng)
✔️ c) Đúng. Khi cùng nồng độ, dung dịch phức chất A phân li được ra ion có điện tích lớn hơn phức chất B nên độ dẫn điện của A tốt hơn B.
✔️ d) Đúng. Có thể dùng các dung dịch thuốc thử chứa ion Ba2+ hoặc ion Ag+ để phân biệt được hai dung dịch phức chất A và B do có tạo kết tủa có màu sắc khác nhau như sau:
Ba2+ + SO42- → BaSO4↓ (màu trắng) → nhận biết được phức chất A.
Ag+ + Br- → AgBr↓ (màu vàng nhạt) → nhận biết được phức chất B.
Câu 22 [703018]: Lactose là một hợp chất carbohydrate có trong sữa và các sản phẩm từ sữa khác.
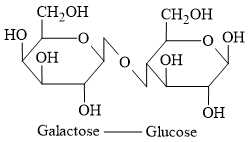
Khi lactose được tiêu hóa, liên kết giữa hai monosaccharide bị phá vỡ. Enzyme chịu trách nhiệm phá vỡ liên kết là lactase, được tìm thấy trong ruột non. Hàng triệu người thiếu hụt đủ lượng lactase, khiến họ không thể tiêu hóa lactose đầy đủ, dẫn đến tình trạng được gọi là không dung nạp lactose. Nghiên cứu biểu đồ và trả lời các câu hỏi.
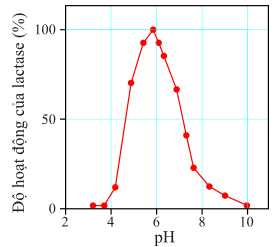

Khi lactose được tiêu hóa, liên kết giữa hai monosaccharide bị phá vỡ. Enzyme chịu trách nhiệm phá vỡ liên kết là lactase, được tìm thấy trong ruột non. Hàng triệu người thiếu hụt đủ lượng lactase, khiến họ không thể tiêu hóa lactose đầy đủ, dẫn đến tình trạng được gọi là không dung nạp lactose. Nghiên cứu biểu đồ và trả lời các câu hỏi.

Phân tích các phát biểu:
✔️ a) Đúng. Enzyme lactase sẽ thủy phân lactose thành glucose và galactose do lactose cấu tạo từ glucose và galactose.
✔️ b) Đúng. Tại pH = 6 độ hoạt động của lactase lớn nhất là 100% nên lượng sản phẩm monosacchride thu được là lớn nhất.
❌ c) Sai. Tại pH = 5,5 độ hoạt động của lactase khoảng 90%.
❌ d) Sai. Độ hoạt động của lactase giảm khi tăng pH từ 6 – 10.
✔️ a) Đúng. Enzyme lactase sẽ thủy phân lactose thành glucose và galactose do lactose cấu tạo từ glucose và galactose.
✔️ b) Đúng. Tại pH = 6 độ hoạt động của lactase lớn nhất là 100% nên lượng sản phẩm monosacchride thu được là lớn nhất.
❌ c) Sai. Tại pH = 5,5 độ hoạt động của lactase khoảng 90%.
❌ d) Sai. Độ hoạt động của lactase giảm khi tăng pH từ 6 – 10.
PHẦN III. Thí sinh trả lời từ câu 1 đến câu 6.
Câu 23 [703019]: Vàng (Au) đơn chất tồn tại trong tự nhiên ở trong quặng vàng thường có hàm lượng vàng thấp. Để thu hồi vàng từ quặng vàng, người ta nghiền quặng, hoà tan chúng vào dung dịch KCN và liên tục sục không khí vào. Vàng bị hoà tan tạo thành phức chất:
4Au(s) + 8KCN(aq) + O2(g) + 2H2O(l) 4K[Au(CN)2](aq) + 4KOH(aq) (1)
4K[Au(CN)2](aq) + 4KOH(aq) (1)
và sau đó kết tủa vàng bằng kẽm (Zn):
Zn(s) + 2K[Au(CN)2] (aq) K2[Zn(CN)4](aq) + 2Au(s) (2)
K2[Zn(CN)4](aq) + 2Au(s) (2)
Nếu dùng 13 kg KCN thì có thể tách được bao nhiêu kg vàng từ quặng theo chuỗi phản ứng trên? Giả thiết các chất khác trong quặng không phản ứng với KCN.
4Au(s) + 8KCN(aq) + O2(g) + 2H2O(l)
 4K[Au(CN)2](aq) + 4KOH(aq) (1)
4K[Au(CN)2](aq) + 4KOH(aq) (1)và sau đó kết tủa vàng bằng kẽm (Zn):
Zn(s) + 2K[Au(CN)2] (aq)
 K2[Zn(CN)4](aq) + 2Au(s) (2)
K2[Zn(CN)4](aq) + 2Au(s) (2)Nếu dùng 13 kg KCN thì có thể tách được bao nhiêu kg vàng từ quặng theo chuỗi phản ứng trên? Giả thiết các chất khác trong quặng không phản ứng với KCN.
Đổi 13 kg = 13000 gam
4Au(s) + 8KCN(aq) + O2(g) + 2H2O(l) → 4K[Au(CN)2](aq) + 4KOH(aq) (1)
Zn(s) + 2K[Au(CN)2](aq) → K2[Zn(CN)4](aq) + 2Au(s) (2)
Số mol của KCN là: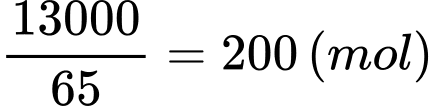
Từ phương trình (1) và (2) ⇒ số mol của Au là 100 (mol)
Khối lượng vàng thu được là:
100.197 = 19 700 (gam) = 19,7 (kg)
⇒ Điền đáp án: 19,7
4Au(s) + 8KCN(aq) + O2(g) + 2H2O(l) → 4K[Au(CN)2](aq) + 4KOH(aq) (1)
Zn(s) + 2K[Au(CN)2](aq) → K2[Zn(CN)4](aq) + 2Au(s) (2)
Số mol của KCN là:
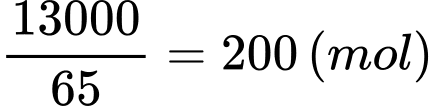
Từ phương trình (1) và (2) ⇒ số mol của Au là 100 (mol)
Khối lượng vàng thu được là:
100.197 = 19 700 (gam) = 19,7 (kg)
⇒ Điền đáp án: 19,7
Câu 24 [703020]: Eicosapentanoic acid (EPA) còn gọi là “chất có tính lọc máu” giúp sản xuất prostaglandin trong máu – một chất giúp giảm độ quánh của máu và ức chế tạo các tiểu cầu nhằm làm và ngăn ngừa chứng huyết khối, làm giảm cholesterol và triglycerides có trong máu.. EPA có công thức cấu tạo như sau:
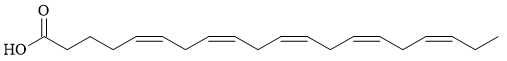
Có bao nhiêu liên kết π có trong một phân tử EPA?

Có bao nhiêu liên kết π có trong một phân tử EPA?
Liên kết π là các liên kết dôi trong phân tử. Một phân tử EPA có các liên kết π ở các vị trí như sau:
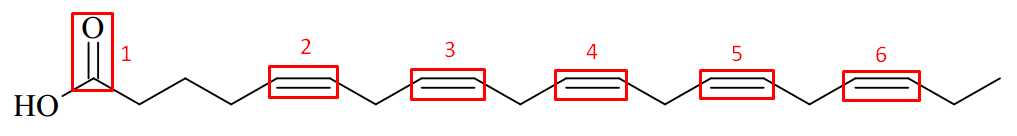
→ Có 6 liên kết π trong một phân tử EPA.

→ Có 6 liên kết π trong một phân tử EPA.
⇒ Điền đáp án: 6
Câu 25 [703021]: Dung dịch glucose ở dạng mạch hở có chứa nhóm aldehyde CHO nên có thể phản ứng oxi hóa khử với Cu(OH)2, các bước tiến hành thí nghiệm như sau:
▪ Bước 1: Chuẩn bị hai ống nghiệm có đánh số (1) và (2); thêm vào mỗi ống nghiệm khoảng 0,5 – 1,0 mL dung dịch CuSO4 5% và 1 mL dung dịch NaOH 10%, lắc nhẹ.
▪ Bước 2: Cho 3 mL dung dịch glucose 2% vào mỗi ống nghiệm, lắc nhẹ.
▪ Bước 3: Đun nhẹ ống (2) đến khi hoá chất trong ống nghiệm đổi màu hoàn toàn.
Cho các phương trình hóa học như sau:
(1) CuSO4 + 2NaOH Cu(OH)2↓ + Na2SO4.
Cu(OH)2↓ + Na2SO4.
(2) Cu(OH)2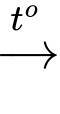 Cu2O.
Cu2O.
(3) 2C6H12O6 + Cu(OH)2 Cu(C6H11O6)2 + 2H2O.
Cu(C6H11O6)2 + 2H2O.
(4) C6H12O6 + 2Cu(OH)2 + NaOH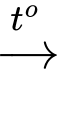 C5H11COONa + Cu2O↓ + 3H2O.
C5H11COONa + Cu2O↓ + 3H2O.
(5) 2C6H12O6 + O2 2C6H12O7.
2C6H12O7.
Hãy sắp xếp các phương trình hóa học dùng để giải thích cho các bước theo đúng thứ tự trong thí nghiệm trên (ví dụ: 123, 135, ...).
▪ Bước 1: Chuẩn bị hai ống nghiệm có đánh số (1) và (2); thêm vào mỗi ống nghiệm khoảng 0,5 – 1,0 mL dung dịch CuSO4 5% và 1 mL dung dịch NaOH 10%, lắc nhẹ.
▪ Bước 2: Cho 3 mL dung dịch glucose 2% vào mỗi ống nghiệm, lắc nhẹ.
▪ Bước 3: Đun nhẹ ống (2) đến khi hoá chất trong ống nghiệm đổi màu hoàn toàn.
Cho các phương trình hóa học như sau:
(1) CuSO4 + 2NaOH
 Cu(OH)2↓ + Na2SO4.
Cu(OH)2↓ + Na2SO4.(2) Cu(OH)2
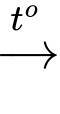 Cu2O.
Cu2O.(3) 2C6H12O6 + Cu(OH)2
 Cu(C6H11O6)2 + 2H2O.
Cu(C6H11O6)2 + 2H2O.(4) C6H12O6 + 2Cu(OH)2 + NaOH
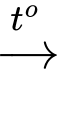 C5H11COONa + Cu2O↓ + 3H2O.
C5H11COONa + Cu2O↓ + 3H2O.(5) 2C6H12O6 + O2
 2C6H12O7.
2C6H12O7.Hãy sắp xếp các phương trình hóa học dùng để giải thích cho các bước theo đúng thứ tự trong thí nghiệm trên (ví dụ: 123, 135, ...).
Các bước tiến hành thí nghiệm phản ứng oxi hóa khử của dung dịch glucose ở dạng mạch hở với Cu(OH)2 như sau:
Bước 1: Phản ứng tạo kết tủa Cu(OH)2
CuSO4 + 2NaOH → Na2SO4 + Cu(OH)2
Bước 2: Tính chất của polyalcohol qua phản ứng của glucose với Cu(OH)2 ở nhiệt độ thường tạo dung dịch màu xanh lam.
Cu(OH)2 + 2C6H12O6 → [C6H11O6]2Cu + 2H2O
Bước 3: Đun nhẹ ống (2) thì xuất hiện kết tủa màu đỏ gạch, tính oxi hóa của glucose.
C6H12O6 + 2Cu(OH)2 + NaOH → C5H11O5COONa + Cu2O + 3H2O
→ Các phương trình hóa học xảy ra theo đúng thức tự các bước thí nghiệm là: 1→3→4.
⇒ Điền đáp án: 134
Bước 1: Phản ứng tạo kết tủa Cu(OH)2
CuSO4 + 2NaOH → Na2SO4 + Cu(OH)2
Bước 2: Tính chất của polyalcohol qua phản ứng của glucose với Cu(OH)2 ở nhiệt độ thường tạo dung dịch màu xanh lam.
Cu(OH)2 + 2C6H12O6 → [C6H11O6]2Cu + 2H2O
Bước 3: Đun nhẹ ống (2) thì xuất hiện kết tủa màu đỏ gạch, tính oxi hóa của glucose.
C6H12O6 + 2Cu(OH)2 + NaOH → C5H11O5COONa + Cu2O + 3H2O
→ Các phương trình hóa học xảy ra theo đúng thức tự các bước thí nghiệm là: 1→3→4.
⇒ Điền đáp án: 134
Câu 26 [703022]: Thuỷ phân hoàn toàn 2 mol Lys-Ala-Val trong dung dịch HCl dư thì số mol HCl phản ứng là bao nhiêu?
Phản ứng thủy phân tripeptide Lys-Ala-Val trong dung dịch HCl xảy ra như sau:
Lys-Ala-Val + 4HCl + 2H2O → ClH3N(CH2)4CH(NH3Cl)COOH + CH3CH(NH3Cl)COOH + CH3CH(CH3)CH(NH3Cl)COOH
Thấy số mol của HCl tỉ lệ 4 : 1 với số mol của tripeptide trên phản ứng nên HCl dư thì số mol HCl phản ứng là:
nHCl = 4nLys-Ala-Val = 4 x 2 = 8 (mol)
⇒ Điền đáp án: 8
Lys-Ala-Val + 4HCl + 2H2O → ClH3N(CH2)4CH(NH3Cl)COOH + CH3CH(NH3Cl)COOH + CH3CH(CH3)CH(NH3Cl)COOH
Thấy số mol của HCl tỉ lệ 4 : 1 với số mol của tripeptide trên phản ứng nên HCl dư thì số mol HCl phản ứng là:
nHCl = 4nLys-Ala-Val = 4 x 2 = 8 (mol)
⇒ Điền đáp án: 8
Câu 27 [703023]: Đá vôi là loại đá trầm tích bao gồm các khoáng vật của calcium và các dạng kết tinh khác nhau của calcium carbonate. Đá vôi hay còn gọi là calcium carbonate là một trong những vật liệu hữu ích và linh hoạt đối với con người. Đá vôi rất phổ biến và được tìm thấy trên thế giới trong trầm tích, đá biến chất và đá lửa. Đá vôi ít khi ở dạng tinh khiết mà thường bị lẫn các tạp chất như đá phiến silic, đá macma, silica, đất sét, bùn, cát... Trong quá trình sản xuất vôi sống từ đá vôi xảy ra phản ứng sau:
CaCO3(s)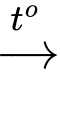 CaO(s) + CO2(g) (1)
CaO(s) + CO2(g) (1)
CH4(g) + O2(g)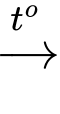 CO2(g) + H2O(l) (2)
CO2(g) + H2O(l) (2)
Nhiệt lượng từ phản ứng số (2) cung cấp cho quá trình nung CaCO3 sản xuất vôi sống. Tính thể tích CH4 (m3) ở đkc được sủa dụng để sản xuất 5,6 tấn vôi sống. Giả thiết hiệu suất chuyển hóa nhiệt năng có ích là 80% và hiệu suất của quá trình sản xuất vôi sống là 85% (làm tròn đến số nguyên). Bảng sau cung cấp enthalpy tiêu chuẩn của một số chất:

CaCO3(s)
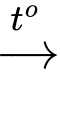 CaO(s) + CO2(g) (1)
CaO(s) + CO2(g) (1)CH4(g) + O2(g)
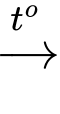 CO2(g) + H2O(l) (2)
CO2(g) + H2O(l) (2)Nhiệt lượng từ phản ứng số (2) cung cấp cho quá trình nung CaCO3 sản xuất vôi sống. Tính thể tích CH4 (m3) ở đkc được sủa dụng để sản xuất 5,6 tấn vôi sống. Giả thiết hiệu suất chuyển hóa nhiệt năng có ích là 80% và hiệu suất của quá trình sản xuất vôi sống là 85% (làm tròn đến số nguyên). Bảng sau cung cấp enthalpy tiêu chuẩn của một số chất:

Đổi 5,6 tấn = 5,6.106 (gam)
Số mol của vôi sống tạo thành là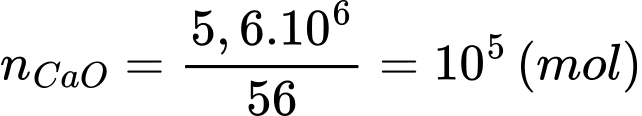
CaCO3(s)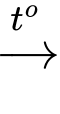 CaO(s) + CO2(g) (1)
CaO(s) + CO2(g) (1) 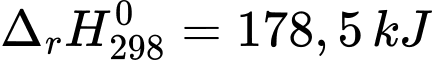
→ Để thu được 1 mol CaO(s), cần phải cung cấp nhiệt lượng là 178,5 kJ để chuyển 1 mol CaCO3(s) thành CaO (s).
CH4(g) + O2(g)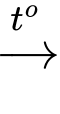 CO2(g) + H2O(l) (2)
CO2(g) + H2O(l) (2) 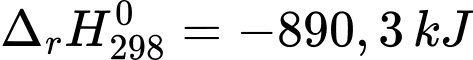
→ Ở điều kiện chuẩn, khi đốt cháy hoàn toàn 1 mol CH4, sản phẩm là CO2(g) và H2O(l) thì sẽ giải phóng một nhiệt lượng là 890,3 kJ.
Gọi số mol CH4 cần dùng ở phản ứng (2) để cung cấp năng lượng cho phản ứng (1) là a, ta có:
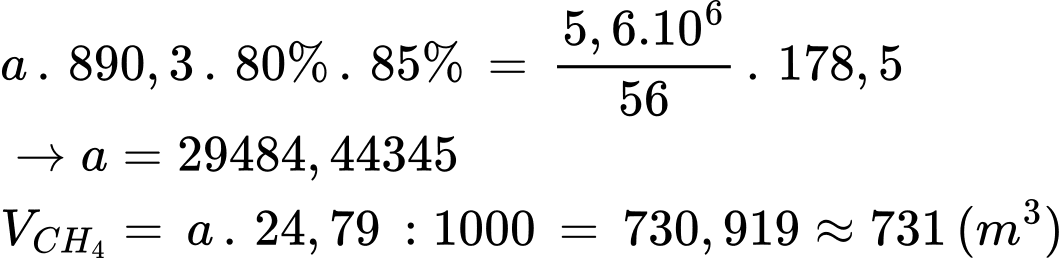
⇒ Điền đáp án: 731
Số mol của vôi sống tạo thành là
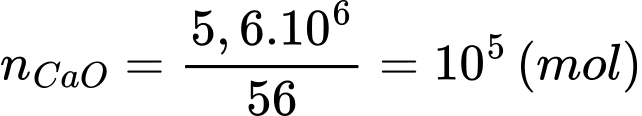
CaCO3(s)
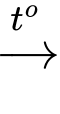 CaO(s) + CO2(g) (1)
CaO(s) + CO2(g) (1) 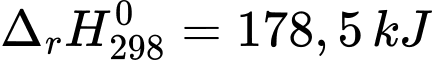
→ Để thu được 1 mol CaO(s), cần phải cung cấp nhiệt lượng là 178,5 kJ để chuyển 1 mol CaCO3(s) thành CaO (s).
CH4(g) + O2(g)
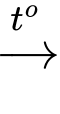 CO2(g) + H2O(l) (2)
CO2(g) + H2O(l) (2) 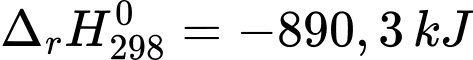
→ Ở điều kiện chuẩn, khi đốt cháy hoàn toàn 1 mol CH4, sản phẩm là CO2(g) và H2O(l) thì sẽ giải phóng một nhiệt lượng là 890,3 kJ.
Gọi số mol CH4 cần dùng ở phản ứng (2) để cung cấp năng lượng cho phản ứng (1) là a, ta có:
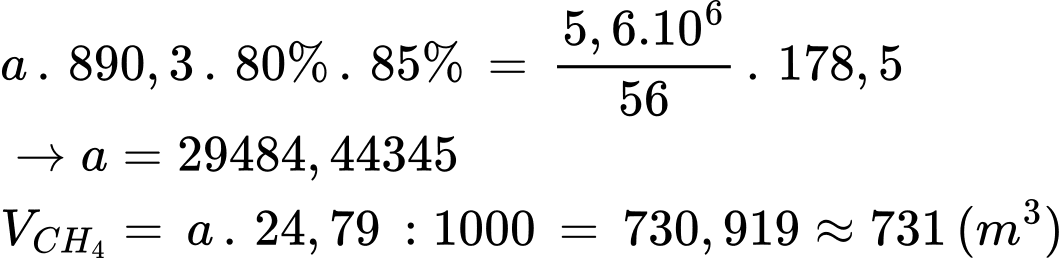
⇒ Điền đáp án: 731
Câu 28 [703024]: Trong quá trình chế biến sản phẩm đông lạnh xuất khẩu cần sử dụng chlorine trong qua trình sơ chế nguyên liệu và diệt vi sinh vật. Thị trường lớn như Mỹ và Châu Âu, được xem là thị trường khó tính, nên tiêu chuẩn chất lượng được kiểm soát chặt chẽ trước khi nhập nguyên liệu và sau khi thành phẩm, đóng gói. Trong danh mục tiêu chuẩn chất lượng sản phẩm có chỉ tiêu về dư lượng chlorine không vượt quá 1mg/l. Phương pháp chuẩn độ iodine – thiosulfate được dùng để xác định dư lượng chlorile trong thực phẩm theo phương trình:
Cl2 + 2KI 2KCl + I2.
2KCl + I2.
Sau đó, I2 được nhận biết bằng hồ tinh bột I2 bị khử bởi dung dịch chuẩn sodiumthiosulfate theo phương trình:
I2 + 2Na2S2O3 2NaI + Na2 S4O6.
2NaI + Na2 S4O6.
Dựa vào thể tích dung dịch Na2S2O3 phản ứng, tính được dư lượng chlorine trong dung dịch mẫu. Công ty A lấy 100 mL mẫu dung dịch tiến hành chuẩn độ bằng dung dịch Na2S2O3 0,01 M, thể tích Na2S2O3 dùng hết 0,42 mL ( dụng cụ chứa dung dịch chuẩn Na2S2O3 là loại microburette 1 mL, vạch chia 0,01 mL). Nồng độ chlorine (mg/L) có trong 1 lít dung dịch trên là bao nhiêu (làm tròn đến hàng phần trăm)?
Cl2 + 2KI
 2KCl + I2.
2KCl + I2.Sau đó, I2 được nhận biết bằng hồ tinh bột I2 bị khử bởi dung dịch chuẩn sodiumthiosulfate theo phương trình:
I2 + 2Na2S2O3
 2NaI + Na2 S4O6.
2NaI + Na2 S4O6.Dựa vào thể tích dung dịch Na2S2O3 phản ứng, tính được dư lượng chlorine trong dung dịch mẫu. Công ty A lấy 100 mL mẫu dung dịch tiến hành chuẩn độ bằng dung dịch Na2S2O3 0,01 M, thể tích Na2S2O3 dùng hết 0,42 mL ( dụng cụ chứa dung dịch chuẩn Na2S2O3 là loại microburette 1 mL, vạch chia 0,01 mL). Nồng độ chlorine (mg/L) có trong 1 lít dung dịch trên là bao nhiêu (làm tròn đến hàng phần trăm)?
Đổi 0,42 mL = 4,2.10-4 L
Cl2 + 2KI → 2KCl + I2 (1)
I2 + 2Na2S2O3 → 2NaI + Na2S4O6 (2)
Số mol của Na2S2O3 phản ứng là:
4,2.10-4 . 0,01 = 4,2.10-6 (mol)
Từ phương trình hóa học (1) và (2) số mol của Cl2 trong 100ml mẫu dung dịch là 2,1.10-6 (mol)
Khối lượng của Cl2 là: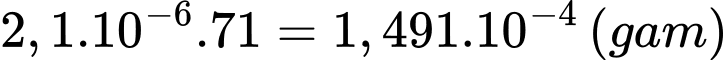
Nồng độ chlorine trong 1 L dung dịch là:
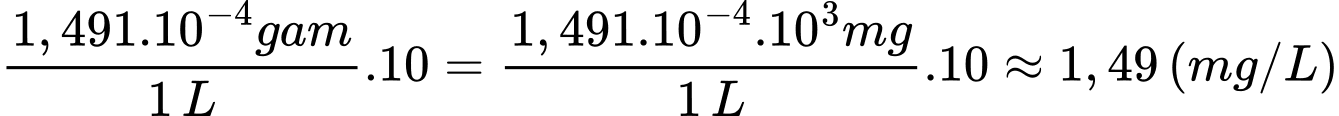
⇒ Điền đáp án: 1,49
Cl2 + 2KI → 2KCl + I2 (1)
I2 + 2Na2S2O3 → 2NaI + Na2S4O6 (2)
Số mol của Na2S2O3 phản ứng là:
4,2.10-4 . 0,01 = 4,2.10-6 (mol)
Từ phương trình hóa học (1) và (2) số mol của Cl2 trong 100ml mẫu dung dịch là 2,1.10-6 (mol)
Khối lượng của Cl2 là:
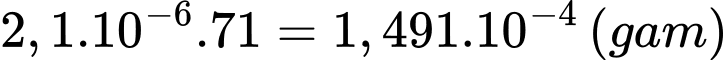
Nồng độ chlorine trong 1 L dung dịch là:
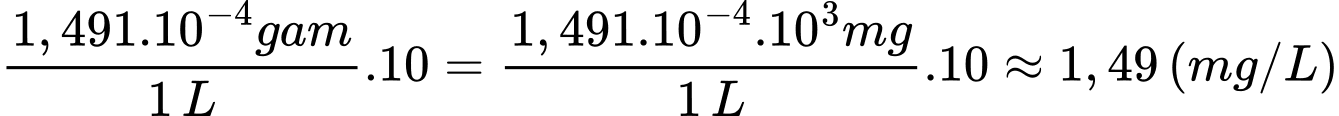
⇒ Điền đáp án: 1,49