Dạng 1: TRẮC NGHIỆM KHÁCH QUAN: mỗi câu hỏi chỉ có một đáp án đúng.
Câu 1 [560595]: Nhôm là kim loại phổ biến nhất trong vỏ Trái Đất và có trong thành phần của đất sét, khoáng vật criolit, quặng boxide. Trong bảng tuần hoàn, nhôm thuộc chu kì 3, nhóm IIIA. Cấu hình electron lớp ngoài cùng của nguyên tử nhôm ở trạng thái cơ bản là
A, 3s23p3.
B, 3s23p1.
C, 3s23p4.
D, 3s23p5.
Nhôm thuộc chu kì 3, nhóm IIIA => nhôm chứa 3 lớp e và có 3 electron lớp ngoài cùng => cấu hình lớp e ngoài cùng là 3s23p1. Đáp án: B
Câu 2 [560596]: Sắt là kim loại được con người sử dụng với khối lượng lớn nhất, chiếm trên 90% tổng khối lượng các kim loại. Dựa vào cấu hình electron của nguyên tử Fe (ở trạng thái cơ bản) là [Ar]3d64s2 thì nguyên tố này được xếp vào bảng tuần hoàn ở nhóm
A, VIB.
B, VIIIA.
C, VIIIB.
D, VIIB.
Cấu hình electron phân lớp ngoài cùng và sát lớp ngoài cùng của Fe là 3d64s2
=> Fe là nguyên tố nhóm B.
Tổng electron của 2 phân lớp (n-1)d và ns là 6 + 2 = 8
=> Fe được xếp vào nhóm VIIIB Đáp án: C
=> Fe là nguyên tố nhóm B.
Tổng electron của 2 phân lớp (n-1)d và ns là 6 + 2 = 8
=> Fe được xếp vào nhóm VIIIB Đáp án: C
Câu 3 [560597]: Một cấu trúc mạng tinh thể kim loại được thể hiện trong sơ đồ. Nội dung nào là phù hợp để điền vào vị trí của X, Y.
A, A: Cation kim loại, B: các ion tích điện âm.
B, A: proton tích điện dương, B: Anion phi kim.
C, A: Cation kim loại, B: Các electron tự do.
D, A: proton tích điện dương, B: Các electron tự do.
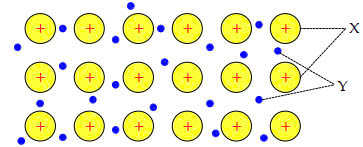
=> X là cation kim loại, Y là các electron tự do.
=> Chọn đáp án C
Câu 4 [560598]: Dãy gồm các kim loại có cùng kiểu mạng tinh thể lập phương tâm khối là
A, Na, K, Ba.
B, Mg, Ca, Ba.
C, Na, K , Ca.
D, Li , Na, Mg.
★ Mạng tinh thể lập phương tâm khối (Li, Na, K, Ba,...)
★ Mạng tinh thể lập phương tâm diện (Cu, Al, Ag, Ca...)
★ Mạng tinh thể lục phương (Be, Mg, Zn,...)
=> Chọn đáp án A
Đáp án: A
★ Mạng tinh thể lập phương tâm diện (Cu, Al, Ag, Ca...)
★ Mạng tinh thể lục phương (Be, Mg, Zn,...)
=> Chọn đáp án A
Đáp án: A
Câu 5 [560599]: Liên kết kim loại được hình thành bởi
A, Lực hút tĩnh điện giữa các nguyên tử.
B, Lực hút tĩnh điện giữa các hạt tích điện dương và các electron hóa trị tự do.
C, Lực hút tĩnh điện giữa các ion mang điện tích trái dấu.
D, Lực hút tĩnh điện giữa hạt nhân hai nguyên tử và cặp electron dùng chung.
Liên kết kim loại là liên kết hình thành từ lực hút tĩnh điện giữa các cation kim loại và các electron hóa trị tự do trong tinh thể kim loại. Đáp án: B
Câu 6 [560600]: Phát biểu nào sau đây về liên kết kim loại là đúng?
A, Liên kết kim loại là liên kết được hình thành từ lực hút tĩnh điện giữa các cation kim loại và các electron hoá trị tự do. Vì vậy, liên kết kim loại cũng chính là liên kết ion.
B, Liên kết kim loại được hình thành do giữa các nguyên tử kim loại có sự dùng chung các electron hoá trị tự do. Vì vậy, liên kết kim loại cũng chính là liên kết cộng hoá trị.
C, Liên kết kim loại là liên kết được hình thành từ lực hút tĩnh điện giữa các cation kim loại và các electron hoá trị tự do trong tinh thể kim loại.
D, Liên kết kim loại là liên kết được hình thành do sự xen phủ các orbital chứa electron hoá trị tự do của các nguyên tử kim loại.
Liên kết kim loại là liên kết hình thành từ lực hút tĩnh điện giữa các cation kim loại và các electron hóa trị tự do trong tinh thể kim loại. Đáp án: C
Câu 7 [560601]: Sự giống nhau giữa liên kết kim loại và liên kết ion là đều có
A, các cation kim loại.
B, các anion.
C, các electron.
D, tương tác tĩnh điện.
So sánh liên kết ion và liên kết kim loại:
★ Giống nhau: đều có tương tác tĩnh điện hình thành giữa điện tích âm và điện tích dương.
★ Khác nhau:
+ Liên kết ion: do lực hút tĩnh điện giữa hai ion mang điện tích trái dấu: anion(-) và phần dương do cation kim loại hoặc NH4+ tạo thành.
+ Liên kết kim loại: do các electron tự do trong kim loại và cation kim loại.
⇒ Chọn đáp án D Đáp án: D
★ Giống nhau: đều có tương tác tĩnh điện hình thành giữa điện tích âm và điện tích dương.
★ Khác nhau:
+ Liên kết ion: do lực hút tĩnh điện giữa hai ion mang điện tích trái dấu: anion(-) và phần dương do cation kim loại hoặc NH4+ tạo thành.
+ Liên kết kim loại: do các electron tự do trong kim loại và cation kim loại.
⇒ Chọn đáp án D Đáp án: D
Câu 8 [560602]: Tính chất vật lí nào sau của kim loại không do các electron tự do quyết định?
A, Tính dẫn điện.
B, Tính dẻo.
C, Khối lượng riêng.
D, Tính dẫn nhiệt.
Tính dẻo, dẫn nhiệt, dẫn điện và có ánh kim chủ yếu do các electron hóa trị tự do trong tinh thể kim loại gây ra.
⇒ Chọn đáp án C Đáp án: C
⇒ Chọn đáp án C Đáp án: C
Câu 9 [560603]: Kim loại dễ bị kéo dài, dát mỏng, dễ bị bẻ cong do có tính chất vật lí đặc trưng là
A, tính dẫn điện.
B, tính dẫn nhiệt.
C, tính dẻo.
D, có ánh kim.
Kim loại có tính chất vật lý đặc trưng là tính dẻo, cho phép chúng có thể kéo dài và dát mỏng, dễ bị bẻ cong.
Các tính chất còn lại:
A. Tính dẫn điện: Do sự di chuyển tự do của electron trong kim loại.
B. Tính dẫn nhiệt: Do sự truyền động năng qua mạng tinh thể và electron tự do.
D. Tính ánh kim: Do sự phản xạ ánh sáng trên bề mặt kim loại.
⇒ Chọn đáp án C Đáp án: C
Các tính chất còn lại:
A. Tính dẫn điện: Do sự di chuyển tự do của electron trong kim loại.
B. Tính dẫn nhiệt: Do sự truyền động năng qua mạng tinh thể và electron tự do.
D. Tính ánh kim: Do sự phản xạ ánh sáng trên bề mặt kim loại.
⇒ Chọn đáp án C Đáp án: C
Câu 10 [560604]: Kim loại nào dưới đây là dẻo nhất (thường được dùng để dát lên các công trình kiến trúc cổ)?
A, Ag.
B, Al.
C, Cu.
D, Au.
Vàng (Au) là kim loại dẻo nhất, có thể dát thành các lá cực mỏng (chỉ khoảng 0,0001 mm) và bền với các chất oxi hóa trong không khí. Vì vậy, vàng thường được dùng để mạ hoặc dát lên các công trình kiến trúc cổ, tượng, đồ trang trí,…
⇒ Chọn đáp án D Đáp án: D
⇒ Chọn đáp án D Đáp án: D
Câu 11 [560605]: Nhờ tính chất vật lí nào mà ta có thể uốn cong được kim loại?
A
Dây kim loại được uốn cong
A
Dây kim loại được uốn cong
A, Tính dẫn điện.
B, Tính dẻo.
C, Khối lượng riêng.
D, Tính dẫn nhiệt.
Kim loại có độ dẻo cao có thể chịu đựng sự biến dạng mà không bị gãy. Những kim loại như nhôm, đồng, và thép mềm có thể uốn cong khi áp dụng lực mà không bị vỡ.
=> Dựa vào tính dẻo ta có thể uốn cong được kim loại.
=> Chọn đáp án B Đáp án: B
=> Dựa vào tính dẻo ta có thể uốn cong được kim loại.
=> Chọn đáp án B Đáp án: B
Câu 12 [560606]: Hình dưới đây là mô tả tính chất vật lí nào của kim loại?
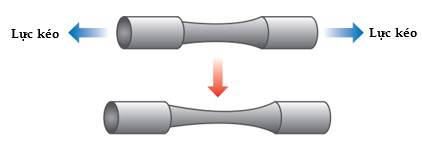

A, Tính dẫn điện.
B, Tính dẻo.
C, Khối lượng riêng.
D, Tính dẫn nhiệt.
- Kim loại có độ dẻo cao có thể chịu đựng sự biến dạng mà không bị gãy. Những kim loại như nhôm, đồng, và thép mềm có thể uốn cong khi áp dụng lực mà không bị vỡ.
- Khi một lực được áp dụng lên kim loại, cấu trúc mạng tinh thể của kim loại sẽ bị biến dạng. Nếu lực đủ lớn và kéo dài, kim loại sẽ uốn cong mà không vỡ.
⇒ Ứng dụng tính dẻo của kim loại.
⇒ Chọn đáp án B Đáp án: B
- Khi một lực được áp dụng lên kim loại, cấu trúc mạng tinh thể của kim loại sẽ bị biến dạng. Nếu lực đủ lớn và kéo dài, kim loại sẽ uốn cong mà không vỡ.
⇒ Ứng dụng tính dẻo của kim loại.
⇒ Chọn đáp án B Đáp án: B
Câu 13 [560607]: Kim loại nào sau đây dẫn điện tốt nhất?
A, Ag.
B, Al.
C, Cu.
D, Hg.
Ag dẫn điện tốt nhất, sau đó đến Cu, Au, Al, Fe,...
Bạc có độ dẫn điện cao nhất trong tất cả các kim loại, nhưng vì giá thành cao nên ít được sử dụng trong dây điện.
⇒ Chọn đáp án A Đáp án: A
Bạc có độ dẫn điện cao nhất trong tất cả các kim loại, nhưng vì giá thành cao nên ít được sử dụng trong dây điện.
⇒ Chọn đáp án A Đáp án: A
Câu 14 [560608]: Kim loại nào dẫn điện kém nhất trong số các kim loại dưới đây?
A, Al.
B, Ag.
C, Au.
D, Fe.
Ag dẫn điện tốt nhất, sau đó đến Cu, Au, Al, Fe,...
⇒ Trong 4 đáp án, kim loại dẫn nhiệt kém nhất là Fe.
⇒ Chọn đáp án D Đáp án: D
⇒ Trong 4 đáp án, kim loại dẫn nhiệt kém nhất là Fe.
⇒ Chọn đáp án D Đáp án: D
Câu 15 [560609]: Nhóm những kim loại có độ dẫn điện tốt nhất là
A, Ag, Cu, Au.
B, Cu, Al, Hg.
C, Li, Na, K.
D, Fe, Cu, Zn.
Ag dẫn điện tốt nhất, sau đó đến Cu, Au, Al, Fe,...
=> Đáp án A Đáp án: A
=> Đáp án A Đáp án: A
Câu 16 [560610]: Hình ảnh dưới đây là mô hình mô tả tính chất nào của kim loai?
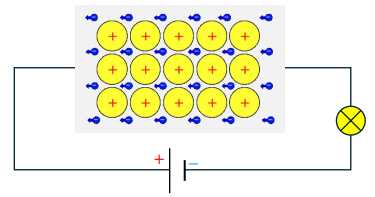

A, Tính dẫn điện.
B, Tính dẻo.
C, Khối lượng riêng.
D, Tính dẫn nhiệt.
Khi đặt một điện trường vào kim loại, các electron tự do sẽ di chuyển có hướng về phía cực dương.
Dòng electron dịch chuyển này tạo thành dòng điện trong kim loại.
Tính dẫn điện của kim loại là do sự có mặt của các electron tự do di chuyển trong mạng tinh thể. Khi có điện trường, các electron này di chuyển có hướng, tạo thành dòng điện.
Chọn đáp án A Đáp án: A
Dòng electron dịch chuyển này tạo thành dòng điện trong kim loại.
Tính dẫn điện của kim loại là do sự có mặt của các electron tự do di chuyển trong mạng tinh thể. Khi có điện trường, các electron này di chuyển có hướng, tạo thành dòng điện.
Chọn đáp án A Đáp án: A
Câu 17 [560611]: Các dụng cụ nấu nướng trong nhà bếp như nồi, xoong, chảo,... thường được chế tạo từ kim loại (hoặc hợp kim) do kim loại có tính chất vật lí đặc trưng là
A, tính dẫn điện.
B, tính dẻo.
C, tính dẫn nhiệt.
D, ánh kim.
Nhờ dẫn nhiệt tốt nên các kim loại (hoặc hợp kim) được dùng làm dụng cụ nhà bếp hoặc làm vật liệu tản nhiệt trong các thiết bị.
⇒ Chọn đáp án C Đáp án: C
⇒ Chọn đáp án C Đáp án: C
Câu 18 [560612]: Các kim loại có khả năng phản xạ hầu hết những tia sáng khả kiến, tạo nên vẻ sáng lấp lánh dưới ánh sáng Mặt Trời và được gọi là
A, tính dẫn điện.
B, ánh kim.
C, tính dẫn nhiệt.
D, tính dẻo.
Tính ánh kim là đặc điểm quan trọng giúp kim loại được sử dụng rộng rãi trong các lĩnh vực trang trí, sản xuất gương, chiếu sáng, và các ứng dụng cần phản xạ ánh sáng. Ví dụ, bạc và vàng là hai kim loại có ánh kim rất rõ rệt, trong khi nhôm cũng có khả năng phản xạ ánh sáng tốt, mặc dù không mạnh bằng bạc.
⇒ Chọn đáp án B Đáp án: B
⇒ Chọn đáp án B Đáp án: B
Câu 19 [560613]: Tính chất nào sau đây là tính chất vật lí chung của kim loại?
A, Tính dẫn điện.
B, Tính cứng.
C, Khối lượng riêng.
D, Nhiệt độ nóng chảy.
Kim loại có 4 tính chất vật lý chung: tính dẻo, dẫn nhiệt, dẫn điện và có ánh kim.
⇒ Chọn đáp án A Đáp án: A
⇒ Chọn đáp án A Đáp án: A
Câu 20 [560614]: Kim loại nào sau đây có khối lượng riêng lớn nhất?
A, Fe.
B, Ag.
C, Li.
D, Os
Fe: ~7.87 g/cm3
Ag: ~10.49 g/cm3
Li: ~0.53 g/cm3
Os: ~22.59 g/cm3
Khối lượng riêng lớn nhất: Osmium (Os)
⟹ Chọn đáp án D Đáp án: D
Ag: ~10.49 g/cm3
Li: ~0.53 g/cm3
Os: ~22.59 g/cm3
Khối lượng riêng lớn nhất: Osmium (Os)
⟹ Chọn đáp án D Đáp án: D
Câu 21 [560615]: Kim loại nào sau đây có khối lượng riêng nhỏ nhất?
A, Fe.
B, Al.
C, Li.
D, Mg.
Khối lượng riêng nhỏ nhất: Lithium (Li).
⇒ Chọn đáp án C Đáp án: C
⇒ Chọn đáp án C Đáp án: C
Câu 22 [560616]: Vì sao người ta thường buộc một mẩu chì vào dây của cần câu mà không phải một mẩu nhôm?
A, Chì có khối lượng riêng lớn nên dễ chìm xuống nước.
B, Chì có giá thành rẻ hơn nhôm.
C, Chì nhẹ hơn hơn nên có thể nổi trên mặt nước.
D, Chì có màu gần như trong suốt nên cá sẽ không phát hiện ra.
Vì chì là kim loại có khối lượng riêng lớn làm dây cần câu chìm sâu xuống nước. Trong khi đó, nhôm là kim loại nhẹ (có khối lượng riêng nhỏ) nên dây cần câu không chìm được sâu dưới nước.
⇒ Chọn đáp án A Đáp án: A
⇒ Chọn đáp án A Đáp án: A
Câu 23 [560617]: Đồng là kim loại dẫn điện tốt nhất trong các kim loại (chỉ xếp sau Ag), tuy nhiên các dây điện cao thế không được làm bằng đồng mà thường được làm bằng kim loại X. Kim loại X là
A, Fe.
B, Na.
C, Al.
D, Au.
Mặc dù khả năng dẫn điện thấp hơn Cu, tuy nhiên dây nhôm nhẹ hơn dây đồng tới hơn 3 lần nên dây điện cao thế được làm bằng nhôm để vận chuyển dễ dàng, tiết kiệm được nguyên liệu, giảm sức lực của dây điện cho các cột điện.
⟹ Chọn đáp án C Đáp án: C
⟹ Chọn đáp án C Đáp án: C
Câu 24 [560618]: Kim loại nào sau có nhiệt độ nóng chảy cao nhất trong tất cả các kim loại?
A, Vonfram.
B, Sắt.
C, Đồng.
D, Kẽm.
Do nhiệt độ nóng chảy cao, tungsten (volfram) được sử dụng làm dây tóc bóng đèn trong loại đèn sợi đốt.
⇒ Chọn đáp án A Đáp án: A
⇒ Chọn đáp án A Đáp án: A
Câu 25 [560619]: Kim loại nào sau đây có nhiệt độ nóng chảy thấp nhất?
A, Li.
B, Cu.
C, Ag.
D, Hg.
Thủy ngân (Hg) là kim loại có nhiệt độ nóng chảy thấp nhất.
⇒ Chọn đáp án D Đáp án: D
⇒ Chọn đáp án D Đáp án: D
Câu 26 [560620]: Ở điều kiện thường, kim loại nào sau đây ở trạng thái lỏng?
A, Hg.
B, Ag.
C, Cu.
D, Al.
Ở điều kiện thường, kim loại Hg (Mercury) tồn tại ở trạng thái lỏng.
⇒ Chọn đáp án A Đáp án: A
⇒ Chọn đáp án A Đáp án: A
Câu 27 [560621]: Wolfram được dùng để chế tạo dây tóc cho bóng đèn sợi đốt là do kim loại này có
A, độ cứng cao.
B, tính ánh kim.
C, khả năng dẫn điện tốt.
D, nhiệt độ nóng chảy cao.
Wolfram, còn gọi là Tungsten hoặc Vonfram, là một nguyên tố hóa học có ký hiệu là W. Trong tất cả kim loại nguyên chất, wolfram có điểm nóng chảy cao nhất (3422 oC), áp suất hơi thấp nhất, (ở nhiệt độ trên 1650 oC).
⇒ Chọn đáp án D Đáp án: D
⇒ Chọn đáp án D Đáp án: D
Câu 28 [560622]: Kim loại X được sử dụng trong nhiệt kế, áp kế và một số thiết bị khác. Ở điều kiện thường, X là chất lỏng. Kim loại X là
A, W.
B, Cr.
C, Hg.
D, Pb.
Ở điều kiện thường, kim loại duy nhất tồn tại ở thể lỏng là thủy ngân (mercury) kí hiệu là Hg. Thủy ngân được ứng dụng để chế tạo nhiệt kế.
Thủy ngân (mercury) thuộc ô số 80, chu kì 6, nhóm IIB trong bảng tuần hoàn.
⇒ Chọn đáp án C Đáp án: C
Thủy ngân (mercury) thuộc ô số 80, chu kì 6, nhóm IIB trong bảng tuần hoàn.
⇒ Chọn đáp án C Đáp án: C
Câu 29 [560623]: Trong cầu chì có một đoạn dây kim loại, thường là kim loại lead (chì) có tác dụng ngắt dòng điện khỏi thiết bị khi có sự cố gia tăng nhiệt. Ứng dụng trên dựa vào tính chất vật lí nào của kim loại lead?
A, Do lead có nhiệt độ nóng chảy thấp.
B, Do lead mềm, dẫn điện tốt.
C, Do lead có giá thành rẻ.
D, Do lead dẻo, dễ dát mỏng.
Nhờ có nhiệt độ nóng chảy thấp nên chì được sử dụng làm dây chảy trong cầu chì, khi hiện tượng đoản mạch xảy ra thì nhiệt độ tăng cao làm nóng chảy chì.
⇒ Chọn đáp án A Đáp án: A
⇒ Chọn đáp án A Đáp án: A
Câu 30 [560624]: X là kim loại cứng nhất, có thể cắt được thủy tinh. X là
A, Fe.
B, W.
C, Cu.
D, Cr.
Chromium (Cr) có độ cứng cao nhất trong các kim loại. Nó có thể cắt được thủy tinh, vì thủy tinh có độ cứng kém hơn.
Tính chất đặc biệt: Cr có độ bền cơ học cao, chống ăn mòn, thường được dùng để mạ cứng lên các dụng cụ.
Ứng dụng: Chế tạo thép không gỉ, dụng cụ cắt gọt, lớp phủ bảo vệ.
⇒ Chọn đáp án D Đáp án: D
Tính chất đặc biệt: Cr có độ bền cơ học cao, chống ăn mòn, thường được dùng để mạ cứng lên các dụng cụ.
Ứng dụng: Chế tạo thép không gỉ, dụng cụ cắt gọt, lớp phủ bảo vệ.
⇒ Chọn đáp án D Đáp án: D
Câu 31 [560625]: Cho dãy các kim loại: Na, Cu, Al, Cr. Kim loại mềm nhất trong dãy là
A, Na.
B, Cr.
C, Cu.
D, Al.
Sodium là một kim loại kiềm, có cấu trúc tinh thể đơn giản và chỉ có một electron tự do trong lớp vỏ ngoài cùng. Điều này làm cho liên kết giữa các nguyên tử trong Sodium khá yếu, làm cho kim loại này dễ bị biến dạng và có độ cứng thấp. Sodium có thể bị cắt bằng dao và bị uốn cong dễ dàng.
Các kim loại khác như Cu, Al và Cr cứng hơn do cấu trúc mạng tinh thể phức tạp hơn và liên kết giữa các nguyên tử mạnh mẽ hơn.
⟹ Chọn đáp án A Đáp án: A
Các kim loại khác như Cu, Al và Cr cứng hơn do cấu trúc mạng tinh thể phức tạp hơn và liên kết giữa các nguyên tử mạnh mẽ hơn.
⟹ Chọn đáp án A Đáp án: A
Câu 32 [560626]: Kim loại nào sau đây có độ cứng cao nhất trong các kim loại, thường được dùng chế tạo hợp kim không gỉ, có độ bền cơ học cao?
A, Chromium.
B, Nhôm.
C, Sắt.
D, Đồng.
Kim loại có độ cứng cao nhất trong các kim loại, thường được dùng để chế tạo hợp kim không gỉ và có độ bền cơ học cao là Chromium (Cr):
- Chromium có độ cứng rất cao, chỉ đứng sau kim cương.
- Chromium được dùng trong thép không gỉ: Khi thêm vào thép, Cr tạo lớp oxide bảo vệ giúp chống ăn mòn, làm cho hợp kim không gỉ.
- Chromium tăng độ bền cơ học của hợp kim: Được dùng trong các hợp kim như thép không gỉ, hợp kim chịu nhiệt, dụng cụ cắt gọt.
⇒ Chọn đáp án A Đáp án: A
- Chromium có độ cứng rất cao, chỉ đứng sau kim cương.
- Chromium được dùng trong thép không gỉ: Khi thêm vào thép, Cr tạo lớp oxide bảo vệ giúp chống ăn mòn, làm cho hợp kim không gỉ.
- Chromium tăng độ bền cơ học của hợp kim: Được dùng trong các hợp kim như thép không gỉ, hợp kim chịu nhiệt, dụng cụ cắt gọt.
⇒ Chọn đáp án A Đáp án: A
Câu 33 [560627]: Hình dưới đây thể hiện sự sắp xếp các ion trong kim loại copper.
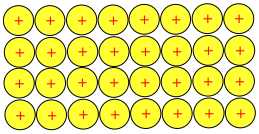
Nhận định nào dưới đây là đúng?

Nhận định nào dưới đây là đúng?
A, Copper có thể dẫn điện vì trong mạng tinh thể copper có chứa các cation kim loại.
B, Copper có nhiệt độ nóng chảy cao vì các ion kim loại hút nhau mạnh.
C, Copper dễ uốn vì các lớp ion có thể trượt lên nhau.
D, Copper dễ uốn vì liên kết kim loại giữa các lớp ion dễ bị phá vỡ.
❌ A. Sai. Kim loại dẫn điện nhờ các electron tự do di chuyển từ cực âm đến cực dương, tạo thành dòng điện.
❌ B. Sai. Các ion kim loại cùng dấu, không hút nhau.|
✔️ C. Đúng. Các lớp ion kim loại trong tinh thể có thể trượt lên nhau mà không tách rời nhờ lực hút tĩnh điện giữa cation và electron tự do => Tính dẻo của kim loại.
❌ D. Sai. Vì liên kết giữa các lớp ion không bị phá vỡ.
=> Đáp án C Đáp án: C
❌ B. Sai. Các ion kim loại cùng dấu, không hút nhau.|
✔️ C. Đúng. Các lớp ion kim loại trong tinh thể có thể trượt lên nhau mà không tách rời nhờ lực hút tĩnh điện giữa cation và electron tự do => Tính dẻo của kim loại.
❌ D. Sai. Vì liên kết giữa các lớp ion không bị phá vỡ.
=> Đáp án C Đáp án: C
Câu 34 [560628]: Cho các phát biểu sau:
(a) Nguyên tử của các nguyên tổ kim loại thường có từ 1 electron đến 3 electron ở lớp electron ngoài cùng.
(b) Tất cả các nguyên tố nhóm B đều là kim loại.
(c) Ở trạng thái rắn, đơn chất kim loại có cấu tạo tinh thể.
(d) Các kim loại đều có bán kính nguyên tử nhỏ hơn bán kính nguyên tử các phi kim thuộc cùng một chu kì.
(đ) Liên kết kim loại được hình thành do lực hút tĩnh điện giữa các electron tự do với các ion dương kim loại trong mạng tinh thể kim loại.
Các phát biểu đúng là
(a) Nguyên tử của các nguyên tổ kim loại thường có từ 1 electron đến 3 electron ở lớp electron ngoài cùng.
(b) Tất cả các nguyên tố nhóm B đều là kim loại.
(c) Ở trạng thái rắn, đơn chất kim loại có cấu tạo tinh thể.
(d) Các kim loại đều có bán kính nguyên tử nhỏ hơn bán kính nguyên tử các phi kim thuộc cùng một chu kì.
(đ) Liên kết kim loại được hình thành do lực hút tĩnh điện giữa các electron tự do với các ion dương kim loại trong mạng tinh thể kim loại.
Các phát biểu đúng là
A, (a), (b), (c), (đ).
B, (a), (b), (c).
C, (a), (b), (c), (d), (đ).
D, (a), (c), (đ).
✔️ (a) Đúng. Kim loại thường chứa 1, 2, 3 electron.
✔️ (b) Đúng. Tất cả các nguyên tố nhóm B đều là kim loại.
✔️ (c) Đúng. Ở trạng thái rắn, đơn chất kim loại có cấu tạo tinh thể.
❌ (d) Sai. Vì các kim loại có bán kính nguyên tử lớn hơn bán kính nguyên tử các phi kim thuộc cùng một chu kì.
✔️ (đ) Đúng. Liên kết kim loại được hình thành do lực hút tĩnh điện giữa các electron tự do với các ion dương kim loại trong mạng tinh thể kim loại.
=> Chọn A Đáp án: A
✔️ (b) Đúng. Tất cả các nguyên tố nhóm B đều là kim loại.
✔️ (c) Đúng. Ở trạng thái rắn, đơn chất kim loại có cấu tạo tinh thể.
❌ (d) Sai. Vì các kim loại có bán kính nguyên tử lớn hơn bán kính nguyên tử các phi kim thuộc cùng một chu kì.
✔️ (đ) Đúng. Liên kết kim loại được hình thành do lực hút tĩnh điện giữa các electron tự do với các ion dương kim loại trong mạng tinh thể kim loại.
=> Chọn A Đáp án: A
Dạng 2: TRẮC NGHIỆM ĐÚNG SAI – mỗi ý a), b), c), d) chọn đúng hoặc sai.
Câu 35 [560629]: Do số lượng electron hóa trị ít và bán kính nguyên tử lớn nên các electron
này dễ dàng tách ra khỏi các nguyên tử kim loại, hình thành nên tính khử của kim loại.
a. Kim loại có bán kính nguyên tử lớn hơn so với phi kim cùng chu kì.
b. Điện tích hạt nhân càng lớn thì tính khử của kim loại càng mạnh.
c. Kim loại thường có 1, 2 ,3 electron lớp ngoài cùng.
d. Trong cùng một nhóm, bán kính nguyên tử tăng dần theo chiều tăng
điện tích hạt nhân nên tính khử của kim loại tăng dần
này dễ dàng tách ra khỏi các nguyên tử kim loại, hình thành nên tính khử của kim loại.
a. Kim loại có bán kính nguyên tử lớn hơn so với phi kim cùng chu kì.
b. Điện tích hạt nhân càng lớn thì tính khử của kim loại càng mạnh.
c. Kim loại thường có 1, 2 ,3 electron lớp ngoài cùng.
d. Trong cùng một nhóm, bán kính nguyên tử tăng dần theo chiều tăng
điện tích hạt nhân nên tính khử của kim loại tăng dần
Phân tích các phát biểu sau:
✔️a. Đúng. Trong cùng một chu kì, kim loại thường nằm ở phía bên trái bảng tuần hoàn, có bán kính nguyên tử lớn hơn phi kim nằm ở bên phải do số proton và lực hút hạt nhân yếu hơn
❌ b. Sai. Điện tích hạt nhân lớn làm lực hút giữa hạt nhân và electron lớp ngoài cùng mạnh hơn, khiến electron khó bị tách ra, làm giảm tính khử. Tính khử mạnh hơn ở những nguyên tố có bán kính lớn và lực hút hạt nhân yếu (như ở các kim loại kiềm hoặc kiềm thổ).
✔️ c. Đúng. Kim loại thường có 1, 2, 3 electron lớp ngoài cùng.
✔️ d. Đúng. Trong cùng một nhóm, khi đi từ trên xuống, bán kính nguyên tử tăng, lực hút giữa hạt nhân và electron lớp ngoài cùng giảm, làm electron dễ bị mất hơn, tính khử tăng.
✔️a. Đúng. Trong cùng một chu kì, kim loại thường nằm ở phía bên trái bảng tuần hoàn, có bán kính nguyên tử lớn hơn phi kim nằm ở bên phải do số proton và lực hút hạt nhân yếu hơn
❌ b. Sai. Điện tích hạt nhân lớn làm lực hút giữa hạt nhân và electron lớp ngoài cùng mạnh hơn, khiến electron khó bị tách ra, làm giảm tính khử. Tính khử mạnh hơn ở những nguyên tố có bán kính lớn và lực hút hạt nhân yếu (như ở các kim loại kiềm hoặc kiềm thổ).
✔️ c. Đúng. Kim loại thường có 1, 2, 3 electron lớp ngoài cùng.
✔️ d. Đúng. Trong cùng một nhóm, khi đi từ trên xuống, bán kính nguyên tử tăng, lực hút giữa hạt nhân và electron lớp ngoài cùng giảm, làm electron dễ bị mất hơn, tính khử tăng.
Câu 36 [560630]: Mô hình mô tả khái quát cation kim loại và các electron hoá trị tự do trong tinh thể kim loại
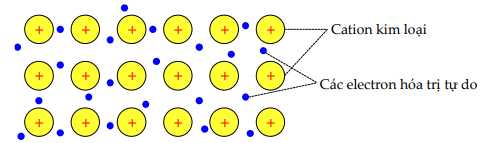
a. Tinh thể kim loại gồm các cation kim loại và electron hóa trị tự do.
b. Trong mạng tinh thể kim loại, các electron hóa trị tự do chuyển động theo một hướng nhất định.
c. Trong tinh thể kim loại, các cation kim loại được sắp xếp theo một trật tự nhất định.
d. Liên kết kim loại được hình thành bởi lực hút tương tự như liên kết cộng hóa trị.

a. Tinh thể kim loại gồm các cation kim loại và electron hóa trị tự do.
b. Trong mạng tinh thể kim loại, các electron hóa trị tự do chuyển động theo một hướng nhất định.
c. Trong tinh thể kim loại, các cation kim loại được sắp xếp theo một trật tự nhất định.
d. Liên kết kim loại được hình thành bởi lực hút tương tự như liên kết cộng hóa trị.
Phân tích các phát biểu sau:
✔️a. Đúng. Tinh thể kim loại gồm các cation kim loại và electron hóa trị tự do.
❌ b. Sai. Các electron chuyển động tự do trong tinh thể kim loại từ nguyên tử kim loại này đến nguyên tử kim loại khác, không theo một hướng nhất định.
✔️ c. Đúng. Các cation kim loại được sắp xếp theo một trật tự nhất định.
❌ d. Sai. Liên kết kim loại tạo thành từ lực hút tĩnh điện. Liên kết cộng hóa trị được hình thành tự sự dùng chung electron giữa 2 nguyên tử tham gia liên kết.
✔️a. Đúng. Tinh thể kim loại gồm các cation kim loại và electron hóa trị tự do.
❌ b. Sai. Các electron chuyển động tự do trong tinh thể kim loại từ nguyên tử kim loại này đến nguyên tử kim loại khác, không theo một hướng nhất định.
✔️ c. Đúng. Các cation kim loại được sắp xếp theo một trật tự nhất định.
❌ d. Sai. Liên kết kim loại tạo thành từ lực hút tĩnh điện. Liên kết cộng hóa trị được hình thành tự sự dùng chung electron giữa 2 nguyên tử tham gia liên kết.
Câu 37 [560631]: Ở điều kiện thường, trừ thủy ngân ở thể lỏng, các kim loại khác đều tồn tại ở thể rắn và có cấu tạo tinh thể được thể hiện dưới dạng mô hình khái quát như hình dưới đây.
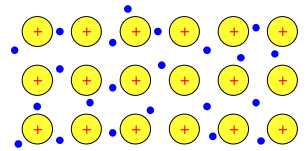
a. Trong tinh thể kim loại M có các cation Mn+
và các electron hoá trị tự do.
b. Các cation Mn+
chuyền động tự do trong mạng tinh thể kim loại.
c. Lực hút giữa cation Mn+
và electron hoá trị tự do trong tinh thể kim loại
M phụ thuộc vào độ âm điện của kim loại M.
d. Trong tinh thể kim loại M, các cation Mn+
và electron hoá trị tự do được
phân bố theo trật tự nhất định.

a. Trong tinh thể kim loại M có các cation Mn+
và các electron hoá trị tự do.
b. Các cation Mn+
chuyền động tự do trong mạng tinh thể kim loại.
c. Lực hút giữa cation Mn+
và electron hoá trị tự do trong tinh thể kim loại
M phụ thuộc vào độ âm điện của kim loại M.
d. Trong tinh thể kim loại M, các cation Mn+
và electron hoá trị tự do được
phân bố theo trật tự nhất định.
Phân tích các phát biểu sau:
✔️a. Đúng. Trong tinh thể kim loại M có các cation Mn+ và các electron hóa trị tự do.
❌ b. Sai. Các cation Mn+ được sắp xếp theo trật tự nhất định.
❌ c. Sai. Lực hút giữa Mn+ và electron hóa trị tự do trong liên kết kim loại không phụ thuộc vào độ âm điện, mà chủ yếu dựa vào bán kính cation, điện tích ion, và mật độ electron tự do.
❌ d. Sai. Trong tinh thể kim loại M, các cation Mn+ phân bố theo trật tự nhất định cùng với electron chuyển động tự do.
✔️a. Đúng. Trong tinh thể kim loại M có các cation Mn+ và các electron hóa trị tự do.
❌ b. Sai. Các cation Mn+ được sắp xếp theo trật tự nhất định.
❌ c. Sai. Lực hút giữa Mn+ và electron hóa trị tự do trong liên kết kim loại không phụ thuộc vào độ âm điện, mà chủ yếu dựa vào bán kính cation, điện tích ion, và mật độ electron tự do.
❌ d. Sai. Trong tinh thể kim loại M, các cation Mn+ phân bố theo trật tự nhất định cùng với electron chuyển động tự do.
Câu 38 [560632]: Các kim loại ở trạng thái rắn đều có tính dẻo, dẫn điện, dẫn nhiệt và có ánh kim. Hình ảnh dưới đây minh họa quá trình trượt của các ion kim loại khi bị tác động bởi lực
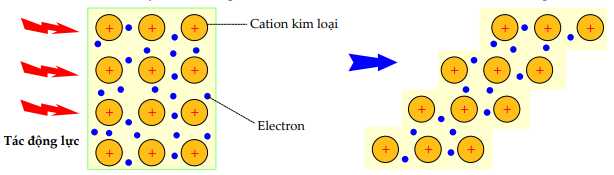
a. Các tính chất vật lí của kim loại chủ yếu do các electron hóa trị tự do trong tinh thể kim loại gây ra.
b. Hình ảnh trên minh họa và giải thích vì sao kim loại có khả năng dẫn điện.
c. Các cation kim loại trong tinh thể kim loại có thể trượt lên nhau mà không tách rời nhờ lực hút tĩnh điện giữa chúng với các electron hoá trị tự do.
d. Do các cation kim loại có thể trượt lên nhau khi có lực tác động nên một số kim loại được ứng dụng làm đồ trang sức với nhiều hình dáng khác nhau.

a. Các tính chất vật lí của kim loại chủ yếu do các electron hóa trị tự do trong tinh thể kim loại gây ra.
b. Hình ảnh trên minh họa và giải thích vì sao kim loại có khả năng dẫn điện.
c. Các cation kim loại trong tinh thể kim loại có thể trượt lên nhau mà không tách rời nhờ lực hút tĩnh điện giữa chúng với các electron hoá trị tự do.
d. Do các cation kim loại có thể trượt lên nhau khi có lực tác động nên một số kim loại được ứng dụng làm đồ trang sức với nhiều hình dáng khác nhau.
Phân tích các phát biểu sau:
✔️a. Đúng. Các tính chất vật lí của kim loại chủ yếu do các electron hóa trị tự do trong tinh thể kim loại gây ra.
❌ b. Sai. Hình ảnh minh họa và giải thích cho tính dẻo của kim loại.
✔️ c. Đúng. Nhờ lực hút tĩnh điện giữa cation và electron tự do trong tinh thể kim loại mà cation kim loại có thể trượt lên nhau, không tách rời tạo nên tính dẻo của kim loại.
✔️ d. Đúng. Do các cation kim loại có thể trượt lên nhau khi có lực tác động nên một số kim loại được ứng dụng làm đồ trang sức với nhiều hình dáng khác nhau.
✔️a. Đúng. Các tính chất vật lí của kim loại chủ yếu do các electron hóa trị tự do trong tinh thể kim loại gây ra.
❌ b. Sai. Hình ảnh minh họa và giải thích cho tính dẻo của kim loại.
✔️ c. Đúng. Nhờ lực hút tĩnh điện giữa cation và electron tự do trong tinh thể kim loại mà cation kim loại có thể trượt lên nhau, không tách rời tạo nên tính dẻo của kim loại.
✔️ d. Đúng. Do các cation kim loại có thể trượt lên nhau khi có lực tác động nên một số kim loại được ứng dụng làm đồ trang sức với nhiều hình dáng khác nhau.
Câu 39 [560633]: Nhiều ứng dụng của kim loại được dựa trên tính chất vật lí của kim loại. Hình dưới đây cho thấy một số ứng dụng quen thuộc của kim loại trong đời sống

a. Vàng có thể kéo thành sợi chỉ dùng để khâu trang trí do vàng là kim loại rất dẻo.
b. Giấy aluminium được dùng trong chế biến thực phẩm là dựa trên cơ sở tính dẫn nhiệt của kim loại.
c. Aluminium được sử dụng làm dây dẫn điện cao thế mà không dùng đồng do có khối lượng riêng lớn hơn đồng.
d. Tính dẻo, tính dẫn nhiệt, dẫn điện của kim loại chủ yếu do các cation trong mạng tinh thể của kim loại gây ra.

a. Vàng có thể kéo thành sợi chỉ dùng để khâu trang trí do vàng là kim loại rất dẻo.
b. Giấy aluminium được dùng trong chế biến thực phẩm là dựa trên cơ sở tính dẫn nhiệt của kim loại.
c. Aluminium được sử dụng làm dây dẫn điện cao thế mà không dùng đồng do có khối lượng riêng lớn hơn đồng.
d. Tính dẻo, tính dẫn nhiệt, dẫn điện của kim loại chủ yếu do các cation trong mạng tinh thể của kim loại gây ra.
Phân tích các phát biểu sau:
✔️ a. Đúng. Vàng có thể kéo thành sợi chỉ dùng để khâu trang trí do vàng là kim loại rất dẻo.
✔️ b. Đúng. Giấy aluminium được dùng trong chế biến thực phẩm dựa trên tính dẫn nhiệt của kim loại.
❌ c. Sai. Aluminium có khối lượng riêng nhỏ hơn đồng.
❌ d. Sai. Tính dẻo, dẫn nhiệt, dẫn điện cảu kim loại chủ yếu do các electron tự do trong mạng tinh thể của kim loại gây ra.
✔️ a. Đúng. Vàng có thể kéo thành sợi chỉ dùng để khâu trang trí do vàng là kim loại rất dẻo.
✔️ b. Đúng. Giấy aluminium được dùng trong chế biến thực phẩm dựa trên tính dẫn nhiệt của kim loại.
❌ c. Sai. Aluminium có khối lượng riêng nhỏ hơn đồng.
❌ d. Sai. Tính dẻo, dẫn nhiệt, dẫn điện cảu kim loại chủ yếu do các electron tự do trong mạng tinh thể của kim loại gây ra.
Dạng 3: TRẮC NGHIỆM YÊU CẦU TRẢ LỜI NGẮN
Câu 40 [560634]: Cấu hình electron nguyên tử nguyên tố X là 1s22s22p63s23p1. Số hiệu nguyên tử của X là
Điền đáp án: ..........
Điền đáp án: ..........
Số hiệu nguyên tử của X là 2 + 2 + 6 + 2 + 1 = 13
=> Điền đáp án: 13
=> Điền đáp án: 13
Câu 41 [560635]: Trong số các kim loại sau đây: Na, K, Mg, Al, Fe, Ca, Hg, Cu, Au. Số kim loại tồn tại ở thể rắn tại nhiệt độ phòng là
Điền đáp án: ..........
Điền đáp án: ..........
Ngoại trừ Hg ra thì các kim loại Na, K, Mg, Al, Fe, Ca, Cu, Au đều tồn tại ở thể rắn ở nhiệt độ phòng.
=> Điền đáp án: 8
=> Điền đáp án: 8
Câu 42 [560636]: Độ dẫn điện của các kim loại bạc, đồng, vàng, nhôm và sắt được cho trong bảng sau:

Độ dẫn điện của kim loại đồng ứng với kí hiệu số mấy?
Điền đáp án: ..........

Độ dẫn điện của kim loại đồng ứng với kí hiệu số mấy?
Điền đáp án: ..........
- Thứ tự giảm dần tính dẫn điện của các kim loại bạc, đồng, vàng, nhôm và sắt là:
=> Điền đáp án: 2
Ag < Cu < Au < Al < Fe => Cu có độ dẫn điện xếp thứ 2 (sau Ag).
- Dựa vào dữ kiện ở bảng thì độ dẫn điện của kim loại Cu ứng với kí hiệu số (2).=> Điền đáp án: 2
Câu 43 [560637]: Một miếng kim loại bạc (Ag) nặng 194,3 gam được đặt vào một ống đong chia độ chứa 242,0 ml nước. Thể tích nước bây giờ là 260,5 mL. Từ những dữ liệu này, khối lượng riêng của của bạc là bao nhiêu (g/cm3)? (làm tròn đến hai chữ số thập phân)
Điền đáp án: ..........
Điền đáp án: ..........
Thể tích tăng lên chính là thể tích của miếng kim loại bạc (Ag)
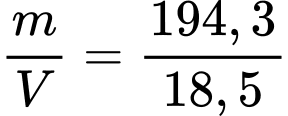 = 10,5 (g/cm3)
= 10,5 (g/cm3)
=> Điền đáp án: 10,5
VAg= 260,5 - 242,0 = 18,5 mL = 18,5 cm3
=> dAg = 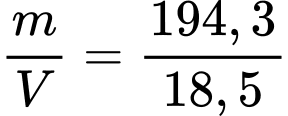 = 10,5 (g/cm3)
= 10,5 (g/cm3)=> Điền đáp án: 10,5
Câu 44 [560638]: Một miếng kim loại có khối lượng 13,2 gam được thả vào một ống đong có chia độ chứa 17,00 mL nước. Thể tích ống đong chia độ sau khi thêm kim loại được hiển thị như hình bên. Xác định khối lượng riêng của miếng kim loại. (làm tròn đến hai chữ số thập phân)

Điền đáp án: ..........

Điền đáp án: ..........
Theo hình, thể tích ống đong sau khi thêm kim loại là 18,45 mL
=> Thể tích của miếng kim loại thêm vào bằng 18,45 - 17 = 1,45 mL
=> Khối lượng riêng của miếng kim loại (g/cm3):
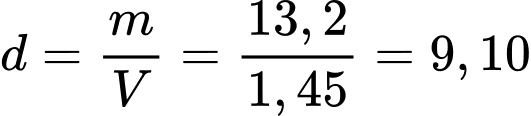
=> Thể tích của miếng kim loại thêm vào bằng 18,45 - 17 = 1,45 mL
=> Khối lượng riêng của miếng kim loại (g/cm3):
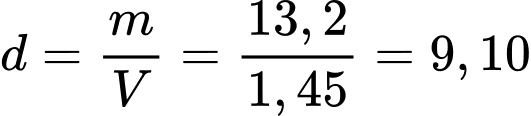
Dạng 4: BÀI TẬP ĐỌC HIỂU – đọc thông tin và trả lời các câu hỏi sau đó
CẤU TRÚC TINH THỂ LẬP PHƯƠNG
Cấu trúc tinh thể của kim loại có thể được hình dung đơn giản hơn theo cách sau. Đầu tiên chúng ta sẽ có một ô mạng cơ sở là một hình lập phương, xung quanh hình ô mạng này sẽ còn rất nhiều các ô mạng khác nằm xung quanh. Tuy nhiên để khi nhìn đỡ bị rối thì thường sẽ chỉ biểu thị một ô mạng cơ sở.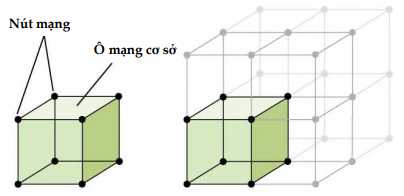
Khi này, các nguyên tử kim loại sẽ được đưa vào các điểm mạng (các đỉnh của hình lập phương). Chúng ta có 8 đỉnh nên sẽ có 8 nguyên tử kim loại tồn tại trên đó.
♦ Cấu trúc này gọi là cấu trúc tinh thể lập phương đơn giản (a).
Nếu chúng ta thêm một nguyên tử kim loại nữa vào chính giữa, trung tâm của cấu trúc (a) thì chúng ta sẽ thu được cấu trúc tinh thể lập phương tâm khối. “Tâm khối” có thể hiểu là có một nguyên tử ở trung tâm của khối lập phương.
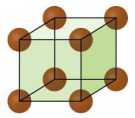
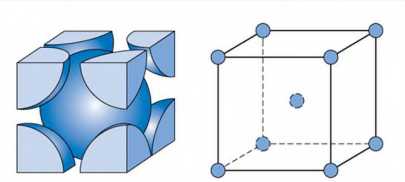
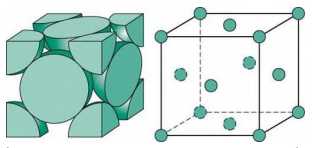
Mặt khác, một khối lập phương sẽ có 6 mặt, nếu chúng ta thêm 6 nguyên tử kim loại vào tâm của 6 mặt trong cấu trúc (a) thì chúng ta sẽ thu được cấu trúc tinh thể lập phương tâm diện. “Diện” có nghĩa là mặt, “tâm diện” có thể hiểu là có một nguyên tử ở trung tâm của mỗi mặt khối lập phương.
Tuy nhiên có một sự nhầm tưởng đáng tai hại mà chúng ta thường mắc phải là
• Cấu trúc tinh thể lập phương đơn giản chứa 4 nguyên tử.
• Cấu trúc tinh thể lập phương tâm khối chứa 5 nguyên tử.
• Cấu trúc tinh thể lập phương tâm diện chứa 10 nguyên tử.
Điều này là hoàn toàn sai lầm vì khi quan sát kĩ, chỉ có một phần của nguyên tử tồn tại trong ô mạng chứ không phải nguyên tử nằm trọn vẹn trong đó.
• Đối với các nguyên tử ở đỉnh của hình lập phương thì chỉ có 1/8 nguyên tử tồn tại trong một ô mạng, phần còn lại của nguyên tử sẽ thuộc ô mạng khác.
• Đối với nguyên tử ở trung tâm hình lập phương thì nguyên tử này sẽ nằm trọn vẹn trong ô mạng.
• Đối với nguyên tử ở tâm các mặt thì chỉ có 1/2 nguyên tử tồn tại trong ô mạng.
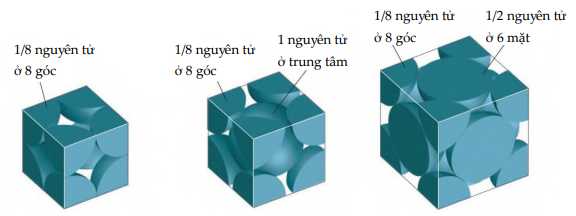
Từ đây ta có thể tính chính xác số nguyên tử trong các cấu trúc tinh thể.
Cấu trúc lập phương đơn giản chứa 1 nguyên tử vì
⇝ 8 (nguyên tử ở đỉnh) × 1/8 = 1 (nguyên tử).
Cấu trúc lập phương tâm khối chứa 2 nguyên tử vì
⇝ 8 (nguyên tử ở đỉnh) × 1/8 + 1 (nguyên tử tâm khối) = 2 (nguyên tử).
Câu 45 [560639]: Các nguyên tử ở đỉnh chỉ đóng góp vào ô mạng bao nhiêu phần trăm của một nguyên tử?
A, 25,0 %.
B, 12,5 %.
C, 50,0 %.
D, 60,5 %.
Các nguyên tử ở đỉnh đóng góp 1/8 nguyên tử trong ô mạng
⇒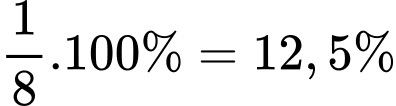
⇒ Chọn đáp án B
⇒
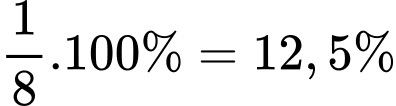
⇒ Chọn đáp án B
Câu 46 [560640]: Dựa vào bài đọc, xác định số nguyên tử tồn tại thực tế trong một cấu trúc tinh thể lập phương tâm diện?
A, 1 nguyên tử.
B, 2 nguyên tử.
C, 3 nguyên tử.
D, 4 nguyên tử.
Cấu trúc lập phương tâm diện:
+ Đối với các nguyên tử ở đỉnh của hình lập phương thì chỉ có 1/8 nguyên tử tồn tại trong ô mạng ⇒ Với 8 đỉnh thì sẽ có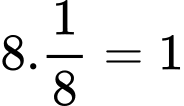 nguyên tử.
nguyên tử.
+ Đối với nguyên tử ở mặt của hình lập phương chỉ có 1/2 nguyên tử trong ô mạng ⇒ với 6 mặt thì sẽ có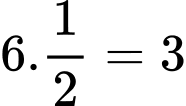 nguyên tử.
nguyên tử.
⇒ Số nguyên tử tồn tại trong cấu trúc lập phương tâm diện là 1+ 3= 4 nguyên tử.
⇒ Chọn đáp án D
+ Đối với các nguyên tử ở đỉnh của hình lập phương thì chỉ có 1/8 nguyên tử tồn tại trong ô mạng ⇒ Với 8 đỉnh thì sẽ có
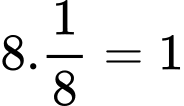 nguyên tử.
nguyên tử.+ Đối với nguyên tử ở mặt của hình lập phương chỉ có 1/2 nguyên tử trong ô mạng ⇒ với 6 mặt thì sẽ có
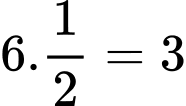 nguyên tử.
nguyên tử.⇒ Số nguyên tử tồn tại trong cấu trúc lập phương tâm diện là 1+ 3= 4 nguyên tử.
⇒ Chọn đáp án D
Câu 47 [560641]: Trong cấu trúc ô mạng cơ sở của một loại chất X được kết hợp bởi hai nguyên tố là Ni và Al, chúng ta có 8 nguyên tử Al ở 8 đỉnh và 6 nguyên tử Ni ở tâm các mặt.
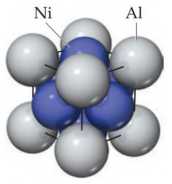
Xác định công thức phân tử của chất X.

Xác định công thức phân tử của chất X.
A, Ni6Al8.
B, Ni4Al3.
C, Ni3Al.
D, Ni3Al4.
Trong thực tế:
+ Mỗi nguyên tử Al ở đỉnh chỉ đóng góp 1/8 nguyên tử vào cấu trúc ô mạng ⇒ trong một ô mạng cơ sở có chứa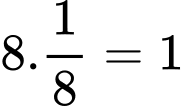 nguyên tử Al.
nguyên tử Al.
+ Mỗi nguyên tử Ni ở tâm mặt chỉ đóng góp 1/2 nguyên tử vào cấu trúc ô mạng ⇒ trong một ô mạng cơ sở có chứa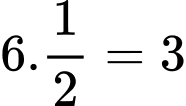 nguyên tử Ni.
nguyên tử Ni.
⇒ Công thức phân tử của X là Ni3Al.
⇒ Chọn đáp án C Đáp án: C
+ Mỗi nguyên tử Al ở đỉnh chỉ đóng góp 1/8 nguyên tử vào cấu trúc ô mạng ⇒ trong một ô mạng cơ sở có chứa
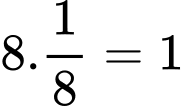 nguyên tử Al.
nguyên tử Al.+ Mỗi nguyên tử Ni ở tâm mặt chỉ đóng góp 1/2 nguyên tử vào cấu trúc ô mạng ⇒ trong một ô mạng cơ sở có chứa
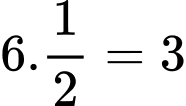 nguyên tử Ni.
nguyên tử Ni.⇒ Công thức phân tử của X là Ni3Al.
⇒ Chọn đáp án C Đáp án: C
Dựa vào các thông tin được cung cấp dưới đây để trả lời các câu hỏi từ 48 đến 50
BÁN KÍNH NGUYÊN TỬ VÀ ION KIM LOẠI
Theo trực giác, chúng ta thường nghĩ bán kính nguyên tử (R) là khoảng cách giữa hạt nhân của một nguyên tử với lớp vỏ electron hóa trị của nó (tức là lớp vỏ ngoài cùng bị chiếm giữ bởi một hoặc nhiều electron), điều này cũng dễ hiểu bởi vì chúng ta thường hình dung các nguyên tử giống như những quả cầu có ranh giới rời rạc.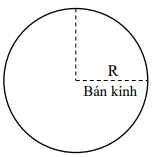
Tuy nhiên, theo mô hình cơ học lượng tử của nguyên tử, không có khoảng cách cụ thể nào từ hạt nhân mà ngoài đó không thể tìm thấy electron. Do đó, bán kính nguyên tử đòi hỏi phải có một định nghĩa cụ thể.
Có hai cách xác định bán kính nguyên tử. Một là bán kính kim loại, bằng một nửa khoảng cách giữa hạt nhân của hai nguyên tử kim loại giống hệt nhau và liền kề với nhau hình 1. Cái còn lại là bán kính cộng hóa trị, bằng một nửa khoảng cách giữa các hạt nhân giống hệt nhau, liền kề nhau trong một phân tử hình 2.
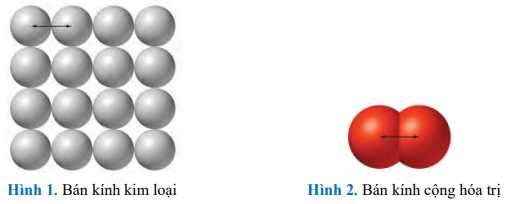
Hình 3 cho thấy bán kính nguyên tử của các nguyên tố nhóm chính theo vị trí của chúng trong bảng tuần hoàn. Có hai xu hướng biến đổi riêng biệt: Xu hướng biến đổi theo chu kì và xu hướng biến đổi theo nhóm.
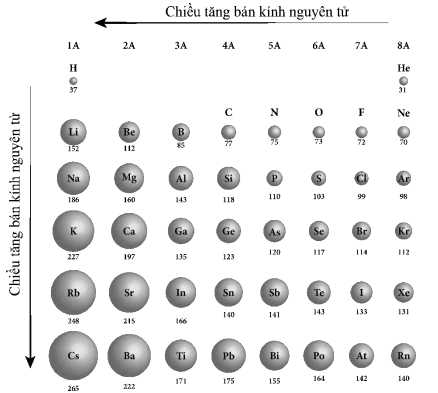
Hình 3. Xu hướng biến đổi bán kính nguyên tử của các nguyên tố nhóm chính
Câu 48 [560642]: Một nửa khoảng cách giữa các hạt nhân giống hệt nhau, liền kề nhau trong một phân tử gọi là
A, bán kính phân tử.
B, bán kính kim loại.
C, đường kính nguyên tử.
D, bán kính cộng hóa trị.
Bán kính cộng hóa trị bằng một nửa khoảng cách giữa các hạt nhân giống hệt nhau, liền kề nhau trong một phân tử.
=> Chọn D Đáp án: D
=> Chọn D Đáp án: D
Câu 49 [560643]: Dựa vào kích thước hình bên và sử dụng thông tin trong hình 3, hãy cho biết các nguyên tử của các nguyên tố: Al, B, Mg và Sr tương ứng với quả cầu nào?


A, Quả cầu (iv) là Mg.
B, Quả cầu (i) là Al.
C, Quả cầu (iii) là Mg.
D, Quả cầu (ii) là B.
Dựa vào hình 3, các nguyên tử được sắp xếp theo chiều tăng dần bán kính nguyên tử như sau:
B < Al < Mg < Sr
Đáp án: C => Quả cầu (i) là B; (ii) là Al; (iii) là Mg và (iv) là Sr
=> Chọn C
=> Chọn C
Câu 50 [560644]: Các ion O2–, F–, Na+, Mg2+ đều có cấu hình là [He]2s22p6. Dãy sắp xếp theo chiều giảm dần bán kính của các ion là
A, O2– > F– > Na+ > Mg2+.
B, Na+ > Mg2+ > O2– > F–.
C, Mg2+ > Na+ > F– > O2–.
D, O2– > F– > Mg2+ > Na+.
Khi số proton tăng lên mà số electron không đổi, lực hút hạt nhân tác dụng lên các electron sẽ lớn hơn, kéo các electron lại gần hạt nhân hơn, làm giảm bán kính ion.
=> Dãy ion sắp xếp theo chiều giảm dần bán kính là:
=> Dãy ion sắp xếp theo chiều giảm dần bán kính là:
O2– > F– > Na+ > Mg2+
Đáp án: A => Chọn đáp án A.