PHẦN I. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
- Calcium có 20e → Số hiệu nguyên tử là 20 → Ô thứ 20 trong bảng tuần hoàn.
- Calcium có 4 lớp 4 → Thuộc chu kì 4.
- Calcium thuộc nguyên tố s, có 2 electron lớp ngoài cùng → Thuộc nhóm IIA
⇒ Chọn đáp án A Đáp án: A
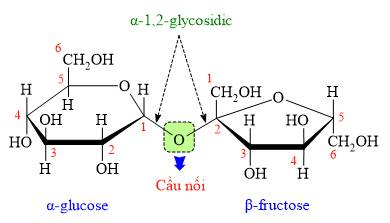
⇒ Trả lời: gốc glucose liên kết với gốc fructose qua nguyên tử đóng vai trò cầu nối là oxygen (O)
⇝ Chọn đáp án C Đáp án: C
- Nylon là một loại polyamide (giống như protein), cũng không bền với acid mạnh và kiềm mạnh.
Phân tích các phát biểu:
✔️A. Len, nylon và tơ tằm đều có cấu trúc là polyamide, dễ bị hư hỏng bởi nhiệt, acid và kiềm mạnh.
❌B. Các chất liệu này không tan trong nước khi gặp xà phòng kiềm, mà chỉ bị hư hỏng.
❌C. Các chất liệu này chịu tác động mạnh của xà phòng có tính kiềm, không phải là "không chịu tác động".
❌D. Xà phòng trung tính không làm tăng khả năng hút nước mà chủ yếu giúp bảo vệ sợi vải
⟹Chọn đáp án A Đáp án: A
Fe2+(aq) + 2e ⇌ Fe(s) Eo = –0,44 V
Cu2+(aq) + 2e ⇌ Cu(s) Eo = +0,34 V
Giá trị suất điện động của pin Fe-Cu là
Trong pin Fe - Cu, điện cực Fe đóng vai trò là Anode và Cu đóng vai trò là cathode
Anode (-) : Fe → Fe2+ + 2e
Cathode (+) : Cu2+ + 2e → Cu
→ EPin = E(+) – E(-) = 0,34 – (-0,44) = 0,78 V
⟹Chọn đáp án B Đáp án: B
Các phần tử đó là
❌A. Sai. vì không phải tất cả cation kim loại đều có khả năng tạo phức chất. Ví dụ Na+, K+, Ca2+ rất ít khi tạo phức mạnh do chúng không có orbital d trống để tiếp nhận electron từ phối tử.
✔️B. Đúng . Phần tử có thể trở thành nguyên tử trung tâm trong phức chất khi chúng sử dụng các orbital trống để nhận cặp electron hoá trị riêng từ phối tử là nguyên tử hoặc cation kim loại.
❌C. Sai. Không phải tất cả nguyên tử nguyên tố chuyển tiếp đều tham gia tạo phức. Ví dụ: Fe, Cu, Zn ở trạng thái trung hòa không tạo phức mạnh, nhưng cation của chúng thì có thể.
❌D. Đúng. Các cation kim loại chuyển tiếp (Fe2+, Cu2+, Zn2+...) có obital d trống, giúp chúng nhận cặp electron từ phối tử để tạo phức. Ngoài ra có các nguyên tử kim loại.
⟹ Chọn đáp án B Đáp án: B
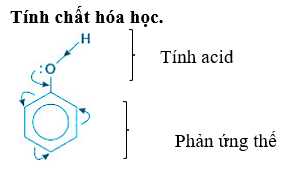
Tính acid của phenol: Phenol thể hiện tính acid yếu. Dung dịch phenol không làm đổi màu quỳ tím.
→ Nên có khả năng tác dụng với Na và NaOH.
Các hợp chất vừa tác dụng với Na, vừa tác dụng với NaOH là C6H5OH, HOC6H4OH, CH3C6H4OH.
Các chất còn lại :
❌C6H5CH2OH (Benzyl alcohol) : Là ancol, không phải phenol → không có tính axit để tác dụng với NaOH.
❌C2H5OH (Ethanol - rượu etylic) : Là ancol → chỉ tác dụng với Na, không tác dụng với NaOH.
❌C6H5CH3 (Toluene); C6H5Cl (Chlorobenzene) : Không có nhóm -OH → không tác dụng với Na hay NaOH.
⟹Chọn đáp án B Đáp án: B
✔️ A. 1740 – 1670 cm–1 là dao động kéo dài của liên kết 1650 – 1620 cm–1 là vùng của dao động liên kết đôi , không liên quan đến nhóm carbonyl.
❌ C. 3650 – 3200 cm–1 là vùng của dao động kéo dài liên kết (như trong alcohol hoặc carboxylic acid)
❌ D. 2250 – 2150 cm–1 là vùng của dao động kéo dài liên kết ba hoặc , không xuất hiện trong acetone.
⇒ Chọn đáp án A Đáp án: A
(a) Soda là chất bột màu trắng, tan trong nước tạo môi trường trung tính.
(b) Soda có thể được dùng để làm mềm nước cứng.
(c) Soda bền với nhiệt hơn so với baking soda.
(d) Chất béo có thể bị thuỷ phân trong dung dịch soda tạo thành xà phòng.
(e) Có thể dùng baking soda thay cho soda trong việc tẩy rửa lớp dầu, mỡ bám vào bồn rửa.
Số phát biểu đúng là
❌(a) .Sai. Soda tan trong nước tạo môi trường base do phản ứng thủy phân:
Na2CO3 + H2O → 2Na+ + HCO3- + OH-
✔️(b). Đúng. Soda phản ứng với các ion Ca2⁺ và Mg2⁺ trong nước cứng, tạo thành kết tủa CaCO3 và MgCO3, giúp làm mềm nước.
✔️(c) Đúng. Soda (Na2CO3) bền nhiệt hơn baking soda (NaHCO3). Baking soda dễ dàng được phân hủy nhiệt hơn.
✔️(d) .Đúng. Soda (
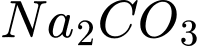 ) là muối của kim loại mạnh và gốc acid yếu. Khi tan trong nước, nó bị thủy phân tạo ra môi trường kiềm theo phương trình sau:
) là muối của kim loại mạnh và gốc acid yếu. Khi tan trong nước, nó bị thủy phân tạo ra môi trường kiềm theo phương trình sau: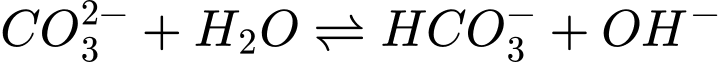 . Chính các ion
. Chính các ion 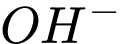 này đóng vai trò quan trọng trong việc phá vỡ cấu trúc của chất béo hay thuỷ phân chát béo.
này đóng vai trò quan trọng trong việc phá vỡ cấu trúc của chất béo hay thuỷ phân chát béo.✔️(e) Đúng. Baking soda có tính kiềm kiềm và khả năng làm sạch dầu mỡ, có thể được sử dụng thay thế soda trong một số trường hợp.
Các phát biểu đúng là (b), (c), (d), (e)
⟹ Chọn đáp án D Đáp án: D
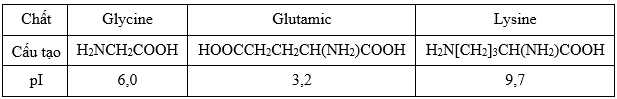
Trong các giá trị pH cho dưới đây, giá trị nào là tối ưu nhất để tách ba chất trên ra khỏi dung dịch hỗn hợp của chúng?
Glutamic acid có pI = 3,2 < pH = 6,0 → Glutamic acid tồn tại trong dung dịch dưới dạng anion nên glutamic acid di chuyển về phía cực dương.
Lysine có pI = 9,7 > pH = 6,0 → Lysine tồn tại trong dung dịch dưới dạng cation nên lysine di chuyển về phía cực âm.
→ pH = 6,0 sẽ là môi trường tối ưu tách được 3 𝞪-amino acid.Đặt hỗn hợp các amino acid gồm lysine, glycine và glutamic acid ở pH = 6,0 vào trong một điện trường.
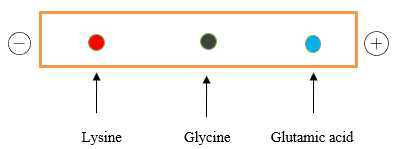
Sự di chuyển của α-amino acid dưới tác dụng của điện trường ở pH = 6
⇒ Chọn đáp án D Đáp án: D
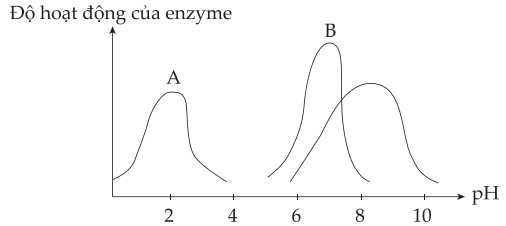
Trong số các enzyme đã nêu trong biểu đồ, amylase là một enzyme tiêu hoá chủ yếu được tiết ra bởi tuyến tụy và tuyến nước bọt, có tác dụng thuỷ phân tinh bột thành maltose. Pepsin và trypsin cũng là các enzyme tiêu hoá, lần lượt có trong dịch vị và ruột non với vai trò phân giải protein. Trypsin hoạt động tốt nhất trong môi trường kiềm nhẹ.
Enzyme A và B lần lượt là
- Enzyme A có độ hoạt động tối ưu ở pH khoảng 2. Pepsin là enzyme tiêu hóa có trong dịch vị, hoạt động tốt nhất trong môi trường acid (pH khoảng 2). Do đó, enzyme A là pepsin.
- Enzyme B có độ hoạt động tối ưu ở pH khoảng 7. Amylase hoạt động tốt nhất trong môi trường trung tính, trong tuyến nước bọt và tuyến tuỵ (pH khoảng 7). Do đó, enzyme B là amylase.
⟹ Chọn đáp án D Đáp án: D
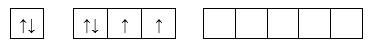

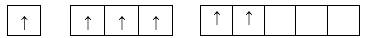
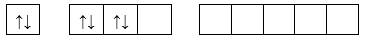
- Cấu hình electron của S: 1s22s22p63s23p4
- Cấu hình e lớp ngoài cùng: 3s23p4
⟹Chọn đáp án A Đáp án: A
✔️A. Đồng có thể bị oxi hóa trong không khí, phản ứng với O2 đơn thuần tạo ra lớp gỉ xanh lục đặc trưng. Thông thường, quá trình này cần có sự tham gia của các khí khác như CO2, H2O và SO2 → Đúng.
❌B. Nếu đồng tác dụng với acid mạnh (như HCl, H2SO4), nó có thể tạo muối đồng (II). Tuy nhiên, lớp gỉ xanh trên bề mặt đồng không phải do phản ứng trực tiếp với acid, mà do tác động của khí CO2, H2O và SO2 trong môi trường ẩm. → Sai.
❌C. Muối đồng (I) không phải là nguyên nhân chính gây ra lớp xanh lục. Lớp gỉ đồng xanh thực chất là hỗn hợp của đồng(II) hydroxit (Cu(OH)2) và đồng(II) cacbonat (CuCO3), hình thành do tác động của CO2, H2O và O2. → Sai.
❌D. Khi đồng tiếp xúc với không khí ẩm và các khí như CO2, SO2, lớp gỉ xanh hình thành là một dạng muối đồng(II) như Cu(OH)2·CuCO3 (gỉ đồng lục - patina). → Sai.
⟹Chọn đáp án A Đáp án: A
- Sodium nitrate được dùng trong phạm vi rộng như là một loại phân bón và nguyên liệu thô cho quá trình sản xuất thuốc súng vào cuối thế kỷ 19. Nó có thể kết hợp với iron(II) hydroxide để tạo nhựa thông.
NaNO3 ⟶ NaNO2 + O2
⟹Chọn đáp án B Đáp án: B
⇒ từ đó người ta gọi phản ứng này là phản ứng xà phòng hóa. Sau đó được mở rộng ra cho phản ứng thủy phân ester trong môi trường base
⟹Chọn đáp án A. Đáp án: A
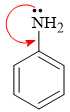
(a) Tính base của amine được gây ra do cặp electron trên nguyên tử N.
(b) Cặp electron bị hút vào vòng trên nguyên tử N là cặp electron chưa tham gia liên kết.
(c) Do ảnh hưởng của vòng phenyl nên aniline có pH lớn hơn diphenylamine.
(d) Ảnh hưởng của gốc C6H5 đến nhóm NH2 so với methylamine có thể được kiểm chứng qua thí nghiệm với quỳ tím.
Trong các phát biểu trên, những phát biểu đúng là
✔️ (a) Đúng. Tính base của amine được gây ra bởi khả năng nhường cặp electron tự do trên nguyên tử N cho proton (H+) để tạo liên kết. Do đó, cặp electron trên N chính là nguyên nhân gây tính base.
✔️ (b) Trong aniline, cặp electron tự do trên nguyên tử N (cặp electron chưa tham gia liên kết) bị hút vào vòng. Do đó, cặp electron này làm giảm mật độ electron trên N, từ đó làm giảm tính base của aniline.
✔️ (c) Ở diphenylamine, nhóm NH2 gắn với hai gốc phenyl làm cặp electron trên N bị hút mạnh hơn, dẫn đến tính base của diphenylamine nhỏ hơn so với aniline ⬌ pH của dung dịch aniline sẽ lớn hơn pH của dung dịch diphenylamine.
✔️ (d) Đúng. Ảnh hưởng của gốc C6H5 đến nhóm NH2 so với methylamine có thể được kiểm chứng qua thí nghiệm với quỳ tím:
- Dung dịch methylamine có tính base mạnh hơn (làm quỳ tím chuyển màu xanh đậm hơn).
- Dung dịch aniline có tính base yếu hơn (làm quỳ tím chuyển màu xanh nhạt hơn hoặc không đổi màu).
➥ Cả 4 phát biểu đều đúng
⇒ Chọn đáp án D Đáp án: D
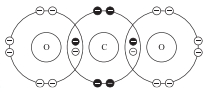
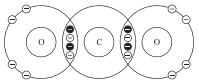
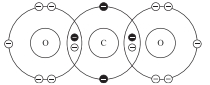
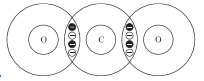
C (Z = 6): 1s22s22p2→ có 4 electron lớp ngoài cùng
O (Z = 8): 1s22s22p4 → có 6 electron lớp ngoài cùng
Theo quy tắc bát tử C cần 4 electron để đạt được cấu hình bát tử. Oxygen cần 2 electron để được cấu hình bát tử.
Suy ra mỗi nguyên tử Oxygen sẽ góp chung 2 electron và mỗi nguyên tử Carbon sẽ góp chung 4 electron chia đều cho cả hai bên.
Phân tích các phát biểu
❌Sai. A. Không đúng. Carbon không đủ liên kết
✔️Đúng. B. Carbon có 4 liên kết (4 cặp electron chia sẻ).
Oxygen có 2 liên kết (2 cặp electron chia sẻ) và 4 electron tự do (2 cặp electron không chia sẻ).
❌Sai. C. Carbon chỉ có 2 liên kết, không đủ 4 liên kết cần thiết.
Oxygen cũng không đủ electron tự do.
❌Sai. D. Carbon chỉ có 2 liên kết, không đủ 4 liên kết cần thiết.
Oxygen cũng không đủ electron tự do.
⟹ Chọn đáp án B Đáp án: B
Sử dụng đoạn thông tin dưới đây để trả lời câu 17 và câu 18:
liên kết với nhau, thường được kí hiệu là R1, R2 và R3. Các ví dụ về các loại như sau:
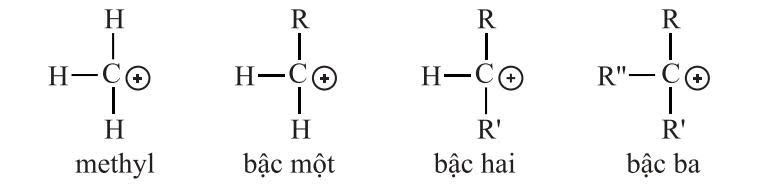
Cho các carbocation sau:
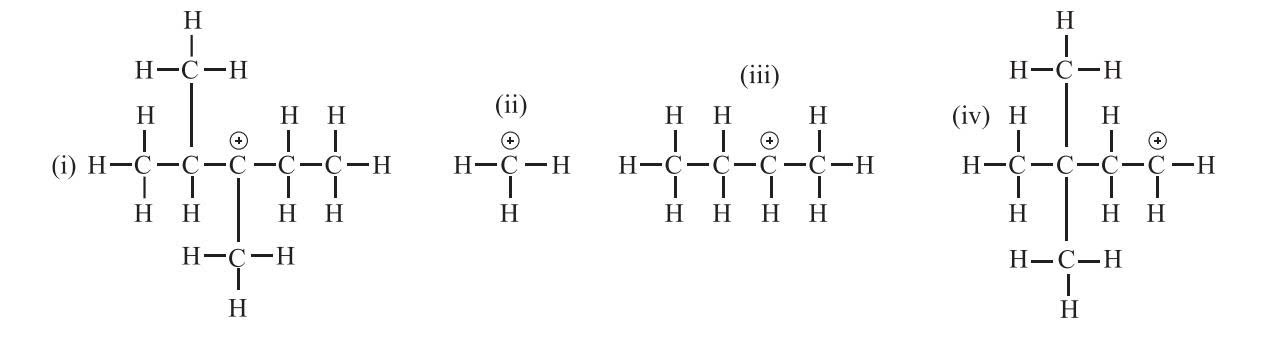
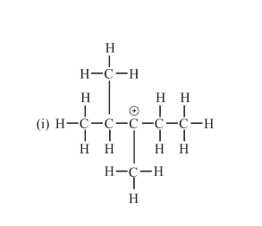
Loại carbocation nào được biểu diễn ở hình (i) là bậc III.
⟹ Chọn đáp án D Đáp án: D
Bậc III (bậc ba) > Bậc II (bậc hai) > Bậc I (bậc nhất) > Methyl
Vì các nhóm alkyl có hiệu ứng đẩy electron (+I), làm ổn định hóa điện tích dương.
Thứ tự độ bền tăng dần của bốn carbocation trên là (ii) – methyl, (iv) – bậc I, (iii) – bậc II, (i) – bậc III.
⟹ Chọn đáp án A Đáp án: A
PHẦN II. Thí sinh trả lời từ câu 1 đến câu 4. Trong mỗi ý a), b), c), d) ở mỗi câu, thí sinh chọn đúng hoặc sai.
Tiến hành thí nghiệm nhận biết các dung dịch mẫu thử đựng trong các ống nghiệm riêng biệt là 1 mL dung dịch MgSO4, FeCl3, và CuSO4 (có cùng nồng độ 0,1 M).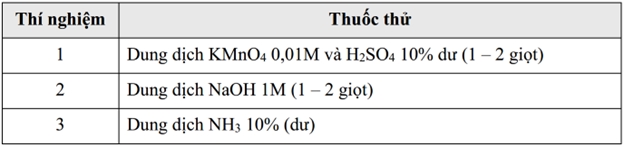
MgSO₄: không màu
FeCl₃: màu vàng
CuSO₄: màu xanh
❌Nhận định b) – Sai, vì: KMnO₄ trong môi trường acid chỉ bị mất màu khi có chất khử mạnh (Fe²⁺, SO₃²⁻,…)
MgSO₄: không phản ứng → dung dịch vẫn màu tím
FeCl₃ (Fe³⁺): không có tính khử → không làm mất màu KMnO₄
CuSO₄ (Cu²⁺): không phản ứng, không tạo phức xanh trong môi trường này
✔️Nhận định c) – Đúng, vì: Hiện tượng xảy ra lần lượt là:
MgSO₄ + NaOH → Mg(OH)₂ ↓ trắng
FeCl₃ + NaOH → Fe(OH)₃ ↓ nâu đỏ
CuSO₄ + NaOH → Cu(OH)₂ ↓ xanh nhạt
✔️Nhận định d) – Đúng, vì: Hiện tượng xảy ra lần lượt là:
MgSO₄ → Mg(OH)₂ ↓ trắng
FeCl₃ → Fe(OH)₃ ↓ nâu đỏ
CuSO₄ → ban đầu kết tủa Cu(OH)₂, sau đó tan trong NH₃ dư tạo phức[Cu(NH3)4]2+ màu xanh lam
Cho hai chất hữu cơ mạch hở E, F có cùng thành phần nguyên tố: 40,00% C; 6,67% H và 53,33% O về khối lượng. Trên phổ MS, peak ion phân tử của E và F đều nhỏ hơn 100. Cho phổ IR của E và F: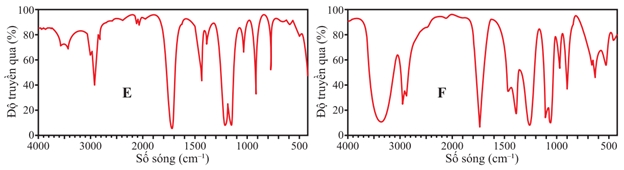
Đun nóng E, F với dung dịch NaOH dư đều tạo ra sản phẩm gồm hai chất hữu cơ.
Có thành phần phần trăm: C: 40%; H: 6,67%; O: 53,33%.
=> Tỉ lệ nguyên tử:
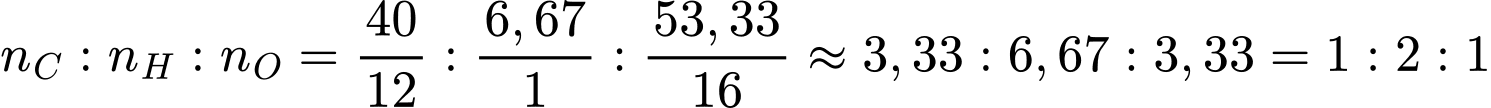 => Công thức đơn giản nhất:
=> Công thức đơn giản nhất: 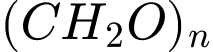 .
.Vì khối lượng phân tử (M) của E và F đều nhỏ hơn 100:
• Nếu
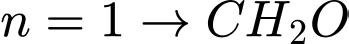 (Formaldehyde - không phù hợp với phản ứng với NaOH).
(Formaldehyde - không phù hợp với phản ứng với NaOH).• Nếu
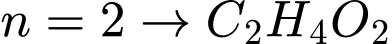 (
( ) - không đủ oxy để tạo 2 sản phẩm hữu cơ khác nhau).
) - không đủ oxy để tạo 2 sản phẩm hữu cơ khác nhau).• Nếu
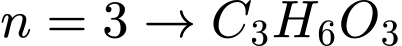 (
( ).
).Xét E và F có cùng CTPT là:

➤ Phổ IR của E:
• Có dải hấp thụ mạnh ở ~1740 cm⁻¹ → đây là dải C=O của ester.
➤ Phổ IR của F:
• Có dải hấp thụ ở ~1710 cm⁻¹ → cũng là C=O, nhưng hơi thấp hơn → có thể là acid carboxylic.
• Có dải rộng, mạnh ở ~3300 cm⁻¹ → O–H.
→ E: có C=O (ester) → có thể là tạp chức chứa chức ester
→ F: có C=O (acid) + O–H → acid carboxylic.
Mà: E và F đều thủy phân trong NaOH cho 2 chất hữu cơ → nếu F là acid thì không thủy phân trong NaOH — mà chỉ tạo muối (1 chất hữu cơ là muối, 1 chất là nước — không phải hữu cơ).
➡️ Vậy F không thể là acid — mà phải là ester.
-------------------------------------------------------------------
Phân tích các nhận định:
✔️Nhận định a) – Đúng, vì: Dựa theo phân tích đề bài ta có thể xác định một số công thức cấu tạo thoả mãn của E và F là:
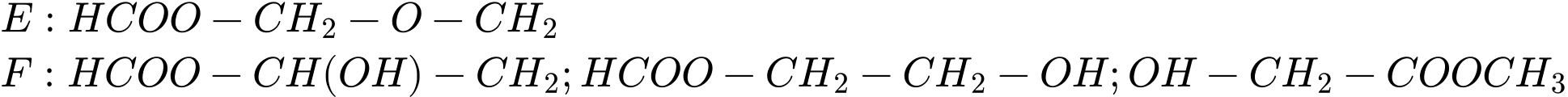
=> Tất cả đều chứa chức ester
✔️Nhận định b) – Đúng, vì: Công thức cấu tạo của F có thể là:
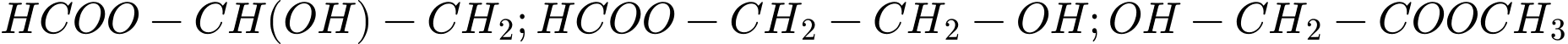
Khi thuỷ phân có thể tạo thành alcohol 2 chức: (Ethylene glycol)
❌Nhận định c) – Sai, vì: F có thể tạo được liên kết hydrogen với nước
❌Nhận định d) – Sai, vì: E có nhiệt độ sôi thấp hơn so với F do F tạo liên kết hydrogen liên phân tử nhờ nhóm chức –OH
Phức chất của Ni²⁺ với dimethylglyoxime (DMG) được sử dụng rộng rãi trong phân tích định tính và định lượng để nhận biết ion Ni2+. Phức chất này có màu đỏ tươi, không tan trong nước, có dạng cấu trúc vuông phẳng, được tạo thành theo phản ứng: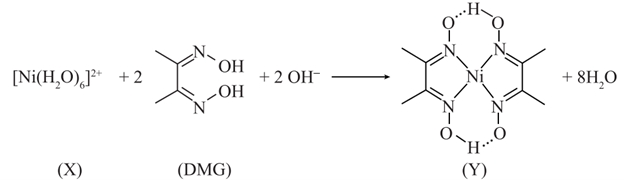
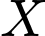 là
là 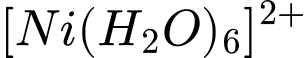 . Trong đó,
. Trong đó, 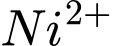 liên kết với 6 phối tử nước (
liên kết với 6 phối tử nước (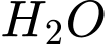 ). Với số phối trí bằng 6, phức chất này luôn có cấu trúc hình học bát diện
). Với số phối trí bằng 6, phức chất này luôn có cấu trúc hình học bát diện✔️ Nhận định b) – Đúng, vì: Dựa vào phương trình ta thấy: 6 phân tử
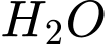 trong cầu nội của
trong cầu nội của 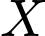 đã bị tách ra và thay thế bởi các phân tử DMG để tạo thành phức
đã bị tách ra và thay thế bởi các phân tử DMG để tạo thành phức 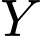 . Đây chính là phản ứng thế phối tử (ligand substitution).
. Đây chính là phản ứng thế phối tử (ligand substitution).❌ Nhận định c) – Sai, vì: Quan sát cấu trúc của
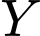 trong hình: Liên kết hydrogen (biểu diễn bằng dấu chấm "...") nằm giữa nguyên tử O và H của hai phối tử DMG với nhau. Nó không nằm giữa nguyên tử trung tâm (
trong hình: Liên kết hydrogen (biểu diễn bằng dấu chấm "...") nằm giữa nguyên tử O và H của hai phối tử DMG với nhau. Nó không nằm giữa nguyên tử trung tâm (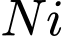 ) và phối tử.
) và phối tử.❌ Nhận định d) – Sai, vì: Nhìn vào phương trình, ta thấy có sự tham gia của
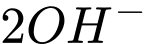 để trung hòa
để trung hòa 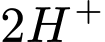 tách ra từ 2 phân tử DMG. Phức
tách ra từ 2 phân tử DMG. Phức 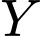 tạo thành là một phân tử trung hòa về điện (không mang điện tích), nên công thức đúng phải là
tạo thành là một phân tử trung hòa về điện (không mang điện tích), nên công thức đúng phải là 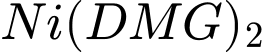 .
.
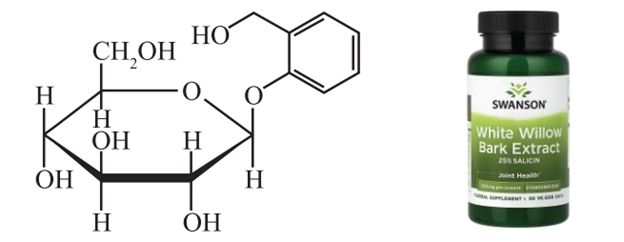
Salicin là một loại thuốc giảm đau, chống viêm được sản xuất từ vỏ cây liễu, có công thức cấu tạo như dưới đây:
❌ Nhận định a) – Sai, vì:
Công thức cấu tạo của Salicin gồm 2 phần:
• Đếm số nguyên tử trong cấu trúc: Phần đường (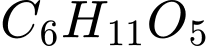 )
)
• Phần aglycone (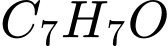 )
)
 Tổng là
Tổng là 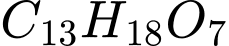 không phải
không phải 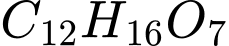 .
.
✔️ Nhận định b) – Đúng, vì: Khi thuỷ phân salicin trong môi trường acid thì liên kết glycosid bị cắt → Sản phẩm thu được gồm: Glucose (chất A) và salicyl alcohol
✔️ Nhận định c) – Đúng, vì: Trong phân tử salicin có chứa đồng thời nhiều nhóm chức khác nhau: nhóm alcohol ( ), nhóm ether (liên kết glycoside) và vòng thơm.
), nhóm ether (liên kết glycoside) và vòng thơm.
✔️ Nhận định d) – Đúng, vì:
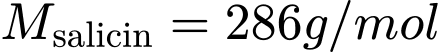 =>
=> 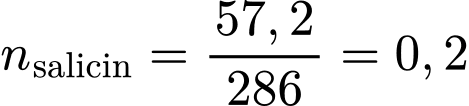 mol.
mol.
Theo sơ đồ, tỉ lệ là 1:1  mol.
mol.
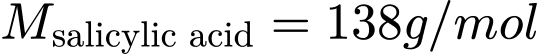
=> Khối lượng thực tế: 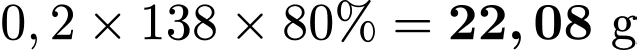 .
.
PHẦN III. Thí sinh trả lời từ câu 1 đến 6. Thí sinh điền kết quả mỗi câu vào mỗi ô trả lời tương ứng theo hướng dẫn của phiếu trả lời.
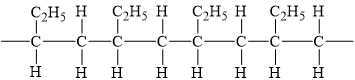
Monomer tạo thành A có chứa mấy nguyên tử carbon?
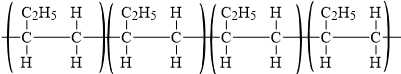
→ Momomer tương ứng có dạng:
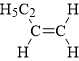 với 4 nguyên tử carbon.
với 4 nguyên tử carbon.⇒ Điền đáp án: 4
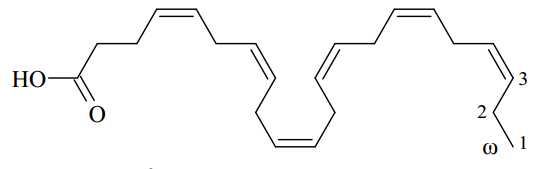
Có bao nhiêu nối đôi C=C trong cấu tạo của phân tử DHA?
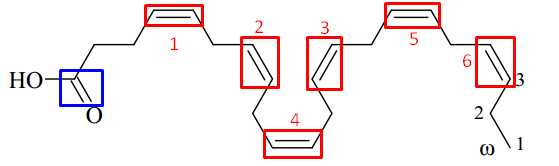
⇒ Điền đáp án: 6
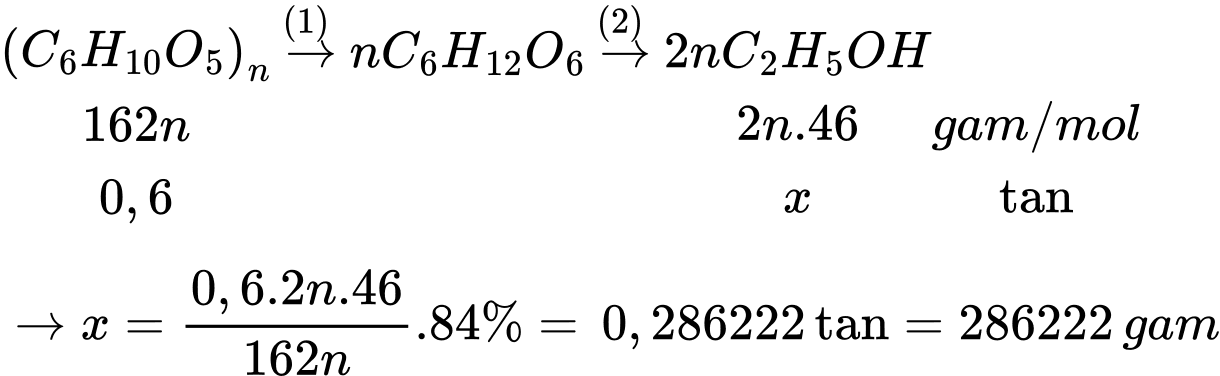
Thể tích xăng E5 thu được là
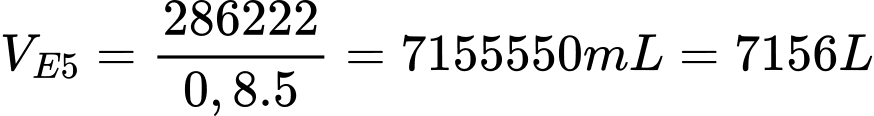
⟹Điền đáp án : 7156
- Để phân hủy 1 kg đá vôi (chứa CaCO3 và 4% tạp chất trơ) cần cung cấp một lượng nhiệt là 1800 kJ.
- Đốt cháy hoàn toàn 1 kg than đá giải phóng ra một lượng nhiệt là 27 000 kJ và có 30% lượng nhiệt bị thất thoát trong quá trình phân hủy đá vôi. Khối lượng (tính theo đơn vị tấn) than đá mà lò nung vôi đã sử dụng mỗi ngày là bao nhiêu (làm tròn đến hàng phần mười)?
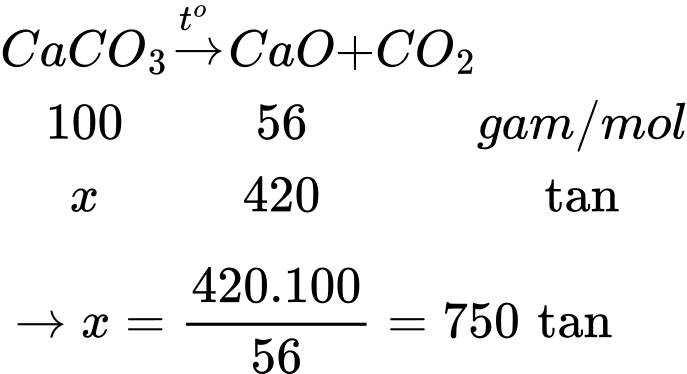
Khối lượng đá vôi là m = 750 ÷ 96% = 781,25 tấn =781250 kg
Phân hủy 1 kg đá vôi cần 1800 kJ
1 kg than đá tỏa ra 27000 kJ
Khối lượng than đá cần để sản xuất 420 tấn vôi sống là
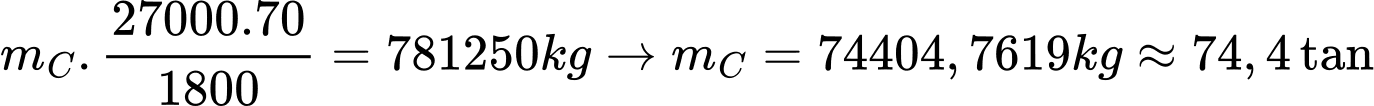
⟹ Điền đáp án : 74,4
100 gam H2O hòa tan 28,3 gam Na2SO4 tạo thành 128,3 gam dung dịch bão hòa
- Gọi x là số mol Na2SO4. 10H2O tách ra → Số mol H2O tách ra là 10x mol
⟹ Khối lượng H2O tách ra: 180x (g)
Khối lượng Na2SO4tách ra: 142x (gam)
- Ở 10oC, SNa2SO4= 9 gam
- Ta có phương trình:
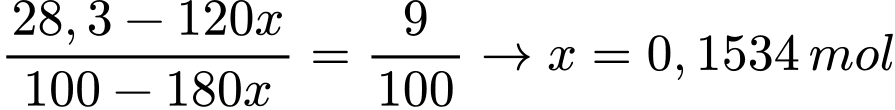
→ Khối lượng Na2SO4.10H2O kết tinh: 322.0,1534 ≈ 49,4 gam.
⟹Điền đáp án : 49,4
H2C2O4 + KMnO4 + H2SO4 → CO2 + MnSO4 + K2SO4 + H2O (1)
Quy trình tiến hành chuẩn độ: Dùng pipette lấy 10,0 mL dung dịch H2C2O4 0,1 M cho vào bình tam giác, thêm khoảng 10,0 mL dung dịch H2SO4 2M, đun nóng trên bếp điện đến 70 – 80°C (không đun sôi). Cho đầy dung dịch KMnO4 cần xác định nồng độ (được pha sẵn) vào burete và điều chỉnh đến vạch số 0. Nhỏ từng giọt dung dịch KMnO4 cần xác định ở trên vào bình tam giác đựng dung dịch H2C2O4 đã acid hóa, lắc đều dung dịch tới khi có màu hồng nhạt bền khoảng 20 giây. Đọc và ghi lại thể tích KMnO4 trên burette như sau:
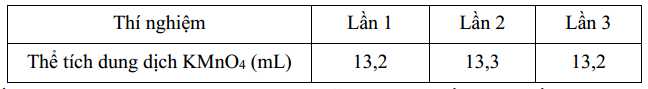
Tính nồng độ (M) của dung dịch KMnO4 được pha sẵn (làm tròn đến hàng phần trăm).
Thể tích trung bình của KMnO4 là:
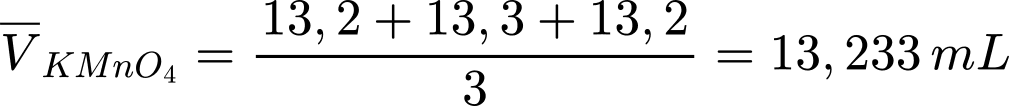
Đổi 13,233 mL = 0,013233 L; 10 mL = 0,01 L
Số mol của H2C2O4 là:
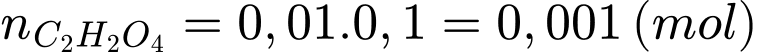
Từ phương trình hóa học số mol của KMnO4 là:
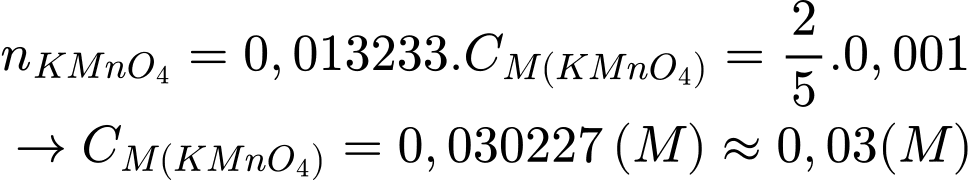
⇒ Điền đáp án: 0,03