PHẦN II. Thí sinh trả lời từ câu 1 đến câu 4. Trong mỗi ý a), b), c), d) ở mỗi câu, thí sinh chọn đúng hoặc sai.
Câu 1 [304839]: Thủy phân ester X trong dung dịch acid, thu được CH3COOH và CH3OH. Công thức cấu tạo của X là
A, HCOOC2H5.
B, CH3COOC2H5.
C, C2H5COOCH3.
D, CH3COOCH3.
Phân tích phản ứng:
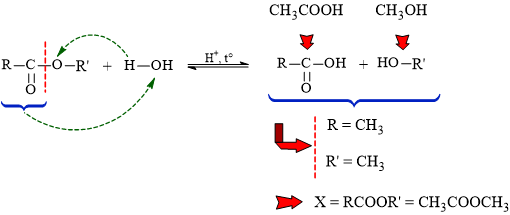
⟹ Vậy ester X là methyl acetate: CH3COOCH3
⟹ Chọn đáp án D Đáp án: D

⟹ Vậy ester X là methyl acetate: CH3COOCH3
⟹ Chọn đáp án D Đáp án: D
Câu 2 [705879]: Carbohydrate nào sau đây kém tan trong nước lạnh nhưng tan được trong nước nóng tạo dung dịch keo, nhớt?
A, Glucose.
B, Tinh bột.
C, Cellulose.
D, Saccharose.
Tinh bột là chất rắn, màu trắng, hầu như không tan trong nước lạnh, trong nước nóng tinh bột tan tạo thành dung dịch keo nhớt gọi là hồ tinh bột.
Chọn đáp án B Đáp án: B
Chọn đáp án B Đáp án: B
Câu 3 [560810]: Sodium hydrogencarbonate được dùng làm thuốc giảm đau dạ dày do thừa acid. Công thức của Sodium hydrogencarbonate là
A, KHCO3.
B, Na2CO3.
C, K2CO3.
D, NaHCO3.
Sodium hydrogencarbonate (NaHCO3), còn gọi là baking soda, có tính chất lưỡng tính, có thể phản ứng với cả acid và base.
Tên của các hợp chất còn lại:
A. KHCO3: Patossium hydrogencarbonate
B. Na2CO3: Sodium carbonate
C. K2CO3: Patossium carbonate
D. NaHCO3: Sodium hydrogencarbonate
⇒ Chọn đáp án D Đáp án: D
Tên của các hợp chất còn lại:
A. KHCO3: Patossium hydrogencarbonate
B. Na2CO3: Sodium carbonate
C. K2CO3: Patossium carbonate
D. NaHCO3: Sodium hydrogencarbonate
⇒ Chọn đáp án D Đáp án: D
Câu 4 [705903]: Phèn nhôm – kali là muối sulfate kép của potassium và nhôm. Công thức hóa học của phèn nhôm – kali là
A, KAl(SO4)2.
B, NaAl(SO4)2.
C, (NH4)Al(SO4)2.
D, KAl(SO4)2.12H2O.
Kali alum là muối sulfate kép của potasium và aluminium. Tên tiếng Việt phổ biến là phèn chua. Công thức hóa học là KAl(SO4)2 và thông thường được thấy ở dạng ngậm nước là KAl(SO4)2.12H2O. Chất này được sử dụng rộng rãi để làm trong nước đục, thuộc da, sản xuất vải chống cháy và bột nở.
Phèn chua là loại muối có tinh thể to nhỏ không đều, không màu hoặc trắng, cũng có thể trong hoặc hơi đục. Phèn chua tan trong nước nhưng không tan trong cồn.
Chọn đáp án D Đáp án: D
Phèn chua là loại muối có tinh thể to nhỏ không đều, không màu hoặc trắng, cũng có thể trong hoặc hơi đục. Phèn chua tan trong nước nhưng không tan trong cồn.
Chọn đáp án D Đáp án: D
Câu 5 [705745]: Trong tự nhiên, phản ứng giữa nitrogen và oxygen (trong cơn mưa dông kèm sấm sét) là khởi đầu cho quá trình tạo và cung cấp loại phân bón nào sau đây cho cây?
A, Phân kali.
B, Phân lân.
C, Phân đạm ammonium.
D, Phân đạm nitrate.
Trong tự nhiên, phản ứng giữa nitrogen và oxygen (trong con mưa dông kèm sấm sét) là khởi đầu cho quá trình tạo và cung cấp loại phân đạm nitrate cho cây.
Quá trình tạo và cung cấp đạm nitrate cho đất từ nước mưa được biểu diễn theo sơ đồ:
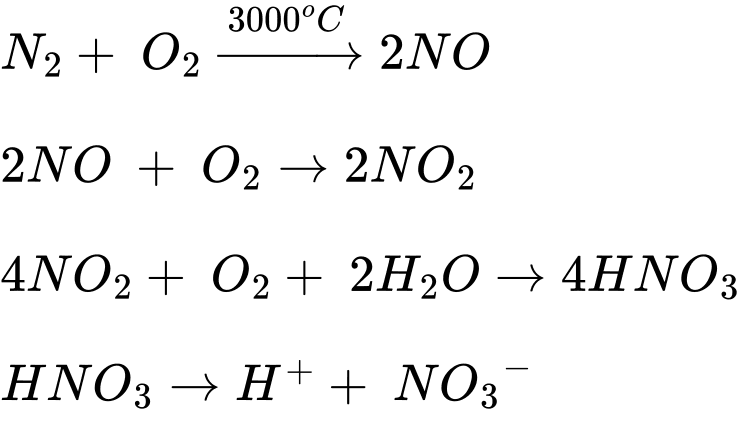
⇒ Chọn đáp án D Đáp án: D
Quá trình tạo và cung cấp đạm nitrate cho đất từ nước mưa được biểu diễn theo sơ đồ:
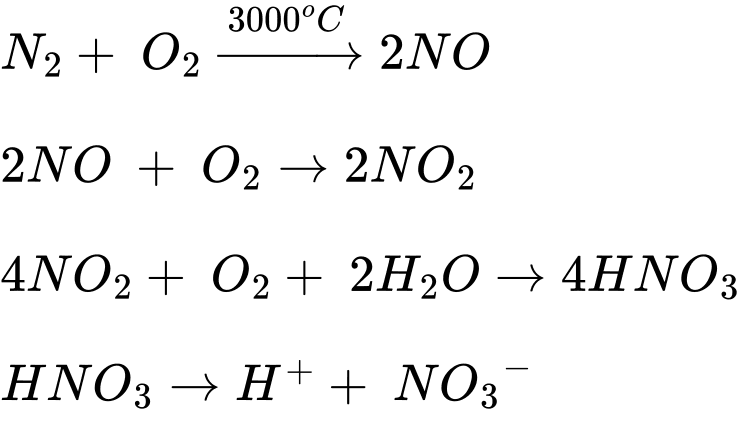
⇒ Chọn đáp án D Đáp án: D
Câu 6 [308668]: Nhóm chức -NH2 có tên gọi là
A, Amino.
B, Nitro.
C, Amine.
D, Nitrile.
Nhóm chức -NH2 có tên gọi là amine.
⇒ Chọn đáp án C Đáp án: C
⇒ Chọn đáp án C Đáp án: C
Câu 7 [575616]: Trong hợp chất ion, để hình thành ion O2– thì mỗi nguyên tử oxygen đã
A, nhường 2 electron.
B, nhận 2 electron.
C, góp chung 2 electron.
D, góp chung 2 cặp electron.
HƯỚNG DẪN GIẢI:
- Nguyên tử O (Z = 8) có cấu hình electron là 1s22s22p4
⟶ Oxygen có 6 electron lớp ngoài cùng cần nhận 2 electron đạt octet tạo thành ion O2–:
O + 2e ⟶ O2–
⇒ Chọn đáp án B Đáp án: B
- Nguyên tử O (Z = 8) có cấu hình electron là 1s22s22p4
⟶ Oxygen có 6 electron lớp ngoài cùng cần nhận 2 electron đạt octet tạo thành ion O2–:
O + 2e ⟶ O2–
⇒ Chọn đáp án B Đáp án: B
Câu 8 [702813]: Câu nào sau đây không đúng khi nói về peptide X có cấu tạo như hình dưới?
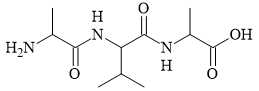

A, Peptide X có chứa ba liên kết peptide.
B, Amino acid đầu N là Ala.
C, Amino acid đầu C là Ala.
D, Thủy phân hoàn toàn peptide X thu được hai loại amino acid khác nhau.
Xét các phát biểu:
❌ A. Sai. Peptide X được tạo bởi 3 amino acid nên có chứa hai liên kết peptide.
✔️ B. Đúng. Amino acid đầu N là Ala: CH3CH(NH2)CO-NH...
✔️ C. Đúng. Amino acid đầu C là Ala: CO-NHCH(CH3)-COOH.
✔️ D. Đúng. Peptide X được tạo bởi 2 amino acid là Ala: CH3CH(NH2)COOH và Valine: (CH3)2CHCH(NH2)COOH nên khi thủy phân hoàn toàn peptide X thu được hai loại amino acid khác nhau.
⇒ Chọn đáp án A Đáp án: A
❌ A. Sai. Peptide X được tạo bởi 3 amino acid nên có chứa hai liên kết peptide.
✔️ B. Đúng. Amino acid đầu N là Ala: CH3CH(NH2)CO-NH...
✔️ C. Đúng. Amino acid đầu C là Ala: CO-NHCH(CH3)-COOH.
✔️ D. Đúng. Peptide X được tạo bởi 2 amino acid là Ala: CH3CH(NH2)COOH và Valine: (CH3)2CHCH(NH2)COOH nên khi thủy phân hoàn toàn peptide X thu được hai loại amino acid khác nhau.
⇒ Chọn đáp án A Đáp án: A
Câu 9 [704022]: Cấu hình electron nào sau đây ứng với nguyên tố có độ âm điện lớn nhất?
A, 1s22s22p5.
B, 1s22s22p6.
C, 1s22s22p63s1.
D, 1s22s2.
Phân tích các nguyên tố:
A.1s22s22p5 → có 7e lớp ngoài cùng → là nguyên tố phi kim
B. 1s22s22p6 → có 8e lớp ngoài cùng → là nguyên tố khí hiếm
C. 1s22s22p63s1 → có 1e lớp ngoài cùng → là nguyên tố kim loại
D. 1s22s2 → có 2e lớp ngoài cùng → là nguyên tố kim loại
Độ âm điện của các chất được sắp xếp theo chiều giảm dần như sau: Phi kim > Kim loại > Khí hiếm.
⇒ Chọn đáp án A Đáp án: A
A.1s22s22p5 → có 7e lớp ngoài cùng → là nguyên tố phi kim
B. 1s22s22p6 → có 8e lớp ngoài cùng → là nguyên tố khí hiếm
C. 1s22s22p63s1 → có 1e lớp ngoài cùng → là nguyên tố kim loại
D. 1s22s2 → có 2e lớp ngoài cùng → là nguyên tố kim loại
Độ âm điện của các chất được sắp xếp theo chiều giảm dần như sau: Phi kim > Kim loại > Khí hiếm.
⇒ Chọn đáp án A Đáp án: A
Câu 10 [703967]: “Xà phòng là hỗn hợp muối ...(1)... của ...(2)... và các chất phụ gia”. Nội dung phù hợp trong ô trống (1), (2) lần lượt là
A, sodium và calcium, chất béo.
B, sodium và potassium, chất béo.
C, sodium và potassium, acid béo.
D, potassium và barium, acid béo.
Xà phòng là hỗn hợp các muối sodium và potassium của acid béo và một số chất phụ gia. Các acid béo ở đây thường là acid no như palmitic acid, stearic acid. Chất phụ gia thường dùng là chất độn làm tăng độ cứng để dễ đúc thành bánh, chất tạo màu và chất tạo hương.
⇒ Chọn đáp án C Đáp án: C
⇒ Chọn đáp án C Đáp án: C
Câu 11 [705884]: Trong ngành dệt may, tơ visco được sử dụng nhiều nhờ đặc tính mềm như sợi tơ lụa nên chúng được ứng dụng để may các bộ trang phục cao cấp. Carbohydrate nào sau đây được dùng làm nguyên liệu sản xuất tơ visco?
A, Saccharose.
B, Tinh bột.
C, Glucose.
D, Cellulose.
Tơ visco (hay tơ rayon) là một loại tơ bán tổng hợp được sản xuất từ cellulose tự nhiên có trong bột gỗ hoặc sợi bông. Được tạo ra từ cellulose tự nhiên qua quá trình xử lý hóa học. Bột gỗ hoặc sợi bông được hòa tan trong dung dịch hóa học (thường là dung dịch xút NaOH), sau đó được tái tạo thành sợi qua quá trình kéo sợi.
Chọn đáp án D Đáp án: D
Chọn đáp án D Đáp án: D
Câu 12 [703947]: Trypsin là một loại enzyme có trong phần đầu tiên của ruột non, bắt đầu quá trình tiêu hóa các phân tử protein bằng cách cắt các chuỗi dài amino acid thành các mảnh nhỏ hơn. Một điểm đặc biệt là trypsin cắt các amino acid một cách có chọn lọc, cắt đứt liên kết CO–NH (với phần carbonyl thuộc về amino acid Arg hoặc Lys).
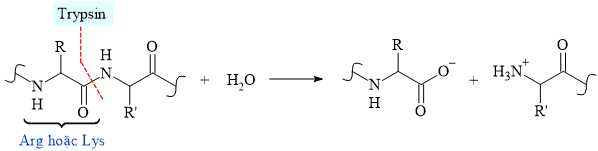
Cho chuỗi amino acid sau: Thr–Pro–Lys–Glu–His–Gly–Phe–Cys–Trp–Val–Val–Phe.
Tiến hành cắt đứt chuỗi amino acid bằng enzyme trypsin thì sản phẩm thu được có thể là

Cho chuỗi amino acid sau: Thr–Pro–Lys–Glu–His–Gly–Phe–Cys–Trp–Val–Val–Phe.
Tiến hành cắt đứt chuỗi amino acid bằng enzyme trypsin thì sản phẩm thu được có thể là
A, Thr–Pro và Lys–Glu–His–Gly–Phe–Cys–Trp–Val–Val–Phe.
B, Thr–Pro–Lys–Glu–His–Gly–Phe–Cys–Trp và Val–Val–Phe.
C, Thr–Pro–Lys và Glu–His–Gly–Phe–Cys–Trp–Val–Val–Phe.
D, Thr–Pro–Lys–Glu–His và Gly–Phe–Cys–Trp–Val–Val–Phe.
Khi tiến hành cắt đứt chuỗi amino acid bằng enzyme trypsin thì trypsin cắt các amino acid một cách có chọn lọc, nó sẽ cắt đứt liên kết CO–NH với phần carbonyl thuộc về amino acid Arg hoặc Lys nên quá trình cắt đứt xảy ra như sau:
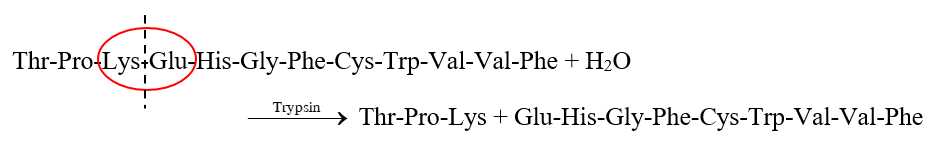
Sản phẩm thu được là Thr–Pro–Lys và Glu–His–Gly–Phe–Cys–Trp–Val–Val–Phe
⇒ Chọn đáp án C Đáp án: C
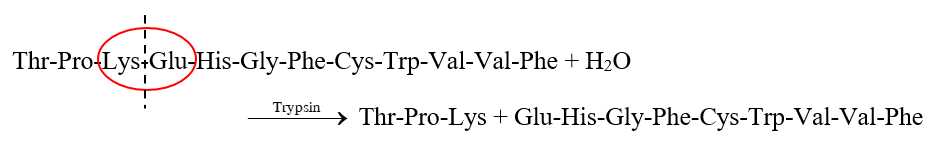
Sản phẩm thu được là Thr–Pro–Lys và Glu–His–Gly–Phe–Cys–Trp–Val–Val–Phe
⇒ Chọn đáp án C Đáp án: C
Câu 13 [705746]: Đồng có độ tinh khiết cao có khả năng dẫn điện tốt, bền về mặt hoá học nên được sử dụng rộng rãi trong các thiết bị điện tử. Đồng có độ tinh khiết cao có thể thu được từ đồng có độ tinh khiết thấp qua quá trình tinh luyện bằng phương pháp điện phân.
∎ Dung dịch chất điện li là dung dịch CuSO4.
∎ Cực dương làm bằng tấm đồng có độ tinh khiết thấp.
∎ Cực âm làm bằng tấm đồng có độ tinh khiết cao.
Nhận định nào sau đây không đúng?
∎ Dung dịch chất điện li là dung dịch CuSO4.
∎ Cực dương làm bằng tấm đồng có độ tinh khiết thấp.
∎ Cực âm làm bằng tấm đồng có độ tinh khiết cao.
Nhận định nào sau đây không đúng?
A, Theo thời gian, khối lượng đồng ở anode giảm dần.
B, Cathode thu được đồng có độ tinh khiết cao.
C, Tổng nồng độ ion Cu2+ trong dung dịch không đổi.
D, Có thể thay dung dịch chất điện li bằng AgNO3.
Phân tích các nhận định:
✔️ A. Đúng. Ở cực dương (anode): Đồng có độ tinh khiết thấp bị oxi hóa thành Cu2+, đi vào dung dịch:
Cu → Cu2+ + 2e
✔️ B. Đúng. Ở cực âm (cathode): Cu2+ trong dung dịch nhận electron và kết tủa thành đồng tinh khiết:
Cu2+ +2e → Cu
Vì chỉ có Cu2+ bị khử nên đồng thu được có độ tinh khiết cao.
✔️ C. Đúng. Số ion Cu2+ bị khử ở cathode đúng bằng số ion Cu2+ sinh ra từ anode. Do đó, nồng độ ion Cu2+ trong dung dịch không đổi.
❌ D. Sai. Nếu thay dung dịch CuSO4 bằng AgNO3 thì:
Anode (đồng) sẽ bị oxi hóa thành Cu2+, không phải Ag+.
Cathode sẽ thu được bạc (Ag), không phải đồng tinh khiết).
⟶ Quá trình này không còn là tinh luyện đồng nữa.
⇒ Chọn đáp án D Đáp án: D
✔️ A. Đúng. Ở cực dương (anode): Đồng có độ tinh khiết thấp bị oxi hóa thành Cu2+, đi vào dung dịch:
Cu → Cu2+ + 2e
✔️ B. Đúng. Ở cực âm (cathode): Cu2+ trong dung dịch nhận electron và kết tủa thành đồng tinh khiết:
Cu2+ +2e → Cu
Vì chỉ có Cu2+ bị khử nên đồng thu được có độ tinh khiết cao.
✔️ C. Đúng. Số ion Cu2+ bị khử ở cathode đúng bằng số ion Cu2+ sinh ra từ anode. Do đó, nồng độ ion Cu2+ trong dung dịch không đổi.
❌ D. Sai. Nếu thay dung dịch CuSO4 bằng AgNO3 thì:
Anode (đồng) sẽ bị oxi hóa thành Cu2+, không phải Ag+.
Cathode sẽ thu được bạc (Ag), không phải đồng tinh khiết).
⟶ Quá trình này không còn là tinh luyện đồng nữa.
⇒ Chọn đáp án D Đáp án: D
Câu 14 [705743]: Chất nào sau đây tác dụng với NaOH theo tỉ lệ mol 1 : 2?
A, 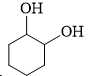

B, 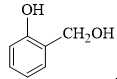

C, 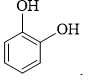

D, 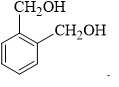

✔️ Nhóm –OH phenol (liên kết với vòng benzen) có tính acid yếu, phản ứng với NaOH tạo muối sodium phenolate.
❌ Nhóm –OH alcohol (liên kết với mạch nhánh hoặc vòng không thơm) không phản ứng với NaOH ở điều kiện thường.
Xét điều kiện phản ứng với NaOH của các chất:
❌ A. Chứa 2 nhóm –OH nhưng không phải phenol → Không phản ứng với NaOH.
❌ B. Chứa 1 nhóm –OH phenol và 1 nhóm –CH2OH → Chỉ có 1 nhóm phản ứng với NaOH → Tỉ lệ 1:1.
✔️ C. Chứa 2 nhóm –OH phenol → Cả hai nhóm phản ứng với NaOH theo tỉ lệ 1:2.
❌ D. Chứa 2 nhóm –CH2OH (không phải phenol) → Không phản ứng với NaOH.
⇒ Chọn đáp án C Đáp án: C
❌ Nhóm –OH alcohol (liên kết với mạch nhánh hoặc vòng không thơm) không phản ứng với NaOH ở điều kiện thường.
Xét điều kiện phản ứng với NaOH của các chất:
❌ A. Chứa 2 nhóm –OH nhưng không phải phenol → Không phản ứng với NaOH.
❌ B. Chứa 1 nhóm –OH phenol và 1 nhóm –CH2OH → Chỉ có 1 nhóm phản ứng với NaOH → Tỉ lệ 1:1.
✔️ C. Chứa 2 nhóm –OH phenol → Cả hai nhóm phản ứng với NaOH theo tỉ lệ 1:2.
❌ D. Chứa 2 nhóm –CH2OH (không phải phenol) → Không phản ứng với NaOH.
⇒ Chọn đáp án C Đáp án: C
Câu 15 [705839]:
Dichloro(ethylenediamine)platinum(II) có công thức PtCl2(en) là một loại bột màu vàng, được sử dụng làm chất xúc tác tiền chất trong công nghiệp và cũng là chất phản ứng bắt đầu cho quá trình mạ điện, một số hợp chất platinum có khả năng chống ung thư.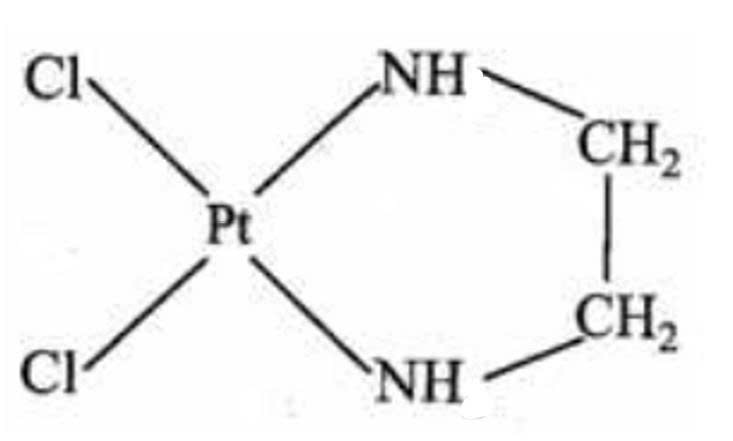
Cho các phát biểu sau:
(a) Điện tích của phức chất bằng 0.
(b) Số liên kết cho – nhận giữa mỗi phối tử với nguyên tử trung tâm là như nhau.
(c) Số oxi hoá của nguyên tử trung tâm trong phức chất là +4.
(d) Tất cả các liên kết trong phức chất đều là liên kết cộng hoá trị.
(e) Theo thuyết liên kết hoá trị, các liên kết quanh nguyên tử trung tâm là liên kết cộng hoá trị theo kiểu cho – nhận.
Số phát biểu đúng là
A, 2.
B, 3.
C, 4.
D, 5.
Phân tích các đáp án:
✔️(a) – Đúng. Điện tích của phức chất bằng 0. Nguyên tử trung tâm Pt có điện tích là 2+ và có 2 phối tử Cl- và phối tử trung hòa H2NCH2CH2NH2.
❌(b) – Sai. Mỗi phối tử có số dung lượng phối trí khác nhau Cl- có dung lượng phối trí là 1 nên có 1 liên kết với ion nguyên tử trung tâm và H2NCH2CH2NH2 có dung lượng phối trí là 2 nên có 2 liên kết với ion nguyên tử trung tâm
❌(c) – Sai. Số oxi hoá của nguyên tử trung tâm trong phức chất là +2.
✔️(d) – Đúng. Liên kết trong phức chất là liên kết cho – nhận (trường hợp của liên kết cộng hóa trị) nên phân tử hoặc anion cần có cặp electron hóa trị riêng.
✔️(e) – Đúng. Theo thuyết liên kết hoá trị, các liên kết quanh nguyên tử trung tâm là liên kết cộng hoá trị theo kiểu cho – nhận.
Có 3 nhận định đúng.
⟹ Chọn đáp án B Đáp án: B
✔️(a) – Đúng. Điện tích của phức chất bằng 0. Nguyên tử trung tâm Pt có điện tích là 2+ và có 2 phối tử Cl- và phối tử trung hòa H2NCH2CH2NH2.
❌(b) – Sai. Mỗi phối tử có số dung lượng phối trí khác nhau Cl- có dung lượng phối trí là 1 nên có 1 liên kết với ion nguyên tử trung tâm và H2NCH2CH2NH2 có dung lượng phối trí là 2 nên có 2 liên kết với ion nguyên tử trung tâm
❌(c) – Sai. Số oxi hoá của nguyên tử trung tâm trong phức chất là +2.
✔️(d) – Đúng. Liên kết trong phức chất là liên kết cho – nhận (trường hợp của liên kết cộng hóa trị) nên phân tử hoặc anion cần có cặp electron hóa trị riêng.
✔️(e) – Đúng. Theo thuyết liên kết hoá trị, các liên kết quanh nguyên tử trung tâm là liên kết cộng hoá trị theo kiểu cho – nhận.
Có 3 nhận định đúng.
⟹ Chọn đáp án B Đáp án: B
Sử dụng thông tin cho dưới đây để trả lời các câu số 16 – 17:
TTrong các nghiên cứu ban đầu, người ta quan sát thấy rằng khi phức chất [Co(NH3)4Br2]Br
được đặt trong nước, độ dẫn điện của dung dịch với nồng độ phức chất 0,05 M thay đổi gia tăng
từ giá trị ban đầu là 191 ohm–1
thành giá trị cuối cùng là 374 ohm–1
trong khoảng thời gian
khoảng một giờ.
Câu 16 [703970]: Viết phương trình hóa học mô tả cho hiện tượng trên là
A, [Co(NH3)4Br2]Br(aq) 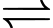 [Co(NH3)4Br2]+(aq) + Br–(aq).
[Co(NH3)4Br2]+(aq) + Br–(aq).
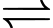 [Co(NH3)4Br2]+(aq) + Br–(aq).
[Co(NH3)4Br2]+(aq) + Br–(aq).B, [Co(NH3)4Br2]Br(aq) 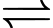 [Co(NH3)4Br]2+(aq) + 2Br–(aq).
[Co(NH3)4Br]2+(aq) + 2Br–(aq).
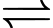 [Co(NH3)4Br]2+(aq) + 2Br–(aq).
[Co(NH3)4Br]2+(aq) + 2Br–(aq).C, [Co(NH3)4Br2]Br(aq) 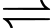 [Co(NH3)4]3+(aq) + 3Br–(aq).
[Co(NH3)4]3+(aq) + 3Br–(aq).
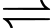 [Co(NH3)4]3+(aq) + 3Br–(aq).
[Co(NH3)4]3+(aq) + 3Br–(aq).D, [Co(NH3)4Br2]Br(aq) 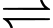 [CoBr3](aq) + 4NH3(aq).
[CoBr3](aq) + 4NH3(aq).
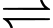 [CoBr3](aq) + 4NH3(aq).
[CoBr3](aq) + 4NH3(aq).
[Co(NH3)4Br2]Br(aq) ⇌ Co(NH3)4Br2]+(aq) + Br-(aq)
Sau 1 giờ phương trình phân li đặt trạng thái cân bằng nên sẽ có thêm nhiều ion trong dung dịch dẫn đến độ dẫn điện tăng.
⇒ Chọn đáp án A Đáp án: A
Sau 1 giờ phương trình phân li đặt trạng thái cân bằng nên sẽ có thêm nhiều ion trong dung dịch dẫn đến độ dẫn điện tăng.
⇒ Chọn đáp án A Đáp án: A
Câu 17 [703971]: Một dung dịch 500 mL được tạo thành bằng cách hòa tan 3,67 gam phức chất. Lấy 25,00 mL dung dịch, chuẩn độ bằng dung dịch AgNO3 0,01 M. Thể tích dung dịch dung dịch AgNO3 để kết tủa Br– tự do là bao nhiêu? Biết nguyên tử khối của Co là 59 g/mol.
A, 50 mL.
B, 25 mL.
C, 10 mL.
D, 5 mL.
Đổi 500 mL = 0,5 L; 25 mL = 0,025 L
Số mol của [Co(NH3)4Br2]Br trong 500 mL là:
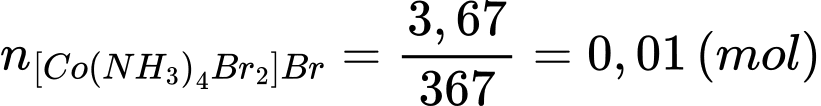
Số mol của [Co(NH3)4Br2]Br trong 25 mL là:
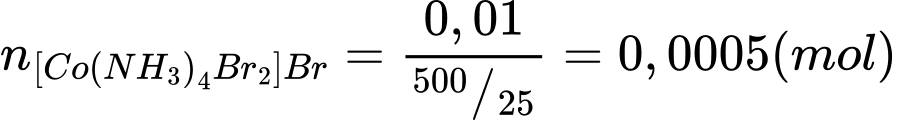
AgNO3 + [Co(NH3)4Br2]Br ⟶ AgBr↓ + [Co(NH3)4Br2]NO3
Thể tích dung dịch AgNO3 đã dùng là:
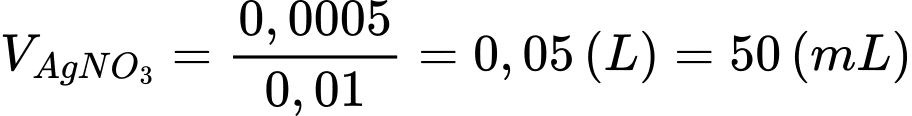
⇒ Chọn đáp án A Đáp án: A
Số mol của [Co(NH3)4Br2]Br trong 500 mL là:
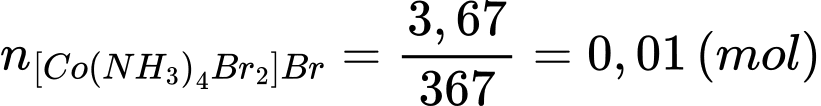
Số mol của [Co(NH3)4Br2]Br trong 25 mL là:
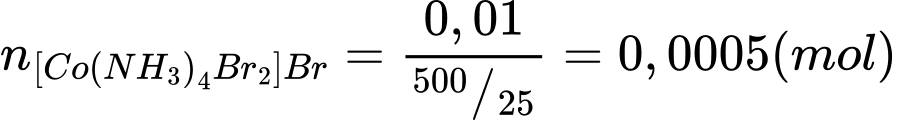
AgNO3 + [Co(NH3)4Br2]Br ⟶ AgBr↓ + [Co(NH3)4Br2]NO3
Thể tích dung dịch AgNO3 đã dùng là:
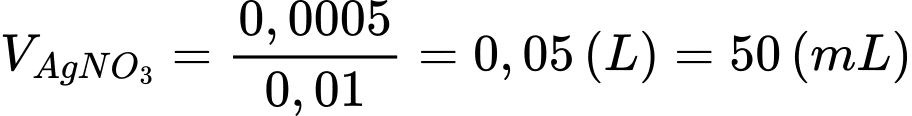
⇒ Chọn đáp án A Đáp án: A
Câu 18 [705832]: Cho phản ứng thuận nghịch: H2(g) + I2(g) ⇌ 2HI(g). Nồng độ tại thời điểm cân bằng của I2 và H2 chỉ bằng nhau khi
A, Nồng độ ban đầu của I2 và H2 bằng nhau.
B, Khối lượng ban đầu của I2 và H2 bằng nhau.
C, Số mol I2 và H2 phản ứng bằng nhau.
D, Tốc độ phản ứng thuận gấp hai lần phản ứng nghịch.
Tỉ lệ phản ứng giữa I2 và H2 là 1:1 nên nồng độ chất mất đi của H2 và I2 là như nhau nên nồng độ ban đầu của H2 và I2 phải bằng nhau thì nồng độ tại cân bằng của I2 và H2 tại cân bằng sẽ bằng nhau.
Chọn đáp án A Đáp án: A
Chọn đáp án A Đáp án: A
PHẦN II. Thí sinh trả lời từ câu 1 đến câu 4. Trong mỗi ý a), b), c), d) ở mỗi câu, thí sinh chọn đúng hoặc sai.
Câu 19 [705753]: Trong bình có dung tích không đổi 1 Lít, ban đầu nạp vào bình hỗn hợp gồm 0,9 mol chất A và 0,6 mol chất B. Giữ nhiệt độ ổn định ở 760 °C, xảy ra cân bằng hóa học:
Sau khi phản ứng đạt trạng thái cân bằng, tiến hành tăng nhiệt độ của bình phản ứng thì thấy số mol khí trong bình tăng lên.
aA(g) + bB(g) ⇌ cC(g) + dD(g)
(a, b, c, d là các hệ số nguyên, tối giản của phản ứng;
biểu thức tính tốc độ phản ứng tuân theo định luật tác dụng khối lượng)
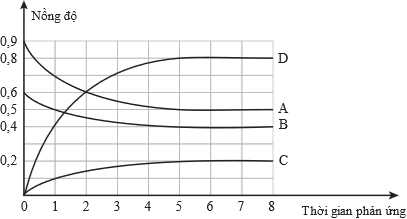
Sau 6 phút, phản ứng đạt tới trạng thái cân bằng. Sự phụ thuộc nồng độ mol/L của các chất trong bình phản ứng vào thời gian (phút) được biểu diễn bằng đồ thị sau:
Sau khi phản ứng đạt trạng thái cân bằng, tiến hành tăng nhiệt độ của bình phản ứng thì thấy số mol khí trong bình tăng lên.
Phân tích các phát biểu:
❌ (a) Sai. Trước thời điểm cân bằng, tốc độ phản ứng nghịch tăng dần theo thời gian do nồng độ sản phẩm tăng lên; tốc độ phản ứng thuận giảm dần theo thời gian do nồng độ sản phẩm giảm xuống.
✔️ (b) Đúng. Hoàn toàn có thể dựa vào sự thay đổi nồng độ của chất phản ứng (hoặc chất sản phẩm) trong một đơn vị thời gian để đánh giá mức độ nhanh, chậm của phản ứng và xác định chất tham gia, chất sản phẩm.
✔️ (c) Đúng.
Nồng độ của các chất A và B tại thời điểm ban đầu lần lượt là 0,9 M và 0,6 M.
Nồng độ của các chất A, B, C, D tại thời điểm cân bằng lần lượt là 0,5 M; 0,4 M; 0,2 M; 0,8 M.
Lượng chất A, B tham gian phản ứng lần lượt là 0,9 – 0,5 = 0,4 M; 0,6 – 0,4 = 0,2 M.
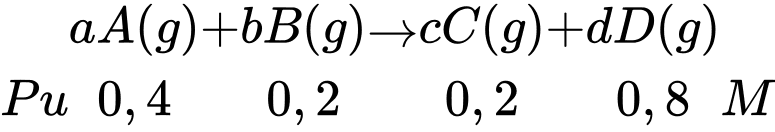
Tỉ lệ nồng độ các chất A, B, C, D là a:b:c:d = 0,4:0,2:0,2:0,8 = 2:1:1:4
→ Phương trình hóa học có dạng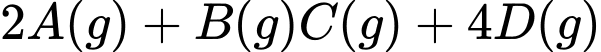
Hằng số cân bằng của phản ứng là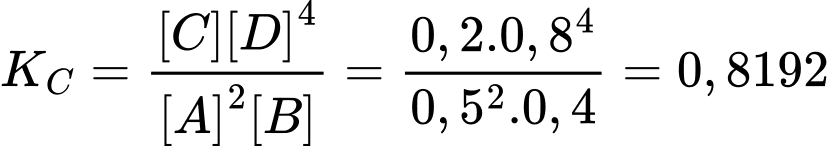
❌ (d) Sai.
Tổng nồng độ khí trước phản ứng là 0,9 + 0,6 = 1,5 M
Tổng nồng độ khi sau phản ứng là 0,5 + 0,4 + 0,2 + 0,8 = 1,9 M
Nồng độ khí sau phản ứng tăng lên chứng tỏ khi tăng nhiệt độ tại thời điểm cân bằng thì cân bằng chuẩn dịch theo chiều thuận → phản ứng trên là phản ứng thu nhiệt.
❌ (a) Sai. Trước thời điểm cân bằng, tốc độ phản ứng nghịch tăng dần theo thời gian do nồng độ sản phẩm tăng lên; tốc độ phản ứng thuận giảm dần theo thời gian do nồng độ sản phẩm giảm xuống.
✔️ (b) Đúng. Hoàn toàn có thể dựa vào sự thay đổi nồng độ của chất phản ứng (hoặc chất sản phẩm) trong một đơn vị thời gian để đánh giá mức độ nhanh, chậm của phản ứng và xác định chất tham gia, chất sản phẩm.
✔️ (c) Đúng.
Nồng độ của các chất A và B tại thời điểm ban đầu lần lượt là 0,9 M và 0,6 M.
Nồng độ của các chất A, B, C, D tại thời điểm cân bằng lần lượt là 0,5 M; 0,4 M; 0,2 M; 0,8 M.
Lượng chất A, B tham gian phản ứng lần lượt là 0,9 – 0,5 = 0,4 M; 0,6 – 0,4 = 0,2 M.
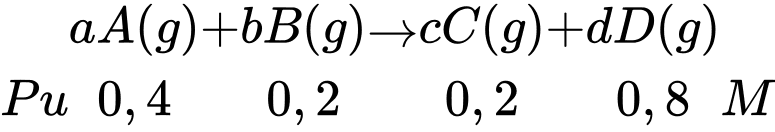
Tỉ lệ nồng độ các chất A, B, C, D là a:b:c:d = 0,4:0,2:0,2:0,8 = 2:1:1:4
→ Phương trình hóa học có dạng
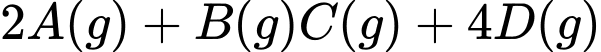
Hằng số cân bằng của phản ứng là
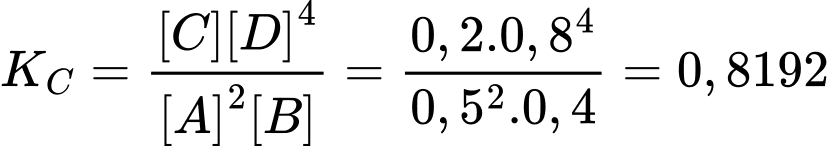
❌ (d) Sai.
Tổng nồng độ khí trước phản ứng là 0,9 + 0,6 = 1,5 M
Tổng nồng độ khi sau phản ứng là 0,5 + 0,4 + 0,2 + 0,8 = 1,9 M
Nồng độ khí sau phản ứng tăng lên chứng tỏ khi tăng nhiệt độ tại thời điểm cân bằng thì cân bằng chuẩn dịch theo chiều thuận → phản ứng trên là phản ứng thu nhiệt.
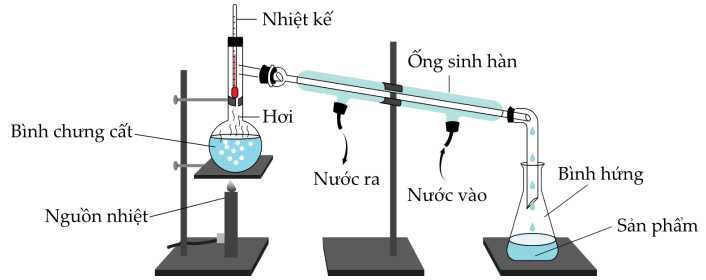
Câu 20 [705845]: Các loại ngũ cốc lên men có thể tạo ra hàm lượng cồn tối đa khoảng 16 %, đây là giới hạn của hầu hết các loại bia và rượu vang, vì sinh vật nấm men được sử dụng không thể tồn tại trong các dung dịch rượu đặc hơn. Tuy nhiên, các loại rượu mạnh thường có hàm lượng cồn khoảng 40 % theo thể tích. Chưng cất là phương pháp được sử dụng để cô đặc dung dịch lên men và sản xuất rượu mạnh.
Quá trình chưng cất rượu vang đỏ có thể được chứng minh là đã cô đặc hơn so với được rượu ban đầu thông qua thử nghiệm ngọn lửa. Vào thế kỉ 16 khi rượu là một mặt hàng trao đổi, nó thường xuyên được thử nghiệm để đảm bảo rằng không bị pha loãng. Một mẫu rượu 57 % theo thể tích có khả năng bắt lửa, trong khi các dung dịch loãng hơn thì không.

Quá trình chưng cất rượu vang đỏ có thể được chứng minh là đã cô đặc hơn so với được rượu ban đầu thông qua thử nghiệm ngọn lửa. Vào thế kỉ 16 khi rượu là một mặt hàng trao đổi, nó thường xuyên được thử nghiệm để đảm bảo rằng không bị pha loãng. Một mẫu rượu 57 % theo thể tích có khả năng bắt lửa, trong khi các dung dịch loãng hơn thì không.
Phân tích các đáp án:
❌A. Sai. Nhiệt độ của quá trình chưng cất được duy trì ở 80 oC. Nếu đun đến 100 oC thì sẽ kéo thêm hơi nước chất thu được theo chưng cất không tinh khiết.
✔️B. Đúng. Nhiệt độ sôi của rượu là 78,37 oC thấp hơn của nước 100 oC
❌C. Sai. Quá trình chưng cất có thể làm giảm hàm lượng rượu trong bình chưng cất nguyên do rượu bị bay hơi và ngưng tụ trong bình hứng.
✔️D. Đúng.Các kho chứa rượu mạnh có nguy cơ xảy ra hoả hoạn do hàm lượng rượu cao có khả năng bắt lửa. Một mẫu rượu 57% theo thể tích có khả năng bắt lửa, trong khi các dung dịch loãng hơn thì không.
❌A. Sai. Nhiệt độ của quá trình chưng cất được duy trì ở 80 oC. Nếu đun đến 100 oC thì sẽ kéo thêm hơi nước chất thu được theo chưng cất không tinh khiết.
✔️B. Đúng. Nhiệt độ sôi của rượu là 78,37 oC thấp hơn của nước 100 oC
❌C. Sai. Quá trình chưng cất có thể làm giảm hàm lượng rượu trong bình chưng cất nguyên do rượu bị bay hơi và ngưng tụ trong bình hứng.
✔️D. Đúng.Các kho chứa rượu mạnh có nguy cơ xảy ra hoả hoạn do hàm lượng rượu cao có khả năng bắt lửa. Một mẫu rượu 57% theo thể tích có khả năng bắt lửa, trong khi các dung dịch loãng hơn thì không.
Câu 21 [702842]: Một ống nghiệm chứa 1 mL dung dịch copper(II) sulfate 0,5 % màu xanh nhạt. Trong dung dịch, ion Cu2+ tạo phức chất với phối tử aqua ở dạng bát diện. Thêm từ từ cho đến hết 2 mL dung dịch hydrochloric acid đặc không màu vào ống nghiệm đó thì thu được dung dịch có màu vàng chanh của phức chất mới (là phức chất tứ diện của Cu2+ với phối tử Cl– có dạng [Cu(Cl)n]2–n).
Phân tích các phát biểu:
❌ a) Sai. Phức chất của Cu2+ với aqua [Cu(H2O)6]2+ có điện tích +2, do phối tử aqua không mang điện.
✔️ b) Đúng. Trong phức chất của [Cu(Cl)n]2–n, giá trị của n là 4.
✔️ c) Đúng. Trong quá trình chuyển đổi giữa các phức, không có sự thay đổi số oxi hoá của các nguyên tố.
✔️ d) Đúng. Trong điều kiện của thí nghiệm, phức chất của Cu2+ với aqua kém bền hơn phức chất của Cu2+ với Cl– do Cl– là một phối tử có khả năng tạo liên kết phối trí mạnh hơn aqua và phức [CuCl4]2− có năng lượng bền hoá cao hơn do sự tương tác mạnh giữa Cu2+ và Cl−.
❌ a) Sai. Phức chất của Cu2+ với aqua [Cu(H2O)6]2+ có điện tích +2, do phối tử aqua không mang điện.
✔️ b) Đúng. Trong phức chất của [Cu(Cl)n]2–n, giá trị của n là 4.
[Cu(H2O)6]2+(aq) + 4Cl-(aq) → [CuCl4]2-(aq) + 6H2O(l)
✔️ c) Đúng. Trong quá trình chuyển đổi giữa các phức, không có sự thay đổi số oxi hoá của các nguyên tố.
✔️ d) Đúng. Trong điều kiện của thí nghiệm, phức chất của Cu2+ với aqua kém bền hơn phức chất của Cu2+ với Cl– do Cl– là một phối tử có khả năng tạo liên kết phối trí mạnh hơn aqua và phức [CuCl4]2− có năng lượng bền hoá cao hơn do sự tương tác mạnh giữa Cu2+ và Cl−.
Câu 22 [703953]: Phản ứng giữa potassium permanganate (KMnO4) và iron(II) sulfate (FeSO4) được acid hóa là phản ứng oxy hóa khử diễn ra như sau:
8H+(aq) + 5Fe2+(aq) + MnO4–(aq) Mn2+(aq) + 5Fe3+(aq) + 4H2O(l)
Mn2+(aq) + 5Fe3+(aq) + 4H2O(l)
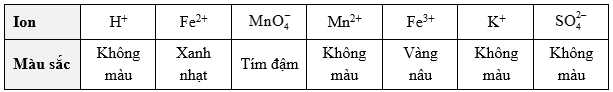
Một dung dịch KMnO4 0,20 M được đặt trong buret để chuẩn độ 50,00 mL dung dịch FeSO4 có nồng độ chưa biết trong một bình tam giác. Bảng sau đây mô tả màu sắc của các ion khác nhau trong dung dịch:
Kết thúc chuẩn độ thì thể tích dung dịch KMnO4 0,20 M đã sử dụng là 12,5 mL.
8H+(aq) + 5Fe2+(aq) + MnO4–(aq)
 Mn2+(aq) + 5Fe3+(aq) + 4H2O(l)
Mn2+(aq) + 5Fe3+(aq) + 4H2O(l)Một dung dịch KMnO4 0,20 M được đặt trong buret để chuẩn độ 50,00 mL dung dịch FeSO4 có nồng độ chưa biết trong một bình tam giác. Bảng sau đây mô tả màu sắc của các ion khác nhau trong dung dịch:

Kết thúc chuẩn độ thì thể tích dung dịch KMnO4 0,20 M đã sử dụng là 12,5 mL.
Đổi 12,5 mL = 0,0125 L; 50 mL = 0,05 L
10FeSO4 + 2KMnO4 + 8H2SO4 ⟶ 5Fe2(SO4)3 + K2SO4 + 2MnSO4 + 8H2O
Số mol của KMnO4 là 0,0125.0,2 = 0,0025 (mol)
Từ PTHH số mol FeSO4 phản ứng là 0,0125 (mol) →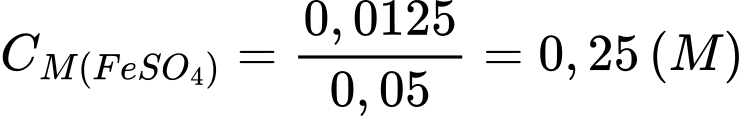
Phân tích các phát biểu:
✔️ a) Đúng. Nồng độ dung dịch FeSO4 trong bình tam giác là 0,25 M.
❌ b) Sai. Tại điểm tương đương, dung dịch chứa các ion Fe3+, Mn2+ được tạo thành và các ion ban đầu không tham gia phản ứng là K+ và SO42-.
❌ c) Sai. Tại điểm tương đương, màu của dung dịch chuyển sang màu vàng nâu, khi đó dung dịch trước phản ứng có màu xanh nhạt của Fe2+ chuyển sang màu vàng nâu của Fe3+.
❌ d) Sai. Nồng độ theo lý thuyết (50mL) của FeSO4 là 0,25M.
Nồng độ thực tế của FeSO4 khi lỗi kĩ thuật xảy ra là:
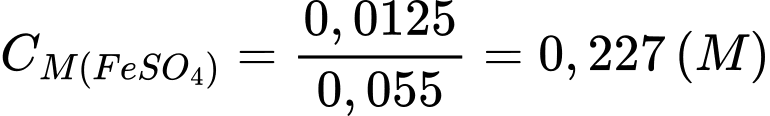
⇒ Khi thể tích dung dịch FeSO4 được thêm vào bình là 55,00 mL thay vì 50,00 mL thì kết quả tính nồng độ FeSO4 (0,25 M)sẽ lớn hơn so với thực tế (0,227 M).
10FeSO4 + 2KMnO4 + 8H2SO4 ⟶ 5Fe2(SO4)3 + K2SO4 + 2MnSO4 + 8H2O
Số mol của KMnO4 là 0,0125.0,2 = 0,0025 (mol)
Từ PTHH số mol FeSO4 phản ứng là 0,0125 (mol) →
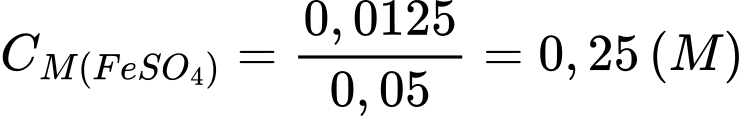
Phân tích các phát biểu:
✔️ a) Đúng. Nồng độ dung dịch FeSO4 trong bình tam giác là 0,25 M.
❌ b) Sai. Tại điểm tương đương, dung dịch chứa các ion Fe3+, Mn2+ được tạo thành và các ion ban đầu không tham gia phản ứng là K+ và SO42-.
❌ c) Sai. Tại điểm tương đương, màu của dung dịch chuyển sang màu vàng nâu, khi đó dung dịch trước phản ứng có màu xanh nhạt của Fe2+ chuyển sang màu vàng nâu của Fe3+.
❌ d) Sai. Nồng độ theo lý thuyết (50mL) của FeSO4 là 0,25M.
Nồng độ thực tế của FeSO4 khi lỗi kĩ thuật xảy ra là:
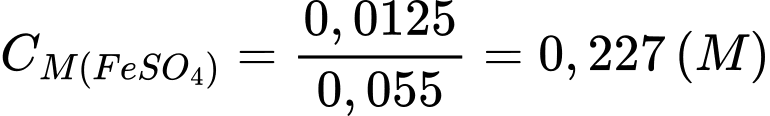
⇒ Khi thể tích dung dịch FeSO4 được thêm vào bình là 55,00 mL thay vì 50,00 mL thì kết quả tính nồng độ FeSO4 (0,25 M)sẽ lớn hơn so với thực tế (0,227 M).
PHẦN III. Thí sinh trả lời từ câu 1 đến 6. Thí sinh điền kết quả mỗi câu vào mỗi ô trả lời tương ứng theo hướng dẫn của phiếu trả lời.
Câu 23 [702821]: Quy trình sản xuất đồng (Cu) từ quặng chứa Cu2S được thực hiện như sau:
Giai đoạn 1: Đốt Cu2S bằng khí oxygen theo phản ứng:
2Cu2S + 3O2 2Cu2O + 2SO2.
2Cu2O + 2SO2.
Giai đoạn 2: Copper(I) oxide sẽ phản ứng với phần còn lại của Cu2S theo phản ứng:
2Cu2O + Cu2S 6Cu + SO2.
6Cu + SO2.
Quặng đồng ban đầu chứa khoảng 40% Cu2S theo khối lượng. Tính khối lượng quặng đồng (theo tấn) cần lấy để điều chế được 1 tấn Cu. Biết hiệu suất của quá trình đạt 90% (làm tròn kết quả đến hàng phần trăm).
Giai đoạn 1: Đốt Cu2S bằng khí oxygen theo phản ứng:
2Cu2S + 3O2
 2Cu2O + 2SO2.
2Cu2O + 2SO2.Giai đoạn 2: Copper(I) oxide sẽ phản ứng với phần còn lại của Cu2S theo phản ứng:
2Cu2O + Cu2S
 6Cu + SO2.
6Cu + SO2.Quặng đồng ban đầu chứa khoảng 40% Cu2S theo khối lượng. Tính khối lượng quặng đồng (theo tấn) cần lấy để điều chế được 1 tấn Cu. Biết hiệu suất của quá trình đạt 90% (làm tròn kết quả đến hàng phần trăm).
Đổi 1 tấn = 1000000 gam
Số mol của Cu là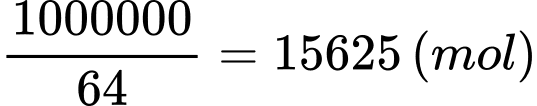
Bảo toàn nguyên tố Cu: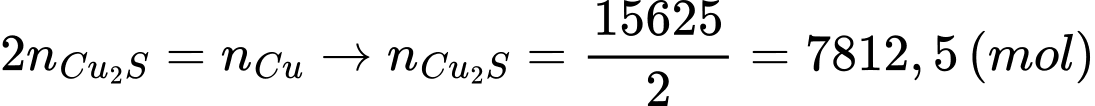
Khối lượng của quặng ban đầu: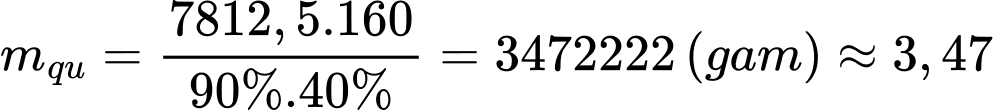 (tấn)
(tấn)
⇒ Điền đáp án: 3,47
Số mol của Cu là
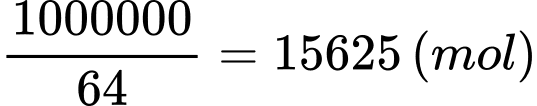
Bảo toàn nguyên tố Cu:
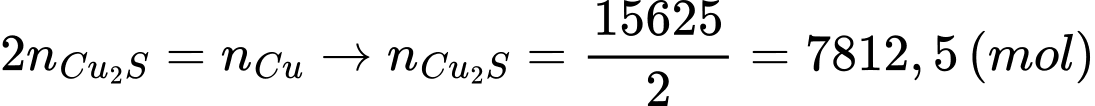
Khối lượng của quặng ban đầu:
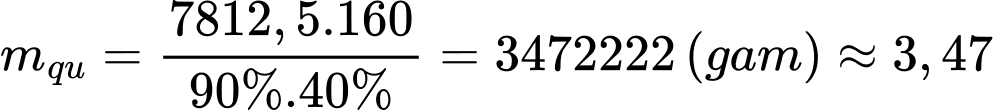 (tấn)
(tấn)⇒ Điền đáp án: 3,47
Câu 24 [704361]: Thủy phân hoàn toàn 1 mol peptide X có cấu tạo Gly-Ala-Lys-Val trong môi trường NaOH thì đã có bao nhiêu mol NaOH phản ứng?
★ Khi thủy phân hoàn toàn peptide X (Gly-Ala-Lys-Val) trong môi trường NaOH, các liên kết peptide bị phá vỡ, đồng thời các nhóm chức cần được trung hòa:
+) Liên kết peptide: Peptide X có 4 amino acid được nối với nhau bởi 3 liên kết peptide. Mỗi liên kết peptide cần 1 mol NaOH để bị thủy phân nên cần 3 mol NaOH cho 3 liên kết peptide
+) Nhóm chức acid amin cần trung hòa: Lysine có nhóm NH2 ở mạch nhánh, nhóm này cũng cần 1 mol NaOH để trung hòa.
★ Phương trình hoá học xảy ra như sau:
Gly-Ala-Lys-Val + 4NaOH ⟶ Gly-Na + Ala-Na + Lys-Na + Val-Na + H2O
⟶ Thủy phân 1 mol peptide Gly-Ala-Lys-Val cần 4 mol NaOH.
⇒ Điền đáp án: 4
+) Liên kết peptide: Peptide X có 4 amino acid được nối với nhau bởi 3 liên kết peptide. Mỗi liên kết peptide cần 1 mol NaOH để bị thủy phân nên cần 3 mol NaOH cho 3 liên kết peptide
+) Nhóm chức acid amin cần trung hòa: Lysine có nhóm NH2 ở mạch nhánh, nhóm này cũng cần 1 mol NaOH để trung hòa.
★ Phương trình hoá học xảy ra như sau:
Gly-Ala-Lys-Val + 4NaOH ⟶ Gly-Na + Ala-Na + Lys-Na + Val-Na + H2O
⟶ Thủy phân 1 mol peptide Gly-Ala-Lys-Val cần 4 mol NaOH.
⇒ Điền đáp án: 4
Câu 25 [704381]: Methyl salicylate dùng làm thuốc xoa bóp giảm đau, được điều chế theo phản ứng sau:
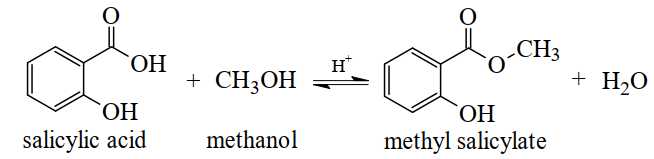
Để sản xuất 1,9 triệu tuýp thuốc xoa bóp giảm đau cần tối thiểu m tấn salicylic acid. Biết mỗi tuýp thuốc chứa 2,7 gam methyl salicylate và hiệu suất phản ứng tính theo salicylic acid là 75%. Giá trị của m là bao nhiêu?
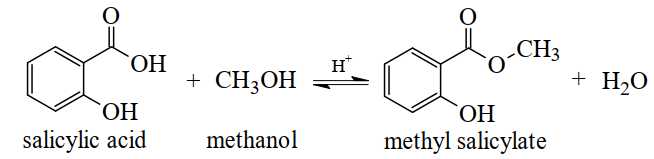
Để sản xuất 1,9 triệu tuýp thuốc xoa bóp giảm đau cần tối thiểu m tấn salicylic acid. Biết mỗi tuýp thuốc chứa 2,7 gam methyl salicylate và hiệu suất phản ứng tính theo salicylic acid là 75%. Giá trị của m là bao nhiêu?
Khối lượng methyl salicylate có trong 1,9 triệu tuýp thuốc xoa bóp giảm đau đau là:
1,9.106.2,7 = 5130000 gam = 5,13 tấn
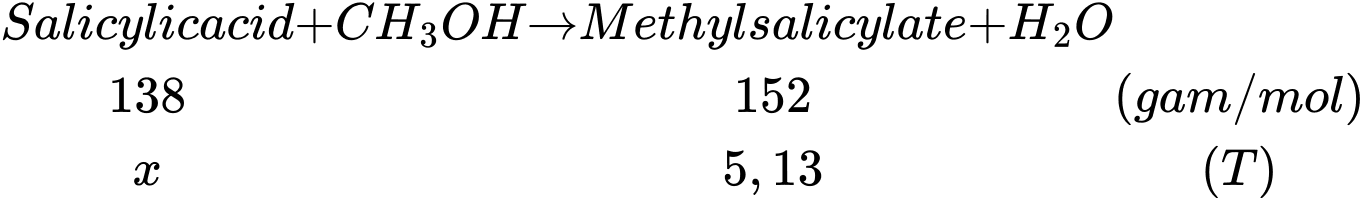
Khối lượng salicylic acid cần dùng là:
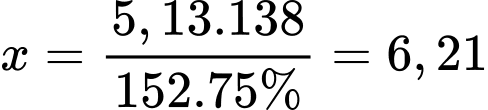 (tấn)
(tấn)
⇒ Điền đáp án: 6,21
1,9.106.2,7 = 5130000 gam = 5,13 tấn
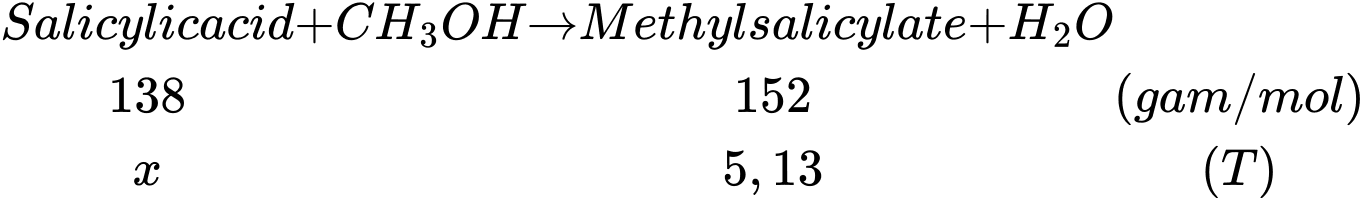
Khối lượng salicylic acid cần dùng là:
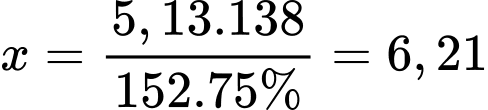 (tấn)
(tấn)⇒ Điền đáp án: 6,21
Câu 26 [704402]: Khi hoà tan hợp chất AgNO3 vào nước thì cation kim loại tồn tại trong dung dịch sẽ tạo thành phức chất aqua dạng tứ diện [Ag(OH2)m]+. Xác định số phối tử aqua (m) trong phức chất [Ag(OH2)m]+.
- Trong dung dịch, khi hòa tan hợp chất AgNO3 vào nước, ion Ag+ sẽ tương tác với phân tử nước để tạo thành phức chất aqua. Phức này có công thức là [Ag(H2O)m]+, trong đó m là số phân tử nước (phối tử aqua) gắn kết với ion Ag+.
- Ion bạc Ag+ có cấu trúc điện tử là [Kr]4d10 có thể tạo thành phức chất với các phân tử nước, với số phối tử (m) thường là 2 hoặc 4 trong trường hợp này.
- Đối với ion Ag+ trong dung dịch, nó có thể tạo ra phức tứ diện với 4 phân tử nước, tức là m = 4. Điều này xảy ra vì ion Ag+ có kích thước nhỏ và điện tích dương cao, có khả năng hút chặt các phân tử nước, tạo thành phức tứ diện ổn định. Do đó, số phối tử aqua (m) trong phức chất [Ag(H2O)m]+ là 4.
⇒ Điền đáp án: 4
- Ion bạc Ag+ có cấu trúc điện tử là [Kr]4d10 có thể tạo thành phức chất với các phân tử nước, với số phối tử (m) thường là 2 hoặc 4 trong trường hợp này.
- Đối với ion Ag+ trong dung dịch, nó có thể tạo ra phức tứ diện với 4 phân tử nước, tức là m = 4. Điều này xảy ra vì ion Ag+ có kích thước nhỏ và điện tích dương cao, có khả năng hút chặt các phân tử nước, tạo thành phức tứ diện ổn định. Do đó, số phối tử aqua (m) trong phức chất [Ag(H2O)m]+ là 4.
⇒ Điền đáp án: 4
Câu 27 [704362]: Trong một nhà máy sản xuất ammonia theo quy trình Haber, giai đoạn sản xuất khí hydrogen bằng phản ứng của methane và nước được thực hiện theo phương trình hóa học (1) như sau:
(1) CH4(g) + H2O(g)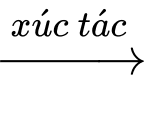 CO(g) + 3H2(g)
CO(g) + 3H2(g)
Phản ứng (1) là phản ứng thu nhiệt mạnh. Lượng nhiệt này được cung cấp từ quá trình đốt cháy hoàn toàn khí methane theo phương trình hóa học (2):
(2) CH4(g) + 2O2(g) → CO2(g) + 2H2O(g)
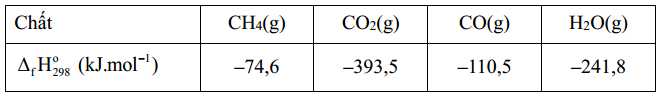
Xét các phản ứng ở điều kiện chuẩn và hiệu suất chuyển hóa của methane là 100 %. Tính khối lượng khí methane (theo tấn, làm tròn đến hàng phần trăm) cần thiết để sản xuất 0,30 tấn H2(g) trong giai đoạn trên. Biết 90 % lượng nhiệt tỏa ra từ phản ứng (2) được cung cấp cho phản ứng (1) và các giá trị nhiệt tạo thành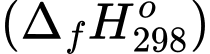 của các chất ở điều kiện chuẩn được cho trong bảng sau:
của các chất ở điều kiện chuẩn được cho trong bảng sau:
(1) CH4(g) + H2O(g)
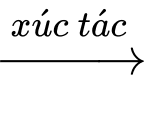 CO(g) + 3H2(g)
CO(g) + 3H2(g)Phản ứng (1) là phản ứng thu nhiệt mạnh. Lượng nhiệt này được cung cấp từ quá trình đốt cháy hoàn toàn khí methane theo phương trình hóa học (2):
(2) CH4(g) + 2O2(g) → CO2(g) + 2H2O(g)
Xét các phản ứng ở điều kiện chuẩn và hiệu suất chuyển hóa của methane là 100 %. Tính khối lượng khí methane (theo tấn, làm tròn đến hàng phần trăm) cần thiết để sản xuất 0,30 tấn H2(g) trong giai đoạn trên. Biết 90 % lượng nhiệt tỏa ra từ phản ứng (2) được cung cấp cho phản ứng (1) và các giá trị nhiệt tạo thành
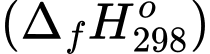 của các chất ở điều kiện chuẩn được cho trong bảng sau:
của các chất ở điều kiện chuẩn được cho trong bảng sau:
(1) 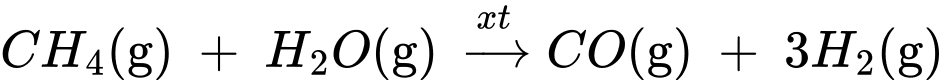
(2)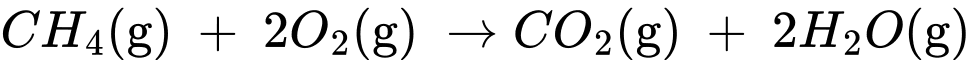
+) Biến thiên enthalpy của phản ứng (1) là:
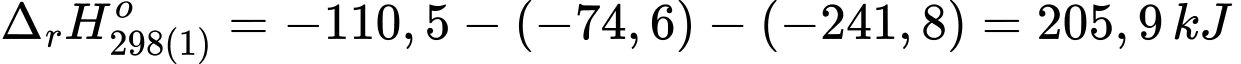
+) Biến thiên enthalpy của phản ứng (2) là:
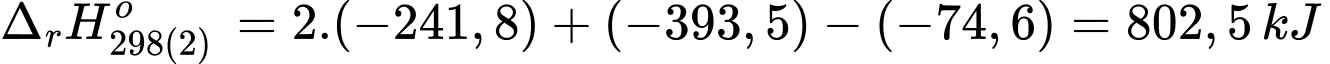
Đổi 0,3 tấn = 0,3.106 gam
+) Số mol của H2 là: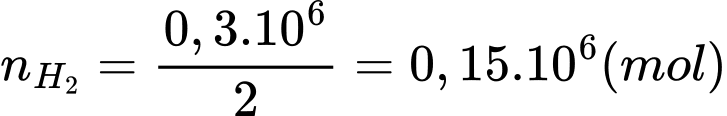
+)Lượng nhiệt thu vào của phản ứng (1) khi điều chế 0,3 tấn hydrogen là:
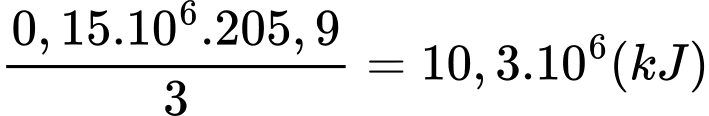
+) Lượng nhiệt toả ra của phản ứng (2) là:
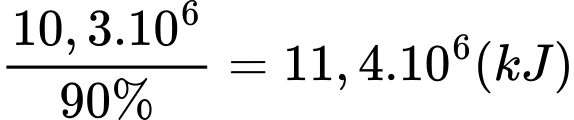
+) Số mol khí methane phản ứng (2) là:
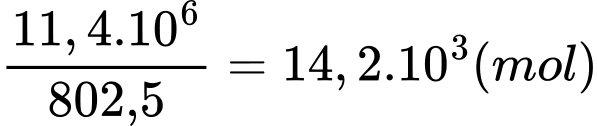
+) Khối lượng khí methane ở phản ứng (1) và (2) là:
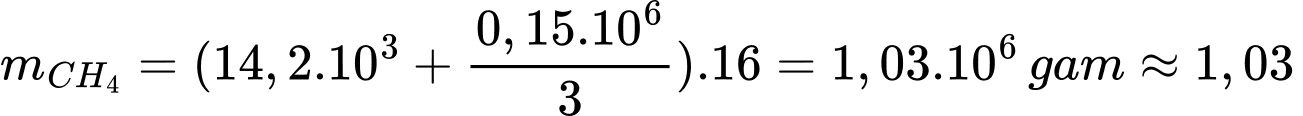 (tấn)
(tấn)
⇒ Điền đáp án: 1,03
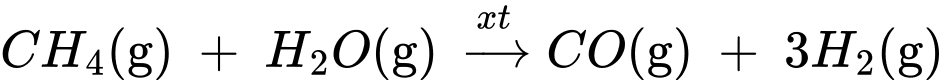
(2)
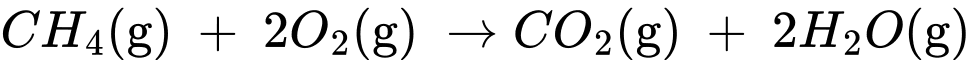
+) Biến thiên enthalpy của phản ứng (1) là:
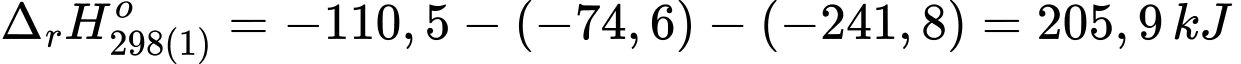
+) Biến thiên enthalpy của phản ứng (2) là:
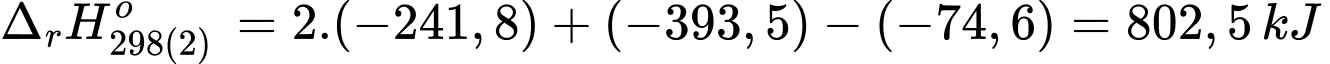
Đổi 0,3 tấn = 0,3.106 gam
+) Số mol của H2 là:
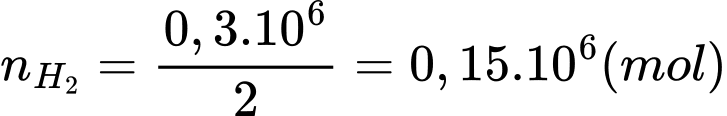
+)Lượng nhiệt thu vào của phản ứng (1) khi điều chế 0,3 tấn hydrogen là:
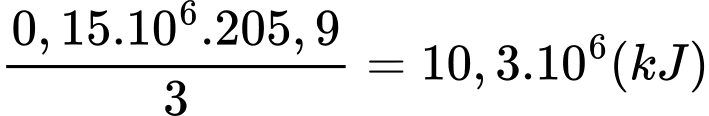
+) Lượng nhiệt toả ra của phản ứng (2) là:
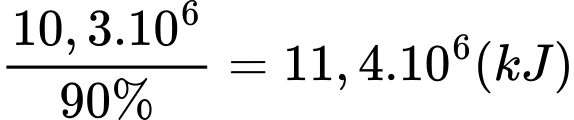
+) Số mol khí methane phản ứng (2) là:
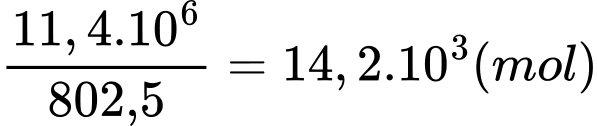
+) Khối lượng khí methane ở phản ứng (1) và (2) là:
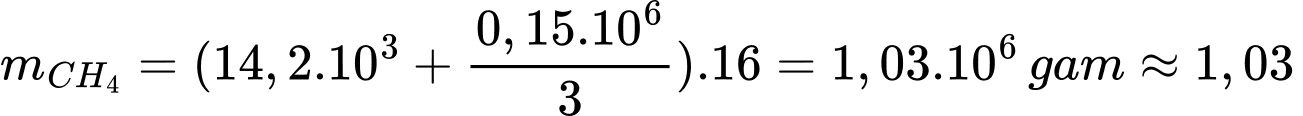 (tấn)
(tấn)⇒ Điền đáp án: 1,03
Câu 28 [703024]: Trong quá trình chế biến sản phẩm đông lạnh xuất khẩu cần sử dụng chlorine trong qua trình sơ chế nguyên liệu và diệt vi sinh vật. Thị trường lớn như Mỹ và Châu Âu, được xem là thị trường khó tính, nên tiêu chuẩn chất lượng được kiểm soát chặt chẽ trước khi nhập nguyên liệu và sau khi thành phẩm, đóng gói. Trong danh mục tiêu chuẩn chất lượng sản phẩm có chỉ tiêu về dư lượng chlorine không vượt quá 1mg/l. Phương pháp chuẩn độ iodine – thiosulfate được dùng để xác định dư lượng chlorile trong thực phẩm theo phương trình:
Cl2 + 2KI 2KCl + I2.
2KCl + I2.
Sau đó, I2 được nhận biết bằng hồ tinh bột I2 bị khử bởi dung dịch chuẩn sodiumthiosulfate theo phương trình:
I2 + 2Na2S2O3 2NaI + Na2 S4O6.
2NaI + Na2 S4O6.
Dựa vào thể tích dung dịch Na2S2O3 phản ứng, tính được dư lượng chlorine trong dung dịch mẫu. Công ty A lấy 100 mL mẫu dung dịch tiến hành chuẩn độ bằng dung dịch Na2S2O3 0,01 M, thể tích Na2S2O3 dùng hết 0,42 mL ( dụng cụ chứa dung dịch chuẩn Na2S2O3 là loại microburette 1 mL, vạch chia 0,01 mL). Nồng độ chlorine (mg/L) có trong 1 lít dung dịch trên là bao nhiêu (làm tròn đến hàng phần trăm)?
Cl2 + 2KI
 2KCl + I2.
2KCl + I2.Sau đó, I2 được nhận biết bằng hồ tinh bột I2 bị khử bởi dung dịch chuẩn sodiumthiosulfate theo phương trình:
I2 + 2Na2S2O3
 2NaI + Na2 S4O6.
2NaI + Na2 S4O6.Dựa vào thể tích dung dịch Na2S2O3 phản ứng, tính được dư lượng chlorine trong dung dịch mẫu. Công ty A lấy 100 mL mẫu dung dịch tiến hành chuẩn độ bằng dung dịch Na2S2O3 0,01 M, thể tích Na2S2O3 dùng hết 0,42 mL ( dụng cụ chứa dung dịch chuẩn Na2S2O3 là loại microburette 1 mL, vạch chia 0,01 mL). Nồng độ chlorine (mg/L) có trong 1 lít dung dịch trên là bao nhiêu (làm tròn đến hàng phần trăm)?
Đổi 0,42 mL = 4,2.10-4 L
Cl2 + 2KI → 2KCl + I2 (1)
I2 + 2Na2S2O3 → 2NaI + Na2S4O6 (2)
Số mol của Na2S2O3 phản ứng là:
4,2.10-4 . 0,01 = 4,2.10-6 (mol)
Từ phương trình hóa học (1) và (2) số mol của Cl2 trong 100ml mẫu dung dịch là 2,1.10-6 (mol)
Khối lượng của Cl2 là: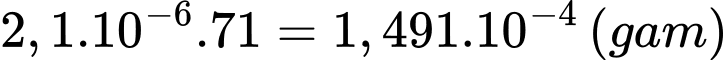
Nồng độ chlorine trong 1 L dung dịch là:
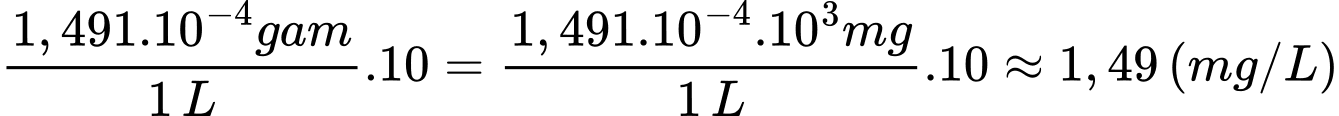
⇒ Điền đáp án: 1,49
Cl2 + 2KI → 2KCl + I2 (1)
I2 + 2Na2S2O3 → 2NaI + Na2S4O6 (2)
Số mol của Na2S2O3 phản ứng là:
4,2.10-4 . 0,01 = 4,2.10-6 (mol)
Từ phương trình hóa học (1) và (2) số mol của Cl2 trong 100ml mẫu dung dịch là 2,1.10-6 (mol)
Khối lượng của Cl2 là:
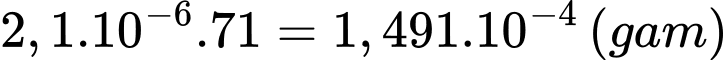
Nồng độ chlorine trong 1 L dung dịch là:
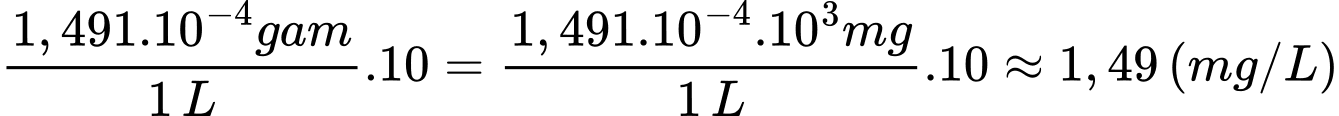
⇒ Điền đáp án: 1,49