PHẦN I. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
❌ A. 19K: 1s22s22p63s23p64s1 có electron cuối cùng điền vào phân lớp s.
❌ B. 20Ca: 1s22s22p63s23p64s2 có electron cuối cùng điền vào phân lớp s.
✔️ C. 24Cr: 1s22s22p63s23p63d54s1 có electron cuối cùng điền vào phân lớp d.
❌ D. 18Ar: 1s22s22p63s23p6 có electron cuối cùng điền vào phân lớp p.
⇒ Chọn đáp án C Đáp án: C
♦ chỉ ank-1-yne dạng RC≡CH + AgNO3 + NH3 → RC≡CAg↓ (tủa màu vàng) + NH4NO3.
⇒ biết được hex-1-yne dựa vào kết tủa vàng khi phản ứng với AgNO3/NH3.
còn lại hex-1-ene và hexane ta dùng Br2, chất nào làm mất màu dung dịch Br2 là alkene → chọn A. ♥.
p/s: các đáp án khác: B sai vì thuốc tím KMnO4 giúp biết được hexane (không phản ứng)
còn hex-1-yne và hex-1-ene đều làm mất màu và tạo ↓MnO2 màu đen
NHƯNG brom không giúp ta phân biệt được hex-1-yne và hex-1-ene.
đáp án C, D tương tự khi không thể dùng thuốc tím hay Br2 hay nước vôi trong
để phân biệt được cặp alkyne (hex-1-yne) và anken (hex-1-ene) ⇒ tự tin chọn A..!
Đáp án: A
❌A. Glucose: C6H12O6
❌B. Ethyl acetate: C4H8O
✔️C. Methylamine: CH5N
❌D. Saccharose:C12H22O11
⇒ Phân tử của Methylamine chứa nguyên tố nitrogen.
⇒ Chọn đáp án C Đáp án: C
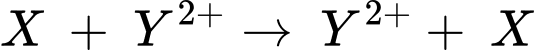
- Dãy điện hóa của kim loại cho phép dự đoán chiều của phản ứng giữa hai cặp oxi hóa – khử theo quy tắc alpha (α): Phản ứng giữa hai cặp oxi hóa – khử sẽ xảy ra theo chiều chất oxi hóa mạnh hơn sẽ oxi hóa chất khử mạnh hơn, sinh ra chất oxi hóa yếu hơn và chất khử yếu hơn.
- Cặp chất phù hợp là Zn và Cu. Zn có tính khử mạnh hơn Cu, Cu2+ có tính oxi hóa mạnh hơn Zn2+
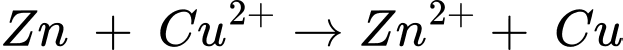
Chọn đáp án D Đáp án: D
M ⟶ M+ + 1e
Trong hợp chất, nguyên tử kim loại nhóm IA chỉ thể hiện số oxi hoá +1.
Chọn đáp án B Đáp án: B
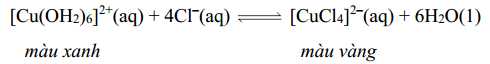
Việc tăng nồng độ Cl–(aq) ảnh hưởng thế nào đến sự thay đổi màu của dung dịch?
⇒ Chọn đáp án B Đáp án: B
Chọn đáp án D Đáp án: D
1 mol HClO4 trong dung dịch phân li hòa toàn thành 1 mol H+ và 1 mol ClO4-
1 mol K2SO4 trong dung dịch phân li hòa toàn thành 2 mol K+ và 1 mol SO42-
1 mol KMnO4 trong dung dịch phân li hòa toàn thành 1 mol K+ và 1 mol MnO4-
→ Dung dịch K2SO4 có độ dẫn điện tốt nhất.
Chọn đáp án C Đáp án: C
CH4 + Cl2
 HCl + CH3Cl.
HCl + CH3Cl.Cơ chế của phản ứng trên xảy ra theo các giai đoạn:
❶ Giai đoạn khơi mào: Cl–Cl
 Cl• + Cl•.
Cl• + Cl•.❷ Giai đoạn phát triển: CH4 + Cl•
 CH3• + HCl;
CH3• + HCl;Cl2 + CH3•
 CH3Cl + Cl•.
CH3Cl + Cl•.❸ Giai đoạn kết thúc: Cl• + CH3•
 CH3Cl;
CH3Cl;Cl• + Cl•
 Cl2.
Cl2.Các chất Cl• và CH3• được gọi là gốc tự do. Nhận định nào sau đây là đúng?
❌ A. Sai. Trong cấu tạo Lewis của gốc tự do Cl• có chứa 7 electron:

❌ B. Sai. Phản ứng trên giúp điều chế chloromethane (CH3Cl) (chỉ 1 Cl bị thay thế) chứ không phải dichloro (Trường hợp 2 nguyên tử Cl bị thay thế sẽ tạo thành chloromethane CH2Cl2).
❌ C. Sai. Phân tử Cl2 gồm hai nguyên tử chlorine liên kết với nhau bằng một liên kết đơn (liên kết đơn là liên kết σ), không phải liên kết π.
✔️ D. Đúng. Trong giai đoạn phát triển, phân tử CH4 có 4 liên kết σ và trong phân tử CH3Cl cũng có 4 liên kết σ → Do đó tổng số liên kết σ trước và sau phản ứng bằng nhau.
⇒ Chọn đáp án D Đáp án: D
Bromine tồn tại dưới hai dạng đồng vị 79Br và 81Br, có hàm lượng bằng nhau. Hình sau cho thấy phổ khối lượng MS không đầy đủ của một mẫu bromine: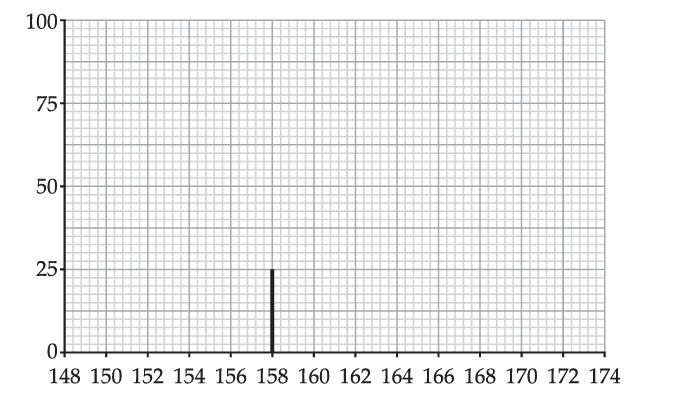
Hai mảnh ion m/z còn thiếu trong phổ khối lượng MS trên là:
(
 ):
): : Khối lượng là
: Khối lượng là 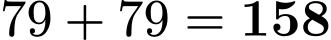
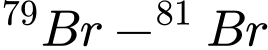
(hoặc
 ): Khối lượng là
): Khối lượng là 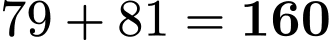
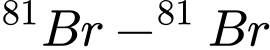 : Khối lượng là
: Khối lượng là 
Trong hình ảnh phổ MS bạn đưa ra, trục hoành (
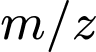 ) đã có sẵn một vạch tại vị trí 158.Dựa vào các tổ hợp tính toán ở trên, hai mảnh ion còn thiếu trong phổ khối lượng của phân tử
) đã có sẵn một vạch tại vị trí 158.Dựa vào các tổ hợp tính toán ở trên, hai mảnh ion còn thiếu trong phổ khối lượng của phân tử 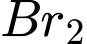 phải là các mảnh có giá trị
phải là các mảnh có giá trị 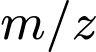 tương ứng với các tổ hợp đồng vị còn lại.Mảnh thứ nhất: 160; Mảnh thứ hai: 162
tương ứng với các tổ hợp đồng vị còn lại.Mảnh thứ nhất: 160; Mảnh thứ hai: 162Đáp án đúng là: C Đáp án: C
- Xà phòng có tính kiềm, nhưng độ pH phải được kiểm soát để không gây kích ứng da.
- Việc thêm NaOH vào xà phòng sẽ làm tăng độ pH quá mức, gây hại cho da.
- Các chất phụ gia khác như chất độn, chất tạo màu, chất tạo hương, chất dưỡng da, chất diệt khuẩn có thể được thêm vào xà phòng, nhưng phải đảm bảo an toàn cho da.
Phân tích các đáp án :
❌A. Sai. Sodium hydroxide (NaOH) là một chất kiềm mạnh. Nếu thêm NaOH vào xà phòng, nó sẽ làm tăng độ pH của xà phòng, khiến xà phòng trở nên quá kiềm và gây kích ứng da.
✔️B. Đúng. Chất độn (như talc, đất sét) có thể được thêm vào xà phòng để tăng khối lượng và giảm giá thành. Tuy nhiên, nếu thêm quá nhiều chất độn, xà phòng sẽ giảm khả năng tạo bọt và làm sạch.
✔️C. Đúng. Chất tạo màu và chất tạo hương thường được thêm vào xà phòng để tăng tính thẩm mỹ và tạo mùi thơm.
✔️D. Đúng. Chất dưỡng da (như glycerin, dầu thực vật) và chất diệt khuẩn (như triclosan) có thể được thêm vào xà phòng để tăng khả năng dưỡng ẩm và diệt khuẩn.
⟹Chọn đáp án A Đáp án: A
Giải thích:
– Amino acid có tính lưỡng tính vì trong phân tử chứa cả nhóm –NH2 (base yếu) và –COOH (acid yếu), nên có thể phản ứng với cả acid và base.
– Amino acid chứa nhóm -COOH (carboxylic acid) có thể phản ứng với alcohol (ROH) trong môi trường acid mạnh (H2SO4 đặc) để tạo ester theo phản ứng ester hóa.
⇒ Chọn đáp án C Đáp án: C

Xét hợp chất hữu cơ X:
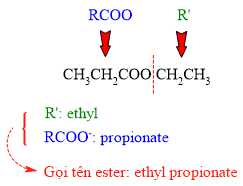
⇒ Chọn đáp án B Đáp án: B
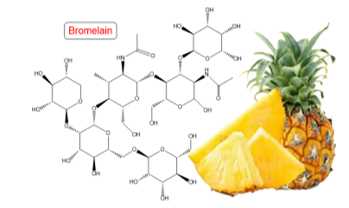
Phát biểu nào dưới đây không đúng?
✔️ A. Đúng. Bromelain là enzyme thủy phân protein, có trong dứa. Khi ướp thịt bò với nước ép dứa, bromelain sẽ phân giải protein trong thịt, làm thịt mềm hơn.
✔️ B. Đúng. X có chứa 2 liên kết amide nên sẽ phản ứng được với dung dịch NaOH. Vậy a mol X tác dụng với 2a mol NaOH trong dung dịch.
❌ C. Sai. công thức cấu tạo của X, có liên kết amide (-CO-NH-).
✔️ D. Đúng. X có 16 nhóm -OH , tương ứng với 8 mol H2 .
⟹Chọn đáp án C Đáp án: C
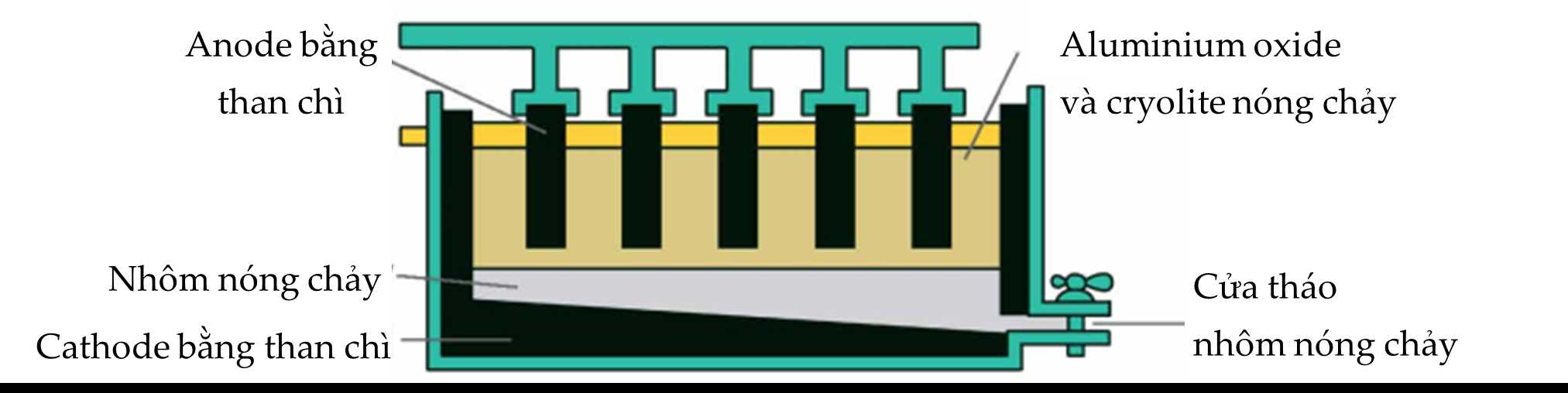
Cho các phát biểu sau:
(a) Cathode xảy ra quá trình khử Al3+ thành kim loại Al nóng chảy.
(b) Ở anode xuất hiện hỗn hợp khí O2, CO và CO2.
(c) Na3AlF6 được thêm vào sẽ nổi lên trên, bảo vệ nhôm nóng chảy khỏi bị oxi hóa bởi O2 không khí.
(d) Trong quá trình điện phân, cực âm luôn phải được thay mới do điện cực làm bằng than chì.Số phát biểu đúng là
✔️ (a) – Đúng. Cathode xảy ra quá trình khử Al3+ thành kim loại Al nóng chảy.
Điện phân nóng chảy:
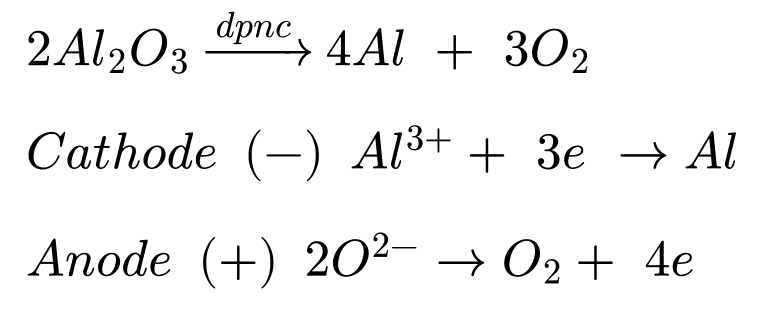
✔️ (b) – Đúng. Ở anode xuất hiện hỗn hợp khí O2, CO và CO2 nguyên do điện cực làm bằng than chì nên sẽ phản ứng với O2 sinh ra.
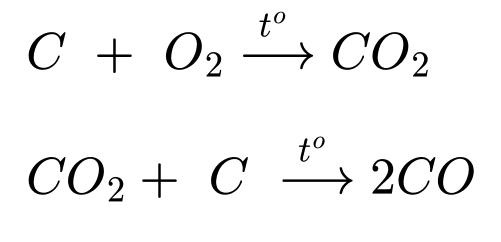
✔️ (c) – Đúng.
Cryolite (Na3AlF6) là nguyên liệu được dùng để sản xuất nhôm với mục đích:
- Làm giảm nhiệt độ nóng chảy của Al2O3.
- Tiết kiệm được năng lượng, tạo được chất lỏng có tính dẫn điện tốt hơn Al2O3.
- Tạo chất lỏng có tỉ khối nhỏ hơn nhôm, nổi lên bề mặt ngăn nhôm nóng chảy bị oxi hoá.
❌ (d) – Sai. Trong quá trình điện phân, cực dương (anode) luôn phải được thay mới do điện cực làm bằng than chì sẽ phản ứng với O2 sinh ra trong quá trình sản xuất nhôm.
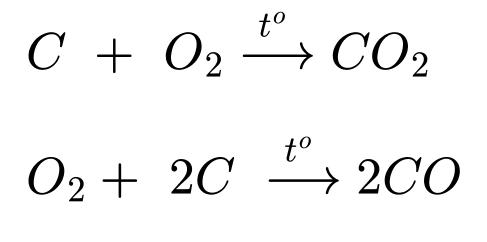
Các phát biểu đúng là (a) (b) (c)
⇒ Chọn đáp án C Đáp án: C
Acetone (CH3COCH3) có phân tử khối là 58.
⇒ Chọn đáp án C Đáp án: C
Sử dụng thông tin cho dưới đây để trả lời các câu số 17 – 18:
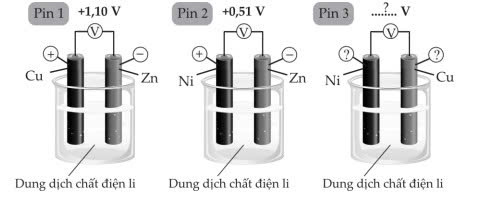
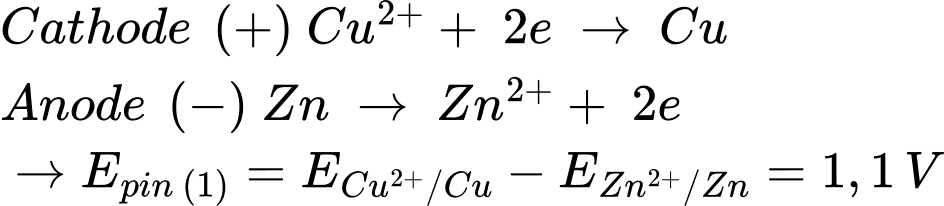
Pin 2: Zn đóng vai trò là cực âm (quá trình oxi hóa) và Ni đóng vai trò là cực dương (quá trình khử)
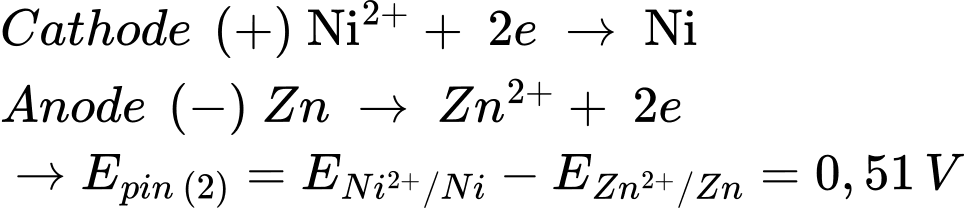
Từ pin 1 và pin 2 → Tính khử của các kim loại giảm dần Zn > Ni > Cu.
Từ pin 1 và pin 2 → Pin 3: Ni đóng vai trò là cực âm và Cu đóng vai trò là cực dương
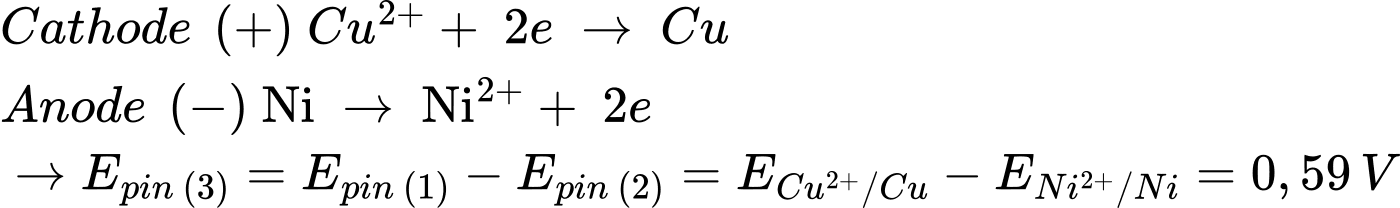
⇒ Chọn đáp án C Đáp án: C
❌ A. Sai. Pin 3: Ni đóng vai trò là cực âm và Cu đóng vai trò là cực dương
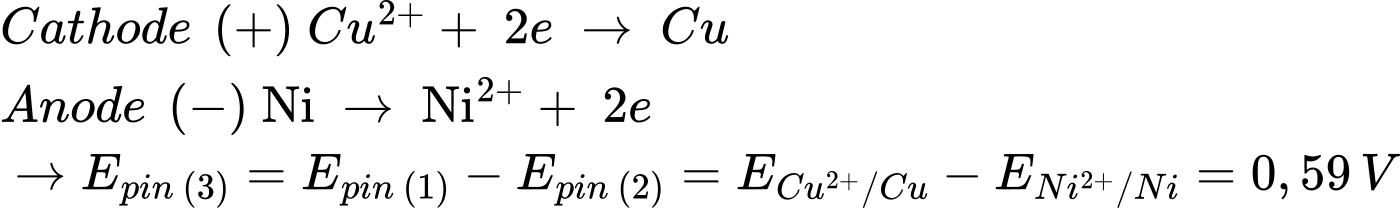
❌ B. Sai. Từ pin 1 và pin 2 → Tính khử của các kim loại giảm dần Zn > Ni > Cu.
❌ C. Sai.
Pin 1: Zn đóng vai trò là cực âm (quá trình oxi hóa) và Cu đóng vai trò là cực dương (quá trình khử)
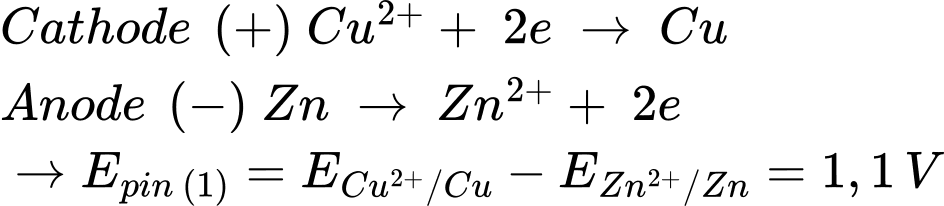
Pin 2: Zn đóng vai trò là cực âm (quá trình oxi hóa) và Ni đóng vai trò là cực dương (quá trình khử)
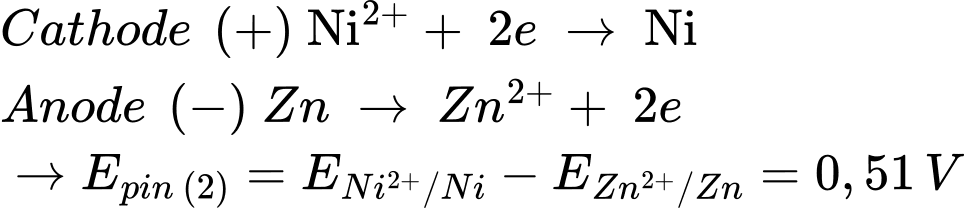
✔️ D. Đúng. Pin 3: Ni đóng vai trò là cực âm và Cu đóng vai trò là cực dương
⇒ Chọn đáp án D Đáp án: D
PHẦN II. Thí sinh trả lời từ câu 1 đến câu 4. Trong mỗi ý a), b), c), d) ở mỗi câu, thí sinh chọn đúng hoặc sai.
▪ Bước 1: Cho vào ống nghiệm khoảng 2 mL dung dịch ZnSO4, thêm từ từ cho đến hết khoảng 10 giọt dung dịch BaCl2, lắc ống nghiệm.
▪ Bước 2: Tiếp tục thêm vào khoảng 2 - 3 giọt dung dịch HCl, lắc đều.
✔️ (a) Đúng. Ở bước 1, có kết tủa trắng BaSO4 xuất hiện.
ZnSO4 + BaCl2 ⟶ BaSO4 + ZnCl2
❌ (b) Sai. BaSO4 là kết tủa trắng, bền không tan trong nước và các dung dịch acid.
✔️ (c) Đúng. Nếu thay dung dịch ZnSO4 bằng dung dịch Na2SO4, hiện tượng xảy ra tương tự.
Na2SO4 + BaCl2 ⟶ BaSO4 + 2NaCl
✔️ (d) Đúng. Sự có mặt của ion Ba2+ trong dung dịch có thể nhận biết bằng dung dịch chứa ion SO42–.
Ba2+ + SO42– ⟶ BaSO4 (kết tủa trắng).
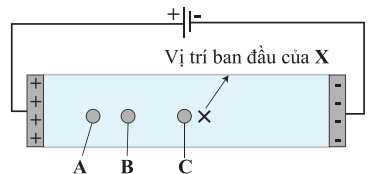
Tại pH = 6,06 dạng tồn tại của glycine, glutamic acid và Glu-Gly như sau: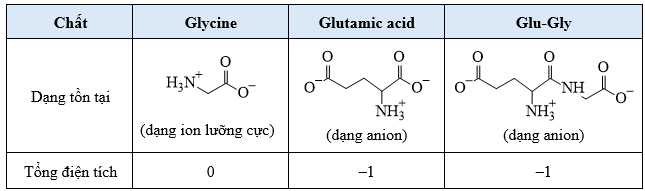
– Tại pH = 6,06 dạng tồn tại của glycine tồn tại dạng ion lưỡng cực nên hầu như không di chuyển trong điện trường → C là Glycine.
– Tại pH = 6,06 dạng tồn tại của Glutamic acid và Glu–Gly tồn tại dạng ion anion và có tổng điện tích là – 1 nên di chuyển về cực dương trong điện trường, nhưng Glutamic acid có kích thước nhỏ hơn nên sẽ đi nhanh hơn về phía cực dương → A là Glutamic acid và B là Glu–Gly.
Phân tích các phát biểu:
❌ (a) Sai. Chất A tiến gần cực dương hơn nên chất A không thể có điện tích nhỏ hơn chất B.
✔️ (b) Đúng. Chất A, B, C lượt là Glu (dạng anion), Glu-Gly (dạng anion) và Ala(dạng trung hòa về điện).
❌ (c) Sai. Tại pH = 6,06 dạng tồn tại của Glutamic acid và Glu-Gly tồn tại dạng ion anion và có tổng điện tích là –1 nên di chuyển về cực dương trong điện trường, nhưng Glutamic acid có kích thước nhỏ hơn nên sẽ đi nhanh hơn về phía cực dương.
❌ (d) Sai. Tại pH = 2, glutamic acid và glycine đều tồn tại dạng cation nên di chuyển về cực âm: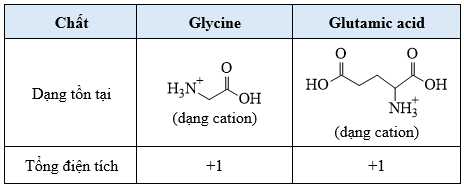
Chuẩn bị: nước ép cà rốt, hexane; cốc thuỷ tinh 100 mL, bình tam giác 100 mL, phễu chiết 60 mL, giá thí nghiệm.
Tiến hành:
- Cho khoảng 20 mL nước ép cà rốt vào phễu chiết. Thêm tiếp khoảng 20 mL hexane, lắc đều khoảng 2 phút.
- Để yên phễu chiết trên giá thí nghiệm khoảng 5 phút để chất lỏng tách thành hai lớp.
- Mở khoá phễu chiết cho phần nước ở dưới chảy xuống, còn lại phần dung dịch β-carotene hoà tan trong hexane.
✔️a. Đúng. Trước khi chiết lớp hexane trong phễu không có màu; sau khi chiết lớp hexane trong phễu có màu vàng cam.
❌ b. Sai. Thí nghiệm tách β-carotene từ nước cà rốt dựa theo nguyên tắc chiết lỏng – lỏng.
✔️ c. Đúng. Dùng dung môi là hexane có khả năng hoà tan β-carotene nhưng không tan trong nước và có nhiệt độ sôi thấp để chiết.
✔️ d. Đúng. Phễu chiết tách thành hai lớp, lớp bên trên là β-carotene hoà tan trong hexane, lớp dưới là nước.
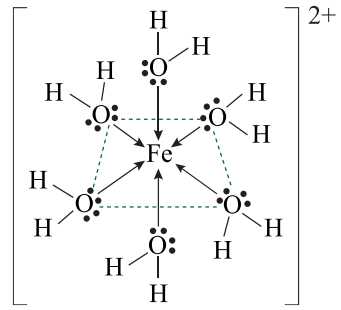
❌ a) Sai. Trong phức [Fe(H2O)6]2+, nguyên tử trung tâm là cation Fe2+, một ion dương có số oxi hóa +2.
✔️ b) Đúng. Liên kết trong phức chất là liên kết cho nhận (liên kết cộng hóa trị phối trí). Trong đó, các phối tử H2O dùng cặp electron chưa liên kết trên nguyên tử oxygen để tạo liên kết với ion Fe2+.
✔️ c) Đúng. Ion Fe2+ có số phối trí là 6 (do có 6 phối tử H2O liên kết), tạo dạng hình học bát diện đặc trưng.
❌ d) Sai. NH3 là phối tử trung tính, tương tự H2O, và kích thước của NH3 không đủ lớn để làm thay đổi số phối trí. Dạng hình học vẫn giữ nguyên là bát diện.
PHẦN III. Thí sinh trả lời từ câu 1 đến 6. Thí sinh điền kết quả mỗi câu vào mỗi ô trả lời tương ứng theo hướng dẫn của phiếu trả lời.
(1) (C6H10O5)n (tinh bột) + nH2O
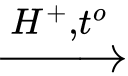 nC6H12O6 (glucose)
nC6H12O6 (glucose)(2) C6H12O6 (glucose)
 2C2H5OH + 2CO2
2C2H5OH + 2CO2(3) C6H12O6 (glucose)
 2CH3CH(OH)COOH
2CH3CH(OH)COOH(4) C6H12O6 (glucose) + 2[Ag(NH3)2]OH
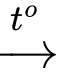 CH2OH(CHOH)4COONH4 + 2Ag + 3NH3 + H2O.
CH2OH(CHOH)4COONH4 + 2Ag + 3NH3 + H2O.Gán số thứ tự phương trình hoá học của các phản ứng theo tên gọi: lên men rượu, thủy phân, lên men lactic, tráng gương và sắp xếp theo trình tự thành dãy bốn số (ví dụ: 1234, 4321,…).
(1) Phản ứng thủy phân tinh bột: mô tả sự thủy phân tinh bột thành glucose (C6H12O6) với sự có mặt của nước.
Phản ứng: (C6H10O5)n (tinh bột) + nH2O
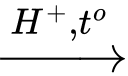 nC6H12O6 (glucose)
nC6H12O6 (glucose)(2) Phản ứng lên men rượu: mô tả quá trình lên men glucose thành ethanol và CO2 dưới tác dụng của enzyme.
Phản ứng: C6H12O6 (glucose)
 2C2H5OH + 2CO2
2C2H5OH + 2CO2(3) Phản ứng lên men lactic acid: mô tả quá trình lên men glucose thành lactic acid (CH3CH(OH)COOH) dưới tác dụng của enzyme.
Phản ứng: C6H12O6 (glucose)
 2CH3CH(OH)COOH
2CH3CH(OH)COOH(4) Phản ứng tráng gương: là phản ứng giữa glucose và dung dịch Ag(NH3)2OH, trong đó Ag được tạo thành, thể hiện phản ứng tráng gương.
Phản ứng: C6H12O6 (glucose) + 2[Ag(NH3)2]OH
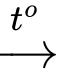 CH2OH(CHOH)4COONH4 + 2Ag + 3NH3 + H2O.
CH2OH(CHOH)4COONH4 + 2Ag + 3NH3 + H2O.⇒ Thứ tự lần lượt ứng với các tên gọi phản ứng lên men rượu, thủy phân, lên men lactic, tráng gương là: 2134
⇒ Điền đáp án: 2134
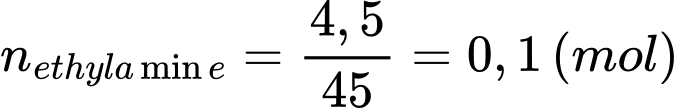
Từ PTHH số mol HCl phản ứng là
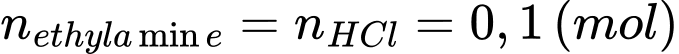
Khối lượng dung dịch HCl 7,3% là
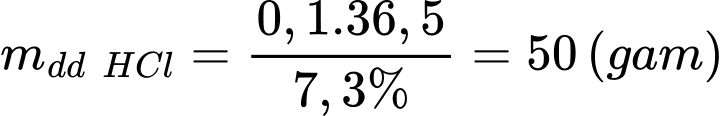
⇒ Điền đáp án: 50
M = 89 × 2 + 117 × 2 + 75 – 4 × 18 = 415 (gam/mol)
⇒ Điền đáp án: 415
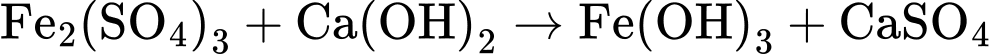
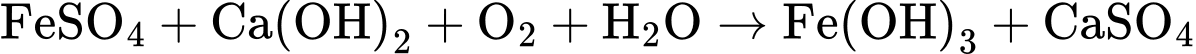
Xác định hàm lượng Fe trong mẫu nước phân tích mg/L.
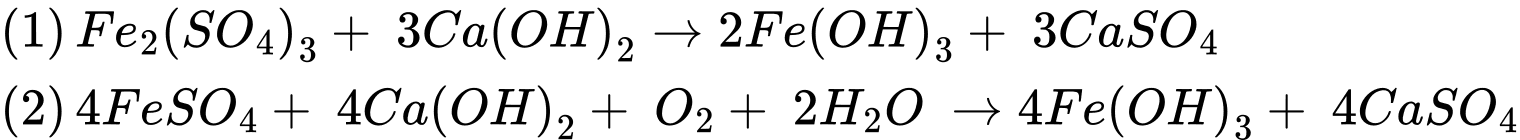
Đổi 10 m3 = 10000 L
Đặt số mol của Fe2(SO4)3 và FeSO4 lần lượt là x và 8x (mol)
Số mol của Ca(OH)2 là: nCa(OH)2 = 91,575 ÷ 74 = 1,2375 (mol)
Từ PTHH số mol của Ca(OH)2 là: nCa(OH)2 = 3x + 8x = 1,2375 (mol) → x = 0,1125 (mol)
Bảo toàn nguyên tố Fe: nFe = 2x + 8x = 1,125 (mol)
Hàm lượng Fe trong mẫu nước phân tích là:
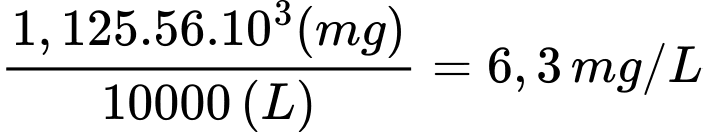
⇒ Điền đáp án: 6,3
C8H18(l) + 12,5O2(g) ⟶ 8CO2(g) + 9H2O(l);

C2H5OH(l) + 3O2(g) ⟶ 2CO2(g) + 3H2O(l);
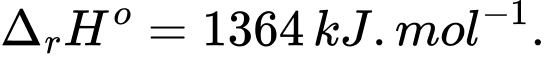
Biết rằng khối lượng riêng của octane và ethanol lần lượt là 0,699 g/mL và 0,785 g/mL. Đốt cháy 1 lít octane tạo ra lượng nhiệt bằng với đốt cháy bao nhiêu L ethanol (Làm tròn đến hàng phần trăm)?
Khối lượng octane là: mC8H18 = V × d = 1 × 0,699 = 0,699 (kg)
Số mol octane là: nC8H18 = m ÷ M = (1 × 0,699) ÷ 114 = 0,0048..(kmol). (lưu ý ở đây không làm tròn, tránh sai số)
Nhiệt lượng tỏa ra khi đốt cháy 1L C8H18 là:
QC8H18 = [(1 × 0,699) ÷ 114] × 5470 = 26,5522... (không làm tròn)
Nhiệt lượng tỏa ra khi đốt cháy lượng C2H5OH là:
QC2H5OH = [(V × 0,785) ÷ 46] × 1364
Mà nhiệt lượng tạo ra khi đốt cháy 1 L octane bằng với nhiệt lượng tạo ra khi đốt cháy V (L) ethanol nên ta có:
[(V × 0,785) ÷ 46] × 1364 = 26,5522... ⟶ V = 1,4408... ≈ 1,44 (L)
⇒ Điền đáp án: 1,44
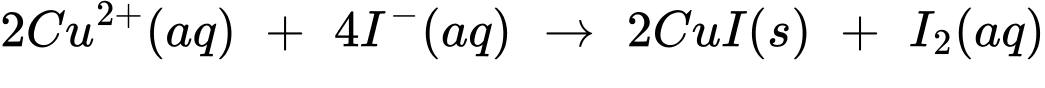
Quy trình được thực hiện như sau:
Bước 1. Hoà tan 0,5 g mẫu hợp kim C60600 trong sulfuric acid đặc, rồi pha loãng bằng nước;
Bước 2. Thêm dung dịch I- đến dư.
Bước 3. Thêm dần dung dịch
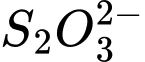 0,50 M để phản ứng với iodine theo phản ứng sau:
0,50 M để phản ứng với iodine theo phản ứng sau: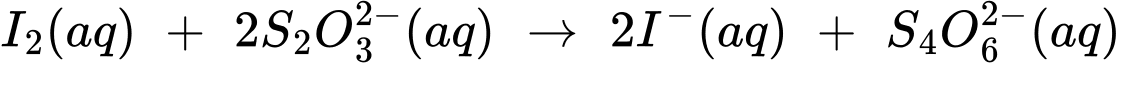
Thể tích dung dịch cần dùng để phản ứng trên xảy ra vừa đủ là 14,85 mL. Hàm lượng phần trăm khối lượng Cu trong mẫu hợp kim C60600 là bao nhiêu? (làm tròn kết quả đến phần chục).
(2) I2(aq) + 2S2O32–(aq) ⟶ 2I– + S4O62–(aq)
Đổi 14,85 mL = 0,01485 L
Số mol của Na2S2O3 là:
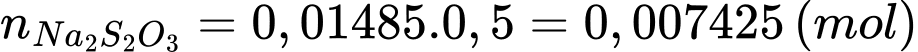
Từ phương trình (1) và (2) số mol của Cu là:
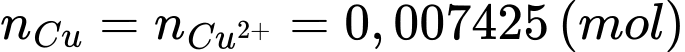
Phần trăm của Cu trong mẫu hợp kim C60600 là:
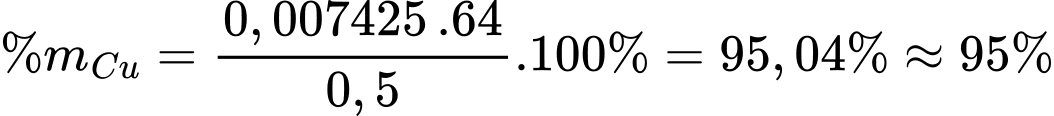
⇒ Điền đáp án: 95,0