PHẦN I. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
Câu 1 [247235]: Mỗi orbital nguyên tử chứa tối đa
A, 1 electron.
B, 2 electron.
C, 3 electron.
D, 4 electron.
HƯỚNG DẪN GIẢI:
- Mỗi orbital nguyên tử chứa tối đa 2 electron.
⟹ Chọn đáp án: B
- Đọc thêm: Mỗi electron trong nguyên tử được đặc trưng bởi một bộ số gọi là bộ 4 số lượng tử (Giống như mã định danh, mỗi electron có một bộ số riêng biệt), bao gồm các số n, m, l, s. Trong đó, giá trị s được gọi là spin quantum number - số lượng tử spin, xác định hướng tự quay của electron. S chỉ có hai giá trị là +1/2 và -1/2, lần lượt được gọi là spin up (↑) và spin down (↓). Các electron trong cùng một AO sẽ có cùng số n, m, l, chỉ khác nhau ở số lượng tử spin. Mà số lượng tử spin cũng chỉ có hai giá trị nên một AO chỉ có tối đa hai electron, electron này nhận giá trị s = +1/2 thì electron còn lại nhận nốt giá trị s = -1/2 còn lại (Nguyên lý loại trừ Pauli) Đáp án: B
- Mỗi orbital nguyên tử chứa tối đa 2 electron.
⟹ Chọn đáp án: B
- Đọc thêm: Mỗi electron trong nguyên tử được đặc trưng bởi một bộ số gọi là bộ 4 số lượng tử (Giống như mã định danh, mỗi electron có một bộ số riêng biệt), bao gồm các số n, m, l, s. Trong đó, giá trị s được gọi là spin quantum number - số lượng tử spin, xác định hướng tự quay của electron. S chỉ có hai giá trị là +1/2 và -1/2, lần lượt được gọi là spin up (↑) và spin down (↓). Các electron trong cùng một AO sẽ có cùng số n, m, l, chỉ khác nhau ở số lượng tử spin. Mà số lượng tử spin cũng chỉ có hai giá trị nên một AO chỉ có tối đa hai electron, electron này nhận giá trị s = +1/2 thì electron còn lại nhận nốt giá trị s = -1/2 còn lại (Nguyên lý loại trừ Pauli) Đáp án: B
Câu 2 [304089]: Có bao nhiêu đồng phân cấu tạo của ester ứng với công thức C3H6O2?
A, 2.
B, 3.
C, 4.
D, 5.
HD: ứng với công thức C3H6O2 chỉ có 2 cấu tạo ester như sau:
(1) HCOOCH2CH3 và (2) CH3COOCH3.
⇝ Chọn đáp án A Đáp án: A
(1) HCOOCH2CH3 và (2) CH3COOCH3.
⇝ Chọn đáp án A Đáp án: A
Câu 3 [705928]: Tại sao ở các vùng ven biển, vật liệu xây dựng làm bằng sắt thường bị ăn mòn nhanh hơn vì
A, sắt dễ bị oxi hóa bởi oxygen có mặt trong không khí.
B, dễ tiếp xúc với nước muối, hình thành môi trường điện li.
C, chi phí bảo trì sắt cao hơn các kim loại khác.
D, nhiệt độ tăng cao nên sắt dễ bị nóng trong thời tiết nắng.
Muối trong không khí đại dương ở các vùng ven biển gây ra các vấn đề lo ngại cho thép và gỗ. Đối với thép, nước là tác nhân chính dẫn đến rỉ sét. Nhưng cuộc sống ven biển đưa muối vào quá trình này, và muối được thêm vào sẽ gây ra các phản ứng hóa học làm tăng tốc độ ăn mòn một cách đáng kể.
Chọn đáp án B Đáp án: B
Chọn đáp án B Đáp án: B
Câu 4 [308783]: Phân biệt được hai dung dịch chứa riêng biệt các dipeptide mạch hở là Ala–Val và Val–Lys bằng thuốc thử là
A, Phenolphthalein.
B, Hydrochloric acid.
C, Sodium hydroxide.
D, Đồng(II) hydroxide.
Nhận xét:
+) Ala–Val có số nhóm NH2 bằng số nhóm COOH.
⇒ Dung dịch có môi trường trung tính → không làm phenolphthalein đổi màu.
+) Val–Lys có số nhóm NH2 hơn số nhóm COOH
⇒ Dung dịch Val–Lys có môi trường base, làm phenolphthalein đổi màu hồng.
⇒ Phenolphtalein giúp ta phân biệt được 2 dung dịch trên.
⟹ Chọn đáp án A Đáp án: A
+) Ala–Val có số nhóm NH2 bằng số nhóm COOH.
⇒ Dung dịch có môi trường trung tính → không làm phenolphthalein đổi màu.
+) Val–Lys có số nhóm NH2 hơn số nhóm COOH
⇒ Dung dịch Val–Lys có môi trường base, làm phenolphthalein đổi màu hồng.
⇒ Phenolphtalein giúp ta phân biệt được 2 dung dịch trên.
⟹ Chọn đáp án A Đáp án: A
Câu 5 [186807]: Trong khí thải của một nhà máy có nhiều khí SO2, khí này là nguyên nhân chính gây ra hiện tượng mưa acid làm ô nhiễm môi trường. Để loại bỏ khí SO2 trong khí thải trên với chi phí thấp có thể dùng dung dịch nào sau đây?
A, Nước vôi trong.
B, NaOH.
C, Br2.
D, KMnO4.
Phân tích các đáp án
✔️A. Nước vôi trong được sản xuất từ nguyên liệu đầu là đá vôi nên chi phí sản xuất thấp nhất.
Trong thực tế thường dùng Ca(OH)2 rắn để xử lý khí thải SO2.
❌B. NaOH đắt hơn nước vôi trong, nên không phải lựa chọn tối ưu về chi phí.
❌C. Br2 không có phản ứng trực tiếp để loại bỏ SO2 trong khí thải.
❌D. Dung dịch KMnO4 đắt tiền, không kinh tế để xử lý khí thải.
⟹ Chọn đáp án A Đáp án: A
✔️A. Nước vôi trong được sản xuất từ nguyên liệu đầu là đá vôi nên chi phí sản xuất thấp nhất.
Trong thực tế thường dùng Ca(OH)2 rắn để xử lý khí thải SO2.
❌B. NaOH đắt hơn nước vôi trong, nên không phải lựa chọn tối ưu về chi phí.
❌C. Br2 không có phản ứng trực tiếp để loại bỏ SO2 trong khí thải.
❌D. Dung dịch KMnO4 đắt tiền, không kinh tế để xử lý khí thải.
⟹ Chọn đáp án A Đáp án: A
Câu 6 [706346]: M là nguyên tố kim loại chuyển tiếp dãy thứ nhất, có một số đặc điểm sau:
∎ Có nhiều số oxi hoá trong các hợp chất, trong đó có số oxi hoá +2 và +3.
∎ Nguyên tử có 4 electron độc thân.
∎ Ở dạng đơn chất, là kim loại nặng.
M là nguyên tố nào sau đây?
∎ Có nhiều số oxi hoá trong các hợp chất, trong đó có số oxi hoá +2 và +3.
∎ Nguyên tử có 4 electron độc thân.
∎ Ở dạng đơn chất, là kim loại nặng.
M là nguyên tố nào sau đây?
A, Cr.
B, Ni.
C, Fe.
D, Cu.
Phân tích các đáp án:
❌A. Cr : Cấu hình electron của Cr là [Ar]3d54s1. Tuy nhiên, Cr thường có thể thực hiện số oxy hóa +6, không phù hợp với yêu cầu có số oxy hóa +2 và +3.
❌B. Ni : Cấu hình electron của Ni là [Ar]3d84s2. Ni chủ yếu thể hiện số oxy hóa +2.
✔️C. Fe : Cấu hình electron của Fe là [Ar]3d64s2. Fe có thể thực hiện nhiều quá trình oxy hóa, bao gồm +2 và +3, và có 4 electron độc thân trong cấu hình 3d6.
❌D. Cu : Cấu hình electron của Cu là [Ar]3d104s1. Cu chủ yếu thể hiện số oxy hóa +1 và +2.
⟹ Chọn đáp án C Đáp án: C
❌A. Cr : Cấu hình electron của Cr là [Ar]3d54s1. Tuy nhiên, Cr thường có thể thực hiện số oxy hóa +6, không phù hợp với yêu cầu có số oxy hóa +2 và +3.
❌B. Ni : Cấu hình electron của Ni là [Ar]3d84s2. Ni chủ yếu thể hiện số oxy hóa +2.
✔️C. Fe : Cấu hình electron của Fe là [Ar]3d64s2. Fe có thể thực hiện nhiều quá trình oxy hóa, bao gồm +2 và +3, và có 4 electron độc thân trong cấu hình 3d6.
❌D. Cu : Cấu hình electron của Cu là [Ar]3d104s1. Cu chủ yếu thể hiện số oxy hóa +1 và +2.
⟹ Chọn đáp án C Đáp án: C
Câu 7 [305422]: Thủy phân triolein có công thức (C17H33COO)3C3H5 trong dung dịch HCl, thu được glixerol và acid X. Công thức của X là
A, C17H35COOH.
B, CH3COOH.
C, C2H5COOH.
D, C17H33COOH.
Phản ứng tổng quát:
(RCOO)3C3H5 + 3H2O –––H⁺, to–→ 3RCOOH + C3H5(OH)3.
Ở câu hỏi này: (RCOO)3C3H5 = (C17H33COO)3C3H5
⇒ R = C17H33COO ⇒ acid thu được là RCOOH = C17H33COOH
⇒ Chọn đáp án D Đáp án: D
(RCOO)3C3H5 + 3H2O –––H⁺, to–→ 3RCOOH + C3H5(OH)3.
Ở câu hỏi này: (RCOO)3C3H5 = (C17H33COO)3C3H5
⇒ R = C17H33COO ⇒ acid thu được là RCOOH = C17H33COOH
⇒ Chọn đáp án D Đáp án: D
Câu 8 [243433]: Nguyên tố calcium có số hiệu nguyên tử là 20. Khi calcium tham gia phản ứng tạo hợp chất ion thì cấu hình electron của cation là
A, 1s22s22p63s23p64s1.
B, 1s22s22p6.
C, 1s22s22p63s23p6.
D, 1s22s22p63s23p63d10.
Nguyên tố calcium có số hiệu nguyên tử là 20 nên khi tham gia phản ứng sẽ có xu hướng nhường đi 2 electron để đạt cấu hình của nguyên tử khí hiếm gần nhất là Argon (Z = 18), tạo thành cation Ca2+.
→ Cấu hình electron của cation Ca2+ là: 1s22s22p63s23p6.
⇒ Chọn đáp án C Đáp án: C
→ Cấu hình electron của cation Ca2+ là: 1s22s22p63s23p6.
⇒ Chọn đáp án C Đáp án: C
Câu 9 [702837]: Trong cấu tạo của polysaccharide sau đây có bao nhiêu liên kết glycoside?
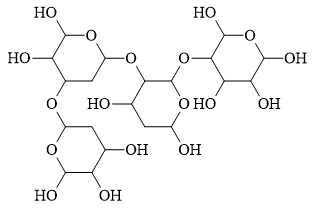

A, 2.
B, 3.
C, 4.
D, 5.
Liên kết glycoside là liên kết giữa một phân tử đường (carbohydrate) và một phân tử khác (có thể là đường khác hoặc một phân tử không phải đường) thông qua nguyên tử oxygen. Liên kết này hình thành khi một phân tử nước bị loại bỏ trong quá trình kết hợp.
Trong cấu tạo của polysaccharide trên có 3 liên kết glycoside được xác định dưới đây:
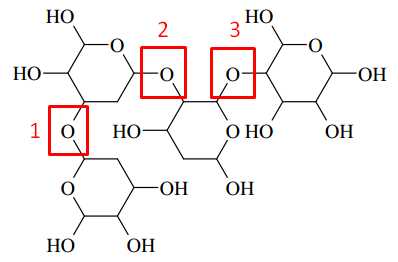
⇒ Chọn đáp án B Đáp án: B
Trong cấu tạo của polysaccharide trên có 3 liên kết glycoside được xác định dưới đây:

⇒ Chọn đáp án B Đáp án: B
Câu 10 [702810]: Potassium nitrate (KNO3) là một trong những phân potassium phổ biến. Phân này có ưu điểm gì so với các loại phân potassium khác?
A, Cung cấp cả potassium và nitrogen cho cây trồng.
B, Tăng độ pH của đất nhanh chóng.
C, Dễ hòa tan trong nước.
D, Không gây ô nhiễm môi trường.
Điểm khác nổi bật của phân potassium nitrate (KNO3) so với các loại phân potassium khác là trong phân tử KNO3 có cả nguyên tố K và N là hai nguyên tố dinh dưỡng thiết yếu cho cây trồng.
⭐ Potassium (K): Thúc đẩy quá trình quang hợp, tăng sức mạnh đề kháng của cây, cải thiện chất lượng và năng suất nông sản.
⭐ Nitrogen (N) dạng nitrate (NO3-): hấp thu dễ dàng và thúc đẩy sự phát triển nhanh chóng của cây.
⇒ Chọn đáp án A Đáp án: A
⭐ Potassium (K): Thúc đẩy quá trình quang hợp, tăng sức mạnh đề kháng của cây, cải thiện chất lượng và năng suất nông sản.
⭐ Nitrogen (N) dạng nitrate (NO3-): hấp thu dễ dàng và thúc đẩy sự phát triển nhanh chóng của cây.
⇒ Chọn đáp án A Đáp án: A
Câu 11 [706348]: Enzyme đóng vai trò xúc tác cho nhiều phản ứng, phổ biến trong phản ứng hữu cơ, môi trường hoạt động ở nhiệt độ không cao. Sự khác nhau về năng lượng hoạt hoá của phản ứng có sử dụng và không sử dụng enzyme xúc tác như sau:
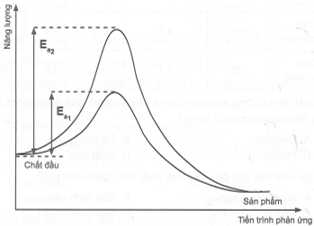
Nhận định nào sau đây không đúng?

Nhận định nào sau đây không đúng?
A, Xúc tác enzyme làm giảm năng lượng hoạt hóa của phản ứng.
B, Đường (2) có năng lượng hoạt hóa cao hơn đường (1).
C, Đường (1) biểu diễn cho phản ứng không sử dụng enzyme làm xúc tác.
D, Trạng thái năng lượng của sản phẩm khi sử dụng enzyme và không sử dụng enzyme bằng nhau.
Phân tích các đáp án:
✔️A – Đúng. Enzyme là chất xúc tác sinh học có khả năng làm giảm năng lượng hoạt hóa của phản ứng hóa học, giúp phản ứng diễn ra nhanh hơn mà không bị tiêu hao trong quá trình phản ứng.
✔️B – Đúng. Từ đồ thị, đường (2) có năng lượng hoạt hóa cao hơn đường (1).
❌C – Sai. Đường (1) biểu diễn cho phản ứng sử dụng enzyme làm xúc tác, có năng lượng hoạt hóa thấp hơn so với đường (2)
✔️D – Đúng. Enzyme chỉ làm giảm năng lượng hoạt hóa (Ea), tức là năng lượng cần thiết để phản ứng bắt đầu. Nhưng nó không ảnh hưởng đến năng lượng tự do của các chất tham gia hay sản phẩm.
⟹ Chọn đáp án C Đáp án: C
✔️A – Đúng. Enzyme là chất xúc tác sinh học có khả năng làm giảm năng lượng hoạt hóa của phản ứng hóa học, giúp phản ứng diễn ra nhanh hơn mà không bị tiêu hao trong quá trình phản ứng.
✔️B – Đúng. Từ đồ thị, đường (2) có năng lượng hoạt hóa cao hơn đường (1).
❌C – Sai. Đường (1) biểu diễn cho phản ứng sử dụng enzyme làm xúc tác, có năng lượng hoạt hóa thấp hơn so với đường (2)
✔️D – Đúng. Enzyme chỉ làm giảm năng lượng hoạt hóa (Ea), tức là năng lượng cần thiết để phản ứng bắt đầu. Nhưng nó không ảnh hưởng đến năng lượng tự do của các chất tham gia hay sản phẩm.
⟹ Chọn đáp án C Đáp án: C
Câu 12 [309447]: Tên gọi của polymer có công thức: 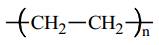 là
là
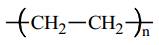 là
là A, Poly(methyl metacrylate).
B, Poly(vinyl chloride).
C, Polyethylene.
D, Polystyrene.
Polymer được tạo bởi các đơn phân (monomer) liên kết với nhau thông qua các liên kết hóa học để tạo thành chuỗi dài.
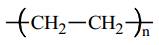 là một polymer được tạo thành từ monomer CH2=CH2 (ethylene) qua phản ứng trùng hợp.
là một polymer được tạo thành từ monomer CH2=CH2 (ethylene) qua phản ứng trùng hợp.
⇒ Chọn đáp án C Đáp án: C
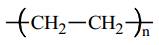 là một polymer được tạo thành từ monomer CH2=CH2 (ethylene) qua phản ứng trùng hợp.
là một polymer được tạo thành từ monomer CH2=CH2 (ethylene) qua phản ứng trùng hợp.⇒ Chọn đáp án C Đáp án: C
Câu 13 [705933]: Chanh là một loài thực vật cho quả nhỏ, thuộc chỉ cam chanh (citrus). Quả chanh được sử dụng làm thực phẩm. Nước ép chanh chứa khoảng 5% citric acid nên chanh có vị chua và độ pH khoảng 2 – 3. Công thức (X) được cho ở hình bên.
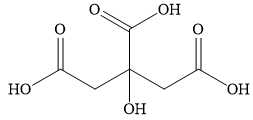
Chọn phát biểu đúng về citric acid

Chọn phát biểu đúng về citric acid
A, Công thức phân tử của citric acid là C4H6O7.
B, 1 mol citric acid tác dụng với Na tạo ra 2 mol H2.
C, Citric acid thuộc loại hợp chất đa chức.
D, Citric acid tác dụng với NaOH theo tỉ lệ mol 1 : 4.
Phân tích các phát biểu:
❌A – Sai. Công thức phân tử của citric acid là C6H8O7.
✔️B – Đúng. Citric acid có 1 nhóm OH (alcohol) và 3 nhóm (carboxylic acid) nên tác dụng với Na theo tỉ lệ 1:4
HOC3H4(COOH)3 + 4Na → NaOC3H4(COONa)3 + 2H2
❌C – Sai. Citric acid thuộc loại hợp chất tạp chức, citric acid có 1 nhóm OH (alcohol) và 3 nhóm (carboxylic acid)
❌D – Sai. Citric acid có 1 nhóm OH (alcohol) và 3 nhóm (carboxylic acid) nên tác dụng với NaOH theo tỉ lệ 1:3
Chọn đáp án B Đáp án: B
❌A – Sai. Công thức phân tử của citric acid là C6H8O7.
✔️B – Đúng. Citric acid có 1 nhóm OH (alcohol) và 3 nhóm (carboxylic acid) nên tác dụng với Na theo tỉ lệ 1:4
HOC3H4(COOH)3 + 4Na → NaOC3H4(COONa)3 + 2H2
❌C – Sai. Citric acid thuộc loại hợp chất tạp chức, citric acid có 1 nhóm OH (alcohol) và 3 nhóm (carboxylic acid)
❌D – Sai. Citric acid có 1 nhóm OH (alcohol) và 3 nhóm (carboxylic acid) nên tác dụng với NaOH theo tỉ lệ 1:3
Chọn đáp án B Đáp án: B
Câu 14 [705913]: Dạng hình học của phức chất được xác nhận bằng thực nghiệm. Phức chất mà xung quanh nguyên tử trung tâm có 4 liên kết σ thường có dạng hình học là tứ diện hoặc vuông phẳng và được gọi là phức chất tứ diện hoặc phức chất vuông phẳng. Phức chất mà xung quanh nguyên tử trung tâm có 6 liên kết σ có dạng hình học là bát diện và được gọi là phức chất bát diện. Cấu trúc của phức chất [PtCl4]2– được cho dưới đây:
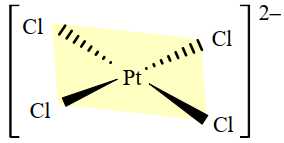
Cho các phát biểu sau:
(a) Phức chất có 4 liên kết xung quanh nguyên tử trung tâm.
(b) Phức chất có dạng hình học là tứ diện.
(c) Hai liên kết Pt–Cl kế cận nhau trong phức chất tạo thành một góc 90o.
(d) Phức chất có thể kết hợp với hai cation K+ để tạo thành hợp chất trung hòa điện.
Số phát biểu đúng là

Cho các phát biểu sau:
(a) Phức chất có 4 liên kết xung quanh nguyên tử trung tâm.
(b) Phức chất có dạng hình học là tứ diện.
(c) Hai liên kết Pt–Cl kế cận nhau trong phức chất tạo thành một góc 90o.
(d) Phức chất có thể kết hợp với hai cation K+ để tạo thành hợp chất trung hòa điện.
Số phát biểu đúng là
A, 1.
B, 2.
C, 3.
D, 4.
Phân tích các phát biểu:
✔️ (a) – Đúng. Phức chất [PtCl4]2- có ion nguyên tử trung tâm là Pt2+ và 4 phối tử Cl- liên kết với nguyên tử trung tâm.
❌ (b) – Sai. Từ cấu tạo, phức chất [PtCl4]2- có dạng vuông phẳng.
✔️(c) – Đúng. [PtCl4]2- là phức chất vuông phẳng. Hai liên kết Pt-Cl kế cận nhau trong anion [PtCl4]2- tạo thành một góc liên kết. Thực nghiệm xác nhận trong anion [PtCl4]- có bốn góc liên kết đều có giá trị xấp xỉ 90°.
✔️ (d) – Đúng. Phức chất [PtCl4]2- là phức chất anion có điện tích 2- nên cần 2 cation K+ để trung hòa về điện.
Có 3 phát biểu đúng.
⟹ Chọn đáp án C Đáp án: C
✔️ (a) – Đúng. Phức chất [PtCl4]2- có ion nguyên tử trung tâm là Pt2+ và 4 phối tử Cl- liên kết với nguyên tử trung tâm.
❌ (b) – Sai. Từ cấu tạo, phức chất [PtCl4]2- có dạng vuông phẳng.
✔️(c) – Đúng. [PtCl4]2- là phức chất vuông phẳng. Hai liên kết Pt-Cl kế cận nhau trong anion [PtCl4]2- tạo thành một góc liên kết. Thực nghiệm xác nhận trong anion [PtCl4]- có bốn góc liên kết đều có giá trị xấp xỉ 90°.
✔️ (d) – Đúng. Phức chất [PtCl4]2- là phức chất anion có điện tích 2- nên cần 2 cation K+ để trung hòa về điện.
Có 3 phát biểu đúng.
⟹ Chọn đáp án C Đáp án: C
Câu 15 [705478]: Acid trong dịch dạ dày có thành phần chủ yếu là HCl. Khi nồng độ acid trong dịch dạ dày quá cao sẽ dẫn đến tình trạng dư thừa acid, gây ra nhiều bệnh lí. Sữa magiê có dạng huyền phù, chứa thành phần chính là Mg(OH)2 được sử dụng như một loại thuốc kháng acid trong dạ dày. Nếu dạ dày chứa 200 mL dung dịch HCl có pH = 1,5 thì khối lượng tối thiểu Mg(OH)2 trong sữa magiê cần dùng để trung hòa toàn bộ lượng HCl này là bao nhiêu (làm tròn kết quả đến chữ số hàng phần mười)?
A, 91,7 mg.
B, 183,4 mg.
C, 348,0 mg.
D, 3,5 gam.
Đổi 200 mL = 0,2 L
Ta có pH = 1,5 → Nồng độ H+ trong dạ dày là [H+] = 10-1,5 M
Số mol H+ là: nH+ = 10-1,5 × 0,2 = 0,006325 mol
PTHH: Mg(OH)2 + 2H+ ⟶ Mg2+ + 2H2O
Từ phương trình số mol của Mg(OH)2 là: nMg(OH)2 = nH+ ÷ 2 = 0,006325 ÷ 2 = 0,0031625 (mol)
Khối lượng của Mg(OH)2 trong “sữa magiê” cần dùng là:
mMg(OH)2 = 0,0031625 × 58 = 0,183425 (g) ≈ 183,4 (mg)
⇒ Chọn đáp án B Đáp án: B
Ta có pH = 1,5 → Nồng độ H+ trong dạ dày là [H+] = 10-1,5 M
Số mol H+ là: nH+ = 10-1,5 × 0,2 = 0,006325 mol
PTHH: Mg(OH)2 + 2H+ ⟶ Mg2+ + 2H2O
Từ phương trình số mol của Mg(OH)2 là: nMg(OH)2 = nH+ ÷ 2 = 0,006325 ÷ 2 = 0,0031625 (mol)
Khối lượng của Mg(OH)2 trong “sữa magiê” cần dùng là:
mMg(OH)2 = 0,0031625 × 58 = 0,183425 (g) ≈ 183,4 (mg)
⇒ Chọn đáp án B Đáp án: B
Câu 16 [705885]: Trong các phản ứng oxi hóa – khử, việc chọn tác nhân oxi hóa để phù hợp với các điều kiện của phản ứng là quan trọng. Một phản ứng cần chọn tác nhân oxi hóa rất mạnh, trong các tác nhân sau, tác nhân oxi hóa mạnh nhất là? Cho các thế điện cực chuẩn: 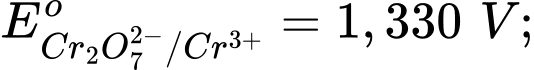
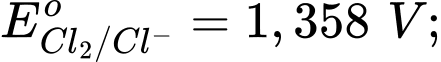
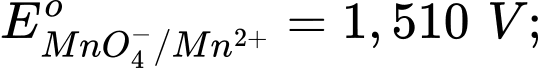
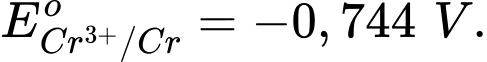
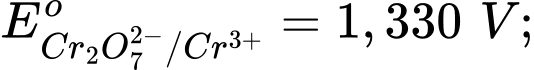
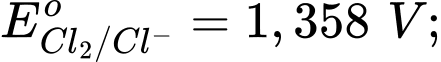
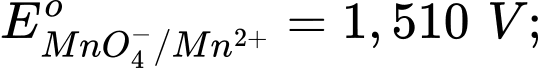
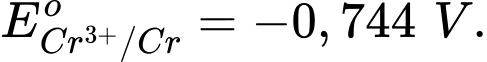
A, Cl–.
B, Mn2+.
C, MnO4–.
D, Cr3+.
-Thế điện cực của cặp oxi hóa – khử của kim loại (đơn vị là Volt – V) trong điều kiện chuẩn (nồng độ ion kim loại trong dung dịch là 1M, nhiệt độ 25oC) được gọi là thế điện cực chuẩn của kim loại (hay thế khử chuẩn của kim loại, kí hiệu là .
-Thế điện cực chuẩn của cặp oxi hóa – khử càng lớn thì tính khử của dạng khử càng yếu, tính oxi hóa của dạng oxi hóa càng mạnh và ngược lại.
Chọn đáp án C Đáp án: C
-Thế điện cực chuẩn của cặp oxi hóa – khử càng lớn thì tính khử của dạng khử càng yếu, tính oxi hóa của dạng oxi hóa càng mạnh và ngược lại.
Chọn đáp án C Đáp án: C
Sử dụng thông tin cho dưới đây để trả lời các câu số 17 – 18:
Phản ứng giữa propene với HBr tạo thành hai sản phẩm khác nhau là 1-bromoproane và 2-bromoproane. Các giai đoạn xảy ra phản ứng như sau:
▪ Giai đoạn 1 của phản ứng là quá trình H+ phản ứng với C=C, tạo carbocation trung gian.
▪ Giai đoạn 2 là quá trình kết hợp giữa carbocation với tác nhân Br-
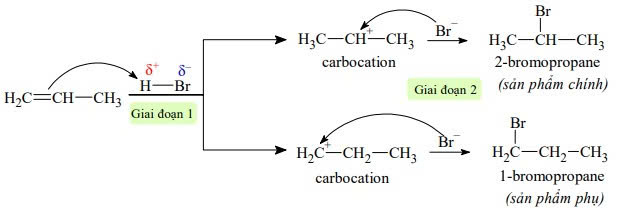
Biết rằng carbocation có điện tích dương tồn tại trên C có bậc cao hơn thì bền hơn và sẽ tạo thành lượng sản phẩm nhiều hơn (sản phẩm chính).
▪ Giai đoạn 1 của phản ứng là quá trình H+ phản ứng với C=C, tạo carbocation trung gian.
▪ Giai đoạn 2 là quá trình kết hợp giữa carbocation với tác nhân Br-

Biết rằng carbocation có điện tích dương tồn tại trên C có bậc cao hơn thì bền hơn và sẽ tạo thành lượng sản phẩm nhiều hơn (sản phẩm chính).
Câu 17 [706048]: Nếu cho but-1-ene tác dụng với HBr thì sản phẩm chính là
A, 1-bromobutane.
B, 2-bromobutane.
C, 3-bromobutane.
D, 1-bromo-1-methylpropane.
Quy tắc Markovnikov: Phản ứng cộng một tác nhân không đối xứng HX như HBr, HCl, HOH,..vào liên kết bội, nguyên tử hydrogen sẽ ưu tiên cộng vào nguyên tử carbon có nhiều hydrogen hơn và X sẽ cộng vào nguyên tử carbon có ít hydrogen hơn.
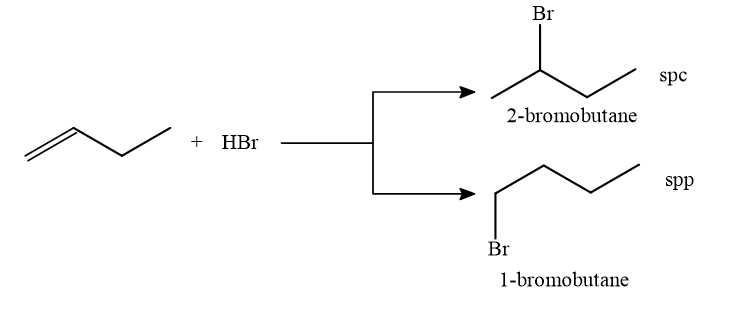
⟹ Chọn đáp án B Đáp án: B

⟹ Chọn đáp án B Đáp án: B
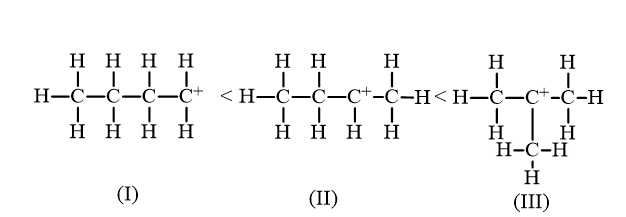
Câu 18 [706049]: Phản ứng cộng HBr (hoặc tổng quát cộng HX) vào alkene bất đối xứng ưu tiên xảy ra theo hướng tạo carbocation bền hơn. Cho các carbocation sau:
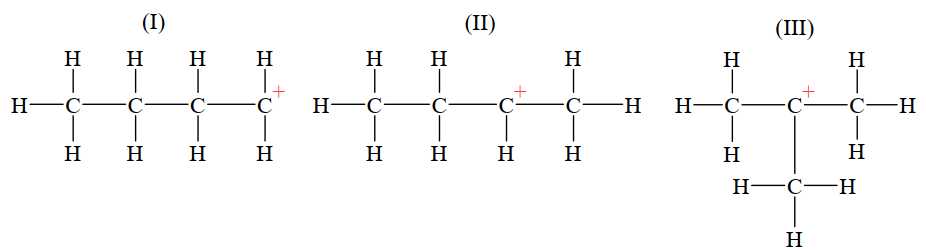
So sánh độ bền của carbocation theo thứ tự giảm dần là

So sánh độ bền của carbocation theo thứ tự giảm dần là
A, (I) > (II) > (III).
B, (III) > (II) > (I).
C, (II) > (I) > (III).
D, (III) > (I) > (II).
Carbocation là tiểu phân trung gian kém bền. Độ bền tương đối của carbocation thường tăng khi bậc của nguyên tử carbon mang điện tích dương tăng.
Thự tự giảm dần độ bền của carbocation là (III), (II), (I)
⟹ Chọn đáp án B Đáp án: B
Thự tự giảm dần độ bền của carbocation là (III), (II), (I)

⟹ Chọn đáp án B Đáp án: B
PHẦN II. Thí sinh trả lời từ câu 1 đến câu 4. Trong mỗi ý a), b), c), d) ở mỗi câu, thí sinh chọn đúng hoặc sai.
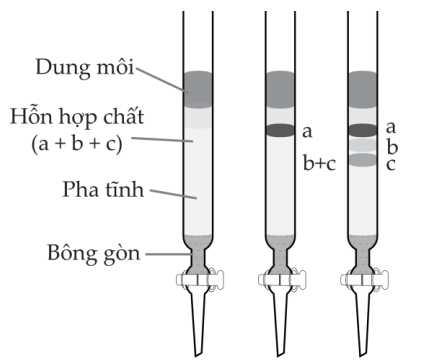
Câu 19 [703954]: Quan sát hình mô phỏng thí nghiệm sắc khí cột hình bên:

Phân tích các phát biểu:
✔️ a) Đúng. Chất a hấp phụ mạnh trên pha tĩnh và tan kém trong dung môi sẽ ra khỏi cột sắc kí sau cùng.
✔️ b) Đúng. Chất c hấp phụ kém trên pha tĩnh và tan tốt trong dung môi sẽ ra khỏi cột sắc kí trước.
❌ c) Sai. Thứ tự hòa tan tốt trong dung môi là c > b > a, vì c được tách ra trước, chất hấp phụ kém trên pha tĩnh và tan tốt trong dung môi sẽ ra khỏi cột sắc kí trước.
✔️ d) Đúng. Cơ sở của sắc kí dựa trên sự khác nhau về khả năng phân bố của mỗi chất trong dung môi thích hợp.
✔️ a) Đúng. Chất a hấp phụ mạnh trên pha tĩnh và tan kém trong dung môi sẽ ra khỏi cột sắc kí sau cùng.
✔️ b) Đúng. Chất c hấp phụ kém trên pha tĩnh và tan tốt trong dung môi sẽ ra khỏi cột sắc kí trước.
❌ c) Sai. Thứ tự hòa tan tốt trong dung môi là c > b > a, vì c được tách ra trước, chất hấp phụ kém trên pha tĩnh và tan tốt trong dung môi sẽ ra khỏi cột sắc kí trước.
✔️ d) Đúng. Cơ sở của sắc kí dựa trên sự khác nhau về khả năng phân bố của mỗi chất trong dung môi thích hợp.
Câu 20 [703972]: Trong công nghiệp copper (II) sulfate pentahydrate được sản xuất từ copper(II) oxide theo sơ đồ sau:
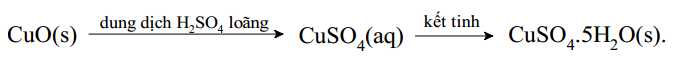
Dung dịch copper(II) sulfate ở các nồng độ thích hợp có thể giúp xử lí tảo xanh trong ao. Nếu tảo xanh phát triển quá mạnh sẽ ngăn cản oxygen khuyếch tán vào trong nước, đồng thời trong quá trình phát triển cũng sẽ lấy đi một phần oxygen. Điều này làm nồng độ oxygen hòa tan trong nước giảm và các sinh vật trong nước như tôm, cá sẽ chết. Một ao nuôi thuỷ sản có diện tích bề mặt nước là 2000 m2, độ sâu trung bình của nước trong ao là 1,0 m đang có hiện tượng phú dưỡng. Để xử lí tảo, người dân cần cho CuSO4.5H2O vào ao trong 3 ngày, mỗi ngày một lần, mỗi lần là 0,25 gam/m3 nước trong ao.
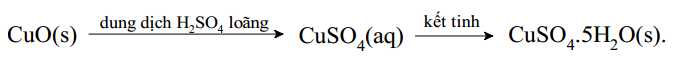
Dung dịch copper(II) sulfate ở các nồng độ thích hợp có thể giúp xử lí tảo xanh trong ao. Nếu tảo xanh phát triển quá mạnh sẽ ngăn cản oxygen khuyếch tán vào trong nước, đồng thời trong quá trình phát triển cũng sẽ lấy đi một phần oxygen. Điều này làm nồng độ oxygen hòa tan trong nước giảm và các sinh vật trong nước như tôm, cá sẽ chết. Một ao nuôi thuỷ sản có diện tích bề mặt nước là 2000 m2, độ sâu trung bình của nước trong ao là 1,0 m đang có hiện tượng phú dưỡng. Để xử lí tảo, người dân cần cho CuSO4.5H2O vào ao trong 3 ngày, mỗi ngày một lần, mỗi lần là 0,25 gam/m3 nước trong ao.
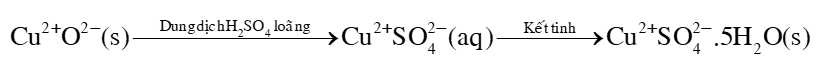
Thể tích của ao cá là 2000.1,0 = 2000 (m3)
Tổng khối lượng CuSO4.5H2O đã cho vào trong ao cá trong 3 ngày là 2000.3.0,25 = 1500 (gam) = 1,5 (kg)
Phân tích các phát biểu:
✔️ a) Đúng. Trong toàn bộ quá trình sản xuất CuSO4.5H2O số oxi hóa của nguyên tố đồng không đổi, số oxi hóa của đồng là +2.
✔️ b) Đúng. Sau khi kết tinh thu được tinh thể đồng CuSO4.5H2O màu xanh lam, CuSO4 khan có màu trắng.
❌ c) Sai. Phú dưỡng hay phú dưỡng hóa là tình trạng mà ao hồ, sông ngòi tiếp nhận các nguồn thải chứa chất dinh dưỡng như phosphorous, nitrogen một cách quá mức.
Việc dư thừa các chất dinh dưỡng trong môi trường nước làm đẩy mạnh sự phát triển của tảo, làm mất cân bằng hệ sinh thái dưới nước và làm suy giảm chất lượng nguồn nước.
❌ d) Sai. Tổng khối lượng CuSO4.5H2O đã cho vào ao trong 3 ngày là 1,5 kg.
Câu 21 [702843]: Chitin là một loại polymer thiên nhiên với trữ lượng rất lớn, đứng thứ hai sau cellulose. Trong động vật, chitin là một thành phần cấu trúc quan trọng trong vỏ của tôm, cua,...
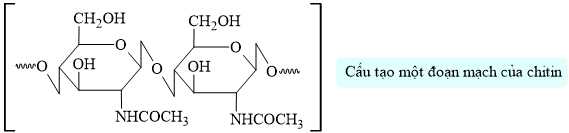
Chitin là nguyên liệu để điều chế glucosamine hydrochloride. Glucosamine giúp hỗ trợ khớp khoẻ mạnh nhờ tái tạo các sụn quanh khớp, đồng thời cũng giúp bảo vệ sụn tránh khỏi phân huỷ bởi các enzyme có trong cơ thể.
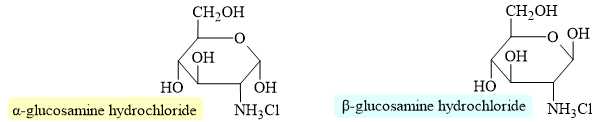
Quá trình điều chế glucosamine hydrochloride từ chitin được thực hiện theo các bước sau:
▪ Bước 1: Lấy 10 gam vỏ tôm khô cho vào bình cầu 250 mL. Cho nước ngập vỏ tôm và đun cách thuỷ trong 2 giờ. Rửa sạch để loại bỏ thịt tôm còn bám trên vỏ.
▪ Bước 2: Cho vỏ tôm vừa rửa sạch ở trên vào bình cầu 250 mL, rồi cho thêm 60 mL dung dịch HCl 5%. Đun cách thuỷ trong 2 giờ để loại khoáng (nếu không đun có thể để qua đêm), sau đó rửa bằng nước đến khi pH = 7.
▪ Bước 3: Cho vỏ tôm thu được ở Bước 2 vào bình cầu 250 mL, đổ ngập vỏ tôm bằng dung dịch NaOH 5%, rồi đun cách thuỷ (duy trì ở nhiệt độ 90 – 95 °C) trong 4 giờ. Rửa bằng nước đến pH = 7 và đem sấy khô. Chitin thu được có màu trắng phớt hồng, mềm, không còn vị tanh.
▪ Bước 4: Lấy chitin thu được ở Bước 3 vào bình cầu, rồi thêm khoảng 80 mL dung dịch HCl 35 – 36%. Đun cách thuỷ trong 4 giờ (duy trì ở nhiệt độ 95 – 100 °C). Lắp sinh hàn hồi lưu vào bình cầu. Sau khi đun, nếu thấy sản phẩm có màu thì tẩy màu bằng than hoạt tính. Sau đó, lọc loại bỏ than hoạt tính, để nguội, tinh thể glucosamine hydrochloride sẽ tách ra. Sấy khô ở nhiệt độ khoảng 60 °C, thu được glucosamine hydrochloride màu trắng.

Chitin là nguyên liệu để điều chế glucosamine hydrochloride. Glucosamine giúp hỗ trợ khớp khoẻ mạnh nhờ tái tạo các sụn quanh khớp, đồng thời cũng giúp bảo vệ sụn tránh khỏi phân huỷ bởi các enzyme có trong cơ thể.

Quá trình điều chế glucosamine hydrochloride từ chitin được thực hiện theo các bước sau:
▪ Bước 1: Lấy 10 gam vỏ tôm khô cho vào bình cầu 250 mL. Cho nước ngập vỏ tôm và đun cách thuỷ trong 2 giờ. Rửa sạch để loại bỏ thịt tôm còn bám trên vỏ.
▪ Bước 2: Cho vỏ tôm vừa rửa sạch ở trên vào bình cầu 250 mL, rồi cho thêm 60 mL dung dịch HCl 5%. Đun cách thuỷ trong 2 giờ để loại khoáng (nếu không đun có thể để qua đêm), sau đó rửa bằng nước đến khi pH = 7.
▪ Bước 3: Cho vỏ tôm thu được ở Bước 2 vào bình cầu 250 mL, đổ ngập vỏ tôm bằng dung dịch NaOH 5%, rồi đun cách thuỷ (duy trì ở nhiệt độ 90 – 95 °C) trong 4 giờ. Rửa bằng nước đến pH = 7 và đem sấy khô. Chitin thu được có màu trắng phớt hồng, mềm, không còn vị tanh.
▪ Bước 4: Lấy chitin thu được ở Bước 3 vào bình cầu, rồi thêm khoảng 80 mL dung dịch HCl 35 – 36%. Đun cách thuỷ trong 4 giờ (duy trì ở nhiệt độ 95 – 100 °C). Lắp sinh hàn hồi lưu vào bình cầu. Sau khi đun, nếu thấy sản phẩm có màu thì tẩy màu bằng than hoạt tính. Sau đó, lọc loại bỏ than hoạt tính, để nguội, tinh thể glucosamine hydrochloride sẽ tách ra. Sấy khô ở nhiệt độ khoảng 60 °C, thu được glucosamine hydrochloride màu trắng.
Phân tích các phát biểu:
✔️ a) Đúng. Hợp chất chứa liên kết amide CO-NH trong chitin bị thủy phân trong môi trường acid nên kém bền.
❌ b) Sai. Ở bước 4 xảy ra quá trình thủy phân chitin thành glucosamine hydrochloride khi cho phản ứng với dung dịch HCl và đun cách thuỷ.
✔️ c) Đúng. Ở bước 4, cần lắp sinh hàn hồi lưu vào bình cầu để hạn chế sự bay hơi của hydrochloride do sinh hàn có tác dụng làm lạnh hydrochloride (ở trạng thái lỏng trong điều kiện thường) đang hóa hơi, đi ngang qua ống sẽ ngưng tụ và quay trở lại bình cầu thay vì thoát ra ngoài.
✔️ d) Đúng. Glucosamine hydrochloride tồn tại ở dạng muối rắn ion nên có độ tan cao trong nước, nhưng khi điều kiện thay đổi (giảm nhiệt độ, giảm dung môi), nó dễ kết tinh và tách ra hơn so với glucosamine tự do.
✔️ a) Đúng. Hợp chất chứa liên kết amide CO-NH trong chitin bị thủy phân trong môi trường acid nên kém bền.
❌ b) Sai. Ở bước 4 xảy ra quá trình thủy phân chitin thành glucosamine hydrochloride khi cho phản ứng với dung dịch HCl và đun cách thuỷ.
✔️ c) Đúng. Ở bước 4, cần lắp sinh hàn hồi lưu vào bình cầu để hạn chế sự bay hơi của hydrochloride do sinh hàn có tác dụng làm lạnh hydrochloride (ở trạng thái lỏng trong điều kiện thường) đang hóa hơi, đi ngang qua ống sẽ ngưng tụ và quay trở lại bình cầu thay vì thoát ra ngoài.
✔️ d) Đúng. Glucosamine hydrochloride tồn tại ở dạng muối rắn ion nên có độ tan cao trong nước, nhưng khi điều kiện thay đổi (giảm nhiệt độ, giảm dung môi), nó dễ kết tinh và tách ra hơn so với glucosamine tự do.
Câu 22 [705467]: Một mẫu magnesium nitrate được nung nóng trong thiết bị được thiết kế sau:
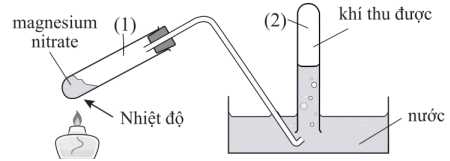
Thu lấy ống nghiệm (2) chứa sản phẩm khí, đưa một que diêm đang cháy lên miệng ống nghiệm và quan sát. Đồng thời tiến hành đo giá trị pH của dung dịch trong máng.

Thu lấy ống nghiệm (2) chứa sản phẩm khí, đưa một que diêm đang cháy lên miệng ống nghiệm và quan sát. Đồng thời tiến hành đo giá trị pH của dung dịch trong máng.
Phản ứng phân hủy 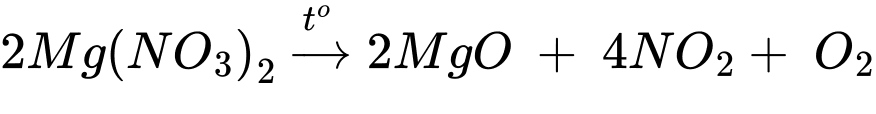
Phân tích các phát biểu:
❌ (a) Sai. Sau phản ứng nhiệt phân hoàn toàn chất rắn còn lại trong ống nghiệm (1) là oxide kim loại MgO.
❌ (b) Sai. Khí thu được trong ống nghiệm (2) là hỗn hợp NO2 và O2. O2 duy trì sự cháy, do đó que diêm có thể bùng cháy mạnh hơn nếu có đủ lượng O2.
✔️ (c) Đúng. Giá trị pH của dung dịch trong máng sau khi nung nóng sẽ nhỏ hơn 7 nguyên nhân có phản ứng hình thành nitric acid.
2H2O + O2 + 4NO2 ⟶ 4HNO3
✔️ (d) Đúng. Tỉ lệ của các chất khí sinh ra ở ống nghiệm (1) 1:4 ứng với O2 và NO2 khác với ở ống nghiệm (2) sau phản ứng của NO2 và O2 với nước tạo ra HNO3 còn lại khí NO và O2.
2H2O + O2 + 4NO2 ⟶ 4HNO3
NO2 + H2O ⟶ HNO3 + NO
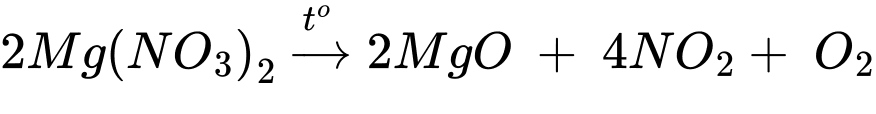
Phân tích các phát biểu:
❌ (a) Sai. Sau phản ứng nhiệt phân hoàn toàn chất rắn còn lại trong ống nghiệm (1) là oxide kim loại MgO.
❌ (b) Sai. Khí thu được trong ống nghiệm (2) là hỗn hợp NO2 và O2. O2 duy trì sự cháy, do đó que diêm có thể bùng cháy mạnh hơn nếu có đủ lượng O2.
✔️ (c) Đúng. Giá trị pH của dung dịch trong máng sau khi nung nóng sẽ nhỏ hơn 7 nguyên nhân có phản ứng hình thành nitric acid.
2H2O + O2 + 4NO2 ⟶ 4HNO3
✔️ (d) Đúng. Tỉ lệ của các chất khí sinh ra ở ống nghiệm (1) 1:4 ứng với O2 và NO2 khác với ở ống nghiệm (2) sau phản ứng của NO2 và O2 với nước tạo ra HNO3 còn lại khí NO và O2.
2H2O + O2 + 4NO2 ⟶ 4HNO3
NO2 + H2O ⟶ HNO3 + NO
PHẦN III. Thí sinh trả lời từ câu 1 đến 6. Thí sinh điền kết quả mỗi câu vào mỗi ô trả lời tương ứng theo hướng dẫn của phiếu trả lời.
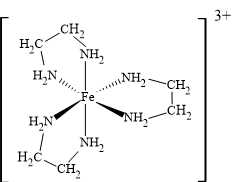
Câu 23 [705433]: Trong phức chất, phân tử NH2CH2CH2NH2 có tên ethylenediamine và thường được viết tắt là en. Trong phức chất [Fe(en)3]Cl3, xung quanh nguyên tử trung tâm có tối đa bao nhiêu liên kết sigma?
Phức chất [Fe(en)3]Cl3 có ion phức là [Fe(en)3]3+, cấu tạo như sau:
Trong đó:
+) Fe3+ là ion trung tâm.
+) Ethylenediamine (en) là phối tử hai càng, nghĩa là mỗi phân tử en có hai nguyên tử N liên kết với Fe3+.
+) Ba phân tử en liên kết với Fe3+, mỗi phân tử tạo 2 liên kết sigma, tổng cộng có: 3 × 2 = 6 liên kết sigma.
Ngoài ra, vì liên kết phối trí trong phức chất đều là liên kết sigma (không có liên kết pi), nên tổng số liên kết sigma trong ion phức là 6.
⇒ Điền đáp án: 6

Trong đó:
+) Fe3+ là ion trung tâm.
+) Ethylenediamine (en) là phối tử hai càng, nghĩa là mỗi phân tử en có hai nguyên tử N liên kết với Fe3+.
+) Ba phân tử en liên kết với Fe3+, mỗi phân tử tạo 2 liên kết sigma, tổng cộng có: 3 × 2 = 6 liên kết sigma.
Ngoài ra, vì liên kết phối trí trong phức chất đều là liên kết sigma (không có liên kết pi), nên tổng số liên kết sigma trong ion phức là 6.
⇒ Điền đáp án: 6
Câu 24 [705755]: Phenylalanine có công thức cấu tạo như dưới đây:
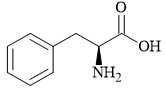
Cho 33 gam phenylalanine phản ứng với dung dịch H2SO4 dư thu được m gam muối. Xác định giá trị của m.

Cho 33 gam phenylalanine phản ứng với dung dịch H2SO4 dư thu được m gam muối. Xác định giá trị của m.
Số mol của phenylalanine là: nphenylalanine = 33 ÷ 165 = 0,2 (mol)
PTHH:
2HOOCC8H8NH2 + H2SO4 ⟶ (HOOCC8H8NH3)2SO4
⟶ Số mol của muối là: n(HOOCC8H8NH3)2SO4 = nHOOCC8H8NH2 ÷ 2 = 0,2 ÷ 2 = 0,1 (mol)
⟶ Khối lượng của muối là: m(HOOCC8H8NH3)2SO4 = 0,1 × 428 = 42,8 (g)
⇒ Điền đáp án: 42,8
PTHH:
2HOOCC8H8NH2 + H2SO4 ⟶ (HOOCC8H8NH3)2SO4
⟶ Số mol của muối là: n(HOOCC8H8NH3)2SO4 = nHOOCC8H8NH2 ÷ 2 = 0,2 ÷ 2 = 0,1 (mol)
⟶ Khối lượng của muối là: m(HOOCC8H8NH3)2SO4 = 0,1 × 428 = 42,8 (g)
⇒ Điền đáp án: 42,8
Câu 25 [684464]: Cho dãy chuyển hóa sau:

Trong đó, X, Y và Z đều là các hợp chất hữu cơ. Xác định khối lượng phân tử của Z.

Trong đó, X, Y và Z đều là các hợp chất hữu cơ. Xác định khối lượng phân tử của Z.
Ta có các phản ứng:
(1)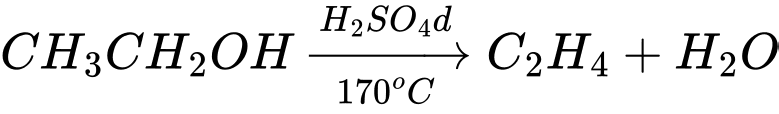
(2)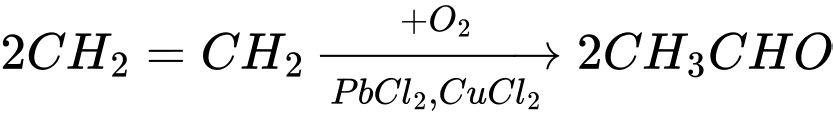
(3)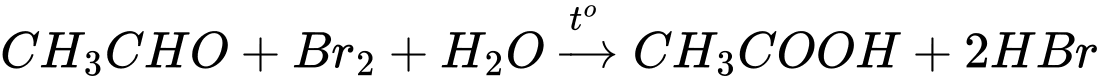
Công thức cấu tạo của Z là: CH3COOH
Khối lượng phân tử của Z là : 12 × 2 + 1 × 4 + 16 × 2 = 60
⇒ Điền đáp án: 60
(1)
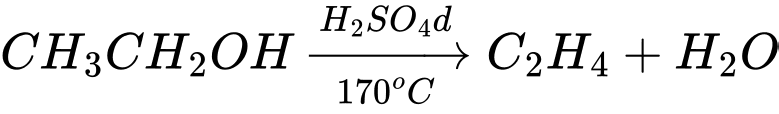
(2)
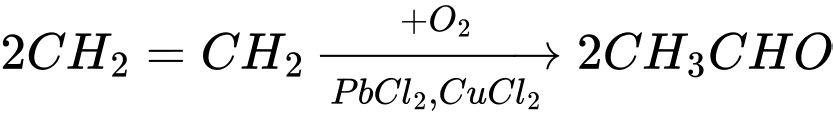
(3)
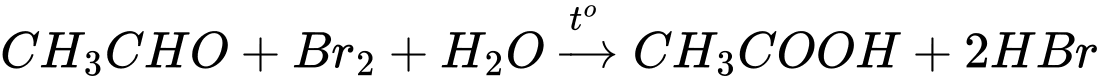
Công thức cấu tạo của Z là: CH3COOH
Khối lượng phân tử của Z là : 12 × 2 + 1 × 4 + 16 × 2 = 60
⇒ Điền đáp án: 60
Câu 26 [705508]: Hình phổ dưới đây là của một hợp chất có công thức tổng quát CnH2n+2. Phân tích và cho biết giá trị của n bằng bao nhiêu?
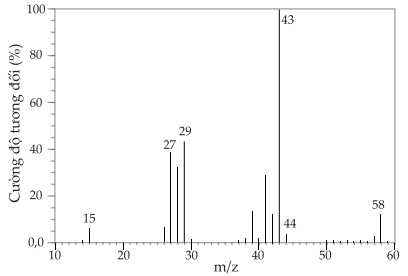

Từ phổ MS ta nhận thấy khối lượng phân tử của hợp chất hữu cơ là 58.
Ta có:
⇒ Điền đáp án: 4
Ta có:

⇒ Điền đáp án: 4
Câu 27 [705778]: Khí Biogas còn gọi là khí sinh học. Thành phần chính của khí sinh học Biogas có khí methane chiếm 60% thể tích còn lại là carbon dioxide và các khí khác. Một bình gas (khí hóa lỏng) chứa hỗn hợp propane và butane với tỉ lệ mol 1 : 2. Khi được đốt cháy hoàn toàn, 1 mol propane tỏa ra lượng nhiệt là 2220 kJ, 1 mol butane tỏa ra lượng nhiệt là 2874 kJ và 1 mol methane tỏa ra lượng nhiệt là 890,5 kJ. Trung bình 60 ngày một hộ gia đình cần dùng hết một bình “ga” loại 12 kg. Thể tích khí Biogas tối thiểu cần dùng để tạo ra lượng nhiệt tương đương khi đốt cháy 1 bình “ga” loại 12 kg là bao nhiêu m3 (đkc)? (Làm tròn đến hàng phần mười)
Gọi nC3H8 = a mol, nC4H10 = b mol
Đổi 12 kg = 12000 gam
Ta có: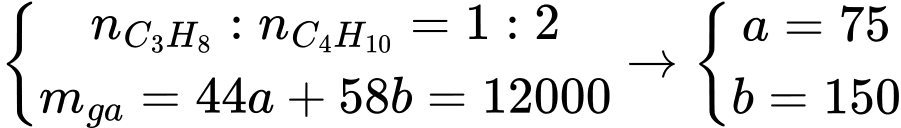
Lượng nhiệt bình ga tỏa ra là: 75 × 2220 + 150 × 2874 = 597600 kJ
Số mol khí biogas cần là: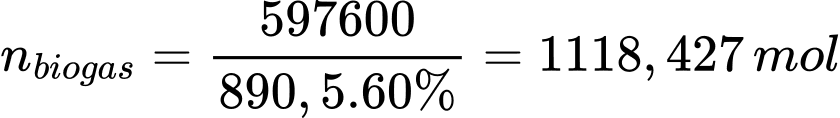
Thể tích khí biogas cần là: Vbiogas = 1118,427 × 24,79 = 27726,92 L ≈ 27,7 m3
⇒ Điền đáp án: 27,7
Đổi 12 kg = 12000 gam
Ta có:
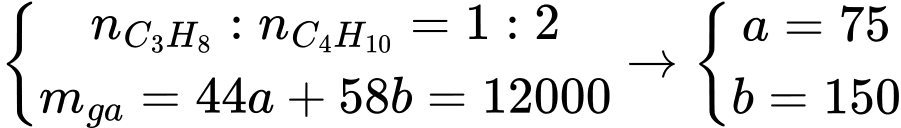
Lượng nhiệt bình ga tỏa ra là: 75 × 2220 + 150 × 2874 = 597600 kJ
Số mol khí biogas cần là:
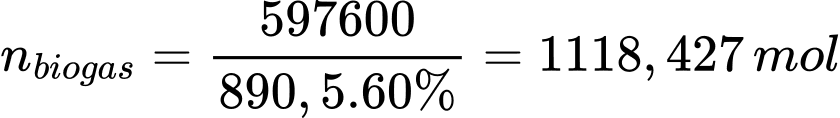
Thể tích khí biogas cần là: Vbiogas = 1118,427 × 24,79 = 27726,92 L ≈ 27,7 m3
⇒ Điền đáp án: 27,7
Câu 28 [702825]: Hiện nay người ta sản xuất ammonia bằng cách chuyển hoá có xúc tác một hỗn hợp gồm không khí, hơi nước và khí methane (thành phần chính của khí thiên nhiên).
Phản ứng điều chế H2:
CH4 + 2H2O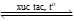 CO2 + 4H2 (1)
CO2 + 4H2 (1)
Phản ứng loại O2 để thu N2: CH4 + 2O2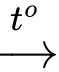 CO2 + 2H2O (2)
CO2 + 2H2O (2)
Phản ứng tổng hợp NH3:
N2 + 3H2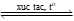 2NH3 (3)
2NH3 (3)
Để sản xuất khí ammonia, nếu lấy 841,4 m3 không khí (chứa 21,03% O2; 78,02% N2, còn lại là khí hiếm theo thể tích), thì cần phải lấy tổng thể tích khí methane và hơi nước là bao nhiêu để có đủ lượng N2 và H2 theo tỉ lệ 1 : 3 về thể tích dùng cho phản ứng tổng hợp ammonia. Giả thiết các phản ứng (1), (2) đều xảy ra hoàn toàn và các thể tích khí đo ở cùng điều kiện.
Phản ứng điều chế H2:
CH4 + 2H2O
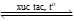 CO2 + 4H2 (1)
CO2 + 4H2 (1)Phản ứng loại O2 để thu N2: CH4 + 2O2
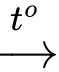 CO2 + 2H2O (2)
CO2 + 2H2O (2)Phản ứng tổng hợp NH3:
N2 + 3H2
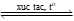 2NH3 (3)
2NH3 (3)Để sản xuất khí ammonia, nếu lấy 841,4 m3 không khí (chứa 21,03% O2; 78,02% N2, còn lại là khí hiếm theo thể tích), thì cần phải lấy tổng thể tích khí methane và hơi nước là bao nhiêu để có đủ lượng N2 và H2 theo tỉ lệ 1 : 3 về thể tích dùng cho phản ứng tổng hợp ammonia. Giả thiết các phản ứng (1), (2) đều xảy ra hoàn toàn và các thể tích khí đo ở cùng điều kiện.
Thể tích O2 và N2 trong không khí là:
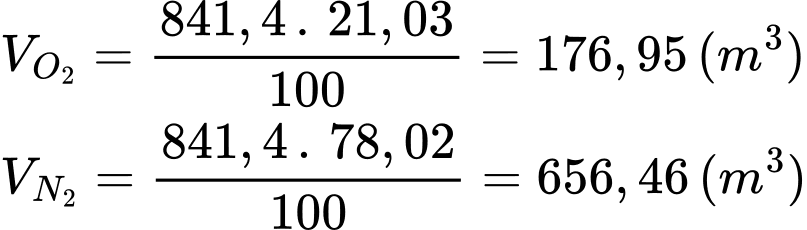
Thể tích khí tỉ lệ thuận với số mol khí.
Từ phản ứng tổng hợp NH3 thể tích H2 tham gia phản ứng là:
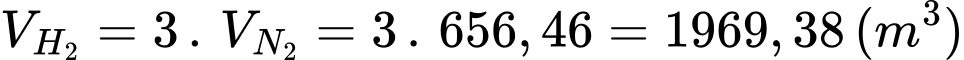
Từ phản ứng điều chế H2 và phản ứng loại O2 thì thể tích CH4 cần dùng là:
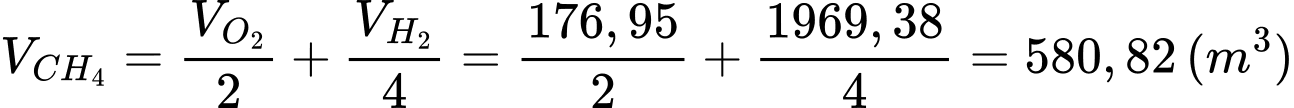
Thể tích hơi nước cần dùng là:
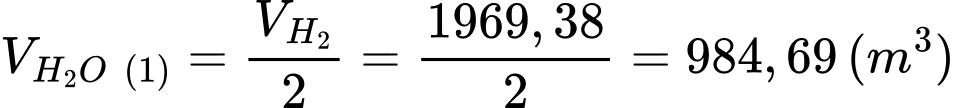
Tổng thể tích CH4 và hơi nước cần dùng là:
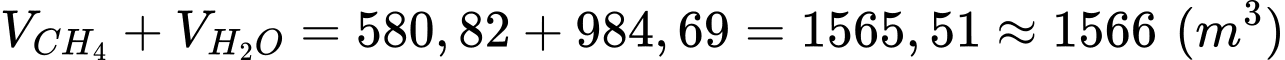
⇒ Điền đáp án: 1566
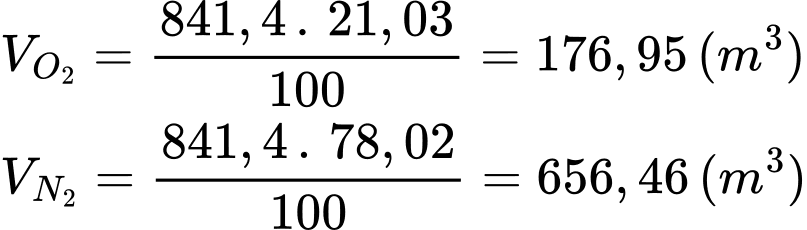
Thể tích khí tỉ lệ thuận với số mol khí.
Từ phản ứng tổng hợp NH3 thể tích H2 tham gia phản ứng là:
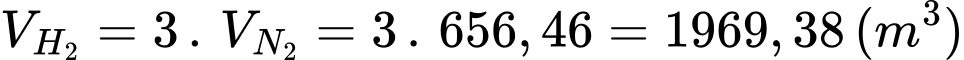
Từ phản ứng điều chế H2 và phản ứng loại O2 thì thể tích CH4 cần dùng là:
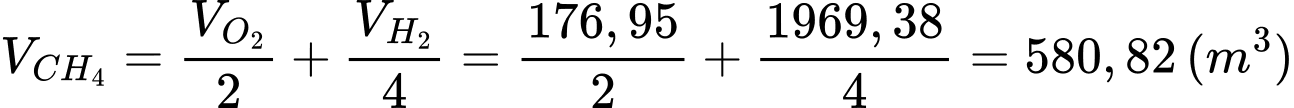
Thể tích hơi nước cần dùng là:
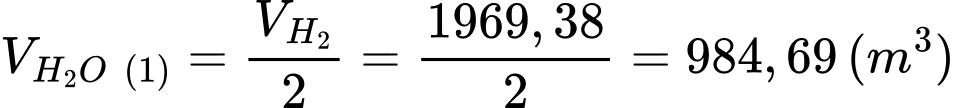
Tổng thể tích CH4 và hơi nước cần dùng là:
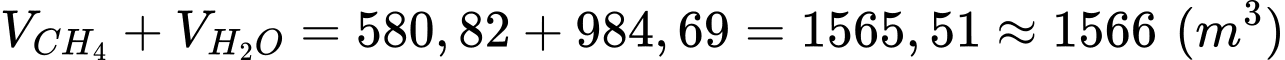
⇒ Điền đáp án: 1566