PHẦN I. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
Câu 1 [705904]: Glucose là đường monosaccharide phổ biến và có nhiều ứng dụng trong đời sống. Trong phân tử glucose ở dạng mạch hở có bao nhiêu nhóm –OH?
A, 5.
B, 4.
C, 6.
D, 3.
-Dạng mạch hở (ít)
+ Glucose: CH2OH-[CHOH]4-CHO có 5 nhóm hydroxy (OH) + 1 nhóm aldehyde (CHO).
- Dạng mạch vòng chủ yếu và luôn chuyển hoá lẫn nhau theo một cân bằng qua dạng mạch hở.
+ Glucose vòng 6 cạnh alpha - glucose và beta -glucose.
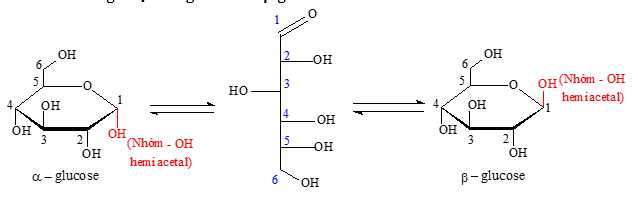
Chọn đáp án A Đáp án: A
+ Glucose: CH2OH-[CHOH]4-CHO có 5 nhóm hydroxy (OH) + 1 nhóm aldehyde (CHO).
- Dạng mạch vòng chủ yếu và luôn chuyển hoá lẫn nhau theo một cân bằng qua dạng mạch hở.
+ Glucose vòng 6 cạnh alpha - glucose và beta -glucose.

Chọn đáp án A Đáp án: A
Câu 2 [702808]: Hợp chất nào thuỷ phân tạo thành butan-2-ol và ethanoic acid?
A, CH3COOCH(CH3)2.
B, CH3COOCH(CH3)CH2CH3.
C, CH3CH(CH3)COOCH2CH3.
D, CH3CH2COOCH(CH3)CH2CH3.
Hợp chất khi thuỷ phân tạo thành alcohol và acid là hợp chất của ester.
Phân tích phản ứng:
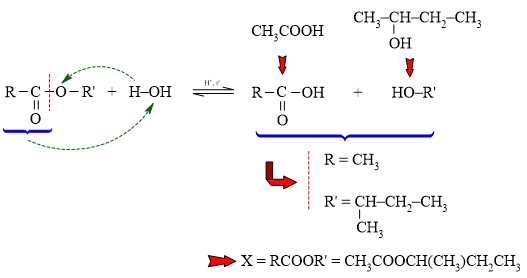
Vậy hợp chất ester này là sec-butyl acetate: CH3COOCH(CH3)CH2CH3
⇝ Chọn đáp án B Đáp án: B
Phân tích phản ứng:

Vậy hợp chất ester này là sec-butyl acetate: CH3COOCH(CH3)CH2CH3
⇝ Chọn đáp án B Đáp án: B
Câu 3 [560410]: Khi nhúng thanh kim loại Cu vào trong dung dịch muối CuSO4 sẽ tạo thành điện cực của cặp oxi hóa – khử nào sau đây?
A, Cu3+/Cu.
B, Cu2+/Cu.
C, Cu2+/Cu3+.
D, Cu2+/SO42–.
Trong kí hiệu cặp oxi hoá – khử, dạng oxi hoá (dạng có số oxi hoá cao hơn) luôn ở bên trên còn dạng khử (dạng có số oxi hoá thấp hơn) luôn ở bên dưới.
→ Cặp oxi hoá - khử của quá trình là Cu2+/Cu.
⇒ Chọn đáp án B Đáp án: B
→ Cặp oxi hoá - khử của quá trình là Cu2+/Cu.
⇒ Chọn đáp án B Đáp án: B
Câu 4 [308564]: Chất có mùi khai là
A, methylamine.
B, methyl formate.
C, aniline.
D, glycine.
✔️ A. Methylamine (CH3NH2) là một amine bậc một có mùi khai đặc trưng (tương tự như mùi ammonia nhưng nhẹ hơn). Mùi khai này là đặc trưng của các amine, do khả năng bay hơi của chúng và tính base yếu.
❌ B. Methyl formate (HCOOCH3) là một ester, thường có mùi thơm dễ chịu, không có mùi khai.
❌ C. Aniline (C6H5NH2) là một amine thơm, có mùi đặc trưng (hắc và khó chịu), nhưng không phải mùi khai.
❌ D. Glycine (H2NCH2COOH) là một amino acid không có mùi khai, mà có mùi nhẹ hoặc không mùi.
⇒ Chọn đáp án A Đáp án: A
❌ B. Methyl formate (HCOOCH3) là một ester, thường có mùi thơm dễ chịu, không có mùi khai.
❌ C. Aniline (C6H5NH2) là một amine thơm, có mùi đặc trưng (hắc và khó chịu), nhưng không phải mùi khai.
❌ D. Glycine (H2NCH2COOH) là một amino acid không có mùi khai, mà có mùi nhẹ hoặc không mùi.
⇒ Chọn đáp án A Đáp án: A
Câu 5 [679600]: Dung dịch nào sau đây được dùng để xử lí lớp cặn CaCO3 bám vào ấm đun nước?
A, Muối ăn.
B, Cồn.
C, Nước vôi trong.
D, Giấm ăn.
HD: Giấm ăn chứa acetic acid: CH3COOH có khả năng hoà tan CaCO3 (thêm nữa là ấm nước dùng để sinh hoạt ăn uống nên cần hoá chất an toàn với sức khoẻ chúng ta, dùng giấm ăn hoặc chanh,... là hợp lý nhất).
Phản ứng xảy ra: 2CH3COOH + CaCO3 → (CH3COO)2Ca + CO2↑ + H2O.
⇒ Chọn đáp án D Đáp án: D
Phản ứng xảy ra: 2CH3COOH + CaCO3 → (CH3COO)2Ca + CO2↑ + H2O.
⇒ Chọn đáp án D Đáp án: D
Câu 6 [561014]: Cấu hình electron biểu diễn theo ô orbital của lớp sát ngoài cùng và ngoài cùng của ion Fe2+ (Z = 26) là
A, 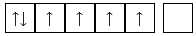

B, 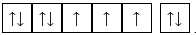

C, 

D, 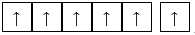

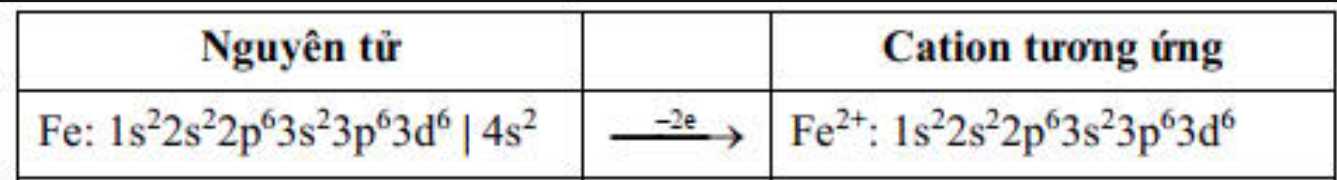
Ion Fe2+ không còn electron trên phân lớp 4s => obital trống, 6 electron ở lớp 3d phân bố đều vào các obital phân lớp 3d.
⟹ Chọn đáp án A
Câu 7 [309446]: Polymer là các phân tử rất lớn hình thành do sự trùng hợp các monomer. Nếu propene CH2=CHCH3 là monomer thì công thức của polymer tương ứng được biễu diễn là
A, 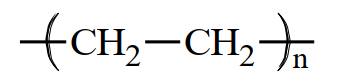
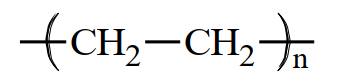
B, 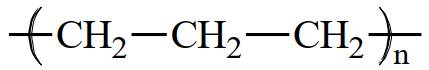
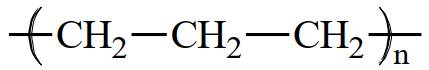
C, 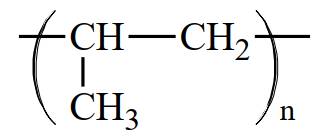
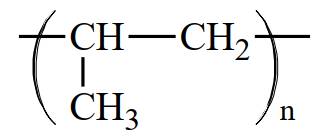
D, 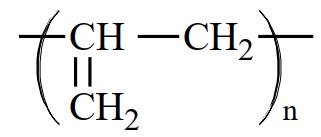
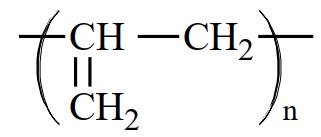
Polymer là các phân tử rất lớn hình thành do sự trùng hợp các monomer. Nếu propene CH2=CHCH3 là monomer thì công thức của polymer tương ứng được biễu diễn là ―(CH(CH3) ― CH2)n―
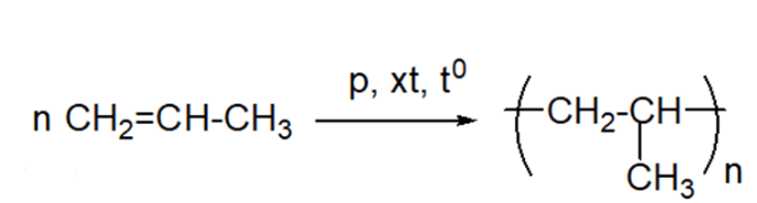
⇒ Chọn đáp án: C Đáp án: C

⇒ Chọn đáp án: C Đáp án: C
Câu 8 [252269]: Cho 5 gam zinc viên vào cốc đựng 50 mL dung dịch H2SO4 4 M ở nhiệt độ thường (25oC). Trường hợp nào tốc độ phản ứng không đổi?
A, Thay 5 gam zinc viên bằng 5 gam zinc bột.
B, Thay dung dịch H2SO4 4 M bằng dung dịch H2SO4 2 M.
C, Thực hiện phản ứng ở 50oC.
D, Dùng gấp đôi thể tích dung dịch H2SO4 4 M.
Tăng thể tích dung dịch H2SO4 nhưng với nồng độ không đổi thì không làm thay đổi tốc độ phản ứng Đáp án: D
Câu 9 [705477]: Tã lót trẻ em sau khi được giặt sạch vẫn còn mùi khai do vẫn lưu lại một lượng ammonia. Đề khử hoàn toàn mùi của ammonia thì người ta cho vào nước xả cuối cùng một ít hoá chất có sẵn trong nhà. Hãy chọn hoá chất thích hợp:
A, Phèn chua.
B, Giấm ăn.
C, Muối ăn.
D, Nước gừng tươi.
Mùi khai còn lại trên tã lót là do ammonia (NH3), một hợp chất có tính base yếu.
Giấm ăn chứa acetic acid (CH3COOH), có thể phản ứng với ammonia theo phương trình:
NH3 + CH3COOH → CH3COO−NH4+
Sản phẩm tạo thành là muối ammonium acetate, tan tốt trong nước và không có mùi khai. Vì vậy, giấm ăn giúp khử mùi ammonia hiệu quả.
⇒ Chọn đáp án B Đáp án: B
Giấm ăn chứa acetic acid (CH3COOH), có thể phản ứng với ammonia theo phương trình:
NH3 + CH3COOH → CH3COO−NH4+
Sản phẩm tạo thành là muối ammonium acetate, tan tốt trong nước và không có mùi khai. Vì vậy, giấm ăn giúp khử mùi ammonia hiệu quả.
⇒ Chọn đáp án B Đáp án: B
Câu 10 [100076]: Khi thay thế nguyên tử H (đính với carbon bậc III) trong phân tử 2-methylbutane bằng nguyên tử Br, thu được dẫn xuất monobromo có tên thay thế là
A, 2-bromo-2-methylbutane.
B, 2-bromopentane.
C, 3-bromo-3-methylbutane.
D, 2-methyl-2-bromobutane.
HD: quá trình tạo sản phẩm thế và cách đánh số C theo quy tắc như sau:
![535858[lg].png](https://asset.moon.vn/img/ai/Teachers/rongden_167/ProS2018/B%C3%80I%203/535858[lg].png)
||→ đọc tên của sản phẩm thế là: 2-bromo-2-methylbutane. Chọn đáp án A. ♥.
Đáp án: A
![535858[lg].png](https://asset.moon.vn/img/ai/Teachers/rongden_167/ProS2018/B%C3%80I%203/535858[lg].png)
||→ đọc tên của sản phẩm thế là: 2-bromo-2-methylbutane. Chọn đáp án A. ♥.
Đáp án: A
Câu 11 [702617]: Ở độ pH = 7, các amino acid: lysine (Lys), glycine (Gly) và glutamic acid (Glu) tồn tại ở các dạng như sau:
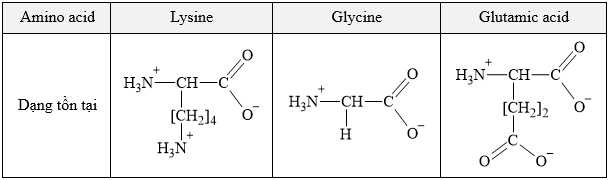
Kết quả khi tiến hành điện di hỗn hợp của ba amino acid được thể hiện trong hình dưới đây:
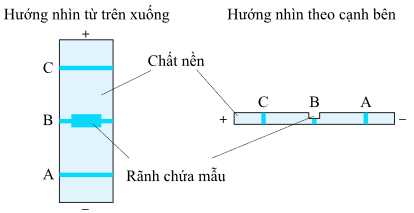
Cho các nhận định sau về quá trình điện di:
(a) Tại môi trường pH = 7 thì tất cả các nhóm NH2 của lysine sẽ chuyển thành nhóm NH3+.
(b) Chất B là glycine có phân tử khối nhỏ nhất nên sẽ không di chuyển.
(c) Chất C là glutamic acid sẽ di chuyển về phía cực dương.
(d) Theo thí nghiệm trên, có thể tách riêng các amino acid trong hỗn hợp của chúng.
Các nhận định đúng là

Kết quả khi tiến hành điện di hỗn hợp của ba amino acid được thể hiện trong hình dưới đây:

Cho các nhận định sau về quá trình điện di:
(a) Tại môi trường pH = 7 thì tất cả các nhóm NH2 của lysine sẽ chuyển thành nhóm NH3+.
(b) Chất B là glycine có phân tử khối nhỏ nhất nên sẽ không di chuyển.
(c) Chất C là glutamic acid sẽ di chuyển về phía cực dương.
(d) Theo thí nghiệm trên, có thể tách riêng các amino acid trong hỗn hợp của chúng.
Các nhận định đúng là
A, (a), (b).
B, (a), (c).
C, (a), (c), (d).
D, (b), (c), (d).
Phân tích các nhận định:
✔️ (a) Đúng. Tại môi trường pH = 7 (môi trường trung tính) thì amino acid tồn tại ở dạng ion lưỡng cực nên tất cả các nhóm NH2 của lysine sẽ chuyển thành nhóm NH3+ và nhóm COOH sẽ chuyển thành nhóm COO‒.
❌ (b) Sai. Chất B là glycine không di chuyển do có tổng điện tích bằng 0 ở pH = 7 chứ không ảnh hưởng bởi phân tử khối.
✔️ (c) Chất C là glutamic acid sẽ di chuyển về phía cực dương do có tổng điện tích ‒1 ở pH = 7.
✔️ (d) Theo thí nghiệm trên, có thể tách riêng các amino acid trong hỗn hợp của chúng vì lysine với điện tích +1 sẽ di chuyển về phía cực âm, glutamic acid di chuyển về phía cực dương với điện tích là -1 và glycine không di chuyển trong môi trường trung tính.
Các nhận định đúng là (a) (c) (d)
⇒ Chọn đáp án C Đáp án: C
✔️ (a) Đúng. Tại môi trường pH = 7 (môi trường trung tính) thì amino acid tồn tại ở dạng ion lưỡng cực nên tất cả các nhóm NH2 của lysine sẽ chuyển thành nhóm NH3+ và nhóm COOH sẽ chuyển thành nhóm COO‒.
❌ (b) Sai. Chất B là glycine không di chuyển do có tổng điện tích bằng 0 ở pH = 7 chứ không ảnh hưởng bởi phân tử khối.
✔️ (c) Chất C là glutamic acid sẽ di chuyển về phía cực dương do có tổng điện tích ‒1 ở pH = 7.
✔️ (d) Theo thí nghiệm trên, có thể tách riêng các amino acid trong hỗn hợp của chúng vì lysine với điện tích +1 sẽ di chuyển về phía cực âm, glutamic acid di chuyển về phía cực dương với điện tích là -1 và glycine không di chuyển trong môi trường trung tính.
Các nhận định đúng là (a) (c) (d)
⇒ Chọn đáp án C Đáp án: C
Câu 12 [247390]: Nguyên tố M có khả năng tạo hợp chất với oxi ở mức hóa trị cao nhất là M2O5. Trong hợp chất của M tạo với hydrogen thì hydrogen chiếm 8,82% về khối lượng. M là
A, N.
B, P.
C, Al.
D, C.
Hợp chất M tạo với H là MH3. 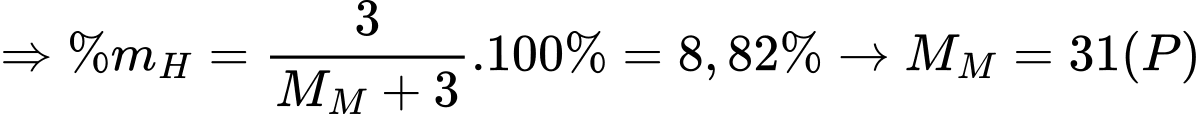
⟹ Chọn đáp án B Đáp án: B
Xét hợp chất MH3:
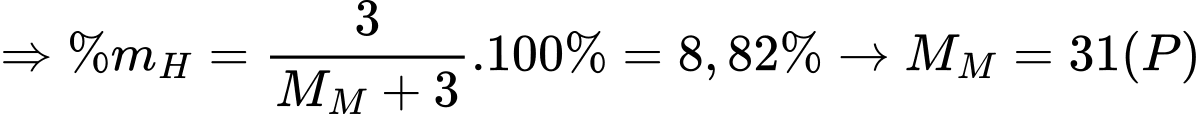
⟹ Chọn đáp án B
Câu 13 [706068]: Đổ dung dịch NaCl bão hòa vào dung dịch gồm sodium palmititate và glycerol. Phát biểu nào sau đây là đúng?
A, Chất rắn màu trắng nổi lên là glycerol.
B, Chất lỏng ở lớp dưới gồm chỉ có dung dịch sodium chloride bão hòa.
C, Chất lỏng ở dưới khả năng hòa tan Cu(OH)2 tạo dung dịch xanh lam thẫm.
D, Chất rắn màu trắng lắng xuống dưới đáy ống nghiệm là xà phòng.
Phương trình phản ứng:
(C15H31COO)3C3H5 + 3NaOH → 3C15H31COONa + C3H5(OH)3
Phân tích các đáp án :
❌A. Sai. Glycerol là một chất lỏng, không phải chất rắn, và nó tan tốt trong nước muối bão hòa.
❌B. Sai. Lớp dưới gồm glycerol, NaCl bão hòa.
✔️C. Sai. Glycerol có nhiều nhóm -OH kề nhau nên có khả năng hòa tan Cu(OH)2 có khả năng tạo phức
❌D. Đúng. Lớp xà phòng nằm ở bên trên.
⟹ Chọn đáp án C Đáp án: C
(C15H31COO)3C3H5 + 3NaOH → 3C15H31COONa + C3H5(OH)3
Phân tích các đáp án :
❌A. Sai. Glycerol là một chất lỏng, không phải chất rắn, và nó tan tốt trong nước muối bão hòa.
❌B. Sai. Lớp dưới gồm glycerol, NaCl bão hòa.
✔️C. Sai. Glycerol có nhiều nhóm -OH kề nhau nên có khả năng hòa tan Cu(OH)2 có khả năng tạo phức
❌D. Đúng. Lớp xà phòng nằm ở bên trên.
⟹ Chọn đáp án C Đáp án: C
Câu 14 [705361]: Tiến hành các thí nghiệm sau:
(a) Cho kim loại đồng (copper) vào dung dịch iron(II) nitrate.
(b) Sục khí carbonic vào dung dịch sodium hydroxide.
(c) Cho sodium hidrogencarbonate vào dung dịch calcium chloride rồi đun nóng.
(d) Cho Fe(NO3)2 vào dung dịch NaHSO4.
Những thí nghiệm có phản ứng hóa học xảy ra là
(a) Cho kim loại đồng (copper) vào dung dịch iron(II) nitrate.
(b) Sục khí carbonic vào dung dịch sodium hydroxide.
(c) Cho sodium hidrogencarbonate vào dung dịch calcium chloride rồi đun nóng.
(d) Cho Fe(NO3)2 vào dung dịch NaHSO4.
Những thí nghiệm có phản ứng hóa học xảy ra là
A, (a), (b), (c).
B, (a), (c), (d).
C, (a), (b), (d).
D, (b), (c), (d).
Phân tích các thí nghiệm:
❌ Thí nghiệm (a) Cho kim loại đồng (copper) vào dung dịch iron(II) nitrate → Không có phản ứng
✔️ Thí nghiệm (b) Sục khí carbonic vào dung dịch sodium hydroxide.
CO2 + NaOH → Na2CO3 + H2O
Na2CO3 + H2O + CO2 → 2NaHCO3
✔️ Thí nghiệm (c) Cho sodium hidrogencarbonate vào dung dịch calcium chloride rồi đun nóng.
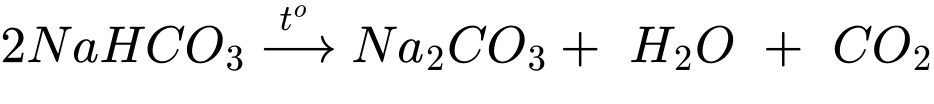
Na2CO3 + CaCl2 → CaCO3 + 2NaCl
✔️ Thí nghiệm (d) Cho Fe(NO3)2 vào dung dịch NaHSO4.
9Fe(NO3)2 + 12NaHSO4 → 2Fe2(SO4)3 + 5Fe(NO3)3 + 6Na2SO4 + 3NO + 6H2O
⇒ Chọn đáp án D Đáp án: D
❌ Thí nghiệm (a) Cho kim loại đồng (copper) vào dung dịch iron(II) nitrate → Không có phản ứng
✔️ Thí nghiệm (b) Sục khí carbonic vào dung dịch sodium hydroxide.
CO2 + NaOH → Na2CO3 + H2O
Na2CO3 + H2O + CO2 → 2NaHCO3
✔️ Thí nghiệm (c) Cho sodium hidrogencarbonate vào dung dịch calcium chloride rồi đun nóng.
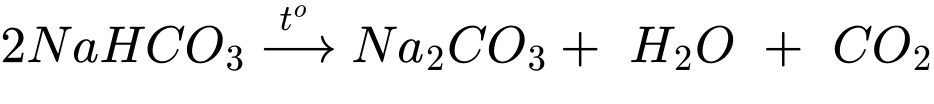
Na2CO3 + CaCl2 → CaCO3 + 2NaCl
✔️ Thí nghiệm (d) Cho Fe(NO3)2 vào dung dịch NaHSO4.
9Fe(NO3)2 + 12NaHSO4 → 2Fe2(SO4)3 + 5Fe(NO3)3 + 6Na2SO4 + 3NO + 6H2O
⇒ Chọn đáp án D Đáp án: D
Câu 15 [704026]: Phát biểu nào sau đây về sulfur dioxide (SO2) là không đúng?
A, Có độc tính đối với con người.
B, Dùng để tẩy trắng giấy, vải, sợi, đường.
C, Phản ứng được với đá vôi ở ngay nhiệt độ thường.
D, Được tạo thành từ hoạt động của núi lửa trong tự nhiên.
Phân tích các phát biểu:
✔️A. Đúng. Sulfur dioxide là khí độc, hít thở không khí chứa sulfur dioxide vượt ngưỡng cho phép sẽ gây viêm đường hô hấp.
✔️B. Đúng. Do có khả năng tẩy trắng và diệt khuẩn, sulfur dioxide được sử dụng để tẩy trắng bột giấy, khử màu trong sản xuất đường, chống nấm mốc cho sản phẩm mây tre đan,...
❌ C. Sai. Sulfur dioxide phản ứng với đá vôi cần cung cấp nhiệt độ.
✔️D. Đúng. SO2 chủ yếu được phát sinh từ các hoạt động công nghiệp như đốt cháy nhiên liệu hóa thạch (than, dầu, khí tự nhiên) và từ các quá trình luyện kim. Trong tự nhiên, SO2 cũng được thải ra qua các hiện tượng phun trào núi lửa.
⇒ Chọn đáp án C Đáp án: C
✔️A. Đúng. Sulfur dioxide là khí độc, hít thở không khí chứa sulfur dioxide vượt ngưỡng cho phép sẽ gây viêm đường hô hấp.
✔️B. Đúng. Do có khả năng tẩy trắng và diệt khuẩn, sulfur dioxide được sử dụng để tẩy trắng bột giấy, khử màu trong sản xuất đường, chống nấm mốc cho sản phẩm mây tre đan,...
❌ C. Sai. Sulfur dioxide phản ứng với đá vôi cần cung cấp nhiệt độ.
✔️D. Đúng. SO2 chủ yếu được phát sinh từ các hoạt động công nghiệp như đốt cháy nhiên liệu hóa thạch (than, dầu, khí tự nhiên) và từ các quá trình luyện kim. Trong tự nhiên, SO2 cũng được thải ra qua các hiện tượng phun trào núi lửa.
⇒ Chọn đáp án C Đáp án: C
Câu 16 [705930]: Một người ngủ quên trong ô tô tắt máy, đóng kín cửa. Sau một thời gian, khi hàm lượng oxygen trong xe giảm xuống còn 16% thể tích không khí thì có người kịp thời phát hiện, phá vỡ kính xe để đưa đi cấp cứu. Tại thời điểm được cứu, tốc độ “phản ứng hô hấp" (υhô hấp = k×O2) của người trong xe giảm bao nhiêu lần so với bình thường? Biết ban đầu oxygen chiếm 21% thể tích không khí.
A, 1,2500.
B, 1,3125.
C, 1,1125.
D, 1,4325.
Tốc độ hô hấp ban đầu 
Tốc độ khi oxygen giảm xuống
Tại thời điểm cấp cứu tốc độ của phản ứng hô hấp giảm xuống là
Chọn đáp án B Đáp án: B
Tốc độ khi oxygen giảm xuống
Tại thời điểm cấp cứu tốc độ của phản ứng hô hấp giảm xuống là
Chọn đáp án B Đáp án: B
Sử dụng thông tin cho dưới đây để trả lời các câu số 17 – 18:
Phản ứng sau xảy ra trong dung dịch nước của Cd2+:
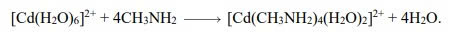
Câu 17 [703990]: Trong hai phức chất ở phương trình trên, số oxi hóa của nguyên tử trung tâm là bao nhiêu?
A, +4.
B, +2.
C, +6.
D, +3.
⭐ Trong [Cd(H2O)6]2+, H2O là phối tử trung hòa (không làm thay đổi số oxi hóa của nguyên tử trung tâm). Do đó, số oxi hóa của Cd là +2 để cân bằng điện tích tổng cộng của phức là +2.
⭐ Trong [Cd(CH3NH2)4(H2O)2]2+, cả CH3NH2 và H2O đều là phối tử trung hòa. Vì vậy, số oxi hóa của Cd vẫn là +2.
⇒ Chọn đáp án B Đáp án: B
⭐ Trong [Cd(CH3NH2)4(H2O)2]2+, cả CH3NH2 và H2O đều là phối tử trung hòa. Vì vậy, số oxi hóa của Cd vẫn là +2.
⇒ Chọn đáp án B Đáp án: B
Câu 18 [703991]: Phát biểu nào sau đây không đúng?
A, Trong phức chất [Cd(CH3NH2)4(H2O)2]2+ chỉ có một loại phối tử.
B, CH3NH2 tạo liên kết với Cd qua nguyên tử nitrogen.
C, H2O tạo liên kết với Cd qua nguyên tử oxygen.
D, Nguyên tử Cd tạo sáu liên kết sigma với các phối tử.
Phân tích các phát biểu:
❌ A. Sai. Phức chất này có hai loại phối tử: CH3NH2 (methylamine) và H2O (nước).
✔️ B. Đúng. Trong CH3NH2, nguyên tử N có cặp electron tự do, nên tạo liên kết phối trí với ion Cd2+.
✔️ C. Đúng. Nguyên tử O trong H2O có cặp electron tự do, nên tạo liên kết phối trí với ion Cd2+.
✔️ D. Đúng. Cd liên kết với 4 phân tử CH3NH2 và 2 phân tử H2O, tổng cộng là 6 liên kết sigma.
⇒ Chọn đáp án A Đáp án: A
❌ A. Sai. Phức chất này có hai loại phối tử: CH3NH2 (methylamine) và H2O (nước).
✔️ B. Đúng. Trong CH3NH2, nguyên tử N có cặp electron tự do, nên tạo liên kết phối trí với ion Cd2+.
✔️ C. Đúng. Nguyên tử O trong H2O có cặp electron tự do, nên tạo liên kết phối trí với ion Cd2+.
✔️ D. Đúng. Cd liên kết với 4 phân tử CH3NH2 và 2 phân tử H2O, tổng cộng là 6 liên kết sigma.
⇒ Chọn đáp án A Đáp án: A
PHẦN II. Thí sinh trả lời từ câu 1 đến câu 4. Trong mỗi ý a), b), c), d) ở mỗi câu, thí sinh chọn đúng hoặc sai.
Câu 19 [702845]: M là chất đầu quan trọng trong công nghiệp hóa chất, đặc biệt là trong sản xuất thuốc nhuộm azo - loại thuốc nhuộm phổ biến dùng trong ngành dệt may. Ngoài ra, M còn là nguyên liệu cơ bản để sản xuất các loại nhựa và cao su tổng hợp. Cho biết số sóng hấp thụ đặc trưng của M trên phổ hồng ngoại như sau:
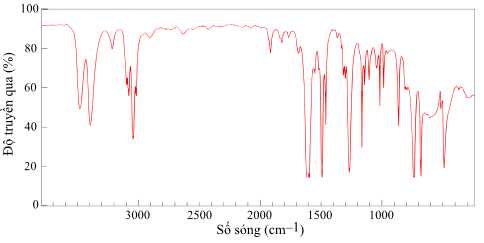
Cho bảng số sóng đặc trưng của các liên kết ở bảng sau:
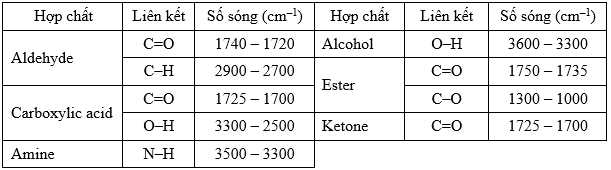

Cho bảng số sóng đặc trưng của các liên kết ở bảng sau:

Phân tích các phát biểu:
❌ a) Sai. Chất đầu trong sản xuất thuốc nhuộm azo là aniline (C6H5NH2) nên M là hợp chất hữu cơ được hình thành khi thay thế một nguyên tử H trong phân tử NH3 bằng một gốc hydrocarbon.
✔️ b) Đúng. Aniline có khả năng phản ứng với nước bromine tạo kết tủa trắng:
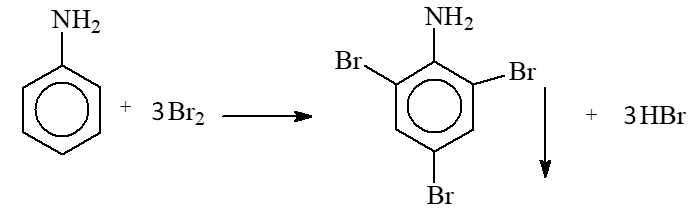
✔️ c) Đúng. Phổ hồng ngoại của M có tín hiệu trong dải hấp thụ 3500-3300 cm-1, là sóng hấp thu đặc trưng của liên kết N–H trong nhóm chức amine.
✔️ d) Dựa vào phổ hồng ngoại có thể phân biệt M với các hợp chất có nhóm chức carbonyl. Do các hợp chất carbonyl chứa C=O nằm trong dải hấp phụ 1740-1720 cm-1 (aldehyde); 1725-1700 cm-1 (ketone) mà M không có.
❌ a) Sai. Chất đầu trong sản xuất thuốc nhuộm azo là aniline (C6H5NH2) nên M là hợp chất hữu cơ được hình thành khi thay thế một nguyên tử H trong phân tử NH3 bằng một gốc hydrocarbon.
✔️ b) Đúng. Aniline có khả năng phản ứng với nước bromine tạo kết tủa trắng:

✔️ c) Đúng. Phổ hồng ngoại của M có tín hiệu trong dải hấp thụ 3500-3300 cm-1, là sóng hấp thu đặc trưng của liên kết N–H trong nhóm chức amine.
✔️ d) Dựa vào phổ hồng ngoại có thể phân biệt M với các hợp chất có nhóm chức carbonyl. Do các hợp chất carbonyl chứa C=O nằm trong dải hấp phụ 1740-1720 cm-1 (aldehyde); 1725-1700 cm-1 (ketone) mà M không có.
Câu 20 [702844]: Trong công nghiệp, một trong những nguồn chính để sản xuất iodine là rong biển. Quy trình được thực hiện như sau:
Bước 1: Người ta phơi khô rong biển, đốt thành tro, ngâm tro trong nước để hòa tan hết các muối.
Bước 2: Gạn lấy dung dịch, đem cô cạn cho đến khi các muối kết tinh, làm lạnh dung dịch xuống 20 °C, phần lớn muối sodium chloride và muối sodium sulfate lắng xuống, còn muối iodide ở lại trong dung dịch.
Bước 3: Cho dung dịch này tác dụng với một lượng khí chlorine (không lấy dư) theo phương trình hóa học: 2NaI(aq) + Cl2(g) 2NaCl(aq) + I2(aq)
2NaCl(aq) + I2(aq)
Bước 4: Sau đó chưng cất để được iodine.
Bước 1: Người ta phơi khô rong biển, đốt thành tro, ngâm tro trong nước để hòa tan hết các muối.
Bước 2: Gạn lấy dung dịch, đem cô cạn cho đến khi các muối kết tinh, làm lạnh dung dịch xuống 20 °C, phần lớn muối sodium chloride và muối sodium sulfate lắng xuống, còn muối iodide ở lại trong dung dịch.
Bước 3: Cho dung dịch này tác dụng với một lượng khí chlorine (không lấy dư) theo phương trình hóa học: 2NaI(aq) + Cl2(g)
 2NaCl(aq) + I2(aq)
2NaCl(aq) + I2(aq)Bước 4: Sau đó chưng cất để được iodine.
Phân tích các phát biểu:
✔️ a) Đúng. Tính oxi hóa của các halogen giảm dần theo thứ tự: F2 > Cl2 > Br2 > I2 nên phản ứng trên chứng tỏ tính oxi hóa của chlorine mạnh hơn iodine.
✔️ b) Đúng. Ở 20 °C, độ tan trong nước của sodium iodide lớn hơn độ tan của sodium chloride do sau phản ứng phần lớn muối NaCl và muối Na2SO4 lắng xuống, còn muối iodide ở lại trong dung dịch.
❌ c) Sai. Không thể thay khí chlorine bằng khí florine vì fluorine sẽ phản ứng trước với nước trong dung dịch, sẽ không phản ứng với NaI:
✔️ a) Đúng. Tính oxi hóa của các halogen giảm dần theo thứ tự: F2 > Cl2 > Br2 > I2 nên phản ứng trên chứng tỏ tính oxi hóa của chlorine mạnh hơn iodine.
✔️ b) Đúng. Ở 20 °C, độ tan trong nước của sodium iodide lớn hơn độ tan của sodium chloride do sau phản ứng phần lớn muối NaCl và muối Na2SO4 lắng xuống, còn muối iodide ở lại trong dung dịch.
❌ c) Sai. Không thể thay khí chlorine bằng khí florine vì fluorine sẽ phản ứng trước với nước trong dung dịch, sẽ không phản ứng với NaI:
2F2 + 2H2O ⟶ 4HF + O2↑
✔️ d) Đúng. Khi dùng dư Cl2 thì Cl2 sẽ phản ứng với I2 gây thất thoát:
I2 + 5Cl2 + 6H2O ⟶ 2HIO3 + 10HCl
Câu 21 [703973]: Tiến trình chuẩn độ acid-base có thể được theo dõi bằng cách đo độ pH của dung dịch được chuẩn độ trong khi thêm base. Đồ thị kết quả, được gọi là đường cong chuẩn độ, là đồ thị của độ pH phụ thuộc vào thể tích của base thêm vào. Đồ thị hiển thị ở dưới đây là đường cong chuẩn độ của acid HX chưa biết nồng độ, được chuẩn độ bằng NaOH 0,100 M.
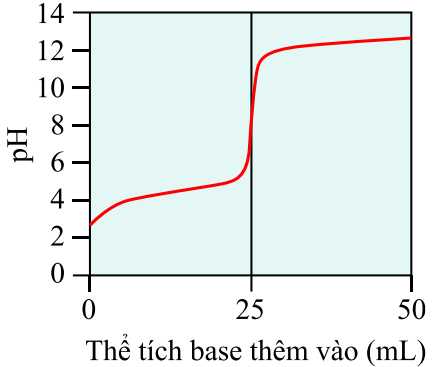

Phân tích các phát biểu:
✔️ a) Đúng. Từ đồ thị thấy rằng khi thể tích của dung dịch base dùng để chuẩn độ tăng thì pH của dung dịch tăng. Ban đầu pH dung dịch khoảng bằng 3, khi thêm thể tích đến 25 mL thì pH lên đến khoảng 12.
❌ b) Sai. Tại điểm tương đương được đánh dấu dưới đây, pH của dung dịch xác định được ở khoảng hơn 8.
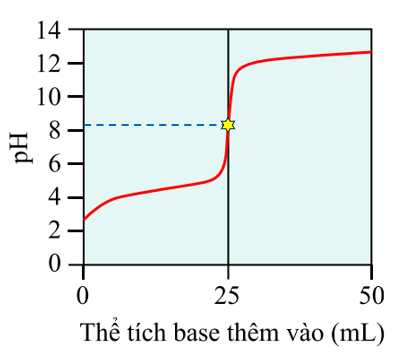
❌ c) Sai. Tại điểm tương đương đã được đánh dấu, dóng xuống thì thu được thể tích dung dịch NaOH đã dùng là 25 mL.
❌ d) Sai. Để xác định được nồng độ của acid HX thì ta cần biết số mol HX và thể tích dung dịch HX đã dùng theo công thức:
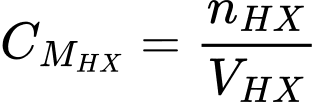
Số mol của HX có thể tính được theo số mol của NaOH theo phương trình: HX + NaOH ⟶ NaX + H2O; nên không cần biết khối lượng của HX.
✔️ a) Đúng. Từ đồ thị thấy rằng khi thể tích của dung dịch base dùng để chuẩn độ tăng thì pH của dung dịch tăng. Ban đầu pH dung dịch khoảng bằng 3, khi thêm thể tích đến 25 mL thì pH lên đến khoảng 12.
❌ b) Sai. Tại điểm tương đương được đánh dấu dưới đây, pH của dung dịch xác định được ở khoảng hơn 8.

❌ c) Sai. Tại điểm tương đương đã được đánh dấu, dóng xuống thì thu được thể tích dung dịch NaOH đã dùng là 25 mL.
❌ d) Sai. Để xác định được nồng độ của acid HX thì ta cần biết số mol HX và thể tích dung dịch HX đã dùng theo công thức:
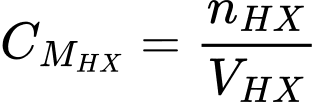
Số mol của HX có thể tính được theo số mol của NaOH theo phương trình: HX + NaOH ⟶ NaX + H2O; nên không cần biết khối lượng của HX.
Câu 22 [1108845]: Một học sinh tiến hành điều chế xà phòng từ dầu dừa như sau:
Bước 1: Cân m gam NaOH cho vào cốc đã chứa sẵn khoảng 100 mL nước và khuấy đều. Để nguội đến khoảng 38 oC.
Bước 2: Cho 300 gam dầu dừa vào cốc thuỷ tinh chịu nhiệt, đun nhẹ và khuấy đều để đưa nhiệt độ của dầu dừa lên khoảng 48 oC.
Bước 3: Rót dung dịch NaOH đã chuẩn bị (phía trên) vào cốc chứa dầu dừa và khuấy nhanh, liên tục trong 30 phút. Khi hỗn hợp chuyển màu sáng kem, sệt, mịn thì ngừng. Thêm ít tinh dầu chanh và khuấy đều.
Bước 4: Đổ hỗn hợp thu được ở bước 3 vào khuôn, vỗ nhẹ thành khuôn để đuổi không khí ra ngoài. Để khuôn nơi khô ráo. Sau
khoảng 24 giờ, lấy xà phòng đã đóng rắn ra khỏi khuôn. Sau 4 – 5 ngày, xà phòng có thể sử dụng được.
Biết chỉ số xà phòng hóa là số miligam KOH cần để xà phòng hóa triglyceride và trung hòa acid béo tự do trong 1g chất béo; chỉ số xà phòng hóa của dầu dừa là 257. Học sinh trên đã lấy m gam NaOH ứng với lượng KOH cần dùng.
Bước 1: Cân m gam NaOH cho vào cốc đã chứa sẵn khoảng 100 mL nước và khuấy đều. Để nguội đến khoảng 38 oC.
Bước 2: Cho 300 gam dầu dừa vào cốc thuỷ tinh chịu nhiệt, đun nhẹ và khuấy đều để đưa nhiệt độ của dầu dừa lên khoảng 48 oC.
Bước 3: Rót dung dịch NaOH đã chuẩn bị (phía trên) vào cốc chứa dầu dừa và khuấy nhanh, liên tục trong 30 phút. Khi hỗn hợp chuyển màu sáng kem, sệt, mịn thì ngừng. Thêm ít tinh dầu chanh và khuấy đều.
Bước 4: Đổ hỗn hợp thu được ở bước 3 vào khuôn, vỗ nhẹ thành khuôn để đuổi không khí ra ngoài. Để khuôn nơi khô ráo. Sau
khoảng 24 giờ, lấy xà phòng đã đóng rắn ra khỏi khuôn. Sau 4 – 5 ngày, xà phòng có thể sử dụng được.
Biết chỉ số xà phòng hóa là số miligam KOH cần để xà phòng hóa triglyceride và trung hòa acid béo tự do trong 1g chất béo; chỉ số xà phòng hóa của dầu dừa là 257. Học sinh trên đã lấy m gam NaOH ứng với lượng KOH cần dùng.
Phản ứng xà phòng hóa: Chất béo (trong dầu dừa) + 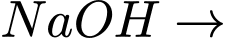 Muối của acid béo (xà phòng) + Glycerol.
Muối của acid béo (xà phòng) + Glycerol.
✔️Nhận định a) – Đúng, vì: Bước 3 là lúc cho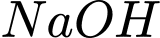 vào dầu dừa và đun nóng, khuấy đều để phản ứng xảy ra.
vào dầu dừa và đun nóng, khuấy đều để phản ứng xảy ra.
✔️Nhận định b) – Đúng, vì: Phản ứng xà phòng hóa chất béo luôn sinh ra glycerol.
✔️Nhận định c) – Đúng, vì: Tính toán giá trị m:
o Chỉ số xà phòng hóa là 257 1g chất béo cần 257 mg
1g chất béo cần 257 mg  .
.
o 300g chất béo cần: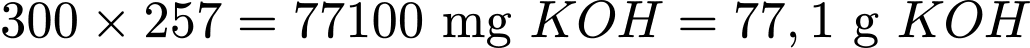 .
.
o Số mol là:
là: 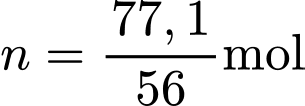 .
.
o Vì học sinh lấy lượng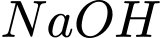 ứng với lượng nên ta có:
ứng với lượng nên ta có: 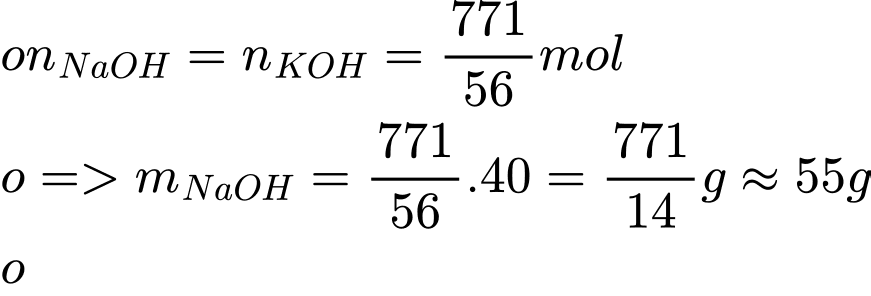
❌Nhận định d) – Sai, vì: Tinh dầu chanh được thêm vào ở cuối để tạo hương thơm cho xà phòng, không phải là chất xúc tác cho phản ứng.
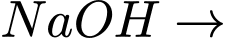 Muối của acid béo (xà phòng) + Glycerol.
Muối của acid béo (xà phòng) + Glycerol.✔️Nhận định a) – Đúng, vì: Bước 3 là lúc cho
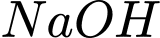 vào dầu dừa và đun nóng, khuấy đều để phản ứng xảy ra.
vào dầu dừa và đun nóng, khuấy đều để phản ứng xảy ra.✔️Nhận định b) – Đúng, vì: Phản ứng xà phòng hóa chất béo luôn sinh ra glycerol.
✔️Nhận định c) – Đúng, vì: Tính toán giá trị m:
o Chỉ số xà phòng hóa là 257
 1g chất béo cần 257 mg
1g chất béo cần 257 mg  .
.o 300g chất béo cần:
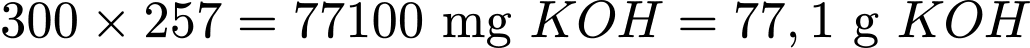 .
.o Số mol
 là:
là: 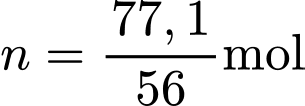 .
.o Vì học sinh lấy lượng
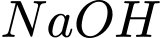 ứng với lượng nên ta có:
ứng với lượng nên ta có: 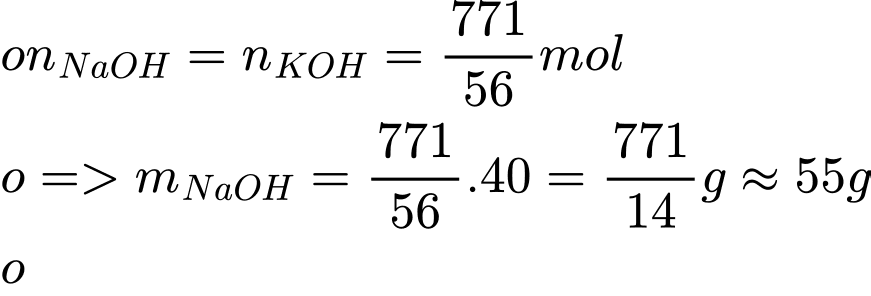
❌Nhận định d) – Sai, vì: Tinh dầu chanh được thêm vào ở cuối để tạo hương thơm cho xà phòng, không phải là chất xúc tác cho phản ứng.
PHẦN III. Thí sinh trả lời từ câu 1 đến 6. Thí sinh điền kết quả mỗi câu vào mỗi ô trả lời tương ứng theo hướng dẫn của phiếu trả lời.
Câu 23 [683551]: Dẫn 10,8 gam but-1-yne qua dung dịch AgNO3 trong NH3 dư, sau phản ứng thu a gam kết tủa. Giá trị của a là bao nhiêu?
Điền đáp án: __________
Điền đáp án: __________
Ta có: Số mol của but-1-yne: nC4H6 = 10,8 ÷ 54 = 0,2mol
Phương trình phản ứng:
CH≡C-CH2-CH3 + AgNO3 + NH3 ⟶ CAg≡C-CH2-CH3 ↓ + NH4NO3
Theo phương trình: nkết tủa = nC4H6 = 0,2 mol
Khối lượng kết tủa thu được là: m↓ = 0,2 × 161 = 32,2 gam
⇒ Điền đáp án: 32,2
Phương trình phản ứng:
CH≡C-CH2-CH3 + AgNO3 + NH3 ⟶ CAg≡C-CH2-CH3 ↓ + NH4NO3
Theo phương trình: nkết tủa = nC4H6 = 0,2 mol
Khối lượng kết tủa thu được là: m↓ = 0,2 × 161 = 32,2 gam
⇒ Điền đáp án: 32,2
Câu 24 [705793]: Trong công nghiệp, kim loại sắt (Iron, Fe) được sản xuất bằng phương pháp nhiệt luyện quặng hemantite. Với hiệu suất chuyển hóa từ Fe2O3 thành Fe là 75%. Để sản xuất được 5,6 tấn Fe cần dùng bao nhiêu tấn nguyên liệu quặng hematite biết quặng có chưa 70% Fe2O3. (Làm tròn đến hàng phần mười)
Trong Fe2O3 có 2 nguyên tử Fe
Số mol Fe = m ÷ M = 5,6.106 ÷ 56 = 0,1.106 mol
⇒ Số mol Fe2O3 = nFe ÷ 2 ÷ Hiệu suất = 0,1 ÷ 2 ÷ 75%
Do trong quặng chứa 70% Fe2O3
⇒ mquặng = mFe2O3 ÷ 70% = 0,1.106 ÷ 2 ÷ 75% × 160 ÷ 70%
= 15238095 gam ≈ 15,2 tấn
⇒ Điền đáp án : 15,2
Số mol Fe = m ÷ M = 5,6.106 ÷ 56 = 0,1.106 mol
⇒ Số mol Fe2O3 = nFe ÷ 2 ÷ Hiệu suất = 0,1 ÷ 2 ÷ 75%
Do trong quặng chứa 70% Fe2O3
⇒ mquặng = mFe2O3 ÷ 70% = 0,1.106 ÷ 2 ÷ 75% × 160 ÷ 70%
= 15238095 gam ≈ 15,2 tấn
⇒ Điền đáp án : 15,2
Câu 25 [705849]: L-leucine hydrochloride, [(CH3)2CHCH2CH(NH3)COOH]+Cl‒, được sử dụng làm chất bổ sung amino acid thiết yếu trong chế độ ăn uống. Thêm từ từ 50 mL dung dịch leucine hydrochloride 0,1 M vào dung dịch NaOH 0,2 M. Thể tích tối thiểu dung dịch NaOH cần dùng để L-leucine hydrochloride phân li toàn bộ H+ là bao nhiêu mL?
Đổi 50 mL = 0,05 L
[(CH3)2CHCH2CH(NH3)COOH] + Cl- + 2NaOH → (CH3)2CHCH2CH(NH3)COONa + NaCl + H2O
Số mol của L-leucine hydrochloride là nL-leucine hydrochloride = 0,05.0,1 = 0,005 mol
Từ phương trình hóa học số mol của NaOH là 0,01 mol
Thể tích tối thiểu của dung dịch NaOH cần dùng là VNaOH = 0,01:0,2 = 0,05 L = 50 mL
Điền đáp án : 50
[(CH3)2CHCH2CH(NH3)COOH] + Cl- + 2NaOH → (CH3)2CHCH2CH(NH3)COONa + NaCl + H2O
Số mol của L-leucine hydrochloride là nL-leucine hydrochloride = 0,05.0,1 = 0,005 mol
Từ phương trình hóa học số mol của NaOH là 0,01 mol
Thể tích tối thiểu của dung dịch NaOH cần dùng là VNaOH = 0,01:0,2 = 0,05 L = 50 mL
Điền đáp án : 50
Câu 26 [705846]: Độ tan của Na2SO4 ở 80 oC là 28,3 gam. Có bao nhiêu gam chất tan trong 256,6 gam dung dịch Na2SO4 ở 80 oC?
Độ tan của Na2SO4 ở 80oC là 28,3 gam/100 gam nước
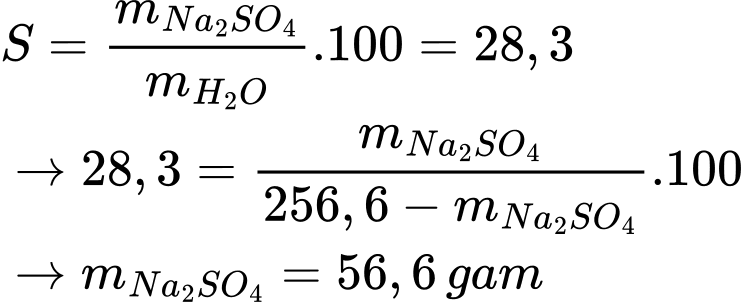
Điền đáp án : 56,6
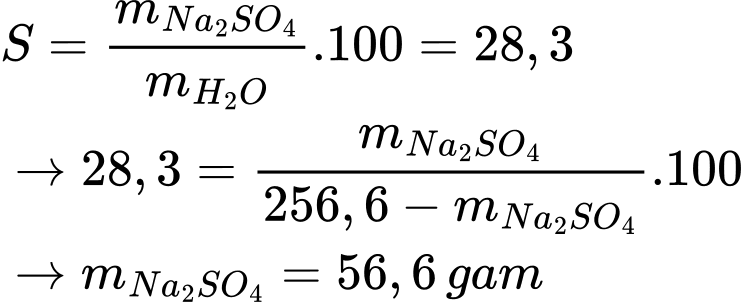
Điền đáp án : 56,6
Câu 27 [705567]: Quan sát dưới và xác định giá trị phân tử khối của naphtalene. Biết phân tử khối tương ứng với peak có cường độ tương đối lớn nhất hiển thị trên phổ khối lượng.
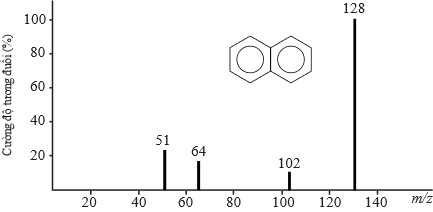

Trong phổ khối lương MS mảnh có giá trị m/z lớn nhất ứng với mảnh ion phân tử [M+] và có giá trị bằng phân tử khối của chất nghiên cứu.
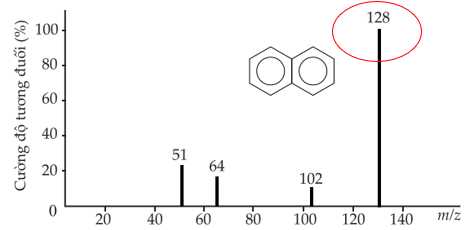
Từ phổ MS phân tử khối của napthtalene là 128.
⇒ Điền đáp án: 128

Từ phổ MS phân tử khối của napthtalene là 128.
⇒ Điền đáp án: 128
Câu 28 [705779]: Hydro peroxide, hoặc hydrogen peroxide (có công thức là H2O2) thường gọi là nước oxi già, là một chất oxy hóa dạng lỏng trong suốt, đặc tính nhớt, có các thuộc tính oxi hóa mạnh, là chất tẩy trắng mạnh được sử dụng như là chất tẩy uế, cũng như làm chất oxi hóa. Để kiểm chứng nồng độ dung dịch H2O2 trong một lọ oxi già nồng độ khoảng 3% thể tích 60 mL. Lấy 10 mL dung dịch H2O2 từ lọ trên, tiến hành chuẩn độ 3 lần bằng dung dịch KMnO4 0,1 M đã được acid hóa H2SO4 thì kết quả thu được theo bảng sau:
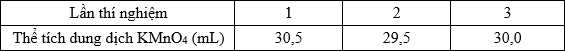
Biết phản ứng chuẩn độ:
5H2O2 + 2KMnO4 + 3H2SO4 K2SO4 + 2MnSO4 + 5O2 + 8H2O.
Xác định hàm lượng H2O2 (%) trong lọ oxi già. Giả sử khối lượng riêng của dung dịch H2O2 trong lọ là 1 g/cm3.
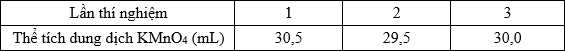
Biết phản ứng chuẩn độ:
5H2O2 + 2KMnO4 + 3H2SO4 K2SO4 + 2MnSO4 + 5O2 + 8H2O.
Xác định hàm lượng H2O2 (%) trong lọ oxi già. Giả sử khối lượng riêng của dung dịch H2O2 trong lọ là 1 g/cm3.
Thể tích trung bình của dich dịch KMnO4 là: 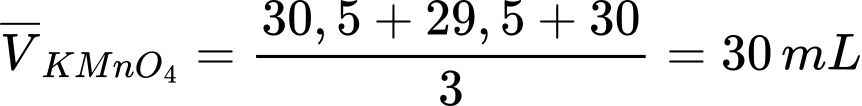
Đổi 30 mL = 0,03 L
Khối lượng của 10 mL H2O2 là 10 gam (dH2O2 = 1 gam/cm3)
Số mol của KMnO4 là: nKMnO4 = 0,03 × 0,1 = 0,003 mol
Từ phương trình hóa học số mol của H2O2 là: nH2O2 = 0,0075 mol
Hàm lượng H2O2 trong lọ oxi già là: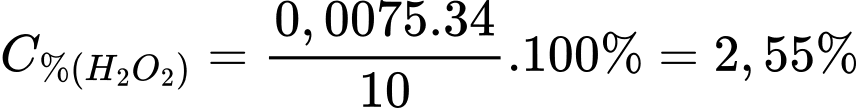
⇒ Điền đáp án: 2,55
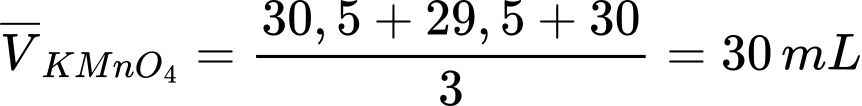
Đổi 30 mL = 0,03 L
Khối lượng của 10 mL H2O2 là 10 gam (dH2O2 = 1 gam/cm3)
Số mol của KMnO4 là: nKMnO4 = 0,03 × 0,1 = 0,003 mol
Từ phương trình hóa học số mol của H2O2 là: nH2O2 = 0,0075 mol
Hàm lượng H2O2 trong lọ oxi già là:
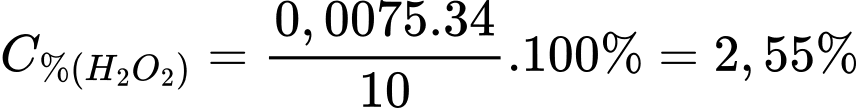
⇒ Điền đáp án: 2,55