PHẦN I. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án
Câu 1 [305726]: Chất nào sau chỉ tác dụng với NaOH dư trong dung dịch theo tỉ lệ số mol 1 : 1?
A, Phenyl acetate.
B, Triolein.
C, Tristearin.
D, Methyl acrylate.
Phân tích các chất:
❌ A. Phenyl acetae: CH3COOC6H5: ester của phenol nên tác dụng NaOH tỉ lệ 1 : 2:
CH3COOC6H5 + 2NaOH ⟶ CH3COONa + C6H5ONa + H2O.
❌ B. Triolein: (C17H33COO)3C3H5: chất béo ⟶ tác dụng NaOH tỉ lệ 1 : 3:
(C17H33COO)3C3H5 + 3NaOH ⟶3C17H33COONa + C3H5(OH)3.
❌ C. Tristearin: (C17H35COO)3C3H5: chất béo ⟶ tác dụng NaOH tỉ lệ 1 : 3:
(C17H35COO)3C3H5 + 3NaOH ⟶ 3C17H35COONa + C3H5(OH)3.
✔️ D. Methyl acrylate: CH2=CHCOOCH3: ester đơn chức thường ⟶ tác dụng NaOH tỉ lệ 1 : 1:
CH2=CHCOOCH3 + NaOH ⟶ CH2=CHCOONa + CH3OH.
⟹Chọn đáp án D Đáp án: D
❌ A. Phenyl acetae: CH3COOC6H5: ester của phenol nên tác dụng NaOH tỉ lệ 1 : 2:
CH3COOC6H5 + 2NaOH ⟶ CH3COONa + C6H5ONa + H2O.
❌ B. Triolein: (C17H33COO)3C3H5: chất béo ⟶ tác dụng NaOH tỉ lệ 1 : 3:
(C17H33COO)3C3H5 + 3NaOH ⟶3C17H33COONa + C3H5(OH)3.
❌ C. Tristearin: (C17H35COO)3C3H5: chất béo ⟶ tác dụng NaOH tỉ lệ 1 : 3:
(C17H35COO)3C3H5 + 3NaOH ⟶ 3C17H35COONa + C3H5(OH)3.
✔️ D. Methyl acrylate: CH2=CHCOOCH3: ester đơn chức thường ⟶ tác dụng NaOH tỉ lệ 1 : 1:
CH2=CHCOOCH3 + NaOH ⟶ CH2=CHCOONa + CH3OH.
⟹Chọn đáp án D Đáp án: D
Câu 2 [705910]: Trong pin Galvani, nếu rút cầu muối ra thì hiệu điện thế giữa hai điện cựccủa pin sẽ
A, bằng 0.
B, không thay đổi.
C, tăng từ từ.
D, giảm từ từ.
Dựa vào lí thuyết về pin điện hoá. Trong pin Galvani, nếu rút cầu muối ra thì hiệu điện thế giữa hai điện cực của pin sẽ bằng 0 vì mạch điện không khép kín, nên sẽ không có dòng điện chạy qua hai điện cực.
⟹ Chọn đáp án A Đáp án: A
⟹ Chọn đáp án A Đáp án: A
Câu 3 [704344]: “Các kim loại nhóm IA đều ...(1)... nóng chảy và có nhiệt độ nóng chảy ...(2)... so với các kim loại nhóm khác”. Nội dung phù hợp trong ô trống (1), (2) lần lượt là
A, khó, cao hơn.
B, dễ, thấp hơn.
C, khó, sắp xỉ.
D, dễ, cao hơn.
Kim loại nhóm IA (kim loại kiềm) có cấu trúc mạng tinh thể kim loại lỏng lẻo, liên kết kim loại yếu do chỉ có một electron hóa trị. Điều này làm cho chúng dễ nóng chảy và có nhiệt độ nóng chảy thấp hơn so với các kim loại khác.
⇒ Chọn đáp án B Đáp án: B
⇒ Chọn đáp án B Đáp án: B
Câu 4 [247280]: Nguyên lí hay quy tắc nào bị vi phạm trong cấu hình theo ô orbital được cho dưới đây?
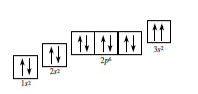

A, Quy tắc của Hund.
B, Không vi phạm nguyên lí, quy tắc nào.
C, Nguyên lí Pauli.
D, Quy tắc Klechkovski.
HƯỚNG DẪN GIẢI:
- Nguyên lí Pau - Li: Trên 1 orbital nguyên tửchứa tối đa 2 electron và có chiều tự quay khác chiều nhau xung quanh trục riêng của mỗi electron.
- Quy tắc Hund: Trong 1 phân lớp, các electron sẽ phân bố trên các obitan sao cho số electron độc thân là tối đa và có chiều tự quay giống nhau.
- Nguyên lý vững bền (quy tắc Klechkovski): Ở trạng thái cơ bản, trong nguyên tử các electron chiếm lần lượt các obitan có mức năng lượng từ thấp đến cao.
⟹ Ta nhận thấy orbital 3s có 2 electron đang có cùng chiều tự quay ⟹ Vi phạm nguyên lý Pauli.
⟹ Chọn đáp án C Đáp án: C
- Nguyên lí Pau - Li: Trên 1 orbital nguyên tửchứa tối đa 2 electron và có chiều tự quay khác chiều nhau xung quanh trục riêng của mỗi electron.
- Quy tắc Hund: Trong 1 phân lớp, các electron sẽ phân bố trên các obitan sao cho số electron độc thân là tối đa và có chiều tự quay giống nhau.
- Nguyên lý vững bền (quy tắc Klechkovski): Ở trạng thái cơ bản, trong nguyên tử các electron chiếm lần lượt các obitan có mức năng lượng từ thấp đến cao.
⟹ Ta nhận thấy orbital 3s có 2 electron đang có cùng chiều tự quay ⟹ Vi phạm nguyên lý Pauli.
⟹ Chọn đáp án C Đáp án: C
Câu 5 [308409]: Phân tử tinh bột được cấu tạo từ các gốc
A, β-fructose.
B, α-fructose.
C, β-glucose.
D, α-glucose.
HD: Tinh bột là polysaccharide, gồm hai poymer nhỏ hơn là amylose và amylopectin. Tinh bột có công thức phân tử là (C6H10O5)n được tạo bởi các mắt xích α-glucose
⇝ Chọn đáp án D Đáp án: D
⇝ Chọn đáp án D Đáp án: D
Câu 6 [704296]: Hợp chất nào sau đây là tên gọi của một amino acid?
A, Ethanoic acid.
B, Alanine.
C, DNA.
D, Amylase.
❌ A. Ethanoic acid là carboxylic acid.
✔️ B. Alanine là amino acid.
❌ C. DNA là những nucleic acid, cùng với protein, lipid và carbohydrate cao phân tử (polysaccharide) đều là những đại phân tử sinh học chính có vai trò quan trọng thiết yếu đối với mọi dạng sống được biết đến.
❌ D. Amylase là tên gọi của một nhóm enzyme (một loại protein) do tuyến tụy và các tuyến nước bọt sản xuất.
⇒ Chọn đáp án B Đáp án: B
✔️ B. Alanine là amino acid.
❌ C. DNA là những nucleic acid, cùng với protein, lipid và carbohydrate cao phân tử (polysaccharide) đều là những đại phân tử sinh học chính có vai trò quan trọng thiết yếu đối với mọi dạng sống được biết đến.
❌ D. Amylase là tên gọi của một nhóm enzyme (một loại protein) do tuyến tụy và các tuyến nước bọt sản xuất.
⇒ Chọn đáp án B Đáp án: B
Câu 7 [704028]: “Peptide là những hợp chất hữu cơ được hình thành từ các đơn vị …(1)… liên kết với nhau qua liên kết …(2)…”. Nội dung phù hợp trong ô trống (1), (2) lần lượt là
A, α-amine, peptide (-CONH-).
B, α-hydroxy acid, ester (-COO-).
C, α-carbonyl acid, ether (-C-O-C-).
D, α-amino aicd, peptide (-CONH-).
Các α-amino acid kết nối với nhau để tạo thành chuỗi peptide thông qua liên kết giữa nhóm carboxyl (-COOH) của một amino acid với nhóm amin (-NH2) của amino acid kế tiếp, gọi là liên kết peptide (-CONH-).
Peptide là những hợp chất hữu cơ được hình thành từ các đơn vị α-amino acid liên kết với nhau qua liên kết peptide (-CONH-).
⇒ Chọn đáp án D Đáp án: D
Peptide là những hợp chất hữu cơ được hình thành từ các đơn vị α-amino acid liên kết với nhau qua liên kết peptide (-CONH-).
⇒ Chọn đáp án D Đáp án: D
Câu 8 [190617]: Geraniol là nguyên liệu chính để tổng hợp dầu dưỡng hoa hồng, công thức cấu tạo của ceranol như hình bên.
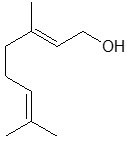
Phát biểu nào đưới đây là không đúng?

Phát biểu nào đưới đây là không đúng?
A, Công thức phân tử của Geraniol là C11H20O.
B, Geraniol làm mất màu dung dịch KMnO4.
C, Geraniol có phản ứng cộng và phản ứng thế.
D, 1 mol Geraniol phản ứng với Na dư thu được 1 gam H2.
Geraniol là một alcohol không no có trong tinh dầu hoa hồng, có công thức phân tử là C10H18O.
Geraniol có 2 nối đôi C=C nên phản ứng cộng được với: dung dịch bromine, H2 (xt Ni, to).
Geraniol có 2 nối đôi C=C nên phản ứng được với dung dịch KMnO4.
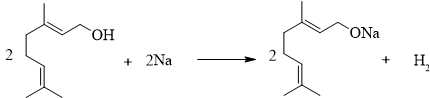
Từ phương trình hóa học 1 mol geraniol tạo được 0,5 mol H2.
Khối lượng của khí H2 là: 0,5 . 2 = 1 gam.
⇒ Chọn đáp án A Đáp án: A
Geraniol có 2 nối đôi C=C nên phản ứng cộng được với: dung dịch bromine, H2 (xt Ni, to).
Geraniol có 2 nối đôi C=C nên phản ứng được với dung dịch KMnO4.

Từ phương trình hóa học 1 mol geraniol tạo được 0,5 mol H2.
Khối lượng của khí H2 là: 0,5 . 2 = 1 gam.
⇒ Chọn đáp án A Đáp án: A
Câu 9 [705886]: Xét phản ứng trong giai đoạn đầu của quá trình Ostwald:
4NH3 + 5O2 → 4NO + 6H2O
Trong công nghiệp, cần trộn 1 thể tích khí ammonia với bao nhiêu thể tích không khí để thực hiện phản ứng trên? Biết không khí chứa 21% thể tích oxygen và các thể tích khí đo ở cùng điều kiện nhiệt độ và áp suất.
4NH3 + 5O2 → 4NO + 6H2O
Trong công nghiệp, cần trộn 1 thể tích khí ammonia với bao nhiêu thể tích không khí để thực hiện phản ứng trên? Biết không khí chứa 21% thể tích oxygen và các thể tích khí đo ở cùng điều kiện nhiệt độ và áp suất.
A, 10,10.
B, 5,95.
C, 2,41.
D, 1,84.
4NH3 + 5O2 → 4NO + 6H2O
Thể tích khí tỉ lệ thuận với số mol khí
Từ PTHH 1 thể tích khí NH3 sẽ cần 1,25 thể tích khí O2
Thể tích không khí cần để thực hiện phản ứng trên là 1,25 : 21% ≈ 5,95
1 thể tích khí NH3 cần 5,95 thể tích không khí để thực hiện phản ứng trên.
Chọn đáp án B Đáp án: B
Thể tích khí tỉ lệ thuận với số mol khí
Từ PTHH 1 thể tích khí NH3 sẽ cần 1,25 thể tích khí O2
Thể tích không khí cần để thực hiện phản ứng trên là 1,25 : 21% ≈ 5,95
1 thể tích khí NH3 cần 5,95 thể tích không khí để thực hiện phản ứng trên.
Chọn đáp án B Đáp án: B
Câu 10 [705964]: Cho phản ứng hóa học: Br2 + HCOOH → 2HBr + CO2.
Lúc đầu nồng độ của HCOOH là 0,010 mol/l, sau 40 giây nồng độ của HCOOH là 0,008 mol/l.
Tốc độ trung bình của phản ứng trong khoảng thời gian 40 giây tính theo HCOOH là
Lúc đầu nồng độ của HCOOH là 0,010 mol/l, sau 40 giây nồng độ của HCOOH là 0,008 mol/l.
Tốc độ trung bình của phản ứng trong khoảng thời gian 40 giây tính theo HCOOH là
A, 5,0.10–5 mol/(L.s).
B, 2,5.10–5 mol/(L.s).
C, 2,5.10–4 mol/(L.s).
D, 2,0.10–4 mol/(L.s).
Br2 + HCOOH → 2HBr + CO2
Tốc độ trung bình của phản ứng trên trong khoảng thời gian 40 giây là :
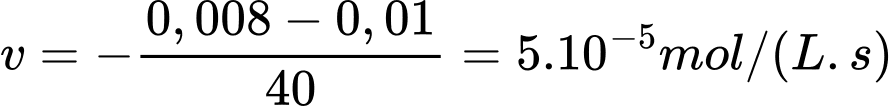
⟹Chọn đáp án A
Tốc độ trung bình của phản ứng trên trong khoảng thời gian 40 giây là :
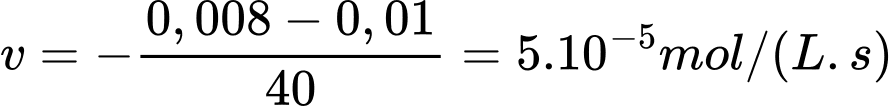
⟹Chọn đáp án A
Câu 11 [1108846]: Cấu trúc của một loại polyme được minh hoạ như sau:
Tên và quy trình có thể hình thành của loại polymer trên lần lượt là:

Tên và quy trình có thể hình thành của loại polymer trên lần lượt là:
A, protein và trùng hợp.
B, carbohydrate và trùng ngưng.
C, polyester và trùng hợp.
D, polyamide và trùng ngưng.
Đáp án đúng là: B
Hướng dẫn:
⭐Trong hình vẽ, chúng ta thấy các đơn vị (hình ô vuông) được kết nối với nhau thông qua nguyên tử Oxy (–O–). Cấu trúc này có dạng: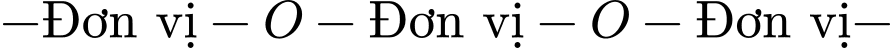
⭐Đây là đặc điểm của liên kết glycoside, thường thấy trong các loại carbohydrate phức tạp (polysaccharide) như tinh bột hoặc cellulose.
Phân tích đáp án:
❌A. Protein và trùng hợp → Sai. Protein có liên kết peptide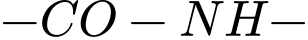 và hình thành qua trùng ngưng.
và hình thành qua trùng ngưng.
✔️B. Carbohydrate và trùng ngưng → Đúng. Các đơn vị đường đơn nối với nhau qua nguyên tử Oxy và giải phóng nước.
❌C. Polyester và trùng hợp → Sai. Polyester hình thành qua trùng ngưng.
❌D. Polyamide và trùng ngưng → Sai. Polyamide có liên kết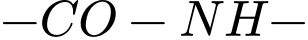 , không phải chỉ có cầu nối
, không phải chỉ có cầu nối  .
Đáp án: B
.
Đáp án: B
Hướng dẫn:
⭐Trong hình vẽ, chúng ta thấy các đơn vị (hình ô vuông) được kết nối với nhau thông qua nguyên tử Oxy (–O–). Cấu trúc này có dạng:
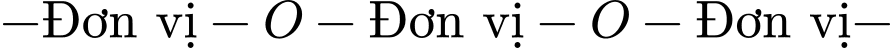
⭐Đây là đặc điểm của liên kết glycoside, thường thấy trong các loại carbohydrate phức tạp (polysaccharide) như tinh bột hoặc cellulose.
Phân tích đáp án:
❌A. Protein và trùng hợp → Sai. Protein có liên kết peptide
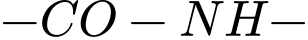 và hình thành qua trùng ngưng.
và hình thành qua trùng ngưng.✔️B. Carbohydrate và trùng ngưng → Đúng. Các đơn vị đường đơn nối với nhau qua nguyên tử Oxy và giải phóng nước.
❌C. Polyester và trùng hợp → Sai. Polyester hình thành qua trùng ngưng.
❌D. Polyamide và trùng ngưng → Sai. Polyamide có liên kết
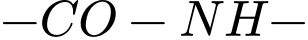 , không phải chỉ có cầu nối
, không phải chỉ có cầu nối  .
Đáp án: B
.
Đáp án: B
Câu 12 [186325]: Trong dung dịch nước của 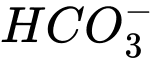 tồn tại cân bằng như sau:
tồn tại cân bằng như sau:
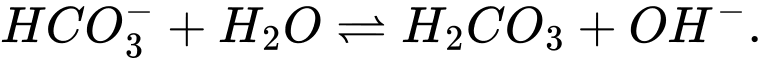
Cặp acid/ base liên hợp trong cân bằng trên là
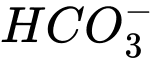 tồn tại cân bằng như sau:
tồn tại cân bằng như sau: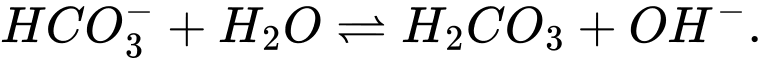
Cặp acid/ base liên hợp trong cân bằng trên là
A, 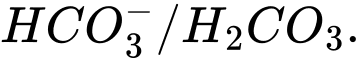
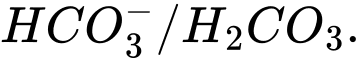
B, 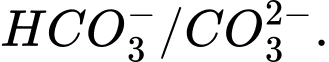
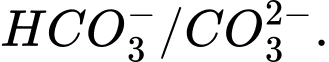
C, 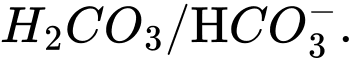
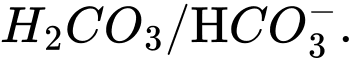
D, 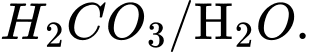
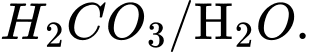
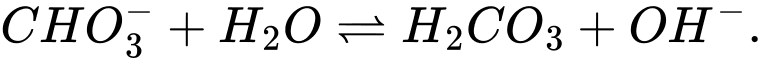
Base acid acid base
Cặp acid/ base liên hợp trong cân bằng trên là
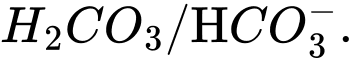
⟹Chọn đáp án C Đáp án: C
Câu 13 [704352]: Khi vừa hoà tan phèn nhôm – kali có công thức K2SO4.Al2(SO4)3.24H2O vào nước thu được dung dịch chứa K+, [Al(OH2)6]3+ và SO42–. Sau đó, một phần phức chất aqua chuyển thành phức chất không tan theo phương trình hoá học sau:
[Al(OH2)6]3+(aq) + 3H2O(1)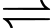 [Al(OH)3(OH2)3]n+(s) + 3H3O+(aq)
[Al(OH)3(OH2)3]n+(s) + 3H3O+(aq)
Có các phát biểu sau đây:
(1) Trong dung dịch có diễn ra quá trình phân li và quá trình hình thành phức chất.
(2) Chỉ có nguyên tố chuyển tiếp mới tạo được phức chất aqua.
(3) Giá trị n ở phức chất trong cân bằng (*) là 1.
(4) Trong phản ứng thuận của cân bằng (*), phức chất aqua đóng vai trò acid theo Brønsted - Lowry.
(5) Trong thực tế, sự hình thành phức chất từ phản ứng thuận của cân bằng (*) giúp giải thích ứng dụng làm trong nước của phèn nhôm – kali.
Các phát biểu đúng là
[Al(OH2)6]3+(aq) + 3H2O(1)
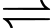 [Al(OH)3(OH2)3]n+(s) + 3H3O+(aq)
[Al(OH)3(OH2)3]n+(s) + 3H3O+(aq)Có các phát biểu sau đây:
(1) Trong dung dịch có diễn ra quá trình phân li và quá trình hình thành phức chất.
(2) Chỉ có nguyên tố chuyển tiếp mới tạo được phức chất aqua.
(3) Giá trị n ở phức chất trong cân bằng (*) là 1.
(4) Trong phản ứng thuận của cân bằng (*), phức chất aqua đóng vai trò acid theo Brønsted - Lowry.
(5) Trong thực tế, sự hình thành phức chất từ phản ứng thuận của cân bằng (*) giúp giải thích ứng dụng làm trong nước của phèn nhôm – kali.
Các phát biểu đúng là
A, (1), (4), (5).
B, (1), (2), (3).
C, (3), (5).
D, (2), (4), (5).
(1) 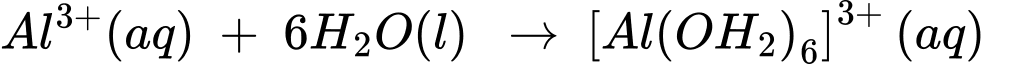
(2)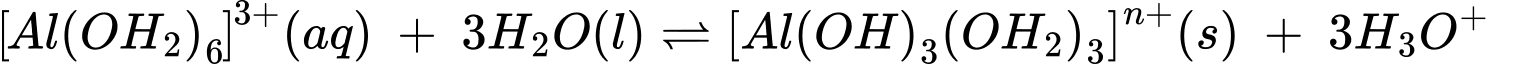
Phân tích các phát biểu:
✔️ (1) Đúng. Quá trình (1) là quá trình tạo phức chất aqua của cation Al3+, quá trình (2) là quá trình phân lí của phức chất tạo ion H3O+.
(2) Sai. Trong dung dịch, cation kim loại chuyển tiếp tồn tại ở dạng phức chất aqua. Hầu hết phức chất aqua của ion kim loại chuyển tiếp dãy thứ nhất đều có màu. Do đó dựa vào các dấu hiệu như màu sắc bị thay đổi, sự xuất hiện kết tủa, kết tủa bị hoà tan,… người ta có thể dự đoán phức chất trong dung dịch được tạo thành.
(3) Sai. Giá trị n = 0, trong [Al(OH)3(OH2)3]3+ có Al3+ và 3OH-
✔️ (4) Đúng. Thuyết bronsted – Lowry: Acid là chất cho proton (H+), base là chất nhận proton. Acid và base có thể là phân tử hoặc ion. Trong phản ứng thuận của cân bằng (*), phức chất aqua đóng vai trò acid theo Brønsted - Lowry.
✔️ (5) Đúng. Kết tủa [Al(OH)3(OH2)3]3+ được tạo ra khi khuấy phèn vào nước đã kết dính các hạt đất nhỏ lơ lửng trong nước đục thành các hát đất to hơn, nặng và chìm xuống làm trong nước. Phèn chua rất cần cho việc xử lí nước đục ở các vùng lũ để có nước dùng cho sinh hoạt của con người.
Các phát biểu đúng là (1) (4) (5)
⇒ Chọn đáp án A Đáp án: A
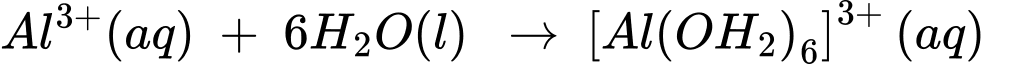
(2)
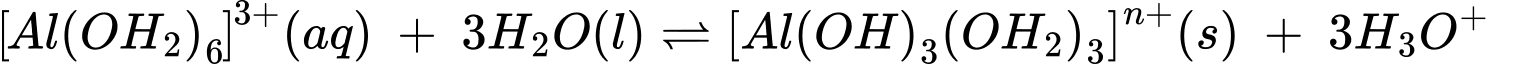
Phân tích các phát biểu:
✔️ (1) Đúng. Quá trình (1) là quá trình tạo phức chất aqua của cation Al3+, quá trình (2) là quá trình phân lí của phức chất tạo ion H3O+.
(2) Sai. Trong dung dịch, cation kim loại chuyển tiếp tồn tại ở dạng phức chất aqua. Hầu hết phức chất aqua của ion kim loại chuyển tiếp dãy thứ nhất đều có màu. Do đó dựa vào các dấu hiệu như màu sắc bị thay đổi, sự xuất hiện kết tủa, kết tủa bị hoà tan,… người ta có thể dự đoán phức chất trong dung dịch được tạo thành.
(3) Sai. Giá trị n = 0, trong [Al(OH)3(OH2)3]3+ có Al3+ và 3OH-
✔️ (4) Đúng. Thuyết bronsted – Lowry: Acid là chất cho proton (H+), base là chất nhận proton. Acid và base có thể là phân tử hoặc ion. Trong phản ứng thuận của cân bằng (*), phức chất aqua đóng vai trò acid theo Brønsted - Lowry.
✔️ (5) Đúng. Kết tủa [Al(OH)3(OH2)3]3+ được tạo ra khi khuấy phèn vào nước đã kết dính các hạt đất nhỏ lơ lửng trong nước đục thành các hát đất to hơn, nặng và chìm xuống làm trong nước. Phèn chua rất cần cho việc xử lí nước đục ở các vùng lũ để có nước dùng cho sinh hoạt của con người.
Các phát biểu đúng là (1) (4) (5)
⇒ Chọn đáp án A Đáp án: A
Câu 14 [1072860]: Sơ đồ nào thể hiện chính xác các điều kiện cần thiết để sắt bị gỉ và kim loại nào có thể được sử dụng để ngăn ngừa gỉ bằng biện pháp bảo vệ hy sinh?
A, 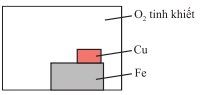

B, 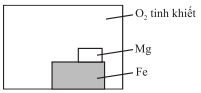

C, 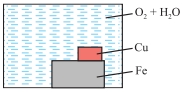

D, 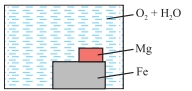

Để sắt bị gỉ cần có
đồng thời O₂ và H₂O → chỉ các sơ đồ có nước và oxygen mới thể hiện đúng điều
kiện này.
Để bảo vệ hy sinh,
kim loại gắn vào phải hoạt động mạnh hơn Fe → Mg dùng được, Cu thì không
(vì Cu kém hoạt động hơn Fe và sẽ làm Fe gỉ nhanh hơn).
Đáp án đúng: D
Câu 15 [306062]: Hợp chất có cấu tạo nào sau đây không được sử dụng để tạo thành xà phòng hoặc chất tẩy rửa tổng hợp?
A, 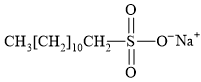

B, 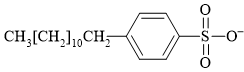

C, 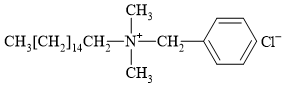

D, 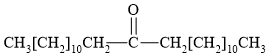
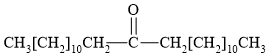
Phân tích các phát biểu:
✔️ A. Thỏa mãn mạch carbon dài không phân nhánh, một đầu mạch hydrocarbon không phân cực; đầu kia là NaSO3 phân cực.
✔️ B. thỏa mãn bởi cấu tạo một đầu là chuối hydrocarbon dài kỵ nước, đầu còn lại phân cực là ion tích điện âm. (Chú ý chất này là sodium dodecyl benzene sulfonate (SDBS) - Một chất tẩy rửa lâu đời và được sử dụng rộng rãi).
✔️ C. Thỏa mãn bởi có cấu tạo tương tự chất B; tuy nhiên phần đầu phân cực là ion tích điện dương (amine) (Thực tế chất này dạng benzalkonium chloride).
❌ D. C=O phân cực yếu nằm ở giữa; 2 đầu gắn với điểm phân cực này là hai gốc hydrocarbon mạch dài không phân cực ⇝ không thỏa mãn (bởi yêu cầu là 1 đầu phân cực + 1 đầu không phân cực thôi).
⟹ Chọn đáp án D Đáp án: D
✔️ A. Thỏa mãn mạch carbon dài không phân nhánh, một đầu mạch hydrocarbon không phân cực; đầu kia là NaSO3 phân cực.
✔️ B. thỏa mãn bởi cấu tạo một đầu là chuối hydrocarbon dài kỵ nước, đầu còn lại phân cực là ion tích điện âm. (Chú ý chất này là sodium dodecyl benzene sulfonate (SDBS) - Một chất tẩy rửa lâu đời và được sử dụng rộng rãi).
✔️ C. Thỏa mãn bởi có cấu tạo tương tự chất B; tuy nhiên phần đầu phân cực là ion tích điện dương (amine) (Thực tế chất này dạng benzalkonium chloride).
❌ D. C=O phân cực yếu nằm ở giữa; 2 đầu gắn với điểm phân cực này là hai gốc hydrocarbon mạch dài không phân cực ⇝ không thỏa mãn (bởi yêu cầu là 1 đầu phân cực + 1 đầu không phân cực thôi).
⟹ Chọn đáp án D Đáp án: D
Câu 16 [705744]: Điểm chớp cháy của một chất là nhiệt độ thấp nhất ở áp suất khí quyển mà hơi của chất đó sẽ bốc cháy trong không khí khi tiếp xúc với nguồn lửa. Điểm chớp cháy của một số chất lỏng như sau:

Chất lỏng có điểm chớp cháy nhỏ hơn 37,8 oC được gọi là chất lỏng dễ cháy. Trong khi các chất lỏng có điểm chớp cháy trên nhiệt độ đó gọi là chất lỏng có thể gây cháy.
Cho các phát biểu sau:
(a) Xăng và ethanol được gọi là chất lỏng dễ cháy.
(b) Dầu hỏa được gọi là chất lỏng có thể gây cháy.
(c) Nguy cơ gây cháy của ethanol cao hơn xăng.
(d) Dưới 160 oC thì dầu diesel sinh học không thể cháy.
Các phát biểu đúng là

Chất lỏng có điểm chớp cháy nhỏ hơn 37,8 oC được gọi là chất lỏng dễ cháy. Trong khi các chất lỏng có điểm chớp cháy trên nhiệt độ đó gọi là chất lỏng có thể gây cháy.
Cho các phát biểu sau:
(a) Xăng và ethanol được gọi là chất lỏng dễ cháy.
(b) Dầu hỏa được gọi là chất lỏng có thể gây cháy.
(c) Nguy cơ gây cháy của ethanol cao hơn xăng.
(d) Dưới 160 oC thì dầu diesel sinh học không thể cháy.
Các phát biểu đúng là
A, (a), (b).
B, (a), (c).
C, (a), (b), (d).
D, (a), (c), (d).
Phân tích các phát biểu:
✔️ (a) Đúng. Xăng và ethanol có điểm chớp cháy lần lượt là –43 oC và 13 oC đều nhỏ hơn 37,8 oC nên đều là chất dễ cháy.
✔️ (b) Đúng. Dầu hỏa có điểm chớp cháy là 38–72 oC lớn hơn 37,8 oC là chất có thể gây cháy.
❌ (c) Sai. Xăng có điểm chớp cháy là –43 oC nhỏ hơn ethanol có điểm chớp cháy 13 oC nên xăng dễ cháy hơn ethanol
✔️(d) Đúng. Điểm chớp cháy của dầu diesel sinh học là 160 oC nghĩa là dưới 160oC dầu diesel sinh học không tạo đủ hơi để bốc cháy.
Các phát biểu đúng là (a) (b) (d)
⇒ Chọn đáp án C Đáp án: C
✔️ (a) Đúng. Xăng và ethanol có điểm chớp cháy lần lượt là –43 oC và 13 oC đều nhỏ hơn 37,8 oC nên đều là chất dễ cháy.
✔️ (b) Đúng. Dầu hỏa có điểm chớp cháy là 38–72 oC lớn hơn 37,8 oC là chất có thể gây cháy.
❌ (c) Sai. Xăng có điểm chớp cháy là –43 oC nhỏ hơn ethanol có điểm chớp cháy 13 oC nên xăng dễ cháy hơn ethanol
✔️(d) Đúng. Điểm chớp cháy của dầu diesel sinh học là 160 oC nghĩa là dưới 160oC dầu diesel sinh học không tạo đủ hơi để bốc cháy.
Các phát biểu đúng là (a) (b) (d)
⇒ Chọn đáp án C Đáp án: C
Sử dụng thông tin cho dưới đây để trả lời các câu số 17 – 18:

Một pin đồng – kẽm được thiết lập bởi hai điện cực chuẩn (với thể tích các dung dịch
CuSO4 1,0 M và ZnSO4 1,0 M bằng nhau. Nối thanh đồng với thanh kẽm bằng một dây dẫn.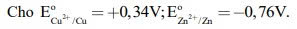
Câu 17 [705465]: Sau một thời gian hoạt động, nồng độ CuSO4 thay đổi 0,5 M. Nồng độ của các dung dịch tại thời điểm này là
A, CuSO4, 0,5M; ZnSO4 0,5 M.
B, CuSO4, 0,5 M; ZnSO4, 1,5 M.
C, CuSO4 1,5 M; ZnSO4 0,5 M.
D, CuSO4, 1,5 M; ZnSO4, 1,5 M.
Ta có: 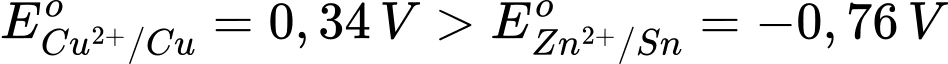
Trong pin điện hóa trên Cu đóng vai trò là cathode và Zn đóng vai trò là anode
Phản ứng trong pin: Cu2+ + Zn ⟶ Cu + Zn2+
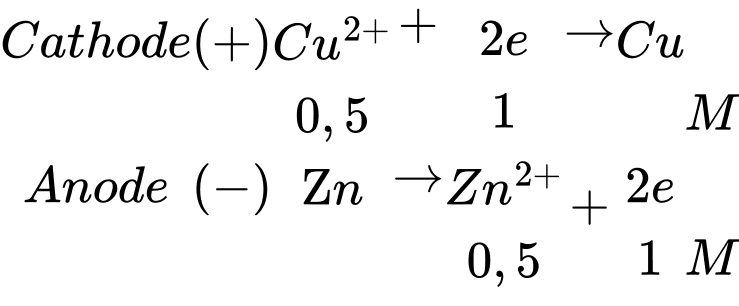
→ Nồng độ các chất trong dung dịch là:
CCuSO4 = 1 – 0,5 = 0,5 M;
CZnSO4 = 1 + 0,5 = 1,5 M.
⇒ Chọn đáp án B Đáp án: B
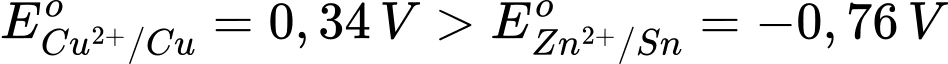
Trong pin điện hóa trên Cu đóng vai trò là cathode và Zn đóng vai trò là anode
Phản ứng trong pin: Cu2+ + Zn ⟶ Cu + Zn2+
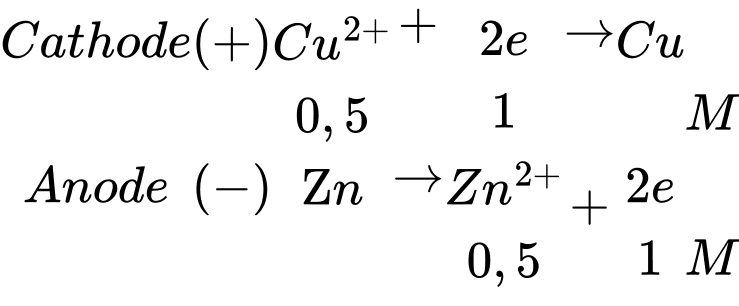
→ Nồng độ các chất trong dung dịch là:
CCuSO4 = 1 – 0,5 = 0,5 M;
CZnSO4 = 1 + 0,5 = 1,5 M.
⇒ Chọn đáp án B Đáp án: B
Câu 18 [705466]: Đồ thị nào thể hiện sự thay đổi sức điện động của pin đồng - kẽm theo thời gian?
A, 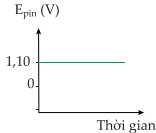

B, 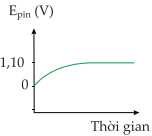

C, 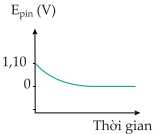

D, 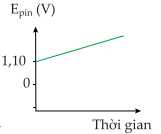

Khi thời gian phản ứng tăng, tức lượng Cu2+ trong pin Đồng – kẽm giảm dần
→ Sức điện động của pin sẽ giảm dần từ 1,10 V đến 0.
⇒ Chọn đáp án C Đáp án: C
→ Sức điện động của pin sẽ giảm dần từ 1,10 V đến 0.
⇒ Chọn đáp án C Đáp án: C
PHẦN II. Thí sinh trả lời từ câu 1 đến câu 4. Trong mỗi ý a), b), c), d) ở mỗi câu, thí sinh chọn đúng hoặc sai.
Câu 19 [703956]: Tiến hành thí nghiệm như sau:
▪ Bước 1: Cho một thìa thủy tinh chất rắn sodium acetate (CH3COONa) vào ống nghiệm A chứa khoảng 5 mL nước cất, lắc đều cho tan hết, rồi thêm vào ống nghiệm 2 – 3 giọt chất chỉ thị phenolphthalein, để một thời gian.
▪ Bước 2: Rót khoảng một nửa dung dịch từ ống nghiệm A sang ống nghiệm B, sau đó đặt ống nghiệm B vào một cốc nước nóng (khoảng 70oC – 80oC) thì thấy màu sắc ống nghiệm B đậm hơn. Cho biết giữa ion acetate và nước có phản ứng thuận nghịch sau:
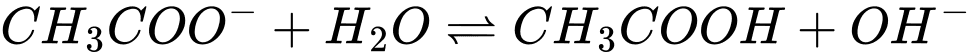
▪ Bước 1: Cho một thìa thủy tinh chất rắn sodium acetate (CH3COONa) vào ống nghiệm A chứa khoảng 5 mL nước cất, lắc đều cho tan hết, rồi thêm vào ống nghiệm 2 – 3 giọt chất chỉ thị phenolphthalein, để một thời gian.
▪ Bước 2: Rót khoảng một nửa dung dịch từ ống nghiệm A sang ống nghiệm B, sau đó đặt ống nghiệm B vào một cốc nước nóng (khoảng 70oC – 80oC) thì thấy màu sắc ống nghiệm B đậm hơn. Cho biết giữa ion acetate và nước có phản ứng thuận nghịch sau:
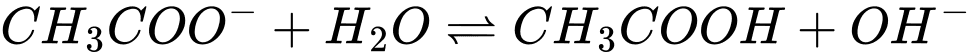
Phân tích các phát biểu:
❌ a) Sai. Sau bước 1 dung dịch trong ống nghiệm A vẫn có màu hồng nhạt do vẫn có phản ứng CH3COO– + H2O ⇌ CH3COOH + OH–.
✔️ b) Đúng. Cả 2 ống đều có phản ứng CH3COO– + H2O ⇌ CH3COOH + OH– tạo ra OH– nên làm đổi màu chất chỉ chị phenolphtalein (màu hồng).
✔️ c) Đúng. Khi tăng nhiệt độ màu của dung dịch chuyển sang màu đậm hơn, tức cân bằng chuyển dịch theo chiều thuận tạo nhiều OH– hơn, phản ứng trên phải là thu nhiệt.
✔️ d) Đúng. Nồng độ OH– trong ống nghiệm B lớn hơn nên màu của dung dịch sau phản ứng đậm hơn.
❌ a) Sai. Sau bước 1 dung dịch trong ống nghiệm A vẫn có màu hồng nhạt do vẫn có phản ứng CH3COO– + H2O ⇌ CH3COOH + OH–.
✔️ b) Đúng. Cả 2 ống đều có phản ứng CH3COO– + H2O ⇌ CH3COOH + OH– tạo ra OH– nên làm đổi màu chất chỉ chị phenolphtalein (màu hồng).
✔️ c) Đúng. Khi tăng nhiệt độ màu của dung dịch chuyển sang màu đậm hơn, tức cân bằng chuyển dịch theo chiều thuận tạo nhiều OH– hơn, phản ứng trên phải là thu nhiệt.
✔️ d) Đúng. Nồng độ OH– trong ống nghiệm B lớn hơn nên màu của dung dịch sau phản ứng đậm hơn.
Câu 20 [702620]: Gỉ đồng được hình thành do sự ăn mòn kim loại đồng, nó có màu xanh lục chứa cả đồng(II) carbonate, CuCO3 và đồng(II) hydroxide, Cu(OH)2, với hàm lượng khác nhau. Cả hai hợp chất đồng đều phản ứng với hydrochloric acid loãng.
CuCO3(s) + 2HCl (aq) CuCl2(aq) + CO2(g) + H2O(l)
CuCl2(aq) + CO2(g) + H2O(l)
Cu(OH)2(s) + 2HCl (aq) CuCl2(aq) + 2H2O(l)
CuCl2(aq) + 2H2O(l)
Một bạn học sinh lập kế hoạch thực hiện một thí nghiệm để xác định phần trăm đồng(II) carbonate trong một mẫu gỉ đồng. Giả thuyết được học sinh đưa ra: “Tìm thể tích hydrochloric acid loãng cần thiết để phản ứng vừa đủ với khối lượng gỉ đồng sẽ là phương pháp phù hợp để xác định hàm lượng đồng(II) carbonate trong mẫu gỉ đồng”. Các hóa chất cần chuẩn bị gồm:
▪ Một mẫu gỉ đồng.
▪ dung dịch hydrochloric acid, HCl 1 M .
▪ Thuốc thử và thiết bị phòng thí nghiệm thông thường.
Giả sử các chất khác có trong gỉ đồng đều không bị ảnh hưởng bởi nhiệt và trơ.
CuCO3(s) + 2HCl (aq)
 CuCl2(aq) + CO2(g) + H2O(l)
CuCl2(aq) + CO2(g) + H2O(l)Cu(OH)2(s) + 2HCl (aq)
 CuCl2(aq) + 2H2O(l)
CuCl2(aq) + 2H2O(l)Một bạn học sinh lập kế hoạch thực hiện một thí nghiệm để xác định phần trăm đồng(II) carbonate trong một mẫu gỉ đồng. Giả thuyết được học sinh đưa ra: “Tìm thể tích hydrochloric acid loãng cần thiết để phản ứng vừa đủ với khối lượng gỉ đồng sẽ là phương pháp phù hợp để xác định hàm lượng đồng(II) carbonate trong mẫu gỉ đồng”. Các hóa chất cần chuẩn bị gồm:
▪ Một mẫu gỉ đồng.
▪ dung dịch hydrochloric acid, HCl 1 M .
▪ Thuốc thử và thiết bị phòng thí nghiệm thông thường.
Giả sử các chất khác có trong gỉ đồng đều không bị ảnh hưởng bởi nhiệt và trơ.
Phân tích các phát biểu:
✔️ a) Đúng. HCl có nhiệm vụ cung cấp H+ cho phản ứng, H2SO4 và HNO3 hoàn toàn có thể thay HCl để tạo ra H+ tương tự. Do H2SO4 và HNO3 trong phản ứng này không thể hiện tính oxi hoá mạnh (Cu2+ đã không còn tính khử)
✔️ b) Đúng. Ta cần một lượng mol HCl nhất định để phản ứng vừa đủ, mà nHCl = CM HCl . VHCl nên nếu nồng độ HCl giảm thì thể tích HCl cần dùng phải tăng để phản ứng hoàn toàn.
✔️ c) Đúng. Giả thuyết là sai vì cả CuCO3 và Cu(OH)2 đều phản ứng với HCl nên không thể dựa vào thể tích acid HCl loãng để xác định hàm lượng đồng(II) carbonate trong mẫu gỉ đồng.
✔️ d) Đúng. Dựa vào 2 phản ứng xảy ra thì chỉ có phản ứng của đồng(II) carbonate với acid là sinh ra khí nên dựa vào thể tích khí sinh ra trong quá trình phản ứng có thể xác định được hàm lượng đồng(II) carbonate.
✔️ a) Đúng. HCl có nhiệm vụ cung cấp H+ cho phản ứng, H2SO4 và HNO3 hoàn toàn có thể thay HCl để tạo ra H+ tương tự. Do H2SO4 và HNO3 trong phản ứng này không thể hiện tính oxi hoá mạnh (Cu2+ đã không còn tính khử)
✔️ b) Đúng. Ta cần một lượng mol HCl nhất định để phản ứng vừa đủ, mà nHCl = CM HCl . VHCl nên nếu nồng độ HCl giảm thì thể tích HCl cần dùng phải tăng để phản ứng hoàn toàn.
✔️ c) Đúng. Giả thuyết là sai vì cả CuCO3 và Cu(OH)2 đều phản ứng với HCl nên không thể dựa vào thể tích acid HCl loãng để xác định hàm lượng đồng(II) carbonate trong mẫu gỉ đồng.
✔️ d) Đúng. Dựa vào 2 phản ứng xảy ra thì chỉ có phản ứng của đồng(II) carbonate với acid là sinh ra khí nên dựa vào thể tích khí sinh ra trong quá trình phản ứng có thể xác định được hàm lượng đồng(II) carbonate.
Câu 21 [702817]: Một bạn học sinh tiến hành phản ứng oxi hóa 2-ethylcyclohexanol bằng CuO.
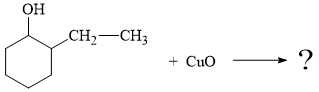
Sau khi tinh chế sản phẩm thu được một chất mà phổ IR của nó được thể hiện như sau:
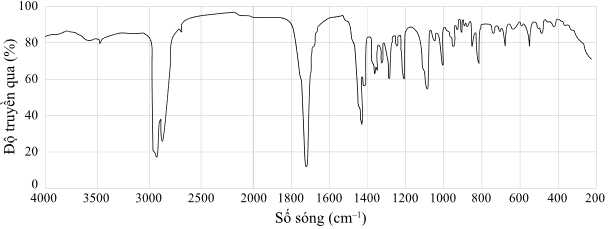
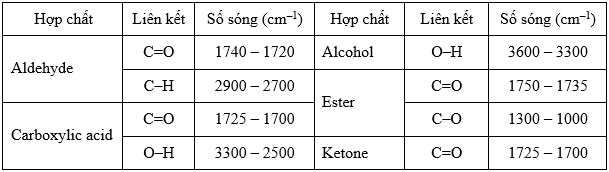
Cho bảng số sóng đặc trưng của các liên kết ở bảng sau:
Sau khi tinh chế sản phẩm thu được một chất mà phổ IR của nó được thể hiện như sau:

Cho bảng số sóng đặc trưng của các liên kết ở bảng sau:

Phản ứng oxi hóa 2-ethylcyclohexanol bằng CuO (chưa cân bằng) xảy ra như sau:
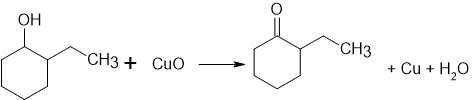
Phân tích các phát biểu:
✔️ a) Đúng. Trong phổ hồng ngoại của sản phẩm, sẽ xuất hiện dải hấp thụ đặc trưng của nhóm C=O ở khoảng 1700 cm–1.
❌ b) Sai. Sản phẩm tạo thành không chứa nhóm chức -OH nên không có sự xuất hiện của dải hấp phụ O-H.
❌ c) Sai. Liên kết C–H của nhóm alkyl không có dải hấp thụ đặc trưng.
✔️ d) Đúng. Sau phản ứng, dải hấp thụ trong vùng 1000 – 1300 cm–1 sẽ trở nên mạnh hơn do sự xuất hiện của nhóm C=O.

Phân tích các phát biểu:
✔️ a) Đúng. Trong phổ hồng ngoại của sản phẩm, sẽ xuất hiện dải hấp thụ đặc trưng của nhóm C=O ở khoảng 1700 cm–1.
❌ b) Sai. Sản phẩm tạo thành không chứa nhóm chức -OH nên không có sự xuất hiện của dải hấp phụ O-H.
❌ c) Sai. Liên kết C–H của nhóm alkyl không có dải hấp thụ đặc trưng.
✔️ d) Đúng. Sau phản ứng, dải hấp thụ trong vùng 1000 – 1300 cm–1 sẽ trở nên mạnh hơn do sự xuất hiện của nhóm C=O.
Câu 22 [702818]: Điểm đẳng điện pI là giá trị pH mà tại đó tổng điện tích của một phân tử amino acid bằng 0.
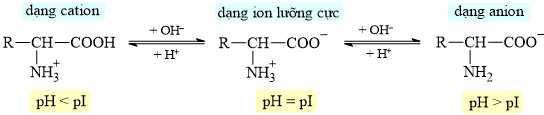
Một hỗn hợp gồm 3 amino acid là glycine, histidine và arginine được đặt vào giữa của tấm gel. Điện di được thực hiện và các xuất hiện 3 chấm tương ứng với 3 amino acid được thể hiện trong sơ đồ bên dưới:
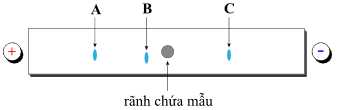
Các giá trị pI của amino acid được cung cấp trong bảng như sau:
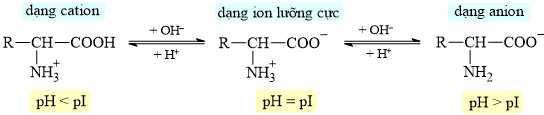
Một hỗn hợp gồm 3 amino acid là glycine, histidine và arginine được đặt vào giữa của tấm gel. Điện di được thực hiện và các xuất hiện 3 chấm tương ứng với 3 amino acid được thể hiện trong sơ đồ bên dưới:

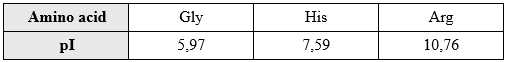
Các giá trị pI của amino acid được cung cấp trong bảng như sau:

Dựa vào giá trị pI và sự di chuyển của 3 amino acid trên tấm gel ⇒ A là Glycine; B là Histidine; C là Arginine.
Phân tích các phát biểu:
✔️ a) Đúng. Tại pH bằng 5,97 thì tổng điện tích của Gly bằng 0 do pH = pI.
✔️ b) Đúng. Ta thấy B là His di chuyển về cực dương, nên H sẽ ở dạng anion dẫn đến pH môi trường lớn hơn điểm đẳng điện của His pI= 7,59.
❌ c) Sai. Ta thấy B là His di chuyển về cực dương, nên His sẽ ở mang điện tích âm.
✔️ d) Đúng. Chất A có mật độ điện tích lớn hơn chất B nên di chuyển về gần cực dương hơn.
Phân tích các phát biểu:
✔️ a) Đúng. Tại pH bằng 5,97 thì tổng điện tích của Gly bằng 0 do pH = pI.
✔️ b) Đúng. Ta thấy B là His di chuyển về cực dương, nên H sẽ ở dạng anion dẫn đến pH môi trường lớn hơn điểm đẳng điện của His pI= 7,59.
❌ c) Sai. Ta thấy B là His di chuyển về cực dương, nên His sẽ ở mang điện tích âm.
✔️ d) Đúng. Chất A có mật độ điện tích lớn hơn chất B nên di chuyển về gần cực dương hơn.
PHẦN III. Thí sinh trả lời từ câu 1 đến 6. Thí sinh điền kết quả mỗi câu vào mỗi ô trả lời tương ứng theo hướng dẫn của phiếu trả lời.
Câu 23 [705921]: Sắn khô chứa 38% khối lượng là tinh bột, còn lại là các chất không có khả năng lên men thành ethanol. Lên men 2 tấn sắn khô với hiệu suất cả quá trình là 74%. Toàn bộ lượng ethanol sinh ra để điều chế xăng E5 (có chứa 5% thể tích ethanol). Biết khối lượng riêng của ethyl alcohol là 0,8 g/mL, thể tích xăng E5 thu được là bao nhiêu lít?
Đổi 2 tấn = 2000 kg; 0,8 g/mL = 0,8 kg/L
Khối lượng của tinh bột trong sắn khô là 2000.38% = 760 kg
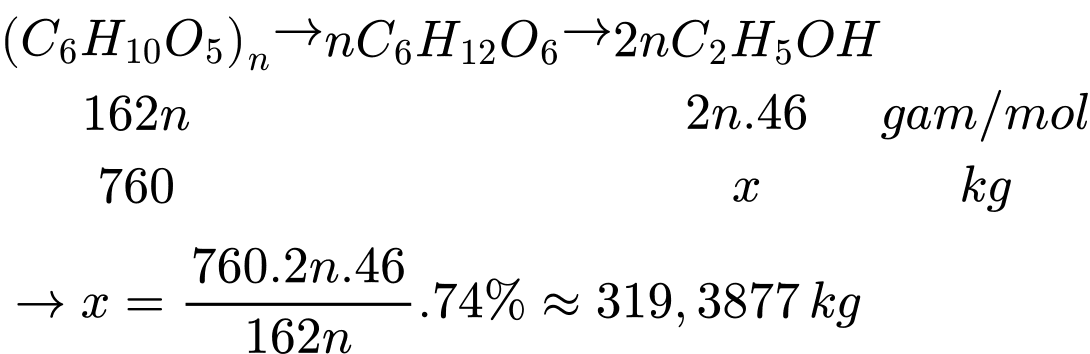
Thể tích alcohol là VC2H5OH = 319,3877:0,8 = 399,2346 L
Thể tích xăng E5 là VE5 = 399,2346:5% ≈ 7985 L
Điền đáp án : 7985
Khối lượng của tinh bột trong sắn khô là 2000.38% = 760 kg
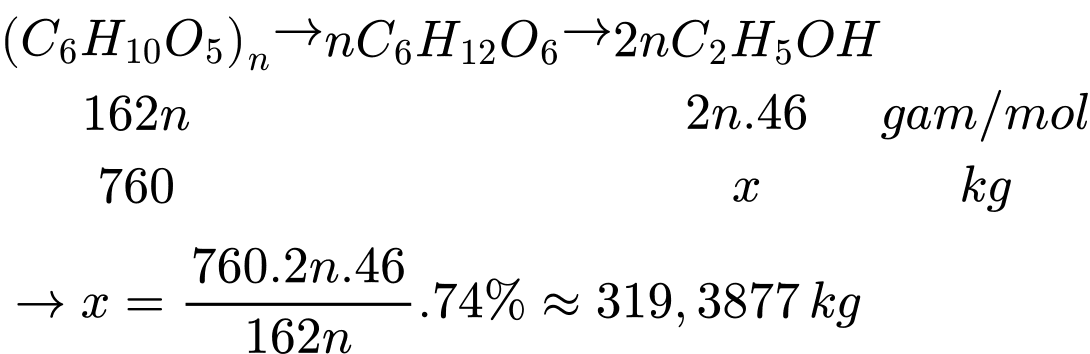
Thể tích alcohol là VC2H5OH = 319,3877:0,8 = 399,2346 L
Thể tích xăng E5 là VE5 = 399,2346:5% ≈ 7985 L
Điền đáp án : 7985
Câu 24 [705920]: Một mẫu nước thải của nhà máy sản xuất dây lưới thép có pH = 4,0. Để thải được ra môi trường, nhà máy đó cần phải tăng pH trong nước thải lên tới 5,8 – 8,6 (theo tiêu chuẩn quy định). Tính lượng vôi sống (g) cần dùng để tăng pH trong 100 m3 nước thải từ 4,0 lên 7,0. Giả thiết thể tích nước thải thay đổi không đáng kể (Kết quả làm tròn đến số nguyên).
Đổi 100 m3 = 100000 L
Ta có của nước thải pH = 4 → [H+] = 10-4 M
Số mol của H+ là nH+ = 10-4.100000 = 10 mol
H+ + OH- → H2O
CaO + H2O → Ca(OH)2
Để pH của nước thải từ pH = 4 đến pH = 7 cần số mol OH- là nH+ = nOH- = 10 mol
2nOH- = nCa(OH)2 = 10 mol → nCa(OH)2 = 5 mol
Từ PTHH số mol của CaO là 5 mol
Khối lượng của CaO là mCaO = 5.56 = 280 gam
Điền đáp án : 280
Ta có của nước thải pH = 4 → [H+] = 10-4 M
Số mol của H+ là nH+ = 10-4.100000 = 10 mol
H+ + OH- → H2O
CaO + H2O → Ca(OH)2
Để pH của nước thải từ pH = 4 đến pH = 7 cần số mol OH- là nH+ = nOH- = 10 mol
2nOH- = nCa(OH)2 = 10 mol → nCa(OH)2 = 5 mol
Từ PTHH số mol của CaO là 5 mol
Khối lượng của CaO là mCaO = 5.56 = 280 gam
Điền đáp án : 280
Câu 25 [705942]: Khi nung nóng, CuSO4.5H2O sẽ bắt đầu mất dần khối lượng. Đồ thị sau đây biểu diễn sự phụ thuộc của khối lượng chất rắn vào nhiệt độ.
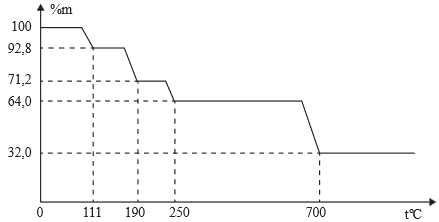
Tại nhiệt độ đạt đến 190 oC, thành phần gần nhất của chất rắn là CuSO4.nH2O. Giá trị của n là bao nhiêu (Làm tròn đến số nguyên)?

Tại nhiệt độ đạt đến 190 oC, thành phần gần nhất của chất rắn là CuSO4.nH2O. Giá trị của n là bao nhiêu (Làm tròn đến số nguyên)?
Tại 190 oC hàm lượng chất rắn còn lại là : 71,2%
CuSO4.nH2O ⟶ CuSO4.xH2O + H2O
m mất đi = m H2O

Điền đáp án : 1
CuSO4.nH2O ⟶ CuSO4.xH2O + H2O
m mất đi = m H2O

Điền đáp án : 1
Câu 26 [705952]: Chlorogenic acid được tìm thấy trong thực vật, trái cây. Nó có khả năng bảo vệ trong các bệnh tim mạch, tiểu đường loại 2 và các tình trạng liên quan đến viêm.
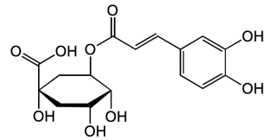
Một mol chlorogenic acid phản ứng được với tối đa bao nhiêu mol NaOH?

Một mol chlorogenic acid phản ứng được với tối đa bao nhiêu mol NaOH?
Chlorogenic acid có 1 nhóm chức ester, 1 nhóm chức carboxylic acid và 2 nhóm chức phenol nên 1 mol Chlorogenic acid sẽ phản ứng với 4 mol NaOH.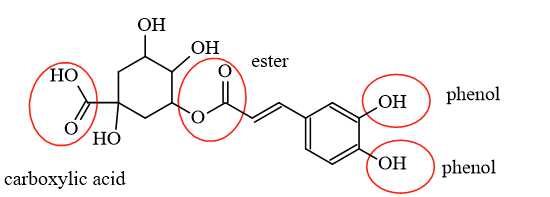
⟹Điền đáp án : 4
Câu 27 [705977]: Một nhà máy sản xuất tấm nhựa dẻo trải bàn cần sản xuất tấm nhựa PVC hình chữ nhật có kích thước là 80 cm × 120 cm, bề dày của tấm nhựa dẻo là 3 mm. Biết hiệu suất phản ứng trùng hợp vinylchloride để điều chế PVC là 65%, quá trình chuyển PVC thành tấm nhựa dẻo có hiệu suất là 95% và biết khối lượng riêng của nhựa PVC là 1,45 g/cm3. Tính khối lượng nguyên liệu vinylchloride (tấn) dùng để sản xuất đơn hàng 5 000 tấm nhựa dẻo trải bàn trên? (Làm tròn kết quả đến số nguyên).
Đổi 3 mm = 0,3 cm
Thể tích 1 tấm PVC là V = 80.120.0,3 = 2880 cm3
Khối lượng PVC trong 5000 tấm nhựa là mPVC = 5000×2880×1,45 = 20880000 gam = 20,88 tấn
Hiệu suất chung của cả quá trình là H = 65%×95% = 61,175%
Khối lượng vinylchloride cần dùng để sản xuất 5000 tấm nhựa dẻo là
mvinylchloride = 20,88 : 61,175% ≈ 34 tấn.
⟹Điền đáp án : 34
Thể tích 1 tấm PVC là V = 80.120.0,3 = 2880 cm3
Khối lượng PVC trong 5000 tấm nhựa là mPVC = 5000×2880×1,45 = 20880000 gam = 20,88 tấn
Hiệu suất chung của cả quá trình là H = 65%×95% = 61,175%
Khối lượng vinylchloride cần dùng để sản xuất 5000 tấm nhựa dẻo là
mvinylchloride = 20,88 : 61,175% ≈ 34 tấn.
⟹Điền đáp án : 34
Câu 28 [705850]: Chlorine được dùng làm chất chống tạo rong rêu trong vệ sinh bể bơi theo phản ứng sau:
Ca(OCl)2 + 2H2O → 2HClO + Ca(OH)2
Calcium hypochlorite phản ứng với nước tạo hypochlorous acid là một tác nhân hoạt động. Ở pH bằng 7,0 có 27,5% acid ion hoá thành ion hypochlorite không hoạt động. Phần hypochlorous acid còn lại (72,5%) chuyển thành chlorine dùng làm sạch hồ bơi.Trong hồ bơi, mức chlorine được duy trì ở 3 ppm. Cần bao nhiêu gam calcium hypochlorite để thêm vào hồ chứa 80 m3 nước để mức chlorine đạt tiêu chuẩn vệ sinh là 3 ppm ở pH bằng 7,0? Biết 1 ppm = 1 g chlorine trên 1 m3 nước (Làm tròn đến số nguyên).
Ca(OCl)2 + 2H2O → 2HClO + Ca(OH)2
Calcium hypochlorite phản ứng với nước tạo hypochlorous acid là một tác nhân hoạt động. Ở pH bằng 7,0 có 27,5% acid ion hoá thành ion hypochlorite không hoạt động. Phần hypochlorous acid còn lại (72,5%) chuyển thành chlorine dùng làm sạch hồ bơi.Trong hồ bơi, mức chlorine được duy trì ở 3 ppm. Cần bao nhiêu gam calcium hypochlorite để thêm vào hồ chứa 80 m3 nước để mức chlorine đạt tiêu chuẩn vệ sinh là 3 ppm ở pH bằng 7,0? Biết 1 ppm = 1 g chlorine trên 1 m3 nước (Làm tròn đến số nguyên).
Ca(OCl)2 + 2H2O → 2HClO + Ca(OH)2
Khối lượng chlorine trong hồ bơi là 80.3 = 240 gam
Bảo toàn nguyên tố Cl: nCl = nHClO = 240 : 35,5 = 480/71 mol
số mol của HClO ban đầu là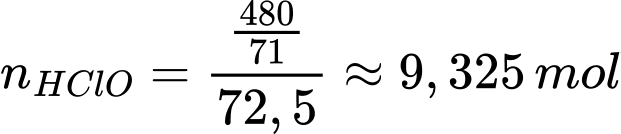
Từ phương trình số mol của Ca(OCl)2 là 4,6625 mol
Khối lượng của Ca(OCl)2 cần dùng là mCa(OCl)2 = 4,6625.143 = 666,7375 gam = 667 gam
Điền đáp án: 667
Khối lượng chlorine trong hồ bơi là 80.3 = 240 gam
Bảo toàn nguyên tố Cl: nCl = nHClO = 240 : 35,5 = 480/71 mol
số mol của HClO ban đầu là
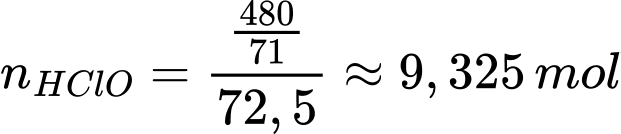
Từ phương trình số mol của Ca(OCl)2 là 4,6625 mol
Khối lượng của Ca(OCl)2 cần dùng là mCa(OCl)2 = 4,6625.143 = 666,7375 gam = 667 gam
Điền đáp án: 667