PHẦN I. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án
Câu 1 [575621]: Anion X2– có cấu hình electron lớp ngoài cùng là 3s23p6. Tổng số electron ở lớp vỏ của X2– là
A, 18.
B, 16.
C, 9.
D, 20.
HƯỚNG DẪN GIẢI:
Anion X2- có cấu hình electron lớp ngoài cùng là 3s23p6
⟹ Cấu hình electron của anion X2- là: 1s22s22p63s23p6
→ Tổng số electron lớp vỏ của X2- là 2 + 2 + 6 + 2 + 6 = 18.
⇒ Chọn đáp án A Đáp án: A
Anion X2- có cấu hình electron lớp ngoài cùng là 3s23p6
⟹ Cấu hình electron của anion X2- là: 1s22s22p63s23p6
→ Tổng số electron lớp vỏ của X2- là 2 + 2 + 6 + 2 + 6 = 18.
⇒ Chọn đáp án A Đáp án: A
Câu 2 [702807]: Trên phổ khối của một hợp chất X chỉ xuất hiện 3 tín hiệu ở m/z = 15, 57 và 72. Công thức cấu tạo nào sau đây phù hợp với tín hiệu trên phổ khối của X?
A, 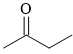

B, 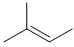

C, 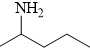

D, 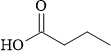

Giá trị tín hiệu m/z lớn nhất chính là khối lượng phân tử của chất X (m/z = 72).
Khối lượng phân tử của các hợp chất là:
✔️ A. CH3-C(O)-CH2-CH3 ⇒ M = 72
❌ B. CH3-C(CH3)=CH-CH3 ⇒ M = 70
❌ C. CH3-CH(NH2)-CH2-CH2-CH3 ⇒ M = 87
❌ D. HO-C(O)-CH2-CH2-CH3 ⇒ M = 88
⟿ Chọn đáp án A Đáp án: A
Khối lượng phân tử của các hợp chất là:
✔️ A. CH3-C(O)-CH2-CH3 ⇒ M = 72
❌ B. CH3-C(CH3)=CH-CH3 ⇒ M = 70
❌ C. CH3-CH(NH2)-CH2-CH2-CH3 ⇒ M = 87
❌ D. HO-C(O)-CH2-CH2-CH3 ⇒ M = 88
⟿ Chọn đáp án A Đáp án: A
Câu 3 [304846]: Etser X có công thức phân tử là C4H8O2. Thủy phân X trong dung dịch H2SO4 loãng, đun nóng, thu được sản phẩm gồm acetic acid và chất hữu cơ Y. Công thức Y là
A, HCOOH.
B, CH3OH.
C, C2H5COOH.
D, C2H5OH.
Phân tích phản ứng thủy phân ester trong môi trường acid:
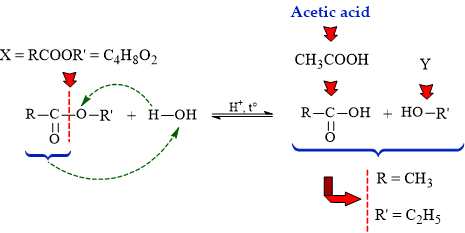
Đơn giản bảo toàn số C, H, O ⇒ gốc R' là C2H5 ⇒ Y là C2H5OH: ethyl alcohol
⇒ Chọn đáp án D Đáp án: D

Đơn giản bảo toàn số C, H, O ⇒ gốc R' là C2H5 ⇒ Y là C2H5OH: ethyl alcohol
⇒ Chọn đáp án D Đáp án: D
Câu 4 [308555]: Amine nào sau đây tồn tại ở trạng thái khí ở điều kiện thường?
A, aniline.
B, isopropylamine.
C, butylamine.
D, trimethylamine.
Ở điều kiện thường các amine như methylamine, dimethylamine, ethylamine, trimethyl amine là chất khí ở điều kiện thường.
⇒ Chọn đáp án D Đáp án: D
⇒ Chọn đáp án D Đáp án: D
Câu 5 [704019]: “Trong pin điện hoá, điện năng được sinh ra từ phản ứng ..(1).. là một quá trình ..(2)..”. Nội dung phù hợp trong ô trống (1), (2) lần lượt là
A, oxi hoá, không tự diễn biến.
B, oxi hoá - khử, tự diễn biến.
C, khử, tự diễn biến.
D, trao đổi, oxi hóa - khử.
- Trong pin điện hóa, điện năng được sinh ra nhờ vào sự chuyển đổi năng lượng hóa học thành năng lượng điện. Phản ứng xảy ra trong pin là một phản ứng oxi hóa - khử do có sự chuyển electron từ chất khử (bị oxi hóa) sang chất oxi hóa (bị khử).
- Phản ứng trong pin điện hóa là một phản ứng tự diễn biến, tức là nó có thể diễn ra mà không cần cung cấp năng lượng từ bên ngoài.
⇒ Trong pin điện hoá, điện năng được sinh ra từ phản ứng oxi hoá - khử là một quá trình tự diễn biến.
⇒ Chọn đáp án B Đáp án: B
- Phản ứng trong pin điện hóa là một phản ứng tự diễn biến, tức là nó có thể diễn ra mà không cần cung cấp năng lượng từ bên ngoài.
⇒ Trong pin điện hoá, điện năng được sinh ra từ phản ứng oxi hoá - khử là một quá trình tự diễn biến.
⇒ Chọn đáp án B Đáp án: B
Câu 6 [560607]: Kim loại nào sau đây dẫn điện tốt nhất?
A, Ag.
B, Al.
C, Cu.
D, Hg.
Ag dẫn điện tốt nhất, sau đó đến Cu, Au, Al, Fe,...
Bạc có độ dẫn điện cao nhất trong tất cả các kim loại, nhưng vì giá thành cao nên ít được sử dụng trong dây điện.
⇒ Chọn đáp án A Đáp án: A
Bạc có độ dẫn điện cao nhất trong tất cả các kim loại, nhưng vì giá thành cao nên ít được sử dụng trong dây điện.
⇒ Chọn đáp án A Đáp án: A
Câu 7 [702806]: Chất nào sau được dùng để khử chua đất trong nông nghiệp?
A, Calcium oxide.
B, Calcium sulfate.
C, Calcium chloride.
D, Calcium nitride.
Đất bị chua là đất có môi trường acid nên chọn chất cho thêm vào đất để trung hòa bớt lượng acid.
Chọn CaO cho vào đất, CaO sẽ tan vào trong nước tạo ra dung dịch kiềm Ca(OH)2 sẽ trung hòa bớt lượng acid có trong đất, từ đó làm cho đất bớt chua.
Chọn CaO cho vào đất, CaO sẽ tan vào trong nước tạo ra dung dịch kiềm Ca(OH)2 sẽ trung hòa bớt lượng acid có trong đất, từ đó làm cho đất bớt chua.
PTHH:
Đáp án: A CaO + H2O → Ca(OH)2
⇒ Chọn đáp án A
Câu 8 [705804]: Cho phản ứng thuận nghịch sau là một phản ứng đơn giản:
4NO(g) + 2O2(g) ⇌ 4NO2(g)
Biểu thức tốc độ phản ứng thuận được viết dưới dạng: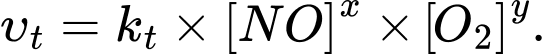 Giá trị của x, y lần lượt là
Giá trị của x, y lần lượt là
4NO(g) + 2O2(g) ⇌ 4NO2(g)
Biểu thức tốc độ phản ứng thuận được viết dưới dạng:
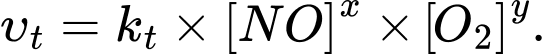 Giá trị của x, y lần lượt là
Giá trị của x, y lần lượt là A, 2, 1.
B, 4, 2.
C, 4, 4.
D, 1, 4.
x và y là hệ số cân bằng của NO và O2.
vt = kt × [NO]4 × [O2]2
x = 4 , y = 2
Chọn đáp án B Đáp án: B
vt = kt × [NO]4 × [O2]2
x = 4 , y = 2
Chọn đáp án B Đáp án: B
Câu 9 [705463]: “…(1)… là quá trình kết hợp nhiều phân tử …(2)… giống nhau hay tương tự nhau tạo thành phân tử có phân tử khối lớn”. Nội dung phù hợp trong ô trống (1), (2) lần lượt là
A, Xà phòng hoá, nhỏ.
B, Trùng hợp, nhỏ.
C, Trùng ngưng, lớn.
D, Lên men, lớn.
Trùng hợp là quá trình kết hợp nhiều phân tử nhỏ giống nhau hay tương tự nhau tạo thành phân tử có phân tử khối lớn.
Ví dụ:
Trùng hợp ethylene (C2H4) tạo polyethylene (PE):
nCH2=CH2 −xt, to⟶ (−CH2−CH2−)n
− Monomer: ethylene (CH2=CH2)
− Polymer: polyethylene ((−CH2−CH2−)n)
− Ứng dụng: Sản xuất túi nhựa, màng bọc thực phẩm, ống nhựa.
⇒ Chọn đáp án B Đáp án: B
Ví dụ:
Trùng hợp ethylene (C2H4) tạo polyethylene (PE):
nCH2=CH2 −xt, to⟶ (−CH2−CH2−)n
− Monomer: ethylene (CH2=CH2)
− Polymer: polyethylene ((−CH2−CH2−)n)
− Ứng dụng: Sản xuất túi nhựa, màng bọc thực phẩm, ống nhựa.
⇒ Chọn đáp án B Đáp án: B
Câu 10 [703986]: Một trong những hóa chất quan trọng nhất được sản xuất và sử dụng trên toàn thế giới là sulfuric acid. Sulfuric acid được sử dụng trong sản xuất kim loại, sản xuất sơn, phân bón, ắc quy ô tô, chất tẩy rửa, thuốc nhuộm và sợi và trong nông nghiệp. Quá trình dưới đây cho phép sản xuất sulfuric acid nồng độ cao với số lượng lớn.
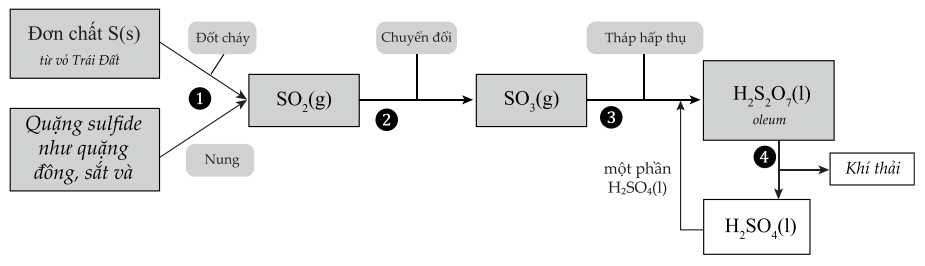
Trong các phát biểu sau:
(a) S trong các nguồn quặng có số oxi hóa 0.
(b) Số oxi hóa của sulfur có xu hướng tăng trong quá trình sản xuất.
(c) Để tăng hiệu suất chuyển hóa trong giai đoạn (2) có thể sử dụng xúc tác V2O5.
(d) Nồng độ của sulfuric acid có thể được tăng lên trong giai đoạn (3).
Các phát biểu đúng là

Trong các phát biểu sau:
(a) S trong các nguồn quặng có số oxi hóa 0.
(b) Số oxi hóa của sulfur có xu hướng tăng trong quá trình sản xuất.
(c) Để tăng hiệu suất chuyển hóa trong giai đoạn (2) có thể sử dụng xúc tác V2O5.
(d) Nồng độ của sulfuric acid có thể được tăng lên trong giai đoạn (3).
Các phát biểu đúng là
A, (a), (b).
B, (b), (c).
C, (a), (b), (c).
D, (b), (c), (d).
Phân tích các phát biểu:
❌ (a) Sai. Đơn chất S có số oxi hóa là 0, nhưng các quặng sulfide như FeS2, MoS2,… S đều có các trặng thái oxi hóa khác.
✔️ (b) Đúng. Số oxi hóa của Sulfur là 0 và các quặng sulfide có số oxi -1 tăng dần lên +6 trong H2SO4.
✔️ (c) Đúng. V2O5 là chất xúc tác cho quá trình từ SO2 thành SO3.
✔️ (d) Đúng. Giai đoạn (3) tháp hấp thụ nSO3 bằng dung dịch H2SO4 tạo thành oleum (H2SO4.nSO3), pha loãng oleum thành H2SO4 với một lượng nước phù hợp thu được các dung dịch H2SO4 với các nồng độ mong muốn.
Các phát biểu đúng là (b), (c), (d)
⇒ Chọn đáp án D Đáp án: D
❌ (a) Sai. Đơn chất S có số oxi hóa là 0, nhưng các quặng sulfide như FeS2, MoS2,… S đều có các trặng thái oxi hóa khác.
✔️ (b) Đúng. Số oxi hóa của Sulfur là 0 và các quặng sulfide có số oxi -1 tăng dần lên +6 trong H2SO4.
✔️ (c) Đúng. V2O5 là chất xúc tác cho quá trình từ SO2 thành SO3.
✔️ (d) Đúng. Giai đoạn (3) tháp hấp thụ nSO3 bằng dung dịch H2SO4 tạo thành oleum (H2SO4.nSO3), pha loãng oleum thành H2SO4 với một lượng nước phù hợp thu được các dung dịch H2SO4 với các nồng độ mong muốn.
Các phát biểu đúng là (b), (c), (d)
⇒ Chọn đáp án D Đáp án: D
Câu 11 [706070]: Với nhu cầu chế tạo vật liệu an toàn với môi trường, năm 2005 sản phẩm “hộp bã mía" - bao bì từ thực vật và an toàn cho sức khoẻ với nhiều tính năng vượt trội so với hộp xốp đã ra đời. Đây là loại bao bì có thành phần hoàn toàn tự nhiên, phần lớn là sợi bã mía từ nhà máy đường, với khả năng chịu nhiệt rộng từ –40°C đến 200°C, bền nhiệt trong lò vi sóng, lò nướng nên an toàn với sức khoẻ con người. Phát biểu nào sau đây không đúng?
A, Thành phần chính của hộp bã mía là cellulose.
B, Hộp bã mía phân huỷ sinh học được nên thân thiện với môi trường.
C, Hộp xốp đựng thức ăn nhanh làm từ chất dẻo PS cũng là vật liệu dễ phân huỷ sinh học.
D, Thành phần chính của hộp bã mía là polymer thiên nhiên, còn hộp xốp là polymer tổng hợp.
Phân tích các đáp án :
✔️A – Đúng. Hộp bã mía là một loại hộp đựng thực phẩm thân thiện với môi trường, được làm từ bã mía – phần còn lại sau khi ép mía lấy nước.
✔️B – Đúng. Hộp bã mía làm từ sợi thực vật tự nhiên nên có thể phân huỷ nhờ vi sinh vật, không gây ô nhiễm, giúp giảm rác thải nhựa, vì vậy thân thiện với môi trường.
❌C – Sai. Hộp xốp đựng thức ăn nhanh làm từ chất dẻo PS không phải là vật liệu dễ phân huỷ sinh học.
✔️D – Đúng. Hộp bã mía làm từ cellulose – polymer có sẵn trong tự nhiên. Hộp xốp làm từ polystyren – polymer do con người tổng hợp từ hóa dầu.
⟹ Chọn đáp án C Đáp án: C
✔️A – Đúng. Hộp bã mía là một loại hộp đựng thực phẩm thân thiện với môi trường, được làm từ bã mía – phần còn lại sau khi ép mía lấy nước.
✔️B – Đúng. Hộp bã mía làm từ sợi thực vật tự nhiên nên có thể phân huỷ nhờ vi sinh vật, không gây ô nhiễm, giúp giảm rác thải nhựa, vì vậy thân thiện với môi trường.
❌C – Sai. Hộp xốp đựng thức ăn nhanh làm từ chất dẻo PS không phải là vật liệu dễ phân huỷ sinh học.
✔️D – Đúng. Hộp bã mía làm từ cellulose – polymer có sẵn trong tự nhiên. Hộp xốp làm từ polystyren – polymer do con người tổng hợp từ hóa dầu.
⟹ Chọn đáp án C Đáp án: C
Câu 12 [307753]: Khi cho dung dịch sulfuric acid H2SO4 đặc vào trong cốc đựng các hợp chất carbohydrate, chúng sẽ bị mất nước và chuyển thành
A, C – carbon.
B, H2 – khí hydrogen.
C, O2 – khí oxygen.
D, H2O2 – hydrogen peroxide.
Hợp chất carbohydrate (hydrate của carbon) có dạng Cn(H2O)m ⇒ tư duy đơn giản, H2SO4 đặc háo nước, lấy mất nước là H2O; mất hết nước là mất mH2O thì phần còn lại chỉ có Cn hay nC chính là carbon:
Cn(H2O)m ––H2SO4 đặc→ nC + mH2O.
⇝ thí nghiệm quan sát được chât rắn có màu đen được hình thành.

⟹ Chọn đáp án A.
Đáp án: A
Câu 13 [309408]: Khi nấu canh cua thì thấy các mảng “riêu cua” nổi lên là do
A, Phản ứng thủy phân của protein.
B, Phản ứng màu của protein.
C, Sự đông tụ của lipid.
D, Sự đông tụ của protein do nhiệt độ.
Protein sẽ bị đông tụ dưới tác dụng của nhiệt, acid, base hoặc ion kim loại nặng. Sự đông tụ này xảy ra do cấu tạo ban đầu của protein bị biến đổi.
⇒ Chọn đáp án D Đáp án: D
⇒ Chọn đáp án D Đáp án: D
Câu 14 [704029]: Histidine là một trong 20 loại amino acid có trong protein. Phân tử histidine được proton hóa hoàn toàn được hiển thị ở đây, trong đó các con số biểu thị Ka của các nhóm tương ứng:
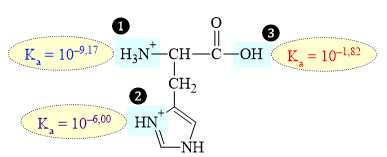
Biết rằng ion H+ đầu tiên sẽ tách ra khỏi nhóm acid mạnh nhất, sau đó là nhóm acid mạnh tiếp theo,… Sau khi tách ion H+ của nhóm nào thì tạo ra được phân tử trung hòa về điện?

Biết rằng ion H+ đầu tiên sẽ tách ra khỏi nhóm acid mạnh nhất, sau đó là nhóm acid mạnh tiếp theo,… Sau khi tách ion H+ của nhóm nào thì tạo ra được phân tử trung hòa về điện?
A, Nhóm ❶.
B, Nhóm ❷.
C, Nhóm ❸.
D, Không tách H+.
Ka càng lớn tính acid càng mạnh → thứ tự tách H+ là 3 > 2 > 1.
Quá trình proton hóa hoàn toàn phân tử histidine được diễn ra như sau:
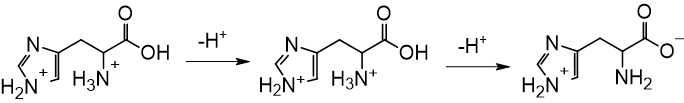
Từ đó thấy được sau khi tách ion H+ của nhóm số 2 thì tạo ra được phân tử trung hòa về điện.
⇒ Chọn đáp án B Đáp án: B
Quá trình proton hóa hoàn toàn phân tử histidine được diễn ra như sau:

Từ đó thấy được sau khi tách ion H+ của nhóm số 2 thì tạo ra được phân tử trung hòa về điện.
⇒ Chọn đáp án B Đáp án: B
Câu 15 [705987]: Tiến hành thí nghiệm:
∎ Bước 1: Thêm hexane (chất lỏng không phân cực) vào dung dịch nước iodine, lắc đều rồi để yên.
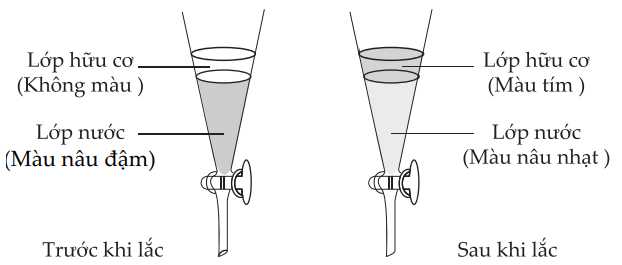
∎ Bước 2: Sau đó thu lấy lớp hữu cơ, làm bay hơi dung môi để thu lấy iodine.
Phát biểu nào sau đây không đúng?
∎ Bước 1: Thêm hexane (chất lỏng không phân cực) vào dung dịch nước iodine, lắc đều rồi để yên.

∎ Bước 2: Sau đó thu lấy lớp hữu cơ, làm bay hơi dung môi để thu lấy iodine.
Phát biểu nào sau đây không đúng?
A, Phương pháp chiết đã được sử dụng trong thí nghiệm trên.
B, Trước khi lắc, lớp hữu cơ không chứa iodine.
C, Sau khi lắc và để yên, toàn bộ iodine được chuyển lên lớp hữu cơ.
D, Để thu được lớp hữu cơ cần mở van và loại bỏ lớp nước ở bên dưới trước.
Phân tích các đáp án :
✔️A – Đúng. Chiết chất từ môi trường lỏng (chiết lỏng – lỏng): Cho dung dd chứa chất cần chiết vào phểu chiết, thêm dung môi cần dùng để chiết, lắc đều phểu chiết, để yên rồi dung dịch sẽ tách thành 2 lớp. Mở khóa phễu chiết sẽ thu được 2 chất lỏng riêng biệt.
✔️B – Đúng. Trước khi lắc, lớp hữu cơ không màu chứng tỏ chưa có iodine tan trong lớp hữu cơ.
❌C – Sai. Sau khi lắc và để yên, một phần iodine được chuyển lên lớp hữu cơ.
✔️D – Đúng. Khi mở van lớp nước ở dưới chảy ra trước và loại bỏ lớp nước còn lại lớp hữu cơ.
⟹Chọn đáp án C Đáp án: C
✔️A – Đúng. Chiết chất từ môi trường lỏng (chiết lỏng – lỏng): Cho dung dd chứa chất cần chiết vào phểu chiết, thêm dung môi cần dùng để chiết, lắc đều phểu chiết, để yên rồi dung dịch sẽ tách thành 2 lớp. Mở khóa phễu chiết sẽ thu được 2 chất lỏng riêng biệt.
✔️B – Đúng. Trước khi lắc, lớp hữu cơ không màu chứng tỏ chưa có iodine tan trong lớp hữu cơ.
❌C – Sai. Sau khi lắc và để yên, một phần iodine được chuyển lên lớp hữu cơ.
✔️D – Đúng. Khi mở van lớp nước ở dưới chảy ra trước và loại bỏ lớp nước còn lại lớp hữu cơ.
⟹Chọn đáp án C Đáp án: C
Câu 16 [561016]: Số hiệu nguyên tử của chromium là 24. Theo các nguyên lí và quy tắc thông thường thì cấu hình electron của nguyên tử chromium được viết ở dạng (I). Tuy nhiên, dựa vào kết quả thực nghiệm về phổ phát xạ của nguyên tử chromium người ta nhận thấy phải có 6 nguyên tử electron độc thân nên cấu hình electron phải được viết ở dạng (II). Dạng (I) và dạng (II) lần lượt là
A, 1s22s22p63s23p63d44s2 và 1s22s22p63s23p63d54s1.
B, 1s22s22p63s23p63d6 và 1s22s22p63s23p63d44s2.
C, 1s22s22p63s23p63d6 và 1s22s22p63s23p63d54s1.
D, 1s22s22p63s23p63d54s2 và 1s22s22p63s23p63d54s24p24d2.
Dạng 1. Cấu hình electron của Cr (các orbital được lấp đầy theo mức năng lượng từ thấp đến cao):
1s22s22p63s23p63d44s2
Dạng 2. Một electron từ orbital 3d chuyển sang 4s, dẫn đến cấu hình electron:
1s22s22p63s23p63d54s1
Chọn đáp án A Đáp án: A
1s22s22p63s23p63d44s2
Dạng 2. Một electron từ orbital 3d chuyển sang 4s, dẫn đến cấu hình electron:
1s22s22p63s23p63d54s1
Chọn đáp án A Đáp án: A
Sử dụng thông tin cho dưới đây để trả lời các câu số 17 – 18:
Cho bảng thế điện cực chuẩn của các cặp oxi hóa – khử như sau:

Thiết lập một pin Galvani nối với bóng đèn hình vẽ bên. Trong đó 2 điện cực A và B là hai trong số các cặp oxi hóa – khử bên trên. Giả sử một bóng đèn cần tối thiểu 1,5 V để hoạt động.
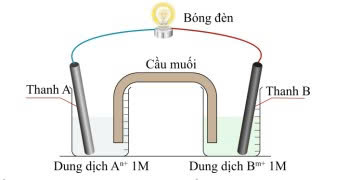

Thiết lập một pin Galvani nối với bóng đèn hình vẽ bên. Trong đó 2 điện cực A và B là hai trong số các cặp oxi hóa – khử bên trên. Giả sử một bóng đèn cần tối thiểu 1,5 V để hoạt động.

Câu 17 [702618]: Nếu dung dịch A và B được thiết lập từ các cặp oxi hoá khử là Fe2+/Fe và Ag+/Ag ở điều kiện chuẩn thì quá trình xảy ra ở cực âm là
A, Fe(s)  Fe2+(aq) +2e.
Fe2+(aq) +2e.
 Fe2+(aq) +2e.
Fe2+(aq) +2e.B, Fe2+(aq) + 2e  Fe(s).
Fe(s).
 Fe(s).
Fe(s).C, Ag+(aq) + 1e  Ag(s).
Ag(s).
 Ag(s).
Ag(s).D, Ag(s)  Ag+(aq) + 1e.
Ag+(aq) + 1e.
 Ag+(aq) + 1e.
Ag+(aq) + 1e.
Pin Galvani gồm hai điện cực được nối với nhau bằng cầu muối. Khi pin hoạt động, ở điện cực âm (anode) xảy ra quá trình oxi hoá kim loại và ở điện cực dương (cathode) xảy ra quá trình khử cation.
Cực dương là kim loại có thế điện cực lớn hơn, cực âm là kim loại có thế điện cực nhỏ hơn.
Vì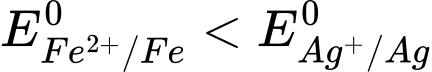 nên cực âm là Fe.
nên cực âm là Fe.
Cực dương là kim loại có thế điện cực lớn hơn, cực âm là kim loại có thế điện cực nhỏ hơn.
Vì
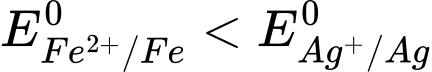 nên cực âm là Fe.
nên cực âm là Fe.Khi pin hoạt động, ở điện cực âm (anode) xảy ra quá trình oxi hoá kim loại: Fe(s) → Fe2+(aq)+ 2e.
⇒ Chọn đáp án A
⇒ Chọn đáp án A
Câu 18 [702619]: Có bao nhiêu cách tạo ra pin Galvani được thiết lập từ hai cặp oxi hóa – khử trong số các cặp trong bảng trên để bóng đèn hoạt động?
A, 1.
B, 2.
C, 3.
D, 4.
Để bóng đèn hoạt động thì cần tối thiểu 1,5 V. Ta xét bảng hiệu điện thế của các cặp oxi hoá - khử như sau:
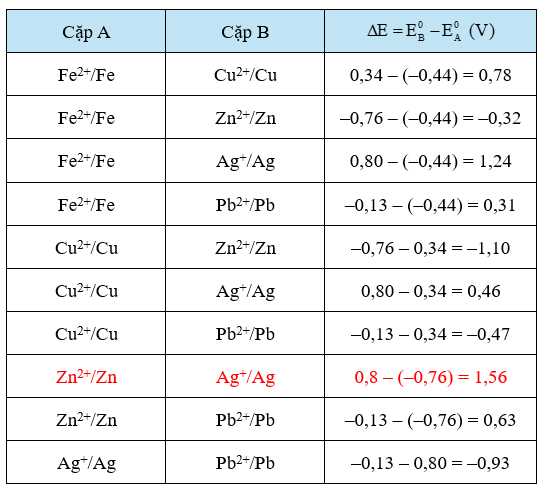
Vậy chỉ có 1 cặp oxi hóa – khử có hiệu điện thế lớn hơn 1,5: Ag được tạo ra ở cực dương, Zn2+ được tạo ra ở cực âm.
⇒ Chọn đáp án A Đáp án: A

Vậy chỉ có 1 cặp oxi hóa – khử có hiệu điện thế lớn hơn 1,5: Ag được tạo ra ở cực dương, Zn2+ được tạo ra ở cực âm.
⇒ Chọn đáp án A Đáp án: A
PHẦN II. Thí sinh trả lời từ câu 1 đến câu 4. Trong mỗi ý a), b), c), d) ở mỗi câu, thí sinh chọn đúng hoặc sai.
Câu 19 [702819]: Đối với các trường hợp đơn giản, trong phức chất, số phối trí là số liên kết được tạo thành giữa một nguyên tử kim loại trung tâm với các phối tử. Xét trường hợp của cobalt tạo thành một phức chất có cấu trúc đơn giản như hình bên.
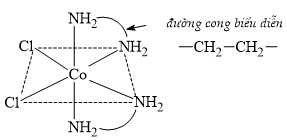

Phân tích các phát biểu:
✔️ a) Đúng. Trong phức chất, số oxi hóa của cobalt là +2.
❌ b) Sai. Số phối tử của phức chất là 4 gồm gồm 2 phối tử Cl- và 2 phối tử đa càng H2N–CH2CH2–NH2 (mỗi phối tử tạo 2 liên kết).
✔️ c) Đúng. Phức chất có 6 đỉnh tạo thành dạng hình học bát diện.
❌ d) Sai. Có thể thay 2 phối tử Cl– bằng 1 phối tử NH2–CH2CH2–NH2 mà vẫn giữ nguyên số phối trí do 1 phối tử NH2–CH2CH2–NH2 tạo 2 liên kết.
✔️ a) Đúng. Trong phức chất, số oxi hóa của cobalt là +2.
❌ b) Sai. Số phối tử của phức chất là 4 gồm gồm 2 phối tử Cl- và 2 phối tử đa càng H2N–CH2CH2–NH2 (mỗi phối tử tạo 2 liên kết).
✔️ c) Đúng. Phức chất có 6 đỉnh tạo thành dạng hình học bát diện.
❌ d) Sai. Có thể thay 2 phối tử Cl– bằng 1 phối tử NH2–CH2CH2–NH2 mà vẫn giữ nguyên số phối trí do 1 phối tử NH2–CH2CH2–NH2 tạo 2 liên kết.
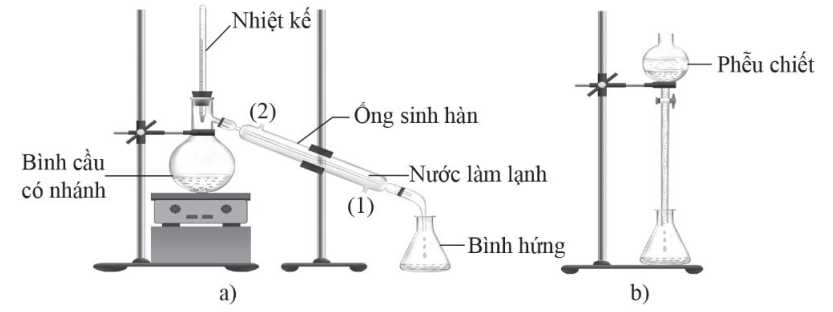
Câu 20 [703974]: Tiến hành thí nghiệm điều chế propyl acetate (chất có mùi thơm như quả lê) theo thứ tự các bước sau đây:
Bước 1: Cho khoảng 10 mL CH3CH2CH2OH, 10 mL CH3COOH và 5 mL H2SO4 đặc vào bình cầu có nhánh.
Bước 2: Tiến hành đun nóng khoảng 5 – 7 phút ở 65 – 70°C.
Bước 3: Làm lạnh bằng ống sinh hàn, thu được chất lỏng ở bình hứng.
Bước 4: Cho chất lỏng ở bình hứng vào phễu chiết, sau đó thêm dung dịch NaCl bão hòa vào phễu chiết và tách lấy ester propyl acetate.
Bước 1: Cho khoảng 10 mL CH3CH2CH2OH, 10 mL CH3COOH và 5 mL H2SO4 đặc vào bình cầu có nhánh.
Bước 2: Tiến hành đun nóng khoảng 5 – 7 phút ở 65 – 70°C.
Bước 3: Làm lạnh bằng ống sinh hàn, thu được chất lỏng ở bình hứng.
Bước 4: Cho chất lỏng ở bình hứng vào phễu chiết, sau đó thêm dung dịch NaCl bão hòa vào phễu chiết và tách lấy ester propyl acetate.

Phân tích các phát biểu:
✔️ a) Đúng. Phản ứng cần đun nóng ở 65 – 70 oC thì mới xảy ra được, dùng nhiệt kế để đảm bảo nhiệt độ trong khoảng đấy (duy trì nhiệt độ này là phù hợp vì chỉ cần đun ở nhiệt độ cao hơn, ví dụ 97 oC thì propan-1-ol đã bị bay hơi).
✔️ b) Đúng. Khi lắp ống sinh hàn thì nước phải được đi vào từ đầu thấp phía dưới và đi ra từ đầu phía trên. Nếu lắp ngược lại sẽ gây ra hiện tượng thiếu nước cho ống sinh hàn, khiến ống bị nóng và có thể gây vết nứt và làm giảm hiệu quả của sự ngưng tụ.
❌ c) Sai. Ester thường nhẹ hơn nước nên sẽ nổi trên mặt nước, phần chất lỏng phía trên là propyl acetate và phía dưới là nước.
❌ d) Sai. Chất có nhiệt độ sôi thấp hơn sẽ bay hơn trước, chất lỏng trong bình hứng có phần lớn là ester.
✔️ a) Đúng. Phản ứng cần đun nóng ở 65 – 70 oC thì mới xảy ra được, dùng nhiệt kế để đảm bảo nhiệt độ trong khoảng đấy (duy trì nhiệt độ này là phù hợp vì chỉ cần đun ở nhiệt độ cao hơn, ví dụ 97 oC thì propan-1-ol đã bị bay hơi).
✔️ b) Đúng. Khi lắp ống sinh hàn thì nước phải được đi vào từ đầu thấp phía dưới và đi ra từ đầu phía trên. Nếu lắp ngược lại sẽ gây ra hiện tượng thiếu nước cho ống sinh hàn, khiến ống bị nóng và có thể gây vết nứt và làm giảm hiệu quả của sự ngưng tụ.
❌ c) Sai. Ester thường nhẹ hơn nước nên sẽ nổi trên mặt nước, phần chất lỏng phía trên là propyl acetate và phía dưới là nước.
❌ d) Sai. Chất có nhiệt độ sôi thấp hơn sẽ bay hơn trước, chất lỏng trong bình hứng có phần lớn là ester.
Câu 21 [703018]: Lactose là một hợp chất carbohydrate có trong sữa và các sản phẩm từ sữa khác.
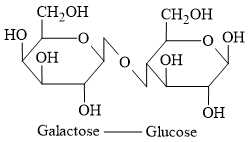
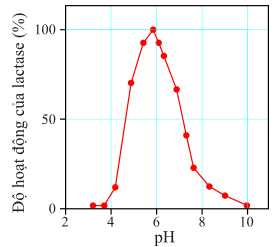
Khi lactose được tiêu hóa, liên kết giữa hai monosaccharide bị phá vỡ. Enzyme chịu trách nhiệm phá vỡ liên kết là lactase, được tìm thấy trong ruột non. Hàng triệu người thiếu hụt đủ lượng lactase, khiến họ không thể tiêu hóa lactose đầy đủ, dẫn đến tình trạng được gọi là không dung nạp lactose. Nghiên cứu biểu đồ và trả lời các câu hỏi.

Khi lactose được tiêu hóa, liên kết giữa hai monosaccharide bị phá vỡ. Enzyme chịu trách nhiệm phá vỡ liên kết là lactase, được tìm thấy trong ruột non. Hàng triệu người thiếu hụt đủ lượng lactase, khiến họ không thể tiêu hóa lactose đầy đủ, dẫn đến tình trạng được gọi là không dung nạp lactose. Nghiên cứu biểu đồ và trả lời các câu hỏi.

Phân tích các phát biểu:
✔️ a) Đúng. Enzyme lactase sẽ thủy phân lactose thành glucose và galactose do lactose cấu tạo từ glucose và galactose.
✔️ b) Đúng. Tại pH = 6 độ hoạt động của lactase lớn nhất là 100% nên lượng sản phẩm monosacchride thu được là lớn nhất.
❌ c) Sai. Tại pH = 5,5 độ hoạt động của lactase khoảng 90%.
❌ d) Sai. Độ hoạt động của lactase giảm khi tăng pH từ 6 – 10.
✔️ a) Đúng. Enzyme lactase sẽ thủy phân lactose thành glucose và galactose do lactose cấu tạo từ glucose và galactose.
✔️ b) Đúng. Tại pH = 6 độ hoạt động của lactase lớn nhất là 100% nên lượng sản phẩm monosacchride thu được là lớn nhất.
❌ c) Sai. Tại pH = 5,5 độ hoạt động của lactase khoảng 90%.
❌ d) Sai. Độ hoạt động của lactase giảm khi tăng pH từ 6 – 10.
Câu 22 [703833]: Sơ đồ dưới đây là các thiết bị được sử dụng để thu thập và đo thể tích khí hydrogen thoát ra khi một mẫu kim loại nhóm IIA phản ứng với hydrochloric acid loãng:
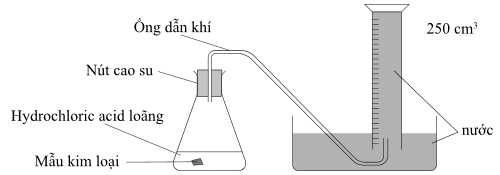
Các bước tiến hành:
▪ Bước 1: Một mẫu kim loại được cân và sau đó đặt vào bình tam giác.
▪ Bước 2: Cho một lượng acid dư vào bình tam giác, nắp bằng nút cao su có dây dẫn khí ra ngoài.
▪ Bước 3: Thu khí bằng phương pháp đẩy nước. Khi phản ứng hoàn tất và khí thu được đã nguội đến nhiệt độ phòng, ghi lại thể tích khí thu được trong ống đong chia vạch.
Giả sử 1 mol hydrogen có thể tích là 24,0 dm3 trong điều kiện thực nghiệm. Kết quả được ghi lại trong bảng sau:


Các bước tiến hành:
▪ Bước 1: Một mẫu kim loại được cân và sau đó đặt vào bình tam giác.
▪ Bước 2: Cho một lượng acid dư vào bình tam giác, nắp bằng nút cao su có dây dẫn khí ra ngoài.
▪ Bước 3: Thu khí bằng phương pháp đẩy nước. Khi phản ứng hoàn tất và khí thu được đã nguội đến nhiệt độ phòng, ghi lại thể tích khí thu được trong ống đong chia vạch.
Giả sử 1 mol hydrogen có thể tích là 24,0 dm3 trong điều kiện thực nghiệm. Kết quả được ghi lại trong bảng sau:

Phân tích các phát biểu:
✔️ a) Đúng. Có thể thay dung dịch hydrochloric acid loãng bằng dung dịch sulfuricacid loãng vì cả hai đều cung cấp ion H+ để giải phóng khí H2.
✔️ b) Đúng. Đổi 230 cm3 = 0,23 dm3
Gọi kim loại cần tìm là M.
2M + 2nHCl → 2MCln + nH2
Số mol của khí là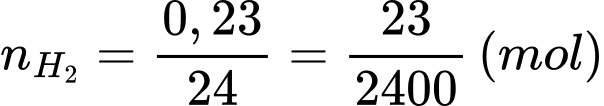
→ Số mol của M là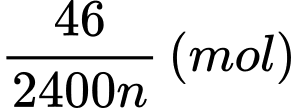
Khối lượng của kim loại là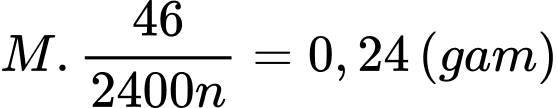 .
.
Ta có bảng sau:
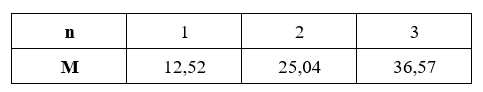
→ M có thể Mg.
❌ c) Sai. H2 nhẹ hơn không khí, nếu dùng phương pháp đẩy không khí ngửa bình thì sẽ bay hết ra ngoài.
✔️ d) Đúng. Mực nước trong trong bình chứa ống đong chia vạch tăng lên so với ban đầu do H2 được đẩy vào trong ống đong chia vạch làm nước trong ống đong đi ra ngoài bình.
✔️ a) Đúng. Có thể thay dung dịch hydrochloric acid loãng bằng dung dịch sulfuricacid loãng vì cả hai đều cung cấp ion H+ để giải phóng khí H2.
✔️ b) Đúng. Đổi 230 cm3 = 0,23 dm3
Gọi kim loại cần tìm là M.
2M + 2nHCl → 2MCln + nH2
Số mol của khí là
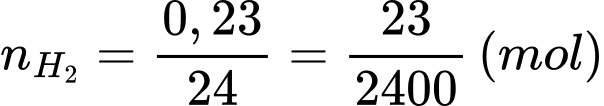
→ Số mol của M là
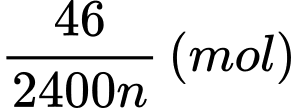
Khối lượng của kim loại là
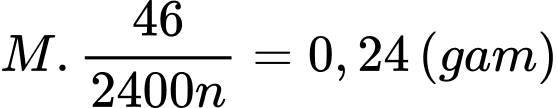 .
.Ta có bảng sau:

→ M có thể Mg.
❌ c) Sai. H2 nhẹ hơn không khí, nếu dùng phương pháp đẩy không khí ngửa bình thì sẽ bay hết ra ngoài.
✔️ d) Đúng. Mực nước trong trong bình chứa ống đong chia vạch tăng lên so với ban đầu do H2 được đẩy vào trong ống đong chia vạch làm nước trong ống đong đi ra ngoài bình.
PHẦN III. Thí sinh trả lời từ câu 1 đến 6. Thí sinh điền kết quả mỗi câu vào mỗi ô trả lời tương ứng theo hướng dẫn của phiếu trả lời.
Câu 23 [703836]: Thuỷ phân 1 mol tetrapeptide Lys-Gly-Val-Glu trong lượng dư dung dịch NaOH, sau khi các phản ứng xảy ra hoàn toàn thì có bao nhiêu mol NaOH đã tham gia?
Khi thuỷ phân 1 mol tetrapeptide Lys-Gly-Val-Glu trong lượng dư dung dịch NaOH, phản ứng xảy ra như sau:
Lys−Gly−Val−Glu + 5NaOH → Gly−Na + Lys−Na + Val−Na + Glu−Na2 + 2H2O
⤏ Tetrapeptide phản ứng với NaOH theo tỉ lệ 1:5 nên số mol NaOH đã tham gia thuỷ phân 1 mol tetrapeptide là 5 mol.
⇒ Điền đáp án: 5
Lys−Gly−Val−Glu + 5NaOH → Gly−Na + Lys−Na + Val−Na + Glu−Na2 + 2H2O
⤏ Tetrapeptide phản ứng với NaOH theo tỉ lệ 1:5 nên số mol NaOH đã tham gia thuỷ phân 1 mol tetrapeptide là 5 mol.
⇒ Điền đáp án: 5
Câu 24 [703937]: Conidiogene B có nhiều hoạt tính sinh học quan trọng, trong đó Conidiogenone B thể hiện đặc tính kháng khuẩn rõ rệt với chủng Staphylococcus aureus kháng methicillin. Conidiogenone B có công thức cấu tạo như hình bên. Có bao nhiêu nhánh methyl (–CH3) có trong một phân tử Conidiogene B?
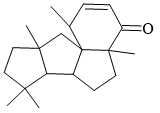

Các nhánh methyl có trong phân tử Conidiogene B ở các vị trí như sau:
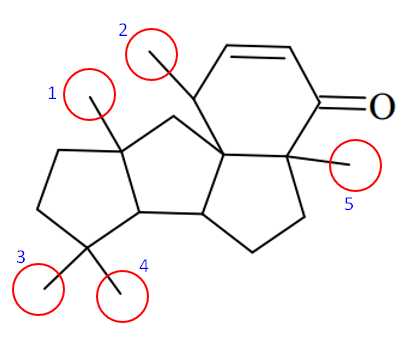
⇒ Điền đáp án: 5

⇒ Điền đáp án: 5
Câu 25 [702624]: Để sản xuất được 1 triệu chiếc chảo gang có hàm lượng sắt là 95% thì cần dùng tối thiểu x tấn quặng magnetite chứa 80% Fe3O4. Giả sử mỗi chiếc chảo gang nặng 3,2 kg và trong quá trình sản xuất lượng sắt bị hao hụt là 8%. Giá trị của x là bao nhiêu? (làm tròn đến số nguyên)
Khối lượng sắt có trong 1 triệu chảo gang là: 1000000.3,2.95% = 3040000 kg = 3040 tấn
Lượng Fe thực tế là: mFe = 100% - 8% hao hụt = 92%
Sơ đồ phản ứng: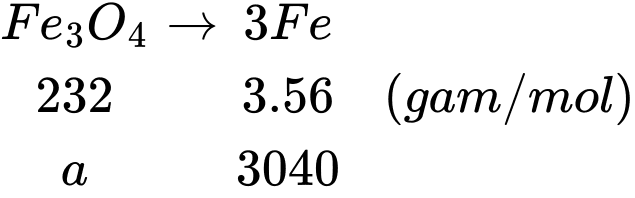
→ Khối lượng Fe3O4 trong quặng magnetite là: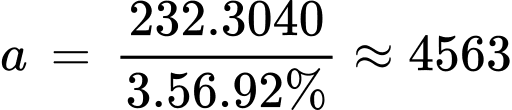 (tấn)
(tấn)
→ Khối lượng quặng magnetite là: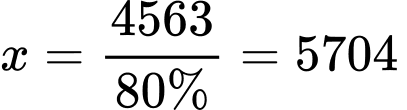 (tấn)
(tấn)
⇒ Điền đáp án: 5704
Lượng Fe thực tế là: mFe = 100% - 8% hao hụt = 92%
Sơ đồ phản ứng:
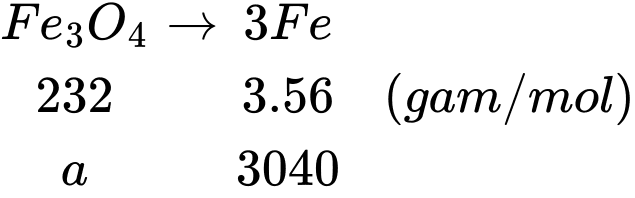
→ Khối lượng Fe3O4 trong quặng magnetite là:
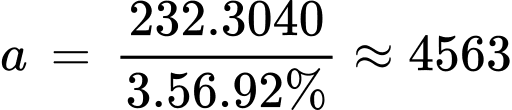 (tấn)
(tấn)→ Khối lượng quặng magnetite là:
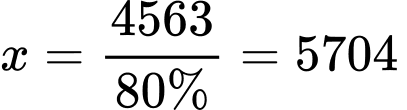 (tấn)
(tấn)⇒ Điền đáp án: 5704
Câu 26 [703939]: Một bạn học sinh tiến hành điều chế xà phòng tại nhà từ dầu thực vật theo các bước trong một quy trình như sau:
(1) Thêm từ từ dung dịch sodium hydroxide vào dầu, khuấy liên tục.
(2) Thu lấy chất rắn nổi bên trên. Rửa hai lần bằng nước cất để loại bỏ NaOH dư và thu lấy sản phẩm.
(3) Sau khoảng 30 phút, hỗn hợp sẽ trở nên đặc và giống như kem. Đổ hỗn hợp vào cốc chứa NaCl bão hòa, để nguội.
(4) Đổ dầu thực vật vào 1 cốc thủy tinh 150 mL, đun cách thủy.
Hãy viết liền các số tương ứng với bốn bước theo đúng trình của quá trình sản xuất xà phòng (ví dụ: 1234, 4213, ...).
(1) Thêm từ từ dung dịch sodium hydroxide vào dầu, khuấy liên tục.
(2) Thu lấy chất rắn nổi bên trên. Rửa hai lần bằng nước cất để loại bỏ NaOH dư và thu lấy sản phẩm.
(3) Sau khoảng 30 phút, hỗn hợp sẽ trở nên đặc và giống như kem. Đổ hỗn hợp vào cốc chứa NaCl bão hòa, để nguội.
(4) Đổ dầu thực vật vào 1 cốc thủy tinh 150 mL, đun cách thủy.
Hãy viết liền các số tương ứng với bốn bước theo đúng trình của quá trình sản xuất xà phòng (ví dụ: 1234, 4213, ...).
Quy trình điều chế xà phòng:
▫️ Bước 1: Đổ dầu thực vật vào 1 cốc thủy tinh 150 mL, đun cách thủy. → Ứng với (4).
▫️ Bước 2: Thêm từ từ dung dịch sodium hydroxide vào dầu, khuấy đều liên tục. → Ứng với (1).
▫️ Bước 3: Sau 30 phút, hỗn hợp sẽ trở lên đặc và giống như kem. Đổ hỗn hợp vào cốc chứa NaCl bão hòa, để nguội. → Ứng với (3).
▫️ Bước 4: Thu lấy chất rắn nổi bên trên. Rửa hai lần bằng nước cất để loại bỏ NaOH dư và thu lấy sản phẩm. → Ứng với (2).
⇒ Điền đáp án: 4132
▫️ Bước 1: Đổ dầu thực vật vào 1 cốc thủy tinh 150 mL, đun cách thủy. → Ứng với (4).
▫️ Bước 2: Thêm từ từ dung dịch sodium hydroxide vào dầu, khuấy đều liên tục. → Ứng với (1).
▫️ Bước 3: Sau 30 phút, hỗn hợp sẽ trở lên đặc và giống như kem. Đổ hỗn hợp vào cốc chứa NaCl bão hòa, để nguội. → Ứng với (3).
▫️ Bước 4: Thu lấy chất rắn nổi bên trên. Rửa hai lần bằng nước cất để loại bỏ NaOH dư và thu lấy sản phẩm. → Ứng với (2).
⇒ Điền đáp án: 4132
Câu 27 [308749]: Cho sơ đồ chuyển hóa sau:
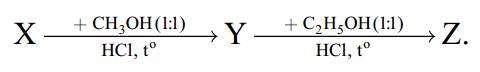
Biết X là glutamic acid, Y, Z, T là các chất hữu cơ chứa nitrogen. Số nguyên tử hydrogen trong phân tử Z là bao nhiêu?
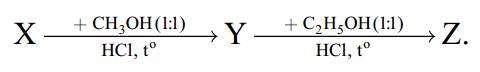
Biết X là glutamic acid, Y, Z, T là các chất hữu cơ chứa nitrogen. Số nguyên tử hydrogen trong phân tử Z là bao nhiêu?
Các phản ứng xảy ra:
H2NC3H5(COOH)2 (X) + CH3OH + HCl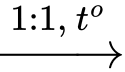 ClH3NC3H5(COOCH3)(COOH) (Y) + H2O
ClH3NC3H5(COOCH3)(COOH) (Y) + H2O
ClH3NC3H5(COOCH3)(COOH) (Y) + C2H5OH + HCl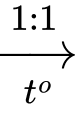 ClH3NC3H5(COOCH3)(COOC2H5) (Z) + H2O
ClH3NC3H5(COOCH3)(COOC2H5) (Z) + H2O
→ Số nguyên tử hydrogen trong phân tử Z là 16.
⇒ Điền đáp án: 16
H2NC3H5(COOH)2 (X) + CH3OH + HCl
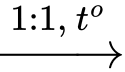 ClH3NC3H5(COOCH3)(COOH) (Y) + H2O
ClH3NC3H5(COOCH3)(COOH) (Y) + H2OClH3NC3H5(COOCH3)(COOH) (Y) + C2H5OH + HCl
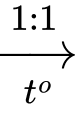 ClH3NC3H5(COOCH3)(COOC2H5) (Z) + H2O
ClH3NC3H5(COOCH3)(COOC2H5) (Z) + H2O→ Số nguyên tử hydrogen trong phân tử Z là 16.
⇒ Điền đáp án: 16
Câu 28 [702628]: Nescafe đã sản xuất thành công lon cafe tự làm nóng. Để làm nóng cafe, chỉ cần ấn nút (trên lon) để trộn nguyên liệu gồm một dung dịch KOH hoặc NaOH rất loãng và CaO; 210 mL cafe trong lon sẽ được hâm nóng đến khoảng 40°C. Giả sử nhiệt dung riêng của cafe là 4,2 J/g.K (nhiệt dung riêng là nhiệt lượng cần cung cấp để 1 gam chất tăng lên 1oC). Biết enthalpy tiêu chuẩn của các chất được cho trong bảng sau:
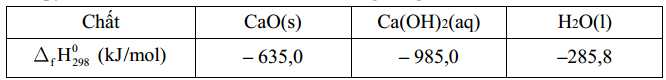
Nhiệt tỏa ra từ phản ứng thất thoát vào sản phẩm, vỏ hộp và môi trường là 20%. Cần cung cấp bao nhiêu gam CaO để làm nóng 210 mL cafe từ 25oC đến 40oC (d = 1,0 g/ml) (làm tròn đến phần hàng phần mười)?

Nhiệt tỏa ra từ phản ứng thất thoát vào sản phẩm, vỏ hộp và môi trường là 20%. Cần cung cấp bao nhiêu gam CaO để làm nóng 210 mL cafe từ 25oC đến 40oC (d = 1,0 g/ml) (làm tròn đến phần hàng phần mười)?
CaO(s) + H2O(l) ⟶ Ca(OH)2(aq)
Biến thiên enthalpy của phản ứng trên là 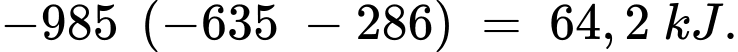
Nhiệt cà phê hấp thụ để tăng từ 25oC lên 40oC cần 4,2.210.(40 – 25) = 13230 J = 13,23 kJ
Vậy khối lượng CaO cần cung cấp là
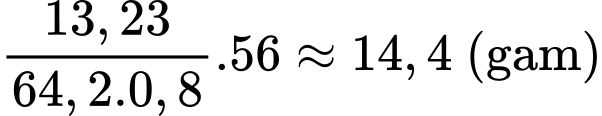
⇒ Điền đáp án: 14,4