PHẦN I. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
Câu 1 [60608]: Cho dãy chuyển hóa sau: 
Bộ ba các chất theo thứ tự X, Y, Z nào sau đây không thỏa mãn?

Bộ ba các chất theo thứ tự X, Y, Z nào sau đây không thỏa mãn?
A, Cl2, Fe, HNO3.
B, Cl2, Cu, HNO3.
C, Cl2, Fe, AgNO3.
D, HCl, Cl2, AgNO3.
Bộ ba các chất theo thứ tự X, Y, Z không thỏa mãn là HCl, Cl2, AgNO3.
Nguyên nhân khi cho Fe tác dụng với HCl (X) thì chỉ thu được FeCl2 không phải FeCl3 như yêu cầu của đề bài.
⇒ Chọn đáp án D Đáp án: D
Nguyên nhân khi cho Fe tác dụng với HCl (X) thì chỉ thu được FeCl2 không phải FeCl3 như yêu cầu của đề bài.
⇒ Chọn đáp án D Đáp án: D
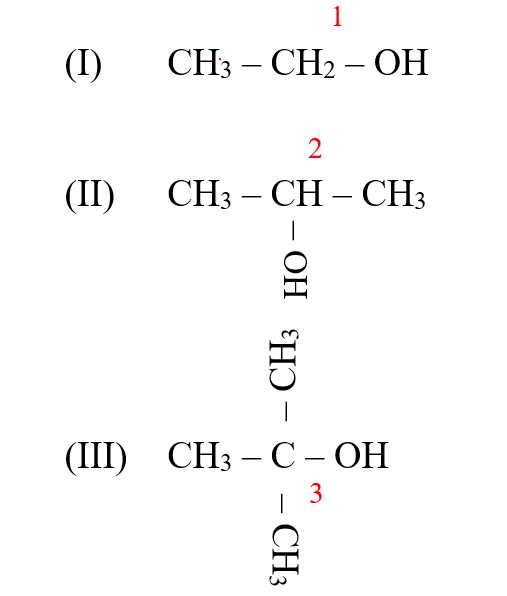
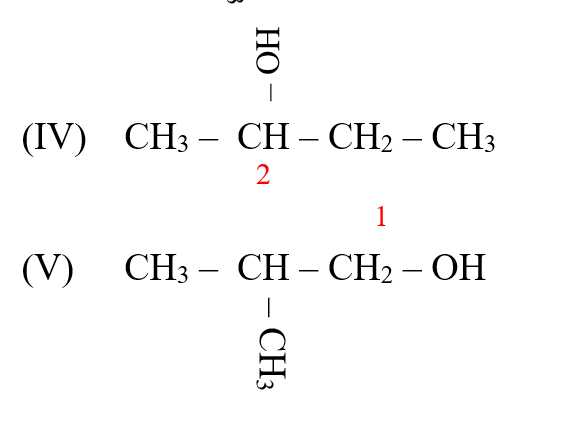
Câu 2 [14958]: Cho dãy gồm các alcohol sau: (I) CH3CH2OH; (II) CH3CH(OH)CH3; (III) (CH3)3C(OH); (IV) CH3CH(OH)CH2CH3; (V) CH3CH(CH3)CH2OH.
Số alcohol bậc hai là
Số alcohol bậc hai là
A, 5.
B, 3.
C, 4.
D, 2.
Alcohol bậc hai = OH liên kết với carbon bậc 2 => (II), (IV)
 ⟹Chọn đáp án D Đáp án: D
⟹Chọn đáp án D Đáp án: D

 ⟹Chọn đáp án D Đáp án: D
⟹Chọn đáp án D Đáp án: D
Câu 3 [679452]: Tiến hành các thí nghiệm sau:
(a) Nhúng thanh đồng nguyên chất vào dung dịch FeCl3.
(b) Cắt miếng sắt tây (sắt tráng thiếc), để trong không khí ẩm.
(c) Nhúng thanh kẽm vào dung dịch H2SO4 loãng có nhỏ vài giọt dung dịch CuSO4.
(d) Quấn sợi dây đồng vào đinh sắt rồi nhúng vào cốc nước muối.
Trong các thí nghiệm trên, số thí nghiệm chỉ xảy ra ăn mòn hóa học là
(a) Nhúng thanh đồng nguyên chất vào dung dịch FeCl3.
(b) Cắt miếng sắt tây (sắt tráng thiếc), để trong không khí ẩm.
(c) Nhúng thanh kẽm vào dung dịch H2SO4 loãng có nhỏ vài giọt dung dịch CuSO4.
(d) Quấn sợi dây đồng vào đinh sắt rồi nhúng vào cốc nước muối.
Trong các thí nghiệm trên, số thí nghiệm chỉ xảy ra ăn mòn hóa học là
A, 2.
B, 3.
C, 4.
D, 1.
HD: ► Điều kiện xảy ra ăn mòn điện hoá:
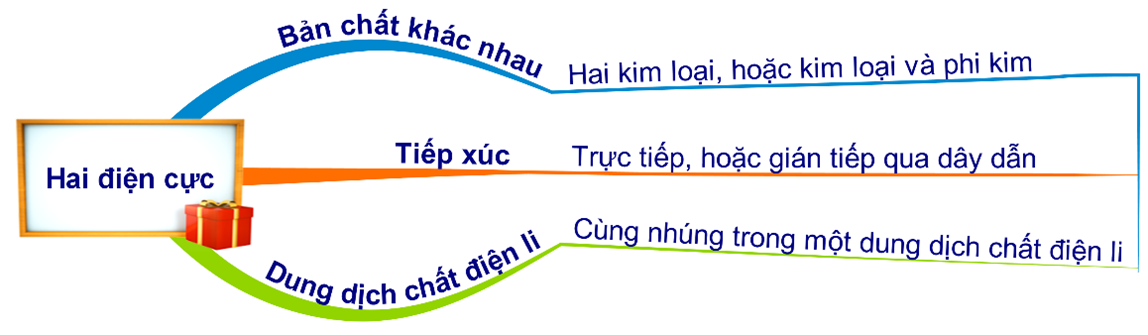
⇝ Phân tích các thí nghiệm tiến hành:
✔️ (a) Cu + FeCl3 → 2FeCl2 + CuCl2: chỉ xảy ra ăn mòn hoá học.
❌ (b) Cặp cực Fe-Sn tiếp xúc nhau, không khí ẩm là điều kiện dung dịch điện ly ⇒ xảy ra ăn mòn điện hoá học.
❌ (c) đầu tiên: Zn + CuSO4 → ZnSO4 + Cu; Cu sinh ra bám vào Zn tạo thành cặp cực trong dung dịch H2SO4 ⇒ xảy ra ăn mòn điện hoá.
❌ (d) Fe-Cu là cặp cực tiếp xúc nhau trong dung dịch điện ly là muối ⇒ xảy ra ăn mòn điện hoá.
⇝ chỉ có 1/4 thí nghiệm thoả mãn yêu cầu
⇒ Chọn đáp án D Đáp án: D

⇝ Phân tích các thí nghiệm tiến hành:
✔️ (a) Cu + FeCl3 → 2FeCl2 + CuCl2: chỉ xảy ra ăn mòn hoá học.
❌ (b) Cặp cực Fe-Sn tiếp xúc nhau, không khí ẩm là điều kiện dung dịch điện ly ⇒ xảy ra ăn mòn điện hoá học.
❌ (c) đầu tiên: Zn + CuSO4 → ZnSO4 + Cu; Cu sinh ra bám vào Zn tạo thành cặp cực trong dung dịch H2SO4 ⇒ xảy ra ăn mòn điện hoá.
❌ (d) Fe-Cu là cặp cực tiếp xúc nhau trong dung dịch điện ly là muối ⇒ xảy ra ăn mòn điện hoá.
⇝ chỉ có 1/4 thí nghiệm thoả mãn yêu cầu
⇒ Chọn đáp án D Đáp án: D
Câu 4 [186225]: Hệ cân bằng sau được thực hiện trong bình kín:
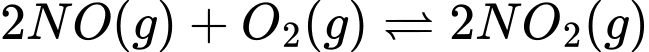 ;
; 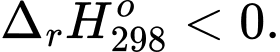
Cân bằng trên chuyển dịch theo chiều thuận khi
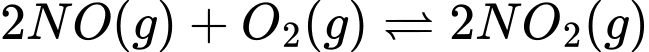 ;
; 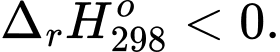
Cân bằng trên chuyển dịch theo chiều thuận khi
A, thêm khí NO2 vào hệ.
B, tăng áp suất chung của hệ.
C, cho chất xúc tác vào hệ.
D, tăng nhiệt độ của hệ.
Đáp án B.
A. thêm khí NO2 vào hệ làm tăng nồng độ NO2, CBCD theo chiều làm giảm nồng độ NO2 → chiều nghịch.
B. tăng áp suất chung của hệ cân bằng chuyển dịch theo chiều thuận.
2NO(g) + O2(g)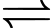 2NO2(g);
2NO2(g); 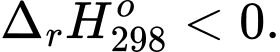
3 mol khí 2 mol khíC. cho chất xúc tác vào hệ: Chất xúc tác không làm chuyển dịch cân bằng hóa học nên cân bằng không chuyển dịch.
D. tăng nhiệt độ của hệ: phản ứng tỏa nhiệt nên tăng nhiệt độ CBCD theo chiều nghịch. Đáp án: B
A. thêm khí NO2 vào hệ làm tăng nồng độ NO2, CBCD theo chiều làm giảm nồng độ NO2 → chiều nghịch.
B. tăng áp suất chung của hệ cân bằng chuyển dịch theo chiều thuận.
2NO(g) + O2(g)
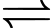 2NO2(g);
2NO2(g); 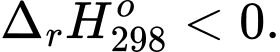
3 mol khí 2 mol khíC. cho chất xúc tác vào hệ: Chất xúc tác không làm chuyển dịch cân bằng hóa học nên cân bằng không chuyển dịch.
D. tăng nhiệt độ của hệ: phản ứng tỏa nhiệt nên tăng nhiệt độ CBCD theo chiều nghịch. Đáp án: B
Câu 5 [308552]: Đối với amine (no, đơn chức, mạch hở), n nguyên tử C và 1 nguyên tử N ngoài tạo liên kết với nhau còn cần liên kết với (2n + 3) nguyên tử H, hình thành công thức tổng quát CnH2n+3N. Tổng số electron hóa trị dùng để tạo liên kết C–C và C–N là
A, 2n + 1.
B, 2n.
C, 3n – 1.
D, 2n – 2.
Công thức tổng quát của amine no, đơn chức là CnH2n+3N
Số electron hóa trị của n nguyên tử C bằng 4, của 1 nguyên tử N bằng 3
Giữa n nguyên tử C và 1 nguyên tử N hình thành n liên kết σ bằng 2n electron hóa trị.
⇒ Tổng số electron hóa trị dùng để tạo liên kết C-C và C-N là 2n
⟹ Chọn đáp án B Đáp án: B
Số electron hóa trị của n nguyên tử C bằng 4, của 1 nguyên tử N bằng 3
Giữa n nguyên tử C và 1 nguyên tử N hình thành n liên kết σ bằng 2n electron hóa trị.
⇒ Tổng số electron hóa trị dùng để tạo liên kết C-C và C-N là 2n
⟹ Chọn đáp án B Đáp án: B
Câu 6 [308236]: Carbohydrate nào sau đây thuộc loại disaccharide?
A, Cellulose.
B, Amylose.
C, Saccharose.
D, Glucose.
HD: Bài học phân loại hợp chất carbohydrate:
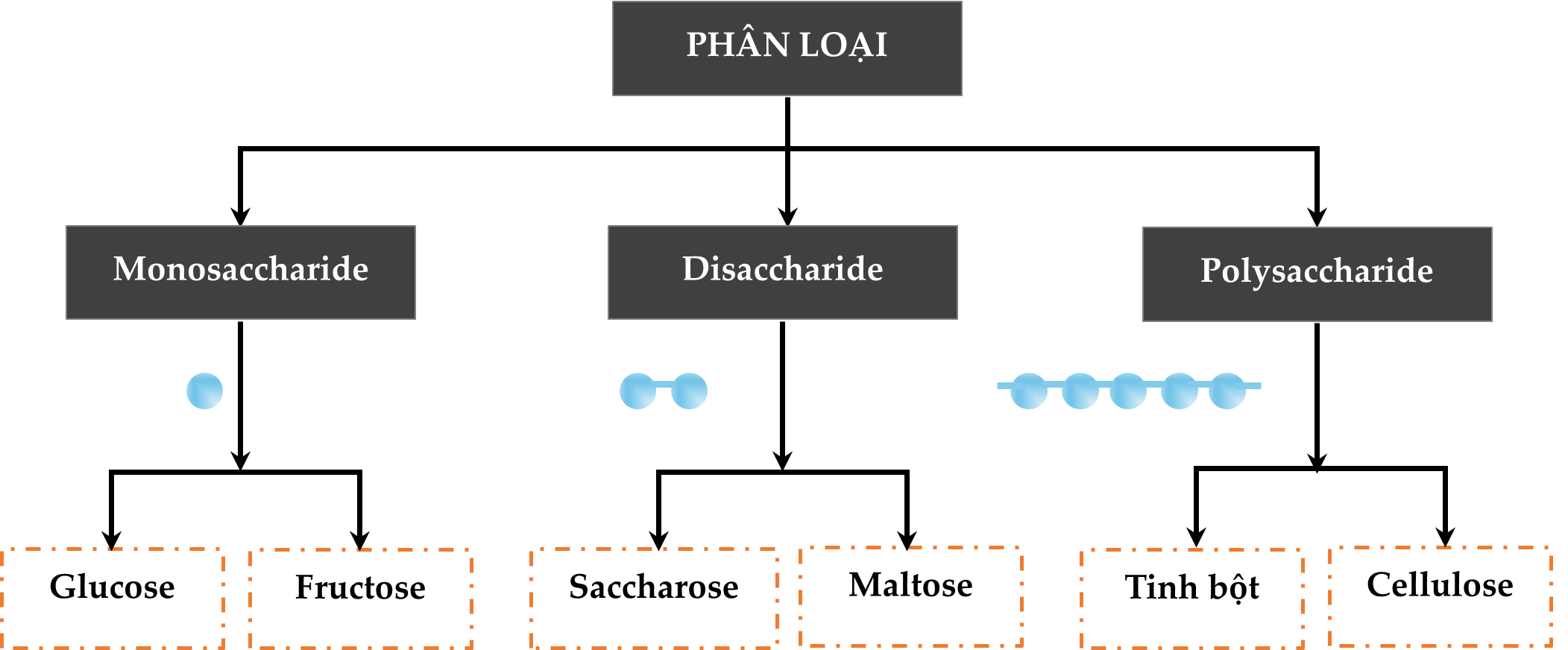
⇒ Saccharose là một loại disaccharide
⇝ Chọn đáp án C. Đáp án: C

⇒ Saccharose là một loại disaccharide
⇝ Chọn đáp án C. Đáp án: C
Câu 7 [705498]: “Chất béo là nguyên liệu cho ngành công nghiệp ...(1)..., sản xuất xà phòng và ...(2)...”. Nội dung phù hợp trong ô trống (1), (2) lần lượt là
A, dệt may, alcohol.
B, luyện kim, alcohol.
C, khai khoáng, glycerol.
D, thực phẩm, glycerol.
Chất béo là nguyên liệu cho ngành công nghiệp thực phẩm, sản xuất xà phòng và glycerol.
Các ứng dụng của chất béo:
- Cung cấp một lượng đáng kể năng lượng cho cơ thể và được xem là nguồn dinh dưỡng quan trọng.
- Được dùng để tổng hợp các chất cần thiết khác cho cơ thể, đồng thời có tác dụng đảm bảo sự vận chuyển và hấp thụ các chất tan được trong chất béo.
- Dùng để điều chế xà phòng và glycerol.
- Dùng nhiều trong chế biến thực phẩm. Ngày nay một số loại dầu thực vật còn được dùng để sản xuất nhiên liệu sinh học (biodiesel).
- Là nguồn cũng cấp acid béo omega-3 và omega-6 cho cơ thể.
⇒ Chọn đáp án D Đáp án: D
Các ứng dụng của chất béo:
- Cung cấp một lượng đáng kể năng lượng cho cơ thể và được xem là nguồn dinh dưỡng quan trọng.
- Được dùng để tổng hợp các chất cần thiết khác cho cơ thể, đồng thời có tác dụng đảm bảo sự vận chuyển và hấp thụ các chất tan được trong chất béo.
- Dùng để điều chế xà phòng và glycerol.
- Dùng nhiều trong chế biến thực phẩm. Ngày nay một số loại dầu thực vật còn được dùng để sản xuất nhiên liệu sinh học (biodiesel).
- Là nguồn cũng cấp acid béo omega-3 và omega-6 cho cơ thể.
⇒ Chọn đáp án D Đáp án: D
Câu 8 [705827]: Polymer polyvinyl acetate thuộc loại chất dẻo, trong suốt được dùng để sản xuất kính ô tô, cửa ra vào. Polyvinyl acetate được tạo ra bằng phản ứng trùng hợp chất nào sau đây?
A, CH2=CHCOOCH3.
B, CH2=C(CH3)COOCH3.
C, CH3COOCH=CH2.
D, CH3COOC(CH3)=CH2.
Phương trình phản ứng trùng hợp polyvinyl acetate như sau:
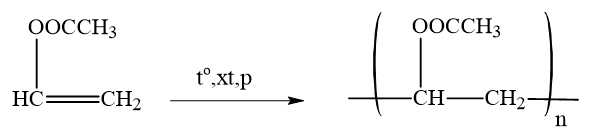
Chọn đáp án C Đáp án: C

Chọn đáp án C Đáp án: C
Câu 9 [706031]: Mặt nạ thở phòng cháy chữa cháy có chứa KO2. Trong điều kiện thiếu khí, KO2 cũng có thể phản ứng với CO2 giúp tạo ra O2 để hỗ trợ hô hấp cho người đeo:
aKO2(s) + bCO2(g) → cK2CO3(s) + dO2(g)
Với a, b, c, d là các hệ số tỉ lượng ứng với các chất. Hệ số a và b lần lượt là
aKO2(s) + bCO2(g) → cK2CO3(s) + dO2(g)
Với a, b, c, d là các hệ số tỉ lượng ứng với các chất. Hệ số a và b lần lượt là
A, 5, 2.
B, 3, 2.
C, 4, 2.
D, 1, 3.
4KO2 + 2CO2 → 2K2CO3 + 3O2
Hệ số a, b, c, d lần lượt là 4; 2; 2; 3
Hệ số a và b lần lượt là 4 và 2
⟹Chọn đáp án C Đáp án: C
Hệ số a, b, c, d lần lượt là 4; 2; 2; 3
Hệ số a và b lần lượt là 4 và 2
⟹Chọn đáp án C Đáp án: C
Câu 10 [1072884]: Copper(II) sulfate dạng nước được điện phân bằng điện cực đồng. Dòng điện không đổi và anode được cân sau các khoảng thời gian bằng nhau. Đồ thị nào dưới đây biểu diễn mối liên hệ giữa khối lượng anode với thời gian?
A, 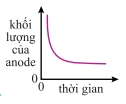

B, 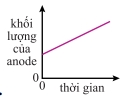

C, 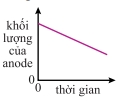

D, 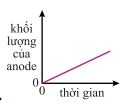

Trong điện phân dung dịch
CuSO₄ với điện cực đồng:
Anode (Cu) bị oxi hóa: Cu → Cu2+
+ 2e
→ Anode bị mòn dần, khối lượng giảm đều theo thời gian nếu
dòng điện không đổi.
Vì dòng điện không đổi → lượng chất oxi hóa theo thời gian tỉ lệ tuyến
tính (theo định luật Faraday).
Vậy đồ thị khối lượng anode theo thời gian là đường thẳng giảm đều.
Đáp án: C
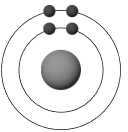
Câu 11 [702805]: Hình bên mô tả mô hình nguyên tử Bohr của nguyên tử nguyên tố X. Trong các cấu tạo Lewis sau đây, cấu tạo nào biểu diễn đúng nhất nguyên tử được thể hiện trong mô hình Bohr đó?

A, 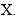
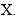
B, 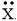
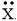
C, 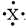
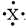
D, 
Dựa vào mô hình Borh thấy X có 2 electron hoá trị ở lớp ngoài cùng nên cấu tạo Lewis của X cũng biểu diễn 2 electron
⟿ Chọn đáp án B Đáp án: B
⟿ Chọn đáp án B Đáp án: B
Câu 12 [703946]: Khi bón phân kali, ion K+ sẽ đẩy các ion Ca2+; Mg2+ ra khỏi keo đất, do đó bón lâu ngày, nhất là khi bón lượng nhiều thì dễ làm cho đất bị
A, chua.
B, phèn.
C, cứng.
D, khô.
Đất ít chua hay không chua, khi bón phân kali vào thì ion K+ sẽ đẩy Ca2+, Mg2+ ra khỏi keo đất, do đó bón lâu ngày, nhất là khi bón lượng nhiều thì dễ làm cho đất bị chua hóa. Vậy nên phải bón vôi khử chua, bổ sung Ca2+, Mg2+ cho đất.
⇒ Chọn đáp án A Đáp án: A
⇒ Chọn đáp án A Đáp án: A
Câu 13 [704023]: Kim loại nào đây phản ứng chậm với nước ở điều kiện thường?
A, Na.
B, Ba.
C, K.
D, Mg.
- Na, Ba, K là các kim loại có tính khử mạnh nên phản ứng mạnh với nước.
2Na + 2H2O ⟶ 2NaOH + H2
2K + 2H2O ⟶ 2KOH + H2
Ba+ 2H2O ⟶ Ba(OH)2 + H2
- Ở nhiệt độ thường, Mg phản ứng rất chậm với nước vì nó có lớp màng oxide (MgO) mỏng bảo vệ bề mặt, ngăn cản nước tiếp xúc trực tiếp với kim loại.
⇒ Chọn đáp án D Đáp án: D
2Na + 2H2O ⟶ 2NaOH + H2
2K + 2H2O ⟶ 2KOH + H2
Ba+ 2H2O ⟶ Ba(OH)2 + H2
- Ở nhiệt độ thường, Mg phản ứng rất chậm với nước vì nó có lớp màng oxide (MgO) mỏng bảo vệ bề mặt, ngăn cản nước tiếp xúc trực tiếp với kim loại.
⇒ Chọn đáp án D Đáp án: D
Câu 14 [704178]: Một số hydrocarbon trong bình gas tạo với không khí hỗn hợp nổ ngay ở nồng độ rất thấp: pentane C5H12 là 1,4%; butane C4H10 là 1,6%, methane CH4 là 4,4% vì phản ứng cháy của các hydrocarbon đều tỏa rất nhiều nhiệt, tốc độ phản ứng nhanh nên thể tích không khí giãn nở đột ngột và gây ra vụ nổ hóa học. Cho các phát biểu sau:
(a) Các hydrocarbon không có mùi nhưng khí gas lại có mùi hắc là do nhà sản xuất đã pha trộn thêm chất tạo mùi đặc trưng, giúp phát hiện khí gas khi xảy ra rò rỉ.
(b) Khi thấy có “mùi gas” báo hiệu có gas rò rỉ, nhanh chóng dùng bật lửa hoặc bật công tắc đèn… để tìm vị trí gas bị rò rỉ.
(c) Không nên dùng tay trần để tìm vị trí gas rò rỉ vì có thể cháy tĩnh điện hoặc nguồn nhiệt từ cơ thể (dù nhỏ) cũng có thể gây cháy nổ trong điều kiện nồng độ khí gas cao.
(d) Khi phát hiện vị trí rò rỉ thì dùng băng keo quấn lại, di chuyển bình gas đến vị trí an toàn, nơi thông gió, tránh xa nguồn nhiệt rồi báo cơ sở gas xử lí.
Các phát biểu đúng là
(a) Các hydrocarbon không có mùi nhưng khí gas lại có mùi hắc là do nhà sản xuất đã pha trộn thêm chất tạo mùi đặc trưng, giúp phát hiện khí gas khi xảy ra rò rỉ.
(b) Khi thấy có “mùi gas” báo hiệu có gas rò rỉ, nhanh chóng dùng bật lửa hoặc bật công tắc đèn… để tìm vị trí gas bị rò rỉ.
(c) Không nên dùng tay trần để tìm vị trí gas rò rỉ vì có thể cháy tĩnh điện hoặc nguồn nhiệt từ cơ thể (dù nhỏ) cũng có thể gây cháy nổ trong điều kiện nồng độ khí gas cao.
(d) Khi phát hiện vị trí rò rỉ thì dùng băng keo quấn lại, di chuyển bình gas đến vị trí an toàn, nơi thông gió, tránh xa nguồn nhiệt rồi báo cơ sở gas xử lí.
Các phát biểu đúng là
A, (a), (b), (c).
B, (a), (b), (d).
C, (b), (c), (d).
D, (a), (c), (d).
Phân tích các phát biểu:
✔️ (a) Đúng. Đặc tính của khí gas là không màu, không mùi, không vị nhưng người dùng vẫn ngửi thấy mùi gas khi nó thoát ra bên ngoài. Lý do là trong quá trình sản xuất các chuyên gia đã pha trộn thêm mùi trứng thối, bắp cải thối lẫn vào khí gas để có thể phát hiện và xử lý kịp thời nếu có sự cố rò rỉ gas. Do khứu giác của con người nhạy cảm gấp nhiều lần với mùi khó chịu nên dễ phát hiện rỏ rỉ khí gas.
❌ (b) Sai. Khí gas dễ cháy, nếu dùng bật lửa hay bật công tắc đèn tìm nơi rò rỉ khí gas sẽ gây cháy nổ.
✔️ (c) Đúng. tĩnh điện được sinh ra khi 2 bề mặt vật liệu tiếp xúc và tách ra nhau. Cụ thể khi con người di chuyển, tĩnh điện đã được nạp lên cơ thể từ 1 kV -5 kV do ma sát giữa giày/dép (thông thường) và bề mặt sàn (thông thường). Điện áp tĩnh này sẽ tồn tại trên cơ thể con người, chúng có thể truyền đi khi con người được nối đất hoặc tiếp xúc, chạm vào đối tượng dẫn điện nên khi dùng tay trần vẫn có nguy cơ gây cháy nổ khi tiếp xúc với khí gas.
✔️ (d) Đúng. Cách làm trên ngăn khí gas tiếp xúc với nguồn nhiệt gây cháy nổ.
Các phát biểu đúng là (a) (c) (d)
⇒ Chọn đáp án D Đáp án: D
✔️ (a) Đúng. Đặc tính của khí gas là không màu, không mùi, không vị nhưng người dùng vẫn ngửi thấy mùi gas khi nó thoát ra bên ngoài. Lý do là trong quá trình sản xuất các chuyên gia đã pha trộn thêm mùi trứng thối, bắp cải thối lẫn vào khí gas để có thể phát hiện và xử lý kịp thời nếu có sự cố rò rỉ gas. Do khứu giác của con người nhạy cảm gấp nhiều lần với mùi khó chịu nên dễ phát hiện rỏ rỉ khí gas.
❌ (b) Sai. Khí gas dễ cháy, nếu dùng bật lửa hay bật công tắc đèn tìm nơi rò rỉ khí gas sẽ gây cháy nổ.
✔️ (c) Đúng. tĩnh điện được sinh ra khi 2 bề mặt vật liệu tiếp xúc và tách ra nhau. Cụ thể khi con người di chuyển, tĩnh điện đã được nạp lên cơ thể từ 1 kV -5 kV do ma sát giữa giày/dép (thông thường) và bề mặt sàn (thông thường). Điện áp tĩnh này sẽ tồn tại trên cơ thể con người, chúng có thể truyền đi khi con người được nối đất hoặc tiếp xúc, chạm vào đối tượng dẫn điện nên khi dùng tay trần vẫn có nguy cơ gây cháy nổ khi tiếp xúc với khí gas.
✔️ (d) Đúng. Cách làm trên ngăn khí gas tiếp xúc với nguồn nhiệt gây cháy nổ.
Các phát biểu đúng là (a) (c) (d)
⇒ Chọn đáp án D Đáp án: D
Câu 15 [705711]: Từ tinh dầu hoa nhài người ta tách được chất hữu cơ X. Kết quả phân tích nguyên tố cho thấy X chứa 72,0% carbon, 6,66% hydrogen còn lại là oxygen. Trên phố khối lượng của X thấy peak ion phân tử M+ = 150. Trên phổ hồng ngoại của X thấy có số sóng hấp thụ ở 1716 cm–1 (mạnh), không thấy số sóng hấp thụ đặc trưng của nhóm OH. Thủy phân X trong dung dịch NaOH thu được một trong các sản phẩm là benzyl alcohol. Công thức cấu tạo phù hợp cho X là
A, 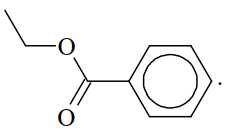

B, 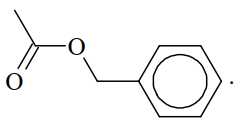

C, 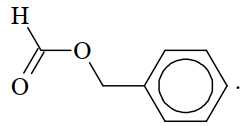

D, 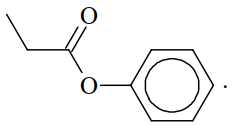

Gọi công thức của X có dạng CaHbOc
Từ phổ MS phân tử khối của X là 150 gam/mol
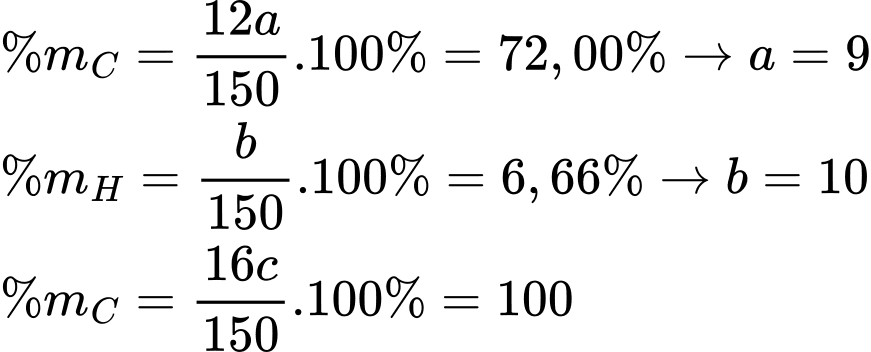
Công thức phân tử của X là C9H10O2
Mà phổ hồng ngoại của X có tín hiệu hấp thụ ở 1716 cm-1 → X có chứa nhóm C=O.
Thủy phân X bằng NaOH thu được benzyl alcohol (C6H5CH2OH) → X là ester đơn chức
Công thức cấu tạo của X là

⇒ Chọn đáp án B Đáp án: B
Từ phổ MS phân tử khối của X là 150 gam/mol
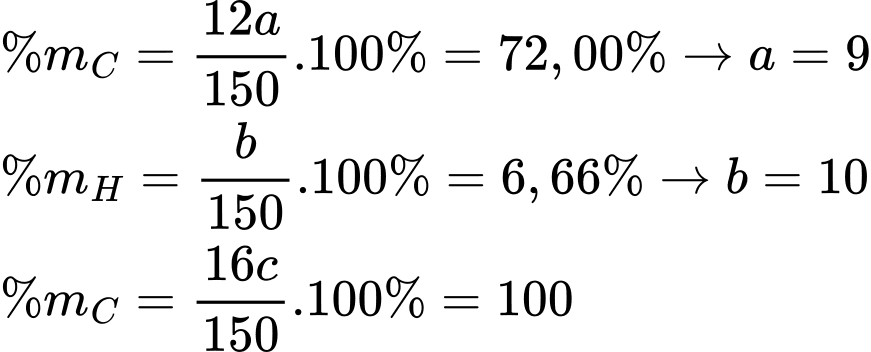
Công thức phân tử của X là C9H10O2
Mà phổ hồng ngoại của X có tín hiệu hấp thụ ở 1716 cm-1 → X có chứa nhóm C=O.
Thủy phân X bằng NaOH thu được benzyl alcohol (C6H5CH2OH) → X là ester đơn chức
Công thức cấu tạo của X là

⇒ Chọn đáp án B Đáp án: B
Câu 16 [705464]: Các enzyme đóng vai trò quan trọng đối với cơ thể sinh vật, như xúc tác cho các quá trình sinh hoá và hoá học. Ví dụ, lipase là enzyme xúc tác cho quá trình thuỷ phân các chất béo chuỗi dài; protease là enzyme xúc tác cho quá trình thuỷ phân các liên kết peptide có trong protein và polypeptide;... Các enzyme chỉ tồn tại và phát triển ở môi trường gần trung tính và nhiệt độ tương đối thấp (gần với nhiệt độ của cơ thể sinh vật). Khi đóng vai trò là chất xúc tác trong các quá trình sinh hoá, các enzyme không có đặc điểm nào sau đây?
A, Có tính chọn lọc cao.
B, Làm tăng tốc độ của các quá trình sinh hoá.
C, Có tác dụng tốt ở nhiệt độ cao hoặc môi trường acid mạnh.
D, Chỉ hoạt động trong điều kiện nhiệt độ phù hợp.
Phân tích các đặc điểm:
✔️ A. Đúng. Enzyme có tính chọn lọc cao, chỉ xúc tác cho một phản ứng cụ thể hoặc nhóm phản ứng có cấu trúc tương tự. Điều này giúp chúng thực hiện các quá trình sinh hóa chính xác và hiệu quả.
✔️ B. Đúng. Enzyme giúp tăng tốc độ phản ứng mà không bị tiêu tốn trong phản ứng đó, thông qua việc giảm năng lượng kích hoạt cần thiết cho phản ứng.
❌ C. Sai. Enzyme thường có dải nhiệt độ và pH thích hợp để hoạt động, thường là ở nhiệt độ thấp (gần nhiệt độ cơ thể sinh vật) và môi trường gần trung tính (pH khoảng 7). Ở nhiệt độ quá cao hoặc môi trường acid mạnh, enzyme có thể bị biến tính (mất cấu trúc và chức năng).
✔️ D. Đúng. Enzyme chỉ hoạt động hiệu quả trong điều kiện nhiệt độ và pH thích hợp. Nhiệt độ quá cao hoặc pH quá cao hoặc thấp có thể làm enzyme bị mất chức năng.
⇒ Chọn đáp án C Đáp án: C
✔️ A. Đúng. Enzyme có tính chọn lọc cao, chỉ xúc tác cho một phản ứng cụ thể hoặc nhóm phản ứng có cấu trúc tương tự. Điều này giúp chúng thực hiện các quá trình sinh hóa chính xác và hiệu quả.
✔️ B. Đúng. Enzyme giúp tăng tốc độ phản ứng mà không bị tiêu tốn trong phản ứng đó, thông qua việc giảm năng lượng kích hoạt cần thiết cho phản ứng.
❌ C. Sai. Enzyme thường có dải nhiệt độ và pH thích hợp để hoạt động, thường là ở nhiệt độ thấp (gần nhiệt độ cơ thể sinh vật) và môi trường gần trung tính (pH khoảng 7). Ở nhiệt độ quá cao hoặc môi trường acid mạnh, enzyme có thể bị biến tính (mất cấu trúc và chức năng).
✔️ D. Đúng. Enzyme chỉ hoạt động hiệu quả trong điều kiện nhiệt độ và pH thích hợp. Nhiệt độ quá cao hoặc pH quá cao hoặc thấp có thể làm enzyme bị mất chức năng.
⇒ Chọn đáp án C Đáp án: C
Sử dụng thông tin cho dưới đây để trả lời các câu số 17 – 18:
Một mẫu nước cứng có nồng độ các ion Na+; Ca2+; Mg2+, Cl–; SO42- và HCO3- tương ứng là 1,2 mM; 3,0 mM; 1,0 mM; 0,6 mM; 0,01 mM và x mM (1 mM = 1 mmol/L), ngoài ra không chứa ion nào khác.
Câu 17 [705576]: Cách nào sau đây không thể làm mất tính cứng của loại nước nào?
A, Sử dụng Na3PO4.
B, Đun sôi.
C, Sử dụng Ca(OH)2.
D, Sử dụng Na2CO3.
Nước cứng tạm thời (do Ca(HCO3)2 và Mg(HCO3)2): có thể khử bằng cách đun sôi.
Nước cứng vĩnh cửu ( do MgSO4, CaCl2, MgCl2): không thể khử bằng đun sôi, cần dùng hóa chất.
⟹ Chọn đáp án B Đáp án: B
Nước cứng vĩnh cửu ( do MgSO4, CaCl2, MgCl2): không thể khử bằng đun sôi, cần dùng hóa chất.
⟹ Chọn đáp án B Đáp án: B
Câu 18 [705577]: Tổng khối lượng chất tan còn lại sau khi đun sôi kỹ 2 lít mẫu nước cứng trên là bao nhiêu? Giả sử các muối MgCO3, CaCO3 hầu như không tan trong nước.
A, 134,52
B, 123,6.
C, 142,2.
D, 141,0 mg.
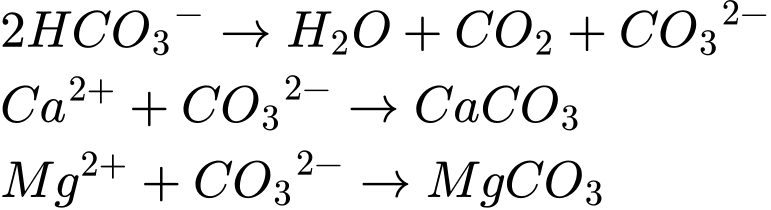
Trong 2L có: Na+ : 2,4mM; Ca2+ : 6,0mM; Mg2+ : 2,0mM; Cl- : 1,2mM; SO42-: 0,02mM; HCO3- : 2x
Bảo toàn điện tích:
1nNa+ + 2nCa2+ + 2nMg2+ = 1nCl- + 2nSO42- + 1nHCO3-
2,4 + 2. 6,0 + 2. 2,0 = 1. 1,2 + 2. 0,02 + 2x
⟹ x = 8,58mM
⟹ Dung dịch sau phản ứng còn:
Na+ : 2,4mM ; Cl- : 1,2mM ; SO42- : 0,02mM ; CO32-: 0,58mM
Khối lượng chất rắn:
m = mNa+ + mCl- + mSO42- + mCO32-
= 2,4 × 23 + 1,2 × 35,5 + 96 × 0,02 + 0,58 × 60
= 134,52
⟹ Chọn đáp án A Đáp án: A
PHẦN II. Thí sinh trả lời từ câu 1 đến câu 4. Trong mỗi ý a), b), c), d) ở mỗi câu, thí sinh chọn đúng hoặc sai.
Câu 19 [703935]: Tiến hành thí nghiệm phản ứng giữa cellulose và nitric acid như sau:
▪ Bước 1: Cho 5 mL dung dịch HNO3 vào cốc thủy tinh ngâm trong chậu nước đá. Thêm từ từ 10 mL dung dịch H2SO4 đặc vào cốc và khuấy đều. Sau đó, lấy cốc ra khỏi chậu nước đá, thêm một nhúm bông vào cốc và dùng đũa thủy tinh ấn bông ngập trong dung dịch.
▪ Bước 2: Ngâm cốc trong chậu nước nóng khoảng 10 phút. Để nguội, lấy sản phẩm thu được ra khỏi cốc, rửa nhiều lần với nước lạnh (đến khi nước rửa không làm đổi màu quỳ tím), sau đó rửa lại bằng dung dịch NaHCO3 loãng.
▪ Bước 3: Cho sản phẩm vào giữa 2 miếng giấy lọc và ép để hút nước, làm khô tự nhiên.
▪ Bước 1: Cho 5 mL dung dịch HNO3 vào cốc thủy tinh ngâm trong chậu nước đá. Thêm từ từ 10 mL dung dịch H2SO4 đặc vào cốc và khuấy đều. Sau đó, lấy cốc ra khỏi chậu nước đá, thêm một nhúm bông vào cốc và dùng đũa thủy tinh ấn bông ngập trong dung dịch.
▪ Bước 2: Ngâm cốc trong chậu nước nóng khoảng 10 phút. Để nguội, lấy sản phẩm thu được ra khỏi cốc, rửa nhiều lần với nước lạnh (đến khi nước rửa không làm đổi màu quỳ tím), sau đó rửa lại bằng dung dịch NaHCO3 loãng.
▪ Bước 3: Cho sản phẩm vào giữa 2 miếng giấy lọc và ép để hút nước, làm khô tự nhiên.
[C6H7O2(OH)3]n + 3nHNO3 ⟶ [C6H7O2(ONO2)3]n + 3nH2O
Phân tích các phát biểu:
✔️ a) Đúng. Có thể sử dụng NaHCO3 loãng để trung hoà acid dư, giúp thu được sản phẩm sạch: HCO3- + H+ ⟶ H2O + CO2
✔️ b) Đúng. H2SO4 đặc đóng vai trò là chất xúc tác.
❌ c) Sai. Không thể thay việc làm khô tự nhiên bằng việc sấy do thuốc súng không khói dễ cháy, nên khi sấy ở nhiệt độ cao có thể gây cháy.
✔️ d) Đúng. Cellulose sẽ bị thủy phân 1 phần trong môi trường acid nên sẽ thu được glucose, phản ứng được với thuốc thử Tollens.
Phân tích các phát biểu:
✔️ a) Đúng. Có thể sử dụng NaHCO3 loãng để trung hoà acid dư, giúp thu được sản phẩm sạch: HCO3- + H+ ⟶ H2O + CO2
✔️ b) Đúng. H2SO4 đặc đóng vai trò là chất xúc tác.
❌ c) Sai. Không thể thay việc làm khô tự nhiên bằng việc sấy do thuốc súng không khói dễ cháy, nên khi sấy ở nhiệt độ cao có thể gây cháy.
✔️ d) Đúng. Cellulose sẽ bị thủy phân 1 phần trong môi trường acid nên sẽ thu được glucose, phản ứng được với thuốc thử Tollens.
Câu 20 [703832]: Các phức chất chứa cùng một thành phần nguyên tử và cùng một trình tự liên kết, nhưng chỉ khác nhau về sự sắp xếp trong không gian được gọi là “đồng phân lập thể”. Đồng phân hình học, hoặc đồng phân cis – trans, cũng thuộc loại đồng phân lập thể. Đồng phân hình học xảy ra khi các nguyên tử hoặc nhóm nguyên tử có thể được sắp xếp ở hai bên của một cấu trúc. Cis có nghĩa là "cùng phía" và trans có nghĩa là “khác phía”.
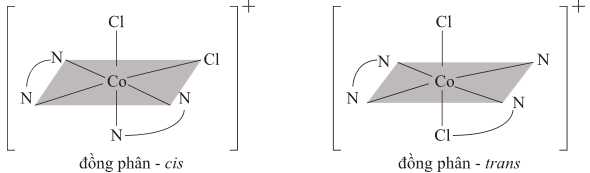
Ion dichlorobis(ethylenediamine)cobalt(III), [Co(en)2Cl2]+, tồn tại dưới dạng một cặp đồng phân cis - trans. Ethylenediamine viết tắt là “en”, được biểu diễn dưới dạng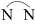 .
.
▪ Cis-dichlorobis(ethylenediamine)cobalt(III) perchlorate, [Co(en)2Cl2]ClO4 có màu tím.
▪ Trans-dichlorobis(ethylenediamine)cobalt(III) chloride, [Co(en)2Cl2]Cl có màu xanh lá cây.

Ion dichlorobis(ethylenediamine)cobalt(III), [Co(en)2Cl2]+, tồn tại dưới dạng một cặp đồng phân cis - trans. Ethylenediamine viết tắt là “en”, được biểu diễn dưới dạng
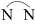 .
. ▪ Cis-dichlorobis(ethylenediamine)cobalt(III) perchlorate, [Co(en)2Cl2]ClO4 có màu tím.
▪ Trans-dichlorobis(ethylenediamine)cobalt(III) chloride, [Co(en)2Cl2]Cl có màu xanh lá cây.
Phân tích các phát biểu:
✔️ a) Đúng. Cả 2 phức chất đều có 2 phối tử en và 2 phối tử Cl–.
❌ b) Sai. Số oxi hóa của cobalt đều bằng +3 trong 2 phức, được xác định như sau:
★ [Co(en)2Cl2]ClO4 có ion phức: [Co(en)2Cl2]+ và anion ngoài phức: ClO4 − do phức chất trung hòa về điện.
- Gọi số oxi hóa của Co là x.
- Ethylenediamine (en) là phối tử trung hòa, không đóng góp vào điện tích (2 × 0 = 0).
- Hai ion chloride (Cl−) mỗi ion mang điện tích -1 (2 × (−1) = −2.
Ta có biểu thức tính điện tích của ion phức như sau:
x + 0 + (−2) = +1 ⤑ x = +3.
★ [Co(en)2Cl2]Cl có ion phức: [Co(en)2Cl2]+ và anion ngoài phức: Cl− do phức chất trung hòa về điện.
- Gọi số oxi hóa của Co là y.
- Ethylenediamine (en): 2 × 0 = 0.
- Hai ion chloride (Cl−): 2 × ( − 1 ) = −2.
Ta có biểu thức tính điện tích của ion phức như sau:
x + 0 + (−2) = +1 ⤑ x = +3.
❌ c) Sai. ở đồng phân dạng cis 4 nguyên tử N không nằm trên 1 mặt phẳng.
✔️ d) Đúng.
- Trong đồng phân cis-, hai ion Cl− nằm cùng phía, tức chúng chiếm hai vị trí liền kề trong cấu trúc bát diện. Điều này làm cho góc giữa hai ion Cl− là 90o.
- Trong đồng phân trans-, hai ion Cl− nằm đối diện nhau, tức chúng chiếm hai vị trí đối xứng qua ion cobalt trung tâm. Điều này làm cho góc giữa hai ion Cl− là 180o.
✔️ a) Đúng. Cả 2 phức chất đều có 2 phối tử en và 2 phối tử Cl–.
❌ b) Sai. Số oxi hóa của cobalt đều bằng +3 trong 2 phức, được xác định như sau:
★ [Co(en)2Cl2]ClO4 có ion phức: [Co(en)2Cl2]+ và anion ngoài phức: ClO4 − do phức chất trung hòa về điện.
- Gọi số oxi hóa của Co là x.
- Ethylenediamine (en) là phối tử trung hòa, không đóng góp vào điện tích (2 × 0 = 0).
- Hai ion chloride (Cl−) mỗi ion mang điện tích -1 (2 × (−1) = −2.
Ta có biểu thức tính điện tích của ion phức như sau:
x + 0 + (−2) = +1 ⤑ x = +3.
★ [Co(en)2Cl2]Cl có ion phức: [Co(en)2Cl2]+ và anion ngoài phức: Cl− do phức chất trung hòa về điện.
- Gọi số oxi hóa của Co là y.
- Ethylenediamine (en): 2 × 0 = 0.
- Hai ion chloride (Cl−): 2 × ( − 1 ) = −2.
Ta có biểu thức tính điện tích của ion phức như sau:
x + 0 + (−2) = +1 ⤑ x = +3.
❌ c) Sai. ở đồng phân dạng cis 4 nguyên tử N không nằm trên 1 mặt phẳng.
✔️ d) Đúng.
- Trong đồng phân cis-, hai ion Cl− nằm cùng phía, tức chúng chiếm hai vị trí liền kề trong cấu trúc bát diện. Điều này làm cho góc giữa hai ion Cl− là 90o.
- Trong đồng phân trans-, hai ion Cl− nằm đối diện nhau, tức chúng chiếm hai vị trí đối xứng qua ion cobalt trung tâm. Điều này làm cho góc giữa hai ion Cl− là 180o.
Câu 21 [702820]: Nước Javel có tính tẩy màu và sát trùng do đó nó thường được dùng để tẩy trắng vải, sợi, giấy và tẩy uế chuồng trại vệ sinh. Nước Javel được điều chế bằng cách điện phân dung dịch NaCl không có màng ngăn theo các bước sau:
Bước 1: Lấy 500 mL nước cất vào cốc thuỷ tinh. Sau đó cho khoảng 150 g muối ăn và khuấy đều. Nếu tan hết, tiếp tục cho thêm muối ăn từng chút một đến nào thấy không thể hòa tan thêm được nữa thì thu được dung dịch NaCl bão hòa.
Bước 2: Cắm hai điện cực vào cốc thuỷ tinh. Nối dây dẫn vào nguồn điện một chiều (hình bên) và duy trì quá trình điện phân trong khoảng 5 phút.
Bước 3: Cho một mẩu cánh hoa màu hồng vào cốc chứa khoảng 5 mL dung dịch sau điện phân.
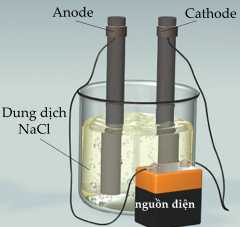
Bước 1: Lấy 500 mL nước cất vào cốc thuỷ tinh. Sau đó cho khoảng 150 g muối ăn và khuấy đều. Nếu tan hết, tiếp tục cho thêm muối ăn từng chút một đến nào thấy không thể hòa tan thêm được nữa thì thu được dung dịch NaCl bão hòa.
Bước 2: Cắm hai điện cực vào cốc thuỷ tinh. Nối dây dẫn vào nguồn điện một chiều (hình bên) và duy trì quá trình điện phân trong khoảng 5 phút.
Bước 3: Cho một mẩu cánh hoa màu hồng vào cốc chứa khoảng 5 mL dung dịch sau điện phân.

Phân tích các phát biểu:
❌ a) Sai. Ion Na+ không bị điện phân trong dung dịch do Na sinh ra là kim loại mạnh sẽ lập tức phản ứng với nước.
✔️ b) Đúng. Có 2 khí thoát ra ở cả 2 điện cực là H2 và Cl2
Cathode (-): H2O(l) + 2e → OH-(aq) + H2(g)
Anode (+) Cl-(aq) → Cl2(g) + 2e
✔️c) Đúng. Hỗn hợp sau phản ứng chứa NaCl, NaClO:
2NaCl + 2H2O -(đpdd)→ 2NaOH + Cl2 ↑ + H2 ↑
2NaOH + Cl2 → NaClO + NaCl + H2O
✔️ d) Đúng. Ion ClO- có tính oxi hóa mạnh, gốc acid này có khả năng phá vỡ cấu trúc sắc tố màu sắc nên khi cho cánh hoa hồng vào sau một thời gian sẽ mất màu.
❌ a) Sai. Ion Na+ không bị điện phân trong dung dịch do Na sinh ra là kim loại mạnh sẽ lập tức phản ứng với nước.
✔️ b) Đúng. Có 2 khí thoát ra ở cả 2 điện cực là H2 và Cl2
Cathode (-): H2O(l) + 2e → OH-(aq) + H2(g)
Anode (+) Cl-(aq) → Cl2(g) + 2e
✔️c) Đúng. Hỗn hợp sau phản ứng chứa NaCl, NaClO:
2NaCl + 2H2O -(đpdd)→ 2NaOH + Cl2 ↑ + H2 ↑
2NaOH + Cl2 → NaClO + NaCl + H2O
✔️ d) Đúng. Ion ClO- có tính oxi hóa mạnh, gốc acid này có khả năng phá vỡ cấu trúc sắc tố màu sắc nên khi cho cánh hoa hồng vào sau một thời gian sẽ mất màu.
Câu 22 [702622]: Một học sinh đưa ra giả thuyết rằng có thể oxi hóa pentan-2-ol để tạo thành pentan-2-one như sau:
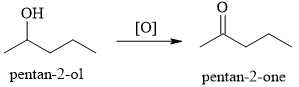
Tiến hành thực hiện phản ứng oxi hóa, để kiểm tra phản ứng oxi hóa có xảy ra hay không thì học sinh tách riêng từng chất trong hỗn hợp sản phẩm và tiến hành đo phổ hồng ngoại. Phổ hồng ngoại của một chất X được cho như sau:
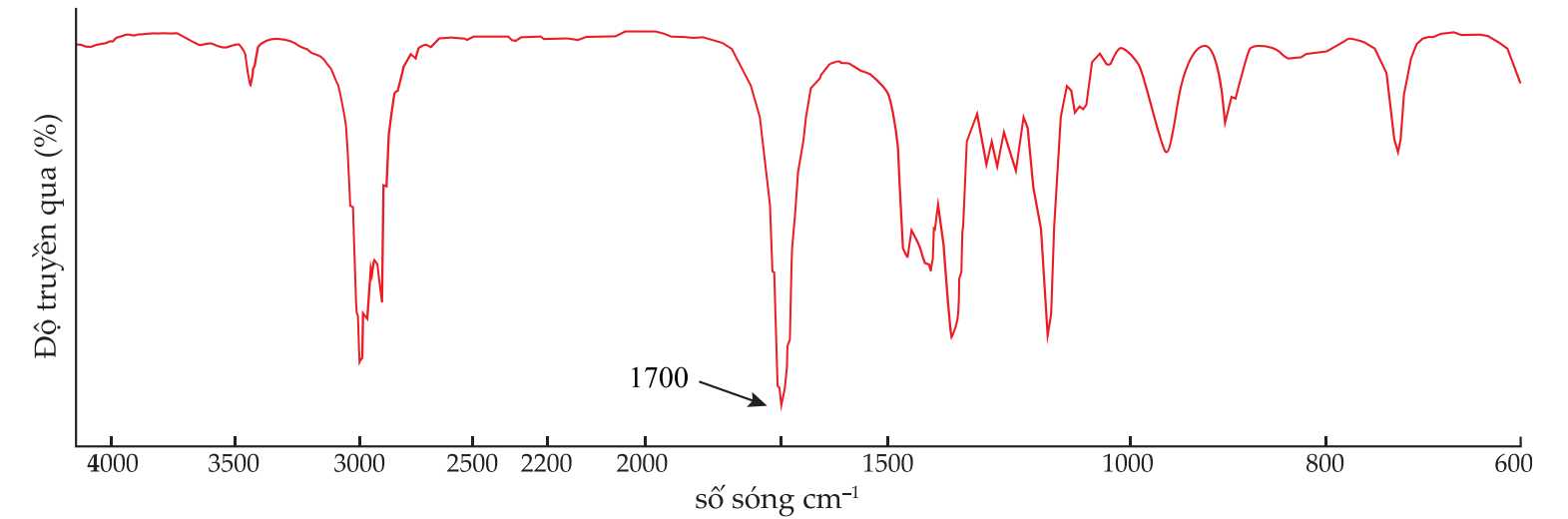

Tiến hành thực hiện phản ứng oxi hóa, để kiểm tra phản ứng oxi hóa có xảy ra hay không thì học sinh tách riêng từng chất trong hỗn hợp sản phẩm và tiến hành đo phổ hồng ngoại. Phổ hồng ngoại của một chất X được cho như sau:

Phân tích các phát biểu:
❌ a) Sai. Tín hiệu đặc trưng cho liên kết O-H (alcohol) là 3600 – 3200 cm-1; O-H trong carboxylic acid là 3300-2500 cm-1. Còn tín hiệu 1700 cm-1 là của liên kết C=O.
❌ b) Sai. Phổ hồng ngoại dùng để xác định các nhóm chức có thể có trong phân tử hợp chất hữu cơ.
✔️ c) Đúng. Tín hiệu đặc trưng cho liên kết O-H (alcohol) trong pentan-2-ol xuất hiện ở số sóng 3600 – 3200 cm-1.
✔️ d) Đúng. Dựa vào phổ hồng ngoại có thể thấy sự xuất hiện của tín hiệu nhóm C=O của sản phẩm chứng tỏ phản ứng oxi hoá đã xảy ra.
❌ a) Sai. Tín hiệu đặc trưng cho liên kết O-H (alcohol) là 3600 – 3200 cm-1; O-H trong carboxylic acid là 3300-2500 cm-1. Còn tín hiệu 1700 cm-1 là của liên kết C=O.
❌ b) Sai. Phổ hồng ngoại dùng để xác định các nhóm chức có thể có trong phân tử hợp chất hữu cơ.
✔️ c) Đúng. Tín hiệu đặc trưng cho liên kết O-H (alcohol) trong pentan-2-ol xuất hiện ở số sóng 3600 – 3200 cm-1.
✔️ d) Đúng. Dựa vào phổ hồng ngoại có thể thấy sự xuất hiện của tín hiệu nhóm C=O của sản phẩm chứng tỏ phản ứng oxi hoá đã xảy ra.
PHẦN III. Thí sinh trả lời từ câu 1 đến 6. Thí sinh điền kết quả mỗi câu vào mỗi ô trả lời tương ứng theo hướng dẫn của phiếu trả lời.
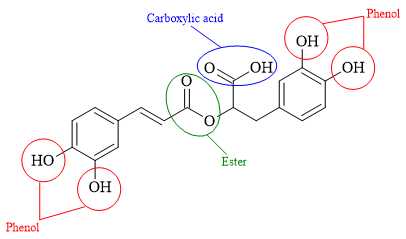
Câu 23 [684510]: Rosmarinic acid thường có trong các loại thảo mộc như hương thảo, xô thơm, cỏ xạ hương....có công thức cấu tạo như sau:
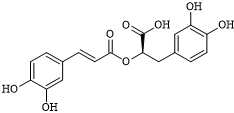
Khi đun nóng 1 mol rosmarinic acid phản ứng được bao nhiêu mol NaOH?

Khi đun nóng 1 mol rosmarinic acid phản ứng được bao nhiêu mol NaOH?
Rosmarinic acid là một hợp chất tạp chức có chứa các nhóm chức phenol, ester, carboxylic acid.
Khi cho Rosmarinic acid tác dụng với NaOH các nhóm chức phenol và carboxylic acid sẽ phản ứng.
Trong đó, phân tử Rosmarinic acid chứa 4 nhóm chức -OH (phenol) gắn trực tiếp vào vòng benzene, 1 nhóm chức (-COO-) ester và 1 nhóm chức -COOH (carboxylic acid) nên khi đun nóng 1 mol Rosmarinic acid phản ứng với 6 mol NaOH.
⇒ Điền đáp án: 6
Khi cho Rosmarinic acid tác dụng với NaOH các nhóm chức phenol và carboxylic acid sẽ phản ứng.
Trong đó, phân tử Rosmarinic acid chứa 4 nhóm chức -OH (phenol) gắn trực tiếp vào vòng benzene, 1 nhóm chức (-COO-) ester và 1 nhóm chức -COOH (carboxylic acid) nên khi đun nóng 1 mol Rosmarinic acid phản ứng với 6 mol NaOH.

⇒ Điền đáp án: 6
Câu 24 [704405]: Hydrogen cũng là một trong những loại nhiên liệu có nhiều hữu ích trong ngành hàng không. Hydrogen có thể được điều chế từ ethanol. Ethanol có thể thu được bằng cách lên men ngô. Sơ đồ dưới đây biểu diễn quá trình chuyển hóa:
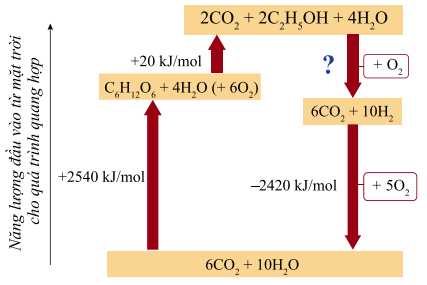
Biến thiên enthalpy khi chuyển đổi ethanol thành hydrogen trong biểu đồ trên là bao nhiêu kJ?

Biến thiên enthalpy khi chuyển đổi ethanol thành hydrogen trong biểu đồ trên là bao nhiêu kJ?
Từ sơ đồ biểu diễn quá trình chuyển hóa, ta thấy tổng năng lượng để điều chế hydrogen từ ethanol với tổng năng lượng khi lên men ngô để thu được ethanol bằng 0. Ta có:
2540 + 20 + ΔHo + (-2420)
⟶ ΔHo = 2540 + 20 + (-2420) = -140 (kJ)
⇒ Điền đáp án: -140
2540 + 20 + ΔHo + (-2420)
⟶ ΔHo = 2540 + 20 + (-2420) = -140 (kJ)
⇒ Điền đáp án: -140
Câu 25 [705719]: Phức chất [Co(NH3)5Clx]y– có dạng hình học bát diện, nguyên tử trung tâm là Co3+. Tổng giá trị của x và y là bao nhiêu?
Phức chất [Co(NH3)5Clx]y– có dạng hình học bát diện nên có dạng tổng quát là [ML6]
→ 5 + x = 6 → x = 1
Phức chất [Co(NH3)5Clx]y– có ion trung tâm Co3+ với NH3 là phối tử trung hòa và 1 ion Cl– là phối tử
→ y = 2
Tổng giá trị của x + y = 1 + 2 = 3
⇒ Điền đáp án: 3
→ 5 + x = 6 → x = 1
Phức chất [Co(NH3)5Clx]y– có ion trung tâm Co3+ với NH3 là phối tử trung hòa và 1 ion Cl– là phối tử
→ y = 2
Tổng giá trị của x + y = 1 + 2 = 3
⇒ Điền đáp án: 3
Câu 26 [705722]: Khái niệm chlorine hoạt động được hiểu ngoài Cl2 phân tử còn bao gồm chlorine oxide, chloramine, hypochlorite, chlorite. Người ta tiến hành phân tích mẫu đất gần nhà máy.
∎ Bước 1: 20 gam đất khô lắc đều 5 phút trong nước cất với tốc độc 160 vòng/phút tạo thành 100 mL dung dịch. Để yên 30 phút rồi lọc, thêm 1 gam tinh thể KNO3 vào dung dịch để chống đục (giả sử thể tích dung dịch không thay đổi).
∎ Bước 2: Lấy 25 ml dung dịch + 1 ml dung dịch K2CrO4 10% rồi tiến hành chuẩn độ bằng AgNO3 0,01 M. Lúc đầu thấy xuất hiện kết tủa trắng. Sau đó chuẩn độ đến xuất hiện kết tủa đỏ gạch thì dừng chuẩn độ, thấy hết 4,6 mL dung dịch AgNO3. Hàm lượng phần trăm của ion Cl– trong mẫu đất là a×10–2 %. Xác định giá trị của a (Làm tròn đến hàng phần trăm).
∎ Bước 1: 20 gam đất khô lắc đều 5 phút trong nước cất với tốc độc 160 vòng/phút tạo thành 100 mL dung dịch. Để yên 30 phút rồi lọc, thêm 1 gam tinh thể KNO3 vào dung dịch để chống đục (giả sử thể tích dung dịch không thay đổi).
∎ Bước 2: Lấy 25 ml dung dịch + 1 ml dung dịch K2CrO4 10% rồi tiến hành chuẩn độ bằng AgNO3 0,01 M. Lúc đầu thấy xuất hiện kết tủa trắng. Sau đó chuẩn độ đến xuất hiện kết tủa đỏ gạch thì dừng chuẩn độ, thấy hết 4,6 mL dung dịch AgNO3. Hàm lượng phần trăm của ion Cl– trong mẫu đất là a×10–2 %. Xác định giá trị của a (Làm tròn đến hàng phần trăm).
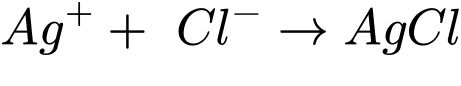
Đổi 4,6 mL = 0,0046 L
Số mol của AgNO3 là nAgNO3 = 0,0046.0,01 = 4,6.10-5 mol
Số mol của Cl- trong mẫu đất là
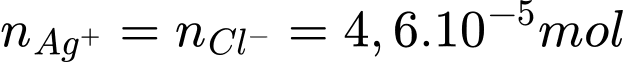
Hàm lượng của ion Cl- trong mẫu đất là:
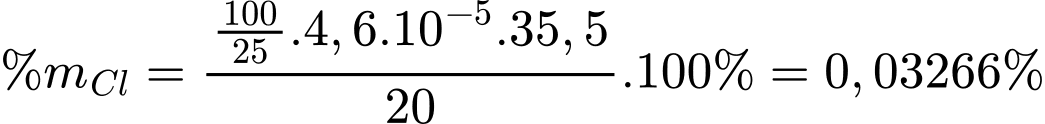
Ta có:
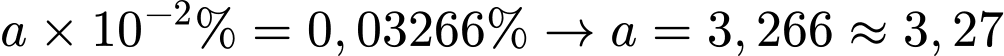
⇒ Điền đáp án: 3,27
Câu 27 [706026]: Cục quản lí thực phẩm và dược phẩm Hoa Kì (FDA) đã công nhận khí ethylene an toàn trong việc kích thích trái cây mau chín. Trong phòng ủ chín, ethylene được sử dụng ở nồng độ 100 – 150 ppm (1ppm = 1/106). Tuy nhiên, nếu sử dụng vượt quá nồng độ cho phép, một tia lửa điện có thể đốt cháy ethylene và gây ra cháy nổ. Tính khối lượng khí ethylene (gam) cần thiết cho vào phòng ủ chín có diện tích 50 m2 và chiều cao 3 m để đạt nồng độ 120 ppm ở 25°C, 1 atm (làm tròn đến hàng phần mười).
Thể tích phòng ủ là V = 50.3 = 150 m3 = 150000 L
Thể tích ethylene có trong phòng ủ là VC2H4 = 150000.120.10-6 = 18 L
Khối lượng ethylene có trong phòng ủ là
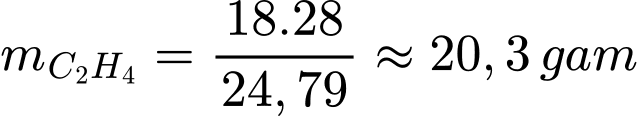
⟹Điền đáp án : 20,3
Thể tích ethylene có trong phòng ủ là VC2H4 = 150000.120.10-6 = 18 L
Khối lượng ethylene có trong phòng ủ là
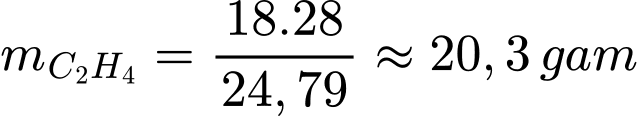
⟹Điền đáp án : 20,3
Câu 28 [706180]: Calcium là nguyên tố cần thiết đối với cơ thể con người, là thành phần chủ yếu cấu tạo nên xương và răng, không thể thiếu trong quá trình đông máu. Theo khuyến cáo của Viện Dinh dưỡng Quốc gia Việt Nam, mỗi ngày người lớn cũng như trẻ em cần khoảng 500 mg calcium dưới dạng ion Ca2+. Hãy số mol calcium được đưa vào cơ thể khi một người uống 300 g sữa bò, biết nồng độ ion calcium trong sữa bò là 2%.
Khối lượng của Ca2+ trong 300 gam sữa bò là:
mCa2+ = 300 × 2% = 6 gam
Số mol của Ca2+ là nCa2+ = 6 ÷ 40 = 0,15 mol
⟹ Điền đáp án: 0,15
mCa2+ = 300 × 2% = 6 gam
Số mol của Ca2+ là nCa2+ = 6 ÷ 40 = 0,15 mol
⟹ Điền đáp án: 0,15