PHẦN I. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
Câu 1 [308680]: Công thức của glycine là
A, CH3NH2.
B, H2NCH(CH3)COOH.
C, H2NCH2COOH.
D, C2H5NH2.
Glycine là amino acid đơn giản nhất, thuộc nhóm amino acid không phân cực, có một nhóm amine (−NH2) gắn vào nguyên tử carbon số 2 và một nhóm carboxyl (−COOH).
Công thức của glycine là H2NCH2COOH.
⇒ Chọn đáp án C Đáp án: C
Công thức của glycine là H2NCH2COOH.
⇒ Chọn đáp án C Đáp án: C
Câu 2 [304801]: Có thể tạo ra mùi thơm của quả mơ từ ester có tên pentyl butanoate. Công thức cấu tạo của hợp chất này được cho dưới đây:
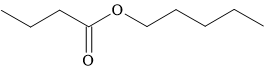
Alcohol nào đã cấu tạo nên pentyl butanoate?

Alcohol nào đã cấu tạo nên pentyl butanoate?
A, C5H11OH.
B, C4H9OH.
C, C3H7OH.
D, C2H5OH.
HD: Phân tích cấu tạo ester:
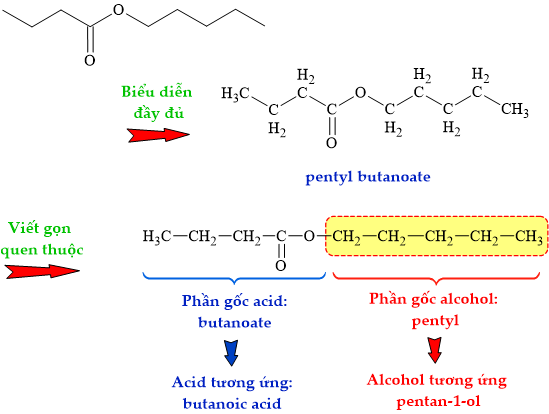
⇒ Alcohol cấu tạo nên ester pentyl butanoate là pentan-1-ol: CH3CH2CH2CH2CH2OH ⇄ công thức rút gọn: C5H11OH
⇒ Chọn đáp án A Đáp án: A

⇒ Alcohol cấu tạo nên ester pentyl butanoate là pentan-1-ol: CH3CH2CH2CH2CH2OH ⇄ công thức rút gọn: C5H11OH
⇒ Chọn đáp án A Đáp án: A
Câu 3 [560549]: Giải thích tại sao để điều chế Al người ta điện phân Al2O3 nóng chảy mà không điện phân AlCl3 nóng chảy là
A, AlCl3 nóng chảy ở nhiệt độ cao hơn Al2O3.
B, AlCl3 là hợp chất cộng hoá trị nên không nóng chảy mà thăng hoa.
C, Điện phân AlCl3 tạo ra Cl2 rất độc.
D, Điện phân Al2O3 cho ra Al tinh khiết hơn.
Không dùng AlCl3 vì ở nhiệt độ cao AlCl3 nhị hợp thành Al2Cl6 nên không thể tồn tại ở dạng nóng chảy.
⭒ Al2O3 bền nhiệt hơn rất nhiều nên có thể tồn tại ở dạng nóng chảy
❌A sai: Nhiệt độ nóng chảy của AlCl3 thấp hơn Al2O3.
❌C sai: Điện phân AlCl3 nóng chảy vẫn tạo ra Cl2, nhưng đây không phải là lý do chính khiến người ta không sử dụng nó để điều chế Al.
❌D sai: Điện phân Al2O3 nóng chảy tạo ra Al có độ tinh khiết cao, nhưng đây không phải là yếu tố quyết định duy nhất. Tính chất thăng hoa của AlCl3 mới là lý do chính.
⟹ Chọn đáp án B Đáp án: B
⭒ Al2O3 bền nhiệt hơn rất nhiều nên có thể tồn tại ở dạng nóng chảy
❌A sai: Nhiệt độ nóng chảy của AlCl3 thấp hơn Al2O3.
❌C sai: Điện phân AlCl3 nóng chảy vẫn tạo ra Cl2, nhưng đây không phải là lý do chính khiến người ta không sử dụng nó để điều chế Al.
❌D sai: Điện phân Al2O3 nóng chảy tạo ra Al có độ tinh khiết cao, nhưng đây không phải là yếu tố quyết định duy nhất. Tính chất thăng hoa của AlCl3 mới là lý do chính.
⟹ Chọn đáp án B Đáp án: B
Câu 4 [906802]: Phát biểu nào sau đây đúng?
A, Kim loại Al không tác dụng với dung dịch H2SO4 đặc, nóng.
B, Kim loại K có độ cứng lớn hơn kim loại Cr.
C, Ở nhiệt độ thường, CO khử được Al2O3.
D, Cho Fe vào dung dịch Cu(NO3)2 có xảy ra ăn mòn điện hóa học.
Phân tích các đáp án :
❌A. sai vì Al bị thụ động hóa trong H2SO4 đặc nguội chứ không phải đặc nóng.
❌B. sai. Cr là kim loại cứng nhất, các kim loại kiềm mềm.
❌C. sai. CO, H2 không có khả năng khử các oxit kim loại kiềm, kiềm thổ và nhôm.
✔️D. đúng. Đầu tiên: Fe + Cu(NO3)2 → Fe(NO3)2 + Cu. Kim loại đồng sinh ra bám vào thanh sắt sẽ tạo thành cặp điện cực Fe-Cu → tiếp đó xảy ra ăn mòn điện hóa học.
⟹Chọn đáp án D Đáp án: D
❌A. sai vì Al bị thụ động hóa trong H2SO4 đặc nguội chứ không phải đặc nóng.
❌B. sai. Cr là kim loại cứng nhất, các kim loại kiềm mềm.
❌C. sai. CO, H2 không có khả năng khử các oxit kim loại kiềm, kiềm thổ và nhôm.
✔️D. đúng. Đầu tiên: Fe + Cu(NO3)2 → Fe(NO3)2 + Cu. Kim loại đồng sinh ra bám vào thanh sắt sẽ tạo thành cặp điện cực Fe-Cu → tiếp đó xảy ra ăn mòn điện hóa học.
⟹Chọn đáp án D Đáp án: D
Câu 5 [247341]: Cho các nguyên tố 4Be, 11Na, 12Mg, 19K. Tính bazơ của các hydroxide được xếp theo thứ tự:
A, Be(OH)2 > Mg(OH)2 > KOH > NaOH.
B, KOH < NaOH < Mg(OH)2 < Be(OH)2.
C, Be(OH)2 < Mg(OH)2 < NaOH < KOH.
D, Mg(OH)2 < Be(OH)2 < NaOH < KOH.
Cấu hình electron của các nguyên tố Be, Na, Mg, K:
Be (Z = 4): 1s22s2 → Chu kì 2, nhóm IIA
Na (Z = 11): 1s22s22p63s1→ Chu kì 3, nhóm IA
Mg (Z = 12): 1s22s22p63s2→ Chu kì 3, nhóm IIA
K (Z = 19): 1s22s22p63s23p64s1→ Chu kì 4, nhóm IA
Thứ tự tăng dần tính kim loại là Be < Mg < Na < K.
Tính base tăng dần của các hydroxide được hình thành từ các kim loại trên là
Be(OH)2 < Mg(OH)2 < NaOH < KOH.
⟹Chọn đáp án C
Đáp án: C
Be (Z = 4): 1s22s2 → Chu kì 2, nhóm IIA
Na (Z = 11): 1s22s22p63s1→ Chu kì 3, nhóm IA
Mg (Z = 12): 1s22s22p63s2→ Chu kì 3, nhóm IIA
K (Z = 19): 1s22s22p63s23p64s1→ Chu kì 4, nhóm IA
Thứ tự tăng dần tính kim loại là Be < Mg < Na < K.
Tính base tăng dần của các hydroxide được hình thành từ các kim loại trên là
Be(OH)2 < Mg(OH)2 < NaOH < KOH.
⟹Chọn đáp án C
Đáp án: C
Câu 6 [305721]: Thủy phân tristearin ((C17H35COO)3C3H5) trong dung dịch KOH, thu được muối có công thức là
A, CH3COOK.
B, C17H33COOK.
C, C2H5COOK.
D, C17H35COOK.
Phản ứng tổng quát:
(RCOO)3C3H5 + 3KOH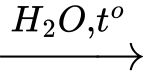 3RCOOK + C3H5(OH)3.
3RCOOK + C3H5(OH)3.
Ở câu hỏi này: (RCOO)3C3H5 = (C17H35COO)3C3H5
⇒ R = C17H35COO ⇒ Ngoài glycerol: C3H5(OH)3 thì muối tương ứng thu được có dạng RCOONa = C17H35COOK
⇒ Chọn đáp án D Đáp án: D
(RCOO)3C3H5 + 3KOH
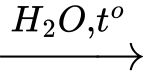 3RCOOK + C3H5(OH)3.
3RCOOK + C3H5(OH)3.Ở câu hỏi này: (RCOO)3C3H5 = (C17H35COO)3C3H5
⇒ R = C17H35COO ⇒ Ngoài glycerol: C3H5(OH)3 thì muối tương ứng thu được có dạng RCOONa = C17H35COOK
⇒ Chọn đáp án D Đáp án: D
Câu 7 [705496]: Số nhóm hydroxy trong phân tử glucose ở dạng mạch hở là
A, 4.
B, 3.
C, 5.
D, 6.
- Dạng mạch hở:
+ Glucose: CH2OH-[CHOH]4-CHO có 5 nhóm hydroxy (OH) và 1 nhóm aldehyde (CHO).
⇒ Chọn đáp án C Đáp án: C
+ Glucose: CH2OH-[CHOH]4-CHO có 5 nhóm hydroxy (OH) và 1 nhóm aldehyde (CHO).
⇒ Chọn đáp án C Đáp án: C
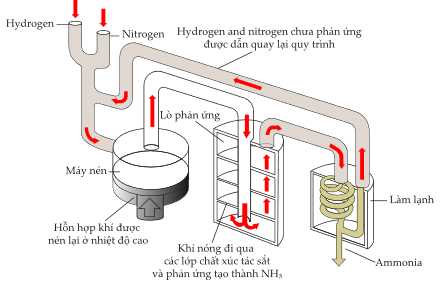
Câu 8 [704004]: Quy trình Haber được phát triển vào năm 1915 và bao gồm việc bổ sung nitrogen và hydrogen để tạo thành ammonia. Ammonia được tạo ra sau đó được sử dụng làm nguyên liệu để sản xuất phân bón:
(*) N2(g) + 3H2(g)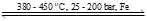 2NH3(g);
2NH3(g); 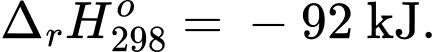
Cho các phát biểu sau:
(a) Chiều thuận của phản ứng (*) là quá trình tỏa nhiệt.
(b) Khi tăng áp suất, cân bằng của phản ứng (*) chuyển dịch theo chiều nghịch.
(c) Chất xúc tác (Fe) giúp phản ứng nhanh đạt trạng thái cân bằng.
(d) NH3 có nhiệt độ sôi cao hơn N2 và H2.
(e) N2 và H2 dư có thể được đưa trở lại hỗn hợp ban đầu để tái sử dụng.
Số phát biểu đúng là

(*) N2(g) + 3H2(g)
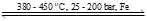 2NH3(g);
2NH3(g); 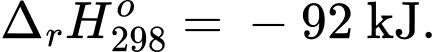
Cho các phát biểu sau:
(a) Chiều thuận của phản ứng (*) là quá trình tỏa nhiệt.
(b) Khi tăng áp suất, cân bằng của phản ứng (*) chuyển dịch theo chiều nghịch.
(c) Chất xúc tác (Fe) giúp phản ứng nhanh đạt trạng thái cân bằng.
(d) NH3 có nhiệt độ sôi cao hơn N2 và H2.
(e) N2 và H2 dư có thể được đưa trở lại hỗn hợp ban đầu để tái sử dụng.
Số phát biểu đúng là
A, 1.
B, 2.
C, 3.
D, 4.
Phân tích các phát biểu:
✔️ (a) Đúng. Giá trị biến thiên enthalpy của phản ứng là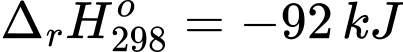 nên chiều thuận của phản ứng là tỏa nhiệt.
nên chiều thuận của phản ứng là tỏa nhiệt.
❌ (b) Sai. Theo nguyên lí chuyển dịch cân bằng, khi tăng áp suất cân bằng của phản ứng chuyển dịch theo chiều giảm áp suất là chiều thuận.
✔️ (c) Đúng. Fe là chất xúc tác có vai trò đẩy nhanh tốc độ phản ứng, giúp phản ứng nhanh đạt trạng thái cân bằng.
✔️ (d) Đúng. Nhiệt độ sôi của NH3, H2 và N2 lần lượt là -33,34 oC, -252,9 oC và -195,8 oC.
✔️ (e) Đúng. Trong chu trình tại nơi làm lạnh để ngưng tụ NH3 thì phần khí N2 và H2 chưa phản ứng sẽ dẫn quay lại đầu chu trình để điều chế NH3.
Có 4 phát biểu đúng là (a) (c) (d) (e)
⇒ Chọn đáp án D Đáp án: D
✔️ (a) Đúng. Giá trị biến thiên enthalpy của phản ứng là
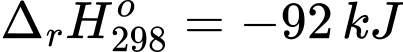 nên chiều thuận của phản ứng là tỏa nhiệt.
nên chiều thuận của phản ứng là tỏa nhiệt.❌ (b) Sai. Theo nguyên lí chuyển dịch cân bằng, khi tăng áp suất cân bằng của phản ứng chuyển dịch theo chiều giảm áp suất là chiều thuận.
✔️ (c) Đúng. Fe là chất xúc tác có vai trò đẩy nhanh tốc độ phản ứng, giúp phản ứng nhanh đạt trạng thái cân bằng.
✔️ (d) Đúng. Nhiệt độ sôi của NH3, H2 và N2 lần lượt là -33,34 oC, -252,9 oC và -195,8 oC.
✔️ (e) Đúng. Trong chu trình tại nơi làm lạnh để ngưng tụ NH3 thì phần khí N2 và H2 chưa phản ứng sẽ dẫn quay lại đầu chu trình để điều chế NH3.
Có 4 phát biểu đúng là (a) (c) (d) (e)
⇒ Chọn đáp án D Đáp án: D
Câu 9 [706046]: Hình dưới đây cho thấy phổ khối của một hợp chất ketone X có 5C.
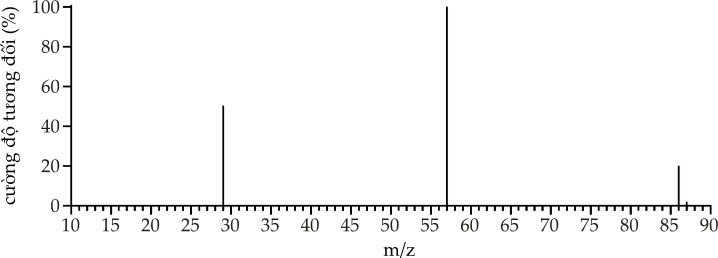
Biết rằng X có cấu tạo mạch nhánh. X có thể là

Biết rằng X có cấu tạo mạch nhánh. X có thể là
A, 3-methylbut-2-one.
B, 1-methylpent-2-one.
C, pent-3-one.
D, 2-methylbut-3-one.
Từ phổ khối lượng phân tử khối của hchc cần tìm là 86 amu
Biết phân tử X có cấu tạo mạch phân nhánh
Công thức cấu tạo phù hợp của X là
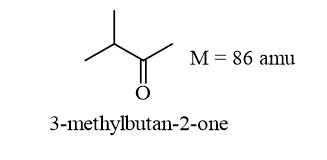
⟹ Chọn đáp án A Đáp án: A
Biết phân tử X có cấu tạo mạch phân nhánh
Công thức cấu tạo phù hợp của X là

⟹ Chọn đáp án A Đáp án: A
Câu 10 [704181]: Amino acid là những thành phần xây dựng lên protein. Hãy xem xét glycine (NH2CH2COOH). Tùy thuộc vào độ pH của dung dịch, glycine có thể tồn tại ở một trong ba dạng có thể:
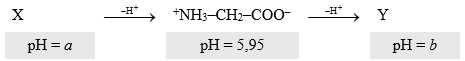
Cho các phát biểu sau:
(a) Ở pH = 5,95, glycine tồn tại ở dạng ion lưỡng cực.
(b) Giá trị pH a lớn hơn giá trị pH b.
(c) Ở pH = a, dạng tồn tại của glycine có tổng điện tích là +2.
(d) Ở pH = b, dạng tồn tại của glycine sẽ di chuyển về phía cực dương trong quá trình điện di.
Số phát biểu đúng là
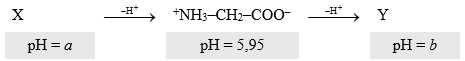
Cho các phát biểu sau:
(a) Ở pH = 5,95, glycine tồn tại ở dạng ion lưỡng cực.
(b) Giá trị pH a lớn hơn giá trị pH b.
(c) Ở pH = a, dạng tồn tại của glycine có tổng điện tích là +2.
(d) Ở pH = b, dạng tồn tại của glycine sẽ di chuyển về phía cực dương trong quá trình điện di.
Số phát biểu đúng là
A, 1.
B, 2.
C, 3.
D, 4.
Phân tích các phát biểu:
(a) Đúng. Từ dạng tồn tại trên, pH = 5,95, glycine tồn tại dạng ion lưỡng cực.
(b) Sai. Tại pH = a glycine tồn tại dạng cation, Tại pH = b glycine tồn tại dạng anion nên pH = a < pH = b.
(c) Sai. pH = a dạng tồn tại của glycine là +NH3CH2COOH có điện tích +1.
(d) Đúng. pH = b dạng tồn tai của glycine là dạng anion H2NCH2CHOO- nên sẽ di chuyển về phía cực dương trong quá trình điện di.
Các phát biểu đúng là (a) (d)
⇒ Chọn đáp án B Đáp án: B
(a) Đúng. Từ dạng tồn tại trên, pH = 5,95, glycine tồn tại dạng ion lưỡng cực.
(b) Sai. Tại pH = a glycine tồn tại dạng cation, Tại pH = b glycine tồn tại dạng anion nên pH = a < pH = b.
(c) Sai. pH = a dạng tồn tại của glycine là +NH3CH2COOH có điện tích +1.
(d) Đúng. pH = b dạng tồn tai của glycine là dạng anion H2NCH2CHOO- nên sẽ di chuyển về phía cực dương trong quá trình điện di.
Các phát biểu đúng là (a) (d)
⇒ Chọn đáp án B Đáp án: B
Câu 11 [705497]: Sự phụ thuộc của tốc độ thủy phân tinh bột (r) vào nhiệt độ (T) của phản ứng được xúc tác bởi một loại enzyme amylase (có cấu tạo từ protein) được mô tả như hình bên. Phát biểu nào sau đây là đúng?
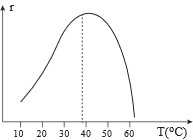

A, Ở nhiệt độ cao (khoảng 60 °C - 70°C), tốc độ phản ứng giảm do phản ứng tỏa nhiệt nên cân bằng bị chuyển dịch.
B, Trong khoảng nhiệt độ nghiên cứu, tốc độ phản ứng tăng khi nhiệt độ tăng do phản ứng được xúc tác bởi enzyme.
C, Ở nhiệt độ cao (khoảng 60 °C - 70°C), tốc độ phản ứng giảm do cấu trúc của protein trong enzyme bị biến đổi làm giảm khả năng xúc tác.
D, Tốc độ phản ứng thủy phân không phụ thuộc vào nhiệt độ do nhiệt độ không ảnh hưởng tới cấu trúc enzyme cấu tạo từ protein chứa các liên kết peptide bền vững.
❌ A. Sai. Ở nhiệt độ cao (khoảng 60 oC - 70 oC), tốc độ phản ứng giảm do emzyme bị giảm khả năng hoạt động.
❌ B. Sai. Từ đồ thị trong khoảng nhiệt độ nghiên cứu, tốc độ phản ứng chỉ tăng khi nhiệt độ tăng đến 50 oC khi tăng nhiệt độ cao hơn tốc độ phản ứng giảm.
✔️ C. Đúng. Ở nhiệt độ cao (khoảng 60 oC - 70 oC), tốc độ phản ứng giảm do cấu trúc của protein trong enzyme bị biến đổi làm giảm khả năng xúc tác.
❌ D. Sai. Tốc độ phản ứng thủy phân phụ thuộc vào nhiệt độ do tại nhiệt độ cao sẽ ảnh hưởng đến tới cấu trúc enzyme cấu tạo từ protein, các enzyme sẽ bị biến tính.
⇒ Chọn đáp án C Đáp án: C
❌ B. Sai. Từ đồ thị trong khoảng nhiệt độ nghiên cứu, tốc độ phản ứng chỉ tăng khi nhiệt độ tăng đến 50 oC khi tăng nhiệt độ cao hơn tốc độ phản ứng giảm.
✔️ C. Đúng. Ở nhiệt độ cao (khoảng 60 oC - 70 oC), tốc độ phản ứng giảm do cấu trúc của protein trong enzyme bị biến đổi làm giảm khả năng xúc tác.
❌ D. Sai. Tốc độ phản ứng thủy phân phụ thuộc vào nhiệt độ do tại nhiệt độ cao sẽ ảnh hưởng đến tới cấu trúc enzyme cấu tạo từ protein, các enzyme sẽ bị biến tính.
⇒ Chọn đáp án C Đáp án: C
Câu 12 [705571]: Khi một chất lỏng dễ cháy (ví dụ: xăng) bốc cháy, chất thực sự bốc cháy là phần hơi được tạo ra từ phần chất lỏng. Nếu nồng độ hơi trong không khí phía trên chất lỏng vượt quá một mức nhất định, hơi sẽ bốc cháy nếu tiếp xúc với tia lửa hoặc nguồn đánh lửa khác. Sau khi bốc cháy, nhiệt giải phóng có khả năng gây ra sự bốc hơi thêm của chất lỏng và đám cháy kết quả có thể tiếp tục cho đến khi tất cả các vật liệu dễ cháy đã được tiêu thụ. Cách nào sau đây không thể được sử dụng để đảm bảo an toàn khu vực cất trữ xăng?
A, Không để tia lửa hoặc nguồn đánh lửa ở gần khu vực cất trữ xăng.
B, Cất trữ trong không gian kín, cô lập với không khí bên ngoài.
C, Làm mát bằng nước ở các khu vực xung quanh cất trữ xăng.
D, Cất trữ xăng với các chất hữu cơ khác để hạn chế sự bay hơi của xăng.
✔️A. Không để tia lửa hoặc nguồn đánh lửa gần khu vực cất trữ xăng là một biện pháp an toàn quan trọng. Hơi xăng dễ cháy khi tiếp xúc với nguồn lửa, nên cần tránh xa để ngăn ngừa nguy cơ cháy nổ.
✔️B. Cất trữ trong không gian kín, cô lập với không khí bên ngoài giúp giảm thiểu sự bay hơi của xăng, tránh tạo môi trường dễ cháy trong khu vực cất trữ
✔️C. Làm mát bằng nước ở các khu vực xung quanh giúp giảm nhiệt độ, ngăn hơi xăng đạt đến giới hạn nồng độ cháy và hạn chế nguy cơ bốc cháy.
❌D. Cất trữ xăng với các chất hữu cơ khác là không an toàn vì có thể tạo phản ứng hóa học nguy hiểm hoặc làm tăng nguy cơ cháy nổ. Xăng nên được cất trữ riêng biệt trong thùng chứa chuyên dụng.
Chọn đáp án D Đáp án: D
✔️B. Cất trữ trong không gian kín, cô lập với không khí bên ngoài giúp giảm thiểu sự bay hơi của xăng, tránh tạo môi trường dễ cháy trong khu vực cất trữ
✔️C. Làm mát bằng nước ở các khu vực xung quanh giúp giảm nhiệt độ, ngăn hơi xăng đạt đến giới hạn nồng độ cháy và hạn chế nguy cơ bốc cháy.
❌D. Cất trữ xăng với các chất hữu cơ khác là không an toàn vì có thể tạo phản ứng hóa học nguy hiểm hoặc làm tăng nguy cơ cháy nổ. Xăng nên được cất trữ riêng biệt trong thùng chứa chuyên dụng.
Chọn đáp án D Đáp án: D
Câu 13 [702607]: Một polymer có cấu tạo một đoạn ngắn như sau:
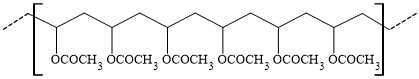
Monomer nào sau đây tạo nên polymer trên?

Monomer nào sau đây tạo nên polymer trên?
A, 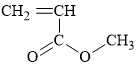

B, 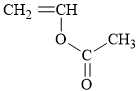

C, 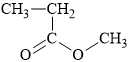

D, 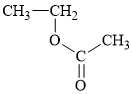

Dựa vào cấu tạo của polymer để dự đoán được monomer tạo nên là CH2=CH‒O‒C(=O)‒CH3.
⇒ Chọn đáp án B Đáp án: B
⇒ Chọn đáp án B Đáp án: B
Câu 14 [561080]: Chlorophyll là phức chất tạo màu xanh cho lá cây, có cấu tạo như hình bên.
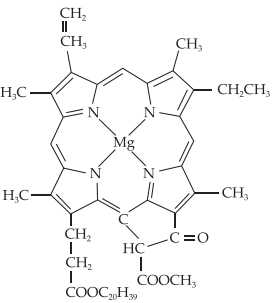
Số liên kết quanh nguyên tử trung tâm và số phối tử trong chlorophyll lần lượt là

Số liên kết quanh nguyên tử trung tâm và số phối tử trong chlorophyll lần lượt là
A, 6 và 6.
B, 4 và 1.
C, 4 và 4.
D, 6 và 4.
Mg là nguyên tử trung tâm trong chlorophyll được phối trí bởi bốn nguyên tử (N) trong vòng tạo thành 4 liên kết nằm trong 1 vòng.
Phối tử là porphyrin => Có 1 phối tử
⟹ Chọn đáp án B Đáp án: B
Phối tử là porphyrin => Có 1 phối tử
⟹ Chọn đáp án B Đáp án: B
Câu 15 [706103]: Một học sinh thực hiện các thí nghiệm để nhận biết hai dung dịch chất X và chất Y, thu được một số kết quả như sau:
Dung dịch chất X và chất Y đều làm dung dịch phenolphthalein chuyển sang màu hồng.
- Trộn X và Y thu được kết tủa màu trắng.
- Chất X cháy với ngọn lửa màu lục trên đèn khí, trong khi chất Y cháy với ngọn lửa màu tím.
Biết mỗi chất X, Y đều chỉ chứa một loại cation và một loại anion. Cho các phát biểu sau:
(a) Chất X có chứa cation Ba2+, chất Y chứa cation K+.
(b) Chất X không thể là barium chloride.
(c) Chất Y phải là potassium carbonate.
(d) Kết tủa màu trắng phải là hợp chất của barium.
Số phát biểu đúng là
Dung dịch chất X và chất Y đều làm dung dịch phenolphthalein chuyển sang màu hồng.
- Trộn X và Y thu được kết tủa màu trắng.
- Chất X cháy với ngọn lửa màu lục trên đèn khí, trong khi chất Y cháy với ngọn lửa màu tím.
Biết mỗi chất X, Y đều chỉ chứa một loại cation và một loại anion. Cho các phát biểu sau:
(a) Chất X có chứa cation Ba2+, chất Y chứa cation K+.
(b) Chất X không thể là barium chloride.
(c) Chất Y phải là potassium carbonate.
(d) Kết tủa màu trắng phải là hợp chất của barium.
Số phát biểu đúng là
A, 1.
B, 2.
C, 3.
D, 4.
Dung dịch chất X và chất Y đều làm dung dịch phenolphthalein chuyển sang màu hồng.
→ Dung dịch X và Y có tính kiềm.
Chất X cháy với ngọn lửa màu lục trên đèn khí, trong khi chất Y cháy với ngọn lửa màu tím.
X là hợp chất chứa ion Ba2+, Y là hợp chất chứa ion K+.
Phân tích các phát biểu:
✔️(a) – Đúng. Chất X cháy với ngọn lửa màu lục trên đèn khí, trong khi chất Y cháy với ngọn lửa màu tím. X là hợp chất chứa ion Ba2+, Y là hợp chất chứa ion K+.
✔️(b) – Đúng. X chuyển phenolphtalein sang màu hồng, BaCl2 không làm đổi màu dung dịch phenolphtalein do là muối trung tính ( gốc acid mạnh Cl- và gốc base mạnh Ba2+)
❌(c) – Sai. Y có thể là KHCO3, K2SO3, K3PO4…
✔️(d) – Đúng. Đúng vì các hợp chất của K (Y) tan trong nước.
Có 3 phát biểu đúng.
⟹Chọn đáp án C Đáp án: C
→ Dung dịch X và Y có tính kiềm.
Chất X cháy với ngọn lửa màu lục trên đèn khí, trong khi chất Y cháy với ngọn lửa màu tím.
X là hợp chất chứa ion Ba2+, Y là hợp chất chứa ion K+.
Phân tích các phát biểu:
✔️(a) – Đúng. Chất X cháy với ngọn lửa màu lục trên đèn khí, trong khi chất Y cháy với ngọn lửa màu tím. X là hợp chất chứa ion Ba2+, Y là hợp chất chứa ion K+.
✔️(b) – Đúng. X chuyển phenolphtalein sang màu hồng, BaCl2 không làm đổi màu dung dịch phenolphtalein do là muối trung tính ( gốc acid mạnh Cl- và gốc base mạnh Ba2+)
❌(c) – Sai. Y có thể là KHCO3, K2SO3, K3PO4…
✔️(d) – Đúng. Đúng vì các hợp chất của K (Y) tan trong nước.
Có 3 phát biểu đúng.
⟹Chọn đáp án C Đáp án: C
Câu 16 [247410]: Hai nguyên tử A, B thuộc hai nhóm liên tiếp nhau trong bảng tuần hoàn 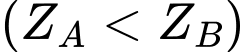 có tổng số hạt electron trong hai nguyên tử là 29 hạt. Điện tích hạt nhân của nguyên tử A, B lần lượt là
có tổng số hạt electron trong hai nguyên tử là 29 hạt. Điện tích hạt nhân của nguyên tử A, B lần lượt là
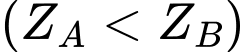 có tổng số hạt electron trong hai nguyên tử là 29 hạt. Điện tích hạt nhân của nguyên tử A, B lần lượt là
có tổng số hạt electron trong hai nguyên tử là 29 hạt. Điện tích hạt nhân của nguyên tử A, B lần lượt là A, +14, +15.
B, +13, +16.
C, +15, +14.
D, +16, +13.
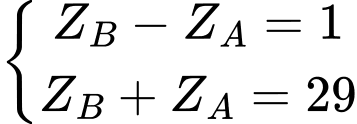
⇒
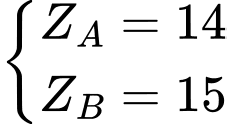
⟹ Chọn đáp án A Đáp án: A
Sử dụng thông tin cho dưới đây để trả lời các câu số 17 – 18:
Cho thế điện cực chuẩn của các cặp oxi hóa – khử như sau:
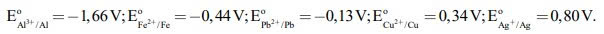
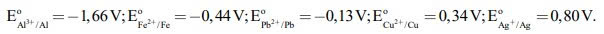
Câu 17 [704182]: Trong số các kim loại: Fe, Pb, Ag và Al, kim loại nào hoạt động mạnh hơn kim loại Cu?
A, Fe, Pb.
B, Al, Ag.
C, Fe, Pb, Al.
D, Fe.
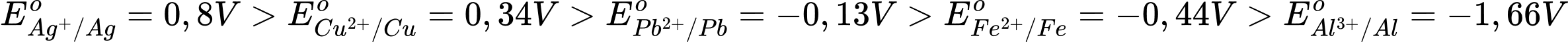
Kim loại có độ hoạt động mạnh hơn Cu là những kim loại có thế điện cực chuẩn nhỏ hơn Cu
→ Pb, Fe, Al hoạt động mạnh hơn Cu.
⇒ Chọn đáp án C Đáp án: C
Câu 18 [704183]: Sức điện động chuẩn nhỏ nhất của pin Galvani được thiết lập từ hai cặp oxi hóa khử trong số các cặp trên có giá trị là
A, 0,46 V.
B, 0,21 V.
C, 0,31 V.
D, 0,47 V.
Sức điện động nhỏ nhất của pin galvani thiết lặp từ cặp Fe2+/Fe và Pb2+/Pb
Với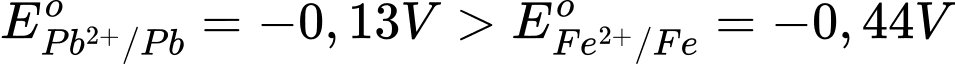 → Fe đóng vai trò là anode (-) và Pb đóng vai trò là cathode (+)
→ Fe đóng vai trò là anode (-) và Pb đóng vai trò là cathode (+)
Fe + Pb+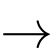 Fe2+ + Pb
Fe2+ + Pb
Phản ứng trong pin:
Cathode (+) Pb2+ + 2e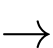 Pb
Pb
Anode (-) Fe Fe2+ + 2e
Fe2+ + 2e
Sức điện của pin là: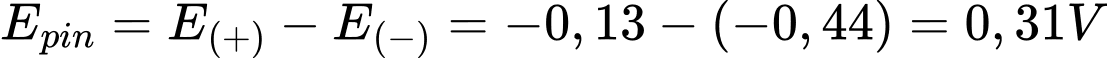
⇒ Chọn đáp án C Đáp án: C
Với
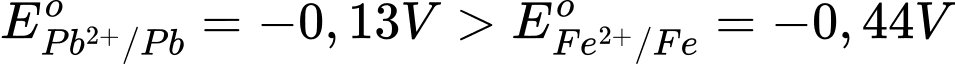 → Fe đóng vai trò là anode (-) và Pb đóng vai trò là cathode (+)
→ Fe đóng vai trò là anode (-) và Pb đóng vai trò là cathode (+)Fe + Pb+
 Fe2+ + Pb
Fe2+ + PbPhản ứng trong pin:
Cathode (+) Pb2+ + 2e
 Pb
Pb Anode (-) Fe
 Fe2+ + 2e
Fe2+ + 2eSức điện của pin là:
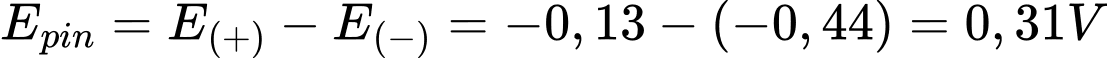
⇒ Chọn đáp án C Đáp án: C
PHẦN II. Thí sinh trả lời từ câu 1 đến câu 4. Trong mỗi ý a), b), c), d) ở mỗi câu, thí sinh chọn đúng hoặc sai.
Câu 19 [703975]: Một học sinh tiến hành tống hợp isoamyl acetate (thành phần chính của dầu chuối) từ acetic acid và isoamyl alcohol theo phương trình hóa học sau:
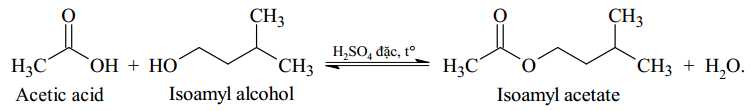
Sau thí nghiệm, tiến hành phân tách sản phẩm. Ghi phổ hồng ngoại của acetic acid, isoamyl alcohol và isoamyl acetate. Cho biết số sóng hấp thụ đặc trưng của một số liên kết trên phổ hồng như sau:
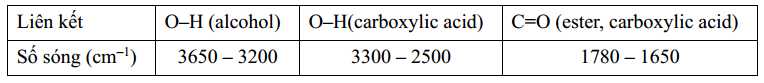
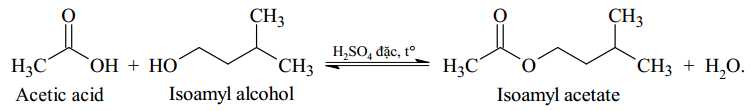
Sau thí nghiệm, tiến hành phân tách sản phẩm. Ghi phổ hồng ngoại của acetic acid, isoamyl alcohol và isoamyl acetate. Cho biết số sóng hấp thụ đặc trưng của một số liên kết trên phổ hồng như sau:
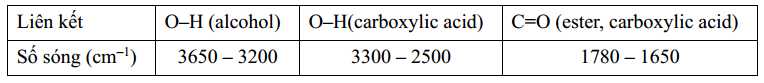
Phân tích các phát biểu:
❌ a) Sai. Phản ứng trong thí nghiệm là phản ứng ester hóa.
✔️ b) Đúng. Tín hiệu của nhóm O-H (alcohol) có số sóng hấp thụ đặc trung 3650-3200 cm-1.
✔️ c) Đúng. Isoamyl acetate, có tín hiệu đặc trưng cho liên kết C=O (ester, carboxylic acid) với số sóng 1780 - 1650 cm-1.
✔️ d) Đúng.
Isoamyl acetate, có tín hiệu đặc trưng cho liên kết C=O (ester, carboxylic acid) với số sóng 1780 - 1650 cm-1.
Isoamyl alcohol, có tín hiệu đặc trưng cho liên kết O-H (alcohol) với số sóng 3650 - 3200 cm-1.
Acetic acid, có tín hiệu đặc trưng cho liên kết C=O (ester, carboxylic acid) với số sóng 1780-1650 cm-1 và O-H (carboxylic acid) với số sóng 3300 - 2500 cm-1.
❌ a) Sai. Phản ứng trong thí nghiệm là phản ứng ester hóa.
✔️ b) Đúng. Tín hiệu của nhóm O-H (alcohol) có số sóng hấp thụ đặc trung 3650-3200 cm-1.
✔️ c) Đúng. Isoamyl acetate, có tín hiệu đặc trưng cho liên kết C=O (ester, carboxylic acid) với số sóng 1780 - 1650 cm-1.
✔️ d) Đúng.
Isoamyl acetate, có tín hiệu đặc trưng cho liên kết C=O (ester, carboxylic acid) với số sóng 1780 - 1650 cm-1.
Isoamyl alcohol, có tín hiệu đặc trưng cho liên kết O-H (alcohol) với số sóng 3650 - 3200 cm-1.
Acetic acid, có tín hiệu đặc trưng cho liên kết C=O (ester, carboxylic acid) với số sóng 1780-1650 cm-1 và O-H (carboxylic acid) với số sóng 3300 - 2500 cm-1.
Câu 20 [704210]: Lindane hay hexachlorane là chất có tác dụng trừ sâu mạnh, từng được sử dụng phổ biến trong nông nghiệp và làm dược phẩm (trị ghẻ, diệt chấy,...). Tuy nhiên, do là chất độc phân huỷ rất chậm trong tự nhiên nên vào năm 2009, hexachlorane đã bị đưa vào phụ lục cấm sản xuất và sử dụng của Công ước Stockholm về các chất ô nhiễm hữu cơ khó phân huỷ và bị cấm sử dụng tại 169 quốc gia trên thế giới. Thành phần phần trăm khối lượng của các nguyên tố có trong hexachlorane là: 24,78% C; 2,08% H và 73,14% Cl. Dựa vào phổ MS, xác định được phân tử khối của hexachlorane là 288 (ứng với 35Cl) hoặc 300 (ứng với 37Cl). Trong tự nhiên, 35Cl chiếm 75,77% số lượng nguyên tử còn 37Cl chiếm 24,23% số lượng nguyên tử.
Nguyên tử khối trung bình của chlorine là:
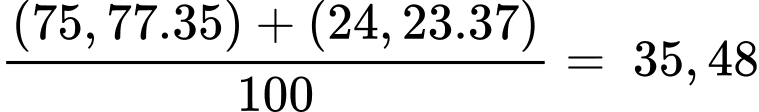
Tỉ lệ về số nguyên tử C : H : Cl có trong phân tử hexachlorane là:
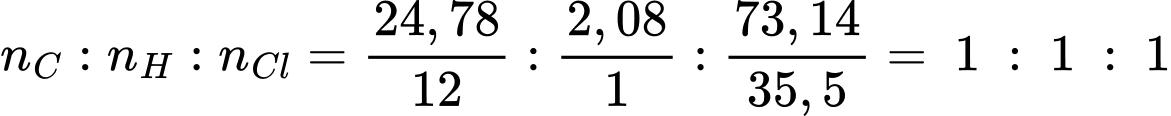
→ Công thức thực nghiệm của Lindane là CHCl.
+) Với 35Cl, hexachlorane có phân tử khối 288: (CHCl)n = 288 → n = 6
+) Tương tự, với 37Cl, hexachlorane có phân tử khối 300: (CHCl)n = 300 → n = 6
Vậy công thức phân tử của hexaclorane là C6H6Cl6.
Phân tích các phát biểu:
❌ (a) Sai. Đồng vị 35Cl ít hơn 2 neutron so với 37Cl.
✔️ (b) Đúng. Nguyên tử khối trung bình của Cl là 35,48.
✔️ (c) Đúng. Hexachlorane có chứa 6 nguyên tử Cl.
❌ (d) Sai. Công thức phân tử của hexaclorane là C6H6Cl6.
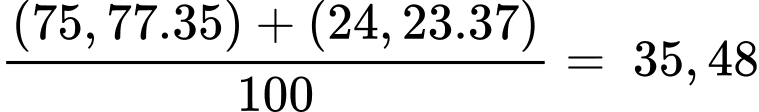
Tỉ lệ về số nguyên tử C : H : Cl có trong phân tử hexachlorane là:
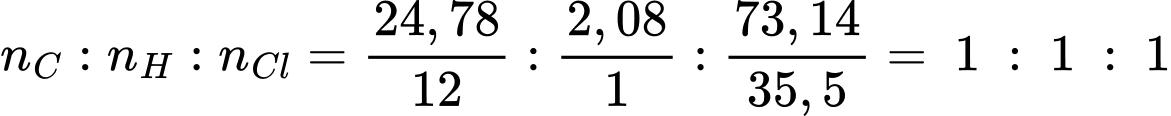
→ Công thức thực nghiệm của Lindane là CHCl.
+) Với 35Cl, hexachlorane có phân tử khối 288: (CHCl)n = 288 → n = 6
+) Tương tự, với 37Cl, hexachlorane có phân tử khối 300: (CHCl)n = 300 → n = 6
Vậy công thức phân tử của hexaclorane là C6H6Cl6.
Phân tích các phát biểu:
❌ (a) Sai. Đồng vị 35Cl ít hơn 2 neutron so với 37Cl.
✔️ (b) Đúng. Nguyên tử khối trung bình của Cl là 35,48.
✔️ (c) Đúng. Hexachlorane có chứa 6 nguyên tử Cl.
❌ (d) Sai. Công thức phân tử của hexaclorane là C6H6Cl6.
Câu 21 [704377]: Trong các dung dịch luôn hòa tan một lượng nhỏ khí oxygen hoặc khi để dung dịch ngoài không khí thì khí oxygen trong không khí có thể khuyếch tán vào trong dung dịch. Các kim loại ngâm trong các dung dịch có thể bị ăn mòn và để nghiên cứu hiện tượng thì tiến hành thí nghiệm như sau:
▪ Rót dung dịch NaCl vào 2 cốc thuỷ tinh. Ngâm một đinh sắt vào cốc (1). Ngâm một đinh sắt có quấn dây kẽm vào cốc (2).
▪ Quan sát hiện tượng xảy ra sau 5 ngày.
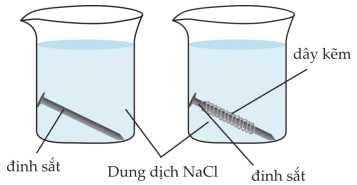
▪ Rót dung dịch NaCl vào 2 cốc thuỷ tinh. Ngâm một đinh sắt vào cốc (1). Ngâm một đinh sắt có quấn dây kẽm vào cốc (2).
▪ Quan sát hiện tượng xảy ra sau 5 ngày.

Cốc (1): Đinh sắt bị ăn mòn và chuyển sang màu vàng nâu của của FeCl3.
Do kim loại tác dụng với những chất mà nó tiếp xúc trong môi trường, trong nước muối có oxygen hòa tan.
2Fe + 3Cl2 ⟶ 2FeCl3
3Fe + 4H2O ⟶ Fe3O4 + 4H2
3Fe + 2O2 ⟶ Fe3O4
Cốc (2): Xảy ra ăn mòn điện hóa
Cathode cực dương là Fe: 2H2O + O2 + 4e ⟶ 4OH–
Anode cực âm là Zn: Zn ⟶ Zn2+ + 2e
Phân tích các phát biểu:
✔️ (a) Đúng. Trong cốc (1), đinh sắt bị ăn mòn bởi oxygen hòa tan và ion Cl– trong dung dịch NaCl, dẫn đến sự hình thành hợp chất FeCl3 có màu vàng nâu.
✔️ (b) Đúng. Ở cốc (2), dây kẽm quấn quanh đinh sắt hoạt động như một cực dương (anode), và kẽm bị oxi hóa thay vì sắt. Do đó, oxygen trong dung dịch sẽ phản ứng với kẽm trước, bảo vệ đinh sắt.
✔️ (c) Đúng. Dung dịch NaCl đóng vai trò như một chất điện li, tạo ra các ion trong dung dịch (Na+, Cl–), giúp quá trình ăn mòn điện hóa xảy ra dễ dàng hơn.
✔️ (d) Đúng. Thí nghiệm minh họa phương pháp bảo vệ điện hóa. Việc quấn dây kẽm quanh đinh sắt cho thấy kẽm bị ăn mòn thay vì sắt, đây là cách bảo vệ sắt thông qua một kim loại hoạt động hơn.
Do kim loại tác dụng với những chất mà nó tiếp xúc trong môi trường, trong nước muối có oxygen hòa tan.
2Fe + 3Cl2 ⟶ 2FeCl3
3Fe + 4H2O ⟶ Fe3O4 + 4H2
3Fe + 2O2 ⟶ Fe3O4
Cốc (2): Xảy ra ăn mòn điện hóa
Cathode cực dương là Fe: 2H2O + O2 + 4e ⟶ 4OH–
Anode cực âm là Zn: Zn ⟶ Zn2+ + 2e
Phân tích các phát biểu:
✔️ (a) Đúng. Trong cốc (1), đinh sắt bị ăn mòn bởi oxygen hòa tan và ion Cl– trong dung dịch NaCl, dẫn đến sự hình thành hợp chất FeCl3 có màu vàng nâu.
✔️ (b) Đúng. Ở cốc (2), dây kẽm quấn quanh đinh sắt hoạt động như một cực dương (anode), và kẽm bị oxi hóa thay vì sắt. Do đó, oxygen trong dung dịch sẽ phản ứng với kẽm trước, bảo vệ đinh sắt.
✔️ (c) Đúng. Dung dịch NaCl đóng vai trò như một chất điện li, tạo ra các ion trong dung dịch (Na+, Cl–), giúp quá trình ăn mòn điện hóa xảy ra dễ dàng hơn.
✔️ (d) Đúng. Thí nghiệm minh họa phương pháp bảo vệ điện hóa. Việc quấn dây kẽm quanh đinh sắt cho thấy kẽm bị ăn mòn thay vì sắt, đây là cách bảo vệ sắt thông qua một kim loại hoạt động hơn.
Câu 22 [704305]: Khả năng hoạt động hóa học của hai kim loại có thể được so sánh thông quá thí nghiệm như sau:
Bước 1: Chuẩn bị một đinh sắt đã được đánh sạch bề mặt, một dung dịch copper(II) sulfate 1 M được đựng trong cốc thuỷ tinh.
Bước 2: Cho đinh sắt vào cốc thuỷ tinh chứa dung dịch copper(II) sulfate 1 M. Sau khoảng 10 phút thì quan sát hiện tượng.
Bước 1: Chuẩn bị một đinh sắt đã được đánh sạch bề mặt, một dung dịch copper(II) sulfate 1 M được đựng trong cốc thuỷ tinh.
Bước 2: Cho đinh sắt vào cốc thuỷ tinh chứa dung dịch copper(II) sulfate 1 M. Sau khoảng 10 phút thì quan sát hiện tượng.
Fe + CuSO4 → FeSO4 + Cu
Quá trình oxi hóa Fe → Fe2+ + 2e
Quá trình khử Cu2+ + 2e → Cu
Phân tích các phát biểu:
✔️ (a) Đúng. Sau phản ứng sinh ra kim loại Cu màu nâu bám trên đinh sắt.
❌ (b) Sai. Sau phản ứng sinh ra kim loại Cu nên nồng độ của Cu2+ giảm dần.
❌ (c) Sai. Thế khử chuẩn của Fe2+/Fe nhỏ hơn thế khử chuẩn của Cu2+/Cu, Eo Mn+/M càng lớn thì tính oxi hóa của Mn+ càng mạnh; tính khử của M càng yếu
✔️ (d) Đúng. Từ hiện tượng ta thấy được Fe đã chiếm vị trí của Cu trong muối, Fe có độ hoạt động mạnh hơn Cu.
Quá trình oxi hóa Fe → Fe2+ + 2e
Quá trình khử Cu2+ + 2e → Cu
Phân tích các phát biểu:
✔️ (a) Đúng. Sau phản ứng sinh ra kim loại Cu màu nâu bám trên đinh sắt.
❌ (b) Sai. Sau phản ứng sinh ra kim loại Cu nên nồng độ của Cu2+ giảm dần.
❌ (c) Sai. Thế khử chuẩn của Fe2+/Fe nhỏ hơn thế khử chuẩn của Cu2+/Cu, Eo Mn+/M càng lớn thì tính oxi hóa của Mn+ càng mạnh; tính khử của M càng yếu
✔️ (d) Đúng. Từ hiện tượng ta thấy được Fe đã chiếm vị trí của Cu trong muối, Fe có độ hoạt động mạnh hơn Cu.
PHẦN III. Thí sinh trả lời từ câu 1 đến 6. Thí sinh điền kết quả mỗi câu vào mỗi ô trả lời tương ứng theo hướng dẫn của phiếu trả lời.
Câu 23 [706286]: Một mẫu nước cứng có nồng độ các ion như sau: Ca2+ x M; Mg2+ y M; HCO3– 0,005 M; Cl– 0,004 M; SO42– 0,001 M. Để làm mềm 10 L nước này cần dùng tối thiểu bao nhiêu gam sodium carbonate?
Áp dụng định luật bảo toàn điện tích:
2x + 2y = 0,005 + 0,004 + 0,001.2 → x + y = 0,0055 M
Tổng số mol của Mg2+ và Ca2+ là nCa2+ + nMg2+ = 0,0055 × 10 = 0,055 mol
Mg2+ + CO32- → MgCO3
Ca2+ + CO32- → CaCO3
Theo phương trình số mol của CO32- là 0,055 mol
Khối lượng của Na2CO3 cần thiết là mNa2CO3 = 0,055 × 106 = 5,83 gam
⟹ Điền đáp án: 5,83
2x + 2y = 0,005 + 0,004 + 0,001.2 → x + y = 0,0055 M
Tổng số mol của Mg2+ và Ca2+ là nCa2+ + nMg2+ = 0,0055 × 10 = 0,055 mol
Mg2+ + CO32- → MgCO3
Ca2+ + CO32- → CaCO3
Theo phương trình số mol của CO32- là 0,055 mol
Khối lượng của Na2CO3 cần thiết là mNa2CO3 = 0,055 × 106 = 5,83 gam
⟹ Điền đáp án: 5,83
Câu 24 [705820]: Khi đun nóng X với hỗn hợp HNO3 đặc và H2SO4 đặc có thể thu được cellulose trinitrate, là chất dễ cháy và nổ mạnh, dùng để chế tạo thuốc súng không khói. Từ 4 lít dung dịch HNO3 63% (khối lượng riêng 1,5 g/mL) có thể điều chế m kg cellulose trinitrate với hiệu suất phản ứng đạt 70%. Xác định giá trị của m (làm tròn đến hàng phần trăm).
Ta có phương trình:
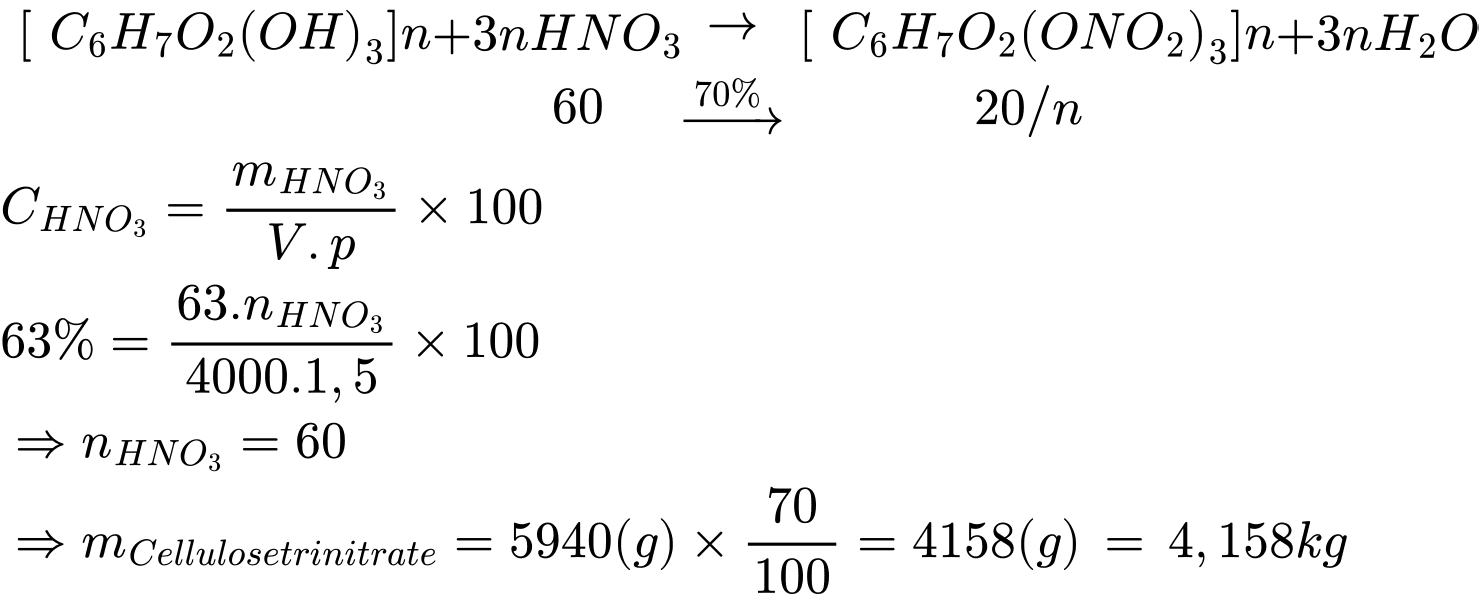
⟹ Đáp án đúng là: 4,16
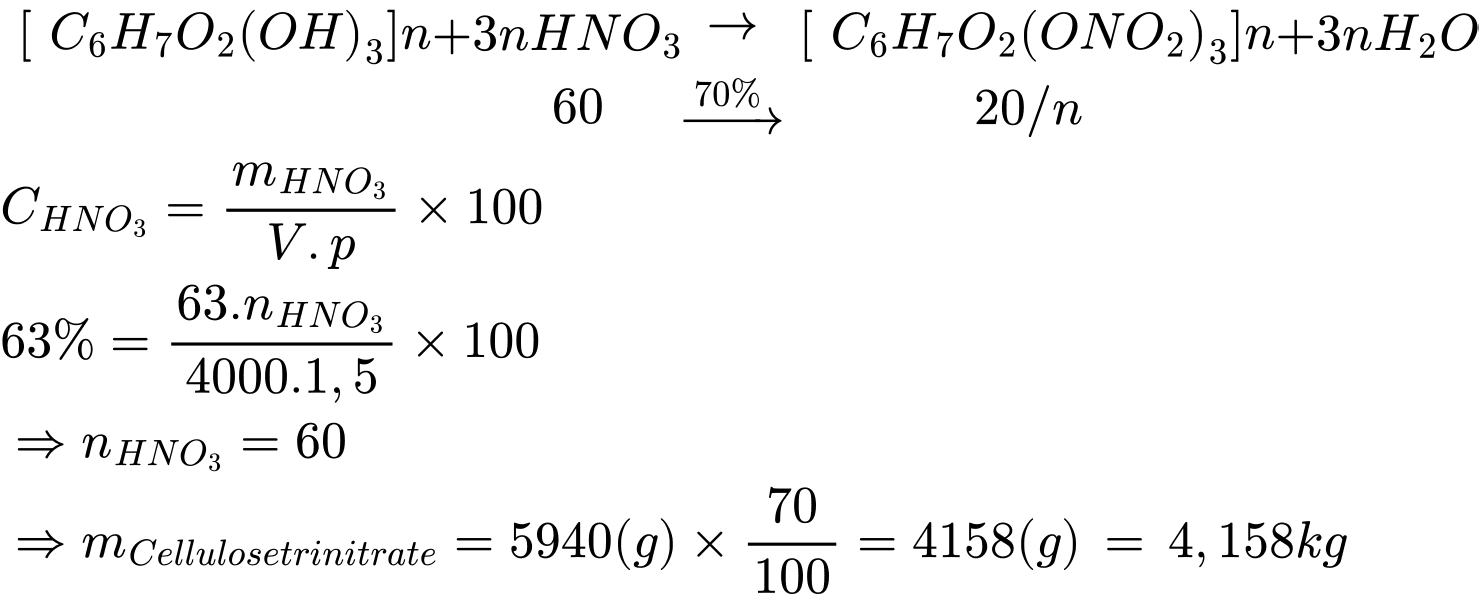
⟹ Đáp án đúng là: 4,16
Câu 25 [706228]: Cho các mẫu chất và dán nhãn tương ứng như sau: Glycine (1), glutamic acid (2), aniline (3), methylamine (4). Hiện tượng khi làm thí nghiệm với các chất sau ở dạng dung dịch X, Y, Z, T được ghi lại như sau:

Gán nhãn dán các chất tương ứng với hiện tượng của dung dịch X, Y, Z, T theo trình tự dãy bốn số (ví dụ: 1234, 4213, ...).

Gán nhãn dán các chất tương ứng với hiện tượng của dung dịch X, Y, Z, T theo trình tự dãy bốn số (ví dụ: 1234, 4213, ...).
🌟Mẫu thử X: Làm quỳ tím hóa xạnh, và không tạo kết tủa với bromine
→ Chất tương ứng là methylamine (4)
🌟Mẫu thử Y: Không làm quỳ tím đổi màu, nhưng tạo kết tủa trắng khí tác dụng với Bromine
→ Chất tương ứng là aniline (3)
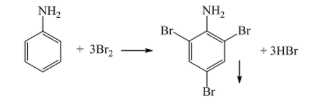
🌟Mẫu thử Z: không làm đổi màu quì tím, không phản ứng với dung dịch Bromine,
→ Chất tương ứng là glycine (1)
🌟Mẫu thử T: làm quỳ tím hóa đỏ, không phản ứng với dung dịch Bromine,
→ Chất tương ứng là glutamic acid (2)
⟹ Điền đáp án: 4312
→ Chất tương ứng là methylamine (4)
🌟Mẫu thử Y: Không làm quỳ tím đổi màu, nhưng tạo kết tủa trắng khí tác dụng với Bromine
→ Chất tương ứng là aniline (3)

🌟Mẫu thử Z: không làm đổi màu quì tím, không phản ứng với dung dịch Bromine,
→ Chất tương ứng là glycine (1)
🌟Mẫu thử T: làm quỳ tím hóa đỏ, không phản ứng với dung dịch Bromine,
→ Chất tương ứng là glutamic acid (2)
⟹ Điền đáp án: 4312
Câu 26 [706227]: Trong tự nhiên quặng bauxite có thành phần chính là Al2O3. Quặng bauxite mỏ Tây Tân Rai – Lâm Đồng nói riêng và các mỏ thuộc vùng Tây nguyên của Việt Nam nói chung là loại quặng bauxite có nguồn gốc phong hóa từ các loại đá bazan, quặng thường có màu nâu sẫm, nâu đỏ, hoặc xám, xám phớt vàng.
Có phương trình nhiệt hóa học:
2Al2O3(s) 4Al(s) + 3O2(g);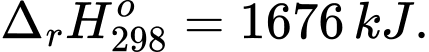
Để thu được 1 tấn Al với hiệu suất sử dụng năng lượng đạt 75% và 1 W = 1 J/s, tính lượng điện đã tiêu thụ để sản xuất lượng nhôm trên theo kWh (làm tròn đến hàng phần trăm)?
Có phương trình nhiệt hóa học:
2Al2O3(s) 4Al(s) + 3O2(g);
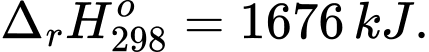
Để thu được 1 tấn Al với hiệu suất sử dụng năng lượng đạt 75% và 1 W = 1 J/s, tính lượng điện đã tiêu thụ để sản xuất lượng nhôm trên theo kWh (làm tròn đến hàng phần trăm)?
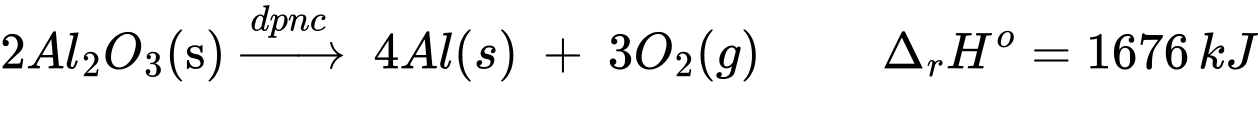
Đổi 1 tấn = 1000000 gam; 1 kWh = 3600 kJ
Để điều chế 4 mol Al cần 1676 kJ
→ Để điều chế 108 gam Al cần 1676 kJ
→ Để điều chế 1000000 gam A cần 15518518,52 kJ
Lượng điện năng cần tiêu thụ để sản xuất nhôm là: 15518518,52 ÷ 3600 × 100 ÷ 75 ≈ KWh.
⟹ Điền đáp án: 5748
Câu 27 [705821]: Cấu trúc của một peptide được đưa ra dưới đây:
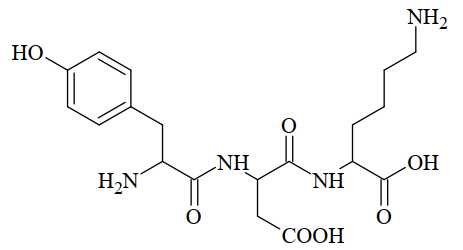
Nếu giá trị tuyệt đối của điện tích ứng với dạng tồn tại chủ yếu của peptide ở pH = 2, pH = 6 và pH = 11 lần lượt là |z1 |, |z2 | và |z3 | thì |𝑧1 | + |𝑧2 | + |𝑧3 | bằng bao nhiêu?

Nếu giá trị tuyệt đối của điện tích ứng với dạng tồn tại chủ yếu của peptide ở pH = 2, pH = 6 và pH = 11 lần lượt là |z1 |, |z2 | và |z3 | thì |𝑧1 | + |𝑧2 | + |𝑧3 | bằng bao nhiêu?
- Tại pH = 2 : cung cấp môi trường H+
2 nhóm NH2 ⟹ NH3+
2 nhóm COOH điện tích = 0
⟹ |z1| = 2
- Tại pH = 6 : tồn tại dạng ion lưỡng cực
2 nhóm NH2 ⟹ NH3+
2 nhóm COOH ⟹ COO-
⟹ |z2| = 0
- Tại pH = 11: cung cấp ion OH-
2 nhóm COOH ⟹ COO-
Nhóm OH ⟹ O-
⟹ |z3| = 3
⟹ |z1| + |z2| + |z3| = 2 + 0 + 3 = 5
Điền đáp án: 5
Câu 28 [706144]: Trong công nghiệp chlorine-kiềm, dung dịch sodium chloride (NaCl) bão hoà có nồng độ khoảng 300 g.L–1 chỉ được điện phân một phần thành “nước muối nghèo” có nồng độ 220 g.L–1. “Nước muối nghèo" sau đó được dẫn ra khỏi bể điện phân, trong khi nước muối bão hoà mới được bơm vào. Từ x lít dung dịch NaCl bão hoà điện phân thành “nước muối nghèo” sẽ sản xuất được một thùng 10 lít xút 50% thương phẩm có khối lượng riêng là 1,52 g.mL–1. Biết lượng xút trong quá trình điều chế thất thoát 20% và trong quá trình điện phân, thể tích dung dịch thay đổi không đáng kể. Tính giá trị của x (làm tròn đến hàng đơn vị).
Đổi 10 L = 10000 mL
Khối lượng dung dịch NaOH là mdd NaOH = 10000 × 1,52 = 15200 gam
Khối lượng NaOH là mNaOH = 15200 × 50% = 7600 gam
Số mol của NaOH là nNaOH = 7600 ÷ 40 = 190 mol
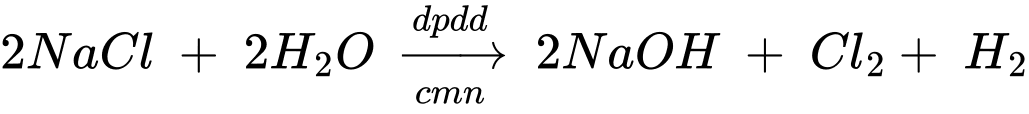
Theo phương trình số mol của NaCl là 190 mol
Khối lượng của NaCl là: x.(300 – 220) = 190 × 58,5 : 80% → x ≈ 173,67
⟹ Điền đáp án: 174
Khối lượng dung dịch NaOH là mdd NaOH = 10000 × 1,52 = 15200 gam
Khối lượng NaOH là mNaOH = 15200 × 50% = 7600 gam
Số mol của NaOH là nNaOH = 7600 ÷ 40 = 190 mol
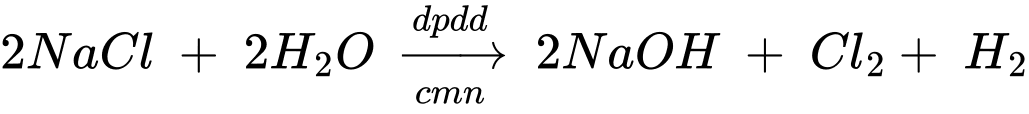
Theo phương trình số mol của NaCl là 190 mol
Khối lượng của NaCl là: x.(300 – 220) = 190 × 58,5 : 80% → x ≈ 173,67
⟹ Điền đáp án: 174