PHẦN I. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
Câu 1 [702829]: Hạt cơ bản nào sau đây không bị lệch trong điện trường?
A, Electron.
B, Proton.
C, Neutron.
D, Hydrogen.
Nguyên tử chứa 3 loại hạt cơ bản:
+ Electron mang điện tích âm nên lệch về phía cực dương trong điện trường
+ Proton mang điện tích dương nên lệch về phía cực âm trong điện trường
+ Neutron không mang điện tích nên không bị lệch trong điện trường.
⇒ Chọn đáp án C Đáp án: C
+ Electron mang điện tích âm nên lệch về phía cực dương trong điện trường
+ Proton mang điện tích dương nên lệch về phía cực âm trong điện trường
+ Neutron không mang điện tích nên không bị lệch trong điện trường.
⇒ Chọn đáp án C Đáp án: C
Câu 2 [704177]: Kết quả ghi phổ MS của acetone (CH3COCH3) cho biết ion phân tử [CH3COCH3+] có giá trị m/z nào sau đây?
A, 57.
B, 58.
C, 60.
D, 59.
Trong phổ MS mảnh có giá trị m/z lớn nhất ứng với mảnh ion phân tử [M+] và có giá trị bằng phân tử khối của chất nghiên cứu nên kết quả ghi phổ MS của acetone (CH3COCH3) cho biết ion phân tử [CH3COCH3+] có giá trị m/z bằng 58.
⇒ Chọn đáp án B Đáp án: B
⇒ Chọn đáp án B Đáp án: B
Câu 3 [190529]: Bromomethane (CH3Br) được sử dụng làm chất để tiêu diệt côn trùng gây hại trong hạt. Bromomethane có thể được tạo ra bằng cách cho methanol phản ứng với hydrogen bromide theo phương trình sau:
CH3OH + HBr ⟶ CH3Br + H2O.
Phản ứng trên thuộc loại phản ứng nào?
CH3OH + HBr ⟶ CH3Br + H2O.
Phản ứng trên thuộc loại phản ứng nào?
A, Phản ứng cộng.
B, Phản ứng thế.
C, Phản ứng tách.
D, Phản ứng oxi hóa.
CH3OH + HBr ⟶ CH3Br + H2O.
Nguyên tử Br đã thay thế nhóm OH trong alcohol ⇒ Phản ứng trên là phản ứng thế.
⇒ Đáp án B Đáp án: B
Nguyên tử Br đã thay thế nhóm OH trong alcohol ⇒ Phản ứng trên là phản ứng thế.
⇒ Đáp án B Đáp án: B
Câu 4 [304967]: Chất nào sau đây không phải acid béo?
A, Oleic acid.
B, Stearic acid.
C, Acetic acid.
D, Palmitic acid.
4 acid béo cần nhớ trong chương trình hóa THPT để ⇒ các chất béo tương ứng gồm:
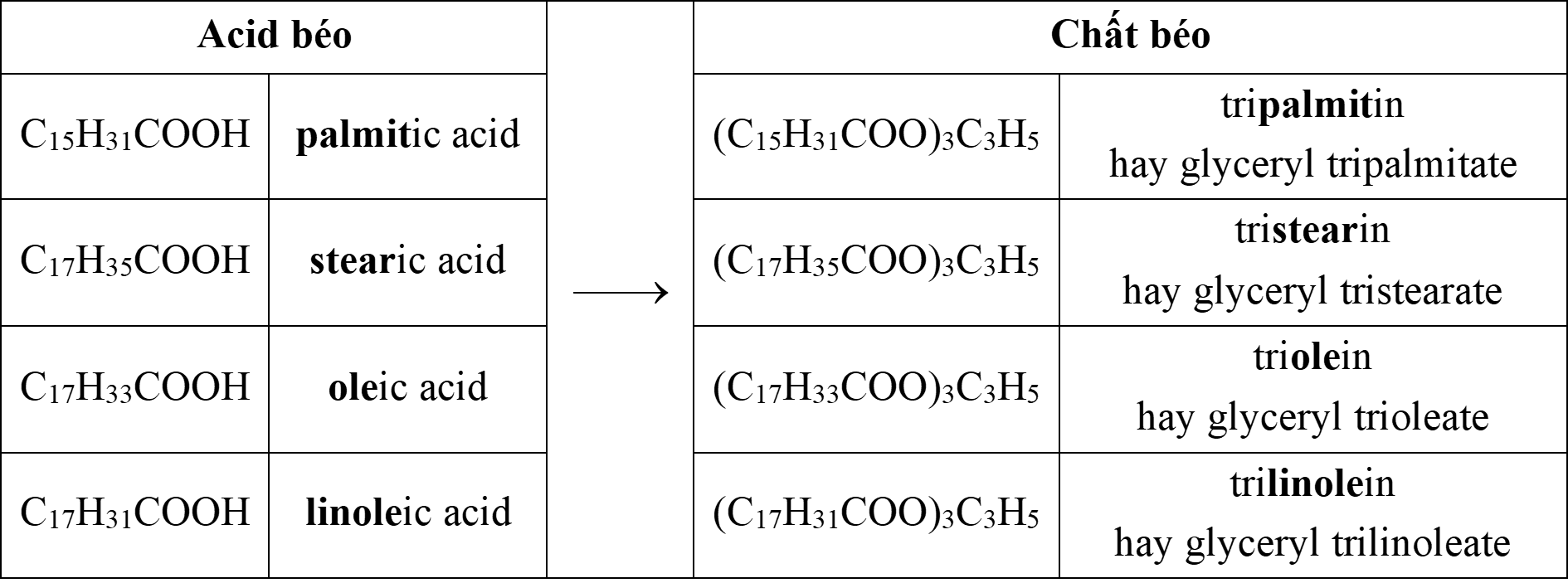
⇒ Quan sát 4 đáp án thì C. acetic acid không phải là acid béo
⟹Chọn đáp án C. Đáp án: C

⇒ Quan sát 4 đáp án thì C. acetic acid không phải là acid béo
⟹Chọn đáp án C. Đáp án: C
Câu 5 [308236]: Carbohydrate nào sau đây thuộc loại disaccharide?
A, Cellulose.
B, Amylose.
C, Saccharose.
D, Glucose.
HD: Bài học phân loại hợp chất carbohydrate:
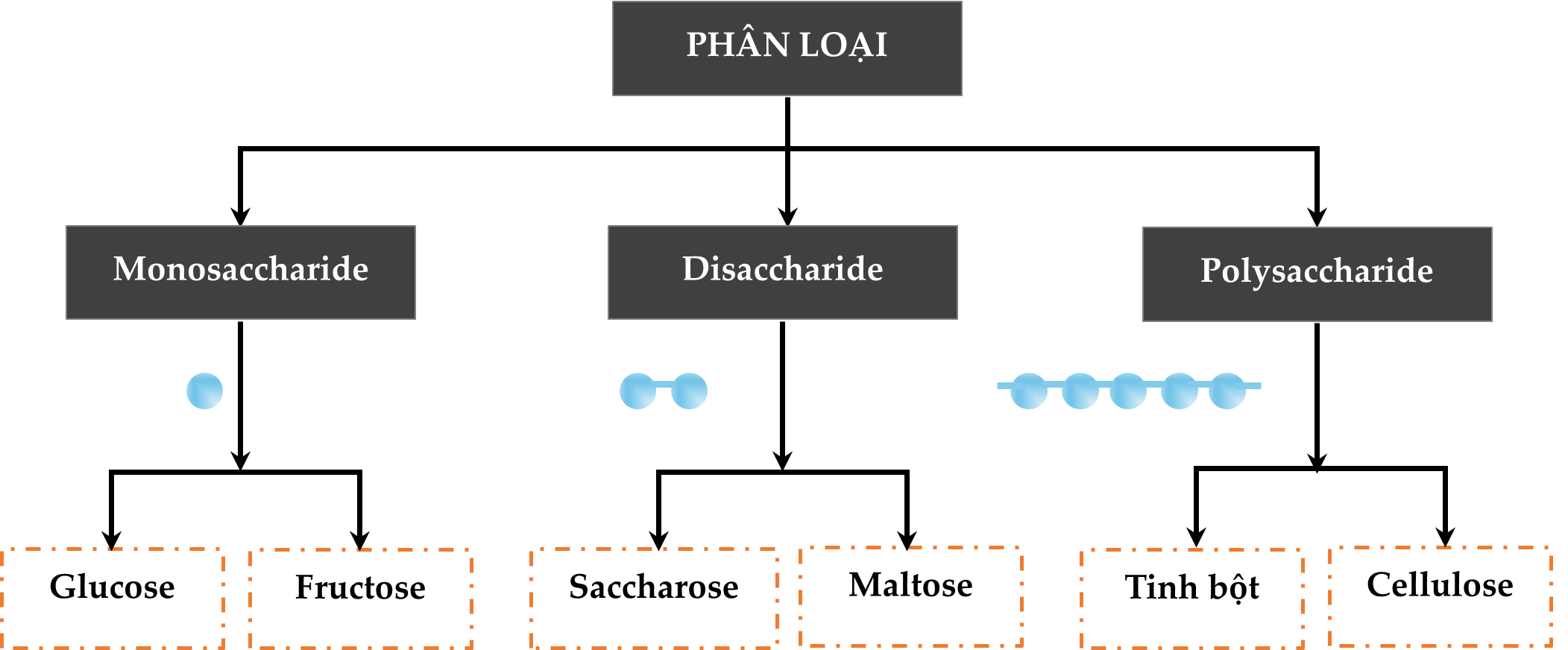
⇒ Saccharose là một loại disaccharide
⇝ Chọn đáp án C. Đáp án: C

⇒ Saccharose là một loại disaccharide
⇝ Chọn đáp án C. Đáp án: C
Câu 6 [308505]: Khi thay nguyên tử H trong phân tử NH3 bằng gốc hydrocarbon, thu được
A, amine.
B, lipid.
C, ester.
D, amino acid.
Khi thay thế một hay nhiều nguyên tử H trong phân tử NH3 bằng gốc hydrocarbon thì thu được amine.
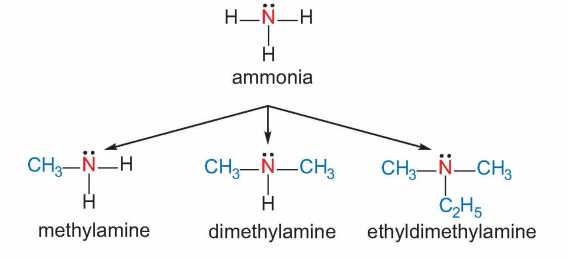
⇒ Chọn đáp án A Đáp án: A

⇒ Chọn đáp án A Đáp án: A
Câu 7 [560617]: Đồng là kim loại dẫn điện tốt nhất trong các kim loại (chỉ xếp sau Ag), tuy nhiên các dây điện cao thế không được làm bằng đồng mà thường được làm bằng kim loại X. Kim loại X là
A, Fe.
B, Na.
C, Al.
D, Au.
Mặc dù khả năng dẫn điện thấp hơn Cu, tuy nhiên dây nhôm nhẹ hơn dây đồng tới hơn 3 lần nên dây điện cao thế được làm bằng nhôm để vận chuyển dễ dàng, tiết kiệm được nguyên liệu, giảm sức lực của dây điện cho các cột điện.
⟹ Chọn đáp án C Đáp án: C
⟹ Chọn đáp án C Đáp án: C
Câu 8 [560907]: Thuốc diệt chuột cần phải không tan trong nước mưa nhưng hòa tan ở độ pH thấp của chất chứa trong dạ dày. Hợp chất barium nào thích hợp để dùng làm thuộc diệt chuột?
A, Barium carbonate.
B, Barium chloride.
C, Barium hydroxide.
D, Barium sulfate.
Barium carbonate BaCO3 không tan trong nước mưa (pH trung tính) nhưng sẽ hòa tan trong môi trường có độ pH thấp, như trong dạ dày, tạo ra barium ion (Ba2+) có tính độc hại. Khi chuột nuốt phải barium carbonate, nó sẽ bị hòa tan trong dạ dày, giải phóng barium ion gây độc cho cơ thể.
❌ B. Barium chloride (BaCl2): Là một muối tan trong nước, không có đặc tính phù hợp với yêu cầu của thuốc diệt chuột.
❌ C. Barium hydroxide (Ba(OH)2): Là một base mạnh, tan trong nước và có tính kiềm cao, không phù hợp để làm thuốc diệt chuột.
❌ D. Barium sulfate (BaSO4): Là một muối không tan trong nước và cũng không có tính độc hại ở nồng độ bình thường, không phù hợp với mục đích diệt chuột.
⟹ Chọn đáp án A. Đáp án: A
❌ B. Barium chloride (BaCl2): Là một muối tan trong nước, không có đặc tính phù hợp với yêu cầu của thuốc diệt chuột.
❌ C. Barium hydroxide (Ba(OH)2): Là một base mạnh, tan trong nước và có tính kiềm cao, không phù hợp để làm thuốc diệt chuột.
❌ D. Barium sulfate (BaSO4): Là một muối không tan trong nước và cũng không có tính độc hại ở nồng độ bình thường, không phù hợp với mục đích diệt chuột.
⟹ Chọn đáp án A. Đáp án: A
Câu 9 [706036]: Một pin điện hoá được thiết lập từ hai điện cực tạo bởi hai cặp oxi hoá khử là Mn+/M và Cu2+/Cu. Cho bảng sau:
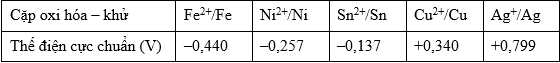
Nếu M là kim loại nào thì sức điện động chuẩn của pin tạo ra sẽ lớn nhất?

Nếu M là kim loại nào thì sức điện động chuẩn của pin tạo ra sẽ lớn nhất?
A, Fe.
B, Ni.
C, Sn.
D, Ag.
Phân tích các phát biểu :
✔️A. Fe
Pin Fe-Cu: Anode (-) Fe và Cathode (+) Cu
E pin = E(+) – E(-) = 0,34 – (-0,44) = 0,78 V
❌B. Ni
Pin Ni-Cu: Anode (-) Ni và Cathode (+) Cu
E pin = E(+) – E(-) = 0,34 – (-0,257) = 0,597 V
❌C. Sn
Pin Sn-Cu: Anode (-) Sn và Cathode (+) Cu
E pin = E(+) – E(-) = 0,34 – (-0,137) = 0,477 V
❌D. Ag
Pin Cu-Ag, Anode (-) Cu và cathode (+) Ag
Epin = E(+) – E(-) = 0,799 – 0,34 = 0,459 V
⟹Chọn đáp án A Đáp án: A
✔️A. Fe
Pin Fe-Cu: Anode (-) Fe và Cathode (+) Cu
E pin = E(+) – E(-) = 0,34 – (-0,44) = 0,78 V
❌B. Ni
Pin Ni-Cu: Anode (-) Ni và Cathode (+) Cu
E pin = E(+) – E(-) = 0,34 – (-0,257) = 0,597 V
❌C. Sn
Pin Sn-Cu: Anode (-) Sn và Cathode (+) Cu
E pin = E(+) – E(-) = 0,34 – (-0,137) = 0,477 V
❌D. Ag
Pin Cu-Ag, Anode (-) Cu và cathode (+) Ag
Epin = E(+) – E(-) = 0,799 – 0,34 = 0,459 V
⟹Chọn đáp án A Đáp án: A
Câu 10 [705424]: Phát biểu nào sau đây là đúng?
A, Ở điều kiện thường, đơn chất fluorine, chlorine và bromine đều ở thể khí.
B, So sánh màu sắc của các đơn chất halogen ở điều kiện thường thì fluorine có màu nhạt nhất.
C, Nhiệt độ nóng chảy của các đơn chất halogen tăng dần khi đi từ iodine đến fluorine.
D, Đơn chất iodine được thêm vào muối ăn để phòng bệnh bướu cổ.
Phân tích các phát biểu:
❌ A. Sai. Trạng thái tập hợp của đơn chất ở 20 oC thay đổi: fluorine và chlorine ở thể khí, bromine ở thể lỏng, iodine ở thể rắn.
✔️ B. Đúng. Các đơn chất halogen có màu sắc đậm dần từ fluorine đến iodine:

❌ C. Sai. Nhiệt độ nóng chảy và nhiệt độ sôi của đơn chất halogen bị ảnh hưởng bởi tương tác van der Waals giữa các phân tử. Từ fluorine đến iodine, khối lượng phân tử và bán kính nguyên tử tăng, làm tăng tương tác van der Waals, dẫn đến nhiệt độ nóng chảy, nhiệt độ sôi tăng.
❌ D. Sai. KI, KIO3 được cho vào muối ăn để bổ sung nguyên tố iodine, cung cấp iodine ngăn ngừa bệnh bướu cổ.
⇒ Chọn đáp án B Đáp án: B
❌ A. Sai. Trạng thái tập hợp của đơn chất ở 20 oC thay đổi: fluorine và chlorine ở thể khí, bromine ở thể lỏng, iodine ở thể rắn.
✔️ B. Đúng. Các đơn chất halogen có màu sắc đậm dần từ fluorine đến iodine:

❌ C. Sai. Nhiệt độ nóng chảy và nhiệt độ sôi của đơn chất halogen bị ảnh hưởng bởi tương tác van der Waals giữa các phân tử. Từ fluorine đến iodine, khối lượng phân tử và bán kính nguyên tử tăng, làm tăng tương tác van der Waals, dẫn đến nhiệt độ nóng chảy, nhiệt độ sôi tăng.
❌ D. Sai. KI, KIO3 được cho vào muối ăn để bổ sung nguyên tố iodine, cung cấp iodine ngăn ngừa bệnh bướu cổ.
⇒ Chọn đáp án B Đáp án: B
Câu 11 [702830]: Vấn đề nào sau đây có thể xảy ra nếu nông dân bón quá nhiều NH4NO3 cho cây trồng?
A, Lượng NH4NO3 dư thừa (do thực vật không sử dụng hết) làm cho đất bị kiềm hóa.
B, Mưa rửa trôi một số NH4NO3 vào nước sông và tạo thành kết tủa.
C, NH4NO3 hòa tan trong nước ngầm và có thể đi vào cơ thể qua đường uống.
D, Ammonia (NH3) được tạo thành, dẫn đến độ pH của đất giảm đáng kể.
Phân tích các vấn đề:
❌ A. Sai. Lượng NH4NO3 dư thừa (do thực vật không sử dụng hết) làm cho đất bị acid hóa do quá trình phân li của NH4NO3 như sau:
NH4NO3 → NH4+ + NO3-. Lúc này, NH4 tiếp tục phân li cho ra NH3 và H+. H+ là môi trường acid nên đất sẽ bị acid hoá.
❌ B. Sai. Mưa rửa trôi một số NH4NO3 vào nước sông nhưng không tạo kết tủa do ion NH4+ và NO3- không có khả năng tạo kết tủa.
❌ C. Sai. NH4NO3 hòa tan tốt trong nước nên chỉ tổn tại trên tầng nước bề mặt nên để trải qua nhiều lớp đá, nhiều tầng khác để xuống nguồn nước ngầm là không thể.
✔️ D. Đúng. Ammonia (NH3) được tạo thành, dẫn đến độ pH của đất giảm đáng kể do phân li ra ion H+, làm cho đất có môi trường acid như ý a đã nhắc đến. Đáp án: D
❌ A. Sai. Lượng NH4NO3 dư thừa (do thực vật không sử dụng hết) làm cho đất bị acid hóa do quá trình phân li của NH4NO3 như sau:
NH4NO3 → NH4+ + NO3-. Lúc này, NH4 tiếp tục phân li cho ra NH3 và H+. H+ là môi trường acid nên đất sẽ bị acid hoá.
❌ B. Sai. Mưa rửa trôi một số NH4NO3 vào nước sông nhưng không tạo kết tủa do ion NH4+ và NO3- không có khả năng tạo kết tủa.
❌ C. Sai. NH4NO3 hòa tan tốt trong nước nên chỉ tổn tại trên tầng nước bề mặt nên để trải qua nhiều lớp đá, nhiều tầng khác để xuống nguồn nước ngầm là không thể.
✔️ D. Đúng. Ammonia (NH3) được tạo thành, dẫn đến độ pH của đất giảm đáng kể do phân li ra ion H+, làm cho đất có môi trường acid như ý a đã nhắc đến. Đáp án: D
Câu 12 [304803]: Ester có công thức cấu tạo như hình vẽ sau đây được tạo bởi phản ứng ester hóa giữa cặp carboxylic acid và alcohol nào sau đây?
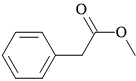

A, Formic acid và benzyl alcohol.
B, Phenylacetic acid và methyl alcohol.
C, Benzoic acid và methyl alcohol.
D, Acetic acid và benzyl alcohol.
Phân tích cấu tạo của ester:
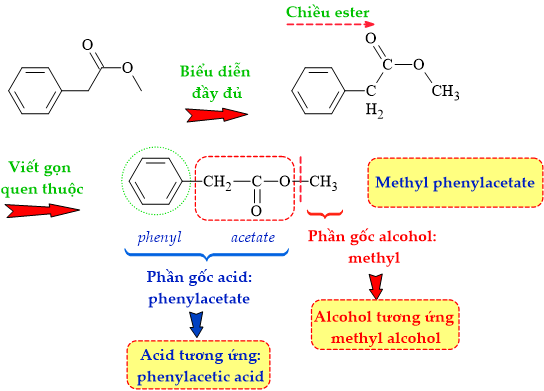
⇒ cặp acid và alcohol tương ứng là phenylacetic acid (C6H5CH2COOH) và methyl alcohol (CH3OH) ⇝ Chọn đáp án B. ♦ Đáp án: B

⇒ cặp acid và alcohol tương ứng là phenylacetic acid (C6H5CH2COOH) và methyl alcohol (CH3OH) ⇝ Chọn đáp án B. ♦ Đáp án: B
Câu 13 [702839]: Hỗn hợp dipeptide Lys-Asn và hai amino acid thành phần của nó, asparagine và lysine, được phân tách bằng phương pháp điện di sử dụng đệm ở pH 5,0. Biết rằng tại pH = 5 thì lysine và asparagine tồn tại chủ yếu ở các dạng dưới đây:
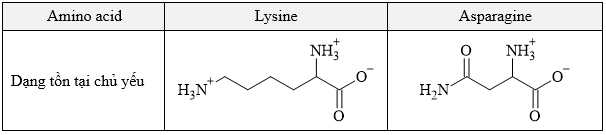
Kết quả khi tiến hành điện di được thể hiện trong hình dưới đây:
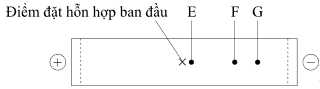
Cho các nhận định sau về quá trình điện di:
(a) Tại môi trường pH = 5 thì dạng tồn tại chủ yếu của lysine có tổng điện tích là +1.
(b) Chất E có thể là dipeptide Lys-Asn do có phân tử khối lớn.
(c) Điện tích dương càng lớn thì càng dễ dàng di chuyển về phía cực âm.
(d) Lysine có phân tử khối lớn hơn asparagine nên di chuyển chậm hơn và cách xa cực âm hơn.
Các nhận định đúng là

Kết quả khi tiến hành điện di được thể hiện trong hình dưới đây:

Cho các nhận định sau về quá trình điện di:
(a) Tại môi trường pH = 5 thì dạng tồn tại chủ yếu của lysine có tổng điện tích là +1.
(b) Chất E có thể là dipeptide Lys-Asn do có phân tử khối lớn.
(c) Điện tích dương càng lớn thì càng dễ dàng di chuyển về phía cực âm.
(d) Lysine có phân tử khối lớn hơn asparagine nên di chuyển chậm hơn và cách xa cực âm hơn.
Các nhận định đúng là
A, (a), (c).
B, (a), (d).
C, (a), (c), (d).
D, (b), (c), (d).
Tại pH = 5:
Chất G (lysine, mang điện tích dương mạnh nhất).
Chất F (dipeptide Lys-Asn, mang điện tích dương nhưng yếu hơn lysine).
Chất E (asparagine, mang điện tích bằng 0, di chuyển chậm hoặc không di chuyển).
Phân tích các nhận định:
✔️ (a) Đúng. Tại môi trường pH = 5 thì dạng tồn tại chủ yếu của lysine có tổng điện tích là +1.
❌ (b) Sai. Chất E là asparagine mang điện tích bằng 0, di chuyển chậm hoặc không di chuyển.
✔️ (c) Đúng. Điện tích dương càng lớn thì càng dễ dàng di chuyển về phía cực âm.
❌ (d) Sai. Lysine có phân tử khối lớn hơn asparagine nhưng có điện tích dương hơn nên di chuyển nhanh hơn và gần cực âm hơn.
Các nhận định đúng là (a) và (c)
⇒ Chọn đáp án A Đáp án: A
Chất G (lysine, mang điện tích dương mạnh nhất).
Chất F (dipeptide Lys-Asn, mang điện tích dương nhưng yếu hơn lysine).
Chất E (asparagine, mang điện tích bằng 0, di chuyển chậm hoặc không di chuyển).
Phân tích các nhận định:
✔️ (a) Đúng. Tại môi trường pH = 5 thì dạng tồn tại chủ yếu của lysine có tổng điện tích là +1.
❌ (b) Sai. Chất E là asparagine mang điện tích bằng 0, di chuyển chậm hoặc không di chuyển.
✔️ (c) Đúng. Điện tích dương càng lớn thì càng dễ dàng di chuyển về phía cực âm.
❌ (d) Sai. Lysine có phân tử khối lớn hơn asparagine nhưng có điện tích dương hơn nên di chuyển nhanh hơn và gần cực âm hơn.
Các nhận định đúng là (a) và (c)
⇒ Chọn đáp án A Đáp án: A
Câu 14 [309483]: Phân tử polymer nào sau đây chỉ chứa hai nguyên tố C và H?
A, Poly(vinyl acetate).
B, Polyethylene.
C, Polyacrylonitrile.
D, Poly(vinyl chloride).
Phân tích các đáp án:
❌A. Poly(vinyl acetate): [-CH2-CH(OOCCH3)-]n: chứa các nguyên tố C, H và O.
✔️B. Polyethylene: (-CH2-CH2-)n: chỉ chứa hai nguyên tố C và H.
❌C. Polyacrylonitrile: [-CH2-CH(CN)-]n: chứa các nguyên tố C, H và N.
❌D. Poly(vinyl chloride): [-CH2-CH(Cl)-]n: chứa các nguyên tố C, H và Cl.
⇒ Chọn đáp án B Đáp án: B
❌A. Poly(vinyl acetate): [-CH2-CH(OOCCH3)-]n: chứa các nguyên tố C, H và O.
✔️B. Polyethylene: (-CH2-CH2-)n: chỉ chứa hai nguyên tố C và H.
❌C. Polyacrylonitrile: [-CH2-CH(CN)-]n: chứa các nguyên tố C, H và N.
❌D. Poly(vinyl chloride): [-CH2-CH(Cl)-]n: chứa các nguyên tố C, H và Cl.
⇒ Chọn đáp án B Đáp án: B
Câu 15 [706081]: Khi hoà tan zinc(II) chloride trong nước diễn ra một số quá trình cơ bản sau:
Zn2+(aq) + 6H2O(l) → [Zn(OH2)6]2+(aq) (I)
[Zn(OH2)6]2+(aq) ⇌ [Zn(OH)(OH2)5]+(aq) + H+(aq); KC = 10–9 (II)
H+(aq) + H2O(l) → H3O+(aq) (III)
Cho các phát biểu sau:
(1) Quá trình (I) và (III) có thể diễn ra yếu hơn quá trình (II).
(2) Từ quá trình (II) có thể suy ra “[Zn(OH2)6]2+ là acid theo Arrhenius”.
(3) Từ quá trình (III) có thể suy ra “H2O là base theo Brønsted–Lowry”.
(4) Từ quá trình (I), (II) và (III) suy ra “trong nước, cation Zn2+ là acid theo Brønsted–Lowry”.
(5) Dung dịch zinc(II) chloride có tính acid khá mạnh.
(6) Trong dung dịch zinc(II) chloride, nước vừa là dung môi, vừa đóng vai trò base theo Brønsted–Lowry.
Số phát biểu đúng là:
Zn2+(aq) + 6H2O(l) → [Zn(OH2)6]2+(aq) (I)
[Zn(OH2)6]2+(aq) ⇌ [Zn(OH)(OH2)5]+(aq) + H+(aq); KC = 10–9 (II)
H+(aq) + H2O(l) → H3O+(aq) (III)
Cho các phát biểu sau:
(1) Quá trình (I) và (III) có thể diễn ra yếu hơn quá trình (II).
(2) Từ quá trình (II) có thể suy ra “[Zn(OH2)6]2+ là acid theo Arrhenius”.
(3) Từ quá trình (III) có thể suy ra “H2O là base theo Brønsted–Lowry”.
(4) Từ quá trình (I), (II) và (III) suy ra “trong nước, cation Zn2+ là acid theo Brønsted–Lowry”.
(5) Dung dịch zinc(II) chloride có tính acid khá mạnh.
(6) Trong dung dịch zinc(II) chloride, nước vừa là dung môi, vừa đóng vai trò base theo Brønsted–Lowry.
Số phát biểu đúng là:
A, 2.
B, 3.
C, 4.
D, 5.
Phân tích các phát biểu :
❌(1) – Sai. vì quá trình (II) xảy ra không hoàn toàn (thuận nghịch)
✔️(2) – Đúng. Trong dung dịch [Zn(OH2)6]2+ phân li ra H+ nên coi là acid theo Arrhenius.
✔️(3) – Đúng. Thuyết bronsted – Lowry: Acid là chất cho proton (H+), base là chất nhận proton. Acid và base có thể là phân tử hoặc ion.H2O nhận H+ nên là base.
✔️(4) – Đúng. Từ quá trình (I), (II) và (III) suy ra "trong nước, cation Zn2+ là acid theo Bronsted-Lowry", Zn2+ là chất nhường proton (H+)
❌(5) – Sai. Hằng số cân bằng của quá trình phân li nhỏ 10-9 nên phân lí ra lượng H+ nhỏ tính acid yếu.
✔️(6) – Đúng. Trong dung dịch zinc (II) chloride, nước vừa là dung môi (môi trường điện li), vừa đóng vai trò base (chất nhận proton) theo Bronsted-Lowry.
Có 4 phát biểu đúng.
⟹Chọn đáp án C Đáp án: C
❌(1) – Sai. vì quá trình (II) xảy ra không hoàn toàn (thuận nghịch)
✔️(2) – Đúng. Trong dung dịch [Zn(OH2)6]2+ phân li ra H+ nên coi là acid theo Arrhenius.
✔️(3) – Đúng. Thuyết bronsted – Lowry: Acid là chất cho proton (H+), base là chất nhận proton. Acid và base có thể là phân tử hoặc ion.H2O nhận H+ nên là base.
✔️(4) – Đúng. Từ quá trình (I), (II) và (III) suy ra "trong nước, cation Zn2+ là acid theo Bronsted-Lowry", Zn2+ là chất nhường proton (H+)
❌(5) – Sai. Hằng số cân bằng của quá trình phân li nhỏ 10-9 nên phân lí ra lượng H+ nhỏ tính acid yếu.
✔️(6) – Đúng. Trong dung dịch zinc (II) chloride, nước vừa là dung môi (môi trường điện li), vừa đóng vai trò base (chất nhận proton) theo Bronsted-Lowry.
Có 4 phát biểu đúng.
⟹Chọn đáp án C Đáp án: C
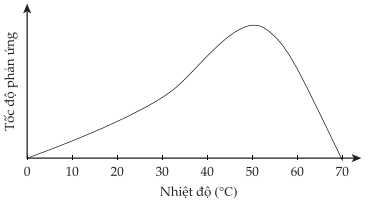
Câu 16 [706259]: Hầu hết những phản ứng sinh hoá xảy ra nhờ sự xúc tác của các enzyme. Biểu đồ dưới đây thể hiện tốc độ của một phản ứng sinh hoá do enzyme X làm xúc tác theo nhiệt độ:

A, 0 oC.
B, 50 oC.
C, 60 oC.
D, 70 oC.
Biểu đồ cho thấy tốc độ phản ứng tăng dần khi nhiệt độ tăng từ 0oC đến khoảng 50oC.
Tốc độ phản ứng đạt cực đại ở khoảng 50oC.
Sau đó, tốc độ phản ứng giảm nhanh khi nhiệt độ tiếp tục tăng.
⟹ Chọn đáp án B Đáp án: B
Tốc độ phản ứng đạt cực đại ở khoảng 50oC.
Sau đó, tốc độ phản ứng giảm nhanh khi nhiệt độ tiếp tục tăng.
⟹ Chọn đáp án B Đáp án: B
PHẦN II. Thí sinh trả lời từ câu 1 đến câu 4. Trong mỗi ý a), b), c), d) ở mỗi câu, thí sinh chọn đúng hoặc sai.
Câu 17 [706207]: Nếu chỉ đưa vào hệ ban đầu các hạt A, sơ đồ biểu diễn hệ ở trạng thái cân bằng là
A, sơ đồ (a).
B, sơ đồ (b).
C, sơ đồ (c).
D, sơ đồ (d).
Nếu ban đầu hệ chỉ gồm các hạt A, khi đạt đến trạng thái cân bằng có KC = 10, tại cân bằng sẽ có 10 hạt B ứng với 1 hạt A . Sơ đồ phù hợp là sơ đồ (a)
So sánh các sơ đồ:
(a) : chênh lệch nồng độ lớn B >> A
(b) : chỉ có A , không có B
(c) : phù hợp
(d) : chênh lệch nồng độ lớn A >> B
Sơ đồ phù hợp là sơ đồ (a)
⟹ Chọn đáp án A Đáp án: A
So sánh các sơ đồ:
(a) : chênh lệch nồng độ lớn B >> A
(b) : chỉ có A , không có B
(c) : phù hợp
(d) : chênh lệch nồng độ lớn A >> B
Sơ đồ phù hợp là sơ đồ (a)
⟹ Chọn đáp án A Đáp án: A
Câu 18 [706208]: Giả sử cho vào hệ ban đầu 10 hạt A và 2 hạt B thì tổng số hạt trong hệ khi hệ đạt trạng thái cân bằng là
A, 2.
B, 3.
C, 6.
D, 12.
A(g) ⥤ B(g)
Từ PTHH cứ 1 hạt A phản ứng hình thành 1 hạt B
→ Tổng số hạt của hệ trước và sau phản ứng không đổi
Tổng số hạt là 10 + 2 = 12 hạt
⟹ Chọn đáp án D Đáp án: D
Từ PTHH cứ 1 hạt A phản ứng hình thành 1 hạt B
→ Tổng số hạt của hệ trước và sau phản ứng không đổi
Tổng số hạt là 10 + 2 = 12 hạt
⟹ Chọn đáp án D Đáp án: D
PHẦN II. Thí sinh trả lời từ câu 1 đến câu 4. Trong mỗi ý a), b), c), d) ở mỗi câu, thí sinh chọn đúng hoặc sai.
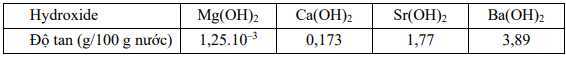
Câu 19 [704378]: Các kim loại nhóm IIA (trừ beryllium) phản ứng với nước tạo ra khí hydrogen và hydroxide kim loại. Mức độ của phản ứng này thường liên quan đến độ tan của hydroxide tạo thành: hydroxide có độ tan lớn hơn thì phản ứng của kim loại đó với nước thuận lợi hơn. Độ tan trong nước của các hydroxide nhóm IIA ở 20 °C cho trong bảng sau:

Phân tích các phát biểu:
❌ a. Sai. Phản ứng tổng quát với nước của kim loại nhóm IIA (trừ Be) là: M + 2H2O → M(OH)2 + H2.
Beryllium không phản ứng với nước, kể cả khi đun nóng.
✔️ b. Đúng. Dựa vào bảng độ tan trên, thấy độ tan của các hydroxide nhóm IIA tăng dần từ Mg(OH)2 đến Ba(OH)2.
❌ c. Sai. Mức độ của phản ứng với nước thường liên quan đến độ tan của hydroxide tạo thành: hydroxide
có độ tan lớn hơn thì phản ứng của kim loại đó với nước thuận lợi hơn nên bọt khí xuất hiện nhanh nhất trên bề mặt kim loại Ba.
❌ d. Sai. Có 3 kim loại (Ca, Sr, Ba) đều phản ứng nhanh với nước ở nhiệt độ thường.
❌ a. Sai. Phản ứng tổng quát với nước của kim loại nhóm IIA (trừ Be) là: M + 2H2O → M(OH)2 + H2.
Beryllium không phản ứng với nước, kể cả khi đun nóng.
✔️ b. Đúng. Dựa vào bảng độ tan trên, thấy độ tan của các hydroxide nhóm IIA tăng dần từ Mg(OH)2 đến Ba(OH)2.
❌ c. Sai. Mức độ của phản ứng với nước thường liên quan đến độ tan của hydroxide tạo thành: hydroxide
có độ tan lớn hơn thì phản ứng của kim loại đó với nước thuận lợi hơn nên bọt khí xuất hiện nhanh nhất trên bề mặt kim loại Ba.
❌ d. Sai. Có 3 kim loại (Ca, Sr, Ba) đều phản ứng nhanh với nước ở nhiệt độ thường.
Câu 20 [705410]: Có ba chất hữu cơ A, B và C là ba đồng phân cấu tạo của nhau. Trên phổ IR, A và B có tín hiệu đặc trưng ở vùng 1 740 – 1 670 cm–1; C có tín hiệu đặc trưng ở vùng 3 650 – 3 200 cm–1. A là hợp chất đơn chức và có phản ứng với thuốc thử Tollens, còn B thì không. Bằng các kĩ thuật phổ hiện đại, người ta thấy rằng trong phân tử của A có 6 nguyên tử hydrogen và 3 nguyên tử carbon.
Trên phổ IR, A và B có tín hiệu đặc trưng ở vùng 1 740 − 1 670 cm−1 nên A và B là hợp chất carbonyl.
C có tín hiệu đặc trưng ở vùng 3 650 − 3 200 cm−1 nên C là hợp chất alcohol. A là aldehyde đơn chức nên phân tử A chỉ có 1 nguyên tử oxygen. Vậy A, B và C có cùng công thức phân tử C3H6O.
Vì A là aldehyde và B là ketone nên A và B có công thức như sau:
A: CH3CH2CHO (propanal)
B: CH3COCH3 (acetone hay propanone)
C là alcohol nên C có công thức: CH2=CHCH2OH.
Phân tích các phát biểu:
✔️ a) Đúng. A, B, C là đồng phân cấu tạo nên chúng có cùng công thức phân tử.
✔️ b) Đúng. A là aldehyde (C=O), B là ketone (C=O). Cả hai đều có tín hiệu đặc trưng của liên kết C=O trong vùng 1 740 – 1 670 cm−1.
✔️ c) Đúng. C có công thức là CH2=CHCH2OH nên C có chứa 1 nhóm chức OH và 1 liên kết C=C.
❌ d) Sai. Khử C bằng H2 xúc tác Ni thu được CH3CH2CH2OH, sau đó oxi hóa bằng CuO sẽ thu được chất A là CH3CH2CHO
CH2=CHCH2OH + H2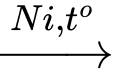 CH3CH2CH2OH
CH3CH2CH2OH
CH3CH2CH2OH + CuO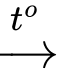 CH3CH2CHO + Cu + H2O
CH3CH2CHO + Cu + H2O
C có tín hiệu đặc trưng ở vùng 3 650 − 3 200 cm−1 nên C là hợp chất alcohol. A là aldehyde đơn chức nên phân tử A chỉ có 1 nguyên tử oxygen. Vậy A, B và C có cùng công thức phân tử C3H6O.
Vì A là aldehyde và B là ketone nên A và B có công thức như sau:
A: CH3CH2CHO (propanal)
B: CH3COCH3 (acetone hay propanone)
C là alcohol nên C có công thức: CH2=CHCH2OH.
Phân tích các phát biểu:
✔️ a) Đúng. A, B, C là đồng phân cấu tạo nên chúng có cùng công thức phân tử.
✔️ b) Đúng. A là aldehyde (C=O), B là ketone (C=O). Cả hai đều có tín hiệu đặc trưng của liên kết C=O trong vùng 1 740 – 1 670 cm−1.
✔️ c) Đúng. C có công thức là CH2=CHCH2OH nên C có chứa 1 nhóm chức OH và 1 liên kết C=C.
❌ d) Sai. Khử C bằng H2 xúc tác Ni thu được CH3CH2CH2OH, sau đó oxi hóa bằng CuO sẽ thu được chất A là CH3CH2CHO
CH2=CHCH2OH + H2
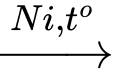 CH3CH2CH2OH
CH3CH2CH2OH
CH3CH2CH2OH + CuO
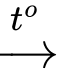 CH3CH2CHO + Cu + H2O
CH3CH2CHO + Cu + H2O
Câu 21 [704401]: Một nhóm học sinh tìm hiểu sự ảnh hưởng của nồng độ kim loại tại điện cực tới sức điện động của pin điện. Giả thuyết của nhóm học sinh đưa ra: “Nồng độ của ion kim loại trong dung dịch của bất kì điện cực nào giảm đều làm cho thế khử của điện cực đó giảm, dẫn đến sức điện động của pin giảm”. Để kiểm tra giả thuyết này, nhóm học sinh thiết lập một pin điện như hình bên dưới:
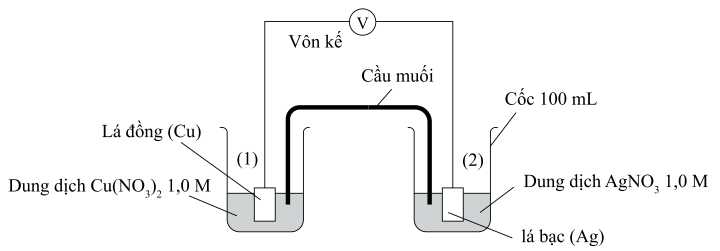
Khi pha loãng dung dịch AgNO3 tới nồng độ 0,5 M ở điện cực 2 và giữ nguyên nồng độ CuSO4 ở điện cực 1 thì thấy giá trị trên vôn kế giảm. Biết thế khử chuẩn của các điện cực:
Ag+(aq) + 1e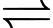 Ag(s);
Ag(s); 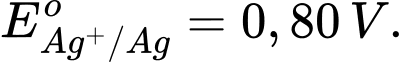
Cu2+(aq) + 2e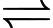 Cu(s);
Cu(s); 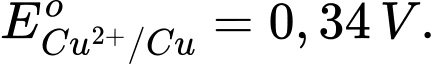

Khi pha loãng dung dịch AgNO3 tới nồng độ 0,5 M ở điện cực 2 và giữ nguyên nồng độ CuSO4 ở điện cực 1 thì thấy giá trị trên vôn kế giảm. Biết thế khử chuẩn của các điện cực:
Ag+(aq) + 1e
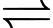 Ag(s);
Ag(s); 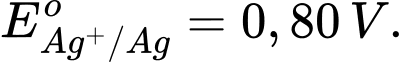
Cu2+(aq) + 2e
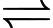 Cu(s);
Cu(s); 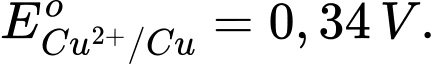
Ta có 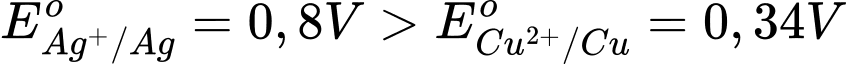
Trong pin galvani trên Ag đóng vai trò là cực dương (cathode)
Cu đóng vai trò là cực âm (anode)
Các quá trình xảy ra trong pin:
Cathode (+): Ag+ + 1e ⟶ Ag
Anode (-): Cu ⟶ Cu2+ + 2e
Phản ứng xảy ra: Cu + 2Ag+ ⟶ 2Ag + Cu2+
Phân tích các phát biểu:
✔️ (a) Đúng. Thế điện cực chuẩn của cặp Ag+/Ag (0,80) lớn hơn cặp Cu2+/Cu (0,34) nên Ag+ bị khử tại cathode.
❌ (b) Sai. Electron luôn di chuyển từ anode (Cu) sang cathode (Ag).
✔️ (c) Đúng. Cả CuSO4 1 M và Cu(NO3)2 1 M đều cung cấp ion Cu2+ với nồng độ như nhau nên không ảnh hưởng đến thế điện cực.
❌ (d) Sai. Khi pha loãng nồng độ AgNO3 thì giá trị trên vôn kế giảm nhưng nếu pha loãng nồng độ CuSO4 thì giá trị trên vôn kế lại tăng nên giả thuyết ban đầu “Nồng độ của ion kim loại trong dung dịch của bất kì điện cực nào giảm đều làm cho thế khử của điện cực đó giảm, dẫn đến sức điện động của pin giảm” là sai.
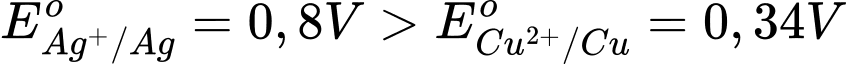
Trong pin galvani trên Ag đóng vai trò là cực dương (cathode)
Cu đóng vai trò là cực âm (anode)
Các quá trình xảy ra trong pin:
Cathode (+): Ag+ + 1e ⟶ Ag
Anode (-): Cu ⟶ Cu2+ + 2e
Phản ứng xảy ra: Cu + 2Ag+ ⟶ 2Ag + Cu2+
Phân tích các phát biểu:
✔️ (a) Đúng. Thế điện cực chuẩn của cặp Ag+/Ag (0,80) lớn hơn cặp Cu2+/Cu (0,34) nên Ag+ bị khử tại cathode.
❌ (b) Sai. Electron luôn di chuyển từ anode (Cu) sang cathode (Ag).
✔️ (c) Đúng. Cả CuSO4 1 M và Cu(NO3)2 1 M đều cung cấp ion Cu2+ với nồng độ như nhau nên không ảnh hưởng đến thế điện cực.
❌ (d) Sai. Khi pha loãng nồng độ AgNO3 thì giá trị trên vôn kế giảm nhưng nếu pha loãng nồng độ CuSO4 thì giá trị trên vôn kế lại tăng nên giả thuyết ban đầu “Nồng độ của ion kim loại trong dung dịch của bất kì điện cực nào giảm đều làm cho thế khử của điện cực đó giảm, dẫn đến sức điện động của pin giảm” là sai.
Câu 22 [705560]: Thử nghiệm một số thí nghiệm với chất rắn tinh thể màu trắng X, kết quả được đưa ra trong bảng sau:
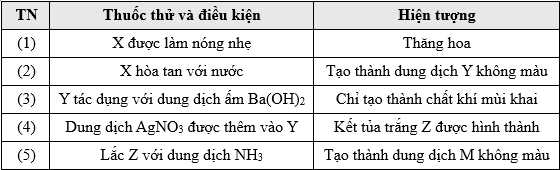

X hòa tan trong nước tạo dung dịch Y không màu, Y tác dụng với Ba(OH)2 tạo khí có mùi khai là NH3.
→ X là muối ammonium.
Dung dịch Y tác dụng với dung dịch AgNO3 tạo thành kết tủa trắng
→ Muối X có gốc Cl-
→ Công thức của muối muối X là NH4Cl
Phân tích các phát biểu:
❌ (a) Sai. X bị thăng hoa và phân hủy tạo thành NH3 và HCl.

✔️ (b) Đúng. Kết tủa trắng Z là AgCl
NH4Cl + AgNO3 → AgCl↓ + NH4NO3
✔️ (c) Đúng. Dung dịch M chứa phức chất [Ag(NH3)2]Cl.
AgCl + NH3 + H2O → [Ag(NH3)2](OH) + HCl
❌ (d) Sai. Từ thí nghiệm (3) chưa thể kết luận dung dịch Y không chứa anion SO42- hoặc NO3-. Vì với anion SO42- tạo kết tủa trắng với Ag+.
→ X là muối ammonium.
Dung dịch Y tác dụng với dung dịch AgNO3 tạo thành kết tủa trắng
→ Muối X có gốc Cl-
→ Công thức của muối muối X là NH4Cl
Phân tích các phát biểu:
❌ (a) Sai. X bị thăng hoa và phân hủy tạo thành NH3 và HCl.

✔️ (b) Đúng. Kết tủa trắng Z là AgCl
NH4Cl + AgNO3 → AgCl↓ + NH4NO3
✔️ (c) Đúng. Dung dịch M chứa phức chất [Ag(NH3)2]Cl.
AgCl + NH3 + H2O → [Ag(NH3)2](OH) + HCl
❌ (d) Sai. Từ thí nghiệm (3) chưa thể kết luận dung dịch Y không chứa anion SO42- hoặc NO3-. Vì với anion SO42- tạo kết tủa trắng với Ag+.
PHẦN III. Thí sinh trả lời từ câu 1 đến 6. Thí sinh điền kết quả mỗi câu vào mỗi ô trả lời tương ứng theo hướng dẫn của phiếu trả lời.
Câu 23 [704188]: Lên men glucose để điều chế ethyl alcohol (khối lượng riêng của ethyl alcohol nguyên chất là 0,8 g/mL), hiệu suất phản ứng lên men ethyl alcohol là 80%. Để thu được 100 lít rượu vang 12° thì khối lượng glucose cần dùng?
Đổi 100 L = 100000 mL
Khối lượng ethanol trong rượu là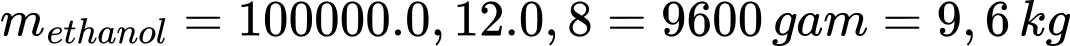
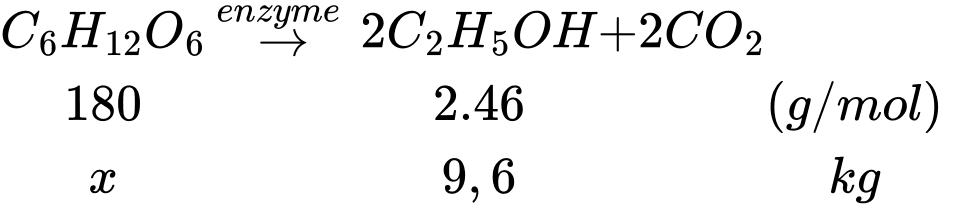
Khối lượng glucose cần dùng là:
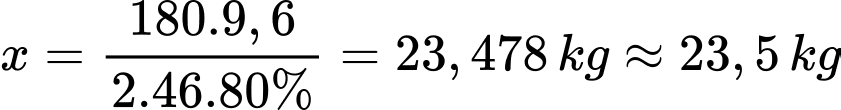
⇒ Điền đáp án: 23,5
Khối lượng ethanol trong rượu là
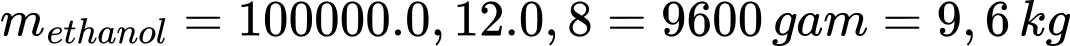
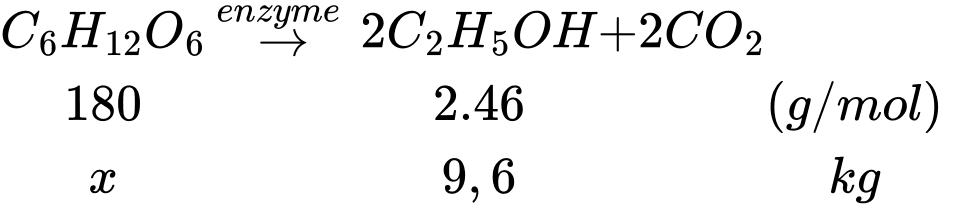
Khối lượng glucose cần dùng là:
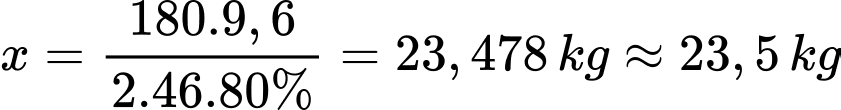
⇒ Điền đáp án: 23,5
Câu 24 [704310]: Chất béo P có công thức cấu tạo như sau:
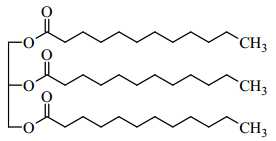
Cho P phản ứng với dung dịch NaOH, sản phẩm thu được có chứa muối sodium duy nhất của một acid béo. Phân tử khối của acid béo này là bao nhiêu?

Cho P phản ứng với dung dịch NaOH, sản phẩm thu được có chứa muối sodium duy nhất của một acid béo. Phân tử khối của acid béo này là bao nhiêu?
Chất béo P trên là triester của glycerol với acid béo C11H23COOH
Phân tử khối của acid béo là 200 gam/mol.
⇒ Điền đáp án: 200
Phân tử khối của acid béo là 200 gam/mol.
⇒ Điền đáp án: 200
Câu 25 [705819]: Cho 4 dung dịch riêng biệt sau: (a) Fe2(SO4)3; (b) H2SO4 loãng; (c) CuSO4; (d) H2SO4 loãng có lẫn CuSO4. Nhúng vào mỗi dung dịch thanh Zn nguyên chất. Số trường hợp xuất hiện ăn mòn điện hóa là
Ăn mòn điện hóa xảy ra khi có các điều kiện sau:
- Có hai chất dẫn điện khác nhau (kim loại hoặc phi kim) tiếp xúc trực tiếp hoặc gián tiếp qua dung dịch điện ly.
- Có môi trường điện ly (dung dịch chứa ion).
- Có sự chênh lệch điện thế giữa hai chất dẫn điện, dẫn đến dòng electron di chuyển.
Phân tích các trường hợp:
(a) Fe2(SO4)3 : có phản ứng:
Zn + 2Fe3+ ⟶ Zn2+ + 2Fe2+
Fe2+ tiếp tục bị khử thành Fe kim loại bám lên Zn, sẽ tạo thành cặp điện cực Zn - Fe trong dung dịch điện ly → Xảy ra ăn mòn điện hóa.
(b) H2SO4 loãng : Chỉ có một kim loại tham gia, không hình thành cặp điện cực → Không có ăn mòn điện hóa.
Zn + H2SO4 ⟶ ZnSO4 + H2
(c) CuSO4: (Cu) bám lên Zn, tạo thành cặp điện cực Zn - Cu → Xảy ra ăn mòn điện hóa.
Zn + Cu2+ ⟶ Zn2+ + Cu
(d) H2SO4 loãng lẫn CuSO4 : Cu kết tủa trên bề mặt Zn, tạo thành cặp điện cực Zn - Cu trong môi trường điện ly → Xảy ra ăn mòn điện hóa.
Có 3 trường hợp xảy ra ăn mòn điện hóa là : a, c, d
Điền đáp án: 3
- Có hai chất dẫn điện khác nhau (kim loại hoặc phi kim) tiếp xúc trực tiếp hoặc gián tiếp qua dung dịch điện ly.
- Có môi trường điện ly (dung dịch chứa ion).
- Có sự chênh lệch điện thế giữa hai chất dẫn điện, dẫn đến dòng electron di chuyển.
Phân tích các trường hợp:
(a) Fe2(SO4)3 : có phản ứng:
Zn + 2Fe3+ ⟶ Zn2+ + 2Fe2+
Fe2+ tiếp tục bị khử thành Fe kim loại bám lên Zn, sẽ tạo thành cặp điện cực Zn - Fe trong dung dịch điện ly → Xảy ra ăn mòn điện hóa.
(b) H2SO4 loãng : Chỉ có một kim loại tham gia, không hình thành cặp điện cực → Không có ăn mòn điện hóa.
Zn + H2SO4 ⟶ ZnSO4 + H2
(c) CuSO4: (Cu) bám lên Zn, tạo thành cặp điện cực Zn - Cu → Xảy ra ăn mòn điện hóa.
Zn + Cu2+ ⟶ Zn2+ + Cu
(d) H2SO4 loãng lẫn CuSO4 : Cu kết tủa trên bề mặt Zn, tạo thành cặp điện cực Zn - Cu trong môi trường điện ly → Xảy ra ăn mòn điện hóa.
Có 3 trường hợp xảy ra ăn mòn điện hóa là : a, c, d
Điền đáp án: 3
Câu 26 [706231]: Reppe Carbonylation là một phương pháp tổng hợp acrylic acid từ acetylene và CO với xúc tác Ni(CO)4, nhiệt độ 50 – 100oC, áp suất 10 – 20 atm.
HC≡CH + CO + H2O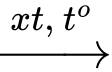 CH2=CH–COOH
CH2=CH–COOH
Trong các quá trình công nghiệp, khí CO sẽ thu từ phản ứng khí than ướt:
C + H2O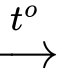 CO + H2
CO + H2
Giả sử có 150 g than (chứa 96% C), hiệu suất của phản ứng khí than ướt là 60% và lượng acetylene thu được là từ 260 g đất đèn (chứa 85% CaC2):
CaC2 + H2O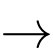 Ca(OH)2 + HC≡CH
Ca(OH)2 + HC≡CH
Hãy cho biết lượng acrylic acid (tính theo gam) có thể thu được nếu hiệu suất tổng hợp của phản ứng là 75% (làm tròn đến hàng đơn vị).
HC≡CH + CO + H2O
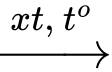 CH2=CH–COOH
CH2=CH–COOH Trong các quá trình công nghiệp, khí CO sẽ thu từ phản ứng khí than ướt:
C + H2O
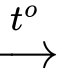 CO + H2
CO + H2 Giả sử có 150 g than (chứa 96% C), hiệu suất của phản ứng khí than ướt là 60% và lượng acetylene thu được là từ 260 g đất đèn (chứa 85% CaC2):
CaC2 + H2O
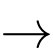 Ca(OH)2 + HC≡CH
Ca(OH)2 + HC≡CH Hãy cho biết lượng acrylic acid (tính theo gam) có thể thu được nếu hiệu suất tổng hợp của phản ứng là 75% (làm tròn đến hàng đơn vị).
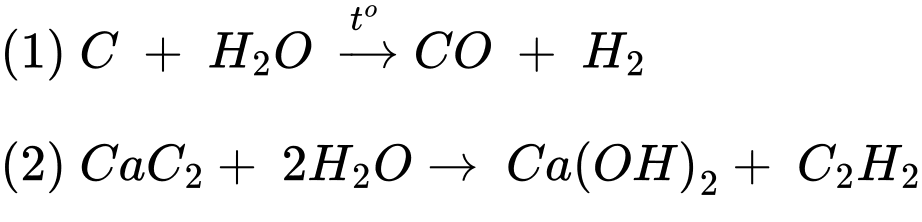
Khối lượng carbon là mC = 150 × 96% = 144 gam
Số mol của C là nC = 144 ÷ 12 = 12 mol
Theo phương trình số mol của CO là nCO = 12 × 60% = 7,2 mol
Số mol của CaC2 là
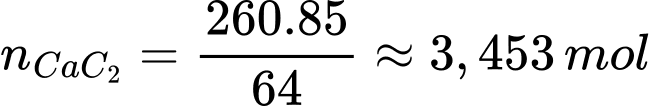
Theo phương trình số mol của C2H2 là 3,453 mol
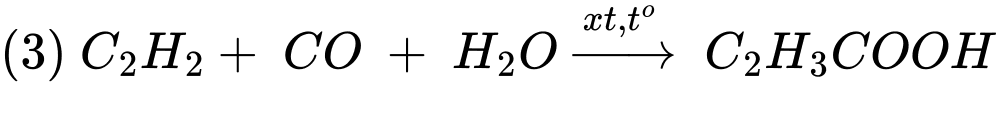
Ta có số mol của CO và C2H2 lần lượt là 7,2 mol và 3,453 mol
Khối lượng của acrylic acid là mC2H3COOH = 3,453 × 72 × 75% ≈ 186 gam
⟹ Điền đáp án: 186
Câu 27 [705451]: Muối Fe2(SO4)3 khi tan trong nước sẽ phân li thành các ion Fe3+ và SO42–. Môi trường của dung dịch có tính acid do quá trình hình thành H3O+:
Fe3+(aq) + nH2O(l) → [Fe(OH2)6](aq)
[Fe(OH2)6](aq) + nH2O(l) → [Fe(OH)n(OH2)6-n]p+(aq) + nH3O+(aq)
Nếu điện tích của phức chất [Fe(OH)n(OH2)6-n]p+ là 1+ thì giá trị của n là bao nhiêu?
Fe3+(aq) + nH2O(l) → [Fe(OH2)6](aq)
[Fe(OH2)6](aq) + nH2O(l) → [Fe(OH)n(OH2)6-n]p+(aq) + nH3O+(aq)
Nếu điện tích của phức chất [Fe(OH)n(OH2)6-n]p+ là 1+ thì giá trị của n là bao nhiêu?
Phức chất [Fe(OH)n(OH2)6-n]p+ với ion trung tâm là Fe3+ và phối tử là OH- và phối tử trung hòa H2O.
Điện tích của phức chất [Fe(OH)n(OH2)6-n]p+ là 1+
→ +3 + [n × (-1)] + 0 = +1 → n = 2
⇒ Điền đáp án: 2
Điện tích của phức chất [Fe(OH)n(OH2)6-n]p+ là 1+
→ +3 + [n × (-1)] + 0 = +1 → n = 2
⇒ Điền đáp án: 2
Câu 28 [705416]: Trong quá trình bảo quản, một phần Fe2+ trong muối FeSO4.7H2O bị oxygen oxi hoá thành Fe3+ (chất X). Lấy 1,12 g X đem hòa vào 10,0 mL dung dịch H2SO4 1,00 M thu được dung dịch Y. Chia Y thành hai phần bằng nhau:
Phần 1. Thêm nước vào thu được 100 mL dung dịch Y1. Lượng Fe2+ trong 10,0 mL dung dịch Y1 phản ứng vừa đủ với 1,85 mL dung dịch KMnO4 0,02 M.
Phần 2. Cho qua cột chứa Zn (Hg) để khử hoàn toàn ion Fe3+ thành ion Fe2+, thêm tiếp 5 mL dung dịch H2SO4 1M và nước vào dung dịch sau khi qua cột đến 100,0 mL (dung dịch Y2). Lượng Fe trong 10,00 mL Y2 phản ứng vừa đủ với 4,0 mL dung dịch KMnO4 0,01 М.
Xác định % iron(II) đã bị oxygen trong không khí oxi hoá thành iron(III). (Làm tròn kết quả đến hàng phần mười)
Phần 1. Thêm nước vào thu được 100 mL dung dịch Y1. Lượng Fe2+ trong 10,0 mL dung dịch Y1 phản ứng vừa đủ với 1,85 mL dung dịch KMnO4 0,02 M.
Phần 2. Cho qua cột chứa Zn (Hg) để khử hoàn toàn ion Fe3+ thành ion Fe2+, thêm tiếp 5 mL dung dịch H2SO4 1M và nước vào dung dịch sau khi qua cột đến 100,0 mL (dung dịch Y2). Lượng Fe trong 10,00 mL Y2 phản ứng vừa đủ với 4,0 mL dung dịch KMnO4 0,01 М.
Xác định % iron(II) đã bị oxygen trong không khí oxi hoá thành iron(III). (Làm tròn kết quả đến hàng phần mười)
Đổi 4 mL = 0,004 L; 1,85 mL = 0,00185 L
Zn + 2Fe3+ ⟶ 2Fe2+ + Zn2+
10FeSO4 + 2KMnO4 + 8H2SO4 ⟶ 5Fe2(SO4)3 + K2SO4 + 2MnSO4 + 8H2O
Phần 1:
Số mol của KMnO4 phản ứng là: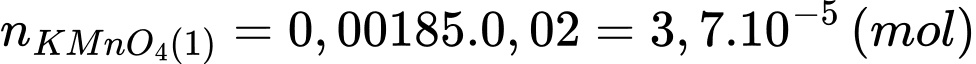
Số mol của Fe2+ trong phần 1 đã phản ứng là: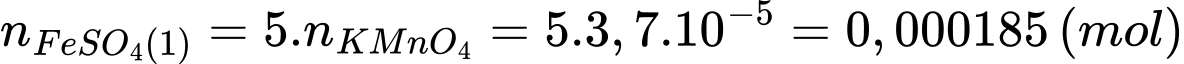
Tổng số mol Fe2+ trong phần 1 là: nFe2+ = 0,000185 × 10 = 1,85 × 10-3 (mol)
Phần 2: toàn bộ Fe3+ đã được chuyển hóa thành Fe2+
Số mol của KMnO4 phản ứng là: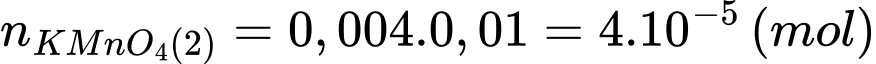
Số mol của Fe2+ trong phần 2 đã phản ứng là: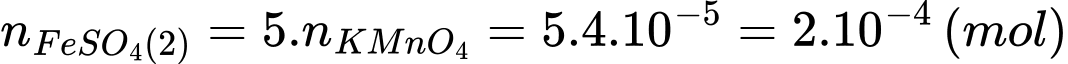
Tổng số mol Fe2+ (kể cả lượng được chuyển hóa từ Fe3+) trong phần 2 là: nFe2+ = 2.10-4 × 10 = 2 × 10-3 (mol)
→ Lượng Fe3+ đã chuyển hóa thành Fe2+ là:
2 × 10-3 – 1,85 × 10-3 = 1,5 × 10-4 (mol)
Phần trăm Fe2+ bị oxi hóa thành Fe3+ là:
⇒ Điền đáp án: 7,5
Zn + 2Fe3+ ⟶ 2Fe2+ + Zn2+
10FeSO4 + 2KMnO4 + 8H2SO4 ⟶ 5Fe2(SO4)3 + K2SO4 + 2MnSO4 + 8H2O
Phần 1:
Số mol của KMnO4 phản ứng là:
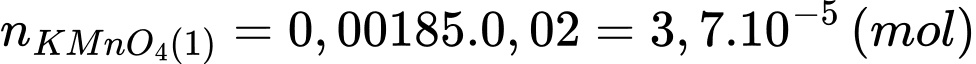
Số mol của Fe2+ trong phần 1 đã phản ứng là:
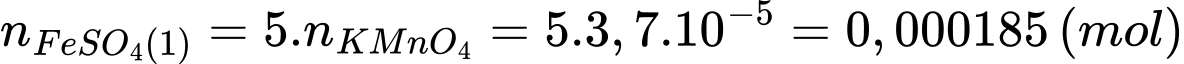
Tổng số mol Fe2+ trong phần 1 là: nFe2+ = 0,000185 × 10 = 1,85 × 10-3 (mol)
Phần 2: toàn bộ Fe3+ đã được chuyển hóa thành Fe2+
Số mol của KMnO4 phản ứng là:
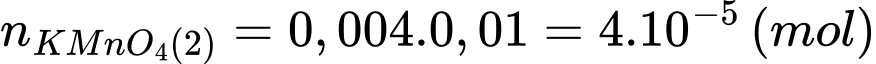
Số mol của Fe2+ trong phần 2 đã phản ứng là:
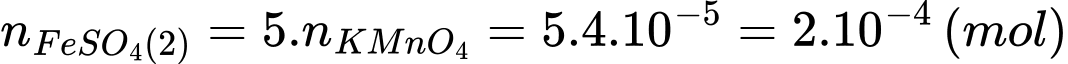
Tổng số mol Fe2+ (kể cả lượng được chuyển hóa từ Fe3+) trong phần 2 là: nFe2+ = 2.10-4 × 10 = 2 × 10-3 (mol)
→ Lượng Fe3+ đã chuyển hóa thành Fe2+ là:
2 × 10-3 – 1,85 × 10-3 = 1,5 × 10-4 (mol)
Phần trăm Fe2+ bị oxi hóa thành Fe3+ là:

⇒ Điền đáp án: 7,5