PHẦN I. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
Cấu hình electron của K (Z = 19) là: 1s22s22p63s23p64s1
- Để đạt được cấu hình electron bền vững giống khí hiếm, K có xu hướng mất đi 1 electron ở lớp ngoài cùng, thay vì nhận thêm 7 electron.Khi K mất 1 electron, nó trở thành ion dương (cation) K+, mang điện tích +1.
⇒ Chọn đáp án A
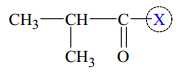
Nhóm được gắn vào vị trí X được khoanh tròn trên là
⇒ X chính là OCH3.
⇒ Chọn đáp án C Đáp án: C
⇒ Chọn đáp án D Đáp án: D
- Tại anode: xảy ra quá trình oxi hóa (nhường electron)
Ion Cl- (anion) di chuyển về anode. Phản ứng: 2Cl- → Cl2 + 2e
- Tại cathode: nơi xảy ra quá trình khử (nhận electron)
Ion Na+ (cation) di chuyển về cathode. Phản ứng: Na+ + e → Na
⟹ Chọn đáp án C Đáp án: C
✔️ B. Đúng. Phân SA được sản xuất bằng cách cho khí NH3 phản ứng với sulfuric acid H2SO4:
2NH3 + H2SO4 → (NH4)2SO4
✔️ C. Đúng. NH4+ trong phân bón khi bị hòa tan trong đất sẽ phân li ra H+ gây nên độ chua của đất.
NH4+ ⇌ NH3 + H+
❌ D. Sai. Do dễ làm đất bị chua nên phân SA không phù hợp với các loại đất chua hoặc ngập mặn.
⇒ Chọn đáp án D Đáp án: D
Acid béo tạo nên chất béo thường là các monocarboxylic acid có đặc điểm:
⭐ Mạch carbon dài, không phân nhánh → phù hợp với tính chất kỵ nước và khả năng tạo ester với glycerol.
⭐ Có số nguyên tử carbon chẵn (thường từ 12 đến 24 carbon) → do quá trình sinh tổng hợp acid béo trong cơ thể diễn ra theo cơ chế gắn thêm từng cặp nguyên tử carbon (C2) từ acetyl-CoA (acetyl coenzyme A).
⇒ Chọn đáp án D Đáp án: D
Br2 + 2I- ⟶ 2Br- + I2
⟹ Chọn đáp án A Đáp án: A
Chọn đáp án B Đáp án: B
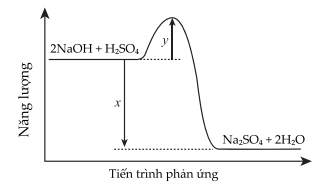
Giá trị biến thiên enthalpy của quá trình trung hòa bên trên là bao nhiêu?
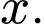
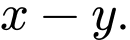
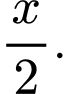
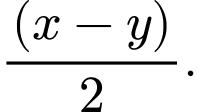
Từ sơ đồ biến thiên enthalpy của quá trình trung hòa trên là x
⇒ Chọn đáp án A Đáp án: A
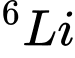 và
và 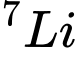 với tỉ lệ phần trăm số nguyên tử mỗi đồng vị lần lượt là 7,42 % và 92,58 %. Nguyên tử khối trung bình của mẫu lithium này (kết quả lấy đến hai chữ số thập phân) là
với tỉ lệ phần trăm số nguyên tử mỗi đồng vị lần lượt là 7,42 % và 92,58 %. Nguyên tử khối trung bình của mẫu lithium này (kết quả lấy đến hai chữ số thập phân) là - Áp dụng công thức tính nguyên tử khối trung bình:
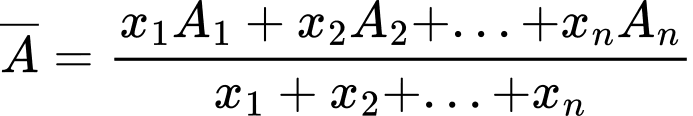
- Với A1, A2, ... là số khối của các đồng vị tương ứng (chỉ số trên trong ký hiệu nguyên tử)
- x1, x2,... là phần trăm số nguyên tử của mỗi đồng vị tương ứng.
- Vậy nguyên tử khối trung bình của mẫu lithium này là:
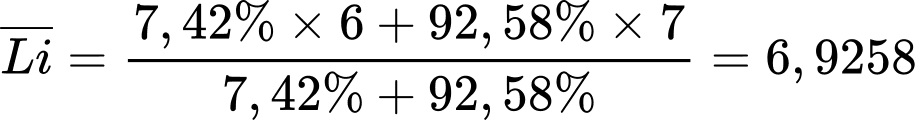
⟹ Chọn đáp án: D Đáp án: D
Potassium (K; Z = 19) thuộc nhóm IA, không phải kim loại chuyển tiếp.
⇒ Chọn đáp án C
Đáp án: C
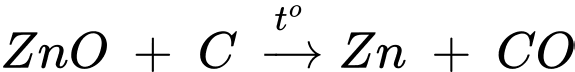
⇒ Chọn đáp án D Đáp án: D
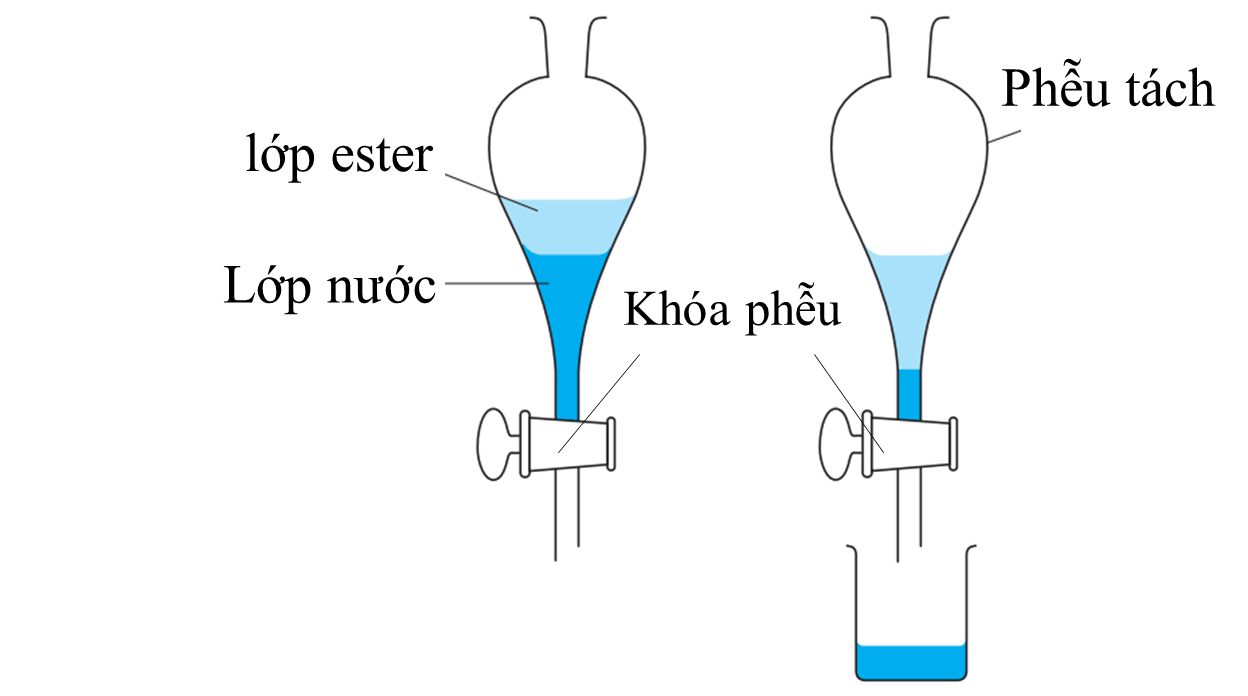
☆ Các phương pháp còn lại có thể dùng để:
✨ Chưng cất: tách 2 chất lỏng hòa tan vào nhau nhưng có nhiệt độ sôi khác nhau, ví dụ chưng cất rượu.
✨ Kết tinh: có thể tách các chất kết tinh ở những nhiệt độ khác nhau.
✨ Lọc để loại bỏ chất rắn ra khỏi dung dịch...
⟹ Chọn đáp án B Đáp án: B
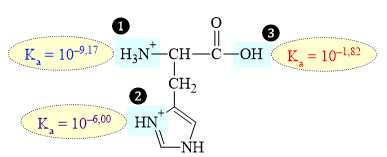
Biết rằng ion H+ đầu tiên sẽ tách ra khỏi nhóm acid mạnh nhất, sau đó là nhóm acid mạnh tiếp theo,… Sau khi tách ion H+ của nhóm nào thì tạo ra được phân tử trung hòa về điện?
Quá trình proton hóa hoàn toàn phân tử histidine được diễn ra như sau:
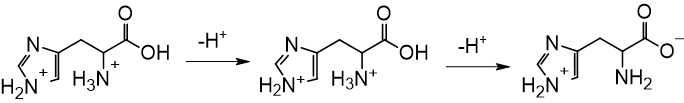
Từ đó thấy được sau khi tách ion H+ của nhóm số 2 thì tạo ra được phân tử trung hòa về điện.
⇒ Chọn đáp án B Đáp án: B
Cấu tạo của các polymer:
(1) Polybutadiene: 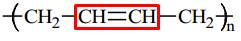
(2) Polyisoprene: 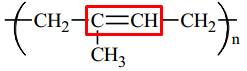
(3) Poly(methyl methacrylate): 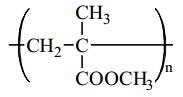
(4) Poly(vinyl chloride): 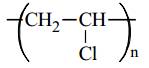
(5) Polyacrylonitrile: 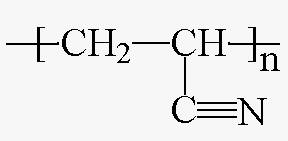
⇒ Số polymer có chứa nối đôi C=C trong phân tử là 2.
⟹ Chọn đáp án B
Sử dụng thông tin cho dưới đây để trả lời các câu số 16 – 17:
Một học sinh được cấp một pin điện tiêu chuẩn trình bày ở dưới đây. Điện cực Cu nhúng trong dung dịch Cu(NO3)2 1M và điện cực Sn nhúng trong dung dịch Sn(NO3)2 1M. Khi dòng điện chạy qua tim, học sinh xác định rằng khối lượng điện cực Cu tăng và điện cực Sn giảm khối lượng.
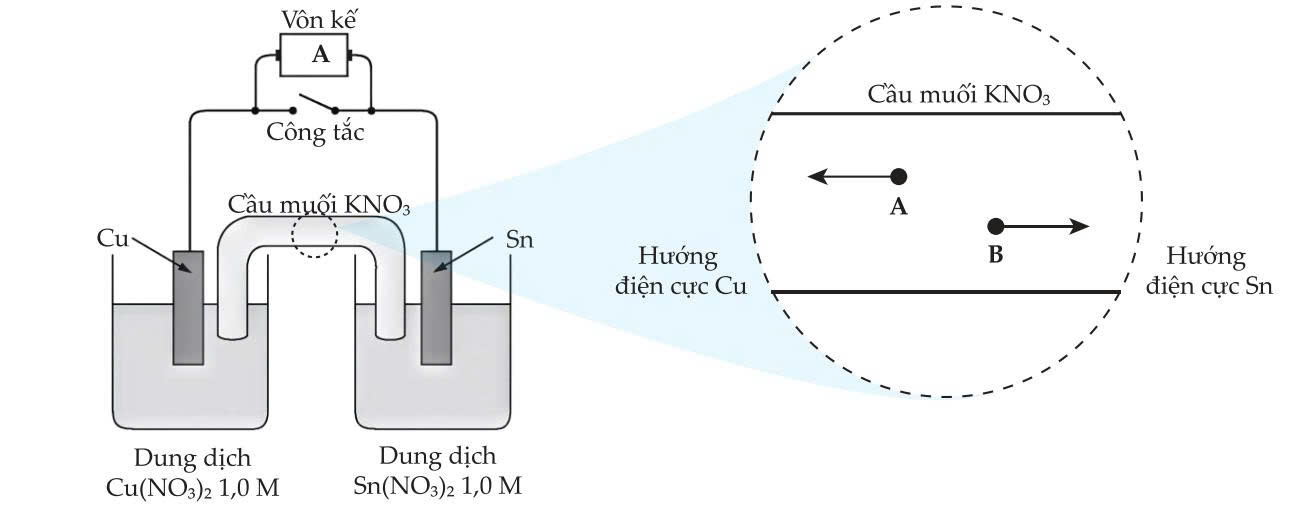
Trong khung mở rộng của phần trung tâm cầu muối được hiển thị trong sơ đồ bên dưới, quan sát thấy có các hạt A và B di chuyển ngược phía nhau về các điện cực khi pin bắt đầu hoạt động. Chú ý bỏ qua các phân tử dung môi.
Cu2+ + Sn ⟶ Cu + Sn2+
Từ phương trình hóa học: nSn = nCu = 0,15 mol
Khối lượng Sn mất đi là: mSn = 0,15 × 119 = 17,85 gam
⇒ Chọn đáp án B Đáp án: B
(i) Hạt A là hạt ion K+.
(ii) Hạt B là hạt ion NO3- .
(iii) Các electron di chuyển qua cầu muối.
(iv) Khối lượng điện cực Cu tăng lên bằng khối lượng điện cực Sn giảm đi.
(v) Khi điện cực Cu ngừng thì điện cực Sn cũng ngừng hoạt động.
Vai trò của cầu muối là trung hòa điện tích của 2 dung dịch: các ion dương Na+ hoặc K+ và Zn2+ di chuyển qua cầu muối đến cốc đựng dung dịch CuSO4. Ngược lại, các ion âm SO42- hoặc NO3- di chuyển qua cầu muối đến dung dịch ZnSO4.
Phân tích các nhận định:
✔️ (i) – Đúng. Tại điện cực Cathode mất đi cation Cu2+ nên bổ sung bằng 1 cation khác nên hạt A là hạt ion K+.
✔️ (ii) – Đúng. Tại điện cực Anode tạo ra thêm anion Sn2+ nên bổ sung bằng anion khác nên hạt B là hạt ion NO3-.
❌ (iii) – Sai. Các electron di chuyển qua dây dẫn.
❌ (iv) – Sai. Khối lượng điện cực Cu tăng lên khác khối lượng điện cực Sn giảm đi nguyên do có sự chênh lệch nguyên tử khối với tăng lên 1 mol Cu ứng với 64 gam thì sẽ giảm đi 1 mol Sn ứng với 119 gam.
✔️ (v) – Đúng. Khi điện cực Cu ngừng thì điện cực Sn cũng ngừng hoạt động.
Các phát biểu đúng là (i) (ii) (v).
⇒ Chọn đáp án C Đáp án: C
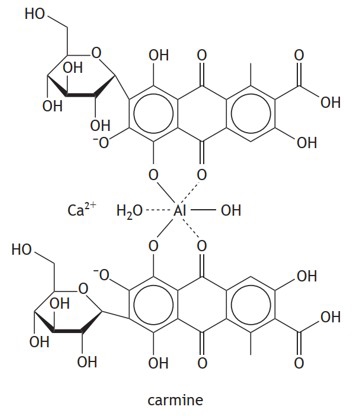
Các nhận định được đưa ra về carmine:
(1) Trong phức chất carmine, nguyên tử Al và ion Ca2+ đóng vai trò là nguyên tử trung tâm.
(2) Phối tử trong phức chất carmine có chứa phân tử glucose.
(3) Phối tử của phức chất carmine là phối tử hai càng, có khả năng liên kết với nguyên tử trung tâm thông qua 2 nguyên tử O trong phân tử.
(4) Phối tử của phức trên là hợp chất hữu cơ đa chức.
(5) Trong cấu tạo của phối tử có chứa hệ vòng anthraquinone thơm, là phần tạo nên màu đỏ đặc trưng của carmine.
Có bao nhiêu nhận định đúng?
Nhận định (1) – Sai. Phức carmine có thể chứa Al³⁺ hoặc Ca²⁺ tùy điều chế, nhưng không đồng thời cả hai làm ion trung tâm trong cùng một phức
Nhận định (2) – Đúng. Acid carminic (C₂₂H₂₀O₁₃) là một dẫn xuất anthraquinon gắn với glucose
Nhận định (3) – Sai. Ngoài phối tử hai càng (tạo liên kết phối trí qua 2 nguyên tử O), còn có phối tử đơn càng là H2O và OH-
Nhận định (4) – Sai. Acid carminic chứa nhiều nhóm chức: –COOH, –OH, carbonyl, vòng anthraquinon, đường → tạp chức
Nhận định (5) – Đúng. Anthraquinon là chromophore tạo màu đỏ đặc trưng
⟹ Chọn đáp án B. 2
PHẦN II. Thí sinh trả lời từ câu 1 đến câu 4. Trong mỗi ý a), b), c), d) ở mỗi câu, thí sinh chọn đúng hoặc sai.
▪ Phản ứng ở anode: Zn → Zn2+ + 2e.
▪ Phản ứng ở cathode: 2MnO2 + 2H+ + 2e → Mn2O3 + H2O.
▪ Phản ứng phụ: Zn2+ + 2NH4Cl → Zn(NH3)2Cl2 + 2H+.
Pin này có sức điện động 1,5 V. Đây là loại Pin đã có từ rất lâu, có giá rất rẻ, là lựa chọn tốt cho các thiết bị tiêu thụ ít điện năng (đèn pin và đồ chơi).
Sự Oxi hóa:
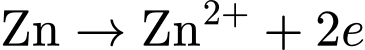 (cực âm).
(cực âm). Sự Khử:
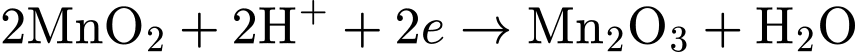 (cực dương).
(cực dương). → Sự khử xảy ra ở
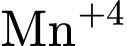 (trong
(trong  ) thành
) thành 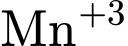 (trong
(trong 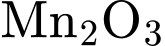 ).
).❌ Nhận định b) – Sai, vì:
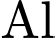 có thế điện cực rất âm, nó sẽ đóng vai trò là cực âm và bị oxi hóa mạnh mẽ, thay thế
có thế điện cực rất âm, nó sẽ đóng vai trò là cực âm và bị oxi hóa mạnh mẽ, thay thế 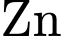 . Điều này sẽ làm thay đổi nguyên tắc hoạt động của pin Leclanché (cực dương là
. Điều này sẽ làm thay đổi nguyên tắc hoạt động của pin Leclanché (cực dương là  và
và  ). Hơn nữa,
). Hơn nữa, 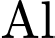 sẽ phản ứng với chất điện ly.
sẽ phản ứng với chất điện ly.✔️ Nhận định c) – Đúng, vì: Cực âm là vỏ kẽm,
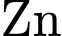 bị oxi hóa thành
bị oxi hóa thành 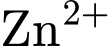 khi pin phóng điện. Khi pin để lâu, quá trình ăn mòn hóa học
khi pin phóng điện. Khi pin để lâu, quá trình ăn mòn hóa học 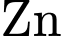 bởi
bởi  và
và 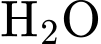 vẫn diễn ra, làm vỏ pin bị thủng (ăn mòn), gây rò rỉ và hỏng pin.
vẫn diễn ra, làm vỏ pin bị thủng (ăn mòn), gây rò rỉ và hỏng pin.✔️ Nhận định d) – Đúng, vì: Cộng ba phương trình lại, ta được phương trình tổng cộng:
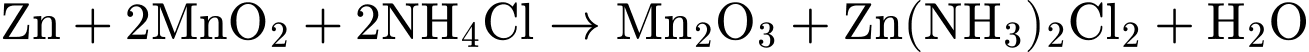 .
. ▪ Bước 1: Cho vào ống nghiệm khoảng 0,5 mL dung dịch NaOH 10 % và khoảng 0,5 mL dung dịch CuSO4 5 %, lắc đều.
▪ Bước 2: Thêm tiếp vào ống nghiệm khoảng 4 mL dung dịch saccharose 3 %, lắc đều ống nghiệm đến khi thu được dung dịch đồng nhất (nếu còn chất rắn thì thêm tiếp dung dịch saccharose).
▪ Bước 3: Đun nóng dung dịch trong ống nghiệm.
❌ a. Sai. Bước 1 không chỉ là bước điều chế Cu(OH)2 mà còn tạo môi trường kiềm ngay trong ống nghiệm. Saccharose chỉ có thể hoà tan kết tủa Cu(OH)2 trong môi trường kiềm tạo dung dịch màu xanh.
✔️ b. Đúng. Tại bước 2 đã có phản ứng của dung dịch saccharose với Cu(OH)2:
2C12H22O11 + Cu(OH)2 ⟶ [Cu(C12H21O11)2] + 2H2O
✔️ c. Đúng. Saccharose có phản ứng với Cu(OH)2 chứng tỏ phân tử saccharose có ít nhất 2 nhóm OH liền kề.
❌ d. Sai. Phân tử saccharose không có khả năng mở vòng → không có nhóm chức aldehyde nên không phản ứng Cu(OH)2/OH- để tạo được Cu2O.
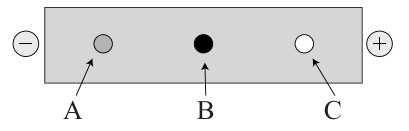
Công thức của arginine và aspatic acid được cho trong bảng
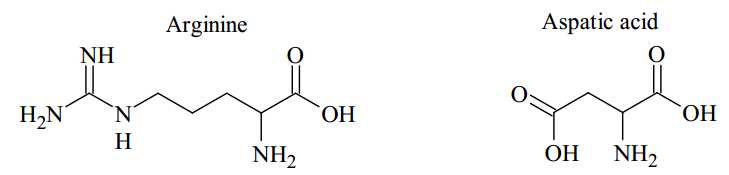
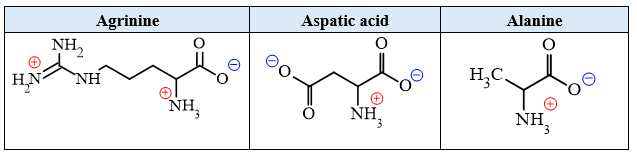
+) Aspartic acid tồn tại chủ yếu dưới dạng anion (-1) → bị kéo về cực dương → C là aspartic acid.
+) Alanine trung hòa, gần như không di chuyển trong điện trường → B là alanine.
+) Arginine tồn tại chủ yếu dưới dạng cation (+1) → bị kéo về cực âm → A là arginine.
Phân tích các phát biểu:
✔️ a) Đúng. Có thể tách riêng arginine, alanine và aspatic acid tại pH = 6 bằng phương pháp điện di vì các amino acid có điện tích khác nhau nên sẽ di chuyển về các hướng khác nhau trong điện trường.
❌ b) Sai. Tại pH = 6, A là arginine (dạng cation), C là aspartic acid (dạng anion).
✔️ c) Đúng. B (Alanine) ở dạng trung hòa nên có điện tích bằng 0 và C (Aspartic acid) mang điện tích -1.
✔️ d) Đúng. Ở pH thấp (pH = 2), môi trường có tính acid, chứa nhiều ion H+ nên arginine và aniline sẽ phản ứng với H+ để tạo thành dạng cation mang điện tích dương (+) → bị kéo về cực âm.

Biết trong thành phần của X nước chiếm 36,0% khối lượng. Trong nông nghiệp, muối X được dùng để pha chế thuốc Bordeaux dùng để diệt nấm mốc cho cây trồng. Cách pha chế 10 lít dung dịch Bordeaux 1% như sau:
▪ Bước 1: Pha 0,1 kg muối X trong 8,0 lít nước.
▪ Bước 2: Pha 0,1 kg vôi sống (CaO) trong 2,0 lít nước.
▪ Bước 3: Đổ dung địch muối X vào nước vôi, vừa đổ vừa khuấy, thu được dung dịch Bordeaux 1% ở dạng keo, màu xanh nhạt, pH = 7 – 8, độ lắng chậm.
Có: %H2O = 36% => %M2(SO4)n = 64%
Xét 0,1kg muối = 100g muối, có:
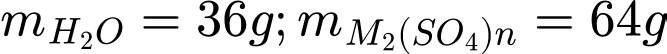 =>
=> 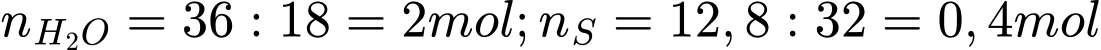 =>
=> 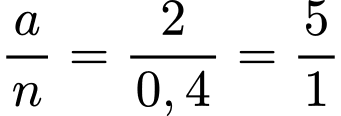
=> Trong muối có 1 phân tử
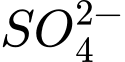 và ngậm 5 phân tử nước=> Muối có dạng:
và ngậm 5 phân tử nước=> Muối có dạng: 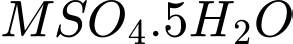 - 0,4 mol
- 0,4 mol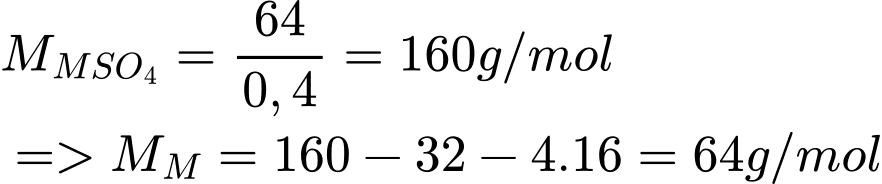 => M là: Cu (Copper)
=> M là: Cu (Copper)Vậy X có dạng:
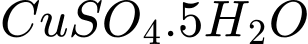
✔️Nhận định a) – Đúng, vì: Công thức của X có dạng
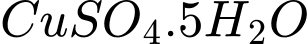 , chứa 5 phân tử nước
, chứa 5 phân tử nước✔️Nhận định b) – Đúng, vì:
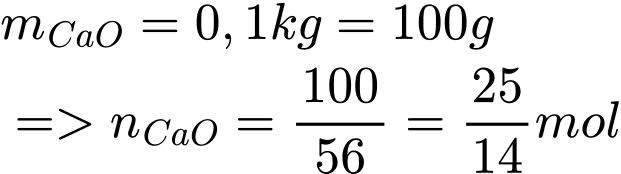
Nếu thay vôi sống (CaO) thành vôi tôi (Ca(OH)2) thì:
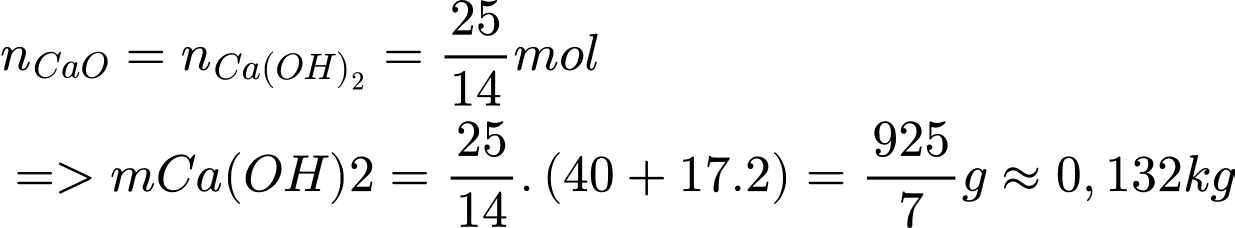
❌Nhận định c) – Sai, vì:
• Thuốc Bordeaux là hỗn hợp của
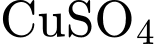 và
và 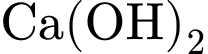 , có tính kiềm nhẹ (
, có tính kiềm nhẹ (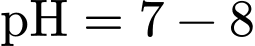 ).
).• Kim loại
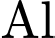 (Aluminium/Nhôm) là kim loại lưỡng tính, bị ăn mòn mạnh trong môi trường kiềm (do
(Aluminium/Nhôm) là kim loại lưỡng tính, bị ăn mòn mạnh trong môi trường kiềm (do 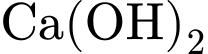 ):
): 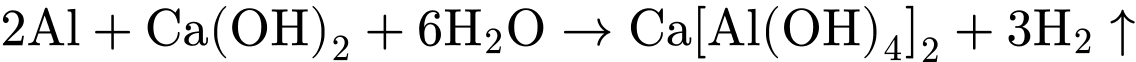
• Ngoài ra,
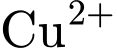 có thể bị khử bởi
có thể bị khử bởi 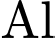 (Al có tính khử mạnh hơn
(Al có tính khử mạnh hơn
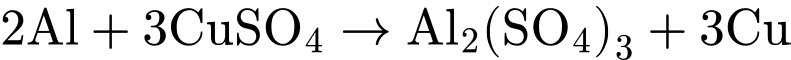
• Kim loại
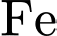 (Iron/Sắt) là kim loại có tính khử mạnh hơn
(Iron/Sắt) là kim loại có tính khử mạnh hơn  , sẽ phản ứng với
, sẽ phản ứng với 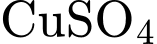 (phản ứng thế):
(phản ứng thế): 
• Do đó, cả thùng
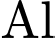 và
và 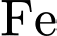 đều bị phản ứng hóa học (ăn mòn) làm hỏng thuốc và thùng.
đều bị phản ứng hóa học (ăn mòn) làm hỏng thuốc và thùng.=> Thường phải dùng thùng gỗ, nhựa hoặc thủy tinh.
❌Nhận định d) – Sai, vì: Cách pha chế tiêu chuẩn (Đổ muối vào vôi) tạo ra thuốc Bordeaux chất lượng cao, có độ dính tốt, ít bị lắng, và bền hơn.
• Nếu đổ vào dung dịch (thao tác ngược), hỗn hợp tạo thành sẽ có độ lắng cao, kém bền, và chất lượng thuốc trừ nấm không tốt bằng.
• Theo quy tắc pha chế nông nghiệp, thao tác đúng là Đổ dung dịch muối vào dung dịch vôi.
PHẦN III. Thí sinh trả lời từ câu 1 đến 6. Thí sinh điền kết quả mỗi câu vào mỗi ô trả lời tương ứng theo hướng dẫn của phiếu trả lời.
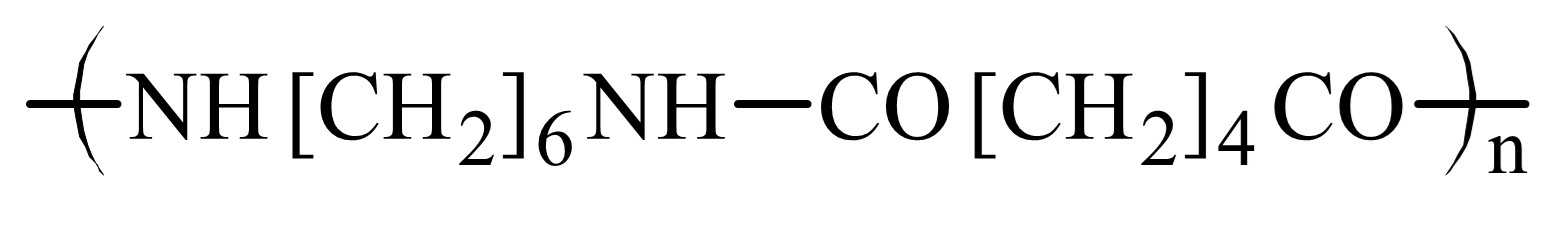
Khối lượng của một đoạn mạch tơ nylon-6,6 là 27 346 amu. Số lượng mắt xích trong đoạn mạch nylon-6,6 là bao nhiêu?
M1mắt xích = 226
Số lượng mắt xích là : 27346 : 226 = 121
⟹ Điền đáp án: 121
∎ Cation Co3+ tạo được 6 liên kết sigma kiểu cho – nhận với các phối tử.
∎ Mỗi anion C2O42– sử dụng 2 cặp electron hoá trị riêng để tạo liên kết cho – nhận với cation kim loại.
Nếu số phối tử H2O trong phức chất [Co(OH2)x(ox)y]p+ là 4 thì giá trị của p bằng bao nhiêu?
★ Co3+ (cation trung tâm) (điện tích +3) có số phối trí = 6, nghĩa là nó tạo 6 liên kết sigma kiểu cho – nhận với các phối tử.
★ Mỗi anion oxalate (C2O42-) (điện tích -2) tạo 2 liên kết cho – nhận, nên một oxalate chiếm 2 vị trí liên kết (phối tử 2 càng).
★ H2O là phối tử đơn càng (trung hòa, không mang điện tích) nên mỗi phân tử H2O chỉ chiếm 1 vị trí liên kết.
Nếu số phối tử H2O trong phức chất [Co(OH2)x(ox)y]p+ là 4, tức x = 4 và tổng số liên kết của Co3+ phải là 6 thì ta có:
x + 2 y= 6 ⇔ 4 + 2y = 6 ⇔ 2y = 2 ⇒ y=1
⟶ Phức chất có dạng [Co(OH2)4(ox)]p+.
⟶ Điện tích của phức là: p = +3 + (−2) = +1.
Vậy giá trị của p là 1.
⇒ Điền đáp án: 1
CuCO3(s) + H₂SO4(aq) + 5H2O(l) → CuSO4.5H2O(s) + H2O(I) + CO2(g)
Nhóm chuẩn bị 2,5 gam copper(II) carbonate và 45 mL sulfuric acid 1 M, sau phản ứng thu được 4,6 gam sản phẩm CuSO4.5H2O. Hiệu suất của phản ứng là bao nhiêu phần trăm?
Số mol của copper(II) carbonate là:
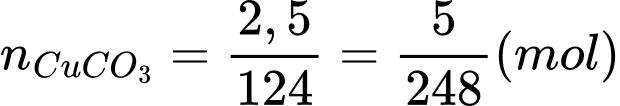
Khối lượng của CuSO4.5H2O tạo thành theo lí thuyết là:
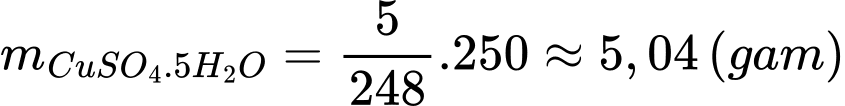
Hiệu suất của phản ứng là:
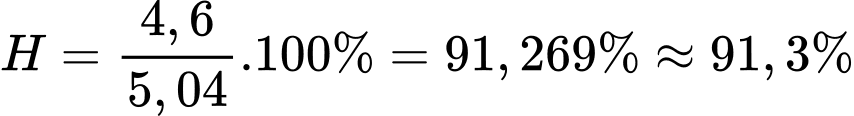
⇒ Điền đáp án: 91,3
Tính tốc độ ăn mòn trung bình của tấm kẽm theo đơn vị g/ngày (làm tròn đến hàng đơn vị).
Khối lượng của khối kẽm là mZn = 6720 × 7,13 = 47913,6 gam
Đổi 40,04 kg = 40040 gam
Khối lượng kẽm mất đi trong 30 ngày là 47913,6 – 40040 = 7873,6 gam
Tốc độ ăn mòn trung bình của tấm kẽm là v = 7873,6 ÷ 30 ≈ 262 gam/ngày
⟹ Điền đáp án: 262
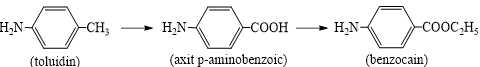
Để sản xuất một lô thuốc benzocain gồm 12500 lọ (mỗi lọ chứa 25 gam benzocain) thì cần dùng m kg toluidin. Biết hiệu suất mỗi quá trình là 75%. Giá trị của m là bao nhiêu? (kết quả làm tròn đến hàng đơn vị).
Hiệu suất mỗi quá trình là 75 % nên hiệu suất cả quá trình là: 75% × 75% = 56,25%.
Sơ đồ đơn giản hóa quá trình sản xuất benzocain từ toluidin như sau:
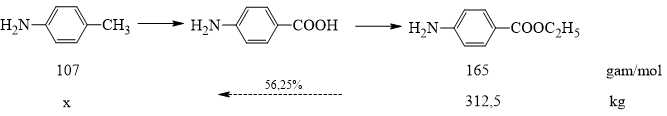
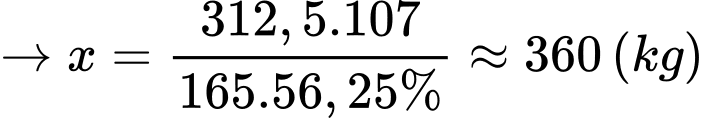
⇒ Điền đáp án: 360
Bước 1: Cân 30 gam “muối i-ốt” rồi hòa tan trong nước cất thu được 100 mL dung dịch X đựng trong bình nón 250 mL (có nút nhám) thêm dung dịch KI 1 M (dư), dung dịch H2SO4 1 M.
KIO3 + 5KI + 3H2SO4
 3K2SO4 + 3I2 + 3H2O
3K2SO4 + 3I2 + 3H2OBước 2: Đậy nắp và lắc nhanh mẫu, để mẫu yên tĩnh nơi tối 5 phút. Sau 5 phút, thêm 1 mL dung dịch hồ tinh bột 1%, rồi đem chuẩn độ chậm (4 giây một giọt) bằng dung dịch Na2S2O3 0,005 M tới khi mất màu thì thể tích dung dịch Na2S2O3 đã dùng là 11,0 mL.
I2 + 2Na2S2O3
 2NaI + Na2S4O6
2NaI + Na2S4O6Tính hàm lượng iodine (mg/kg muối) trong KIO3 của mẫu “muối i-ốt” trên (làm tròn đến hàng đơn vị)
(2) 2Na2S2O3 + I2 → Na2S4O6 + 2NaI
Đổi 11 mL = 0,011 L
Số mol Na2S2O3 đã phản ứng là nNa2S2O3 = 0,011.0,005 = 5,5.10-5 mol
Số mol I2 = nNa2S2O3 : 2 = 2,75×10−5 mol
Từ PTHH (1) và (2) số mol của KIO3 là: 11/1200000 mol
Hàm lượng iodine trong muối trên là:
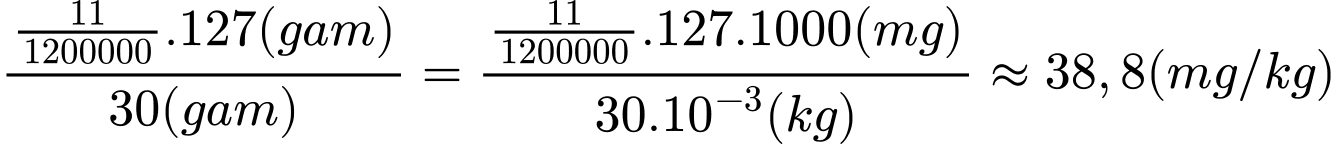
Làm tròn kết quả đến hàng đơn vị: 39mg/kg
⟹Điền đáp án : 39