PHẦN I. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
Câu 1 [241772]: Hạt nhân của nguyên tử nào có số hạt neutron là 30?
A, 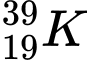 .
.
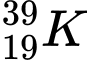 .
.B, 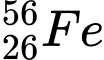 .
.
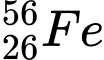 .
.C, 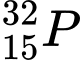 .
.
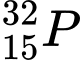 .
.D, 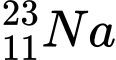 .
.
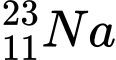 .
.
HƯỚNG DẪN GIẢI:
Số hạt neutron (N) = Số khối (A) – Số hạt proton (P).
Xét hạt nhân của các nguyên tử:
❌ A.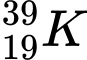 : N = 39 – 19 = 20
: N = 39 – 19 = 20
✔️ B.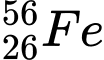 : N = 56 – 26 = 30
: N = 56 – 26 = 30
❌ C.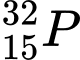 : N = 32 – 15 = 17
: N = 32 – 15 = 17
❌ D.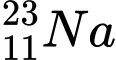 : N = 23 – 11 = 12
: N = 23 – 11 = 12
⇒ Chọn đáp án B Đáp án: B
Số hạt neutron (N) = Số khối (A) – Số hạt proton (P).
Xét hạt nhân của các nguyên tử:
❌ A.
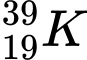 : N = 39 – 19 = 20
: N = 39 – 19 = 20✔️ B.
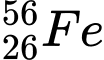 : N = 56 – 26 = 30
: N = 56 – 26 = 30❌ C.
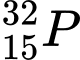 : N = 32 – 15 = 17
: N = 32 – 15 = 17❌ D.
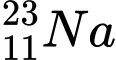 : N = 23 – 11 = 12
: N = 23 – 11 = 12⇒ Chọn đáp án B Đáp án: B
Câu 2 [190813]: C2H5COCH3 tham gia phản ứng với I2 trong môi trường kiềm tạo thành kết tủa có màu
A, tím.
B, đỏ gạch.
C, vàng.
D, trắng bạc.
C2H5COCH3 là hợp chất có chứa nhóm methyl ketone (CH3CO-) phản ứng với iodine trong môi trường kiềm tạo ra kết tủa iodoform (triiodomethane) màu vàng.
Phương trình hoá học:
CH3CHO + 3I2 + 4NaOH → CHI3 (kết tủa vàng) + HCOONa + 3NaI + 3H2O.
⟹Chọn đáp án C Đáp án: C
Phương trình hoá học:
CH3CHO + 3I2 + 4NaOH → CHI3 (kết tủa vàng) + HCOONa + 3NaI + 3H2O.
⟹Chọn đáp án C Đáp án: C
Câu 3 [560483]: Cho bán phản ứng và giá trị thế điện cực chuẩn như sau:
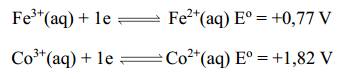
Giá trị suất điện động của pin Fe – Co là
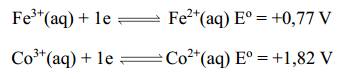
Giá trị suất điện động của pin Fe – Co là
A, 2,59 V.
B, +1,05 V.
C, –1,05 V.
D, –2,59 V.
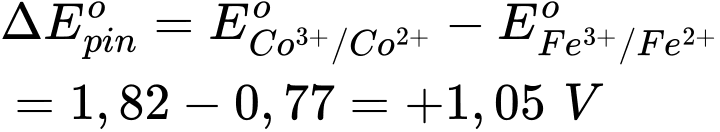
⇒ Chọn đáp án B Đáp án: B
Câu 4 [561035]: M là nguyên tố kim loại chuyển tiếp dãy thứ nhất, có một số đặc điểm sau:
• Nguyên tử có 4 electron độc thân.
• Có nhiều số oxi hoá trong các hợp chất, trong đó có số oxi hoá +2 và +3.
• Ở dạng đơn chất, là kim loại nặng.
M là nguyên tố nào sau đây?
• Nguyên tử có 4 electron độc thân.
• Có nhiều số oxi hoá trong các hợp chất, trong đó có số oxi hoá +2 và +3.
• Ở dạng đơn chất, là kim loại nặng.
M là nguyên tố nào sau đây?
A, Cr.
B, Ni.
C, Fe.
D, Cu.
Cấu hình electron và sự phân bố electron ở các ô orbital của các nguyên tố như sau:
❌ A. Cr (Z = 24)
+ Cấu hình electron: [Ar] 3d5 4s1
+ Ô orbital:
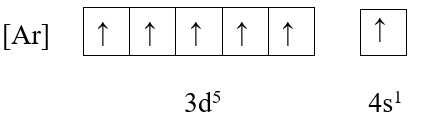
→ Có 6 electron độc thân
❌ B. Ni (Z = 28)
+ Cấu hình electron: [Ar] 3d8 4s2
+ Ô orbital:
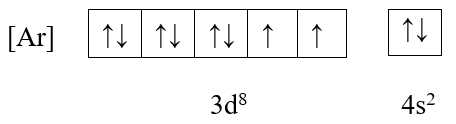
→ Có 2 electron độc thân
✔️ C. Fe (Z = 26)
+ Cấu hình electron: [Ar] 3d6 4s2
+ Ô orbital:
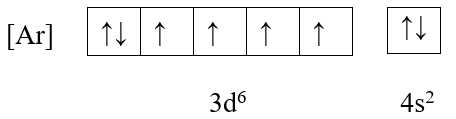
→ Có 4 electron độc thân
❌ D. Cu (Z = 29)
Cấu hình electron: [Ar] 3d10 4s1
+ Ô orbital:
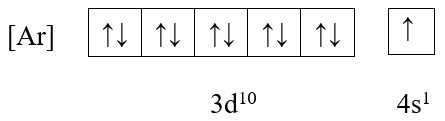
→ Có 1 electron độc thân
Vì nguyên tử M có 4 electron độc thân nên chỉ Fe là thỏa mãn. Fe có 4 electron độc thân, có số oxi hóa +2 và +3 trong hợp chất và là kim loại nặng.
⇒ Chọn đáp án C Đáp án: C
❌ A. Cr (Z = 24)
+ Cấu hình electron: [Ar] 3d5 4s1
+ Ô orbital:

→ Có 6 electron độc thân
❌ B. Ni (Z = 28)
+ Cấu hình electron: [Ar] 3d8 4s2
+ Ô orbital:

→ Có 2 electron độc thân
✔️ C. Fe (Z = 26)
+ Cấu hình electron: [Ar] 3d6 4s2
+ Ô orbital:

→ Có 4 electron độc thân
❌ D. Cu (Z = 29)
Cấu hình electron: [Ar] 3d10 4s1
+ Ô orbital:

→ Có 1 electron độc thân
Vì nguyên tử M có 4 electron độc thân nên chỉ Fe là thỏa mãn. Fe có 4 electron độc thân, có số oxi hóa +2 và +3 trong hợp chất và là kim loại nặng.
⇒ Chọn đáp án C Đáp án: C
Câu 5 [308693]: Ở điều kiện thường, chất hữu cơ nào sau đây là chất rắn, tan tốt trong nước?
A, Triolein.
B, Aniline.
C, Methylamine.
D, Alanine.
+ Alanine thuộc loại amino acid, ở điều kiện thường nó là chất rắn, tan cực tốt trong nước.
+ Methylamine tan tốt trong nước nhưng ở điều kiện thường methylamine là chất khí.
+ Triolein là chất béo, không tan trong nước.
+ Aniline là amine thơm, ít tan trong nước.
⟹ Chọn đáp án D Đáp án: D
+ Methylamine tan tốt trong nước nhưng ở điều kiện thường methylamine là chất khí.
+ Triolein là chất béo, không tan trong nước.
+ Aniline là amine thơm, ít tan trong nước.
⟹ Chọn đáp án D Đáp án: D
Câu 6 [703950]: “Các amino acid có khả năng di chuyển khác nhau trong …(1)… tuỳ thuộc vào …(2)… của môi trường”. Nội dung phù hợp trong ô trống (1), (2) lần lượt là
A, điện trường, pH.
B, dung dịch, nồng độ.
C, điện trường, nồng độ.
D, dung dịch, pH.
Các amino acid tồn tại ở dạng ion lưỡng cực nên khi đặt trong điện trường (như trong kỹ thuật điện di), các amino acid di chuyển về phía cực âm hoặc cực dương tùy thuộc vào điện tích của chúng trong môi trường. Điện tích của một amino acid phụ thuộc vào pH của môi trường:
⋆ Ở pH < (điểm đẳng điện): Amino acid mang điện tích dương (cation) và di chuyển về cực âm.
⋆ Ở pH > : Amino acid mang điện tích âm (anion) và di chuyển về cực dương.
⋆ Ở pH = : Amino acid trung hòa về điện tích, không di chuyển trong điện trường.
⇒ Các amino acid có khả năng di chuyển khác nhau trong điện trường tuỳ thuộc vào pH của môi trường.
⇒ Chọn đáp án A Đáp án: A
⋆ Ở pH < (điểm đẳng điện): Amino acid mang điện tích dương (cation) và di chuyển về cực âm.
⋆ Ở pH > : Amino acid mang điện tích âm (anion) và di chuyển về cực dương.
⋆ Ở pH = : Amino acid trung hòa về điện tích, không di chuyển trong điện trường.
⇒ Các amino acid có khả năng di chuyển khác nhau trong điện trường tuỳ thuộc vào pH của môi trường.
⇒ Chọn đáp án A Đáp án: A
Câu 7 [560601]: Sự giống nhau giữa liên kết kim loại và liên kết ion là đều có
A, các cation kim loại.
B, các anion.
C, các electron.
D, tương tác tĩnh điện.
So sánh liên kết ion và liên kết kim loại:
★ Giống nhau: đều có tương tác tĩnh điện hình thành giữa điện tích âm và điện tích dương.
★ Khác nhau:
+ Liên kết ion: do lực hút tĩnh điện giữa hai ion mang điện tích trái dấu: anion(-) và phần dương do cation kim loại hoặc NH4+ tạo thành.
+ Liên kết kim loại: do các electron tự do trong kim loại và cation kim loại.
⇒ Chọn đáp án D Đáp án: D
★ Giống nhau: đều có tương tác tĩnh điện hình thành giữa điện tích âm và điện tích dương.
★ Khác nhau:
+ Liên kết ion: do lực hút tĩnh điện giữa hai ion mang điện tích trái dấu: anion(-) và phần dương do cation kim loại hoặc NH4+ tạo thành.
+ Liên kết kim loại: do các electron tự do trong kim loại và cation kim loại.
⇒ Chọn đáp án D Đáp án: D
Câu 8 [705802]: Khi một đinh sắt được cắm vào củ khoai tây tươi, hiện tượng ăn mòn nào có thể xảy ra ngay tại thời điểm đó?
A, Ăn mòn hóa học.
B, Ăn mòn điện hóa.
C, Không có hiện tượng ăn mòn.
D, Cả ăn mòn hóa học và điện hóa.
Ăn mòn xảy ra là ăn mòn hóa học, do sắt phản ứng trực tiếp với các acid hữu cơ và oxygen trong khoai tây.
Ở đây, chỉ có một kim loại (Fe) phản ứng với môi trường, không có sự di chuyển điện tích giữa hai điện cực khác nhau, nên không thể coi là ăn mòn điện hóa.
Chọn đáp án A Đáp án: A
Ở đây, chỉ có một kim loại (Fe) phản ứng với môi trường, không có sự di chuyển điện tích giữa hai điện cực khác nhau, nên không thể coi là ăn mòn điện hóa.
Chọn đáp án A Đáp án: A
Câu 9 [703010]: Phương trình tổng quát cho sự đốt cháy alkane có công thức phân tử C5H12 là
C5H12 + 8O2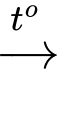 5CO2 + 6H2O
5CO2 + 6H2O
Các giá trị ∆Ho cho sự đốt cháy ba đồng phân pentane là
CH3CH2CH2CH2CH3 = –3536 kJ/mol
(CH3)2CHCH2CH3 = –3529 kJ/mol
(CH3)4C = –3515 kJ/mol
Trong các phát biểu sau, phát biểu nào không đúng?
C5H12 + 8O2
 5CO2 + 6H2O
5CO2 + 6H2OCác giá trị ∆Ho cho sự đốt cháy ba đồng phân pentane là
CH3CH2CH2CH2CH3 = –3536 kJ/mol
(CH3)2CHCH2CH3 = –3529 kJ/mol
(CH3)4C = –3515 kJ/mol
Trong các phát biểu sau, phát biểu nào không đúng?
A, Quá trình đốt cháy cả ba đồng phân pentane đều tỏa nhiệt.
B, Cùng khối lượng đốt cháy, 2-methylbutane tỏa nhiệt nhiều hơn n-pentane.
C, Giá trị ∆Ho càng âm thì quá trình đốt cháy tỏa nhiệt càng mạnh.
D, Sự phân nhánh của cấu tạo sẽ làm hợp chất trở nên ổn định hơn.
Phân tích các phát biểu:
✔️ A. Đúng. Tất cả các giá trị ốt cháy của các đồng phân đều âm, cho thấy quá trình đốt cháy đều tỏa nhiệt.
❌ B. Sai. 2-methylbutane và n-pentane là đồng phân cấu tạo, nhiệt lượng tỏa ra khi đốt 2-methylbutane là 3529 kJ.mol-1 và n-pentane là -3536kJ.mol-1 nên pentane tỏa nhiều nhiệt hơn do giá trị ∆Ho càng âm thì quá trình đốt cháy tỏa nhiệt càng mạnh.
✔️ C. Đúng.Giá trị ∆Ho âm biểu thị năng lượng tỏa ra trong quá trình đốt cháy. Giá trị càng âm thì năng lượng tỏa ra càng lớn.
✔️ D. Đúng. Đồng phân càng phân nhánh (như neopentane) thì càng bền nhiệt hơn, dẫn đến
⇒ Chọn đáp án B
Đáp án: B
✔️ A. Đúng. Tất cả các giá trị ốt cháy của các đồng phân đều âm, cho thấy quá trình đốt cháy đều tỏa nhiệt.
❌ B. Sai. 2-methylbutane và n-pentane là đồng phân cấu tạo, nhiệt lượng tỏa ra khi đốt 2-methylbutane là 3529 kJ.mol-1 và n-pentane là -3536kJ.mol-1 nên pentane tỏa nhiều nhiệt hơn do giá trị ∆Ho càng âm thì quá trình đốt cháy tỏa nhiệt càng mạnh.
✔️ C. Đúng.Giá trị ∆Ho âm biểu thị năng lượng tỏa ra trong quá trình đốt cháy. Giá trị càng âm thì năng lượng tỏa ra càng lớn.
✔️ D. Đúng. Đồng phân càng phân nhánh (như neopentane) thì càng bền nhiệt hơn, dẫn đến
⇒ Chọn đáp án B
Đáp án: B
Câu 10 [560799]: Cho một mẩu nhỏ postassium vào nước thu được dung dịch. Giá trị pH của dung dịch sau phản ứng có thể nhận giá trị nào dưới đây?
A, pH = 11.
B, pH = 2.
C, pH = 7.
D, pH = 6.
2K + 2H2O  2KOH + H2
2KOH + H2
Phản ứng của K với nước sinh ra KOH tạo môi trường base (kiềm) mạnh nên dung dịch sau phản ứng có thể có giá trị pH = 11.
⇒ Chọn đáp án A Đáp án: A
 2KOH + H2
2KOH + H2Phản ứng của K với nước sinh ra KOH tạo môi trường base (kiềm) mạnh nên dung dịch sau phản ứng có thể có giá trị pH = 11.
⇒ Chọn đáp án A Đáp án: A
Câu 11 [705712]: Thuộc da là quá trình mà da động vật được chuyển hoá thành da thuộc với những đặc tính ưu việt hơn như chịu nhiệt độ cao, không thối rữa khi tiếp xúc với nước và các môi trường khác. Quá trình thuộc da xử lí với HCHO là phản ứng tăng mạch carbon của protein dưới tác dụng của HCHO tạo sản phẩm có cấu trúc không gian.
Cho các phát biểu sau:
(a) Polymer khâu mạch khó nóng chảy và khó hoà tan hơn polymer chưa khâu mạch.
(b) Ở phản ứng khâu mạch carbon, các mạch polymer nối lại với nhau tạo mạng không gian nên bền hơn.
(c) Phản ứng xảy ra ở trên thuộc loại phản ứng trùng ngưng.
(d) Khi đun nóng da động vật trong dung dịch NaOH, sẽ xảy ra phản ứng depolymer hoá.
Số phát biểu đúng là
Cho các phát biểu sau:
(a) Polymer khâu mạch khó nóng chảy và khó hoà tan hơn polymer chưa khâu mạch.
(b) Ở phản ứng khâu mạch carbon, các mạch polymer nối lại với nhau tạo mạng không gian nên bền hơn.
(c) Phản ứng xảy ra ở trên thuộc loại phản ứng trùng ngưng.
(d) Khi đun nóng da động vật trong dung dịch NaOH, sẽ xảy ra phản ứng depolymer hoá.
Số phát biểu đúng là
A, 1
B, 2
C, 3
D, 4
Phân tích các phát biểu:
✔️ (a) Đúng. Polymer khâu mạch khó nóng chảy và khó hòa tan hơn polymer chưa khâu mạch nguyên do có sự tăng mạch carbon giúp tăng độ bền của polymer.
✔️ (b) Đúng. Ở phản ứng khâu mạch carbon, các mạch polymer nối lại với nhau tạo mạng không gian nên bền hơn.
❌ (c) Sai. Phản ứng xảy ra ở trên thuộc loại phản ứng tăng mạch carbon.
✔️ (d) Đúng. Khi đun nóng da động vật trong dung dịch NaOH, sẽ xảy ra phản ứng depolymer hóa. Do da động vật có thành phần chính là protein nên sẽ phản ứng depolymer hóa khi phản ứng với NaOH.
Các phát biểu đúng là (a) (b) và (d)
⇒ Chọn đáp án C Đáp án: C
✔️ (a) Đúng. Polymer khâu mạch khó nóng chảy và khó hòa tan hơn polymer chưa khâu mạch nguyên do có sự tăng mạch carbon giúp tăng độ bền của polymer.
✔️ (b) Đúng. Ở phản ứng khâu mạch carbon, các mạch polymer nối lại với nhau tạo mạng không gian nên bền hơn.
❌ (c) Sai. Phản ứng xảy ra ở trên thuộc loại phản ứng tăng mạch carbon.
✔️ (d) Đúng. Khi đun nóng da động vật trong dung dịch NaOH, sẽ xảy ra phản ứng depolymer hóa. Do da động vật có thành phần chính là protein nên sẽ phản ứng depolymer hóa khi phản ứng với NaOH.
Các phát biểu đúng là (a) (b) và (d)
⇒ Chọn đáp án C Đáp án: C
Câu 12 [308304]: Tiến hành thí nghiệm theo các bước sau:
Bước 1: Cho 1 mL dung dịch AgNO3 1% vào ống nghiệm sạch.
Bước 2: Thêm từ từ từng giọt dung dịch NH3, lắc đều cho đến khi kết tủa tan hết.
Bước 3: Thêm tiếp khoảng 1 mL dung dịch glucose 1% vào ống nghiệm; đun nóng nhẹ.
Phát biểu nào sau đây sai?
Bước 1: Cho 1 mL dung dịch AgNO3 1% vào ống nghiệm sạch.
Bước 2: Thêm từ từ từng giọt dung dịch NH3, lắc đều cho đến khi kết tủa tan hết.
Bước 3: Thêm tiếp khoảng 1 mL dung dịch glucose 1% vào ống nghiệm; đun nóng nhẹ.
Phát biểu nào sau đây sai?
A, Sản phẩm hữu cơ thu được sau bước 3 là ammonium gluconate.
B, Thí nghiệm trên chứng minh glucose có tính chất của polyalcohol.
C, Sau bước 3, có lớp bạc kim loại bám trên thành ống nghiệm.
D, Trong phản ứng ở bước 3, glucose đóng vai trò là chất khử.
HD: Phân tích thí nghiệm:
• Sau bước 2: Ống nghiệm xuất hiện kết tủa AgOH màu trắng.
NH3 + H2O ⇄ NH4+ + OH–.
Ag+ + OH– → AgOH↓.
Tiếp tục nhỏ NH3 vào thì kết tủa tan do tạo thành phức chất [Ag(NH3)2]OH.
AgOH + 2NH3 → [Ag(NH3)2]OH.
• Sau bước 3: Ống nghiệm xuất hiện một lớp kim loại bạc bám trên bề mặt của ống nghiệm.
CH2OH[CHOH]4CHO + [Ag(NH3)2]OH → CH2OH[CHOH]4COONH4 + 2Ag↓ + 3NH3 + H2O.
⇒ Phân tích các phát biểu:
✔️ A. đúng. CH2OH[CHOH]4COONH4 có tên là ammonium gluconate.
❌ B. sai. Thí nghiệm chứng minh tính chất của nhóm chức aldehyde CHO.
✔️ C. đúng theo phân tích trên.
✔️ D. đúng. Mẹo nhỏ: AgNO3 → Ag nên AgNO3 thể hiện tính oxy hóa ⇒ glucose thể hiện tính khử là đúng.
⟹ Chọn đáp án B Đáp án: B
• Sau bước 2: Ống nghiệm xuất hiện kết tủa AgOH màu trắng.
NH3 + H2O ⇄ NH4+ + OH–.
Ag+ + OH– → AgOH↓.
Tiếp tục nhỏ NH3 vào thì kết tủa tan do tạo thành phức chất [Ag(NH3)2]OH.
AgOH + 2NH3 → [Ag(NH3)2]OH.
• Sau bước 3: Ống nghiệm xuất hiện một lớp kim loại bạc bám trên bề mặt của ống nghiệm.
CH2OH[CHOH]4CHO + [Ag(NH3)2]OH → CH2OH[CHOH]4COONH4 + 2Ag↓ + 3NH3 + H2O.
⇒ Phân tích các phát biểu:
✔️ A. đúng. CH2OH[CHOH]4COONH4 có tên là ammonium gluconate.
❌ B. sai. Thí nghiệm chứng minh tính chất của nhóm chức aldehyde CHO.
✔️ C. đúng theo phân tích trên.
✔️ D. đúng. Mẹo nhỏ: AgNO3 → Ag nên AgNO3 thể hiện tính oxy hóa ⇒ glucose thể hiện tính khử là đúng.
⟹ Chọn đáp án B Đáp án: B
Câu 13 [304799]: Ester tạo ra mùi thơm của chuối chín được gọi là 3-methylbutyl ethanoate. Công thức cấu tạo của hợp chất này được cho dưới đây:
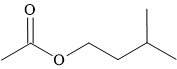
Carboxylic acid nào đã cấu tạo nên ester trên?

Carboxylic acid nào đã cấu tạo nên ester trên?
A, C2H3COOH.
B, CH3COOH.
C, C4H9COOH.
D, C2H5COOH.
HD: Phân tích cấu tạo của ester:
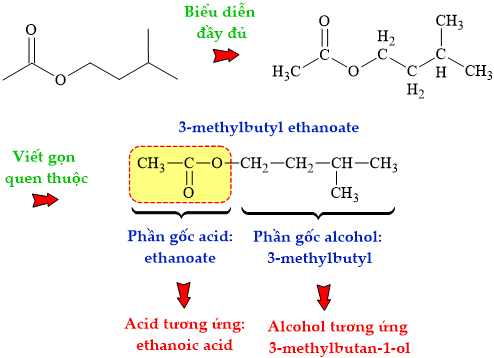
⇒ Carboxylic acid cấu tạo nên ester là ethanoic acid (acetic acid): CH3COOH
⇝ Chọn đáp án B Đáp án: B

⇒ Carboxylic acid cấu tạo nên ester là ethanoic acid (acetic acid): CH3COOH
⇝ Chọn đáp án B Đáp án: B
Câu 14 [703013]: Giả sử các chất ở điều kiện chuẩn. Hiệu điện thế tối thiểu cần đặt vào để phản ứng điện phân xảy ra là
A, 3,73 V.
B, 1,01 V.
C, 2,16 V.
D, 3,43 V.
MgCl2 –(đpnc)→ Mg + Cl2
Cathode (–): Mg2+ + 2e → Mg
Anode (+): 2Cl– → Cl2 + 2e
→ E = –2,37 – 1,26 = –3,73 V
→ Hiệu điện thế tối thiểu cần đặt vào để phản ứng điện phân là 3,73 V
⇒ Chọn đáp án A Đáp án: A
Cathode (–): Mg2+ + 2e → Mg
Anode (+): 2Cl– → Cl2 + 2e
→ E = –2,37 – 1,26 = –3,73 V
→ Hiệu điện thế tối thiểu cần đặt vào để phản ứng điện phân là 3,73 V
⇒ Chọn đáp án A Đáp án: A
Câu 15 [703014]: Nếu dòng điện trong bình được giữ ở mức không đổi 5 A, giả sử hằng số Faraday bằng 96485 C thì mất bao nhiêu giây để tạo ra 2,00 gam Mg(l) ở cực âm?
A, 2160.
B, 4190.
C, 3180.
D, 3216.
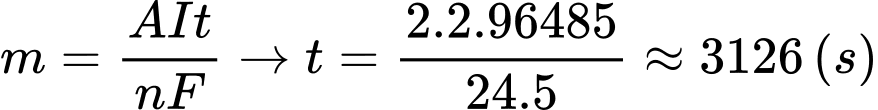
⇒ Chọn đáp án D Đáp án: D
Câu 16 [702814]: Ethylene phản ứng với bromine theo phương trình hóa học là
CH2=CH2 + Br2 CH2Br–CH2Br
CH2Br–CH2Br
Cơ chế của phản ứng được mô tả như sau:
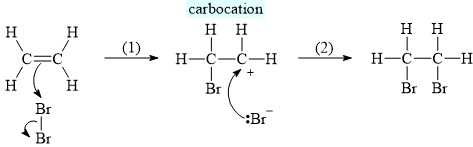
Nhận định nào sau đây là không đúng?
CH2=CH2 + Br2
 CH2Br–CH2Br
CH2Br–CH2BrCơ chế của phản ứng được mô tả như sau:

Nhận định nào sau đây là không đúng?
A, Phân tử ethylene có chứa 4 liên kết σ.
B, Liên kết đôi chứa nhiều electron hơn liên kết đơn.
C, Trong giai đoạn (1) có sự phân cắt liên kết π.
D, Trong giai đoạn (2) số liên kết σ tăng thêm 1.
Xét các phát biểu:
❌ A. Sai. Phân tử ethylene có chứa 5 liên kết σ: 4 ở liên kết C-H và 1 ở liên kết C=C.
✔️ B. Đúng. Liên kết đôi chứa 4 electron, nhiều hơn liên kết đơn có 2 electron.
✔️ C. Đúng. Trong giai đoạn (1) có sự phân cắt liên kết π để thành liên kết σ khi cộng thêm Br vào phân tử.
✔️ D. Đúng. Trong giai đoạn (2) số liên kết σ (liên kết đơn) tăng thêm từ 6 lên 7 (tăng 1 liên kết)
⇒ Chọn đáp án A . Đáp án: A
❌ A. Sai. Phân tử ethylene có chứa 5 liên kết σ: 4 ở liên kết C-H và 1 ở liên kết C=C.
✔️ B. Đúng. Liên kết đôi chứa 4 electron, nhiều hơn liên kết đơn có 2 electron.
✔️ C. Đúng. Trong giai đoạn (1) có sự phân cắt liên kết π để thành liên kết σ khi cộng thêm Br vào phân tử.
✔️ D. Đúng. Trong giai đoạn (2) số liên kết σ (liên kết đơn) tăng thêm từ 6 lên 7 (tăng 1 liên kết)
⇒ Chọn đáp án A . Đáp án: A
Câu 17 [702616]: Hiện nay, hàng trăm amino acid khác nhau đã được tìm ra, cả tổng hợp và tự nhiên, nhưng trong số này chỉ có 20 loại …(1)… xây dựng nên tất cả các …(2)… trong cơ thể con người. Nội dung phù hợp trong các ô trống (1), (2) lần lượt là
A, β-amino acid, enzyme.
B, amide, peptide.
C, α-amino acid, protein.
D, peptide, nucleotide.
Hiện nay, hàng trăm amino acid khác nhau đã được tìm ra, cả tổng hợp và tự nhiên, nhưng trong số này chỉ có 20 loại α-amino acid xây dựng nên tất cả các protein trong cơ thể con người.
⇒ Chọn đáp án C Đáp án: C
⇒ Chọn đáp án C Đáp án: C
Câu 18 [186429]: Mục đích chính của chuẩn độ acid - base là
A, xác định xem phản ứng hóa học có xảy ra hay không.
B, xác định nồng độ của một chất bằng dung dịch chuẩn đã biết nồng độ.
C, kiểm tra lại nồng độ của dung dịch đã biết.
D, để kiểm tra chất lượng của chất phản ứng.
Mục đích chính của chuẩn độ acid - base là xác định nồng độ của một chất bằng dung dịch chuẩn đã biết nồng độ.
⟹Chọn đáp án B Đáp án: B
⟹Chọn đáp án B Đáp án: B
PHẦN II. Thí sinh trả lời từ câu 1 đến câu 4. Trong mỗi ý a), b), c), d) ở mỗi câu, thí sinh chọn đúng hoặc sai.
Câu 19 [703017]: Đồng phân là những hợp chất khác nhau nhưng có cùng công thức phân tử, chúng có cùng số lượng và loại nguyên tử nhưng được sắp xếp khác nhau. Phức chất tồn tại một loại đồng phân gọi là đồng phân ion hóa. Chúng sẽ khác nhau về vị trí của phối tử ion có mặt trong cầu nội hoặc cầu ngoại. Cùng xem xét hai đồng phân ion hóa sau:
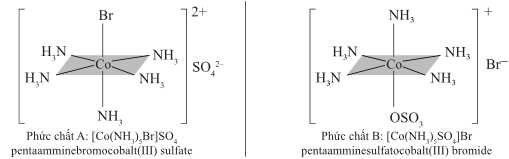
▪ Phức chất A: [Co(NH3)5Br]SO4 màu đỏ tím với phối tử Br– ở cầu nội và SO42– ở cầu ngoại.
▪ Phức chất B: [Co(NH3)5SO4]Br màu đỏ với phối tử SO42– ở cầu nội và Br– ở cầu ngoại.
Các phối tử ở cầu ngoại dễ dàng phân li trong dung dịch, đồng nghĩa với tính chất hóa học và khả năng dẫn điện của các đồng phân ion hóa cũng sẽ khác nhau.

▪ Phức chất A: [Co(NH3)5Br]SO4 màu đỏ tím với phối tử Br– ở cầu nội và SO42– ở cầu ngoại.
▪ Phức chất B: [Co(NH3)5SO4]Br màu đỏ với phối tử SO42– ở cầu nội và Br– ở cầu ngoại.
Các phối tử ở cầu ngoại dễ dàng phân li trong dung dịch, đồng nghĩa với tính chất hóa học và khả năng dẫn điện của các đồng phân ion hóa cũng sẽ khác nhau.
Phân tích các phát biểu:
✔️ a) Đúng. Cả hai phức chất A và B đều có 6 đỉnh tạo thành dạng hình học bát diện (8 mặt).
✔️ b) Đúng. Cho BaCl2 vào dung dịch phức chất A, thấy xuất hiện kết tủa trắng:
Ba2+ + SO42- → BaSO4↓ (màu trắng)
✔️ c) Đúng. Khi cùng nồng độ, dung dịch phức chất A phân li được ra ion có điện tích lớn hơn phức chất B nên độ dẫn điện của A tốt hơn B.
✔️ d) Đúng. Có thể dùng các dung dịch thuốc thử chứa ion Ba2+ hoặc ion Ag+ để phân biệt được hai dung dịch phức chất A và B do có tạo kết tủa có màu sắc khác nhau như sau:
Ba2+ + SO42- → BaSO4↓ (màu trắng) → nhận biết được phức chất A.
Ag+ + Br- → AgBr↓ (màu vàng nhạt) → nhận biết được phức chất B.
✔️ a) Đúng. Cả hai phức chất A và B đều có 6 đỉnh tạo thành dạng hình học bát diện (8 mặt).
✔️ b) Đúng. Cho BaCl2 vào dung dịch phức chất A, thấy xuất hiện kết tủa trắng:
Ba2+ + SO42- → BaSO4↓ (màu trắng)
✔️ c) Đúng. Khi cùng nồng độ, dung dịch phức chất A phân li được ra ion có điện tích lớn hơn phức chất B nên độ dẫn điện của A tốt hơn B.
✔️ d) Đúng. Có thể dùng các dung dịch thuốc thử chứa ion Ba2+ hoặc ion Ag+ để phân biệt được hai dung dịch phức chất A và B do có tạo kết tủa có màu sắc khác nhau như sau:
Ba2+ + SO42- → BaSO4↓ (màu trắng) → nhận biết được phức chất A.
Ag+ + Br- → AgBr↓ (màu vàng nhạt) → nhận biết được phức chất B.
Câu 20 [705789]: Trong nước thải của một nhà máy, hàm lượng ion amonium là 192 mg/L. Để xử lí ion amonium về nồng độ cho phép là không quá 5 mg/L (theo quy chuẩn Việt Nam), người ta tiến hành xử lí nước thải theo phương pháp Anammox (Anaerobic Ammonium Oxidation). Phương pháp này gồm 2 giai đoạn:
▪ Giai đoạn 1: Oxi hóa một phần ion amonium thành ion nitrite theo phản ứng sau:
2NH4+(aq) + 3O2(g) +4HCO3–(aq) 2NO2–(aq) + 4CO2(aq) + 6H2O(aq)
2NO2–(aq) + 4CO2(aq) + 6H2O(aq)
Trong đó, sử dụng muối NaHCO3 để cung cấp ion HCO3–, sục không khí liên tục để cung cấp O2.
▪ Giai đoạn 2: Diễn ra trong điều kiện yếm khí, lượng amonium còn lại sẽ được oxi hoá trực tiếp bằng ion nitrite từ giai đoạn 1, sản phẩm tạo thành là khí nitrogen theo phản ứng:
NH4+(aq) + NO2–(aq) N2(g) + 2H2O
N2(g) + 2H2O
Biết các phản ứng xảy ra hoàn toàn.
▪ Giai đoạn 1: Oxi hóa một phần ion amonium thành ion nitrite theo phản ứng sau:
2NH4+(aq) + 3O2(g) +4HCO3–(aq)
 2NO2–(aq) + 4CO2(aq) + 6H2O(aq)
2NO2–(aq) + 4CO2(aq) + 6H2O(aq)Trong đó, sử dụng muối NaHCO3 để cung cấp ion HCO3–, sục không khí liên tục để cung cấp O2.
▪ Giai đoạn 2: Diễn ra trong điều kiện yếm khí, lượng amonium còn lại sẽ được oxi hoá trực tiếp bằng ion nitrite từ giai đoạn 1, sản phẩm tạo thành là khí nitrogen theo phản ứng:
NH4+(aq) + NO2–(aq)
 N2(g) + 2H2O
N2(g) + 2H2OBiết các phản ứng xảy ra hoàn toàn.
Phân tích các phát biểu:
✔️A. Đúng. CM (NH4+) = n : V = 192.10-3 : 18 : 1 = 1,07.10-2 M.
❌B. Sai. Số oxi hóa theo PT:
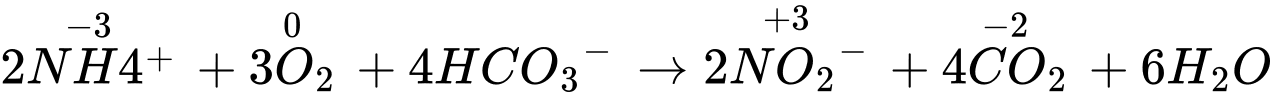
⟹ Chất khử là NH4+, chất oxi hóa là O2.
❌C. Sai. Nếu số oxi hóa thay đổi trong cùng 1 phân tử ⟹ oxi hóa nội phân tử. Nhưng ở giai đoạn 2 có 2 phân tử thay đổi số oxi hóa là NH4+ và NO2-.
✔️D. Đúng. 1mol NH4+ ⟹ 1mol HCO3-
✔️A. Đúng. CM (NH4+) = n : V = 192.10-3 : 18 : 1 = 1,07.10-2 M.
❌B. Sai. Số oxi hóa theo PT:
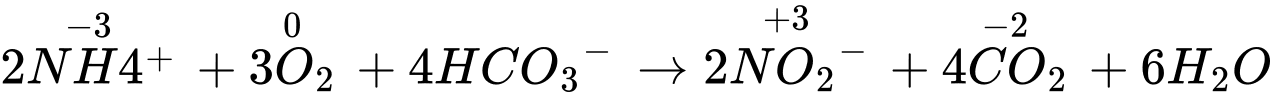
⟹ Chất khử là NH4+, chất oxi hóa là O2.
❌C. Sai. Nếu số oxi hóa thay đổi trong cùng 1 phân tử ⟹ oxi hóa nội phân tử. Nhưng ở giai đoạn 2 có 2 phân tử thay đổi số oxi hóa là NH4+ và NO2-.
✔️D. Đúng. 1mol NH4+ ⟹ 1mol HCO3-
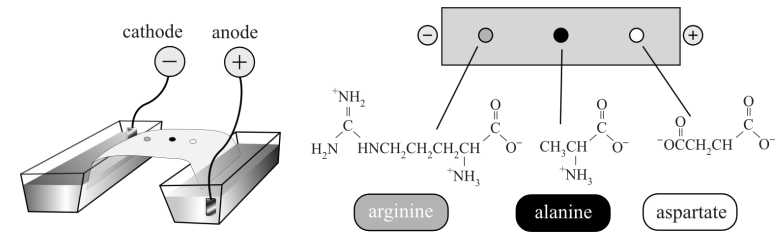
Câu 21 [705484]: Một vài giọt dung dịch hỗn hợp amino acid được nhỏ vào giữa một tờ giấy lọc (hoặc gel). Khi tờ giấy (hoặc gel) được đặt trong dung dịch đệm (giữ ổn định pH = 5) giữa hai điện cực và một điện trường được áp dụng, kết quả sau khi điện di được thể hiện như dưới đây:

Phân tích các phát biểu:
✔️ (a) Đúng. Tại pH = 5, alanine tồn tại chủ yếu ở dạng trung hòa về điện với tổng điện tích bằng 0.
CH3–CH(NH3+)–COO–
✔️ (b) Đúng. Tại pH = 5, aspartate tồn tại chủ yếu ở dạng anion bị phân li tất cả ion H+ trong gốc COOH.
✔️ (c) Đúng. Tại pH = 5, dạng tồn tại của arginine là dạng cation với tổng điện tích là +1 di chuyển về cực âm trong điện trường.
✔️ (d) Đúng. pH càng thấp thì dạng tồn tại chủ yếu của amino acid là dạng cation càng nhiều nguyên tử H, do dễ nhận thêm proton (H+)
✔️ (a) Đúng. Tại pH = 5, alanine tồn tại chủ yếu ở dạng trung hòa về điện với tổng điện tích bằng 0.
CH3–CH(NH3+)–COO–
✔️ (b) Đúng. Tại pH = 5, aspartate tồn tại chủ yếu ở dạng anion bị phân li tất cả ion H+ trong gốc COOH.
✔️ (c) Đúng. Tại pH = 5, dạng tồn tại của arginine là dạng cation với tổng điện tích là +1 di chuyển về cực âm trong điện trường.
✔️ (d) Đúng. pH càng thấp thì dạng tồn tại chủ yếu của amino acid là dạng cation càng nhiều nguyên tử H, do dễ nhận thêm proton (H+)
Câu 22 [705790]: Tiến hành theo sơ đồ và các thí nghiệm sau đây:
Điều chế X: Mở khóa phễu cho H2O chảy từ từ xuống bình cầu đựng CaC2 thì có khí X xuất hiện.
Thử tính chất của X:
Thí nghiệm 1: Dẫn X vào bình đựng dung dịch Br2 thì dung dịch Br2 mất màu.
Thí nghiệm 2: Dẫn X vào bình đựng dung dịch AgNO3 trong NH3 xuất hiện kết tủa vàng.
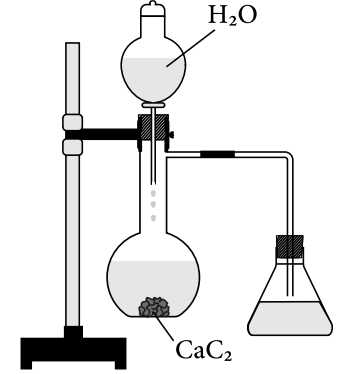
Điều chế X: Mở khóa phễu cho H2O chảy từ từ xuống bình cầu đựng CaC2 thì có khí X xuất hiện.
Thử tính chất của X:
Thí nghiệm 1: Dẫn X vào bình đựng dung dịch Br2 thì dung dịch Br2 mất màu.
Thí nghiệm 2: Dẫn X vào bình đựng dung dịch AgNO3 trong NH3 xuất hiện kết tủa vàng.

CaC2 + 2H2O ⟶ Ca(OH)2 + C2H2
Phân tích các phát biểu:
✔️A. Đúng. Khí thu được là acetylene ( C2H2 ).
✔️B. Đúng. Dẫn C2H2 vào thấy mất màu nước Bromine => Có phản ứng xảy ra. Do C2H2 có liên kết pi.
✔️C. Chỉ có alk - 1yne mới có phản ứng với AgNO3.
C2H2 + 2AgNO3 + 2NH3 = Ag2C2 + 2NH4NO3.
✔️D. Đúng. Phản ứng điều chế C2H2 tỏa 1 lượng nhiệt mạnh, nên cần cho từ từ nước vào.
Phân tích các phát biểu:
✔️A. Đúng. Khí thu được là acetylene ( C2H2 ).
✔️B. Đúng. Dẫn C2H2 vào thấy mất màu nước Bromine => Có phản ứng xảy ra. Do C2H2 có liên kết pi.
✔️C. Chỉ có alk - 1yne mới có phản ứng với AgNO3.
C2H2 + 2AgNO3 + 2NH3 = Ag2C2 + 2NH4NO3.
✔️D. Đúng. Phản ứng điều chế C2H2 tỏa 1 lượng nhiệt mạnh, nên cần cho từ từ nước vào.
PHẦN III. Thí sinh trả lời từ câu 1 đến 6. Thí sinh điền kết quả mỗi câu vào mỗi ô trả lời tương ứng theo hướng dẫn của phiếu trả lời.
Câu 23 [705818]: Khi làm lạnh dung dịch FeCl3 thu được tinh thể FeCl3.6H2O. Cho độ tan của FeCl3.6H2O trong nước ở một số nhiệt độ như sau:
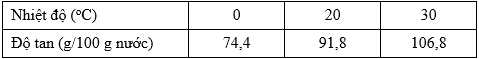
Để tạo ra dung dịch bão hoà của FeCl3 ở 20oC từ 50 g nước thì cần bao nhiêu gam FeCl3.6H2O?

Để tạo ra dung dịch bão hoà của FeCl3 ở 20oC từ 50 g nước thì cần bao nhiêu gam FeCl3.6H2O?
Trong 100g nước độ tan của FeCl3.6H2O là 91,8 g
Trong 50g nước độ tan của FeCl3.6H2O là :
91,8 : 2 = 45,9 (g)
Điền đáp án: 45,9
Trong 50g nước độ tan của FeCl3.6H2O là :
91,8 : 2 = 45,9 (g)
Điền đáp án: 45,9
Câu 24 [304188]: Aspirin, hay acetylsalicylic acid, là một dẫn xuất được điều chế từ acid salicylic; có tác dụng giảm đau, hạ sốt, chống viêm. Quá trình điều chế aspirin được cho như sau:
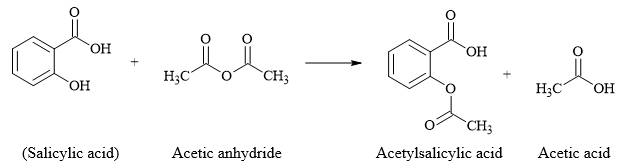
Tính giá trị độ bất bão hoà k của aspirin.

Tính giá trị độ bất bão hoà k của aspirin.
HD: Phân tích cấu tạo của aspirin:

► Độ bất bão hòa k là tổng số liên kết π và vòng có trong cấu tạo của hợp chất.
☆ Cách 1: đếm k dựa vào cấu tạo, ở đây kaspirin = 3πC=C + 2πC=O + 1vòng = 6.
☆ Cách 2: dựa vào công thức phân tử aspirin là C9H8O4 và công thức tính tổng quát k:
Đối với phân tử chỉ chứa carbon, hydro, halogen, nitơ và oxy, công thức:
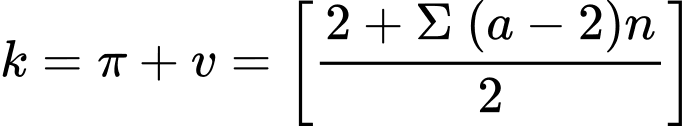
Trong đó a là hóa trị của nguyên tố, n là số nguyên tử của nguyên tố đó.
Áp dụng: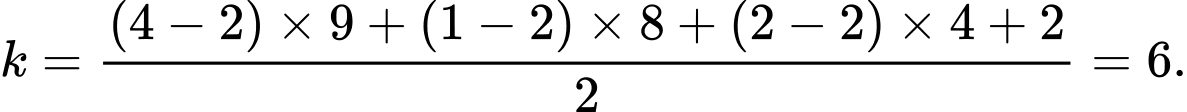
⟹ Điền đáp án: 6.

► Độ bất bão hòa k là tổng số liên kết π và vòng có trong cấu tạo của hợp chất.
☆ Cách 1: đếm k dựa vào cấu tạo, ở đây kaspirin = 3πC=C + 2πC=O + 1vòng = 6.
☆ Cách 2: dựa vào công thức phân tử aspirin là C9H8O4 và công thức tính tổng quát k:
Đối với phân tử chỉ chứa carbon, hydro, halogen, nitơ và oxy, công thức:
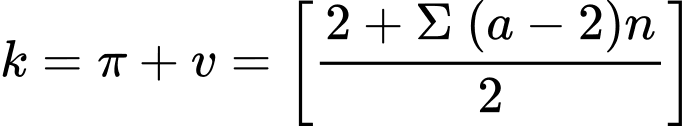
Trong đó a là hóa trị của nguyên tố, n là số nguyên tử của nguyên tố đó.
Áp dụng:
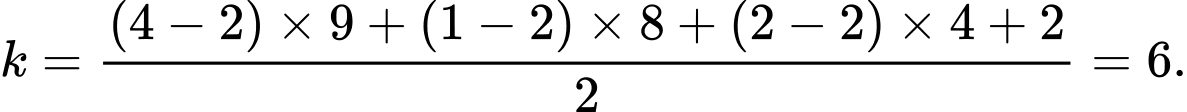
⟹ Điền đáp án: 6.
Câu 25 [973669]: [TN THPT 2020 – Đ2]: Hòa tan Fe3O4 bằng lượng vừa đủ dung dịch HCl, thu được dung dịch X. Có bao nhiêu chất khi cho vào X thì xảy ra phản ứng hóa học trong các chất: Ca(OH)2, Cu, AgNO3, Na2SO4?
HD: Fe3O4 + 8HCl → FeCl2 + 2FeCl3 + 4H2O.
Vừa đủ nên dung dịch X thu được gồm FeCl2 và FeCl3.
Phân tích các chất trong dãy:
✔️ Ca(OH)2 cung cấp OH– để tạo kết tủa Fe(OH)2↓ và Fe(OH)3.
✔️ Cu + 2FeCl3 → CuCl2 + 2FeCl3.
✔️ AgNO3 cung cấp Ag+ tạo kết tủa với Cl– → AgCl↓; ngoài ra Ag+ + Fe2+ → Fe3+ + Ag↓.
❌ Na2SO4 không có phản ứng với cả FeCl2 và FeCl3.
⟶ có 3/4 chất thỏa mãn yêu cầu
Vừa đủ nên dung dịch X thu được gồm FeCl2 và FeCl3.
Phân tích các chất trong dãy:
✔️ Ca(OH)2 cung cấp OH– để tạo kết tủa Fe(OH)2↓ và Fe(OH)3.
✔️ Cu + 2FeCl3 → CuCl2 + 2FeCl3.
✔️ AgNO3 cung cấp Ag+ tạo kết tủa với Cl– → AgCl↓; ngoài ra Ag+ + Fe2+ → Fe3+ + Ag↓.
❌ Na2SO4 không có phản ứng với cả FeCl2 và FeCl3.
⟶ có 3/4 chất thỏa mãn yêu cầu
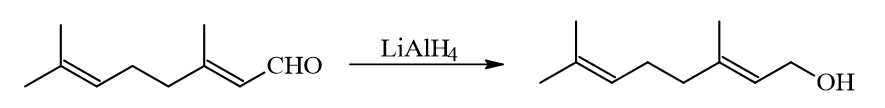
Câu 26 [705848]: Geraniol là một alcohol có trong tinh dầu hoa hồng. Nó được điều chế từ phản ứng khử geranial (một chất có trong tinh dầu sả) theo phản ứng:
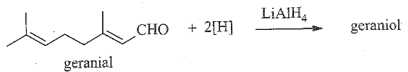
Khi phản ứng khử xảy ra, geranial bị phá vỡ bao nhiêu liên kết π?
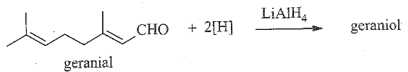
Khi phản ứng khử xảy ra, geranial bị phá vỡ bao nhiêu liên kết π?
Tác nhân LiAlH4 chỉ phá vỡ liên kết trong liên kết C=O, không thể phá vỡ liên kết trong C=C nguyên do C=C có mật độ điện tích âm cao và tác nhân LiAlH4 là tác nhân khử.
→ geranial chỉ có 1 liên kết trong nhóm CHO bị phá vỡ.
Điền đáp án : 1
→ geranial chỉ có 1 liên kết trong nhóm CHO bị phá vỡ.

Điền đáp án : 1
Câu 27 [705875]: Thực vật sử dụng quá trình quang hợp để chuyển đổi năng lượng ánh sáng từ mặt trời thành năng lượng hóa học. Trong quá trình quang hợp xảy ra phản ứng giữa khí carbonic và nước theo phương trình hóa học:
6CO2(g) + 6H2O(l)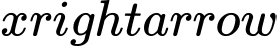 C6H12O6(aq) + 6O2(g).
C6H12O6(aq) + 6O2(g).
Biến thiên enthalpy chuẩn của phản ứng có giá trị là bao nhiêu kJ? (Cho enthalpy tạo thành chuẩn của CO2(g) bằng −394 kJ/mol; H2O(l) bằng −286 kJ/mol và C6H12O6(aq) bằng −1271 kJ/mol).
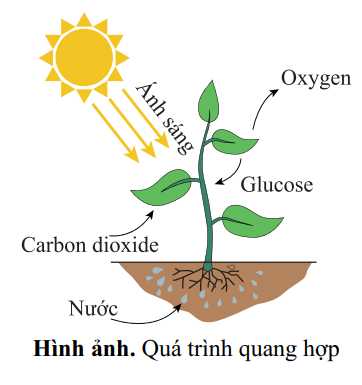
6CO2(g) + 6H2O(l)
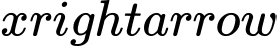 C6H12O6(aq) + 6O2(g).
C6H12O6(aq) + 6O2(g).Biến thiên enthalpy chuẩn của phản ứng có giá trị là bao nhiêu kJ? (Cho enthalpy tạo thành chuẩn của CO2(g) bằng −394 kJ/mol; H2O(l) bằng −286 kJ/mol và C6H12O6(aq) bằng −1271 kJ/mol).

6CO2(g) + 6H2O(l) → C6H12O6(aq) + 6O2(g)
Biến thiên enthalpy của phản ứng là
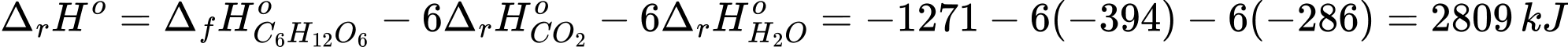
⟹Điền đáp án : 2809
Biến thiên enthalpy của phản ứng là
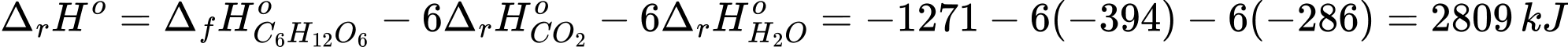
⟹Điền đáp án : 2809
Câu 28 [705823]: Phân tích nhiệt trọng là kỹ thuật phân tích để xác định thành phần các chất rắn bị phân hủy khi đun nóng. Sự thay đổi khối lượng được đo trong quá trình đun nóng sẽ cung cấp các thông tin về thành phần của chất ban đầu. Đun nóng 4,96 gam hỗn hợp CaC2O4 và MgC2O4 đến 1200°C, trong quá trình này khối lượng hỗn hợp chất rắn được đo liên tục. Biết rằng có 2 phản ứng phân hủy xảy ra ở khoảng 400°C:
MgC2O4(s) → MgO(s) + CO(g) + CO2(g)
CaC2O4(s) → CaCO3(s) + CO(g)
Ở 900°C quan sát được phản ứng phân hủy thứ 3. Khi các phản ứng xảy ra hoàn toàn thu được 2,008 gam chất rắn. Tính phần trăm khối lượng của CaC2O4 trong 4,96 gam hỗn hợp ban đầu (Làm tròn đến hàng phần mười).
MgC2O4(s) → MgO(s) + CO(g) + CO2(g)
CaC2O4(s) → CaCO3(s) + CO(g)
Ở 900°C quan sát được phản ứng phân hủy thứ 3. Khi các phản ứng xảy ra hoàn toàn thu được 2,008 gam chất rắn. Tính phần trăm khối lượng của CaC2O4 trong 4,96 gam hỗn hợp ban đầu (Làm tròn đến hàng phần mười).
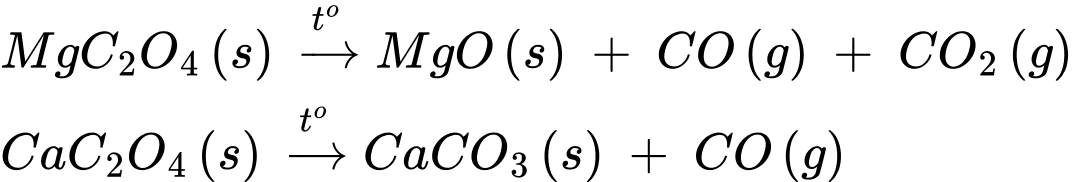
Ở 900 oC quan sát được phản ứng phân hủy thứ 3 là phân hủy CaCO3
 .
.
Gọi: nMgC2O4 = a (mol); nCaC2O4 = b (mol)
Khối lượng hỗn hợp là: mMgC2O4 + mCaC2O4 = 112a + 128b = 4,96 (gam) (1)
Từ PTHH số mol của MgO và CaO lần lượt là a và b mol
Khối lượng chất rắn sau nung là: mMgO + mCaO = 40a + 56b = 2,008 (gam) (2)
Từ phương trình (1) và (2) → a = 0,018 mol; b = 0,023 mol
Phần trăm khối lượng của CaC2O4 trong 4,96 gam hỗn hợp ban đầu là:
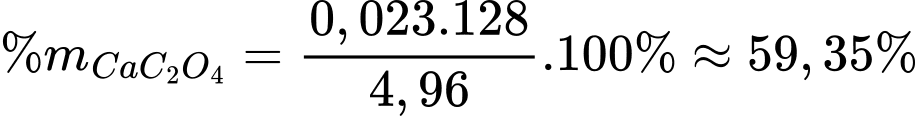
⇒ Điền đáp án: 59,4