PHẦN I. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
⇒ Chọn đáp án D Đáp án: D
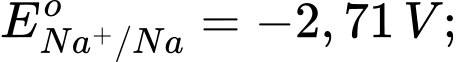
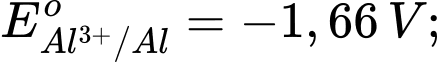
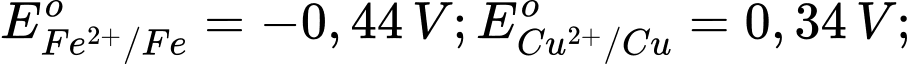
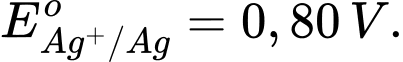
Kim loại nào sau đây có tính khử yếu nhất?
Phân tích các giá trị thế điện cực chuẩn:
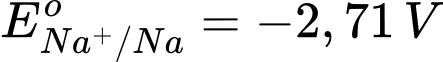 : Kim loại NaNa có tính khử mạnh nhất.
: Kim loại NaNa có tính khử mạnh nhất.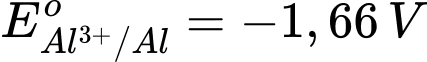 : Kim loại Al có tính khử mạnh, nhưng yếu hơn Na.
: Kim loại Al có tính khử mạnh, nhưng yếu hơn Na.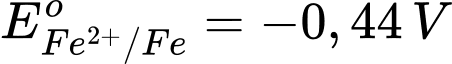 : Kim loại Fe có tính khử yếu hơn Al.
: Kim loại Fe có tính khử yếu hơn Al. 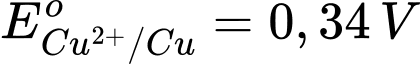 : Kim loại Cu có tính khử yếu hơn Fe.
: Kim loại Cu có tính khử yếu hơn Fe.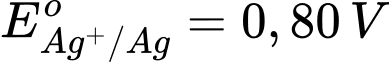 : Kim loại Ag có tính khử yếu nhất trong các kim loại này.
: Kim loại Ag có tính khử yếu nhất trong các kim loại này.⇒ Chọn đáp án A Đáp án: A
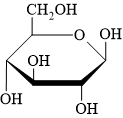
Theo đó, ở câu hỏi này quan sát thấy 1 vòng nên hợp chất thuộc loại monosaccharide
⇝ Chọn đáp án A. ♥
p/s: Cụ thể, cấu tạo được cho tương ứng là β-glucose:
 Đáp án: A
Đáp án: A 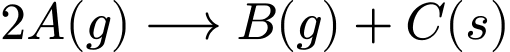 , tốc độ phản ứng (
, tốc độ phản ứng (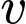 ) chỉ phụ thuộc vào nồng độ của chất phản ứng ở thể khí hoặc lỏng.
) chỉ phụ thuộc vào nồng độ của chất phản ứng ở thể khí hoặc lỏng.Biểu thức tốc độ phản ứng được viết là:
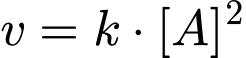
Gọi
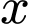 là số lần nồng độ
là số lần nồng độ 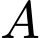 tăng lên. Nồng độ mới của
tăng lên. Nồng độ mới của 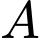 sẽ là
sẽ là 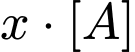 .
.Tốc độ phản ứng mới (
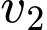 ) sẽ là:
) sẽ là: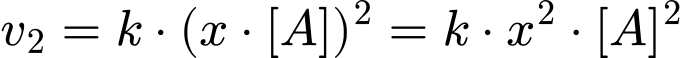
Theo đề bài, tốc độ phản ứng tăng lên 8 lần, nghĩa là:
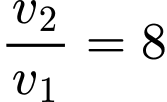
Thay các biểu thức vào, ta có:
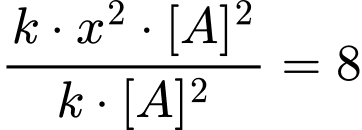
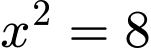
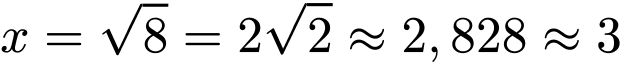
Chọn đáp án đúng: B.3 Đáp án: B
Vậy số liên kết peptide có trong một phân tử Ala-Gly-Val-Gly-Ala là: 5 – 1 = 4.
⇒ Chọn đáp án B Đáp án: B
CH3-CH2-CH2-COO-CH2-CH3 + NaOH → CH3-CH2-CH2-COONa + CH3-CH2OH
⇒ Chọn đáp án A Đáp án: A
Các chất giặt rửa tổng hợp có thể không phải là muối của acid béo, nhưng chúng vẫn có tính chất giặt rửa giống như xà phòng.
⟹ Chất giặt rửa có thành phần không phải muối của acid béo , nhưng có tính chất giặt rửa như xà phòng.
⟹Chọn đáp án C Đáp án: C
⇒ Chọn đáp án D Đáp án: D
⤑ Platinum không phải là nguyên tố dinh dưỡng thiết yếu cho cây trồng.
⇒ Chọn đáp án B Đáp án: B
❌ A. calcium oxide có công thức là CaO
❌ B. calcium carbonate có công thức là CaCO3
❌ D. calcium chloride có công thức là CaCl2
⇒ Chọn đáp án C Đáp án: C
Thí nghiệm 1: Điện phân dung dịch sodium chloride dư bằng điện cực trơ, không màng ngăn.
Thí nghiệm 2: Dẫn khí hydrogen sulfide vào dung dịch iron(III) chloride.
Thí nghiệm 3: Dẫn luồng khí ammonia qua ống sứ chứa copper(II) oxide nung nóng.
Thí nghiệm 4: Cho bột zinc vào dung dịch iron(III) nitrate dư.
Các thí nghiệm thu được đơn chất là
Thí nghiệm 1:
2NaCl + 2H2O –(đpdd)⟶ 2NaOH + Cl2↑ + H2↑
2NaOH + Cl2 ⟶ NaClO + NaCl + H2O
Thí nghiệm 2:
2FeCl3 + H2S → 2FeCl2 + 2HCl + S↓
Thí nghiệm 3:
3CuO + 2NH3 –(to)⟶ 3Cu + N2↑ + 3H2O
Thí nghiệm 4:
Zn + 2Fe(NO3)3 ⟶ Zn(NO3)2 + 2Fe(NO3)2
Các thí nghiệm thu được đơn chất là (1) (2) (3)
⇒ Chọn đáp án: A Đáp án: A
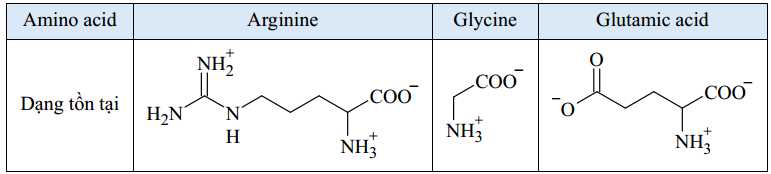
Sau quá trình điện di, kết quả thu được như sau:
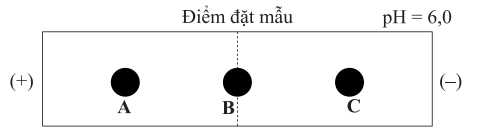
Cho các nhận định sau về quá trình điện di:
(a) Chất B gần như không di chuyển trong điện trường.
(b) Nếu đảo chiều điện cực thì vị trí của A và C cũng sẽ bị đảo tương ứng.
(c) Tại môi trường pH = 6 chất C là arginine mang điện tích dương di chuyển về phía cực âm.
(d) Ngoài phương pháp điện di để tách 3 amino acid thì có thể sử dụng phương pháp kết tinh để tách.
Các nhận định đúng là
⇾ Trong quá trình điện di:
- Arginine mang điện dương sẽ di chuyển về cực âm ⤏ Arginine là chất C
- Glycine trung hoà về điện nên gần như không di chuyển trong điện trường ⤏ Glycine là chất B
- Glutamic acid mang điện âm sẽ di chuyển về cực dương ⤏ Glutamic là chất A.
Phân tích các nhận định:
✔️ (a) Đúng. Chất B không bị ảnh hưởng điện trường nên gần như không di chuyển.
✔️ (b) Đúng. Nếu đảo chiều điện cực thì vị trí của A và C cũng sẽ bị đảo tương ứng vì A bị hút về cực dương, C bị hút về cực âm.
✔️ (c) Đúng. Tại môi trường pH = 6 chất C là arginine mang điện tích dương di chuyển về phía cực âm.
❌ (d) Sai. Arginine, glycine và glutamic acid đều có khả năng hòa tan trong nước.
Điểm nóng chảy của chúng cũng rất cao (hàng trăm độ C) nên việc kết tinh tách riêng chúng là không khả thi.
⇾ Các phát biểu đúng là (a) (b) (c)
⇒ Chọn đáp án: C Đáp án: C
Amine: Được hình thành khi các nguyên tử H trong NH3 được thay thế bởi các gốc hydrocarbon (như CH3, C2H5,...) hoặc các nhóm alkyl/aryl.
⇒ Khi thay thế một hay nhiều nguyên tử hydrogen trong phân tử ammonia bằng một hay nhiều gốc hydrocarbon thu được amine.
⇒ Chọn đáp án C Đáp án: C
- Quá trình cracking là quá trình phá vỡ các phân tử alkane mạch dài thành các hydrocarbon (alkane, alkene) mạch ngắn hơn.
- Quá trình reforming là quá trình sắp xếp lại mạch hydrocarbon để tạo ra nhiều hydrocarbon mạch nhánh.
⇒ Chọn đáp án C Đáp án: C
Trong heme B, vòng porphyrin đóng vai trò như một phối tử, liên kết với nguyên tử trung tâm Fe(II) bằng 4 nguyên tử nitrogen.
Mặc dù có 4 liên kết, nhưng vì chúng đều thuộc một vòng porphyrin, nên chỉ được tính là một phối tử.
⇒ Chọn đáp án A Đáp án: A
✔️ A. Đúng. Trong heme B, nguyên tử trung tâm là sắt (Fe(II)), liên kết với vòng porphyrin.
✔️B. Đúng. Mỗi phân tử hemoglobin (Hb) có 4 tiểu đơn vị, mỗi tiểu đơn vị chứa 1 nhóm heme B.Mỗi heme B có thể liên kết với 1 phân tử O2, nên tối đa 1 hemoglobin có thể gắn 4 O2.
✔️ C. Đúng. Liên kết giữa Fe và CO trong heme B bền hơn liên kết giữa Fe và O2 gấp ~200-250 lần.Điều này giải thích tại sao CO rất độc, vì nó chiếm chỗ của O2 trong hemoglobin, khiến máu không vận chuyển được oxygen.
❌ D. Sai. Chỉ có 4 liên kết N-Fe nên không tạo hình bát diện.
⇒ Chọn đáp án D Đáp án: D
- Phản ứng điều chế là quá trình trùng hợp methyl methacrylate thành PMMA:
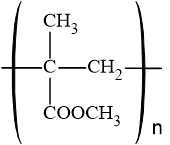
⇒ Chọn đáp án B Đáp án: B
Thành phần chính của khí Biogas gồm có methane (60 – 70%), hydrogen sulfide, carbon dioxide. Dựa vào mô hình dưới đây hãy giải thích vì sao khí đi ra từ hầm sinh khí lại phải cho đi qua nước?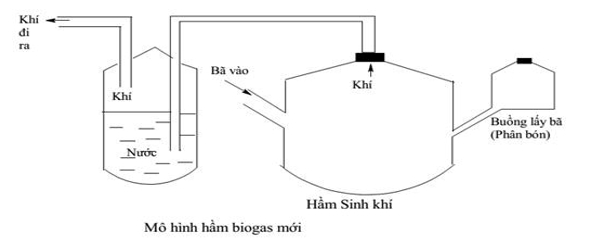
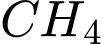 ), hydrogen sulfide (
), hydrogen sulfide (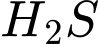 ) và carbon dioxide (
) và carbon dioxide (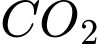 ).
).Mục đích cho qua nước:
•
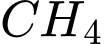 (thành phần chính để đốt cháy) không tan trong nước nên sẽ thoát ra ngoài để sử dụng.
(thành phần chính để đốt cháy) không tan trong nước nên sẽ thoát ra ngoài để sử dụng.•
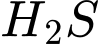 (Hydro sulfide) là một khí độc, có mùi trứng thối đặc trưng và gây ăn mòn kim loại (hỏng bếp ga, đường ống).
(Hydro sulfide) là một khí độc, có mùi trứng thối đặc trưng và gây ăn mòn kim loại (hỏng bếp ga, đường ống). 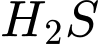 có khả năng tan khá tốt trong nước.
có khả năng tan khá tốt trong nước.• Việc dẫn khí qua nước giúp loại bỏ bớt tạp chất
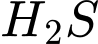 , giúp khí sạch hơn và bảo vệ thiết bị.
, giúp khí sạch hơn và bảo vệ thiết bị.Chọn đáp án đúng là: C Đáp án: C
PHẦN II. Thí sinh trả lời từ câu 1 đến câu 4. Trong mỗi ý a), b), c), d) ở mỗi câu, thí sinh chọn đúng hoặc sai.
Độ tan của NaHCO3 ở t1 = 20 °C và ở t2 = 40 °C lần lượt là 9,6 g/100 g nước và 12,7 g/100 g nước.
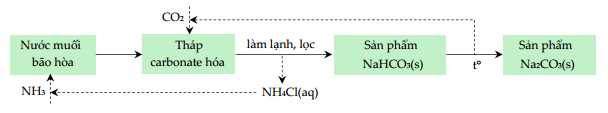
2. Nung CaCO3 ở 950 - 1100 oC rồi dẫn khí thoát ra vào dung dịch bão hòa của NaCl trong NH3, thực tế trong công nghiệp người ta sử dụng các phản ứng này:
CaCO3(s) → CaO(s) + CO2(g)
NaCl(s) + NH3(aq) + CO2(g) + H2O(l) → NaHCO3(s) + NH4Cl(aq)
3. Tách NaHCO3 khỏi dung dịch nhờ tính tan. Nung NaHCO3 ở nhiệt độ 450 - 500 oC thu được soda:
2NaHCO3(s) → Na2CO3(s) + CO2(g) + H2O(l)
Quá trình nhiệt phân NaHCO3 đã giải phóng một nửa lượng CO2 đã sử dụng, khí này tiếp tục được đưa vào quá trình sản xuất. Còn sản phẩm phụ khác là NH4Cl được chế hóa với vôi tôi (Ca(OH)2) để thu lại khí NH3 và sau đó khí này cũng được đưa trở lại quá trình:
2NH4Cl(aq) + Ca(OH)2 (aq) → CaCl2 (aq) + 2NH3(g) + 2H2O(l)
Các khí CO2, NH3 bay lên được tuần hoàn trở lại, chất thải chính của quá trình là CaCl2 và một số chất không phản ứng khác. NH3 được tuần hoàn trong quá trình sản xuất, vì vậy phương pháp này còn gọi là phương pháp tuần hoàn ammonia.
Phân tích các phát biểu:
✔️ (a) Đúng. Đá vôi đóng vai trò cung cấp CO2 cho quá trình Solvay.
✔️ (b) Đúng. Phương trình hóa học chuyển hóa NaHCO3 thành Na2CO3 là:
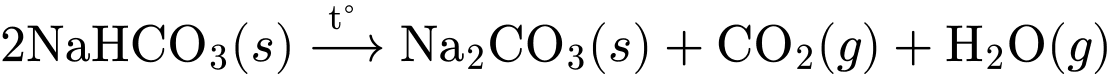
✔️ (c) Đúng. Quy trình trên CO2 chưa phản ứng, hay các khí NH3 và CO2 từ các giai đoạn sau sẽ được hồi quy về giai đoạn đầu để tiếp tục sử dụng.
❌ (d) Sai.
Số gam NaHCO3 có trong 225,4 gam dung dịch NaHCO3 ở nhiệt độ t2 là:
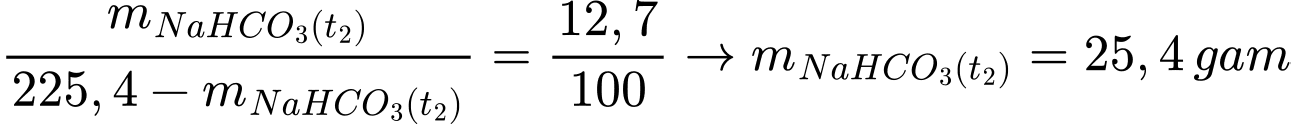
Số gam nước trong dung dịch là:
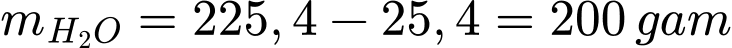
Khối lượng muối NaHCO3 trong dung dịch ở nhiệt độ t1 là:
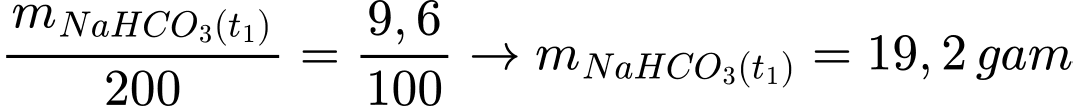
Số gam muối tách ra khi hạ nhiệt độ từ t2 xuống t1 là:
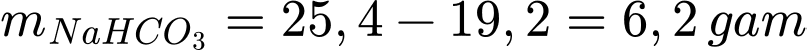
Trong công nghiệp, thuốc nổ trinitrotoluene (kí hiệu là TNT) được điều chế từ toluene bằng phản ứng nitro hóa (với HNO3) qua ba giai đoạn như sau:
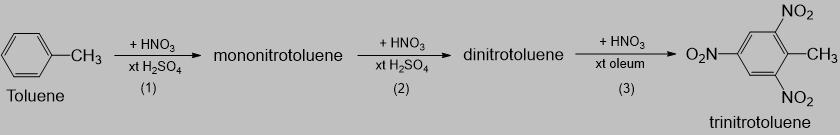
TNT(s) ⇢ CO(g) + H2O(g) + N2(g) + C(s)
Carbon sinh ra ở dạng muội than. Ở đkc, khi 1,0 mol TNT (s) nổ theo phản ứng trên sẽ tỏa ra lượng nhiệt là 1477,6kJ. Cho giá trị nhiệt hình thành của các chất như sau:
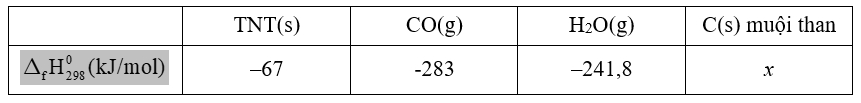
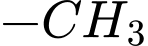 định hướng.
định hướng. ✔️Nhận định b) – Đúng, vì: Cân bằng phản ứng nổ:

Tổng số mol sản phẩm từ 2 mol TNT là:
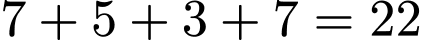 mol. Vậy 1 mol TNT sinh ra 11 mol sản phẩm.
mol. Vậy 1 mol TNT sinh ra 11 mol sản phẩm.✔️Nhận định c) – Đúng, vì: Tính giá trị
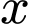 (nhiệt tạo thành của
(nhiệt tạo thành của  muội than):
muội than):Dựa vào công thức:
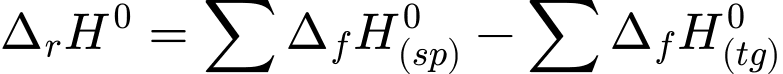
Ta có nhiệt tỏa ra là
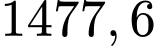 kJ cho 1 mol TNT
kJ cho 1 mol TNT 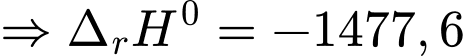 kJ.
kJ.Dựa vào phương trình tỉ lệ 1 mol TNT:
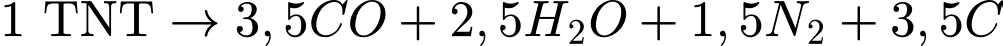
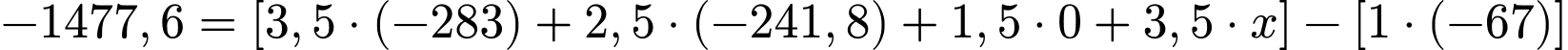
Giải phương trình:
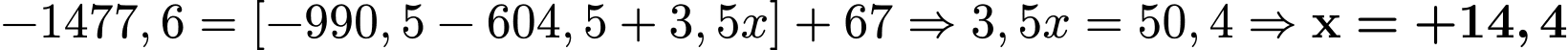 .
.❌Nhận định d) – Sai, vì: Toluene (
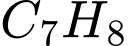 ) thế 2 nhóm
) thế 2 nhóm 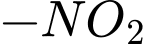 vào 2 nguyên tử của vòng benzene
vào 2 nguyên tử của vòng benzene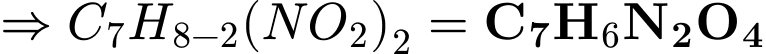 .
.
Chuẩn bị: Kim loại lithium, sodium, potassium, nước, dung dịch phenolphthalein.
▪ Bước 1: Dùng dao cắt các mẩu kim loại to bằng hạt đậu.
▪ Bước 2: Dùng kẹp lấy mẩu kim loại (Li, Na hoặc K) cho vào chậu thuỷ tinh chứa khoảng 1/3 thể tích nước.
▪ Bước 3: Thêm vài giọt dung dịch phenolphthalein vào chậu sau khi kim loại tan hết.
Mức độ phản ứng của các kim loại điển hình nhóm IA với nước:
☆ Lithium (Li): Phản ứng yếu nhất trong nhóm, sủi bọt nhẹ và tan dần trong nước.
☆ Sodium (Na): Phản ứng mạnh hơn, tạo thành khối cầu, chạy nhanh trên mặt nước do khí hydrogen thoát ra đẩy mẩu kim loại.
☆ Potassium (K): Phản ứng rất mạnh, thường bốc cháy với ngọn lửa màu tím do nhiệt độ sinh ra cao, thậm chí có thể gây nổ.
Phân tích các phát biểu:
✔️ A. Đúng. Mẩu Na phản ứng mạnh với nước, tạo thành khối cầu, chạy nhanh trên mặt nước do khí hydrogen thoát ra đẩy mẩu kim loại.
❌ B. Sai. Khả năng phản ứng với nước tăng dần từ Li đến K nên khả năng phản ứng của K mãnh liệt hơn Li.
✔️ C. Đúng. Phenolphthalein trong cả ba chậu chuyển sang màu hồng vì dung dịch sau phản ứng là kiềm MOH.
✔️ D. Đúng. Từ hiện tượng của thí nghiệm đã phân tích ở trên, có thể kết luận khả năng phản ứng của Li, Na, K với nước tăng dần.
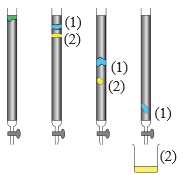
❌A. Sai. Pha động là dung môi, là chất lỏng hoặc khí mang các chất cần tách qua pha tĩnh. Alumina và silica là pha tĩnh, là chất rắn được sử dụng để hấp phụ các chất.
✔️B. Đúng. Chất nào tương tác tốt hơn với pha động (dung môi) sẽ di chuyển nhanh hơn và do đó đi ra khỏi cột trước.
✔️C. Đúng. Trong sắc ký cột, chất phân cực sẽ tương tác tốt hơn với dung môi phân cực và di chuyển nhanh hơn. Trong hình, chất (2) đi ra khỏi cột trước, chứng tỏ nó di chuyển nhanh hơn, do đó nó phân cực hơn chất (1).
❌D. Sai. Thứ tự đi ra khỏi cột trong sắc ký cột phụ thuộc vào tương tác giữa các chất với pha tĩnh và pha động, không phụ thuộc vào khối lượng riêng.
PHẦN III. Thí sinh trả lời từ câu 1 đến 6. Thí sinh điền kết quả mỗi câu vào mỗi ô trả lời tương ứng theo hướng dẫn của phiếu trả lời.
❌Glucose: Là monosaccharide (đường đơn), không có liên kết peptit, không có phản ứng biure.
✔️Gly-Ala-Gly: Là tripeptide, có 3 liên kết peptide, phản ứng biuret tạo màu tím.
❌Gly-Ala: Là đipeptide, có 2 liên kết peptide, không phản ứng biuret (cần từ tripeptide trở lên).
❌Propan-1,2-diol: Alcohol hai chức, không có liên kết peptide, không phản ứng biuret.
✔️Albumin: Là protein, có nhiều liên kết peptide, phản ứng biuret tạo màu tím.
Các chất có phản ứng màu biuret là: Gly-Ala-Gly, Albumin.
⟹ Điền đáp án: 2
HCOOCH3; CH3CHO; CH3OH; CH3COOC2H5; (CH3)2NH; CH3COOH; HCOOCH3; C2H6.
Số hợp chất có thể tạo liên kết hydrogen liên phân tử là
HD: Khái niệm: "liên kết hydrogen là một loại liên kết yếu được hình thành giữa nguyên tử H (đã liên kết với một nguyên tử khác có độ âm điện lớn) với một nguyên tử khác (có độ âm điện lớn) còn cặp electron riêng."
Để gọi là liên phân tử thì phân tử đang xét phải chứa đồng thời "nguyên tử H" và "nguyên tử khác". Thêm một lưu ý nữa; carbon là nguyên tử có độ âm điện không lớn, nên các H mà liên kết với carbon không đủ điều kiện.
Một cách trực quan, phân tử xét phải vừa chứa phần δ+ và δ–.
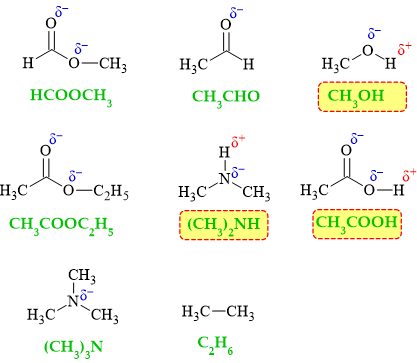
⇒ Có 3chất trong dãy thỏa mãn yêu cầu
⟹ Điền đáp án: 3
(a) Ethylamine và dimethylamine đều là những chất khí ở điều kiện thường.
(b) Methylamine có khả năng làm dung dịch phenolphtalein chuyển màu hồng.
(c) Aniline có khả năng làm xanh giấy quỳ tím.
(d) Nhỏ vài giọt aniline vào nước, lắc kĩ thấy xuất hiện kết tủa.
(e) Khế chua có thể làm mất mùi tanh của cá đồng (gây ra do một số amine).
(g) Alanin là amine thơm, không làm quỳ tím ẩm đổi màu.
Số phát biểu đúng là
✔️Đúng. a. Trạng thái: Methylamine, ethylamine, dimethylamine và trimethylamine là những chất khí, có mùi tanh của cá hoặc mùi khai tương ammonia tự (tuỳ nồng độ), các amine còn lại là chất lỏng hoặc rắn.
✔️Đúng. b. Trong phân tử amine: N còn một cặp e chưa liên kết ⟹ có thể tạo ra liên kết cho nhận (giống NH3) do đó các amine có tính chất hóa học tương tự ammonia.
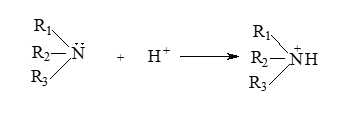
Dung dịch các alkylamine có thể làm quỳ tím đổi màu xanh hoặc phenolphthalein hóa hồng, còn dung dịch aniline không làm đổi màu quỳ tím hoặc phenolphthalein hóa hồng.
❌Sai. c. Aniline không cod khả năng làm đổi màu quỳ tím. Dung dịch các alkylamine có thể làm quỳ tím đổi màu xanh hoặc phenolphthalein hóa hồng.
❌Sai. d. Aniline là chất lỏng, ít tan trong nước.
✔️Đúng. e. Trong cá có các loại amin như: dimethyl amine, trimethyl amine là những chất tạo ra mùi tanh của cá. Khi cho thêm chất chua tức là cho thêm acid để chúng tác dụng với amine trên tạo muối làm giảm độ tanh cho cá.
RN + H+ → RNH+
❌Sai. Alanin là amino acid không làm quỳ tím đổi màu.
Số phát biểu đúng là: (a), (b), (e)
⟹ Điền đáp án: 3
(Làm tròn kết quả đến hàng phần chục)
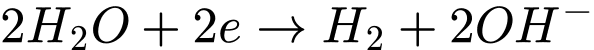
Phản ứng tại cực dương ( anode):
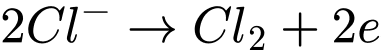
Q= I.t = 0,81.150 = 121,5 C
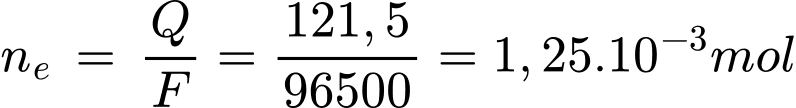
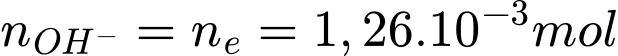
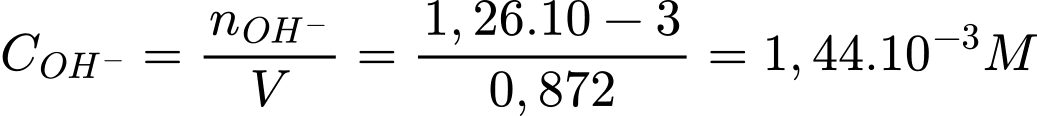
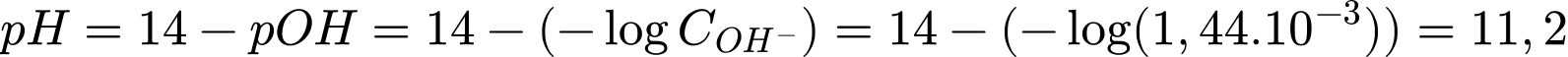
Điền đáp án: 11,2
Tính tốc độ ăn mòn trung bình của tấm kẽm theo đơn vị g/ngày (làm tròn đến hàng đơn vị).
Khối lượng của khối kẽm là mZn = 6720 × 7,13 = 47913,6 gam
Đổi 40,04 kg = 40040 gam
Khối lượng kẽm mất đi trong 30 ngày là 47913,6 – 40040 = 7873,6 gam
Tốc độ ăn mòn trung bình của tấm kẽm là v = 7873,6 ÷ 30 ≈ 262 gam/ngày
⟹ Điền đáp án: 262
NH4Cl(s)
 NH4Cl(aq);
NH4Cl(aq); 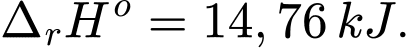
Sự giảm nhiệt độ khi phản ứng hòa tan ammonium chloride vào nước giúp nó được ứng dụng trong các túi chườm giúp giảm đau, giảm viêm một cách tạm thời. Nếu mỗi túi chườm lạnh chứa 20 gam muối và 100 mL nước cất (có D = 1 g/mL) thì khi hoạt động, nhiệt độ của túi chườm hạ xuống là t2 (oC). Biết nhiệt lượng cần để nâng nhiệt độ của 1,0 gam sản phẩm lên 1 oC là 4,184 J. Xác định giá trị của t2 (làm tròn đến hàng đơn vị).
⟶ Lượng nhiệt tạo ra : 20 ÷ 53,5 × 14,76 × 1000 (J)
Nhiệt lượng NH4Cl hấp thụ khi hòa tan vào nước là:
20 ÷ 53,5 × 14,76 × 1000 = 100 × 4,184 × (t2 - 25 )
→ t2 = 11,8oC.
⟹ Điền đáp án: 12