PHẦN I. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
Câu 1 [186356]: Pha loãng 1 lít dung dịch NaOH có pH = 13 bằng bao nhiêu lít nước để được dung dịch mới có pH = 11?
A, 9.
B, 99.
C, 10.
D, 100.
Đáp án B
Dung dịch NaOH có pH = 13 => pOH = 1 => C1 = [OH-] = 10-1
Dung dịch NaOH sau khi pha loãng có pH = 11 => pOH = 3 => C2 = [OH-] = 10-3
Áp dụng công thức cô cạn, pha loãng dung dịch ta có :
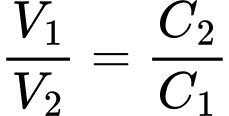

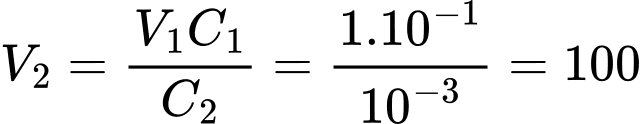 lít
lít 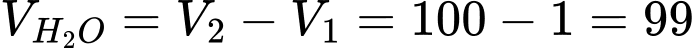 lít.
Đáp án: B
lít.
Đáp án: B
Dung dịch NaOH có pH = 13 => pOH = 1 => C1 = [OH-] = 10-1
Dung dịch NaOH sau khi pha loãng có pH = 11 => pOH = 3 => C2 = [OH-] = 10-3
Áp dụng công thức cô cạn, pha loãng dung dịch ta có :
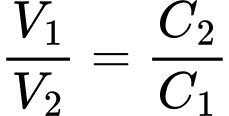

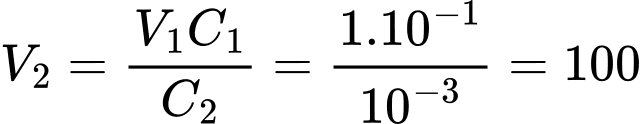 lít
lít 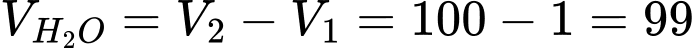 lít.
Đáp án: B
lít.
Đáp án: B
Câu 2 [308506]: Trong phân tử chất nào sau đây có chứa nguyên tố nitrogen?
A, Glucose.
B, Ethyl acetate.
C, Methylamine.
D, Saccharose.
Công thức phân tử của:
❌A. Glucose: C6H12O6
❌B. Ethyl acetate: C4H8O
✔️C. Methylamine: CH5N
❌D. Saccharose:C12H22O11
⇒ Phân tử của Methylamine chứa nguyên tố nitrogen.
⇒ Chọn đáp án C Đáp án: C
❌A. Glucose: C6H12O6
❌B. Ethyl acetate: C4H8O
✔️C. Methylamine: CH5N
❌D. Saccharose:C12H22O11
⇒ Phân tử của Methylamine chứa nguyên tố nitrogen.
⇒ Chọn đáp án C Đáp án: C
Câu 3 [702828]: Tinh thể kim loại chứa các …(1)… sắp xếp theo trật tự nhất định cùng với các …(2)… chuyển động tự do. Nội dung phù hợp trong các ô trống (1), (2) lần lượt là
A, hạt kim loại, hạt nhân nguyên tử.
B, hạt nhân nguyên tử, hạt kim loại.
C, electron tự do, cation kim loại.
D, cation kim loại, electron tự do.
- Trong kim loại, khi các nguyên tử mất đi electron ở lớp vỏ ngoài cùng sẽ trở thành các ion dương (cation). Những ion này chiếm các vị trí cố định trong mạng tinh thể kim loại, tạo nên cấu trúc trật tự.
- Các electron bị mất không bị giữ cố định bởi bất kỳ ion dương nào mà chuyển động tự do trong tinh thể kim loại.
⇒ Tinh thể kim loại chứa các cation kim loại sắp xếp theo trật tự nhất định cùng với các electron tự do chuyển động tự do.
Chọn đáp án D Đáp án: D
- Các electron bị mất không bị giữ cố định bởi bất kỳ ion dương nào mà chuyển động tự do trong tinh thể kim loại.
⇒ Tinh thể kim loại chứa các cation kim loại sắp xếp theo trật tự nhất định cùng với các electron tự do chuyển động tự do.
Chọn đáp án D Đáp án: D
Câu 4 [560616]: Vì sao người ta thường buộc một mẩu chì vào dây của cần câu mà không phải một mẩu nhôm?
A, Chì có khối lượng riêng lớn nên dễ chìm xuống nước.
B, Chì có giá thành rẻ hơn nhôm.
C, Chì nhẹ hơn hơn nên có thể nổi trên mặt nước.
D, Chì có màu gần như trong suốt nên cá sẽ không phát hiện ra.
Vì chì là kim loại có khối lượng riêng lớn làm dây cần câu chìm sâu xuống nước. Trong khi đó, nhôm là kim loại nhẹ (có khối lượng riêng nhỏ) nên dây cần câu không chìm được sâu dưới nước.
⇒ Chọn đáp án A Đáp án: A
⇒ Chọn đáp án A Đáp án: A
Câu 5 [705834]: Cho các nguyên tử sau: 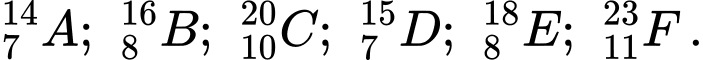 Các nguyên tử nào thuộc cùng một nguyên tố hóa học?
Các nguyên tử nào thuộc cùng một nguyên tố hóa học?
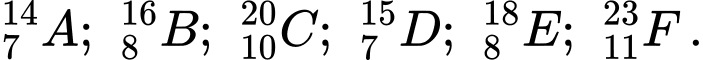 Các nguyên tử nào thuộc cùng một nguyên tố hóa học?
Các nguyên tử nào thuộc cùng một nguyên tố hóa học? A, A và B, C và D.
B, A và C, B và D.
C, B và E, C và F.
D, A và D, B và E.
Các nguyên tử của cùng một nguyên tố có cùng số proton, hay còn gọi là số nguyên tử.
Các nguyên tố cùng một nguyên tố hóa học là
A và D có cùng số proton là 7
B và E có cùng số proton là 8
Chọn đáp án D Đáp án: D
Các nguyên tố cùng một nguyên tố hóa học là
A và D có cùng số proton là 7
B và E có cùng số proton là 8
Chọn đáp án D Đáp án: D
Câu 6 [252458]: Sục khí chlorine dư vào dung dịch chứa muối sodium bromide và potassium bromide thu được hỗn hợp muối, đồng thời thấy khối lượng muối giảm 4,45 gam. Lượng chlorine đã tham gia phản ứng là
A, 0,1 mol.
B, 0,05 mol.
C, 0,02 mol.
D, 0,01 mol.
Cl2 + 2NaBr → 2NaCl + Br2 lần lượt là a + 2a --->2a + a mol
Cl2 + 2KBr → 2KCl + Br2 lần lượt là b +2b ---> 2b + b mol
Khối lượng muối giảm = KL NaBr + KL KBr – KL NaCl – KL KCl
103.2a + 119.2b – 58,5.2a – 74,5.2b = 4,45
=> 89a + 89b = 4,45 => a+b = 0,05
Lượng Cl2 phản ứng = a+ b = 0,05
Chọn đáp án B
Đáp án: B Chọn đáp án B
Câu 7 [702836]: Chất nào sau đây biểu diễn cấu tạo của một ester?
A, 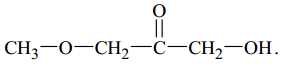
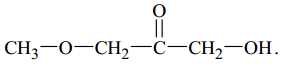
B, 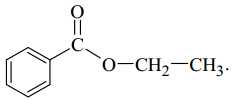

C, 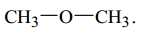
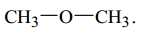
D, 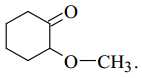

Ester là một loại hợp chất hữu cơ có công thức chung RCOOR' (trong phân tử có nhóm COO)
❌ A. Phân tử chỉ chứa nhóm C=O (ketone)
✔️ B. Phân tử chứa nhóm O-C=O (ester)
❌ C. Phân tử chứa chức -O- (ether)
❌ D. Phân tử chứa nhóm C=O và C-O.
⇒ Chọn đáp án B Đáp án: B
❌ A. Phân tử chỉ chứa nhóm C=O (ketone)
✔️ B. Phân tử chứa nhóm O-C=O (ester)
❌ C. Phân tử chứa chức -O- (ether)
❌ D. Phân tử chứa nhóm C=O và C-O.
⇒ Chọn đáp án B Đáp án: B
Câu 8 [190812]: Khi phản ứng với chất khử mạnh, aldehyde chuyển thành
A, ketone.
B, dẫn xuất halogen.
C, alcohol bậc 1.
D, alcohol bậc 2.
Phân tích các đáp án:
❌Sai. A. Ketone. Aldehyde khi phản ứng chất khử tạo thành ketone.
❌Sai. B. Dẫn xuất Halogen . Aldehyde không chuyển thành dẫn xuất halogen khi bị khử.
✔️Đúng. C. Alcohol. Khử Aldehyde bằng LiAlH4 hay NaBH4, H2/Pt tạo thành alcohol bậc 1.
❌Sai. D. Ketone. Khử ketone bằng LiAlH4 hay NaBH4, H2/Pt tạo thành alcohol bậc 2.
⟹ Chọn đáp án C Đáp án: C
❌Sai. A. Ketone. Aldehyde khi phản ứng chất khử tạo thành ketone.
❌Sai. B. Dẫn xuất Halogen . Aldehyde không chuyển thành dẫn xuất halogen khi bị khử.
✔️Đúng. C. Alcohol. Khử Aldehyde bằng LiAlH4 hay NaBH4, H2/Pt tạo thành alcohol bậc 1.
❌Sai. D. Ketone. Khử ketone bằng LiAlH4 hay NaBH4, H2/Pt tạo thành alcohol bậc 2.
⟹ Chọn đáp án C Đáp án: C
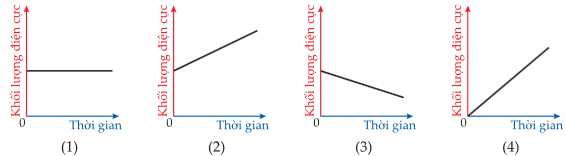
Câu 9 [1016565]: Điện phân dung dịch copper(II) sulfate bằng cặp điện cực copper với cường độ dòng điện không đổi. Đồ thị nào sau đây biểu diễn sự thay đổi khối lượng anode và cathode theo thời gian?

A, (3) và (2).
B, (3) và (4).
C, (2) và (3).
D, (1) và (3).
Điện phân dung dịch copper(II) sulfate bằng cặp điện cực copper với cường độ dòng điện không đổi.
Quá trình xảy ra trên các điện cực
Anode (+) Cu → Cu2+ + 2e
Cathode (-) Cu2+ + 2e → Cu
Trong quá trình điện phân xảy ra hiện tượng dương cực tan, Cu trên Anode tan dần nên khối lượng điện cực anode sẽ giảm đi
Trên điện cực cathode có Cu sinh ra bám lên, nên khối lượng sẽ tăng lên.
Sơ đồ (3) biểu diễn cho anode
Sơ đồ (2) biểu diễn cho cathode.
⟹ Chọn đáp án A Đáp án: A
Quá trình xảy ra trên các điện cực
Anode (+) Cu → Cu2+ + 2e
Cathode (-) Cu2+ + 2e → Cu
Trong quá trình điện phân xảy ra hiện tượng dương cực tan, Cu trên Anode tan dần nên khối lượng điện cực anode sẽ giảm đi
Trên điện cực cathode có Cu sinh ra bám lên, nên khối lượng sẽ tăng lên.
Sơ đồ (3) biểu diễn cho anode
Sơ đồ (2) biểu diễn cho cathode.
⟹ Chọn đáp án A Đáp án: A
Câu 10 [679747]: Đun nước cứng lâu ngày trong ấm nước xuất hiện một lớp cặn. Thành phần chính của lớp cặn đó là
A, CaCl2.
B, CaCO3.
C, Na2CO3.
D, CaO.
HD: Thành phần chính của lớp cặn đó là CaCO3. Nguyên nhân:
Ca(HCO3)2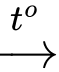 CaCO3↓ + CO2↑ + H2O.
CaCO3↓ + CO2↑ + H2O.
☆ Để làm sạch, có thể sử dụng giấm ăn:
2CH3COOH + CaCO3 → (CH3COO)2Ca + 2H2O.
⇒ Chọn đáp án B Đáp án: B
Ca(HCO3)2
 CaCO3↓ + CO2↑ + H2O.
CaCO3↓ + CO2↑ + H2O.☆ Để làm sạch, có thể sử dụng giấm ăn:
2CH3COOH + CaCO3 → (CH3COO)2Ca + 2H2O.
⇒ Chọn đáp án B Đáp án: B
Câu 11 [186602]: Nguyên nhân nào dưới đây không gây ra hiện tượng phú dưỡng?
A, Nguồn nước thải chứa chất làm mềm chưa xử lí triệt để làm dư thừa hàm lượng hợp chất phosphorus đi vào hệ thống nước tự nhiên.
B, Các nguồn phân bón như NH4NO3, (NH2)2CO, (NH4)2HPO4, Ca(H2PO4)2,… dư thừa chảy vào vùng nước tù đọng.
C, Chất thải sinh hoạt, chất thải công nghiệp không được xử lí theo quy chuẩn, đi vào sông hồ gây hiện tượng phú dưỡng.
D, Sự thay đổi về điều kiện thiên nhiên do thiên tai làm thay đổi hàm lượng nitrogen và phosphorus có trong nước.
Các nguyên nhân gây hiện tượng phú dưỡng là:
- Nguồn nước thải chưa xử lí triệt để: hầu hết chất tẩy rửa đều chứa chất làm mềm từ hợp chất phosphorus, chất thải này từ máy giặt, bồn rửa đi vào hệ thống nước tự nhiên.
- Các nguồn phân bón như NH4NO3, (NH2)2CO, (NH4)2HPO4, Ca(H2PO4)2,… dư thừa chảy vào vùng nước tù đọng.
Sự thay đổi về điều kiện thiên nhiên do thiên tai không phải nguyên nhân gây ra hiện tượng phú dưỡng.
⇒ Chọn đáp án D Đáp án: D
- Nguồn nước thải chưa xử lí triệt để: hầu hết chất tẩy rửa đều chứa chất làm mềm từ hợp chất phosphorus, chất thải này từ máy giặt, bồn rửa đi vào hệ thống nước tự nhiên.
- Các nguồn phân bón như NH4NO3, (NH2)2CO, (NH4)2HPO4, Ca(H2PO4)2,… dư thừa chảy vào vùng nước tù đọng.
Sự thay đổi về điều kiện thiên nhiên do thiên tai không phải nguyên nhân gây ra hiện tượng phú dưỡng.
⇒ Chọn đáp án D Đáp án: D
Câu 12 [703817]: Trùng hợp acrylonitrile (CH2=CHCN) thu được polymer được sử dụng để sản xuất loại tơ nào sau đây?
A, Tơ capron.
B, Tơ lapsan.
C, Tơ visco.
D, Tơ nitron.
Trùng hợp acrylonitrile (CH2=CHCN) sẽ tạo ra polymer polyacrylonitrile (PAN), đây là nguyên liệu chính để sản xuất tơ nitron (hay còn gọi là tơ olon), một loại tơ nhân tạo bền, dai và nhẹ.
Quá trình trùng hợp:
nCH2=CHCN → [−CH2−CH(CN)−]n
Polymer thu được là polyacrylonitrile (PAN).
⇒ Chọn đáp án: D Đáp án: D
Quá trình trùng hợp:
nCH2=CHCN → [−CH2−CH(CN)−]n
Polymer thu được là polyacrylonitrile (PAN).
⇒ Chọn đáp án: D Đáp án: D
Câu 13 [703921]: Dung dịch chất nào sau đây làm quỳ tím chuyển sang màu xanh?
A, NaCl.
B, NaOH.
C, KHSO4.
D, KNO3.
- Dung dịch NaCl và KNO3 là các muối trung tính nên không làm đổi màu quỳ tím.
- KHSO4 là một muối acid, có tính acid nhẹ. Dung dịch của nó làm quỳ tím chuyển sang màu đỏ.
- NaOH là một base mạnh, tạo dung dịch có tính kiềm. Dung dịch này làm quỳ tím chuyển sang màu xanh.
⇒ Chọn đáp án B
Đáp án: B
- KHSO4 là một muối acid, có tính acid nhẹ. Dung dịch của nó làm quỳ tím chuyển sang màu đỏ.
- NaOH là một base mạnh, tạo dung dịch có tính kiềm. Dung dịch này làm quỳ tím chuyển sang màu xanh.
⇒ Chọn đáp án B
Đáp án: B
Câu 14 [706172]: M là nguyên tố kim loại chuyển tiếp dãy thứ nhất, có một số đặc điểm sau:
∎ Hợp chất M(II) có tính oxi hoá nên phản ứng được với dung dịch thuốc tím.
∎ Ion M3+ có 5 electron độc thân.
∎ Là nguyên tố kim loại thuộc nhóm nguyên tố hoá học phổ biến trong tự nhiên.
M là nguyên tố nào sau đây?
∎ Hợp chất M(II) có tính oxi hoá nên phản ứng được với dung dịch thuốc tím.
∎ Ion M3+ có 5 electron độc thân.
∎ Là nguyên tố kim loại thuộc nhóm nguyên tố hoá học phổ biến trong tự nhiên.
M là nguyên tố nào sau đây?
A, Fe.
B, Al.
C, Mn.
D, Cu.
Kim loại chuyển tiếp dãy thứ nhất: Điều này giới hạn các nguyên tố M trong dãy từ Sc (Z=21) đến Zn (Z=30).
Hợp chất M(II) có tính oxi hóa, phản ứng được với dung dịch thuốc tím (KMnO4): Cho thấy M(II) có khả năng bị oxi hóa lên số oxi hóa cao hơn.
Hợp chất M(II) có tính oxi hóa, phản ứng được với dung dịch thuốc tím (KMnO4): Cho thấy M(II) có khả năng bị oxi hóa lên số oxi hóa cao hơn.
Ion M3+có 5 electron độc thân: Cho thấy M3+ có cấu hình electron d5.
Là nguyên tố kim loại thuộc nhóm nguyên tố hóa học phổ biến trong tự nhiên: Điều này loại trừ một số nguyên tố hiếm.
Phân tích các đáp án:
Đáp án: A Phân tích các đáp án:
✔️ A. Fe: Cấu hình electron: [Ar] 3d64s2. Fe2+ có cấu hình 3d6, có thể bị oxi hóa lên Fe3+. Fe3+ có cấu hình 3d5, có 5 electron độc thân. Sắt là kim loại phổ biến trong tự nhiên.
❌ B. Al không phải là kim loại chuyển tiếp. Al thuộc nhóm IIIA và nằm ở chu kỳ 3 của bảng tuần hoàn.
❌ C. Mn: Cấu hình electron: [Ar] 3d54s2. Mn2+ có cấu hình 3d5, có thể bị oxi hóa lên Mn3+. Mn3+ có cấu hình 3d4, có 4 electron độc thân, không thỏa mãn điều kiện.
❌ C. Mn: Cấu hình electron: [Ar] 3d54s2. Mn2+ có cấu hình 3d5, có thể bị oxi hóa lên Mn3+. Mn3+ có cấu hình 3d4, có 4 electron độc thân, không thỏa mãn điều kiện.
❌ D. Cu: Cấu hình electron: [Ar] 3d104s1. Cu2+ có cấu hình 3d9, không thể bị oxi hóa lên số oxi hóa cao hơn trong điều kiện thông thường. Cu3+ có cấu hình 3d8, có 2 electron độc thân, không thỏa mãn điều kiện.
⟹ Chọn đáp án A
⟹ Chọn đáp án A
Câu 15 [704195]: Cho dung dịch chứa amino acid X tồn tại ở dạng ion lưỡng cực:
H3N+CH(CH3)COO–
Đặt dung dịch này trong một điện trường. Khi đó:
H3N+CH(CH3)COO–
Đặt dung dịch này trong một điện trường. Khi đó:
A, Chất X sẽ di chuyển về phía cực âm của điện trường.
B, Chất X sẽ di chuyển về phía cực dương của điện trường.
C, Chất X gần như không di chuyển dưới tác dụng của điện trường.
D, Chất X chuyển hoàn toàn về dạng phân tử H2NCH(CH3)COOH dưới tác dụng của điện trường.
Amino acid X tồn tại dạng ion lưỡng cực H3N+CH(CH3)COO–, tổng điện tích bằng 0 nên gần như không di chuyển trong điện trường.
⇒ Chọn đáp án C Đáp án: C
⇒ Chọn đáp án C Đáp án: C
Câu 16 [704179]: Phản ứng cộng HCN vào hợp chất carbonyl thu được sản phẩm cyanohydrin.

Cơ chế của phản ứng như sau:
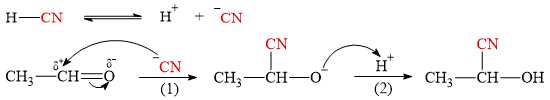
Phát biểu nào sau đây không đúng?

Cơ chế của phản ứng như sau:

Phát biểu nào sau đây không đúng?
A, HCN tan được trong nước và là chất điện li yếu.
B, Giai đoạn (1) có sự tạo thành 1 liên kết σ.
C, Giai đoạn (2), ion H+ có thể lấy từ sự điện li HCN.
D, O có độ âm điện lớn nên C (trong C=O) sẽ có mật độ điện tích âm lớn nhất.
Phân tích các phát biểu:
✔️ A. Đúng. HCN tan được trong nước và là chất điện li yếu do HCN phân li không hoàn toàn, xảy ra phản ứng thuận nghịch.
✔️ B. Đúng. Giai đoạn (1) có sự tạo thành 1 liên kết σ.
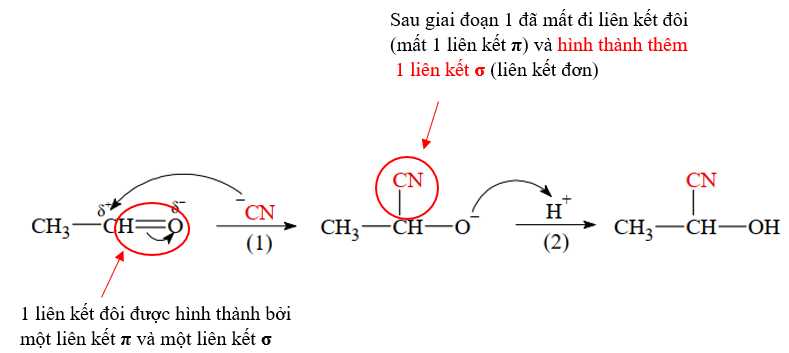
✔️ C. Đúng. Giai đoạn (2), ion H+ có thể lấy từ sự điện li HCN: HCN ⇌ H+ + CN-
❌ D. Sai. O có độ âm điện lớn nên sẽ hút electron mạnh hơn, electron sẽ tập trung ở O dẫn đến C (trong C=O) sẽ có mật độ điện tích dương lớn nhất.
⇒ Chọn đáp án D Đáp án: D
✔️ A. Đúng. HCN tan được trong nước và là chất điện li yếu do HCN phân li không hoàn toàn, xảy ra phản ứng thuận nghịch.
✔️ B. Đúng. Giai đoạn (1) có sự tạo thành 1 liên kết σ.

✔️ C. Đúng. Giai đoạn (2), ion H+ có thể lấy từ sự điện li HCN: HCN ⇌ H+ + CN-
❌ D. Sai. O có độ âm điện lớn nên sẽ hút electron mạnh hơn, electron sẽ tập trung ở O dẫn đến C (trong C=O) sẽ có mật độ điện tích dương lớn nhất.
⇒ Chọn đáp án D Đáp án: D
Sử dụng thông tin ở bảng dưới đây để trả lời các câu 17 - 18:
Trong một nhà máy sản xuất cồn công nghiệp, người ta dùng nguyên liệu là mùn cưa chứa 50% cellulose để sản xuất ethyl alcohol, theo sơ đồ sau (biết hiệu suất toàn bộ quá trình là 35%).
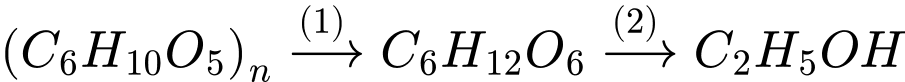
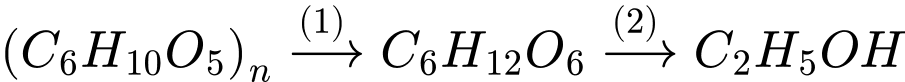
Câu 17 [706083]: Phản ứng xảy ra trong giai đoạn (1) là
A, Oxi hóa.
B, Lên men.
C, Xà phòng hóa.
D, Giảm mạch polymer.
Phản ứng cắt mạch polymer.
- Một số polymer có nhóm chức trong mạch có khả năng bị thủy phân cắt mạch như tinh bột, cellulose, capron, …
- Mạch polymer có thể bị phân hủy thành mạch ngắn hơn hoặc phân hủy hoàn toàn thành monomer tương ứng bởi nhiệt.
=> Phản ứng cắt mạch polymer làm giảm mạch polymer.
⟹Chọn đáp án D Đáp án: D
- Một số polymer có nhóm chức trong mạch có khả năng bị thủy phân cắt mạch như tinh bột, cellulose, capron, …
- Mạch polymer có thể bị phân hủy thành mạch ngắn hơn hoặc phân hủy hoàn toàn thành monomer tương ứng bởi nhiệt.
=> Phản ứng cắt mạch polymer làm giảm mạch polymer.
⟹Chọn đáp án D Đáp án: D
Câu 18 [706084]: Để sản xuất 10000 lít cồn 96° thì khối lượng mùn cưa cần dùng là bao nhiêu? Biết khối lượng riêng của ethyl alcohol là 0,8 gam/mL.
A, 77,28 tấn.
B, 43,28 tấn.
C, 38,64 tấn.
D, 51,18 tấn.
Thể tích C2H5OH trong 10000 lít cồn 96o là VC2H5OH = 10000.0,96 = 9600 L = 9,6.106 mL
Khối lượng C2H5OH là mC2H5OH = 9,6.106.0,8 = 7680000 gam = 7,68 tấn
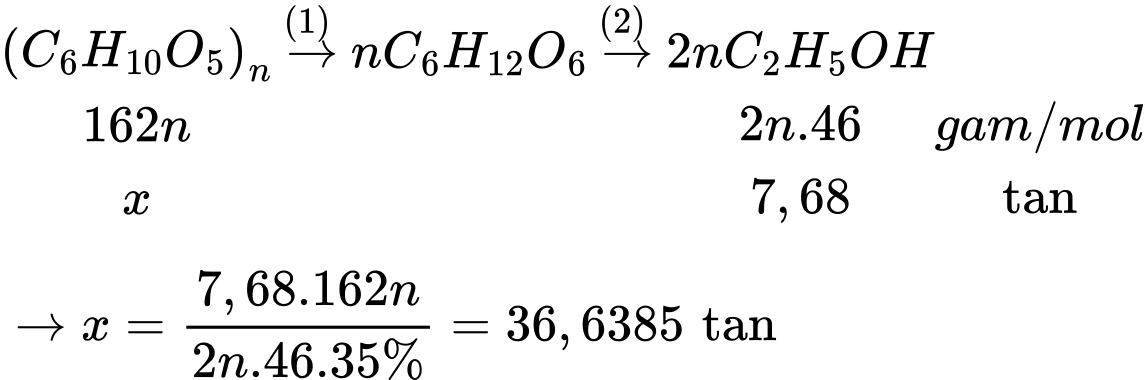
Khối lượng mùn cưa cần dùng là m = 36,6385:50% ≈ 77,28 tấn.
⟹Chọn đáp án A Đáp án: A
Khối lượng C2H5OH là mC2H5OH = 9,6.106.0,8 = 7680000 gam = 7,68 tấn
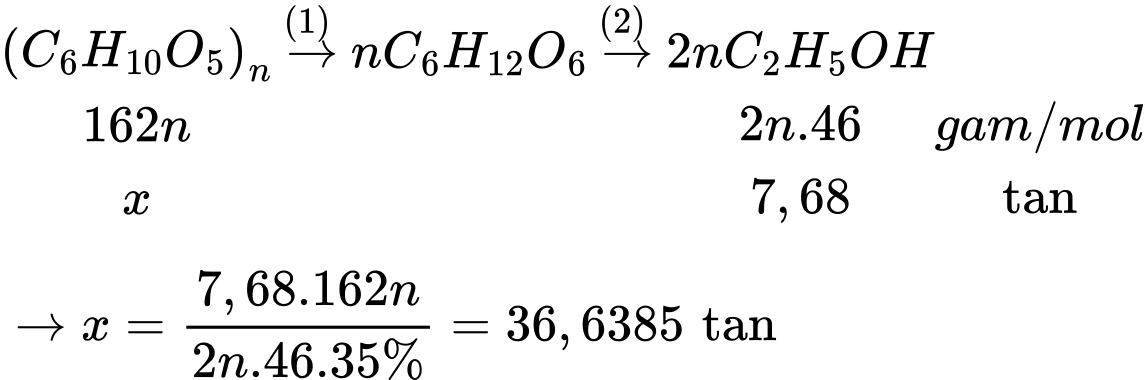
Khối lượng mùn cưa cần dùng là m = 36,6385:50% ≈ 77,28 tấn.
⟹Chọn đáp án A Đáp án: A
PHẦN II. Thí sinh trả lời từ câu 1 đến câu 4. Trong mỗi ý a), b), c), d) ở mỗi câu, thí sinh chọn đúng hoặc sai.
Câu 19 [703830]: Hợp chất hữu cơ X gồm 3 nguyên tố C, H, O. Kết quả phân tích nguyên tố của hợp chất hữu cơ X có mC : mH : mO = 42 : 7 : 16. X có mạch không phân nhánh, có phổ khối lượng và phổ hồng ngoại như sau:
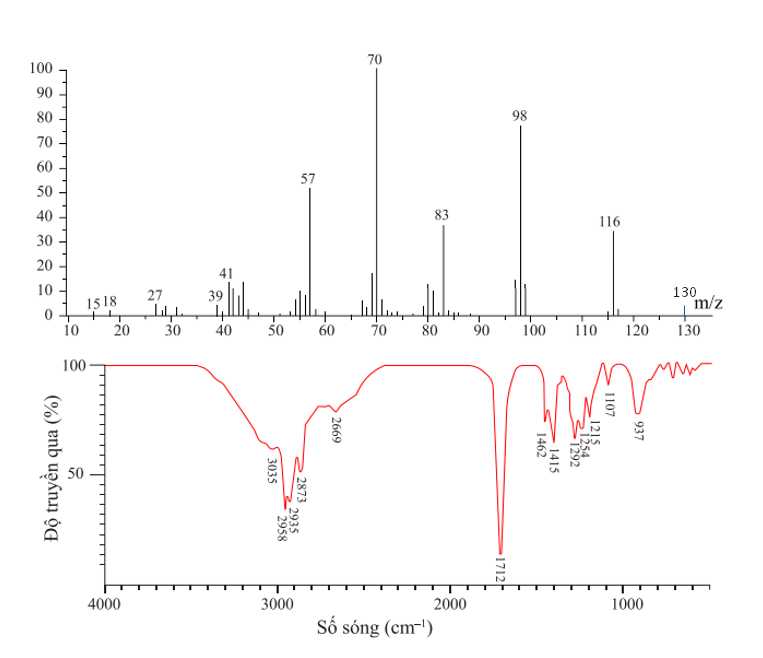
Cho bảng số sóng đặc trưng của các liên kết ở bảng sau:
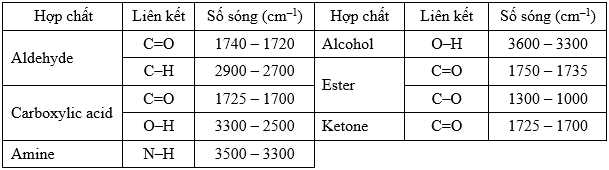

Cho bảng số sóng đặc trưng của các liên kết ở bảng sau:

Gọi công thức đơn giản nhất của X là CxHyOz → nC : nH : nO = x : y : z.
Hay: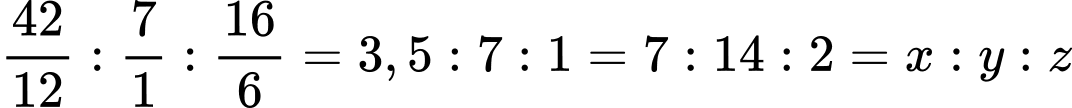
→ Công thức đơn giản nhất của X là C7H16O2
Từ phổ khối lượng → Phân tử khối của X là 130 gam/mol
Ta có:
→ Công thức đơn giản nhất của X là C7H16O2, mà MX = 130, ta có:
CTPT có dạng (C7H16O2)n = 130 ⇒ (12.7 + 16 + 16.2)n = 130 ⇒ n = 1
Vậy CTPT của X là C7H16O2
Từ kết quả phổ hồng ngoại, thấy có xuất hiện số sóng 1712 cm-1 đặc trưng cho liên kết C=O (1725-1700 cm-1), có xuất hiện số sóng đặc trưng của nhóm O-H trong vùng 3300-2500 cm-1
→ X là carboxylic acid
X có mạch C không phân phân nhánh → X có CTCT là CH3CH2CH2CH2CH2CH2COOH
Phân tích các phát biểu:
❌ a) Sai. Dựa vào công thức của X vừa tìm được ở trên, thấy X có 7 nguyên tử carbon.
❌ b) Sai. X thuộc loại hợp chất acid chứ không phải ester.
✔️ c) Đúng. X là acid, tác dụng được với muối NaHCO3 theo phản ứng:
CH3CH2CH2CH2CH2CH2COOH + NaHCO3 ⟶ CH3CH2CH2CH2CH2CH2COONa + H2O + CO2
✔️ d) Đúng. gốc R là gốc kị nước nên khi R tăng (số C tăng) thì tính kị nước tăng dẫn đến độ tan trong nước giảm.
Hay:
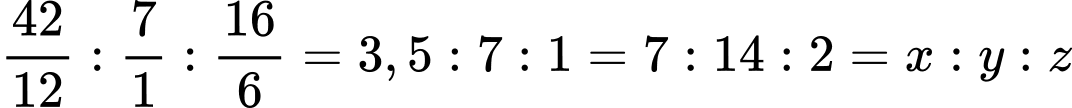
→ Công thức đơn giản nhất của X là C7H16O2
Từ phổ khối lượng → Phân tử khối của X là 130 gam/mol
Ta có:
→ Công thức đơn giản nhất của X là C7H16O2, mà MX = 130, ta có:
CTPT có dạng (C7H16O2)n = 130 ⇒ (12.7 + 16 + 16.2)n = 130 ⇒ n = 1
Vậy CTPT của X là C7H16O2
Từ kết quả phổ hồng ngoại, thấy có xuất hiện số sóng 1712 cm-1 đặc trưng cho liên kết C=O (1725-1700 cm-1), có xuất hiện số sóng đặc trưng của nhóm O-H trong vùng 3300-2500 cm-1
→ X là carboxylic acid
X có mạch C không phân phân nhánh → X có CTCT là CH3CH2CH2CH2CH2CH2COOH
Phân tích các phát biểu:
❌ a) Sai. Dựa vào công thức của X vừa tìm được ở trên, thấy X có 7 nguyên tử carbon.
❌ b) Sai. X thuộc loại hợp chất acid chứ không phải ester.
✔️ c) Đúng. X là acid, tác dụng được với muối NaHCO3 theo phản ứng:
CH3CH2CH2CH2CH2CH2COOH + NaHCO3 ⟶ CH3CH2CH2CH2CH2CH2COONa + H2O + CO2
✔️ d) Đúng. gốc R là gốc kị nước nên khi R tăng (số C tăng) thì tính kị nước tăng dẫn đến độ tan trong nước giảm.
Câu 20 [704209]: Nghiên cứu phản ứng tạo màu của protein với nitric acid được tiến hành thí nghiệm như sau:
▪ Bước 1: Cho vào ống nghiệm khoảng 1,0 mL dung dịch lòng trắng trứng và khoảng 1 mL dung dịch HNO3 đặc.
▪ Bước 2: Lắc đều hỗn hợp, sau đó để yên ống nghiệm trong khoảng 1 - 2 phút.
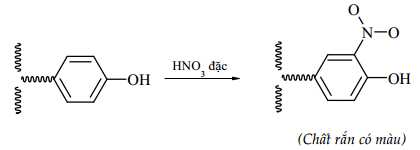
Hiện tượng thu được là hình thành chất rắn có màu do một số đơn vị amino acid chứa vòng benzene trong phân tử protein có thể tham gia phản ứng với dung dịch HNO3 đặc.
▪ Bước 1: Cho vào ống nghiệm khoảng 1,0 mL dung dịch lòng trắng trứng và khoảng 1 mL dung dịch HNO3 đặc.
▪ Bước 2: Lắc đều hỗn hợp, sau đó để yên ống nghiệm trong khoảng 1 - 2 phút.
Hiện tượng thu được là hình thành chất rắn có màu do một số đơn vị amino acid chứa vòng benzene trong phân tử protein có thể tham gia phản ứng với dung dịch HNO3 đặc.

Phân tích các phát biểu:
✔️ (a) Đúng. Một số đơn vị amino acid chứa vòng benzene trong protein có thể tham gia phản ứng với dung dịch HNO3 đặc tạo thành hợp chất rắn có màu vàng, đồng thời protein bị đông tụ tạo thành kết tủa.
✔️ (b) Đúng. Sau khi thế nguyên tử H của vòng benzene bằng nhóm NO2 thu được hợp chất mới không tan trong nước.
❌ (c) Sai. Pentapeptide tạo từ các amino acid không có vòng benzene nên không có phản ứng HNO3 tạo kết tủa vàng.
✔️ (d) Đúng. Protein có thể bị đông tụ dưới tác dụng của nhiệt, acid, base hoặc ion kim loại nặng. Sự đông tụ này xảy ra do cấu tạo ban đầu của protein bị biến đổi.
✔️ (a) Đúng. Một số đơn vị amino acid chứa vòng benzene trong protein có thể tham gia phản ứng với dung dịch HNO3 đặc tạo thành hợp chất rắn có màu vàng, đồng thời protein bị đông tụ tạo thành kết tủa.
✔️ (b) Đúng. Sau khi thế nguyên tử H của vòng benzene bằng nhóm NO2 thu được hợp chất mới không tan trong nước.
❌ (c) Sai. Pentapeptide tạo từ các amino acid không có vòng benzene nên không có phản ứng HNO3 tạo kết tủa vàng.
✔️ (d) Đúng. Protein có thể bị đông tụ dưới tác dụng của nhiệt, acid, base hoặc ion kim loại nặng. Sự đông tụ này xảy ra do cấu tạo ban đầu của protein bị biến đổi.
Câu 21 [704032]: Trong các phòng thí nghiệm, khi pha chế dung dịch của ion Fe3+ thường sẽ không thu được nồng độ theo như mong muốn về mặt tính toán lí thuyết. Lí do là vì trong dung dịch nước, ion Fe3+ bị hydrate hóa và thủy phân theo cân bằng sau:
Fe3+ + 6H2O → [Fe(H2O)6]3+
[Fe(H2O)6]3+ + H2O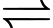 [Fe(OH)(H2O)5]2+ + H3O+; Ka = 10–2,56
[Fe(OH)(H2O)5]2+ + H3O+; Ka = 10–2,56
Tiến hành hòa tan 4g Fe2(SO4)3 vào nước để tạo thành 100 mL dung dịch X.
Fe3+ + 6H2O → [Fe(H2O)6]3+
[Fe(H2O)6]3+ + H2O
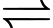 [Fe(OH)(H2O)5]2+ + H3O+; Ka = 10–2,56
[Fe(OH)(H2O)5]2+ + H3O+; Ka = 10–2,56Tiến hành hòa tan 4g Fe2(SO4)3 vào nước để tạo thành 100 mL dung dịch X.
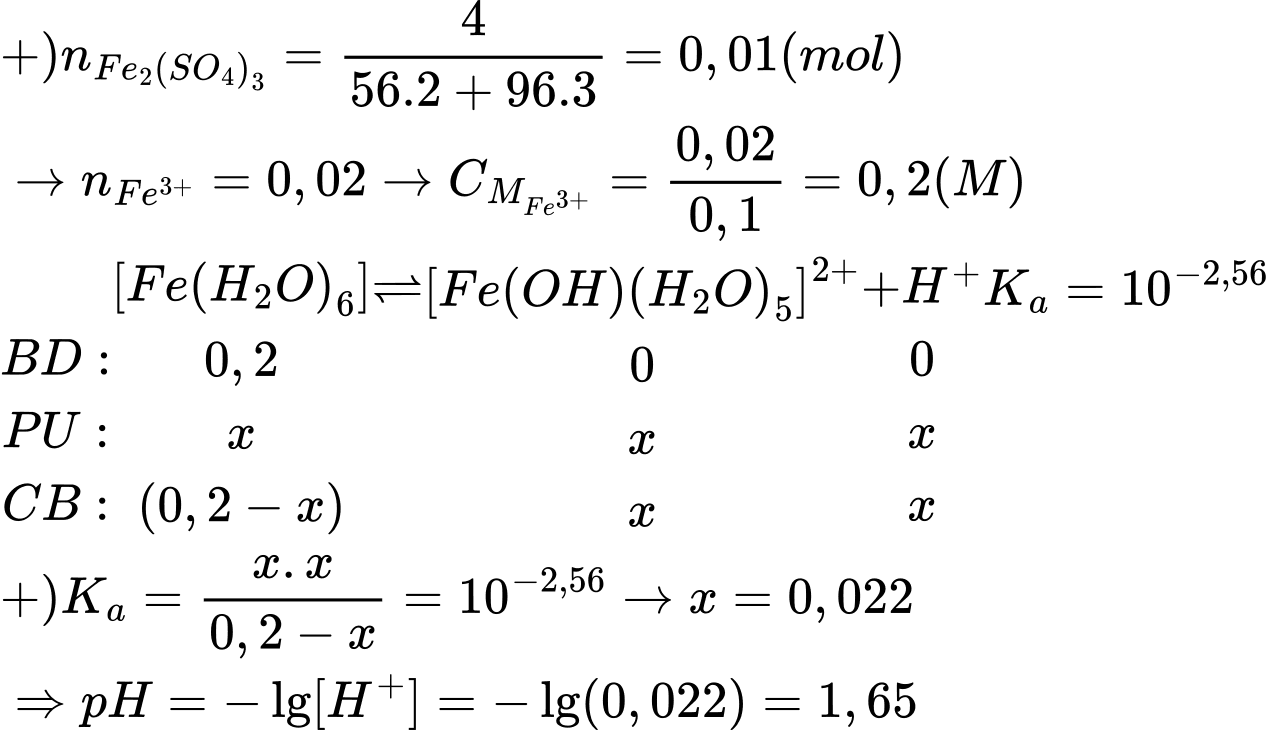
Phân tích các phát biểu:
✔️ a. Đúng. Theo thuyết Brønsted – Lowry: Acid là chất cho proton (H+), base là chất nhận proton. Acid và base có thể là phân tử hoặc ion. → Fe3+ đóng vai trò là acid theo thuyết Brønsted – Lowry vì nhường đi H+.
❌ b. Sai. Giá trị pH của dung dịch là 1,65.
❌ c. Sai. Phần trăm [Fe(H2O)6]3+ bị thủy phân là:
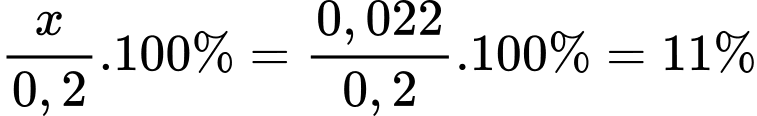
✔️ d. Đúng. Khi thêm HCl vào cân bằng, cân bằng sẽ chuyển dịch theo chiều làm giảm H+ (chính là H3O+), là chiều nghịch nên hạn chế được quá trình thủy phân.
Câu 22 [704208]: Một số kim loại có khả năng tan, đồng thời phản ứng với dung dịch acid HCl từ đó thể hiện được tính khử đặc trưng của các kim loại. Tiến hành thí nghiệm sau:
Cho vào hai ống nghiệm mỗi ống khoảng 5 mL dung dịch HCl 1 M.
▪ Ống nghiệm (1): Thêm tiếp một lá đồng vào ống nghiệm.
▪ Ống nghiệm (2): Thêm tiếp một băng magnesium vào ống nghiệm.
Cho vào hai ống nghiệm mỗi ống khoảng 5 mL dung dịch HCl 1 M.
▪ Ống nghiệm (1): Thêm tiếp một lá đồng vào ống nghiệm.
▪ Ống nghiệm (2): Thêm tiếp một băng magnesium vào ống nghiệm.
Thí nghiệm 1: Cu không phản ứng với dung dịch HCl, không có hiện tượng hóa học
Thí nghiệm 2: Mg tan dần trong dung dịch HCl, có khí không màu thoát ra khỏi chất lỏng.
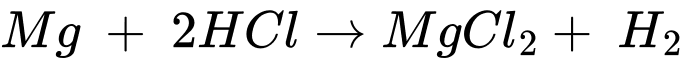
Quá trình oxi hóa: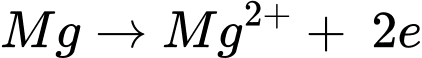
Quá trình khử: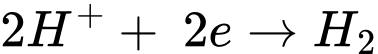
Phân tích các phát biểu:
✔️ A. Đúng. Đồng không phản ứng với dung dịch HCl vì thế khử chuẩn của cặp Cu2+/Cu (0,34) lớn hơn thế khử chuẩn của cặp 2H+/H2 (0,00). Đồng không đủ mạnh để khử H+ thành H2, nên không có hiện tượng xảy ra.
✔️ B. Đúng. Mg phản ứng với HCl, tạo thành MgCl2 và khí H2:
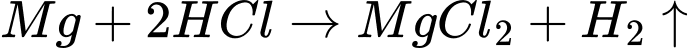
✔️ C. Đúng.Thế khử chuẩn của Mg2+/Mg là −2,37 V, nhỏ hơn thế khử chuẩn của 2H+/H2 0,00 V.
✔️ D. Đúng. Mg phản ứng được với HCl trong khi Cu không phản ứng được với HCl → Mg có tính khử mạnh hơn Cu.
Thí nghiệm 2: Mg tan dần trong dung dịch HCl, có khí không màu thoát ra khỏi chất lỏng.
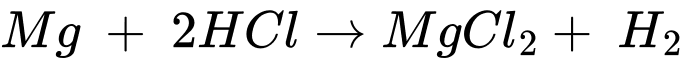
Quá trình oxi hóa:
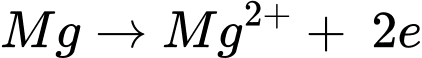
Quá trình khử:
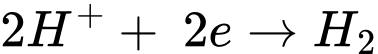
Phân tích các phát biểu:
✔️ A. Đúng. Đồng không phản ứng với dung dịch HCl vì thế khử chuẩn của cặp Cu2+/Cu (0,34) lớn hơn thế khử chuẩn của cặp 2H+/H2 (0,00). Đồng không đủ mạnh để khử H+ thành H2, nên không có hiện tượng xảy ra.
✔️ B. Đúng. Mg phản ứng với HCl, tạo thành MgCl2 và khí H2:
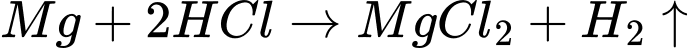
✔️ C. Đúng.Thế khử chuẩn của Mg2+/Mg là −2,37 V, nhỏ hơn thế khử chuẩn của 2H+/H2 0,00 V.
✔️ D. Đúng. Mg phản ứng được với HCl trong khi Cu không phản ứng được với HCl → Mg có tính khử mạnh hơn Cu.
PHẦN III. Thí sinh trả lời từ câu 1 đến 6. Thí sinh điền kết quả mỗi câu vào mỗi ô trả lời tương ứng theo hướng dẫn của phiếu trả lời.
Câu 23 [703978]: Có tổng số bao nhiêu đồng phân cấu tạo amine bậc 3 ứng với công thức phân tử C5H13N?
Amine bậc ba là các amine trong phân tử có nhóm chức dạng ≡N đính với ba gốc hydrocarbon.
Có 3 đồng phân cấu tạo amine bậc 3 ứng với công thức phân tử C5H13N như sau:
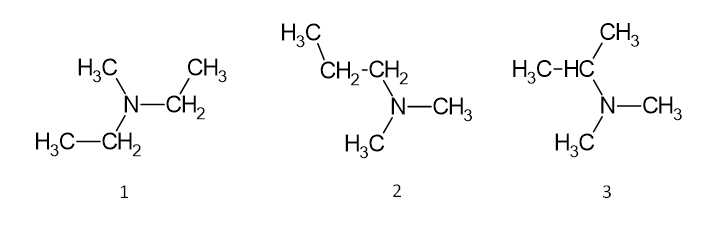
⇒ Điền đáp án: 3
Có 3 đồng phân cấu tạo amine bậc 3 ứng với công thức phân tử C5H13N như sau:

⇒ Điền đáp án: 3
Câu 24 [703996]: Một loại bột khử mùi chân có chứa kẽm. Kẽm trong mẫu bột được kết tủa thành muối kép, ZnNH4PO4. Nung nóng 1,080 gam muối này, tạo ra 0,368 gam Zn2P2O7. Tính phần trăm theo khối lượng kẽm trong bột khử mùi chân (làm tròn đến hàng phần mười).
2ZnNH4PO4 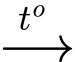 Zn2P2O7 + H2O + 2NH3
Zn2P2O7 + H2O + 2NH3
Số mol của Zn2P2O7 là: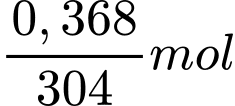
Phần trăm khối lượng Zn trong bột khử mùi chân là:

⇒ Điền đáp án: 14,6
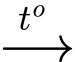 Zn2P2O7 + H2O + 2NH3
Zn2P2O7 + H2O + 2NH3Số mol của Zn2P2O7 là:
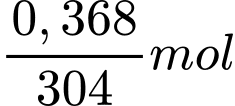
Phần trăm khối lượng Zn trong bột khử mùi chân là:

⇒ Điền đáp án: 14,6
Câu 25 [704037]: Chất béo E có phân tử khối là 858, thuỷ phân hoàn toàn 1 mol E trong dung dịch NaOH dư, thu được 1 mol muối sodium palmitate và 2 mol sodium oleate. Biết phân tử khối của sodium palmitate là 278, giá trị phân tử khối của sodium oleate là bao nhiêu?
Phản ứng tổng quát khi thủy phân chất béo E trong NaOH là:
(RCOO)3C3H5 + 3NaOH ⟶ 1 Sodium palmitate + 2 Sodium oleate + C3H5(OH)3
Bảo toàn khối lượng ta có:
M(RCOO)3C3H5 + 3MNaOH = MSodium palmitate + 2MSodium oleate + MC3H5(OH)3
⇔ 858 + 3.40 = 278 + 2MSodium oleate + 92
⇔ MSodium oleate = 304 (g/mol)
⇒ Điền đáp án: 304
(RCOO)3C3H5 + 3NaOH ⟶ 1 Sodium palmitate + 2 Sodium oleate + C3H5(OH)3
Bảo toàn khối lượng ta có:
M(RCOO)3C3H5 + 3MNaOH = MSodium palmitate + 2MSodium oleate + MC3H5(OH)3
⇔ 858 + 3.40 = 278 + 2MSodium oleate + 92
⇔ MSodium oleate = 304 (g/mol)
⇒ Điền đáp án: 304
Câu 26 [705699]: Các phức chất được tạo thành từ sự tương tác giữa cation Co3+ với đồng thời cả anion C2O42– (oxalate kí hiệu là ox) và phân tử H2O, có dạng [Co(OH2)x(ox)y]p+.Biết rằng trong các phức chất này:
∎ Cation Co3+ tạo được 6 liên kết sigma kiểu cho – nhận với các phối tử.
∎ Mỗi anion C2O42– sử dụng 2 cặp electron hoá trị riêng để tạo liên kết cho – nhận với cation kim loại.
Nếu số phối tử H2O trong phức chất [Co(OH2)x(ox)y]p+ là 4 thì giá trị của p bằng bao nhiêu?
∎ Cation Co3+ tạo được 6 liên kết sigma kiểu cho – nhận với các phối tử.
∎ Mỗi anion C2O42– sử dụng 2 cặp electron hoá trị riêng để tạo liên kết cho – nhận với cation kim loại.
Nếu số phối tử H2O trong phức chất [Co(OH2)x(ox)y]p+ là 4 thì giá trị của p bằng bao nhiêu?
Phức chất có dạng [Co(OH2)x(ox)y]p+, trong đó:
★ Co3+ (cation trung tâm) (điện tích +3) có số phối trí = 6, nghĩa là nó tạo 6 liên kết sigma kiểu cho – nhận với các phối tử.
★ Mỗi anion oxalate (C2O42-) (điện tích -2) tạo 2 liên kết cho – nhận, nên một oxalate chiếm 2 vị trí liên kết (phối tử 2 càng).
★ H2O là phối tử đơn càng (trung hòa, không mang điện tích) nên mỗi phân tử H2O chỉ chiếm 1 vị trí liên kết.
Nếu số phối tử H2O trong phức chất [Co(OH2)x(ox)y]p+ là 4, tức x = 4 và tổng số liên kết của Co3+ phải là 6 thì ta có:
x + 2 y= 6 ⇔ 4 + 2y = 6 ⇔ 2y = 2 ⇒ y=1
⟶ Phức chất có dạng [Co(OH2)4(ox)]p+.
⟶ Điện tích của phức là: p = +3 + (−2) = +1.
Vậy giá trị của p là 1.
⇒ Điền đáp án: 1
★ Co3+ (cation trung tâm) (điện tích +3) có số phối trí = 6, nghĩa là nó tạo 6 liên kết sigma kiểu cho – nhận với các phối tử.
★ Mỗi anion oxalate (C2O42-) (điện tích -2) tạo 2 liên kết cho – nhận, nên một oxalate chiếm 2 vị trí liên kết (phối tử 2 càng).
★ H2O là phối tử đơn càng (trung hòa, không mang điện tích) nên mỗi phân tử H2O chỉ chiếm 1 vị trí liên kết.
Nếu số phối tử H2O trong phức chất [Co(OH2)x(ox)y]p+ là 4, tức x = 4 và tổng số liên kết của Co3+ phải là 6 thì ta có:
x + 2 y= 6 ⇔ 4 + 2y = 6 ⇔ 2y = 2 ⇒ y=1
⟶ Phức chất có dạng [Co(OH2)4(ox)]p+.
⟶ Điện tích của phức là: p = +3 + (−2) = +1.
Vậy giá trị của p là 1.
⇒ Điền đáp án: 1
Câu 27 [706340]: Acetone [(CH3)2CO, M = 58g/mol, nhiệt độ sôi 56 oC] là một chất lỏng không màu và dễ cháy, là dung môi để làm sạch dụng cụ thủy tinh trong phòng thí nghiệm. Ở nhiệt độ 500-600 oC với xúc tác thích hợp, acetone phân hủy thành ethylene như sau:
(CH3)2CO → CO +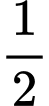 C2H4 + CH4.
C2H4 + CH4.
Sinh viên nghiên cứu sự phân hủy acetone ở 550 oC bằng cách cho acetone vào bình kín chịu nhiệt có dung tích không đổi (1 L) và ghi nhận sự thay đổi áp suất (P) của hỗn hợp phản ứng (X) theo thời gian sau mỗi 75 giây. Kết quả:
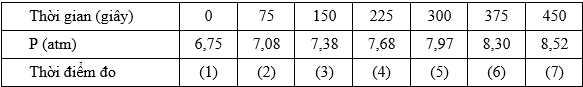
Kết quả đo áp suất ở thời điểm nào được nghi ngờ là sai lầm?
(CH3)2CO → CO +
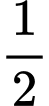 C2H4 + CH4.
C2H4 + CH4.Sinh viên nghiên cứu sự phân hủy acetone ở 550 oC bằng cách cho acetone vào bình kín chịu nhiệt có dung tích không đổi (1 L) và ghi nhận sự thay đổi áp suất (P) của hỗn hợp phản ứng (X) theo thời gian sau mỗi 75 giây. Kết quả:

Kết quả đo áp suất ở thời điểm nào được nghi ngờ là sai lầm?
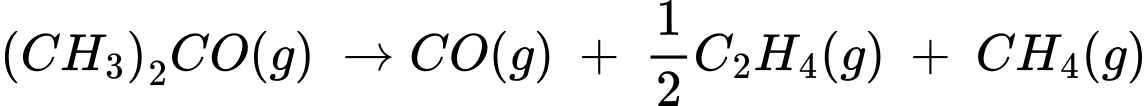
(2) t = 75 giây → ∆p = ps - pt = 7,08 – 6,75 = 0,33 atm
(3) t = 150 giây → ∆p = ps - pt = 7,38 – 7,08 = 0,3 atm
(4) t = 225 giây → ∆p = ps - pt = 7,68 – 7,38 = 0,3 atm
(5) t = 300 giây → ∆p = ps - pt = 7,97 – 6,68 = 0,29 atm
(6) t = 375 giây → ∆p = ps - pt = 8,3 – 7,97 = 0,33 atm
(7) t = 450 giây → ∆p = ps - pt = 8,52 – 8,3 = 0,22 atm
Sau phản ứng lượng biến thiên áp suất giảm dần, nhưng thời điểm thứ (6) biến thiên lại tăng nên đây là thời điểm nghi ngờ.
⟹ Điền đáp án : 6
Câu 28 [703961]: Có thể xác định nồng độ hypochlorite trong chất tẩy trắng bằng cách xử lí mẫu với lượng dư iodide ion trong dung dịch acid, quá trình này dẫn đến sự tạo thành triiodide ion theo phương trình: OCl–(aq) + 3I–(aq) + 2H3O+(aq) → Cl–(aq) + I3–(aq) + 3H2O(l)Sau đó, có thể chuẩn độ triiodide bởi sodium thiosulfate:
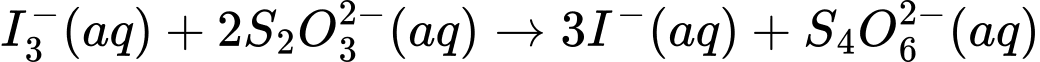
Khi xử lí 75,0 mL mẫu chất tẩy trắng dạng lỏng với lượng dư KI và acid, sau đó đem chuẩn độ với dung dịch sodium thiosulfate 0,0235 M. Quan sát được điểm cuối chuẩn độ là 21,23 mL. Nồng độ hypochlorite trong mẫu chất tẩy rửa là bao nhiêu mmol/L (mM)?
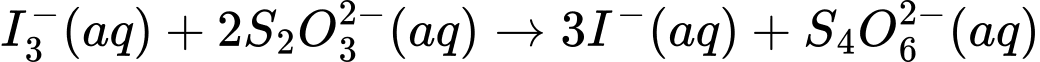
Khi xử lí 75,0 mL mẫu chất tẩy trắng dạng lỏng với lượng dư KI và acid, sau đó đem chuẩn độ với dung dịch sodium thiosulfate 0,0235 M. Quan sát được điểm cuối chuẩn độ là 21,23 mL. Nồng độ hypochlorite trong mẫu chất tẩy rửa là bao nhiêu mmol/L (mM)?
Đổi 75 mL = 0,075 mL; 21,23 mL = 0,02123 L
(1) ClO–(aq) + 3I–(aq) + 2H3O+(aq) ⟶ Cl–(aq) + I3–(aq) + 3H2O(l)
(2) I3–(aq) + 2S2O32–(aq) ⟶ 3I–(aq) + S4O62–(aq)
Số mol của sodium thiosulfate là 0,02123.0,0235 = 4,98905.10-4 (mol)
Từ phương trình (1) và (2) số mol của ClO– là 2,494525.10-4 (mol)
Nồng độ của hypochlorite là
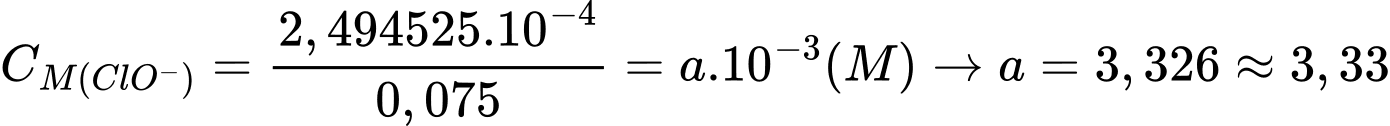
⇒ Điền đáp án: 3,33
(1) ClO–(aq) + 3I–(aq) + 2H3O+(aq) ⟶ Cl–(aq) + I3–(aq) + 3H2O(l)
(2) I3–(aq) + 2S2O32–(aq) ⟶ 3I–(aq) + S4O62–(aq)
Số mol của sodium thiosulfate là 0,02123.0,0235 = 4,98905.10-4 (mol)
Từ phương trình (1) và (2) số mol của ClO– là 2,494525.10-4 (mol)
Nồng độ của hypochlorite là
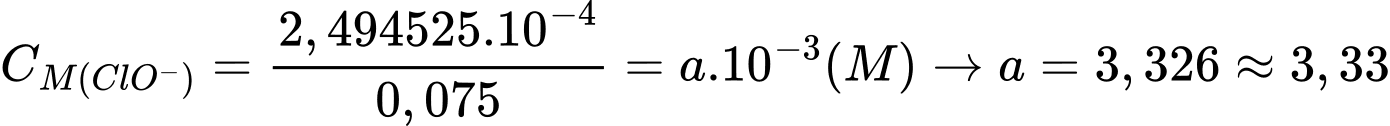
⇒ Điền đáp án: 3,33