PHẦN I. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
Câu 1 [247383]: Nguyên tử của nguyên tố R có cấu hình electron là 1s22s22p63s23p4. R có công thức oxide cao nhất là
A, RO3.
B, R2O3.
C, RO2.
D, R2O.
R thuộc nhóm VIA nên công thức oxide cao nhất RO3.
Lớp ngoài cùng của R có 6 electron (3s23p4).
R thuộc nhóm VIA trong bảng tuần hoàn.
Oxide cao nhất của nguyên tố nhóm VIA có dạng RO3.
Trong RO3, số oxi hóa của R là +6, bằng với số electron lớp ngoài cùng của R.
⟹ Chọn đáp án A Đáp án: A
Lớp ngoài cùng của R có 6 electron (3s23p4).
R thuộc nhóm VIA trong bảng tuần hoàn.
Oxide cao nhất của nguyên tố nhóm VIA có dạng RO3.
Trong RO3, số oxi hóa của R là +6, bằng với số electron lớp ngoài cùng của R.
⟹ Chọn đáp án A Đáp án: A
Câu 2 [702615]: Ester X có công thức cấu tạo CH3COOCH(CH3)CH2CH3. X có thể được điều chế bằng cách đun hồi lưu alcohol Y với ethanoic acid trong xúc tác H+. Tên gọi của Y là
A, butan-1-ol.
B, butan-2-ol.
C, butan-3-ol.
D, methylpropan-2-ol.
CH3COOH + CH3CH(OH)CH2CH3 (Y) -(H+)→ CH3COOCH(CH3)CH2CH3 (X) + H2O
⇒ Chọn đáp án B Đáp án: B
⇒ Chọn đáp án B Đáp án: B
Câu 3 [186755]: Acid X là hóa chất quan trọng trong nhiều ngành như sản xuất phân bón, luyện kim, chất dẻo, acquy, chất tẩy rửa…Trong phòng thí nghiệm acid X còn được dùng làm chất hút ẩm. Chất X là
A, H3PO4.
B, HNO3.
C, H2SO4.
D, HCl.
Acid này chính là acid sulfuric (H2SO4), vì:
- Ứng dụng rộng rãi:
+) H2SO4 là nguyên liệu chính để sản xuất phân bón (superphosphate, ammonium sulfate).
+) Dùng trong luyện kim để tẩy gỉ kim loại.
+) Làm chất điện li trong acquy chì.
+) Tham gia sản xuất nhựa, chất dẻo và chất tẩy rửa.
- Tính chất hút ẩm mạnh:H2SO4 có tính hút nước mạnh do đặc tính khử nước của nó, nên được dùng làm chất hút ẩm trong phòng thí nghiệm.
⇒ Chọn đáp án C Đáp án: C
- Ứng dụng rộng rãi:
+) H2SO4 là nguyên liệu chính để sản xuất phân bón (superphosphate, ammonium sulfate).
+) Dùng trong luyện kim để tẩy gỉ kim loại.
+) Làm chất điện li trong acquy chì.
+) Tham gia sản xuất nhựa, chất dẻo và chất tẩy rửa.
- Tính chất hút ẩm mạnh:H2SO4 có tính hút nước mạnh do đặc tính khử nước của nó, nên được dùng làm chất hút ẩm trong phòng thí nghiệm.
⇒ Chọn đáp án C Đáp án: C
Câu 4 [704027]: Các đồng phân của pentane C5H12 đều có phương trình đốt cháy là
C5H12 + 8O2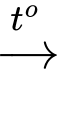 5CO2 + 6H2O
5CO2 + 6H2O
Tuy nhiên các giá trị ∆Ho cho sự đốt cháy của ba đồng phân pentane là khác nhau:
CH3CH2CH2CH2CH3 = –3536 kJ/mol
(CH3)2CHCH2CH3 = –3529 kJ/mol
(CH3)4C = –3515 kJ/mol
Từ các kết quả trên, một giả thuyết được đưa ra: “Cấu tạo mạch của các đồng phân alkane ảnh hưởng đến độ bền của một hợp chất, mạch càng nhiều nhánh thì độ bền càng lớn”. Giả sử giả thuyết này đúng với các hợp chất alkane, đồng phân nào sau đây của C8H18 (octane) là bền nhất?
C5H12 + 8O2
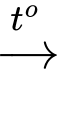 5CO2 + 6H2O
5CO2 + 6H2OTuy nhiên các giá trị ∆Ho cho sự đốt cháy của ba đồng phân pentane là khác nhau:
CH3CH2CH2CH2CH3 = –3536 kJ/mol
(CH3)2CHCH2CH3 = –3529 kJ/mol
(CH3)4C = –3515 kJ/mol
Từ các kết quả trên, một giả thuyết được đưa ra: “Cấu tạo mạch của các đồng phân alkane ảnh hưởng đến độ bền của một hợp chất, mạch càng nhiều nhánh thì độ bền càng lớn”. Giả sử giả thuyết này đúng với các hợp chất alkane, đồng phân nào sau đây của C8H18 (octane) là bền nhất?
A, n-octane.
B, 2-methylheptane.
C, 2,3,4-trimethylpentane.
D, 1,2,3-trimethylpentane.
Cấu tạo mạch của các đồng phân alkane ảnh hưởng đến độ bền của một hợp chất. Mạch càng nhiều nhánh thì độ bền càng lớn.
Cấu trúc các đồng phân của C8H18 (octane) như sau:
A. n-octane:
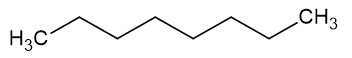
B. 2-methylheptane:
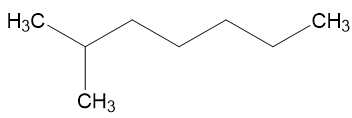
C. 2,3,4-trimethylpentane:
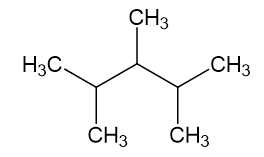
D. 2,3-trimethylpentane:
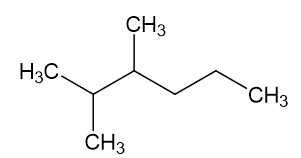
⟶ Đồng phân 2,3,4-trimethylpentane có nhiều nhánh nhất nên sẽ bền nhất.
⇒ Chọn đáp án C Đáp án: C
Cấu trúc các đồng phân của C8H18 (octane) như sau:
A. n-octane:

B. 2-methylheptane:

C. 2,3,4-trimethylpentane:

D. 2,3-trimethylpentane:

⟶ Đồng phân 2,3,4-trimethylpentane có nhiều nhánh nhất nên sẽ bền nhất.
⇒ Chọn đáp án C Đáp án: C
Câu 5 [702801]: Trong các phản ứng hóa học, nguyên tử kim loại dễ …(1)… hóa trị để tạo thành …(2)… kim loại. Nội dung phù hợp trong các ô trống (1), (2) lần lượt là
A, nhường electron, cation.
B, nhường electron, anion.
C, nhận electron, cation.
D, nhận electron, anion.
Trong các phản ứng hóa học, nguyên tử kim loại có tính khử nên dễ nhường electron hóa trị để tạo thành cation kim loại.
⇒ Chọn đáp án A Đáp án: A
⇒ Chọn đáp án A Đáp án: A
Câu 6 [704297]: Số nguyên tử carbon trong một phân tử maltose là
A, 5.
B, 12.
C, 11.
D, 22.
Saccharose và maltose là disaccharide có công thức phân tử chung: C12H22O11, là đồng phân của nhau.
Trong một phân tử maltose có 12 nguyên tử carbon.
⇒ Chọn đáp án B Đáp án: B
Trong một phân tử maltose có 12 nguyên tử carbon.
⇒ Chọn đáp án B Đáp án: B
Câu 7 [704197]: Số electron hóa trị của nguyên tử iron (sắt, Fe, Z = 26) là
A, 8.
B, 2.
C, 3.
D, 5.
Nếu cấu hình electron có dạng: (n – 1)dansb thì số electron hóa trị = a + b (Với n là STT lớp electron)
Cấu hình electron của Fe 1s22s22p63s23p63d64s2
⟶ Số electron hóa trị của Fe là: 6 + 2 = 8.
⇒ Chọn đáp án A Đáp án: A
Cấu hình electron của Fe 1s22s22p63s23p63d64s2
⟶ Số electron hóa trị của Fe là: 6 + 2 = 8.
⇒ Chọn đáp án A Đáp án: A
Câu 8 [252214]: Khi nhiệt độ tăng thêm 10oC, tốc độ phản ứng hoá học tăng thêm 4 lần. Tốc độ phản ứng đó sẽ giảm đi bao nhiêu lần nhiệt khi nhiệt độ giảm từ 70oC xuống 40oC?
A, 32 lần.
B, 64 lần.
C, 8 lần.
D, 16 lần.
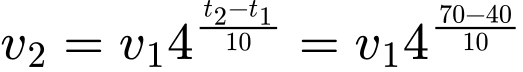 = 43v1 = V1.64
= 43v1 = V1.64Vậy, chọn đáp án B Đáp án: B
Câu 9 [308683]: Công thức của alanine là
A, C6H5NH2.
B, H2NCH2COOH.
C, CH3CH(NH2)COOH.
D, C2H5NH2.
Công thức phân tử của alanine là C3H7NO2.
Công thức cấu tạo thu gọn: NH2-CH(CH3)-COOH.
⇒ Chọn đáp án C Đáp án: C
Công thức cấu tạo thu gọn: NH2-CH(CH3)-COOH.
⇒ Chọn đáp án C Đáp án: C
Câu 10 [705984]: Để bảo vệ đường ống dẫn nước ngầm làm bằng thép, người ta thường gắn thêm các thanh kẽm lên ống. Điều này được giải thích là vì
A, kẽm bị ăn mòn trước, bảo vệ thép.
B, kẽm làm tăng độ bền cơ học cho thép.
C, ngăn chặn thép tiếp xúc với nước.
D, tăng khả năng dẫn điện của đường ống.
Chống ăn mòn kim loại: Phương pháp điện hoá: Nối kim loại cần bảo vệ với một kim loại hoạt động hoá học mạnh hơn.
Kẽm có độ hoạt động hóa học mạnh hơn Fe (có trong ống thép) nên kẽm sẽ bị ăn mòn trước.
⟹Chọn đáp án A Đáp án: A
Kẽm có độ hoạt động hóa học mạnh hơn Fe (có trong ống thép) nên kẽm sẽ bị ăn mòn trước.
⟹Chọn đáp án A Đáp án: A
Câu 11 [560690]: Với quá trình tách sodium bằng phương pháp điện phân sodium chloride nóng chảy, phát biểu nào sau đây là đúng?
A, Tại anode xảy ra quá trình khử ion Na+.
B, Tại cathode xảy ra quá trình khử ion Cl–.
C, Tại cathode xảy ra quá trình khử ion Na+.
D, Tại anode xảy ra quá trình khử ion Cl–.
Khi điện phân nóng chảy NaCl:
Anode (+) xảy ra quá trình oxi hóa: 2Cl- ⟶ Cl2 + 2e
Cathode (-) xảy ra quá trình khử: Na+ + 1e ⟶ Na
⇒ Chọn đáp án C Đáp án: C
Anode (+) xảy ra quá trình oxi hóa: 2Cl- ⟶ Cl2 + 2e
Cathode (-) xảy ra quá trình khử: Na+ + 1e ⟶ Na
⇒ Chọn đáp án C Đáp án: C
Câu 12 [560489]: Hãy xem xét ba pin điện, mỗi pin đều có cấu tạo như sơ đồ dưới đây:
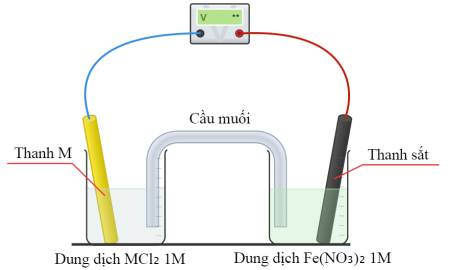
Trong mỗi pin điện, một nửa pin chứa dung dịch Fe(NO3)2(aq) 1,0 M với điện cực Fe. Thành phần của nửa pin còn lại như sau:
• Pin 1: Dung dịch CuCl2(aq) 1,0 M với điện cực Cu.
• Pin 2: Dung dịch NiCl2(aq) 1,0 M với điện cực Ni.
• Pin 3: Dung dịch ZnCl2(aq) 1,0 M với điện cực Zn.
Sắt đóng vai trò là cực dương trong (các) pin điện nào?

Trong mỗi pin điện, một nửa pin chứa dung dịch Fe(NO3)2(aq) 1,0 M với điện cực Fe. Thành phần của nửa pin còn lại như sau:
• Pin 1: Dung dịch CuCl2(aq) 1,0 M với điện cực Cu.
• Pin 2: Dung dịch NiCl2(aq) 1,0 M với điện cực Ni.
• Pin 3: Dung dịch ZnCl2(aq) 1,0 M với điện cực Zn.
Sắt đóng vai trò là cực dương trong (các) pin điện nào?
A, Pin 1.
B, Pin 2.
C, Pin 3.
D, Pin 1 và 2.
Vì sắt đóng vai trò là cực dương (cathode)
⇒ Điện cực anode phải có Eo bé hơn Eo Fe2+/Fe = -0,44
Biết: Eo Cu2+/Cu = +0,34 (V);
Eo Ni2+/Ni = -0,257 (V);
Eo Zn2+/Zn = -0,76 (V)
➝ Nhận thấy Eo Zn2+/Zn < Eo Fe2+/Fe
➝ Pin 3 là đáp án đúng.
⇒ Chọn đáp án C Đáp án: C
⇒ Điện cực anode phải có Eo bé hơn Eo Fe2+/Fe = -0,44
Biết: Eo Cu2+/Cu = +0,34 (V);
Eo Ni2+/Ni = -0,257 (V);
Eo Zn2+/Zn = -0,76 (V)
➝ Nhận thấy Eo Zn2+/Zn < Eo Fe2+/Fe
➝ Pin 3 là đáp án đúng.
⇒ Chọn đáp án C Đáp án: C
Câu 13 [186525]: Nitrogen thường được sử dụng làm khí bảo vệ cho dây tóc tungsten (vonfram) trong bóng đèn sợi đốt vì
A, Nitrogen không tan trong nước.
B, Nitrogen có tính trơ.
C, Nitrogen là phân tử không phân cực.
D, Nitrogen nhẹ hơn không khí.
Nitrogen là chất khá trơ về mặt hoá học, không phản ứng với kim loại, nên dùng khí trơ sẽ làm "tuổi thọ" của sợi đốt tăng cao. Ngoài ra, người ta nạp N2 vào bóng đèn điện thay vì nạp khí hiếm, do giá thành của N2 rẻ hơn nên làm giảm giá thành sản xuất bóng đèn điện.→ Đáp án B Đáp án: B
Câu 14 [704387]: Polypropylene là polymer được dùng chế tạo bao bì thực phẩm. Nó được tổng hợp từ propylene bằng phản ứng
A, trùng hợp.
B, trùng ngưng.
C, thế.
D, trao đổi.
Polypropylene là một polymer được tổng hợp từ monomer propylene (CH2=CH−CH3), được ứng dụng rộng rãi trong sản xuất bao bì thực phẩm, đồ gia dụng, và các sản phẩm nhựa.
Polypropylene được tổng hợp bằng phản ứng trùng hợp, các phân tử monomer propylene liên kết với nhau nhờ cơ chế mở liên kết đôi C=C, tạo thành chuỗi polymer dài:
nCH2=CH−CH3 −xt, to⟶ −[CH2−CH(CH3)]n−
Loại trừ các đáp án sai:
❌ B. Trùng ngưng: Sai, vì trùng ngưng xảy ra khi các monomer phản ứng với nhau bằng cách loại bỏ một phân tử nhỏ (như H2O hoặc HCl), ví dụ như trong tổng hợp nylon hoặc polyester. Polypropylene không hình thành theo cách này.
❌ C. Thế: Sai, vì phản ứng thế là sự thay thế một nguyên tử hoặc nhóm nguyên tử trong phân tử, không phù hợp với quá trình tạo polymer từ propylene.
❌ D. Trao đổi: Sai, vì phản ứng trao đổi thường liên quan đến sự hoán đổi nhóm chức giữa hai hợp chất, không liên quan đến phản ứng tạo polypropylene.
⇒ Chọn đáp án A Đáp án: A
Polypropylene được tổng hợp bằng phản ứng trùng hợp, các phân tử monomer propylene liên kết với nhau nhờ cơ chế mở liên kết đôi C=C, tạo thành chuỗi polymer dài:
nCH2=CH−CH3 −xt, to⟶ −[CH2−CH(CH3)]n−
Loại trừ các đáp án sai:
❌ B. Trùng ngưng: Sai, vì trùng ngưng xảy ra khi các monomer phản ứng với nhau bằng cách loại bỏ một phân tử nhỏ (như H2O hoặc HCl), ví dụ như trong tổng hợp nylon hoặc polyester. Polypropylene không hình thành theo cách này.
❌ C. Thế: Sai, vì phản ứng thế là sự thay thế một nguyên tử hoặc nhóm nguyên tử trong phân tử, không phù hợp với quá trình tạo polymer từ propylene.
❌ D. Trao đổi: Sai, vì phản ứng trao đổi thường liên quan đến sự hoán đổi nhóm chức giữa hai hợp chất, không liên quan đến phản ứng tạo polypropylene.
⇒ Chọn đáp án A Đáp án: A
Câu 15 [57711]: Cho từ từ đến dư một lượng bột sắt vào trong bình đựng một lượng nhỏ khí clo đã được đun nóng. Sau khi các phản ứng xảy ra hoàn toàn, chất rắn thu được trong bình là
A, FeCl2 .
B, FeCl2 và FeCl3.
C, Fe và FeCl2.
D, Fe và FeCl3.
2Fe + 3Cl2 –to⟶ 2FeCl3
Chú ý: Chỉ trong dung dịch thì Fe dư mới có thể phản ứng với FeCl3 để tạo thành FeCl2:
Fe + 2FeCl3 –to⟶ 3FeCl2
Vậy sau phản ứng chất rắn gồm Fe, FeCl3.
⇒ Chọn đáp án D. Đáp án: D
Chú ý: Chỉ trong dung dịch thì Fe dư mới có thể phản ứng với FeCl3 để tạo thành FeCl2:
Fe + 2FeCl3 –to⟶ 3FeCl2
Vậy sau phản ứng chất rắn gồm Fe, FeCl3.
⇒ Chọn đáp án D. Đáp án: D
Câu 16 [705936]: Một mẫu nước có chứa các ion Ca2+, [Cu(OH2)6]2+, [Fe(OH2)6]2+, Na+, Cl–, SO42–. Sau một thời gian tiếp xúc với không khí, mẫu nước này chuyển sang màu vàng và nổi váng màu nâu do quá trình:
[M(OH2)6]n+(aq) + mH2O(l) ⇌ [M(OH)m(OH2)6–m](n–m)+(aq hoặc s) + mH3O+(aq) (3)
Cho các phát biểu sau:
(a) Mẫu nước trên có pH lớn hơn 7.
(b) Ion bị oxi hoá và gây nên hiện tượng trên là [Fe(OH2)6]2+.
(c) Trong nước, ion H+ nhận cặp electron từ H2O để tạo thành ion H3O+.
(d) Chất màu nâu sinh trong mô tả trên là phức chất có công thức là [Fe(OH)2(OH2)4].
Các phát biểu đúng là
[M(OH2)6]n+(aq) + mH2O(l) ⇌ [M(OH)m(OH2)6–m](n–m)+(aq hoặc s) + mH3O+(aq) (3)
Cho các phát biểu sau:
(a) Mẫu nước trên có pH lớn hơn 7.
(b) Ion bị oxi hoá và gây nên hiện tượng trên là [Fe(OH2)6]2+.
(c) Trong nước, ion H+ nhận cặp electron từ H2O để tạo thành ion H3O+.
(d) Chất màu nâu sinh trong mô tả trên là phức chất có công thức là [Fe(OH)2(OH2)4].
Các phát biểu đúng là
A, (a), (b).
B, (b), (c).
C, (a), (b), (c).
D, (b), (c), (d).
Phân tích các phát biểu:
❌(a) – Sai. Mẫu nước trên có pH nhỏ hơn 7. Trong quá trình phức chất phân li trong nước sinh ra H3O+ có tính acid nên tạo môi trường acid có pH nhỏ hơn 7.
✔️(b) – Đúng. Sau một thời gian tiếp xúc với không khí, mẫu nước này chuyển sang màu vàng và nổi váng màu nâu do quá trình lon bị oxi hoá và gây nên hiện tượng trên chất phù hợp là [Fe(OH2)6]2+.
✔️(c) – Đúng. Thuyết bronsted – Lowry: Acid là chất cho proton (H+), base là chất nhận proton. Acid và base có thể là phân tử hoặc ion.H+ + H2O → H3O+
❌(d) – Sai. Chất trong mô tả trên là phức chất có công thức là [Fe(OH)2(OH2)4] có màu trắng xanh, sau khi tiếp xúc với không khí chuyển sang màu vàng và nổi váng màu nâu.
Các phát biểu đúng là (b), (c)
⟹ Chọn đáp án B Đáp án: B
❌(a) – Sai. Mẫu nước trên có pH nhỏ hơn 7. Trong quá trình phức chất phân li trong nước sinh ra H3O+ có tính acid nên tạo môi trường acid có pH nhỏ hơn 7.
✔️(b) – Đúng. Sau một thời gian tiếp xúc với không khí, mẫu nước này chuyển sang màu vàng và nổi váng màu nâu do quá trình lon bị oxi hoá và gây nên hiện tượng trên chất phù hợp là [Fe(OH2)6]2+.
✔️(c) – Đúng. Thuyết bronsted – Lowry: Acid là chất cho proton (H+), base là chất nhận proton. Acid và base có thể là phân tử hoặc ion.H+ + H2O → H3O+
❌(d) – Sai. Chất trong mô tả trên là phức chất có công thức là [Fe(OH)2(OH2)4] có màu trắng xanh, sau khi tiếp xúc với không khí chuyển sang màu vàng và nổi váng màu nâu.
Các phát biểu đúng là (b), (c)
⟹ Chọn đáp án B Đáp án: B
Sử dụng thông tin ở bảng dưới đây để trả lời các câu 17 - 18:
Leucine là một trong những amino acid thiết yếu, cơ thể không thểtự tổng hợp được mà phải lấy từ thức ăn. Leucine được tìm thấy có trong thịt, cá, gia cầm. Leucine có khả năng kích thích sự tổng hợp protein, giúp cơ thể để xây dựng cơ bắp. Công thức cấu tạo của leucine được cho trong hình vẽ bên.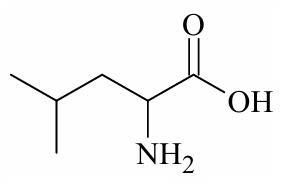
Câu 17 [705840]: Leucine không tham gia phản ứng với dung dịch nào dưới đây?
A, dung dịch NaOH.
B, Dung dịch HCl.
C, Ethanol (xúc tác H2SO4 đặc).
D, Dung dịch NaCl.
- Tính acid – base: Amino acid vừa tác dụng với acid mạnh tạo muối ammonium, vừa tác dụng được với base mạnh tạo muối carboxylate. Vì thế, amino acid là những hợp chất lưỡng tính.
- Phản ứng tạo ester của nhóm – COOH: Tương tự như carboxylic acid, amino acid có thể tác dụng với alcohol khi có mặt xúc tác acid mạnh để tạo thành ester.
Phân tích các đáp án:
✔️A. NaOH là base
✔️B. HCl là acid
✔️C. Ethanol là alcohol
❌D. NaCl là muối
⟹ Chọn đáp án D Đáp án: D
- Phản ứng tạo ester của nhóm – COOH: Tương tự như carboxylic acid, amino acid có thể tác dụng với alcohol khi có mặt xúc tác acid mạnh để tạo thành ester.
Phân tích các đáp án:
✔️A. NaOH là base
✔️B. HCl là acid
✔️C. Ethanol là alcohol
❌D. NaCl là muối
⟹ Chọn đáp án D Đáp án: D
Câu 18 [705841]: Cho 0,2 mol leucine tham gia phản ứng với dung dịch KOH vừa đủ, dung dịch thu được đem cô cạn thu được bao nhiêu gam muối?
A, 34,0.
B, 30,8.
C, 30,8.
D, 33,8.
Phương trình phản ứng:
CH3CH(CH3)CH2CH(NH2)COOH + KOH → CH3CH(CH3)CH2CH(NH2)COOK + H2O
Từ phương trình hóa học số mol của muối là 0,2 mol
Khối lượng của muối là mmuối = 0,2 × 169 = 33,8 gam
⟹ Chọn đáp án D Đáp án: D
CH3CH(CH3)CH2CH(NH2)COOH + KOH → CH3CH(CH3)CH2CH(NH2)COOK + H2O
Từ phương trình hóa học số mol của muối là 0,2 mol
Khối lượng của muối là mmuối = 0,2 × 169 = 33,8 gam
⟹ Chọn đáp án D Đáp án: D
PHẦN II. Thí sinh trả lời từ câu 1 đến câu 4. Trong mỗi ý a), b), c), d) ở mỗi câu, thí sinh chọn đúng hoặc sai.
Câu 19 [308432]: Tiến hành thí nghiệm phản ứng của hồ tinh bột với iodine theo các bước sau đây:
Bước 1: Cho vài giọt dung dịch iodine vào ống nghiệm đựng sẵn 1 – 2 mL dung dịch hồ tinh bột (hoặc nhỏ vài giọt dung dịch iodine lên mặt cắt quả chuối xanh hoặc củ khoai lang tươi, sắn tươi).
Bước 2: Đun nóng dung dịch một lát, sau đó để nguội.
Bước 1: Cho vài giọt dung dịch iodine vào ống nghiệm đựng sẵn 1 – 2 mL dung dịch hồ tinh bột (hoặc nhỏ vài giọt dung dịch iodine lên mặt cắt quả chuối xanh hoặc củ khoai lang tươi, sắn tươi).
Bước 2: Đun nóng dung dịch một lát, sau đó để nguội.
HD: Phân tích thí nghiệm:

• Bước 1: dung dịch I2 là dung dịch có màu vàng nhạt, khi tương tác với hồ tinh bột sẽ tạo thành màu xanh tím đặc trưng. Giải thích: phân tử tinh bột có tạo mạch ở dạng xoắn có lỗ rỗng (giống như lò xo):

⇝ các phân tử iot có thể chui vào và bị hấp phụ, tạo “hợp chất” màu xanh tím.
• Bước 2: khi đun nóng, các phân tử tinh bột sẽ duỗi xoắn, không thể hấp phụ được iot nữa
⇝ màu xanh tím bị mất đi. Chú ý, bước 2 không làm iot bay hơi, thăng hoa hoàn toàn được.
• Sau đó: khi làm nguội, phân tử tinh bột trở lại dạng xoắn, các phân tử iot lại bị hấp phụ, chui vào lỗ rỗng xoắn thu được “hợp chất” màu xanh tím như sau bước 1.
⇒ Phân tích các phát biểu:
✔️ a. Đúng. Theo hiện tượng phân tích trên.
❌ b. Sai. Chuối chín không có tinh bột nữa (đã chuyển hóa thành các đường như glucose, fructose ⇒ chuối chín có vị ngọt).
✔️ c. Đúng. Theo phân tích trên.
✔️ d. Đúng. Theo phân tích trên.

• Bước 1: dung dịch I2 là dung dịch có màu vàng nhạt, khi tương tác với hồ tinh bột sẽ tạo thành màu xanh tím đặc trưng. Giải thích: phân tử tinh bột có tạo mạch ở dạng xoắn có lỗ rỗng (giống như lò xo):

⇝ các phân tử iot có thể chui vào và bị hấp phụ, tạo “hợp chất” màu xanh tím.
• Bước 2: khi đun nóng, các phân tử tinh bột sẽ duỗi xoắn, không thể hấp phụ được iot nữa
⇝ màu xanh tím bị mất đi. Chú ý, bước 2 không làm iot bay hơi, thăng hoa hoàn toàn được.
• Sau đó: khi làm nguội, phân tử tinh bột trở lại dạng xoắn, các phân tử iot lại bị hấp phụ, chui vào lỗ rỗng xoắn thu được “hợp chất” màu xanh tím như sau bước 1.
⇒ Phân tích các phát biểu:
✔️ a. Đúng. Theo hiện tượng phân tích trên.
❌ b. Sai. Chuối chín không có tinh bột nữa (đã chuyển hóa thành các đường như glucose, fructose ⇒ chuối chín có vị ngọt).
✔️ c. Đúng. Theo phân tích trên.
✔️ d. Đúng. Theo phân tích trên.
Câu 20 [705697]: Tiến hành nhỏ vài giọt hỗn hợp chứa các amino acid: arginine, alanine và aspatic acid vào giữa một tờ giấy lọc. Đặt tờ giấy lọc vào dung dịch đệm có pH = 6 giữa hai điện cực và có điện trường tác dụng thu được kết quả như hình dưới đây.
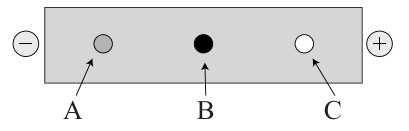
Công thức của arginine và aspatic acid được cho trong bảng
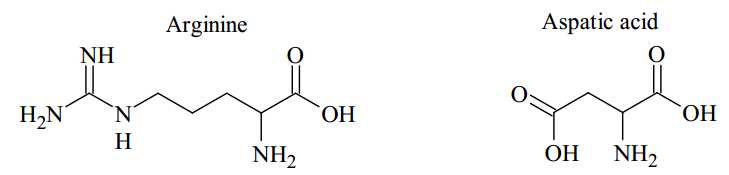

Công thức của arginine và aspatic acid được cho trong bảng

Ở pH trung tính, môi trường trung tính, amino acid tồn tại ở dạng ion lưỡng cực như sau:
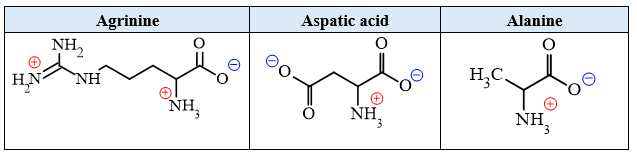
+) Aspartic acid tồn tại chủ yếu dưới dạng anion (-1) → bị kéo về cực dương → C là aspartic acid.
+) Alanine trung hòa, gần như không di chuyển trong điện trường → B là alanine.
+) Arginine tồn tại chủ yếu dưới dạng cation (+1) → bị kéo về cực âm → A là arginine.
Phân tích các phát biểu:
✔️ a) Đúng. Có thể tách riêng arginine, alanine và aspatic acid tại pH = 6 bằng phương pháp điện di vì các amino acid có điện tích khác nhau nên sẽ di chuyển về các hướng khác nhau trong điện trường.
❌ b) Sai. Tại pH = 6, A là arginine (dạng cation), C là aspartic acid (dạng anion).
✔️ c) Đúng. B (Alanine) ở dạng trung hòa nên có điện tích bằng 0 và C (Aspartic acid) mang điện tích -1.
✔️ d) Đúng. Ở pH thấp (pH = 2), môi trường có tính acid, chứa nhiều ion H+ nên arginine và aniline sẽ phản ứng với H+ để tạo thành dạng cation mang điện tích dương (+) → bị kéo về cực âm.

+) Aspartic acid tồn tại chủ yếu dưới dạng anion (-1) → bị kéo về cực dương → C là aspartic acid.
+) Alanine trung hòa, gần như không di chuyển trong điện trường → B là alanine.
+) Arginine tồn tại chủ yếu dưới dạng cation (+1) → bị kéo về cực âm → A là arginine.
Phân tích các phát biểu:
✔️ a) Đúng. Có thể tách riêng arginine, alanine và aspatic acid tại pH = 6 bằng phương pháp điện di vì các amino acid có điện tích khác nhau nên sẽ di chuyển về các hướng khác nhau trong điện trường.
❌ b) Sai. Tại pH = 6, A là arginine (dạng cation), C là aspartic acid (dạng anion).
✔️ c) Đúng. B (Alanine) ở dạng trung hòa nên có điện tích bằng 0 và C (Aspartic acid) mang điện tích -1.
✔️ d) Đúng. Ở pH thấp (pH = 2), môi trường có tính acid, chứa nhiều ion H+ nên arginine và aniline sẽ phản ứng với H+ để tạo thành dạng cation mang điện tích dương (+) → bị kéo về cực âm.
Câu 21 [705450]: Một hợp chất X chứa nhóm chức carbonyl được tiến hành hành nghiên cứu tính chất hóa học như sau:
∎ X không có phản ứng với thuốc thử Tollens.
∎ X không có phản ứng iodoform.
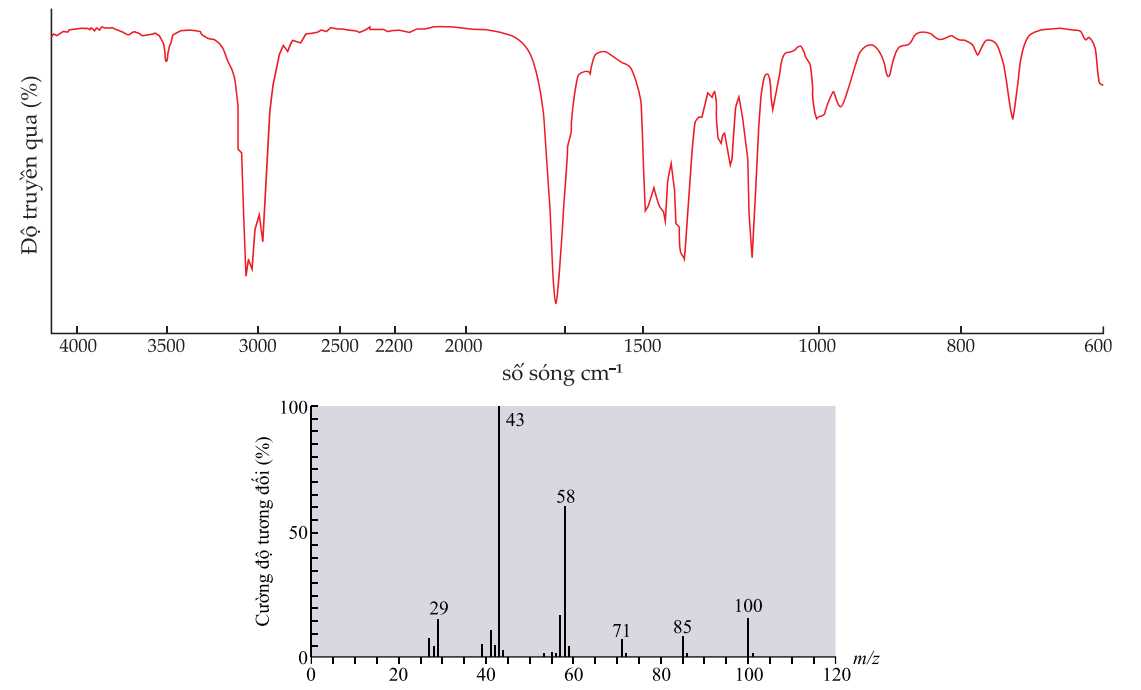
Kết quả phổ hồng ngoại (phổ IR) và phổ khối lượng (phổ MS) của hợp chất X được cho dưới đây:
∎ X không có phản ứng với thuốc thử Tollens.
∎ X không có phản ứng iodoform.
Kết quả phổ hồng ngoại (phổ IR) và phổ khối lượng (phổ MS) của hợp chất X được cho dưới đây:

Một hợp chất X chứa nhóm chức carbonyl được tiến hành hành nghiên cứu tính chất hóa học như sau:
X không có phản ứng với thuốc thử Tollens → X không có nhóm chức -CHO
X không có phản ứng iodoform → X không có dạng CH3-CO-R
Từ phổ hồng ngoại X có tín hiệu ở khoảng số sóng 1700 cm-1 đặc trưng cho liên kết C=O.
Từ phổ MS thấy phân tử khối của X là 100 gam/mol
Gọi công thức của X có dạng CxHyOz
MX = 12x + y + 16z = 100 (gam/mol)
Với z = 1 → x = 6; y = 12
Công thức phân tử của X là C6H12O
Với z = 2 → x = 5; y = 8
Công thức phân tử của X là C5H8O2 (loại vì không có CTCT phù hợp)
Với z = 4 → giá trị x = 2; y = 4 là phù hợp
Công thức phân tử của X là C4H4O3 (loại vì không có CTCT phù hợp)
Khi giá trị z càng lớn thì không có công thức cấu tạo của X thỏa mãn yêu cầu bài ra.
→ X có công thức phân tử là C6H12O
Các công thức cấu tạo thỏa mãn của X là:
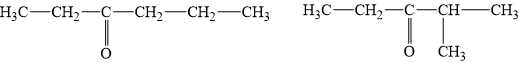
Phân tích các phát biểu:
✔️ a) Đúng. Từ phổ hồng ngoại X có tín hiệu ở khoảng số sóng 1700 cm-1 đặc trưng cho liên kết C=O.
✔️ b) Đúng. X không có phản ứng iodoform → X không có dạng CH3-CO-R
❌ c) Sai. Công thức phân tử của hợp chất X là C6H12O.
❌ d) Sai. X có 2 công thức cấu tạo tỏa mãn điều kiện đề bài.
X không có phản ứng với thuốc thử Tollens → X không có nhóm chức -CHO
X không có phản ứng iodoform → X không có dạng CH3-CO-R
Từ phổ hồng ngoại X có tín hiệu ở khoảng số sóng 1700 cm-1 đặc trưng cho liên kết C=O.
Từ phổ MS thấy phân tử khối của X là 100 gam/mol
Gọi công thức của X có dạng CxHyOz
MX = 12x + y + 16z = 100 (gam/mol)
Với z = 1 → x = 6; y = 12
Công thức phân tử của X là C6H12O
Với z = 2 → x = 5; y = 8
Công thức phân tử của X là C5H8O2 (loại vì không có CTCT phù hợp)
Với z = 4 → giá trị x = 2; y = 4 là phù hợp
Công thức phân tử của X là C4H4O3 (loại vì không có CTCT phù hợp)
Khi giá trị z càng lớn thì không có công thức cấu tạo của X thỏa mãn yêu cầu bài ra.
→ X có công thức phân tử là C6H12O
Các công thức cấu tạo thỏa mãn của X là:
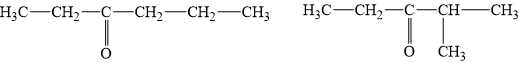
Phân tích các phát biểu:
✔️ a) Đúng. Từ phổ hồng ngoại X có tín hiệu ở khoảng số sóng 1700 cm-1 đặc trưng cho liên kết C=O.
✔️ b) Đúng. X không có phản ứng iodoform → X không có dạng CH3-CO-R
❌ c) Sai. Công thức phân tử của hợp chất X là C6H12O.
❌ d) Sai. X có 2 công thức cấu tạo tỏa mãn điều kiện đề bài.
Câu 22 [705695]: Tiến hành thí nghiệm so sánh độ tan của CaSO4 và BaSO4 như sau:
∎ Bước 1: Cho 2 mL dung dịch BaCl2 vào ống nghiệm (1), 2 mL dung dịch CaCl2 vào ống nghiệm (2).
∎ Bước 2: Cho từ từ từng giọt dung dịch CuSO4 vào mỗi ống nghiệm và lắc đều cho đến khi có kết tủa trong ống nghiệm thì dừng lại.
∎ Bước 1: Cho 2 mL dung dịch BaCl2 vào ống nghiệm (1), 2 mL dung dịch CaCl2 vào ống nghiệm (2).
∎ Bước 2: Cho từ từ từng giọt dung dịch CuSO4 vào mỗi ống nghiệm và lắc đều cho đến khi có kết tủa trong ống nghiệm thì dừng lại.
Phản ứng xảy ra trong từng ống nghiệm:
Khi nhỏ từ từ dung dịch CuSO4 vào BaCl2 và CaCl2, ta có:
Ống nghiệm (1): BaCl2 + CuSO4 → BaSO4↓ + CuCl2
BaSO4 có độ tan rất nhỏ, gần như không tan, tạo kết tủa trắng ngay khi có đủ ion SO42-.
Ống nghiệm (2): CaCl2 + CuSO4 → CaSO4↓ + CuCl2
CaSO4 có độ tan lớn hơn BaSO4 nên khi thêm CuSO4 có thể chỉ xuất hiện vẩn đục nhẹ hoặc không tạo kết tủa ngay.
Phân tích các phát biểu:
❌ a) Sai. BaSO4 rất khó tan, tạo kết tủa trắng rõ ràng chứ không chỉ là vẩn đục nhẹ.
❌ b) Sai. Ống nghiệm (2) chứa CaCl2, nên kết tủa là CaSO4, không phải BaSO4.
✔️ c) Đúng. Các ion Cl⁻ và Cu²⁺ không có mặt trong phương trình ion rút gọn:
Ba2+ + SO42- → BaSO4 ↓
Ca2+ + SO42- → CaSO4 ↓
Cl- và Cu2+ không tham gia vào phản ứng kết tủa.
❌ d) Sai. BaSO4 kết tủa nhanh và hoàn toàn, còn CaSO4 chỉ vẩn đục nhẹ, chứng tỏ BaSO4 ít tan hơn CaSO4, không phải ngược lại.
(Kết luận: BaSO4 không tan trong nước còn CaSO4 ít tan trong nước)
Khi nhỏ từ từ dung dịch CuSO4 vào BaCl2 và CaCl2, ta có:
Ống nghiệm (1): BaCl2 + CuSO4 → BaSO4↓ + CuCl2
BaSO4 có độ tan rất nhỏ, gần như không tan, tạo kết tủa trắng ngay khi có đủ ion SO42-.
Ống nghiệm (2): CaCl2 + CuSO4 → CaSO4↓ + CuCl2
CaSO4 có độ tan lớn hơn BaSO4 nên khi thêm CuSO4 có thể chỉ xuất hiện vẩn đục nhẹ hoặc không tạo kết tủa ngay.
Phân tích các phát biểu:
❌ a) Sai. BaSO4 rất khó tan, tạo kết tủa trắng rõ ràng chứ không chỉ là vẩn đục nhẹ.
❌ b) Sai. Ống nghiệm (2) chứa CaCl2, nên kết tủa là CaSO4, không phải BaSO4.
✔️ c) Đúng. Các ion Cl⁻ và Cu²⁺ không có mặt trong phương trình ion rút gọn:
Ba2+ + SO42- → BaSO4 ↓
Ca2+ + SO42- → CaSO4 ↓
Cl- và Cu2+ không tham gia vào phản ứng kết tủa.
❌ d) Sai. BaSO4 kết tủa nhanh và hoàn toàn, còn CaSO4 chỉ vẩn đục nhẹ, chứng tỏ BaSO4 ít tan hơn CaSO4, không phải ngược lại.
(Kết luận: BaSO4 không tan trong nước còn CaSO4 ít tan trong nước)
PHẦN III. Thí sinh trả lời từ câu 1 đến 6. Thí sinh điền kết quả mỗi câu vào mỗi ô trả lời tương ứng theo hướng dẫn của phiếu trả lời.
Câu 23 [704212]: Một mẫu nước cứng có nồng độ các ion như sau: Ca2+ x M; Mg2+ y M; HCO3– 0,005 M; Cl– 0,004 M; SO42– 0,001 M. Để làm mềm 10 L nước này cần dùng tối thiểu bao nhiêu gam sodium carbonate? (Làm tròn kết quả đến hàng phần mười)
Phản ứng của nước cứng với sodium carbonate xảy ra như sau:
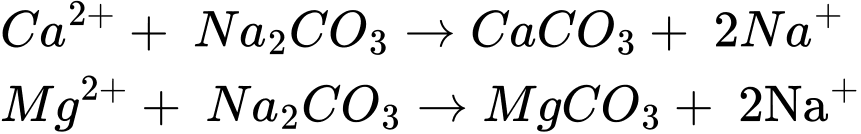
Số mol của Ca2+ và Mg2+ trong 10 L nước cứng lần lượt là 10x và 10y mol
Từ PTHH ta có:
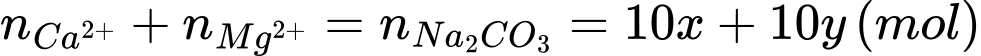
Áp dụng định luật bảo toàn điện tích:
20x + 20y = 0,005.10 + 0,004.10 + 0,001.10.2
→ 10x + 10y = 0,055 (mol)
Khối lượng Na2CO3 cần dùng để làm mềm 10 L nước cứng trên là
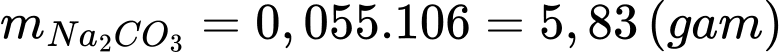 ≈ 5,8 gam.
≈ 5,8 gam.
⇒ Điền đáp án: 5,8
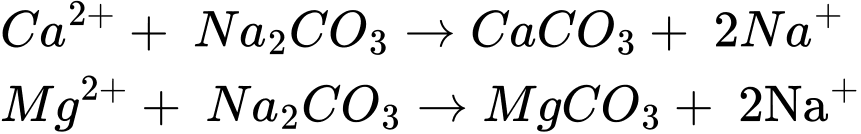
Số mol của Ca2+ và Mg2+ trong 10 L nước cứng lần lượt là 10x và 10y mol
Từ PTHH ta có:
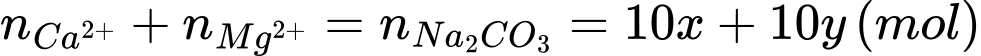
Áp dụng định luật bảo toàn điện tích:
20x + 20y = 0,005.10 + 0,004.10 + 0,001.10.2
→ 10x + 10y = 0,055 (mol)
Khối lượng Na2CO3 cần dùng để làm mềm 10 L nước cứng trên là
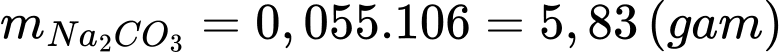 ≈ 5,8 gam.
≈ 5,8 gam.⇒ Điền đáp án: 5,8
Câu 24 [704014]: Trong thành phần của dầu oliu có chứa một số chất béo, trong đó chủ yếu là chất X có cấu trúc như hình dưới đây.
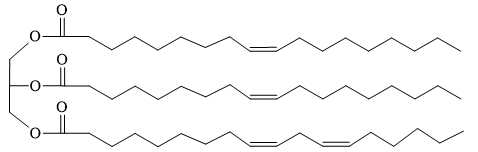
Đun nóng chất béo X với dung dịch KOH thu được hỗn hợp hai muối potassium Y và Z. Giá trị khối lượng phân tử lớn nhất của muối postassium thu được là bao nhiêu?

Đun nóng chất béo X với dung dịch KOH thu được hỗn hợp hai muối potassium Y và Z. Giá trị khối lượng phân tử lớn nhất của muối postassium thu được là bao nhiêu?
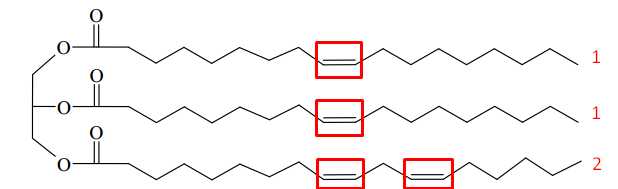
Từ cấu trúc của chất béo X thấy X được tạo nên từ 2 loại acid béo:
+ Loại 1 có 1 liên kết π có CTPT CnH2n-1COOH, có 17 carbon nên CTPT của acid 1 là C17H33COOH ⟶ Muối tạo thành từ acid này và potassium là C17H33COOK (M = 320).
+ Loại 2 có 2 liên kết π có CTPT CnH2n-3COOH, có 17 carbon nên CTPT của acid 1 là C17H31COOH ⟶ Muối tạo thành từ acid này và potassium là C17H31COOK (M = 318).
⇒ Giá trị khối lượng phân tử lớn nhất của muối postassium thu được là 320 (gam/mol).
⇒ Điền đáp án: 320
Câu 25 [1010070]: Chlorinated poly(vinyl chloride) (CPVC) có tính năng tương tự PVC, nhưng khả năng chịu nhiệt cao hơn, chống cháy tốt hơn và chịu được áp suất cao hơn. Người ta điều chế CPVC bằng cách cho khí chlorine đi vào dung dịch PVC trong tetrachloroethane ở 50 oC – 100 oC. Từ 9 tấn PVC thu được bao nhiêu tấn CPVC? Giả thiết CPVC thu được chứa 67,62% chlorine theo khối lượng và hiệu suất phản ứng đạt 95% (làm tròn kết quả đến hàng phần mười).
9 tấn PVC + x tấn mol Cl2 → y tấn CPVC + x tấn mol HCl
Bảo toàn khối lượng: 9 + 71x = y + 36,5x (1)
Bảo toàn nguyên tố Cl:
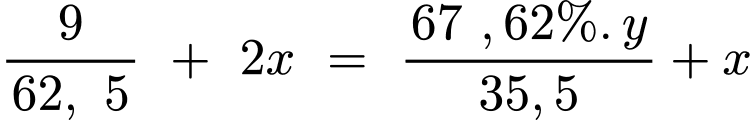 (2)
(2)
Từ (1) và (2) => x = 0 ,081 mol ; y = 11,83 tấn
Do H = 95% → mCPVC = 95%.y = 11,2 (tấn)
Điền đáp án: 11,2
Bảo toàn khối lượng: 9 + 71x = y + 36,5x (1)
Bảo toàn nguyên tố Cl:
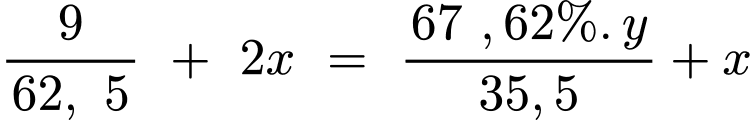 (2)
(2)Từ (1) và (2) => x = 0 ,081 mol ; y = 11,83 tấn
Do H = 95% → mCPVC = 95%.y = 11,2 (tấn)
Điền đáp án: 11,2
Câu 26 [309527]: Kevlar là một polyamide có độ bền kéo rất cao. Loại vật liệu này được dùng để sản xuất áo chống đạn và mũ bảo hiểm cho quân đội. Kevlar được điều chế bằng phản ứng trùng ngưng của hai chất sau:
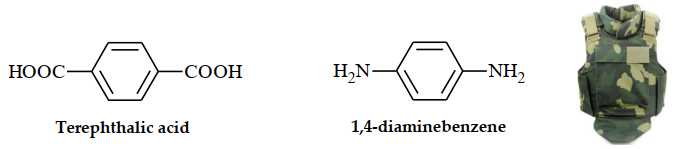
Trong một mắt xích của Kevlar có chứa bao nhiêu nguyên tử oxygen?
Điền đáp án: [..........]

Trong một mắt xích của Kevlar có chứa bao nhiêu nguyên tử oxygen?
Điền đáp án: [..........]
Công thức cấu tạo của Kevlar là:
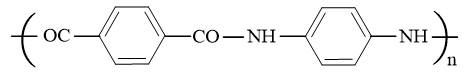
→ Trong một mắt xích của Kevlar có chứa 2 nguyên tử oxygen.
⇒ Điền đáp án: 2
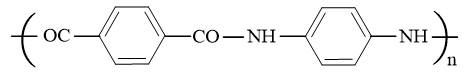
→ Trong một mắt xích của Kevlar có chứa 2 nguyên tử oxygen.
⇒ Điền đáp án: 2
Câu 27 [705563]: Phức chất [X(NH3)6]3+ có 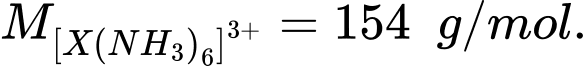 Nguyên tử khối của nguyên tử X là bao nhiêu?
Nguyên tử khối của nguyên tử X là bao nhiêu?
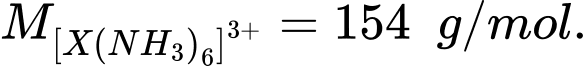 Nguyên tử khối của nguyên tử X là bao nhiêu?
Nguyên tử khối của nguyên tử X là bao nhiêu?
Phức chất [X(NH3)6]3+ có khối lượng phân tử là 154
→ MX + 17 × 6 = 154
→ MX = 52
⇒ Điền đáp án: 52
→ MX + 17 × 6 = 154
→ MX = 52
⇒ Điền đáp án: 52
Câu 28 [705901]: Tác hại của H2S đến môi trường là gây ô nhiễm nguồn nước, ô nhiễm đất, ảnh hưởng đến sức khỏe của con người và động vật. Bên cạnh đó, H2S trong không khí có thể gây ra các vấn đề về sức khỏe hô hấp, cũng như ảnh hưởng đến chất lượng không khí. Tại một phòng thí nghiệm, để kiểm tra hàm lượng hydrogen sulfide có trong mẫu khí lấy từ bãi rác, người ta sục mẫu khí vào dung dịch lead(II) nitrate dư với tốc độ 3 lít mẫu khí/phút trong 5 giờ. Lọc tách kết tủa và đem sấy khô thu được 4,302 mg chất rắn màu đen. Hàm lượng hydrogen sulfide có trong mẫu khí là a×10–4 (tính theo đơn vị mg/m3). Xác định giá trị của a.
Đổi 5 giờ = 300 phút
Thể tích khí H2S là VH2S = 300.3 = 900 L
Số mol của PbS là nPbS = 4,302:239 = 0,018 mmol
H2S + Pb(NO3)2 → PbS + 2HNO3
Từ PTHH số mol của H2S là 0,018 mmol
Hàm lượng H2S trong mẫu khí là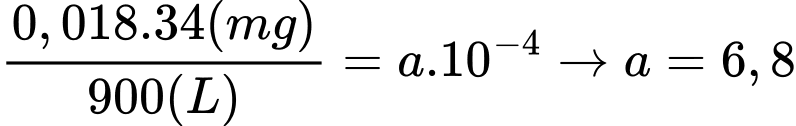
Điền đáp án : 6,8
Thể tích khí H2S là VH2S = 300.3 = 900 L
Số mol của PbS là nPbS = 4,302:239 = 0,018 mmol
H2S + Pb(NO3)2 → PbS + 2HNO3
Từ PTHH số mol của H2S là 0,018 mmol
Hàm lượng H2S trong mẫu khí là
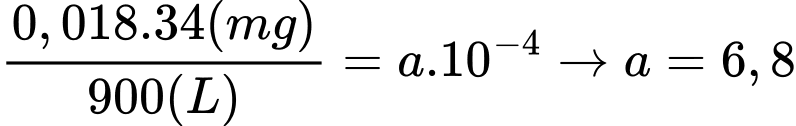
Điền đáp án : 6,8