PHẦN I. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
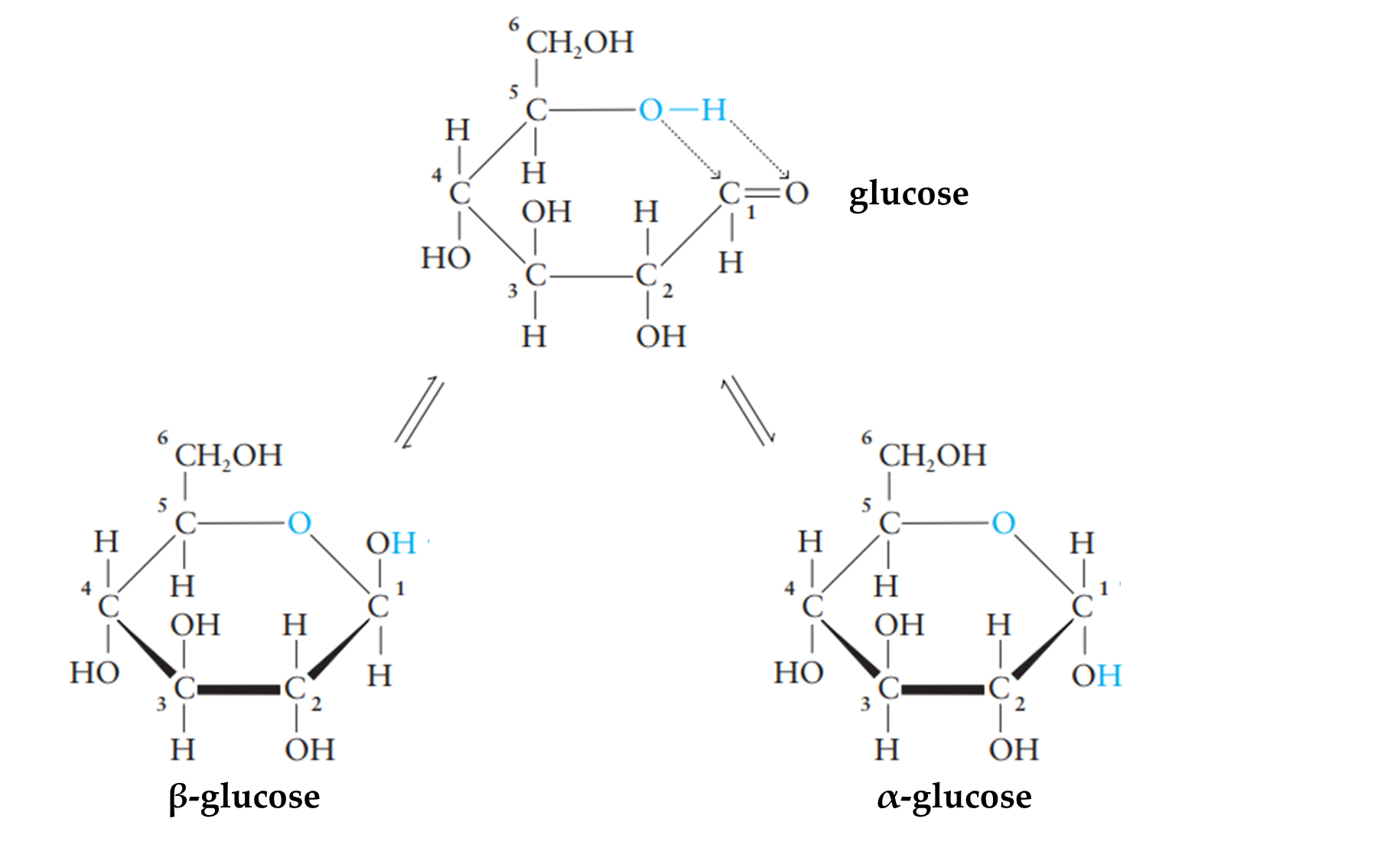
⇝ Công thức phân tử tương ứng: C6H12O6 (M = 180)
⇝ Chọn đáp án B. Đáp án: B
- Trong đó kim loại có xu hướng nhường electron thể hiện tính khử (bị oxi hoá)
⇒ Ăn mòn kim loại là sự phá huỷ kim loại hoặc hợp kim dưới tác dụng của các chất trong môi trường, trong đó kim loại bị oxi hoá.
⇒ Chọn đáp án A Đáp án: A
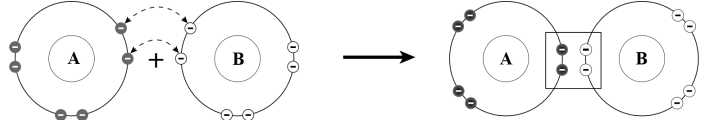
⟹ Chọn đáp án B Đáp án: B
CH3CH2Br
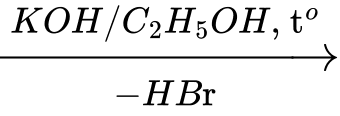 CH2=CH2
CH2=CH2Ethene
Ethene phản ứng với bromine
CH2=CH2 + Br2 → CH2Br–CH2Br
Hiện tượng, nước bromine mất màu.
⇒ Chọn đáp án C Đáp án: C
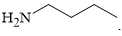
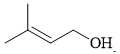
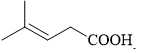
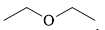
→ Chất có cấu tạo phù hợp là CH3C(CH3)=CHCH2COOH là một carboxylic acid.
⇒ Chọn đáp án C Đáp án: C
❌A.Sai. Chất chỉ thị không tham gia vào phản ứng dưới vai trò là chất xúc tác. Nó chỉ giúp xác định điểm kết thúc của phản ứng mà không làm thay đổi tốc độ hoặc cơ chế phản ứng.
❌B. Sai. Môi trường của phản ứng phụ thuộc vào acid và base tham gia, không phải do chất chỉ thị quyết định. Chất chỉ thị chỉ thay đổi màu sắc khi môi trường thay đổi, giúp xác định điểm tương đương.
❌C. Sai. Chất chỉ thị không ảnh hưởng đến tốc độ phản ứng giữa acid và base. Phản ứng này diễn ra nhanh chóng mà không cần chất chỉ thị hỗ trợ.
✔️D.Đúng. Chất chỉ thị hoạt động bằng cách thay đổi màu sắc khi dung dịch đạt đến pH nhất định, giúp xác định điểm tương đương trong quá trình chuẩn độ. Đây là vai trò chính của chất chỉ thị trong chuẩn độ acid-base
⟹Chọn đáp án D Đáp án: D
(RCOO)3C3H5 + 3NaOH
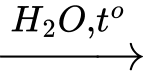 3RCOONa + C3H5(OH)3.
3RCOONa + C3H5(OH)3.Ở câu hỏi này: (RCOO)3C3H5 = (C17H33COO)3C3H5
⇒ R = C17H33COO ⇒ Ngoài glycerol C3H5(OH)3 thì muối X tương ứng dạng RCOONa = C17H33COONa
⇒ Chọn đáp án D Đáp án: D
⇒ Chọn đáp án B Đáp án: B
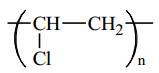
Tên của X là
⇒ Chọn đáp án C Đáp án: C
Khi thuỷ phân ester X trong dung dịch sodium hydroxide, đun nóng thì phản ứng xảy ra như sau: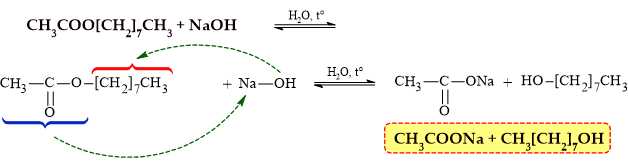
Công thức phân tử của 2 sản phẩm là: C2H3O2Na và C8H18O
⇒ Chọn đáp án B
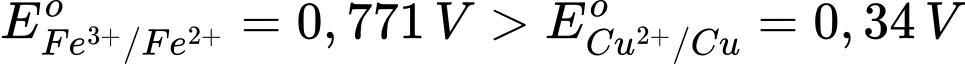
Dạng oxi hóa Fe3+ mạnh hơn Cu2+ và dạng khử Cu mạnh hơn Fe2+
2Fe3+ + Cu → 2Fe2+ + Cu2+
Phân tích các đáp án:
❌(a) – Sai. Tính khử của Cu mạnh hơn tính khử của ion Fe2+
❌(b) – Sai. Tính oxi hoá của ion Cu2+ yếu hơn tính oxi hoá của ion Fe3+.
❌(c) – Sai. Ở điều kiện chuẩn, ion Cu bị oxi hoá lên Cu2+ và có thể khử ion Fe3+ về Fe2+.
✔️(d) – Đúng. Ở điều kiện chuẩn, ion Fe3+ có thể bị khử về ion Fe2+ bởi kim loại Cu.
Ta có:
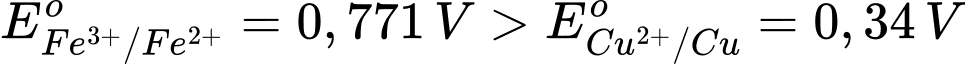
Dạng oxi hóa Fe3+ mạnh hơn Cu2+ và dạng khử Cu mạnh hơn Fe2+
2Fe3+ + Cu → 2Fe2+ + Cu2+
⟹ Chọn đáp án D Đáp án: D
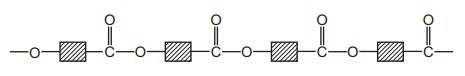
Những phát biểu nào sau đây là đúng khi nói về poly(lactic) acid?
(1) Poly(lactic) acid được tạo ra bằng phản ứng trùng hợp.
(2) Poly(lactic) acid được tạo ra bằng phản ứng trùng ngưng.
(3) Poly(lactic) acid là một loại polyester.
(4) Monomer được sử dụng để tạo ra poly(lactic) là ethene.
Nhận định (1) – Sai.
PLA không phải tạo ra từ phản ứng trùng hợp các monomer vinyl. Thay vào
đó, nó thường được tổng hợp từ lactic acid (axit lactic) thông qua phản
ứng trùng ngưng.
Nhận định (2) – Đúng. Lactic
acid (CH₃-CH(OH)-COOH) có nhóm –OH và –COOH. Khi trùng ngưng, nhóm –OH
và –COOH phản ứng, tạo liên kết ester –COO– và giải phóng H₂O.
Nhận định (3) – Đúng.
PLA chứa liên kết ester trong mạch polymer. Do đó, đúng là một polyester.
Nhận định (4) – Sai.
Monomer của PLA là lactic acid, không phải ethene (CH₂=CH₂).\
Đáp án:
Đáp án: C
⇒ Chọn dung dịch Cu(NO3)2.
Mặc dù dung dịch AgNO3 cũng có thể hòa tan kim loại Zn và Sn lẫn trong bột đồng. Nhưng phản ứng này lại tạo ra kim loại Ag ⇒ không thu được đồng tinh khiết.
⇒ Chọn đáp án A Đáp án: A
⟶ Khi phân bón này được đưa vào đất, nó có thể giải phóng ion H+, gây tăng độ chua của đất (giảm pH đất).
⇒ Chọn đáp án A
Đáp án: A
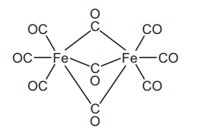
Cho các nhận định sau về phức chất trên:
(1) Công thức phân tử của X là Fe2(CO)9.
(2) Trong công thức cấu tạo của X có liên kết kim loại – kim loại.
(3) Có 2 loại phối tử CO trong cấu tạo của X.
(4) Nguyên tử trung tâm là cation Fe3+.
(5) Phối tử của X là phối tử trung hoà.
Có bao nhiêu nhận định đúng về phức chất X?
Nhận định (2) – Sai. cấu trúc Fe₂(CO)₉ được ổn định bởi các CO cầu, thường không được coi là có một liên kết Fe–Fe đơn rõ rệt trong mô tả cấu trúc chuẩn.
Nhận định (3) – Đúng. có 2 loại CO: CO đầu cuối (terminal) và CO cầu (bridging).
Nhận định (4) – Sai. Fe ở đây có trạng thái xấp xỉ Fe⁰ chứ không phải Fe³⁺.
Nhận định (5) – Đúng. CO là phối tử trung hòa.
Đáp án: C. 3. Đáp án: C
Sử dụng thông tin ở bảng dưới đây để trả lời các câu 17 - 18:
Trong công nghiệp, đồng kim loại được tinh chế bằng phương pháp điện phân như hình minh hoạ sau đây: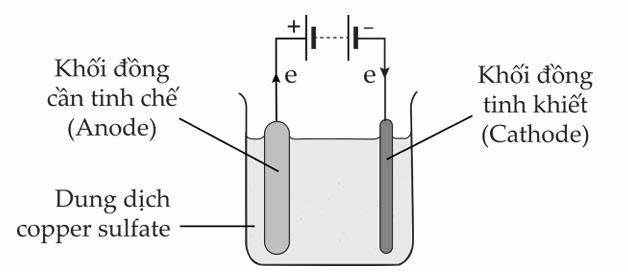
Cathode (–): Cu2+ + 2e ⟶ Cu
Anode (+): Cu ⟶ Cu2+ + 2e
Phân tích các nhận định:
❌ A. Sai. Phản ứng khử xảy ra ở điện cực âm, cực dương xảy ra phản ứng oxi hóa.
❌ B. Sai. Màu xanh của dung dịch không đổi do có sự tạo thành Cu2+ trên cực dương bù cho sự mất đi của Cu2+ trên cực âm.
✔️ C. Đúng. Khối lượng điện cực âm tăng dần do Cu tạo thành bám trên cực âm.
❌ D. Sai. Nồng độ ion Cu2+ trong dung dịch không đổi do có sự tạo thành Cu2+ trên cực dương bù cho sự mất đi của Cu2+ trên cực âm.
⇒ Chọn đáp án C Đáp án: C
Cathode (–): Cu2+ + 2e ⟶ Cu
Anode (+): Cu ⟶ Cu2+ + 2e
Theo định luật bảo toàn lượng Cu mất đi bên anode sẽ bằng đúng lượng Cu tạo thành trên cathode.
Hiệu suất của phản ứng là: H = 45 ÷ 50 × 100% = 90 %.
⇒ Chọn đáp án C Đáp án: C
PHẦN II. Thí sinh trả lời từ câu 1 đến câu 4. Trong mỗi ý a), b), c), d) ở mỗi câu, thí sinh chọn đúng hoặc sai.
∎ Bước 1: Cho vào ống nghiệm khoảng 2 mL dung dịch CaCl2, thêm từ từ cho đến hết khoảng 10 giọt dung dịch Na2CO3, lắc đều.
∎ Bước 2: Tiếp tục thêm vào khoảng 10 giọt dung dịch HCl, lắc đều.
Bước 1: Cho vào ống nghiệm khoảng 2 mL dung dịch CaCl2, thêm từ từ cho đến hết khoảng 10 giọt dung dịch Na2CO3, lắc đều.
Dung dịch đục dần xuất hiện kết tủa màu trắng.
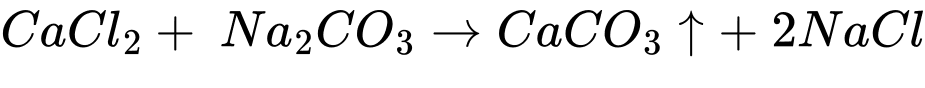
Bước 2: Tiếp tục thêm vào khoảng 10 giọt dung dịch HCI, lắc đều.
Kết tủa tan dần xuất hiện khí không màu thoát ra khỏi dung dịch
Phân tích các phát biểu:
✔️ (a) Đúng. Sau bước 1 xuất hiện CaCO3 kết tủa trắng.
✔️ (b) Đúng. Kết tủa CaCO3 không bền trong môi trường acid H+, tan tạo CO2 và nước.
✔️ (c) Đúng. Khi cho acid HCl ở bước 2 thì kết tủa tan dần, có xuất hiện bọt khí do phản ứng sinh ra khí CO2.
✔️ (d) Đúng. Sự có mặt của ion Ca2+ trong dung dịch có thể nhận biết bằng dung dịch chứa ion CO32- xuất hiện kết tủa trắng.
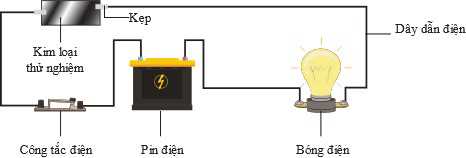
Thay lần lượt chiếc vòng tay và miếng bạc nguyên chất vào vị trí của kim loại thử nghiệm, so sánh độ sáng của bóng đèn giữa các lần thử. Kết quả thí nghiệm được cho trong bảng:
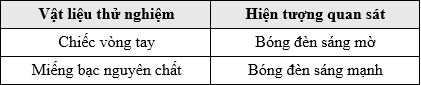
Điều này chứng tỏ cả hai vật liệu đều dẫn điện, nhưng bạc nguyên chất dẫn điện tốt hơn chiếc vòng tay.
Phân tích các phát biểu:
✔️ (a) Đúng. Cả hai đều làm bóng đèn sáng, chứng tỏ có dòng điện chạy qua.
✔️ (b) Đúng. Bạc nguyên chất có độ dẫn điện cao hơn nên làm bóng đèn sáng mạnh hơn.
✔️ (c) Đúng. Trong kim loại, các nguyên tử sắp xếp rất chặt chẽ thành mạng tinh thể. Các electron ở lớp ngoài cùng (electron hóa trị) không bị giữ chặt bởi nguyên tử nào mà di chuyển tự do khắp mạng tinh thể, tạo thành “mây electron tự do”. Khi có hiệu điện thế đặt vào, các electron này sẽ chuyển động có hướng, tạo thành dòng điện. Nhờ vậy, kim loại có khả năng dẫn điện rất tốt..
✔️ (d) Đúng. Nếu chiếc vòng là bạc nguyên chất thì bóng đèn phải sáng mạnh như khi thử với miếng bạc nguyên chất. Nhưng thực tế, bóng đèn chỉ sáng mờ, chứng tỏ chiếc vòng có lẫn tạp chất hoặc không phải bạc nguyên chất.
▪ Thí nghiệm 1: Cho vào ống nghiệm (1) khoảng 1 mL dung dịch ethylamine 5 %. Lấy đũa thuỷ tinh nhúng vào dung dịch rồi chấm vào giấy quỳ tím.
▪ Thí nghiệm 2: Cho vào ống nghiệm (1) khoảng 1 mL dung dịch ethylamine 5 %. Nhúng đũa thuỷ tinh sạch vào dung dịch HCl đặc rồi đưa đầu đũa thuỷ tinh vào miệng ống nghiệm (1).
▪ Thí nghiệm 3: Cho vào ống nghiệm (2) khoảng 5 giọt dung dịch FeCl3 3 %. Vừa lắc vừa thêm từ từ đến hết 2 mL dung dịch ethylamine 5%.
▪ Thí nghiệm 4: Cho vào ống nghiệm (3) khoảng 5 giọt dung dịch CuSO4 5 %. Vừa lắc vừa thêm từ từ đến hết 4 mL dung dịch ethylamine 5%.
C2H5NH2 + H2O ⇌ C2H5NH3+ + OH–.
Thí nghiệm 2: Do HCl và C2H5NH2 là những hợp chất dễ bay hơi nên chúng đã hóa hợp với nhau tạo thành tinh thể muối C2H5NH3Cl, chính tinh thể này đã tạo nên hiện tượng "khói"
C2H5NH2 + HCl ⟶ C2H5NH3Cl
Thí nghiệm 3: Xuất hiện kết tủa màu nâu đỏ là Fe(OH)3.
3C2H5NH2 + 3H2O + FeCl3 ⟶ Fe(OH)3 + 3C2H5NH3Cl
Thí nghiệm 4: Ban đầu xuất hiện kết tủa màu xanh Cu(OH)2, sau đó kết tủa tan dần tạo phức chất màu xanh.
2C2H5NH2 + 2H2O + CuSO4 ⟶ Cu(OH)2 + (C2H5NH3)2SO4
Cu(OH)2 + 4C2H5NH2 ⟶ [Cu(C2H5NH2)4](OH)2
Phân tích các phát biểu:
❌ (a) Sai. Quỳ tím không cần ẩm vì ethylamine (CH3CH2NH2) là chất lỏng dễ bay hơi, hòa tan tốt trong nước, và có khả năng làm giấy quỳ tím chuyển màu ngay cả khi giấy khô.
✔️ (b) Đúng. Thí nghiệm này dựa trên phản ứng giữa hơi ethylamine và hơi HCl, tạo khói trắng CH3CH2NH3Cl. Nếu đưa đũa nhúng ethylamine đến gần miệng lọ HCl đặc thì vẫn xảy ra hiện tượng khói trắng tương tự.
❌ (c) Sai. Trong thí nghiệm 4, dung dịch CuSO4 phản ứng với ethylamine tạo phức chất tan màu xanh đậm, chứ không tạo kết tủa.
❌ (d) Sai. Các thí nghiệm chủ yếu chứng minh tính base của amine (phản ứng làm đổi màu quỳ tím, phản ứng với HCl, phản ứng tạo phức chất với Cu2+). Ethylamine không thể hiện tính acid trong các thí nghiệm này, vì nó không có khả năng nhường proton (H+).

Tiến hành đo phổ hồng ngoại của lọ có nhãn (1) của một trong bốn chất. Kết quả phổ hồng ngoại được cho như dưới đây:
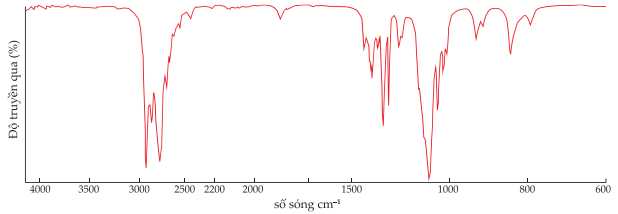
+) CH3COOH có tín hiệu đặc trung cho nhóm -OH (carboxylic acid) có số sóng trong khoảng 3000 – 2500 cm-1 và nhóm C=O (carboxylic acid) có số sóng trong khoảng 1750 – 1680 cm-1.
+) CH3COCH3 có tín hiệu đặc trung cho nhóm C=O (ketone) có số sóng trong khoảng 1740 – 1670 cm-1.
Trên phổ hồng ngoại không có tín hiệu tín hiệu đặc trưng cho các chất C2H5OH, CH3COOH, CH3COCH3.
→ Chất dán nhãn (1) là C2H5OC2H5.
Phân tích các phát biểu:
✔️ (a) Đúng. CH3COCH3 có tín hiệu đặc trung cho nhóm C=O (ketone) có số sóng trong khoảng 1740 – 1670 cm-1.
✔️ (b) Đúng. Nhóm -OH (alocohol) có số sóng trong khoảng 3650 – 3200 cm-1 và nhóm -OH (carboxylic acid) có số sóng trong khoảng 3000 – 2500 cm-1.
❌ (c) Sai. Kết quả phổ hồng ngoại của hợp chất trong lọ gắn nhãn (1) thuộc về hợp chất diethyl ether như đã phân tích.
✔️ (d) Đúng. Có thể sử dụng phổ hồng ngoại để phân biệt được bốn chất tương ứng trong các lọ gắn nhãn do ba chất đều có tín hiệu đặc trưng riêng còn ether không có.
PHẦN III. Thí sinh trả lời từ câu 1 đến 6. Thí sinh điền kết quả mỗi câu vào mỗi ô trả lời tương ứng theo hướng dẫn của phiếu trả lời.
⇒ Điền đáp án: 6
- Điều chế kim loại bằng phương pháp thủy luyện thường được sử dụng trong phòng thí nghiệm với mục đích điều chế những kim loại yếu đứng sau Mg.
Kim loại được điều chế bằng phương pháp thủy luyện gồm Cu và Ag
⇒ Có 2 kim loại.
⟹ Điền đáp án 2
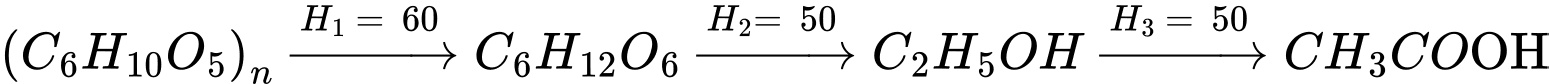
Từ 18,6 tấn bột sắn (chứa 70% tinh bột, còn lại là tạp chất trơ) sản xuất được 32 tấn dung dịch acetic acid có nồng độ a%. Tính giá trị của a? (kết quả làm tròn đến hàng phần trăm).
Hàm lượng tinh bột trong bột sắn là mtinh bột = 18,6.70% = 13,02 tấn
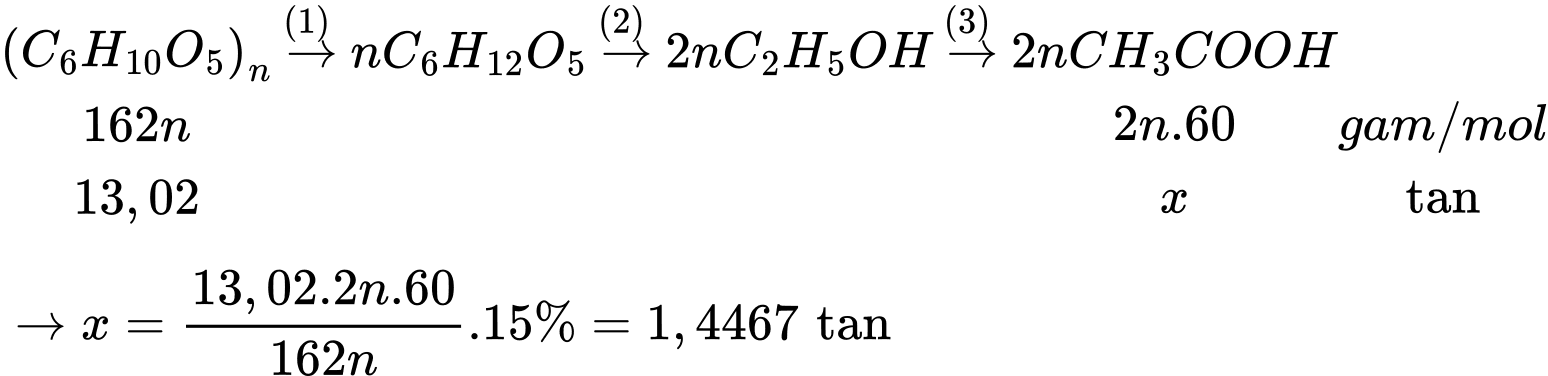
Nồng độ của dung dịch acetic acid là
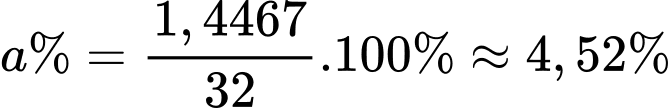
Điền đáp án : 4,52
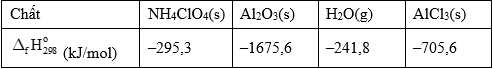
Cần khoảng 783 GJ (1 GJ = 109 J) để nâng một phi thuyền con thoi lên độ cao 88 km và bay được 320 km theo quỹ đạo parabol. Tính khối lượng nhôm (tấn) cần dùng để tạo ra lượng năng lượng 783 GJ bên trên (Làm tròn đến hàng phần mười)?
Biến thiên enthalpy của phản ứng là:
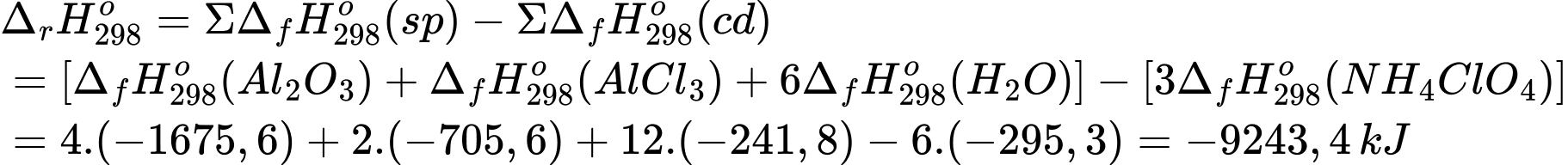
10 mol Al tham gia phản ứng tạo ra lượng nhiệt là 9243,4 kJ
Năng lượng sinh ra trên 1 mol Al là: 9243,4 ÷ 10 = 924,34 kJ
Số mol nhôm cần dùng là:
nAl = Năng lượng cần thiết ÷ Năng lượng giải phóng trên 1 mol Al = 783 × 106 ÷ 924,34 = 847,1 × 103 (mol)
→ Khối lượng nhôm cần dùng là: mAl = 847,1 × 103 × 27 = 22,87 × 106 (g) = 22,9 (tấn)
⇒ Điền đáp án: 22,9
(a) Phân tử lysine chứa số nguyên tử oxygen bằng số nguyên tử nitrogen.
(b) Hydrogen hóa hoàn toàn triolein (Ni, to), thu được tristearin.
(c) Glucose còn gọi là đường nho do có nhiều trong quả nho chín.
(d) Tơ hóa học gồm hai nhóm: tơ tổng hợp và tơ nhân tạo.
(e) Phản ứng ester hóa (H2SO4 đặc, to) xảy ra thuận nghịch.
Số phát biểu đúng là
✔️(a) – Đúng. Phân tử lysine: NH2-(CH2)4-CH(NH2)-COOH chứa 2 nguyên tử oxygen do có chứa 1 nhóm COOH.
✔️(b) – Đúng. Hydrogen hóa hoàn toàn triolein (Ni, to), thu được tristearin.
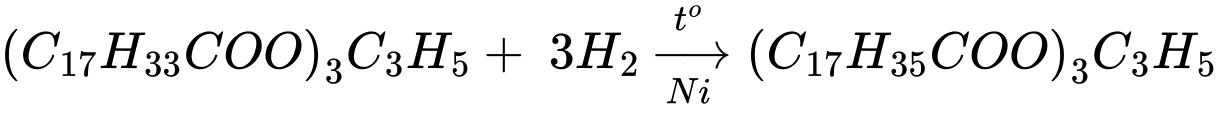
✔️(c) – Đúng. Glucose còn gọi là đường nho do có nhiều trong quả nho chín.
- Glucose là chất rắn, vị ngọt, dễ tan trong nước. Có trong các bộ phận của cây, đặc biệt là trong các quả chín.
- Glucose cũng có trong máu người và động vật. Nồng độ glucose trong máu người trưởng thành khoảng 4,4 – 7,2 mmol/L (hay 80 – 130 mg/dL).
- Glucose là chất dinh dưỡng quan trọng đối với con người. Dùng làm thực phẩm, đồ uống, tráng gương – tráng rột phích, dung dịch truyền tĩnh mạch glucose 5%, sản xuất ethanol, …
✔️(d) – Đúng. Tơ được chia thành hai loại:
- Tơ thiên nhiên (sãn có trong thiên nhiên) như bông, len, tơ tằm.
- Tơ hóa học (chế tạo bằng phương pháp hóa học): được chia làm hai nhóm
+ Tơ tổng hợp (chế tạo từ các polymeẻ tổng hợp) như các tơ polyamide (nilon, capron), tơ vinylic (vinilon).
+ Tơ bán tổng hợp hay tơ nhân tạo (xuất phát từ polymer thiên nhiên nhưng được chế biến thêm bằng phương pháp hóa học)
✔️(e) – Đúng. Phản ứng ester hóa (H2SO4 đặc, to) xảy ra thuận nghịch.
Ester bị thuỷ phân trong môi trường acid thường tạo thành carboxylic acid và alcohol (hoặc phenol) tương ứng.
RCOOR + H2O ⇌ RCOOH + ROH
Có 5 phát biểu đúng.
⟹ Điền đáp án: 5
∎ Giai đoạn 1: Than (80% carbon) được thực hiện phản ứng khí than ướt (hiệu suất 70%) nhằm thu CO và H2.
C(s) + H2O(g)
 CO(g) + H2(g)
CO(g) + H2(g)∎ Giai đoạn 2: Mang CO đi phản ứng với oxygen dư để thu CO2 (hiệu suất 100%).
2CO(g) + O2(g)
 2CO2(g)
2CO2(g)∎ Giai đoạn 3: Cho CO2 và NH3 vừa thu được ở trên phản ứng với nhau để có urea (hiệu suất 70%).
CO2(g) + 2NH3(g)
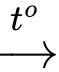 (NH2)2C=O(s) + H2O(l)
(NH2)2C=O(s) + H2O(l)Tính khối lượng urea (kg) thu được sản xuất từ 10 kg than? Các chất phản ứng khác dùng dư.
Hiệu suất chung của cả quá trình là H = 70%.100%.70% = 49%
Sơ đồ phản ứng:
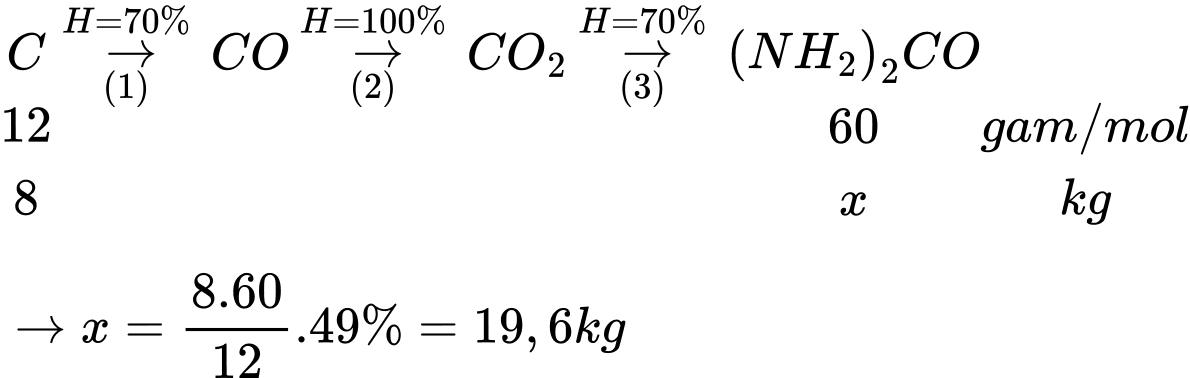
⟹ x = 19,6 kg
⟹ Điền đáp án: 19,6