PHẦN I. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
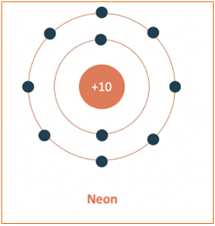
- Cấu hình electron bền vững của khí hiếm Neon có 10 electron nên nguyên tử của nguyên tố Fluorine (Z = 9) có xu hướng nhận thêm 1 electron để đạt cấu hình electron bền vững của khí hiếm Neon khi tham gia hình thành liên kết hoá học.
⟹ Chọn đáp án: B Đáp án: B
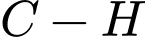 . Mỗi liên kết đơn luôn là 1 liên kết
. Mỗi liên kết đơn luôn là 1 liên kết 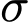 .
.o
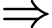 4 liên kết
4 liên kết 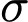 .
.2. Liên kết giữa C và C: Có 1 liên kết đôi
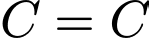 . Trong một liên kết đôi, sẽ bao gồm 1 liên kết
. Trong một liên kết đôi, sẽ bao gồm 1 liên kết 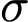 và 1 liên kết
và 1 liên kết 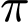 .
.o
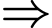 1 liên kết
1 liên kết 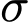 và 1 liên kết
và 1 liên kết 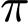 .
.Tổng cộng:
• Tổng số liên kết
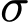 :
: 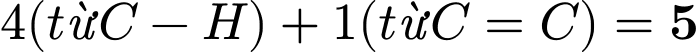
• Tổng số liên kết
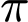 :
: 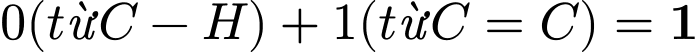
________________________________________
Kết luận: Số liên kết
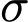 và
và 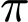 lần lượt là 5 và 1.
lần lượt là 5 và 1.Đáp án đúng là: D. Đáp án: D
⇒ Chọn đáp án A Đáp án: A
- Phần lớn amino acid ở dạng kết tinh là chất không màu, trừ một số amino acid đặc biệt như tyrosine, có thể hơi vàng nhạt.
- Chúng có nhiệt độ nóng chảy cao do lực tương tác mạnh giữa các ion lưỡng cực.
⇒ Ở điều kiện thường, amino acid là chất rắn, khi ở dạng kết tinh, chúng không màu, có nhiệt độ nóng chảy cao và thường tan tốt trong nước
⇒ Chọn đáp án B Đáp án: B
(a) Nhiệt phân muối silver nitrate.
(b) Điện phân dung dịch sodium chloride có màng ngăn xốp.
(c) Dẫn khí hydrogen qua bột copper(II) oxide đun nóng.
(d) Cho dung dịch iron(II) nitrate vào dung dịch silver nitrate.
Sau khi các phản ứng xảy ra hoàn toàn, những thí nghiệm thu được kim loại là
(a) Nhiệt phân muối silver nitrate
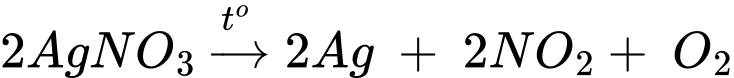
(b) Điện phân dung dịch sodium chloride có màng ngăn xốp
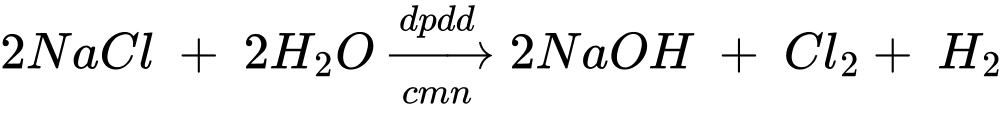
(c) Dẫn khí hydrogen qua bột copper(II) oxide đun nóng
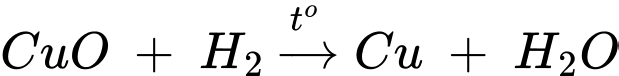
(d) Cho dung dịch iron(II) nitrate vào dung dịch silver nitrate
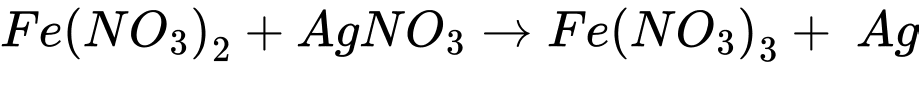
Sau phản ứng, các thí nghiệm thu được kim loại là (a) (c) và (d)
⇒ Chọn đáp án B Đáp án: B
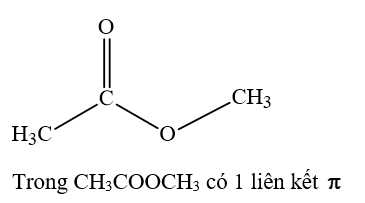
⟹Chọn đáp án A
ester < alcohol < carboxylic acid.
Trong nhóm acid thì số carbon tăng, nhiệt độ sôi tăng. Theo đó:
methyl acetate (T) = CH3COOCH3 < propyl alcohol (Z) = CH3CH2CH2OH < acetic acid (Y) = CH3COOH < propionic acid (X) = CH3CH2COOH.
Vậy, thứ tự ký hiệu các chất chiều nhiệt độ sôi tăng: T, Z, Y, X
⇝ Chọn đáp án A Đáp án: A
1. Dung dịch phải phản ứng được với tất cả các tạp chất (
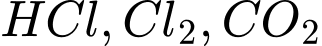 ).
).2. Dung dịch không được phản ứng với khí cần thu hồi (
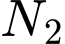 ).
).________________________________________
Phân tích các đáp án:
A.
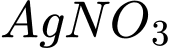 : Chỉ phản ứng tốt với
: Chỉ phản ứng tốt với 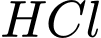 (tạo kết tủa
(tạo kết tủa 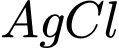 ). Phản ứng với
). Phản ứng với 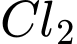 diễn ra phức tạp và không loại bỏ triệt để
diễn ra phức tạp và không loại bỏ triệt để 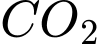 .
.B.
 (Dung dịch kiềm): Đây là lựa chọn tối ưu vì
(Dung dịch kiềm): Đây là lựa chọn tối ưu vì  phản ứng được với cả 3 tạp chất:
phản ứng được với cả 3 tạp chất:o Với
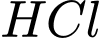 (acid):
(acid): 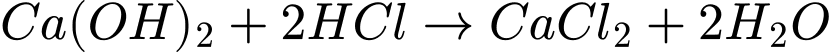
o Với
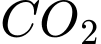 (oxide acid):
(oxide acid): 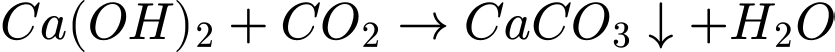
o Với
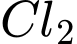 :
: 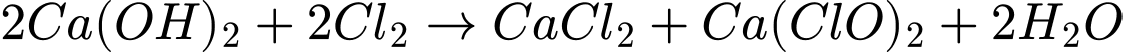 (tạo clorua vôi)
(tạo clorua vôi)o Quan trọng:
 không phản ứng với
không phản ứng với 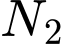 .
.C.
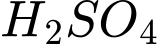 : Là acid, không phản ứng để loại bỏ các khí có tính acid như
: Là acid, không phản ứng để loại bỏ các khí có tính acid như 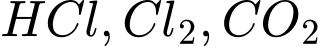 .
.D.
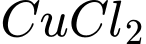 : Không phản ứng với các khí trên.
: Không phản ứng với các khí trên.Kết luận:Để loại bỏ sạch các tạp chất
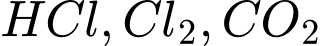 trong khí
trong khí 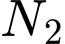 , người ta sử dụng lượng dư dung dịch
, người ta sử dụng lượng dư dung dịch  .
.Đáp án đúng là: B. Đáp án: B
✔️ B. Đúng. Phương pháp li tâm hoạt động dựa trên sự khác biệt về khối lượng riêng, làm dầu và nước tách thành hai lớp rõ rệt. Ngoài ra, dầu và nước không trộn lẫn (không tan vào nhau) nên có thể tách được.
✔️ C. Đúng. Chiết lỏng - lỏng là phương pháp tách hai chất lỏng không tan vào nhau, dựa vào sự khác biệt về khối lượng riêng. Ở đây, dầu nổi lên trên, nước ở dưới và khi mở van xả nước phía dưới thì thu được dầu.
❌ D. Sai. Chưng cất là phương pháp tách dựa vào sự khác biệt nhiệt độ sôi.
- Nhiệt độ sôi của nước (~100 oC) và dầu mỏ (cao hơn 200 oC) rất chênh lệch.
- Khi đun nóng, nước sẽ bay hơi trước, nhưng dầu có thể bị biến chất hoặc cháy khi đun nóng đến nhiệt độ quá cao.
⇒ Không dùng chưng cất để tách dầu ra khỏi nước trong trường hợp này.
⇒ Chọn đáp án D Đáp án: D
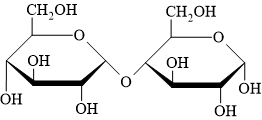
Quan sát + phân tích cấu tạo:
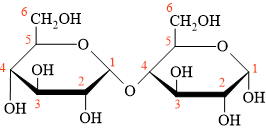
• 1. Hai mắt xích đều giống nhau.
• 2. nhóm OH ở carbon số 1 nằm phía dưới mặt phẳng, khác phía so với nhóm CH2OH ⇒ dạng alpha (α).
⇒ Hai mắt xích đều là dạng α-glucose.
⟹ Chọn đáp án A.
Đáp án: ABảng thế điện cực chuẩn của kim loại có thể được sắp xếp thành một dãy như sau (còn được gọi là dãy điện hóa của kim loại):
Thế điện cực chuẩn của cặp oxi hóa – khử càng lớn thì tính khử của dạng khử càng yếu, tính oxi hóa của dạng oxi hóa càng mạnh và ngược lại.
⟹ Chọn đáp án A
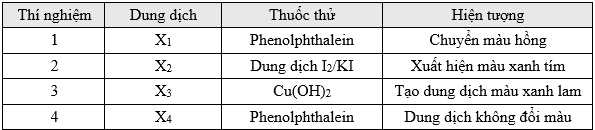
(a) X1 tan trong nước tạo môi trường acid.
(b) Thí nghiệm 2 có xảy ra phản ứng hóa học.
(c) X3 có thể có chứa các nhóm OH liền kề.
(d) X4 là glycine với số nhóm amino bằng nhóm carboxyl.
Các phát biểu đúng là
❌(a) – Sai. X1 tan trong nước tạo dung dịch kiềm, nguyên do làm phenolphtalein chuyển hồng.
✔️(b) – Đúng. Thí nghiệm 2 có 2 phản ứng : KI + I2 → KI3Phân tử tinh bột hấp phụ iodine tạo thành hợp chất màu xanh tím.
✔️(c) – Đúng. X3 phản ứng với Cu(OH)2 tạo dung dịch màu xanh lam, chứng tỏ X3 có ít nhất 2 nhóm OH liền kề nhau.
✔️(d) – Đúng. Glycine có 1 nhóm NH2 và 1 nhóm COOH.
⟹Chọn đáp án D
Đáp án: D
❌A. Na2O : Sodium oxide
✔️B. Na2O2 : Sodium peroxide
❌C. NaO2 : Sodium superoxide
❌D. NaO : vi phạm quy tắc hóa trị.
⟹ Chọn đáp án B Đáp án: B
Ở nước ta, theo TCVN 5502:2003 do Bộ Khoa học - Công nghệ ban hành năm 2003, độ cứng của nước thường được đánh giá dựa vào số mg CaCO3 ứng với tổng số mol Ca2+ và Mg2+ trong 1 lít nước. Trong 1 lít nước có 0,0020 mol Ca2+ và 0,0005 mol Mg2+ thì số mg CaCO3 tính được là 250. Độ cứng của nước được đánh giá theo số liệu sau:

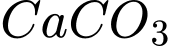 tương ứng với tổng số mol
tương ứng với tổng số mol 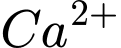 và
và 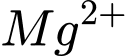 trong 1 lít nước.
trong 1 lít nước.• Trong 50 mL mẫu nước có:
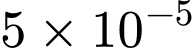 mol
mol 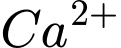 và
và 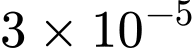 mol
mol 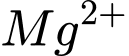 .
.• Tổng số mol trong 50 mL:
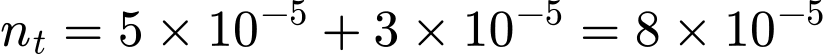 mol.
mol.• Đổi 1 lít = 1000 mL:
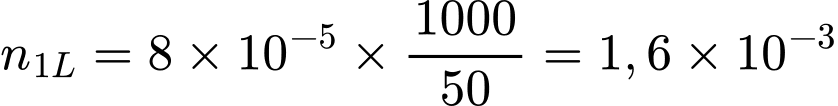 mol.
mol.• Khối lượng CaCO3 là:
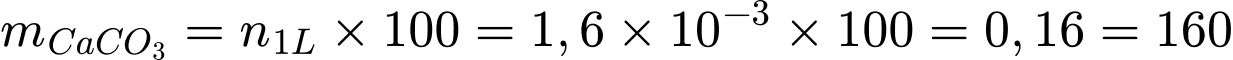 mg.
mg.=> Vì giá trị tính được là 160 mg/L, mẫu nước này thuộc loại nước cứng.
Đáp án đúng là: A. Đáp án: A
- có sáu nguyên tử carbon trong mỗi monomer mà nó được tạo thành.
- không phải là polyester.
- được tạo thành bằng phản ứng trùng ngưng.
Hình nào sau đây biểu diễn một phần cấu trúc của P?
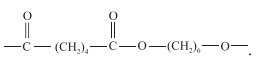
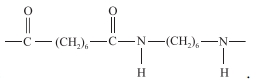
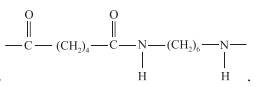
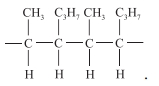
P là một polymer:
▪ có sáu nguyên tử carbon trong mỗi monomer mà nó được tạo thành
▪ không phải là polyester
▪ được tạo thành bằng phản ứng trùng ngưng.
=> Dựa vào các cấu trúc, ta thấy cấu trúc C là cấu trúc đại diện cho Nylon-6,6. Nó được tạo thành từ hai monomer (Acid adipic và Hexamethylenediamine), mỗi monomer có 6 nguyên tử carbon, không phải polyester, và tạo thành bằng phản ứng trùng ngưng.
=> Đáp án đúng là C
(a) CoCl2 là hợp chất của kim loại chuyển tiếp.
(b) Phức chất X không chứa phối tử aqua (phối tử H2O).
(c) Trong phức chất X, liên kết giữa nguyên tử trung tâm và phối tử là liên kết ion.
(d) Khi nhỏ giọt nước lên giấy Y, giấy Y chuyển màu.
Trong các phát biểu trên, những phát biểu đúng là
✔️ (a) Đúng. Cobalt (Co) là kim loại chuyển tiếp thuộc nhóm VIIIB (nhóm 9) trong bảng tuần hoàn.CoCl2 là muối của kim loại chuyển tiếp.
❌ (b) Sai. Khi hòa tan CoCl2 khan (màu xanh) vào nước, thu được dung dịch màu hồng do tạo thành phức chất [Co(H2O)6]2+.
CoCl2 + 6H2O → [Co(H2O)6]2+ + 2Cl−
Phức chất có chứa phối tử aqua (H2O).
❌ (c) Sai. Trong phức chất [Co(H2O)6]2+, nguyên tử trung tâm Co2+ liên kết với phối tử H2O bằng liên kết cho nhận, không phải liên kết ion. Liên kết ion chỉ xuất hiện giữa ion phức với các ion đối (ví dụ Cl−).
✔️ (d) Đúng. Giấy Y (đã tẩm CoCl2 khan, màu xanh) hấp thụ nước tạo thành [Co(H2O)6]2+, có màu hồng. Ứng dụng: Giấy này được dùng làm chỉ thị phát hiện hơi nước.
⟹ Chọn đáp án C Đáp án: C
Sử dụng thông tin ở bảng dưới đây để trả lời các câu 17 – 18:
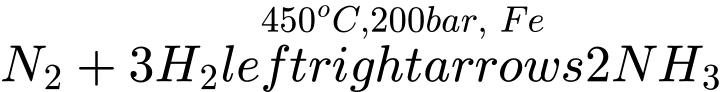
Phản ứng của nitrogen N2 và hydrogen H2 để điều chế ra ammonia NH3 là một phản ứng thuận nghịch.
(a) tăng áp suất;
(b) tăng nồng độ N2 và H2;
(c) tăng nhiệt độ;
(d) giảm nồng độ NH3;
(e) thêm chất xúc tác Fe.
Trong những tác động trên, có bao nhiêu tác động làm tăng hiệu suất của phản ứng tổng hợp?
✔️(a) – Đúng. Tăng áp suất làm cân bằng chuyển dịch theo chiều thuận, tăng hiệu suất phản ứng.
✔️(b) – Đúng. Tăng nồng độ N2 và H2 cân bằng chuyển dịch theo chiều làm giảm N2, H2 nghĩa là chiều thuận.
❌(c) – Sai. Khi tăng nhiệt độ cân bằng chuyển dịch theo nghịch, giảm hiệu suất phản ứng.
✔️(d) – Đúng. Khi giảm nồng độ NH3 làm cân bằng chuyển dịch theo chiều tăng nồng độ NH3 làm cân bằng chuyển dịch theo chiều thuận, tăng hiệu suất phản ứng.
❌(e) – Sai. Chất xúc tác không làm ảnh hưởng đến chuyển dịch cân bằng.
Có 3 tác động làm tăng hiệu suất.
⟹Chọn đáp án C Đáp án: C
Giả sử có 4 mol H2 và 1 mol N2
Gọi áp xuất ban đầu là p
Áp suất tỉ lệ thuận với số mol khí → 4 + 1 = p (1)
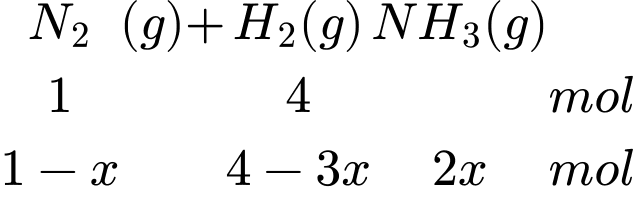
Tổng số mol khí sau phản ứng là: nH2 + nN2 + nNH3 = 4 – 3x + 1 – x + 2x = 5 – 2x (mol)
Sau phản ứng số áp suất khí của hệ giảm đi 9% so với ban đầu → 5 – 2x = 0,91p (2)
Ta có:
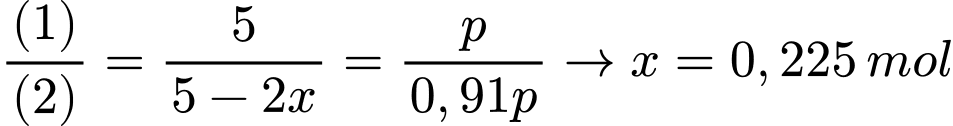
Hiệu suất của phản ứng là
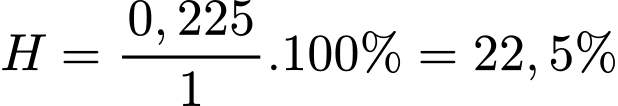
⇒ Chọn đáp án B Đáp án: B
PHẦN II. Thí sinh trả lời từ câu 1 đến câu 4. Trong mỗi ý a), b), c), d) ở mỗi câu, thí sinh chọn đúng hoặc sai.
➊ Gạo được nấu chín, để nguội, rắc men, ủ kín 3-5 ngày, thu được một hỗn hợp gồm nước, ethanol và bã rượu.
➋ Đun nóng hỗn hợp trên đến nhiệt độ sôi, hơi bay ra đi vào đường ống dẫn. Hỗn hợp hơi trong đường ống được làm lạnh sẽ hoá lỏng và chảy vào bình hứng.
Quá trình này gọi là chưng cất rượu. Biết nhiệt độ sôi của ethanol và nước lần lượt là 78 oC và 100 oC.
✔️ (a) Đúng. Ở giai đoạn đầu xảy ra sự chuyển hoá tinh bột thành ethanol.
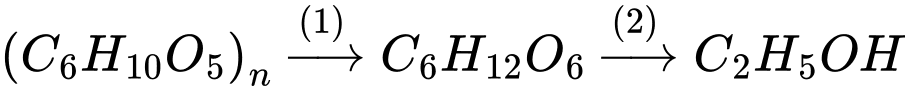
(b) Sai. Nhiệt độ sôi của ethanol và nước lần lượt là 78 oC và 100 oC nên để chưng cất rượu cần nhiệt độ trong khoảng từ 78 oC đến 100 oC, nếu nhiệt độ lớn hơn 100 oC thì quá trình chưng cất sẽ kèm theo hơi nước không thu được rượu nguyên chất.
✔️ (c) Đúng. Trong quá trình chưng cất, hơi ethanol và hơi nước bay ra theo đường ống.
Khi đi qua thùng nước lạnh (bình ngưng tụ), hơi bị làm lạnh và ngưng tụ thành chất lỏng chảy vào bình hứng.
Vì vậy, thùng nước lạnh có vai trò chuyển pha từ hơi sang pha lỏng.
.
✔️ (d) Đúng. Ban đầu, hỗn hợp chứa nhiều ethanol hơn nước do ethanol bay hơi ở nhiệt độ thấp hơn.
Khi chưng cất, ethanol dần thoát ra trước, làm tỉ lệ ethanol/nước trong phần còn lại giảm dần.
Sau một thời gian, khi phần ethanol đã gần hết, phần còn lại chủ yếu là nước, và tỉ lệ này không đổi nữa.
 2Cl− + 2Fe3+
2Cl− + 2Fe3+Sơ đồ bên dưới cho thấy thiết bị cần thiết để đo Eo cho phản ứng trên.
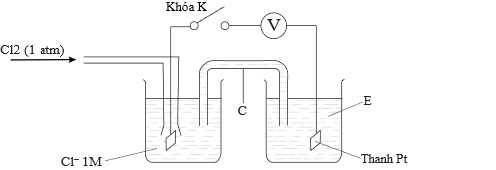
Thay A bằng Cl2 (1 atm); B bằng dung dịch Cl– 1 M; D bằng thanh Pt. S bằng cầu giao.
Cho thế khử chuẩn của các cặp oxi hóa khử:
Fe3+ + 1e
 Fe2+;
Fe2+; 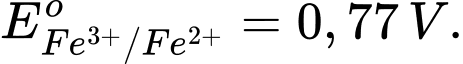
Cl2 + 2e
 2Cl–;
2Cl–; 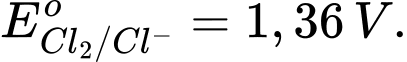
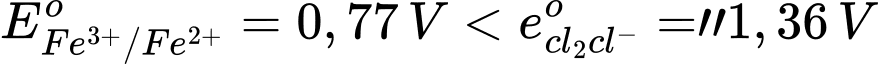 "
" 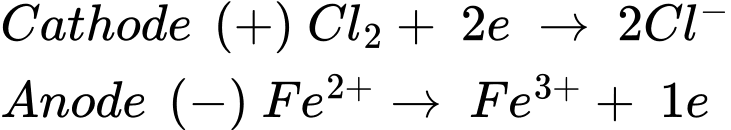 Phản ứng xảy ra là
Phản ứng xảy ra là 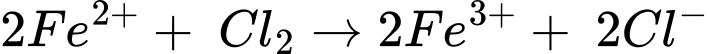
→ Epin = E(+) – E(-) = 1,36 – 0,77 = 0,59 V
Phân tích các phát biểu:
❌ (a) Sai . Dung dịch ban đầu E chỉ chứa cation Fe2+ với nồng độ 1 M, sau khi pin hoạt động chứa các cation Fe2+, Fe3+.
✔️ (b) Đúng. Cầu muối C có thể sử dụng NaCl làm chất điện li.Cầu muối là một bộ phận quan trọng trong pin điện hóa (pin Galvani), giúp cân bằng điện tích giữa hai nửa pin bằng cách cho phép ion di chuyển mà không làm cho hai dung dịch tiếp xúc trực tiếp. Duy trì tính trung hòa điện tích:Anion (ion âm) di chuyển về cực dương và Cation (ion dương) di chuyển về cực âm. Ngăn cản sự tiếp xúc trực tiếp giữa hai dung dịch, tránh phản ứng kết tủa làm giảm hiệu suất pin.
✔️ (c) Đúng. Đây là phản ứng oxi hóa khử, theo định luật bảo toàn electron thì số electron nhường bằng nhận.
✔️ (d) Đúng. Khi thiết bị hoạt động ở điều kiện chuẩn, giá trị hiển thị trên vôn kế là 0,59 V.
▪ Ống nghiệm (1): Cho khoảng 4 – 6 giọt dung dịch NaOH vào ống nghiệm (1) chứa khoảng 1 mL dung dịch CuSO4.
▪ Ống nghiệm (2): Cho khoảng 4 – 6 giọt dung dịch NaOH vào ống nghiệm (2) chứa khoảng 1 mL dung dịch FeCl3.
Ống nghiệm (1): Xuất hiện kết tủa xanh:
CuSO4 + 2NaOH → Cu(OH)2↓ (xanh) + Na2SO4
Ống nghiệm (2): Xuất hiện kết tủa đỏ nâu:
FeCl3 + 3NaOH → Fe(OH)3↓ (đỏ nâu) + 3NaCl
Phân tích các phát biểu:
✔️ (a) Đúng. Ống nghiệm (1) xuất hiện kết tủa xanh trong ống nghiệm là Cu(OH)2.
❌ (b) Sai. Ống nghiệm (2) xuất hiện kết tủa nâu đỏ Fe(OH)3 không bị oxi hóa không khí ẩm nên không chuyển sang màu vàng nâu.
✔️ (c) Đúng. Nếu NaOH bằng dung dịch NH3 thì hiện tượng trong cả hai ống nghiệm vẫn xảy ra tương tự do NH3 và NaOH mang tính base như nhau, đều chứa ion OH-, phản ứng xảy ra:
▪ Bước 1: Cho khoảng 1 mL hexane vào ống nghiệm.
▪ Bước 2: Thêm vài giọt dung dịch KMnO4 1%, lắc đều ống nghiệm trong khoảng 5 phút, sau đó đặt ống nghiệm vào giá rồi để yên khoảng 10 phút.
Biết rằng hexane có khối lượng riêng nhỏ hơn dung dịch potassium permanganate.
- Hexane (C6H14) là một hydrocarbon thuộc nhóm alkane (paraffin), không tan trong nước, nhẹ hơn nước.
- KMnO4 tan tốt trong nước, tạo dung dịch màu tím.
Bước 2:
- Khi thêm dung dịch KMnO₄ vào hexane, do hexane không tan trong nước, hỗn hợp sẽ tạo hai lớp chất lỏng:
+ Lớp trên: Hexane (nhẹ hơn).
+ Lớp dưới: Dung dịch KMnO4 trong nước (nặng hơn).
- Vì hexane là alkane (chỉ có liên kết đơn σ, không có liên kết đôi C=C như alkene hay alkyn), nên nó không phản ứng với KMnO4 ở điều kiện thường.
- KMnO4 tan chủ yếu trong nước, không tan tốt trong hexane.
Phân tích các phát biểu:
✔️ (a) Đúng. KMnO4 là hợp chất ion, tan tốt trong dung môi phân cực như nước, nhưng không tan trong hexane (một dung môi không phân cực).
✔️ (b) Đúng. Hexane không tan trong nước và có khối lượng riêng nhỏ hơn nước nên nổi ở trên. Lớp dưới là KMnO4.
❌ (c) Sai. KMnO4 tan trong nước (lớp dưới), còn lớp trên là hexane không chứa KMnO4, nên không có màu tím.
✔️ (d) Đúng. Hexane là alkane, chỉ có liên kết đơn C-C và C-H rất bền, không dễ bị oxi hóa bởi KMnO4 ở điều kiện thường.
PHẦN III. Thí sinh trả lời từ câu 1 đến 6. Thí sinh điền kết quả mỗi câu vào mỗi ô trả lời tương ứng theo hướng dẫn của phiếu trả lời.
Phương trình :
HOOC–CH(OH)–CH(OH)–COOH + 2NaOH ⟶ NaOOC–CH(OH)–CH(OH)–COONa
Điền đáp án : 2
Vừa đủ nên dung dịch X thu được gồm FeSO4 và Fe2(SO4)3.
Phân tích các chất trong dãy:
✔️ NaOH cung cấp OH– để tạo kết tủa Fe(OH)2↓ và Fe(OH)3.
❌ Ag không phản ứng được với cả FeSO4 và Fe2(SO4)3.
✔️ Ba(NO3)2 cung cấp Ba2+ tạo kết tủa BaSO4↓.
❌ NaCl không có phản ứng với cả FeSO4 và Fe2(SO4)3.
⇝ có 2/4 chất thỏa mãn yêu cầu .
Điền đáp án : 2
Polymer không bị thủy phân trong môi trường acid là poly(vinyl chloride).
Xét từng polymer trong dãy:
✔️Poly(vinyl chloride) - PVC (1)
Cấu trúc: (-CH2-CHCl-)n
Là polymer chuỗi carbon no, không có liên kết dễ bị thủy phân.
Không bị thủy phân trong môi trường acid.
❌Poly(hexamethylen adipamide) - Nylon-6,6 (2)
Có liên kết amide (-CONH-), dễ bị thủy phân trong môi trường acid.
❌Poly(ethylen terephthalate) - PET (3)
Có liên kết ester (-COO-), bị thủy phân trong môi trường acid.
❌Cellulose (4)
Là polysaccharide với liên kết glycosid (-O-), bị thủy phân trong môi trường acid.
⟹ Điền đáp án: 1
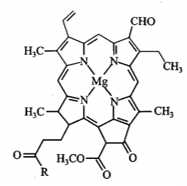
Nguyên tử trung tâm Mg2+ tạo 4 liên kết với 1 phối tử porphyrin.
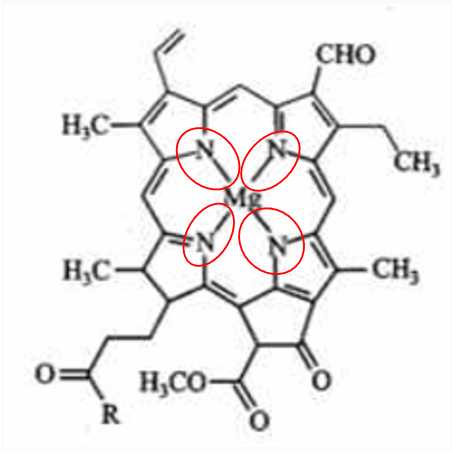
⟹ Điền đáp án: 41
(a) Dipeptide Gly-Ala có phản ứng màu biuret.
(b) Dung dịch glutamic acid đổi màu quỳ tím thành xanh.
(c) Methyl formate và glucose có cùng công thức đơn giản nhất.
(d) Methylamine có lực base mạnh hơn ammonia.
(e) Saccharose có phản ứng thủy phân trong môi trường acid.
(g) Methyl methacrylate làm mất màu dung dịch bromine.
Số phát biểu đúng là
❌(a) – Sai. Trừ các dipeptide, các peptide còn lại có khả năng hoà tan Cu(OH)2 trong môi trường kiềm tạo thành phức chất tan trong nước có màu tím đặc trưng. Phản ứng này được gọi là phản ứng màu biuret.
❌(b) – Sai. Dung dịch glutamic acid đổi màu quỳ tím thành đỏ. Glutamic acid là một amino acid có tính acid do chứa nhóm -COOH (carboxylic acid) nhiều hơn nhóm -NH2 (amine)
✔️(c) – Đúng. Methyl formate (C2H4O2) và glucose (C6H12O6) có cùng công thức đơn giản nhất là CH2O
✔️(d) – Đúng. Methylamine có lực base mạnh hơn ammonia. Nhóm methyl (-CH3) có hiệu ứng cảm ứng đẩy electron làm tăng mật độ electron trên nguyên tử N → Nitrogen trong methylamine dễ nhận proton (H+) hơn.
✔️(e) – Đúng. Saccharose bị thủy phân thành glucose và fructose. Phản ứng xảy ra khi có xúc tác acid hoặc có mặt của enzyme.
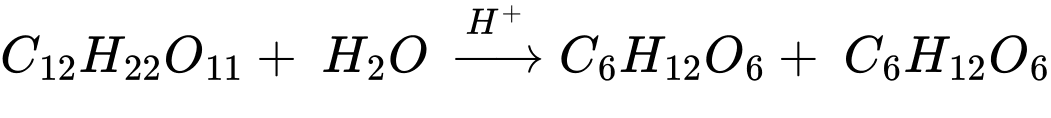
✔️(g) – Đúng. Methyl methacrylate có liên kết đôi C=C làm mất màu dung dịch bromine. CH2=C(CH3)COOCH3 + Br2 → CH2BrCBr(CH3)COOCH3
Có 4 phát biểu đúng.
⟹ Điền đáp án : 4
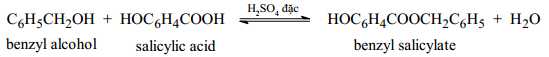
Để sản xuất 4000 (Lít) benzyl salicylate nguyên chất (D=1,17 g/mL) thì cần tối thiểu bao nhiêu (Lít) benzyl alcohol nguyên chất (D=1,04 g/mL), biết hiệu suất phản ứng tính theo benzyl alcohol là 80%? (kết quả làm tròn đến đến số nguyên hàng đơn vị)
→ mbenzyl alcohol = D × V =1,04V (kg) → nbenzyl alcohol = 1,04V ÷ 108 (kmol) = nbenzyl salicylate
Ta có: mbenzyl salicylate = nbenzyl salicylate × Mbenzyl salicylate × 80%
Mà mbenzyl salicylate = D × V = 4000 × 1,17 = 4680 (kg)
Hay mbenzyl salicylate = (1,04V ÷ 108) × 228 × 80% = 4680 (kg)
→ V = 2664,47 ≈ 2664 (L)
⇒ Điền đáp án: 2664