PHẦN I. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
Câu 1 [702804]: Tính chất vật lí nào sau của kim loại không do các electron tự do quyết định?
A, Tính dẫn điện.
B, Tính dẻo.
C, Khối lượng riêng.
D, Tính dẫn nhiệt.
- Electron tự do quyết định đến tính chất vật lí chung như tính dẫn điện, dẫn nhiệt, tính dẻo, ánh kim.
- Khối lượng riêng là tính chất vật lí riêng nên không do electron tự do quyết định.
⇒ Chọn đáp án C Đáp án: C
- Khối lượng riêng là tính chất vật lí riêng nên không do electron tự do quyết định.
⇒ Chọn đáp án C Đáp án: C
Câu 2 [703007]: Chất Y phản ứng với dung dịch sodium hydroxide tạo thành methanol và sodium ethanoate. Công thức của Y là
A, CH3COOCH3.
B, HCOOC2H5.
C, HOOCCH2CHO.
D, HOCH2CH2COOH.
Phản ứng tổng quát khi thủy phân ester trong môi trường kiềm:
RCOOR' + NaOH ⟶ RCOONa + R'OH
⤑ RCOONa = CH3COONa (sodium ethanote)
⤑ R'OH = CH3OH (methanol)
Ester có công thức là: CH3COOCH3
⇒ Chọn đáp án A
Đáp án: A
RCOOR' + NaOH ⟶ RCOONa + R'OH
⤑ RCOONa = CH3COONa (sodium ethanote)
⤑ R'OH = CH3OH (methanol)
Ester có công thức là: CH3COOCH3
⇒ Chọn đáp án A
Đáp án: A
Câu 3 [244519]: Cho chất hữu cơ A có công thức cấu tạo như sau:
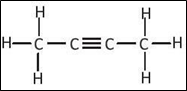

Hình 3.63. Công thức cấu tạo của hợp chất hữu cơ A
Số liên kết σ trong phân tử A là
A, 6.
B, 8.
C, 9.
D, 11.
Dựa vào công thức cấu tạo của chất A, ta có :
• Số liên kết đơn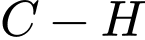 : Có 6 liên kết
: Có 6 liên kết  6 liên kết
6 liên kết 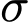 .
.
• Số liên kết đơn : Có 2 liên kết (nối hai nhóm
: Có 2 liên kết (nối hai nhóm 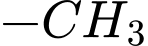 vào mạch chính)
vào mạch chính)  2 liên kết
2 liên kết 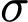 .
.
• Số liên kết ba : Trong 1 liên kết ba có 1 liên kết
: Trong 1 liên kết ba có 1 liên kết 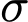 (và 2 liên kết
(và 2 liên kết 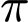 ).
Tổng số liên kết
).
Tổng số liên kết 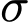 :
:  .
.
Đáp án đúng là: C. 9. Đáp án: C
• Số liên kết đơn
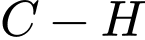 : Có 6 liên kết
: Có 6 liên kết  6 liên kết
6 liên kết 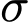 .
.• Số liên kết đơn
 : Có 2 liên kết (nối hai nhóm
: Có 2 liên kết (nối hai nhóm 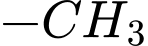 vào mạch chính)
vào mạch chính)  2 liên kết
2 liên kết 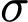 .
.• Số liên kết ba
 : Trong 1 liên kết ba có 1 liên kết
: Trong 1 liên kết ba có 1 liên kết 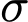 (và 2 liên kết
(và 2 liên kết 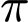 ).
Tổng số liên kết
).
Tổng số liên kết 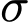 :
:  .
.Đáp án đúng là: C. 9. Đáp án: C
Câu 4 [242121]: Phân tử nào dưới đây có các nguyên tử đều đạt cấu hình electron bão hòa theo quy tắc octet?
A, PCl5.
B, CH4.
C, BF3.
D, SF6.
HƯỚNG DẪN GIẢI:
- Công thức Lewis của các chất được biểu diễn như sau:
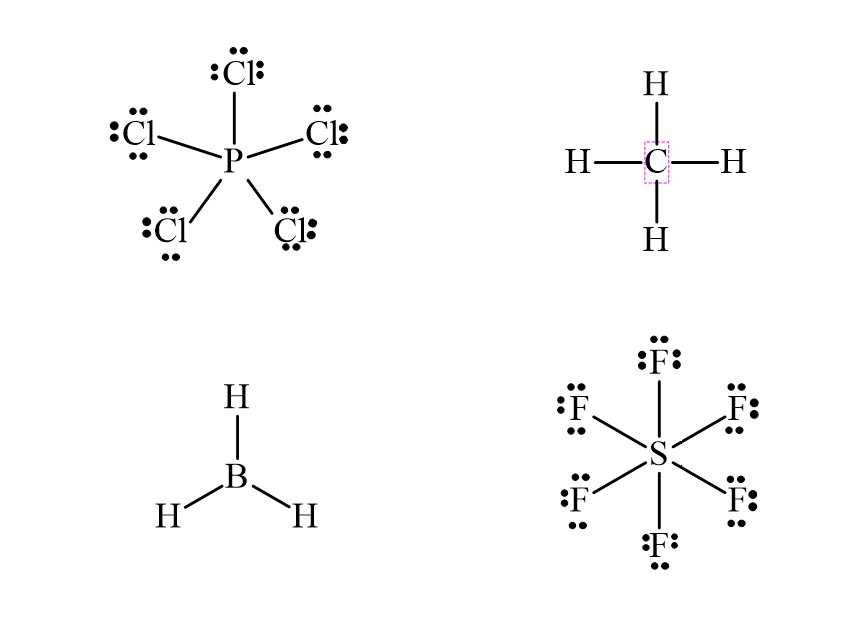
Nhìn vào hình vẽ ta nhận thấy chỉ có nguyên tử C trong CH4 có 8 electron xung quanh (Với mỗi một liên kết ứng với 2 electron)
⟹ Chọn đáp án: B Đáp án: B
- Công thức Lewis của các chất được biểu diễn như sau:

Nhìn vào hình vẽ ta nhận thấy chỉ có nguyên tử C trong CH4 có 8 electron xung quanh (Với mỗi một liên kết ứng với 2 electron)
⟹ Chọn đáp án: B Đáp án: B
Câu 5 [702833]: Sau khi biết công thức thực nghiệm, có thể xác định công thức phân tử của hợp chất hữu cơ dựa trên đặc điểm nào sau đây?
A, Phân tử khối của chất.
B, Thành phần phần trăm về khối lượng các nguyên tố có trong phân tử chất.
C, Khối lượng các sản phẩm thu được khi đốt cháy hoàn toàn một lượng chất xác định.
D, Các hấp thụ đặc trưng trên phổ IR của chất.
Công thức thực nghiệm chỉ cho biết tỷ lệ tối giản giữa các nguyên tố, không phản ánh đầy đủ số lượng thực tế của các nguyên tử trong phân tử nên phân tử khối là yếu tố cần thiết để chuyển từ công thức thực nghiệm (chỉ tỷ lệ nguyên tố) sang công thức phân tử (phản ánh đúng số lượng nguyên tử trong phân tử).
⇒ Chọn đáp án A Đáp án: A
⇒ Chọn đáp án A Đáp án: A
Câu 6 [1108537]: Cặp chất nào sau đây có thể phân biệt bằng phản ứng tạo iodoform?
A, CH3CHO và CH3COCH3.
B, CH3CHO và C2H5COCH3.
C, CH3OCH3 và C2H5COC2H5.
D, CH3CHO và C2H5COC2H5.
⭐Phản ứng iodoform ( ) dùng để nhận biết các hợp chất có nhóm methyl ketone (
) dùng để nhận biết các hợp chất có nhóm methyl ketone (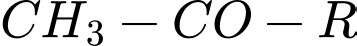 ) hoặc các alcohol có cấu trúc
) hoặc các alcohol có cấu trúc 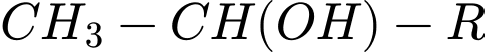 .
.
• A.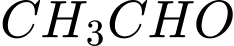 và
và 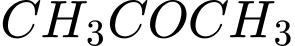 : Cả hai đều có nhóm methyl ketone nên đều phản ứng tạo kết tủa vàng. Không phân biệt được.
: Cả hai đều có nhóm methyl ketone nên đều phản ứng tạo kết tủa vàng. Không phân biệt được.
• B.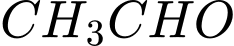 và
và  : Cả hai đều có nhóm methyl ketone. Không phân biệt được.
: Cả hai đều có nhóm methyl ketone. Không phân biệt được.
• C. và
và 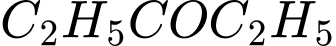 : Cả hai đều không phản ứng. Không phân biệt được.
: Cả hai đều không phản ứng. Không phân biệt được.
• D.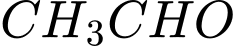 và
và 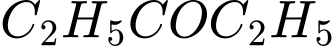 :
:
o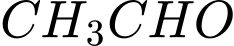 (Acetaldehyde): Có nhóm methyl liên kết với carbonyl
(Acetaldehyde): Có nhóm methyl liên kết với carbonyl  Có phản ứng tạo kết tủa vàng
Có phản ứng tạo kết tủa vàng 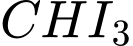 .
.
o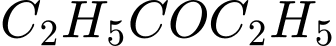 (Diethyl ketone): Không có nhóm methyl ketone (chỉ có nhóm ethyl)
(Diethyl ketone): Không có nhóm methyl ketone (chỉ có nhóm ethyl)  Không phản ứng.
Không phản ứng.
Đáp án đúng là: D. Đáp án: D
 ) dùng để nhận biết các hợp chất có nhóm methyl ketone (
) dùng để nhận biết các hợp chất có nhóm methyl ketone (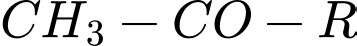 ) hoặc các alcohol có cấu trúc
) hoặc các alcohol có cấu trúc 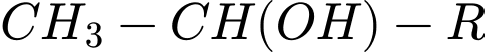 .
.• A.
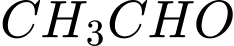 và
và 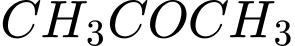 : Cả hai đều có nhóm methyl ketone nên đều phản ứng tạo kết tủa vàng. Không phân biệt được.
: Cả hai đều có nhóm methyl ketone nên đều phản ứng tạo kết tủa vàng. Không phân biệt được.• B.
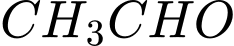 và
và  : Cả hai đều có nhóm methyl ketone. Không phân biệt được.
: Cả hai đều có nhóm methyl ketone. Không phân biệt được.• C.
 và
và 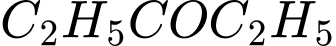 : Cả hai đều không phản ứng. Không phân biệt được.
: Cả hai đều không phản ứng. Không phân biệt được.• D.
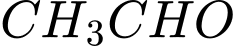 và
và 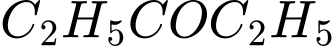 :
:o
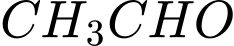 (Acetaldehyde): Có nhóm methyl liên kết với carbonyl
(Acetaldehyde): Có nhóm methyl liên kết với carbonyl  Có phản ứng tạo kết tủa vàng
Có phản ứng tạo kết tủa vàng 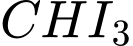 .
.o
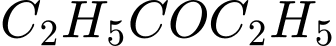 (Diethyl ketone): Không có nhóm methyl ketone (chỉ có nhóm ethyl)
(Diethyl ketone): Không có nhóm methyl ketone (chỉ có nhóm ethyl)  Không phản ứng.
Không phản ứng.Đáp án đúng là: D. Đáp án: D
Câu 7 [186490]: Phát biểu không đúng là
A, Trong điều kiện thường, NH3 là khí không màu, mùi khai.
B, Khí NH3 nặng hơn không khí.
C, Khí NH3 dễ hóa lỏng hơn O2, tan nhiều trong nước.
D, Liên kết giữa N và 3 nguyên tử H là liên kết cộng hoá trị có cực.
B. Sai, tỉ khối của NH3 với không khí = 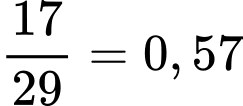 < 1 nên NH3 nhẹ hơn không khí. Đáp án: B
< 1 nên NH3 nhẹ hơn không khí. Đáp án: B
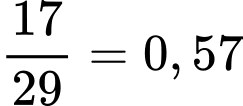 < 1 nên NH3 nhẹ hơn không khí. Đáp án: B
< 1 nên NH3 nhẹ hơn không khí. Đáp án: B
Câu 8 [560808]: Sodium hydroxide (hay xút ăn da) là chất rắn, không màu, dễ nóng chảy, hút ẩm mạnh, tan nhiều trong nước và tỏa ra một lượng nhiệt lớn. Công thức của sodium hydroxide là
A, Ca(OH)2.
B, NaOH.
C, NaHCO3.
D, Na2CO3.
Hydroxide là một nhóm chức hóa học, công thức hóa học là OH−, gồm một nguyên tử oxygen liên kết với một nguyên tử hydrogen
⤑ Sodium là Na; hydroxide là OH nên sodium hydroxide có công thức là NaOH.
⇒ Chọn đáp án B Đáp án: B
⤑ Sodium là Na; hydroxide là OH nên sodium hydroxide có công thức là NaOH.
⇒ Chọn đáp án B Đáp án: B
Câu 9 [706042]: Ion kim loại nào sau đây không bị khử bởi Zn?
A, Cu2+.
B, Ag+.
C, Al3+.
D, Hg2+.
Kim loại hoạt động mạnh hơn có thể đẩy kim loại hoạt động yếu hơn ra khỏi dung dịch muối của nó.
Bảng thế điện cực chuẩn của kim loại có thể được sắp xếp thành một dãy như sau (còn được gọi là dãy điện hóa của kim loại):

→ Zn không thể phản ứng với Al3+.
⟹ Chọn đáp án C Đáp án: C
Bảng thế điện cực chuẩn của kim loại có thể được sắp xếp thành một dãy như sau (còn được gọi là dãy điện hóa của kim loại):

→ Zn không thể phản ứng với Al3+.
⟹ Chọn đáp án C Đáp án: C
Câu 10 [239359]: Dãy gồm các chất đều có thể làm mất tính cứng tạm thời của nước là:
A, HCl, NaOH, Na2CO3.
B, NaOH, Na3PO4, Na2CO3.
C, KCl, Ca(OH)2, Na2CO3.
D, HCl, Ca(OH)2, Na2CO3.
Ta dùng dãy các chất NaOH, Na3PO4; Na2CO3 có thể làm mất tính cứng tạm thời của nước
Ca(HCO3)2 + 2NaOH → CaCO3↓ + Na2CO3 + H2O
3Mg(HCO2)2 + 2Na3PO4 → Mg3(PO4)2↓ + 6NaHCO3
Ca(HCO3)2 + Na2CO3 → CaCO3↓ + 2NaHCO3
⟹ Chọn đáp án B
Đáp án: B
Ca(HCO3)2 + 2NaOH → CaCO3↓ + Na2CO3 + H2O
3Mg(HCO2)2 + 2Na3PO4 → Mg3(PO4)2↓ + 6NaHCO3
Ca(HCO3)2 + Na2CO3 → CaCO3↓ + 2NaHCO3
⟹ Chọn đáp án B
Đáp án: B
Câu 11 [706062]: Một pin Galvani Mg–Cu có sức điện động chuẩn bằng 2,696 V. Biết 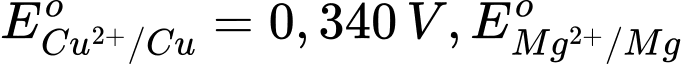 là
là
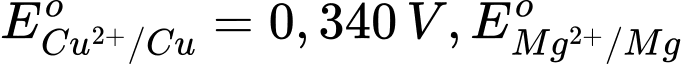 là
là A, 2,344 V.
B, –2,356 V.
C, 3,036 V.
D, –3,260 V.
Eo pin = Eo cathode - Eo anode
Với pin Mg - Cu, phản ứng xảy ra :
Anode : Mg ⟶ Mg2+ + 2e
Cathode : Cu2+ + 2e ⟶ Cu
Eo pin = Eo Cu2+/Cu - Eo Mg2+/Mg
2,696 = 0,340 - Eo Mg2+/Mg
⟶ Eo Mg2+/Mg = -2,356 V
⟹ Chọn đáp án B Đáp án: B
Với pin Mg - Cu, phản ứng xảy ra :
Anode : Mg ⟶ Mg2+ + 2e
Cathode : Cu2+ + 2e ⟶ Cu
Eo pin = Eo Cu2+/Cu - Eo Mg2+/Mg
2,696 = 0,340 - Eo Mg2+/Mg
⟶ Eo Mg2+/Mg = -2,356 V
⟹ Chọn đáp án B Đáp án: B
Câu 12 [706065]: Một nguyên tố của dãy chuyển tiếp thể hiện nhiều số oxi hoá dương trong các hợp chất khác nhau. Đó là do
A, nguyên tử có bán kính lớn và có nhiều electron hoá trị.
B, nguyên tử có nhiều electron hoá trị, nguyên tố có độ âm điện nhỏ.
C, nguyên tử có nhiều electron hoá trị, nguyên tố có độ âm điện lớn.
D, nguyên tử có bán kính lớn, nguyên tố có độ âm điện nhỏ.
Phân tích các đáp án :
❌ A. Nguyên tố có nhiều electron hóa trị, nhưng điều quan trọng là độ âm điện nhỏ mới giúp chúng dễ mất electron và có nhiều số oxi hóa.
✔️ B. Có nhiều electron hóa trị (do phân lớp d chưa bão hòa). Có độ âm điện nhỏ, nên dễ mất nhiều electron và tồn tại ở nhiều mức oxi hóa khác nhau.
❌ C. Nếu độ âm điện lớn, nguyên tử có xu hướng giữ electron thay vì mất electron, nên không thể có nhiều số oxi hóa dương.
❌ D. Bán kính nguyên tử không phải yếu tố quyết định số oxi hóa.
⟹ Chọn đáp án B Đáp án: B
❌ A. Nguyên tố có nhiều electron hóa trị, nhưng điều quan trọng là độ âm điện nhỏ mới giúp chúng dễ mất electron và có nhiều số oxi hóa.
✔️ B. Có nhiều electron hóa trị (do phân lớp d chưa bão hòa). Có độ âm điện nhỏ, nên dễ mất nhiều electron và tồn tại ở nhiều mức oxi hóa khác nhau.
❌ C. Nếu độ âm điện lớn, nguyên tử có xu hướng giữ electron thay vì mất electron, nên không thể có nhiều số oxi hóa dương.
❌ D. Bán kính nguyên tử không phải yếu tố quyết định số oxi hóa.
⟹ Chọn đáp án B Đáp án: B
Câu 13 [703815]: “Trong tinh thể kim loại, liên kết kim loại được hình thành do ...(1)... giữa các electron hoá trị tự do với các ...(2)... kim loại ở các nút mạng”. Nội dung phù hợp trong ô trống (1), (2) lần lượt là
A, lực hút tĩnh điện, ion dương.
B, lực hút tĩnh điện, ion âm.
C, lực hạt nhân, ion dương.
D, lực đẩy tĩnh điện, ion âm.
Trong tinh thể kim loại, các nguyên tử kim loại giải phóng electron hóa trị (electron ở lớp ngoài cùng) để trở thành ion dương. Lực hút tĩnh điện giữa các electron tự do và ion dương kim loại là yếu tố chính giữ các ion dương ở vị trí cố định trong mạng tinh thể. Do đó, lực hút tĩnh điện là đặc trưng cơ bản của liên kết kim loại.
⇒ Trong tinh thể kim loại, liên kết kim loại được hình thành do lực hút tĩnh điện giữa các electron hoá trị tự do với các ion dương kim loại ở các nút mạng.
Chọn đáp án A Đáp án: A
⇒ Trong tinh thể kim loại, liên kết kim loại được hình thành do lực hút tĩnh điện giữa các electron hoá trị tự do với các ion dương kim loại ở các nút mạng.
Chọn đáp án A Đáp án: A
Câu 14 [705735]: Có hai thí nghiệm dưới đây:
∎ Thí nghiệm 1 ở 0 °C: Có một ống nghiệm chứa 1 mL dung dịch copper(II) sulfate 0,5% màu xanh nhạt. Thêm từ từ cho đến hết 2 mL dung dịch hydrochloric acid đặc không màu vào ống nghiệm đó thì thu được dung dịch có màu vàng chanh do có quá trình:
[Cu(OH2)6]2+(aq) + 4Cl–(aq)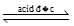 [CuCl4]2–(aq) + 6H2O(l); KC = 4,18×105
[CuCl4]2–(aq) + 6H2O(l); KC = 4,18×105
∎ Thí nghiệm 2 ở 20 °C: Có một ống nghiệm chứa 1 mL dung dịch copper(II) sulfate 0,5% màu xanh nhạt. Thêm từ từ cho đến hết 2 mL dung dịch sodium chloride bão hoà không màu vào ống nghiệm đó thì thu được dung dịch có màu xanh nhạt hơn so với ban đầu.
Trong các phát biểu sau:
(a) Biểu thức tính hằng số cân bằng của phản ứng ở thí nghiệm 1 là:
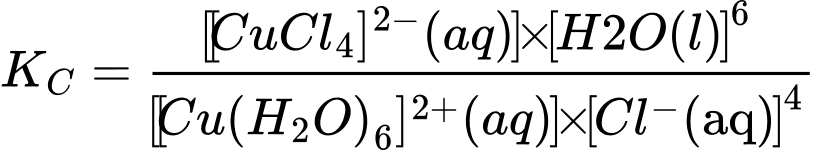
(b) Trong thí nghiệm 1, phản ứng nghịch diễn ra thuận lợi hơn so với phản ứng thuận.
(c) Trong thí nghiệm 1, nồng độ anion Cl– càng cao thì phản ứng thuận càng dễ diễn ra.
(d) Trong thí nghiệm 2 không có dấu hiệu của phản ứng hình thành phức chất.
Các phát biểu đúng là
∎ Thí nghiệm 1 ở 0 °C: Có một ống nghiệm chứa 1 mL dung dịch copper(II) sulfate 0,5% màu xanh nhạt. Thêm từ từ cho đến hết 2 mL dung dịch hydrochloric acid đặc không màu vào ống nghiệm đó thì thu được dung dịch có màu vàng chanh do có quá trình:
[Cu(OH2)6]2+(aq) + 4Cl–(aq)
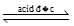 [CuCl4]2–(aq) + 6H2O(l); KC = 4,18×105
[CuCl4]2–(aq) + 6H2O(l); KC = 4,18×105∎ Thí nghiệm 2 ở 20 °C: Có một ống nghiệm chứa 1 mL dung dịch copper(II) sulfate 0,5% màu xanh nhạt. Thêm từ từ cho đến hết 2 mL dung dịch sodium chloride bão hoà không màu vào ống nghiệm đó thì thu được dung dịch có màu xanh nhạt hơn so với ban đầu.
Trong các phát biểu sau:
(a) Biểu thức tính hằng số cân bằng của phản ứng ở thí nghiệm 1 là:
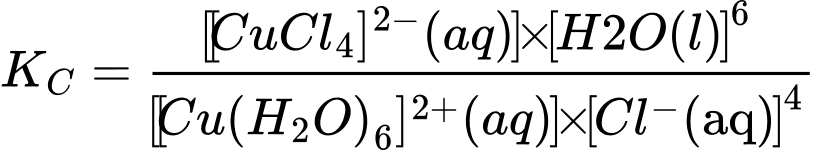
(b) Trong thí nghiệm 1, phản ứng nghịch diễn ra thuận lợi hơn so với phản ứng thuận.
(c) Trong thí nghiệm 1, nồng độ anion Cl– càng cao thì phản ứng thuận càng dễ diễn ra.
(d) Trong thí nghiệm 2 không có dấu hiệu của phản ứng hình thành phức chất.
Các phát biểu đúng là
A, (a), (b).
B, (b), (c).
C, (c), (d).
D, (a), (c), (d).
Đối với hệ phản ứng thuận nghịch đồng thể (hệ chỉ gồm chất khí hoăc chất tan trong dung dịch ) tổng quát dạng :
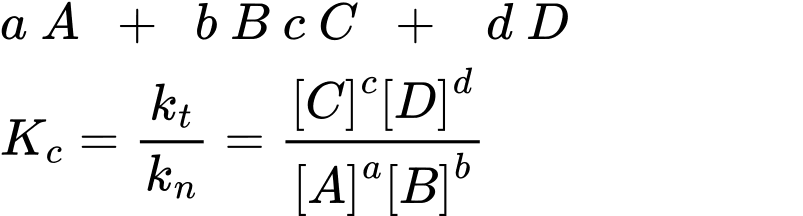
(Trong đó là nồng độ mol/l của các chất A , B , C , D ở trạng thái cân bằng )
là nồng độ mol/l của các chất A , B , C , D ở trạng thái cân bằng )
Phân tích các phát biểu:
✔️(a) – Đúng. Biểu thức tính hằng số cân bằng của phản ứng ở thí nghiệm 1 là:
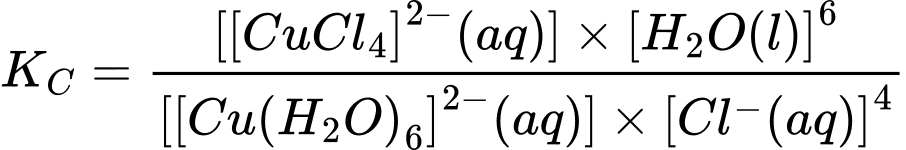
❌(b) – Sai. Phản ứng thuận diễn ra thuận lợi hơn với hằng số cân bằng 4,18.105
✔️(c) – Đúng. Khi nồng độ Cl- càng cao, theo nguyên lí chuyển dịch cân bằng làm cân bằng chuyển dịch theo chiều thuận.
✔️(d) – Đúng. Nếu hình thành phức [CuCl4]2-(aq) phải có màu vàng chanh nhưng thí nghiệm 2 không thấy hiện tượng này.
⟹Có 3 phát biểu đúng là (a), (c), (d).
⟹Chọn đáp án D Đáp án: D
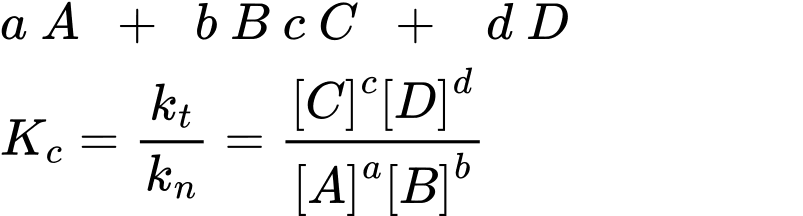
(Trong đó
 là nồng độ mol/l của các chất A , B , C , D ở trạng thái cân bằng )
là nồng độ mol/l của các chất A , B , C , D ở trạng thái cân bằng )Phân tích các phát biểu:
✔️(a) – Đúng. Biểu thức tính hằng số cân bằng của phản ứng ở thí nghiệm 1 là:
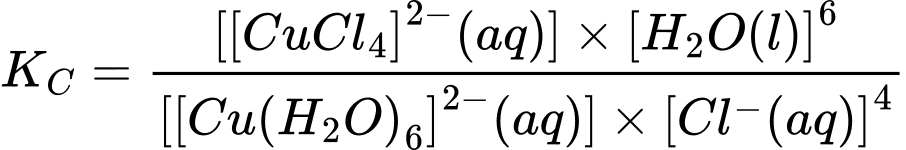
❌(b) – Sai. Phản ứng thuận diễn ra thuận lợi hơn với hằng số cân bằng 4,18.105
✔️(c) – Đúng. Khi nồng độ Cl- càng cao, theo nguyên lí chuyển dịch cân bằng làm cân bằng chuyển dịch theo chiều thuận.
✔️(d) – Đúng. Nếu hình thành phức [CuCl4]2-(aq) phải có màu vàng chanh nhưng thí nghiệm 2 không thấy hiện tượng này.
⟹Có 3 phát biểu đúng là (a), (c), (d).
⟹Chọn đáp án D Đáp án: D
Câu 15 [706135]: Phổ hồng ngoại của hợp chất hữu cơ nào dưới đây không có hấp thụ ở vùng 1750 – 1700 cm–1?
A, Alcohol.
B, Ketone.
C, Ester.
D, Aldehyde.
Phân tích các đáp án:
❌ A. Alcohol có nhóm chứa OH, liên kết O-H số sóng hấp thụ đặc trưng 3650 - 3200 cm-1
✔️ B. Keton có nhóm chứa C=O, liên kết C=O số sóng hấp thụ đặc trưng 1740 - 1670 cm-1
✔️ C. Ester có nhóm chứa - COO, liên kết C=O và C-O số sóng hấp thụ đặc trưng 1750-1715 cm-1 và 1300-1000 cm-1
✔️ D. Aldehyde có nhóm chứa - CHO, liên kết C=O và C-H số sóng hấp thụ đặc trưng 1740-1700cm-1 và 2900-2700 cm-1
⟹ Chọn đáp án A Đáp án: A
❌ A. Alcohol có nhóm chứa OH, liên kết O-H số sóng hấp thụ đặc trưng 3650 - 3200 cm-1
✔️ B. Keton có nhóm chứa C=O, liên kết C=O số sóng hấp thụ đặc trưng 1740 - 1670 cm-1
✔️ C. Ester có nhóm chứa - COO, liên kết C=O và C-O số sóng hấp thụ đặc trưng 1750-1715 cm-1 và 1300-1000 cm-1
✔️ D. Aldehyde có nhóm chứa - CHO, liên kết C=O và C-H số sóng hấp thụ đặc trưng 1740-1700cm-1 và 2900-2700 cm-1
⟹ Chọn đáp án A Đáp án: A
Câu 16 [706136]: Tiến hành đo phổ MS và phổ IR của một hợp chất X, kết quả được cho như sau:
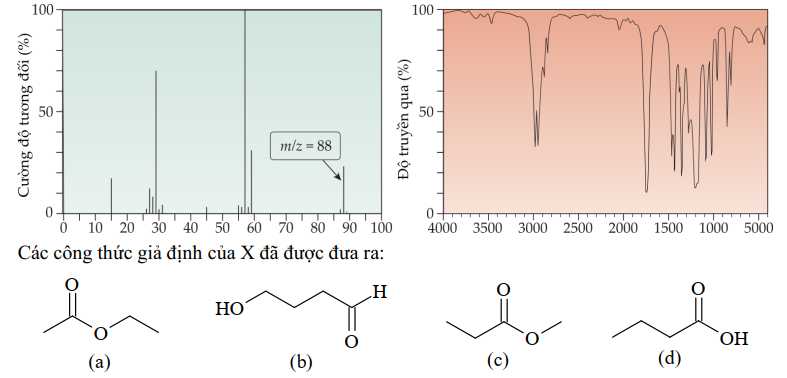
Từ các kết quả đo phổ MS và phổ IR của một hợp chất X, có thể loại bỏ đi được trường hợp giả định nào sau đây?

Từ các kết quả đo phổ MS và phổ IR của một hợp chất X, có thể loại bỏ đi được trường hợp giả định nào sau đây?
A, (a), (b).
B, (b), (d).
C, (a), (b), (c).
D, (a), (c), (d).
Từ phổ khối lượng, phân tử khối của X là 88 amu.
Từ phổ IR, có tín hiệu được trưng trong khoảng 1700 cm-1 cho liên kết C=O
Không có tín hiệu đặc trưng cho liên kết OH (alcohol) 3600 – 3300 cm-1 và OH (carboxylic acid) 3300 – 2500 cm-1
Các trường hợp giả định có thể bỏ qua là
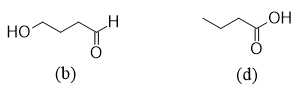
⟹ Chọn đáp án B Đáp án: B
Từ phổ IR, có tín hiệu được trưng trong khoảng 1700 cm-1 cho liên kết C=O
Không có tín hiệu đặc trưng cho liên kết OH (alcohol) 3600 – 3300 cm-1 và OH (carboxylic acid) 3300 – 2500 cm-1
Các trường hợp giả định có thể bỏ qua là
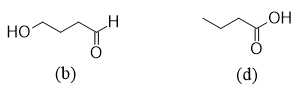
⟹ Chọn đáp án B Đáp án: B
Câu 17 [705864]: Bảng sau đây hiển thị tỉ lệ phần trăm khối lượng của các nguyên tố trong một phân tử sinh học nhất định:
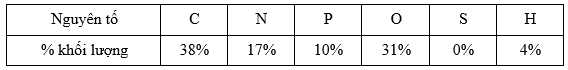
Câu nào sau đây mô tả tốt nhất về phân tử sinh học?

Câu nào sau đây mô tả tốt nhất về phân tử sinh học?
A, Phân tử này là một loại ester.
B, Phân từ này là một nucleic acid.
C, Phân tử này là một loại carbohydrate.
D, Phân tử này là một loại amino acid.
Phân tích các đáp án :
❌A – Sai. Phân tử ester chứa 3 nguyên tố C, H, O.
✔️B – Đúng. Acid nucleic được cấu tạo bởi các đơn phân gọi là nucleotide, chúng được cấu tạo bởi 3 thành phần: đường 5-carbon, nhóm gốc phosphate và nhóm gốc base chứa nitrogen. Có hai loại Acid nucleic chính là deoxyribonucleic acid (DNA) và ribonucleic acid (RNA). Các nguyên tố cấu thành lên nucleic acid là C, H, O, N, P.
❌C – Sai. Phân tử carbohydrate chứa 3 nguyên tố C, H, O.
❌D – Sai. Phân tử amino acid chứa 4 nguyên tố C, H, O, N.
⟹ Chọn đáp án B Đáp án: B
❌A – Sai. Phân tử ester chứa 3 nguyên tố C, H, O.
✔️B – Đúng. Acid nucleic được cấu tạo bởi các đơn phân gọi là nucleotide, chúng được cấu tạo bởi 3 thành phần: đường 5-carbon, nhóm gốc phosphate và nhóm gốc base chứa nitrogen. Có hai loại Acid nucleic chính là deoxyribonucleic acid (DNA) và ribonucleic acid (RNA). Các nguyên tố cấu thành lên nucleic acid là C, H, O, N, P.
❌C – Sai. Phân tử carbohydrate chứa 3 nguyên tố C, H, O.
❌D – Sai. Phân tử amino acid chứa 4 nguyên tố C, H, O, N.
⟹ Chọn đáp án B Đáp án: B
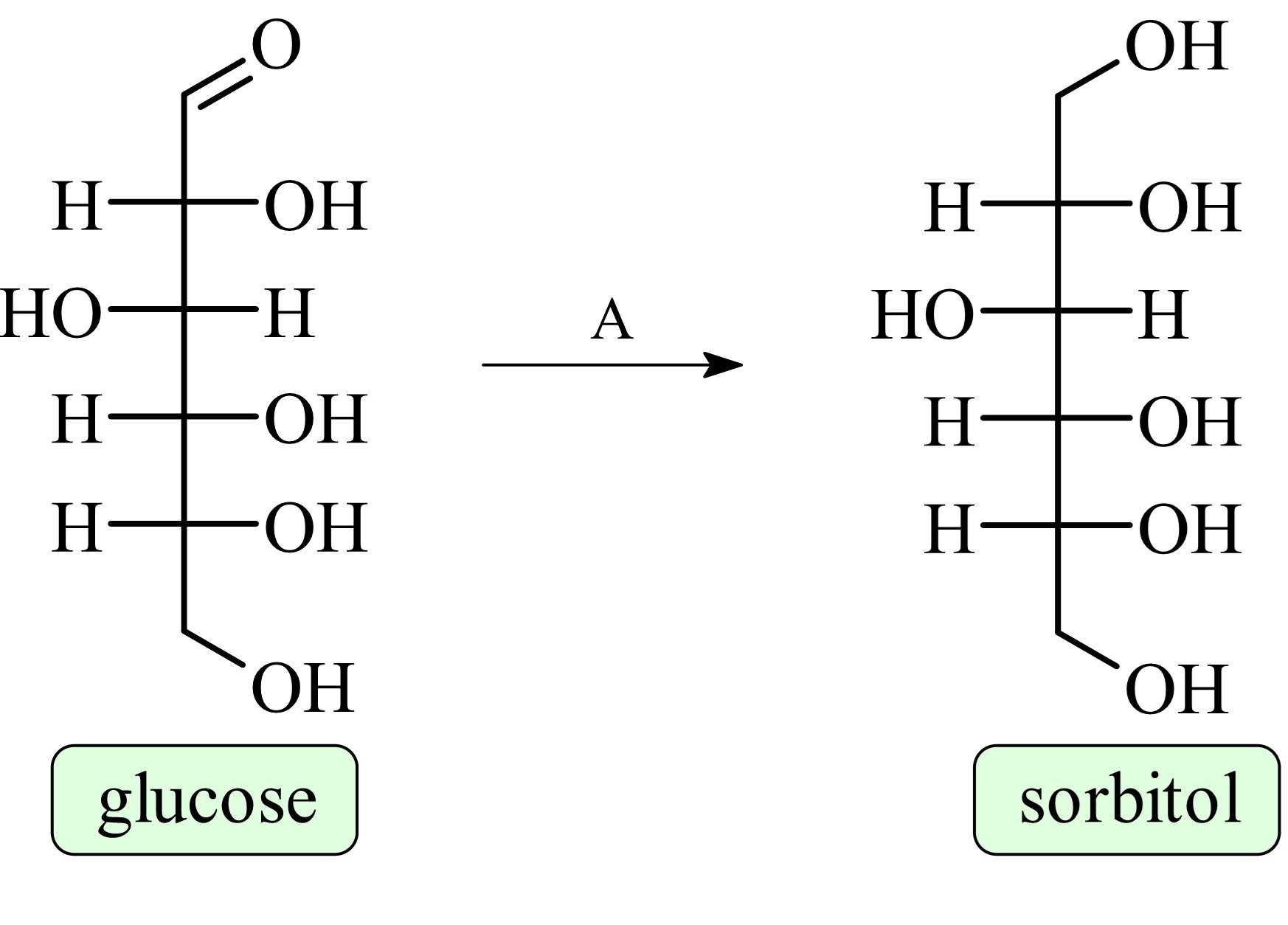
Câu 18 [1009753]: Cho phản ứng chuyển hóa như hình bên. Tác nhân (A) thích hợp cho phản ứng đó là (xem như điều kiện phản ứng có đủ)

A, H2.
B, Br2.
C, [Ag(NH3)2]OH.
D, HCl.
Khử glucose bằng H2 để tạo thành sobitol.
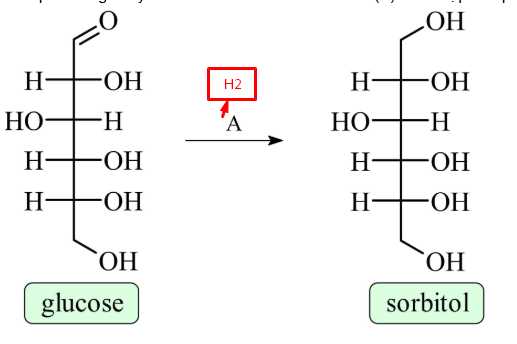

⟹ Chọn đáp án A
Đáp án: APHẦN II. Thí sinh trả lời từ câu 1 đến câu 4. Trong mỗi ý a), b), c), d) ở mỗi câu, thí sinh chọn đúng hoặc sai.
Câu 19 [705939]: Một học sinh tiến hành chuẩn bị hai cốc với các thành phần tương ứng như sau:
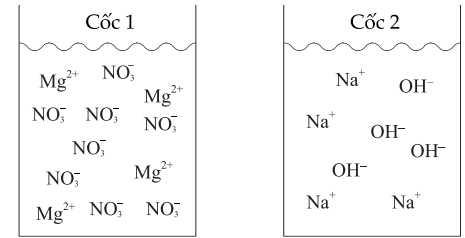
Trộn hai cốc trên vào cốc thứ ba và tạo thành kết tủa Mg(OH)2. Bạn học sinh đưa ra 4 khả năng có thể có về thành phần của cốc thứ ba dưới đây:
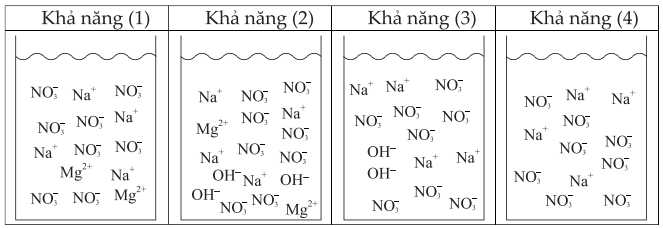

Trộn hai cốc trên vào cốc thứ ba và tạo thành kết tủa Mg(OH)2. Bạn học sinh đưa ra 4 khả năng có thể có về thành phần của cốc thứ ba dưới đây:

Phân tích các phát biểu
✔️A. Đúng. Trộn hai cốc trên vào cốc thứ ba và tạo thành kết tủa Mg(OH)2.
Mg(NO3)2 + 2NaOH → Mg(OH)2 + 2NaNO3
Khi hình thành kết tủa Mg(OH)2 thì ion Mg2+ và OH- mất đi các ion Na+ và NO3- không đổi
✔️B. Đúng. Trộn hai cốc trên vào cốc thứ ba và tạo thành kết tủa Mg(OH)2 tách ra khỏi dung dịch.
❌C. Sai. Số điện tích âm = số điện tích dương, không phải "ion".
❌D. Sai. Từ hình vẽ cốc (1) chứa 4 mol Mg(NO3)2 và cốc (2) chứa 4 mol NaOH
Mg(NO3)2 + 2NaOH → Mg(OH)2 + 2NaNO3
Từ PTHH sau phản ứng NaOH hết, Mg(NO3)2 dư
Dung dịch sau phản ứng gồm: 2 mol Mg(NO3)2 ; 4 mol NaNO3
✔️A. Đúng. Trộn hai cốc trên vào cốc thứ ba và tạo thành kết tủa Mg(OH)2.
Mg(NO3)2 + 2NaOH → Mg(OH)2 + 2NaNO3
Khi hình thành kết tủa Mg(OH)2 thì ion Mg2+ và OH- mất đi các ion Na+ và NO3- không đổi
✔️B. Đúng. Trộn hai cốc trên vào cốc thứ ba và tạo thành kết tủa Mg(OH)2 tách ra khỏi dung dịch.
❌C. Sai. Số điện tích âm = số điện tích dương, không phải "ion".
❌D. Sai. Từ hình vẽ cốc (1) chứa 4 mol Mg(NO3)2 và cốc (2) chứa 4 mol NaOH
Mg(NO3)2 + 2NaOH → Mg(OH)2 + 2NaNO3
Từ PTHH sau phản ứng NaOH hết, Mg(NO3)2 dư
Dung dịch sau phản ứng gồm: 2 mol Mg(NO3)2 ; 4 mol NaNO3
Câu 20 [1108538]:
Sulfuric acid là một trong những hóa chất quan trọng nhất được sử dụng trong công nghiệp; được sản xuất hàng trăm triệu tấn mỗi năm, chiếm nhiều nhất trong ngành công nghiệp hóa chất. Phương pháp sản xuất sulfuric acid phổ biến nhất là phương pháp tiếp xúc, theo đó acid có thể được sản xuất từ quặng pyrite qua các giai đoạn theo sơ đồ sau: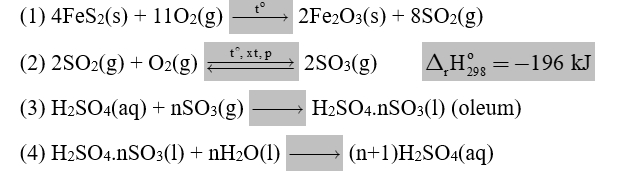
Dùng sulfuric acid 98% hấp thụ SO3(g) trong giai đoạn (3), quá trình này được thực hiện trong tháp tiếp xúc. Để xác định công thức của oleum thu được, người ta pha loãng 8,36 gam oleum vào nước thành 1,0 lít dung dịch sulfuric acid, sau đó tiến hành chuẩn độ 10,00 mL dung dịch acid này bằng dung dịch chuẩn NaOH 0,10 M. Thể tích NaOH trung bình cần sử dụng để chuẩn độ là 20,00 mL.
✔️Nhận định a) – Đúng, vì:
Số mol NaOH dùng chuẩn độ: mol.
mol.
Phản ứng trung hòa: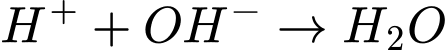 .
.
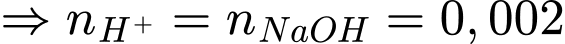 mol.
mol.
Trong 10 mL có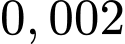 mol
mol  1000 mL có
1000 mL có 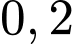 mol
mol 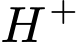 .
.
Vì mỗi phân tử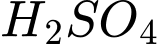 phân ly ra 2
phân ly ra 2 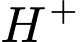 , nên:
, nên:
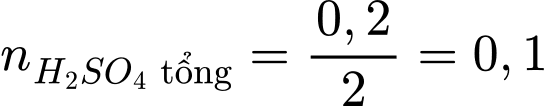 mol.
mol.
Phương trình hòa tan oleum: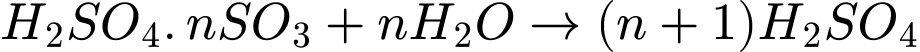 .
.
Số mol oleum là: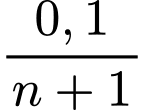 mol.
mol.
Khối lượng oleum: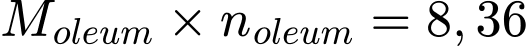
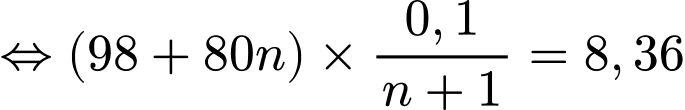
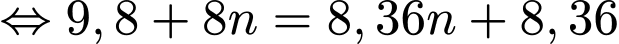
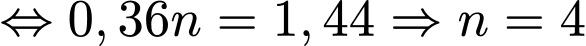 .
.
=> Công thức oleum là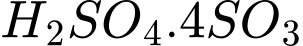 .
.
❌Nhận định b) – Sai, vì: Phản ứng (2) có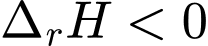 (tỏa nhiệt). Theo nguyên lý Le Chatelier, tăng nhiệt độ sẽ làm cân bằng chuyển dịch theo chiều nghịch (giảm hiệu suất). Người ta chỉ dùng nhiệt độ đủ cao (
(tỏa nhiệt). Theo nguyên lý Le Chatelier, tăng nhiệt độ sẽ làm cân bằng chuyển dịch theo chiều nghịch (giảm hiệu suất). Người ta chỉ dùng nhiệt độ đủ cao (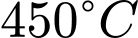 ) để đảm bảo tốc độ phản ứng.
) để đảm bảo tốc độ phản ứng.
✔️Nhận định c) – Đúng, vì: Phản ứng với nước tỏa nhiệt rất mạnh, làm nước bay hơi kéo theo các hạt acid nhỏ tạo thành sương mù (khói mù) khó ngưng tụ và thất thoát acid.
với nước tỏa nhiệt rất mạnh, làm nước bay hơi kéo theo các hạt acid nhỏ tạo thành sương mù (khói mù) khó ngưng tụ và thất thoát acid.
❌Nhận định d) – Sai, vì: Để tăng hiệu quả tiếp xúc (ngược dòng),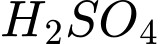 đặc được phun từ trên xuống và
đặc được phun từ trên xuống và  được thổi từ dưới lên.
được thổi từ dưới lên.
Số mol NaOH dùng chuẩn độ:
 mol.
mol.Phản ứng trung hòa:
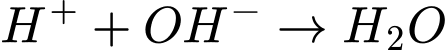 .
.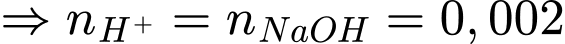 mol.
mol.Trong 10 mL có
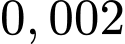 mol
mol  1000 mL có
1000 mL có 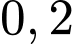 mol
mol 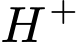 .
.Vì mỗi phân tử
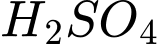 phân ly ra 2
phân ly ra 2 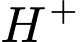 , nên:
, nên: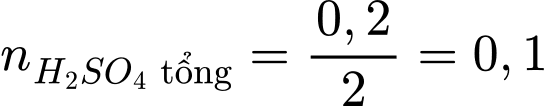 mol.
mol.Phương trình hòa tan oleum:
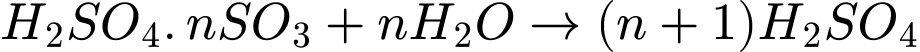 .
.Số mol oleum là:
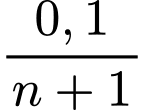 mol.
mol.Khối lượng oleum:
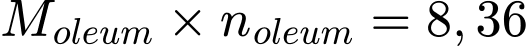
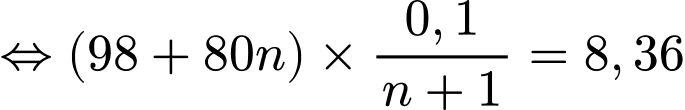
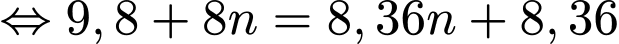
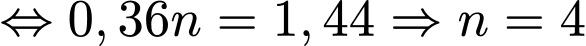 .
.=> Công thức oleum là
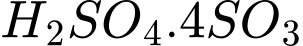 .
.❌Nhận định b) – Sai, vì: Phản ứng (2) có
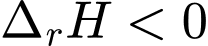 (tỏa nhiệt). Theo nguyên lý Le Chatelier, tăng nhiệt độ sẽ làm cân bằng chuyển dịch theo chiều nghịch (giảm hiệu suất). Người ta chỉ dùng nhiệt độ đủ cao (
(tỏa nhiệt). Theo nguyên lý Le Chatelier, tăng nhiệt độ sẽ làm cân bằng chuyển dịch theo chiều nghịch (giảm hiệu suất). Người ta chỉ dùng nhiệt độ đủ cao (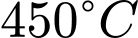 ) để đảm bảo tốc độ phản ứng.
) để đảm bảo tốc độ phản ứng.✔️Nhận định c) – Đúng, vì: Phản ứng
 với nước tỏa nhiệt rất mạnh, làm nước bay hơi kéo theo các hạt acid nhỏ tạo thành sương mù (khói mù) khó ngưng tụ và thất thoát acid.
với nước tỏa nhiệt rất mạnh, làm nước bay hơi kéo theo các hạt acid nhỏ tạo thành sương mù (khói mù) khó ngưng tụ và thất thoát acid.❌Nhận định d) – Sai, vì: Để tăng hiệu quả tiếp xúc (ngược dòng),
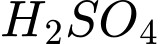 đặc được phun từ trên xuống và
đặc được phun từ trên xuống và  được thổi từ dưới lên.
được thổi từ dưới lên.
Câu 21 [705505]: Giá trị biến thiên enthalpyl chuẩn của phản ứng phân hủy muối carbonate của một số nguyên tố nhóm IIA được cho trong bảng dưới đây:

Biến thiên enthalpy chuẩn của phản ứng phân hủy muối carbonate cũng sẽ cho biết độ bền nhiệt các muối carbonate.

Biến thiên enthalpy chuẩn của phản ứng phân hủy muối carbonate cũng sẽ cho biết độ bền nhiệt các muối carbonate.
Phân tích các phát biểu:
✔️ (a) Đúng. Nhiệt phân muối carbonate của các chất trên đều thu được basic oxide và khí CO2.
Phương trình tổng quát: MCO3 –to⟶ MO + CO2 (M là kim loại kiềm thổ)
❌ (b) Sai. Giá trị biến thiên enthalpy chuẩn của phản ứng lớn hơn 0 thì phản ứng sẽ thu nhiệt.
✔️ (c) Đúng. Độ bền nhiệt của muối có xu hướng tăng từ MgCO3 đến BaCO3 do có biến thiên enthalpy tăng dần càng về sau càng khó phân hủy.
✔️ (d) Đúng. Biến thiên enthalpy chuẩn của phản ứng thì cần nhận vào càng nhiều năng lượng thì phản ứng phân hủy mới xảy ra.
✔️ (a) Đúng. Nhiệt phân muối carbonate của các chất trên đều thu được basic oxide và khí CO2.
Phương trình tổng quát: MCO3 –to⟶ MO + CO2 (M là kim loại kiềm thổ)
❌ (b) Sai. Giá trị biến thiên enthalpy chuẩn của phản ứng lớn hơn 0 thì phản ứng sẽ thu nhiệt.
✔️ (c) Đúng. Độ bền nhiệt của muối có xu hướng tăng từ MgCO3 đến BaCO3 do có biến thiên enthalpy tăng dần càng về sau càng khó phân hủy.
✔️ (d) Đúng. Biến thiên enthalpy chuẩn của phản ứng thì cần nhận vào càng nhiều năng lượng thì phản ứng phân hủy mới xảy ra.
Câu 22 [704379]: Nghiên cứu phản ứng giữa bromine với aniline được tiến hành như sau:
▪ Bước 1: Cho vào ống nghiệm 1 mL dung dịch aniline C6H5NH2.
▪ Bước 2: Thêm tiếp từ từ 0,5 – 1 mL nước bromine, vừa thêm vừa lắc.
▪ Bước 1: Cho vào ống nghiệm 1 mL dung dịch aniline C6H5NH2.
▪ Bước 2: Thêm tiếp từ từ 0,5 – 1 mL nước bromine, vừa thêm vừa lắc.
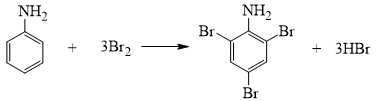
Khi cho dung dịch Br2 tác dụng với dung dịch aniline thấy xuất hiện kết tủa trắng và mất màu dung dịch bromine.
Phân tích các phát biểu:
✔️ (a) Đúng. Lắc đều để bromine và aniline trộn lẫn tốt hơn, tăng diện tích tiếp xúc giữa chúng trong quá trình phản ứng.
✔️ (b) Đúng. Khi bromine tác dụng với aniline, nhóm –NH2 làm tăng hoạt tính của nhân thơm, dẫn đến phản ứng thế 3 nguyên tử bromine vào vị trí 2, 4, 6 trên vòng benzene, tạo ra 2,4,6-tribromoaniline (C6H2NH2(Br)3) kết tủa màu trắng.
❌ (c) Sai. Phản ứng giữa bromine và aniline là phản ứng thế, không phải phản ứng cộng. Ba nguyên tử bromine thay thế 3 nguyên tử hydrogen trên vòng benzen thoe tỉ lệ 1 : 3 chứ không cộng.
✔️ (d) Đúng. Nhóm –NH2 là nhóm đẩy electron mạnh, làm tăng mật độ electron trên vòng benzene, đặc biệt tại các vị trí ortho (2,6) và para (4), giúp vòng benzene phản ứng dễ dàng hơn với bromine và ưu tiên thế ở các vị trí này.
PHẦN III. Thí sinh trả lời từ câu 1 đến 6. Thí sinh điền kết quả mỗi câu vào mỗi ô trả lời tương ứng theo hướng dẫn của phiếu trả lời.
Câu 23 [706001]: Để tráng một số lượng gương soi có diện tích bề mặt 0,5 m2 với độ dày 0,1 μm người ta đun nóng dung dịch chứa 30,6 gam glucose với một lượng dung dịch silver nitrate trong ammonia. Biết khối lượng riêng của bạc là 10,49 g/cm3, hiệu suất phản ứng tráng gương là 85% (tính theo glucose). Số lượng gương soi tối đa sản xuất được là bao nhiêu (Lấy phần nguyên của kết quả)?
Thể tích bạc cần cho 1 tấm gương là VAg = 0,5.0,1.10-6 = 5.10-8 m3 = 5.10-2 cm3
Khối lượng Ag cho 1 tấm gương là mAg = 5.10-2. 10,49 = 0,5245 gam
Số mol của glucose là nC6H12O6 = 30,6 : 180 = 0,17 mol
Số mol Ag = 0,17 × 85% × 2 = 0,289 mol
Khối lượng Ag = 31,212 g
Sơ đồ phản ứng: C6H12O6 → 2Ag
Số tấm gương tối đa được sản xuất là
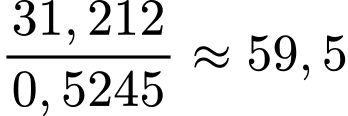
⟹Điền đáp án : 59
Khối lượng Ag cho 1 tấm gương là mAg = 5.10-2. 10,49 = 0,5245 gam
Số mol của glucose là nC6H12O6 = 30,6 : 180 = 0,17 mol
Số mol Ag = 0,17 × 85% × 2 = 0,289 mol
Khối lượng Ag = 31,212 g
Sơ đồ phản ứng: C6H12O6 → 2Ag
Số tấm gương tối đa được sản xuất là
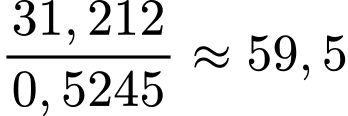
⟹Điền đáp án : 59
Câu 24 [705953]: Hợp chất A là một carboxylic acid đơn chức. Chuẩn bị một mẫu 250 mL dung dịch A bằng cách hòa tan 10,8 g A trong nước. Trong một phép chuẩn độ, 25,00 mL dung dịch NaOH 0,500 M được trung hòa bằng chính xác 21,40 mL dung dịch A. Phân tử khối của carboxylic acid A là bao nhiêu g/mol (Làm tròn đến số nguyên).
RCOOH + NaOH ⟶ RCOONa + H2O
nNaOH = 25 × 0,5 : 1000 = 0,0125 mol = n RCOOH
Trong 21,4 mL dung dịch A ⟶ 0,0125 mol
Trong 250 mL dung dịch A ⟶ 0,146028 mol.
MA = 10,8 : 0,146028 = 73,9 = 74 ( C2H5COOH )
⟹Điền đáp án : 74
nNaOH = 25 × 0,5 : 1000 = 0,0125 mol = n RCOOH
Trong 21,4 mL dung dịch A ⟶ 0,0125 mol
Trong 250 mL dung dịch A ⟶ 0,146028 mol.
MA = 10,8 : 0,146028 = 73,9 = 74 ( C2H5COOH )
⟹Điền đáp án : 74
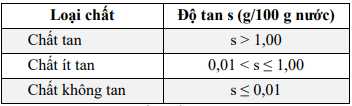
Câu 25 [560951]: Tuỳ theo mục đích sử dụng, có nhiều quy ước phân loại chất tan, chất ít tan và chất không tan. Bảng dưới đây là quy ước phổ biến.
Cho bảng độ tan (g/100 g nước) của một số muối trong nước ở 20 °C như sau:

Có bao nhiêu chất ít tan trong số các chất trên?
Điền đáp án: ..........

Cho bảng độ tan (g/100 g nước) của một số muối trong nước ở 20 °C như sau:

Có bao nhiêu chất ít tan trong số các chất trên?
Điền đáp án: ..........
Chất ít tan có độ tan 0,01< s ≤ 1
=> Có 2 chất ít tan là CaSO4 ( 0,2) và SrSO4 (0,013)
⟹ Điền đáp án: 2
=> Có 2 chất ít tan là CaSO4 ( 0,2) và SrSO4 (0,013)
⟹ Điền đáp án: 2
Câu 26 [705723]: Cho dãy các chất sau: acetic acid, ethyl acetate, isopropylamine, glucose, acetone. Trong số các chất trên, có bao nhiêu tác dụng với Cu(OH)2 ở điều kiện thường?
Các chất tác dụng với Cu(OH)2 ở điều kiện thường là acetic acid, isopropylamine, glucose.
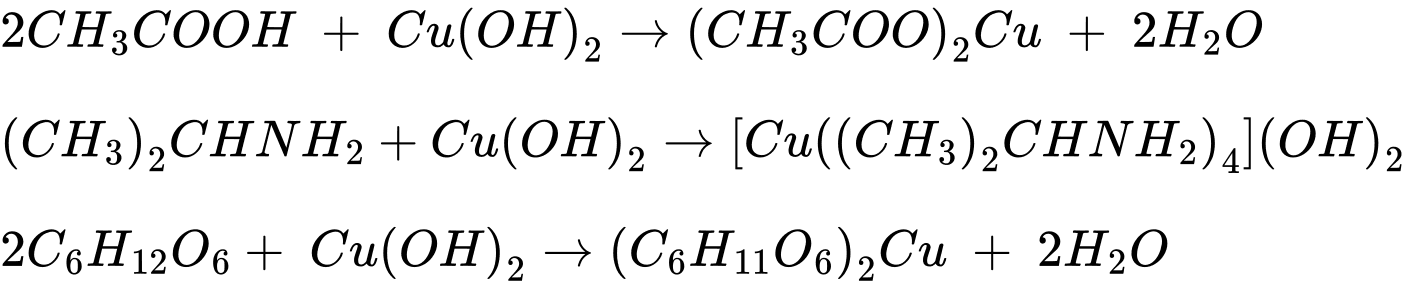
⇒ Điền đáp án: 3
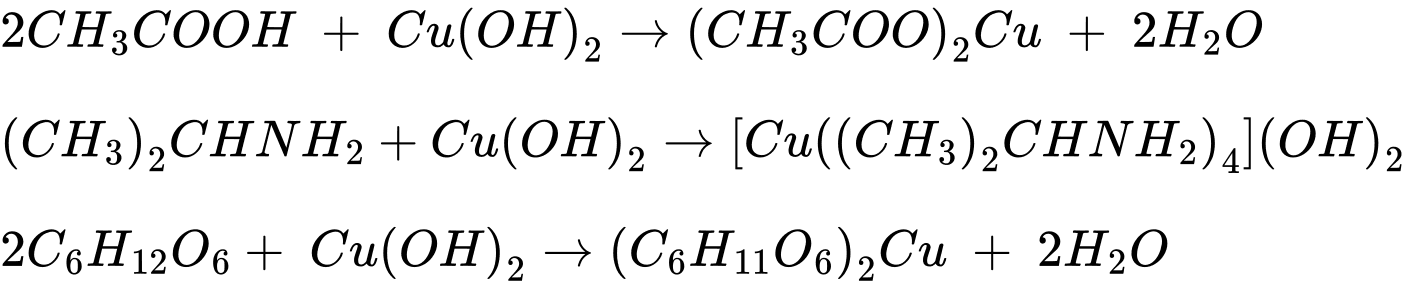
⇒ Điền đáp án: 3
Câu 27 [702627]: Hồng cầu là một loại protein trong máu, có chức năng vận chuyển oxygen từ phổi đến các mô trong cơ thể. Biết hồng cầu chứa 0,33% iron (Fe) theo khối lượng, phân tử khối của hồng cầu là 67 878 g/mol. Có bao nhiêu nguyên tử iron trong một phân tử hồng cầu? (làm tròn đến chữ số nguyên)
Tổng phân tử khối của Fe có trong hồng cầu là: 67878 x 0,33% = 224 (gam.mol-1)
Số nguyên tử Fe có trong 1 phân tử hồng cầu là: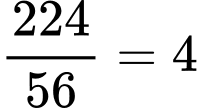 (nguyên tử)
(nguyên tử)
⇒ Điền đáp án: 4
Số nguyên tử Fe có trong 1 phân tử hồng cầu là:
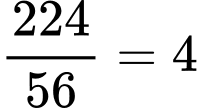 (nguyên tử)
(nguyên tử)⇒ Điền đáp án: 4
Câu 28 [702629]: Viên nén chứa potassium permanganate KMnO4, được hòa tan trong nước tạo thành dung dịch sát trùng để điều trị các bệnh về da. Để kiểm tra hàm lượng KMnO4 có trong một viên thuốc, tiến hành quy trình như sau: Hòa tan năm viên thuốc trong nước cất để tạo thành 100,0 mL dung dịch, thêm dung dịch KMnO4 vào burete. Thêm 25,0 mL dung dịch Na2C2O4 0,200 M vào bình nón và làm ấm, thêm tiếp dung dịch H2SO4 2 M vào bình. Phương trình phản ứng trong phép chuẩn độ như sau:
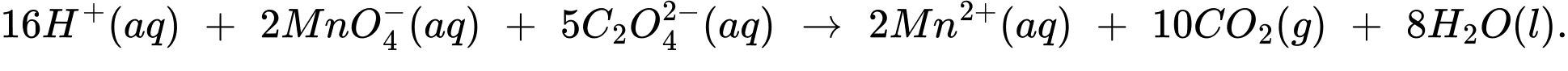
Kết quả trung bình của quá trình chuẩn độ thấy tiêu tốn 16,85 mL dung dịch KMnO4. Tính khối lượng của KMnO4 có trong một viên thuốc (làm tròn kết quả thu được đến phần trăm).
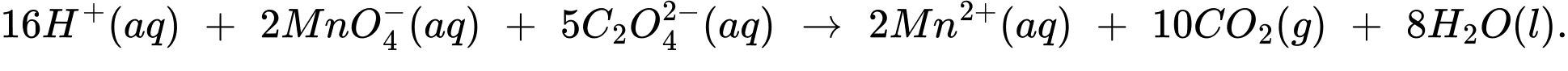
Kết quả trung bình của quá trình chuẩn độ thấy tiêu tốn 16,85 mL dung dịch KMnO4. Tính khối lượng của KMnO4 có trong một viên thuốc (làm tròn kết quả thu được đến phần trăm).
Đổi 25ml = 0,025 L; 16,85 ml = 0,01685 L; 100 ml = 0,1 L
16H+(aq) + 2MnO4-(aq) + 5C2O42-(aq) ⟶ 2Mn2+(aq) + 10CO2(g) + 8H2O(l)
Số mol của dung dịch Na2C2O4 phản ứng là: 0,025 . 0,2 = 0,005 (mol)
Từ PTHH số mol KMnO4 phản ứng là: 0,002 mol
Nồng độ của KMnO4 là: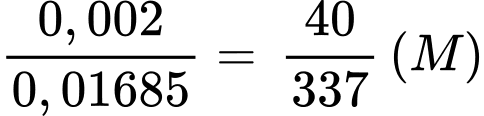
Khối lượng của KMnO4 trong 100ml dung dịch là: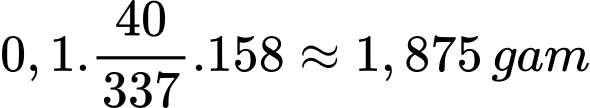
Khối lượng của KMnO4 trong 1 viên thuốc là: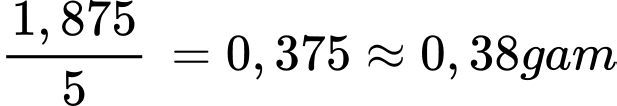
⇒ Điền đáp án: 0,38
16H+(aq) + 2MnO4-(aq) + 5C2O42-(aq) ⟶ 2Mn2+(aq) + 10CO2(g) + 8H2O(l)
Số mol của dung dịch Na2C2O4 phản ứng là: 0,025 . 0,2 = 0,005 (mol)
Từ PTHH số mol KMnO4 phản ứng là: 0,002 mol
Nồng độ của KMnO4 là:
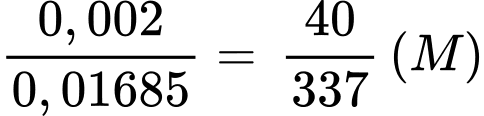
Khối lượng của KMnO4 trong 100ml dung dịch là:
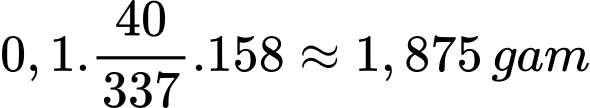
Khối lượng của KMnO4 trong 1 viên thuốc là:
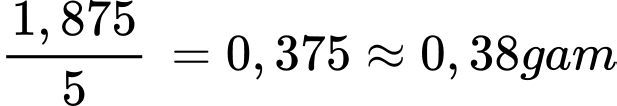
⇒ Điền đáp án: 0,38