Sử dụng đoạn thông tin dưới đây để trả lời câu 17 và câu 18:
Acetic acid thuộc loại acid yếu do khả năng phân li ion H+ không hoàn toàn, quá trình phân li của acetic acid được cho như sau:


Câu 1 [247238]: Dãy nào trong các dãy sau đây gồm các phân lớp electron đã bão hòa?
A, s1, p3, d7, f12.
B, s2, p6, d10, f14.
C, s2, d5, d9, f13.
D, s2, p4, d10, f10.
HƯỚNG DẪN GIẢI:
- Phân lớp electron được gọi là "bão hoà" khi nó chứa số electron đến mức tối đa có thể chứa được
- Một AO chứa được tối đa 2 electron.
+) Phân lớp s có 1 AO, vậy phân lớp s chứa tối đa 2 electron (s2)
+) Phân lớp p có 3 AO, vậy phân lớp p chứa tối đa 2 . 3 = 6 electron (p6)
+) Phân lớp d có 5 AO, vậy phân lớp d chứa tối đa 2 . 5 = 10 electron (d10)
+) Phân lớp f có 7 AO, vậy phân lớp f chứa tối đa 2 . 7 = 14 electron (d14)
⟹ Chọn đáp án: B Đáp án: B
- Phân lớp electron được gọi là "bão hoà" khi nó chứa số electron đến mức tối đa có thể chứa được
- Một AO chứa được tối đa 2 electron.
+) Phân lớp s có 1 AO, vậy phân lớp s chứa tối đa 2 electron (s2)
+) Phân lớp p có 3 AO, vậy phân lớp p chứa tối đa 2 . 3 = 6 electron (p6)
+) Phân lớp d có 5 AO, vậy phân lớp d chứa tối đa 2 . 5 = 10 electron (d10)
+) Phân lớp f có 7 AO, vậy phân lớp f chứa tối đa 2 . 7 = 14 electron (d14)
⟹ Chọn đáp án: B Đáp án: B
Câu 2 [560791]: Tính chất hóa học chung của kim loại kiềm là
A, tính acid.
B, tính base.
C, tính oxi hóa mạnh.
D, tính khử mạnh.
Tính chất hóa học chung của kim loại kiềm là tính khử mạnh.
⇒ Chọn đáp án D Đáp án: D
⇒ Chọn đáp án D Đáp án: D
Câu 3 [308567]: Nhúng giấy quỳ tím vào dung dịch methylamine, màu quỳ tím chuyển thành
A, xanh.
B, đỏ.
C, vàng.
D, tím.
Methylamine có tính base yếu nên sẽ làm quỳ tím chuyển thành màu xanh.
⟹ Chọn đáp án A Đáp án: A
⟹ Chọn đáp án A Đáp án: A
Câu 4 [705800]: Trong các hợp chất cho dưới đây, hợp chất nào chứa mắt xích fructose trong phân tử?
A, Saccharose.
B, Maltose.
C, Tinh bột.
D, Cellulose.
Phân tích các đáp án:
✔️A. Saccharose : Là đisaccharide gồm glucose và fructose
❌B. Maltose: Gồm hai phân tử glucose → Không chứa fructose
❌C. Tinh bột: Là polysaccharide chỉ gồm nhiều mắt xích glucose
❌D. Cellulose: Cũng là polysaccharide, chỉ chứa glucose Đáp án: A
✔️A. Saccharose : Là đisaccharide gồm glucose và fructose
❌B. Maltose: Gồm hai phân tử glucose → Không chứa fructose
❌C. Tinh bột: Là polysaccharide chỉ gồm nhiều mắt xích glucose
❌D. Cellulose: Cũng là polysaccharide, chỉ chứa glucose Đáp án: A
Câu 5 [705805]: Số liên kết sigma (σ) trong phân tử pentane CH3CH2CH2CH2CH3 là
A, 10.
B, 12.
C, 15.
D, 16.
Số liên kết sigma = số H + số liên kết C - C
Phân tử CH3CH2CH2CH2CH3 có 12 H và 4 liên kết C - C.
⟹ Số liên kết sigma = 12 + 4 = 16
Chọn đáp án D Đáp án: D
Phân tử CH3CH2CH2CH2CH3 có 12 H và 4 liên kết C - C.
⟹ Số liên kết sigma = 12 + 4 = 16
Chọn đáp án D Đáp án: D
Câu 6 [186432]: Một học sinh đang tiến hành chuẩn độ bằng chất chỉ thị phenolphthalein. Màu đúng của chất chỉ thị này trong môi trường acid và môi trường kiềm loãng lần lượt là
A, màu hồng và không màu.
B, Không màu và màu hồng.
C, màu đỏ và màu vàng.
D, màu hồng và màu xanh.
Trong môi trường acid: Phenolphtalein không có màu.
Trong môi trường base: Phenolphtalein chuyển sang màu hồng.
Màu đúng của chất chỉ thị này trong môi trường acid và môi trường kiềm loãng lần lượt là : không màu và màu hồng.
⟹Chọn đáp án B
Đáp án: B
Trong môi trường base: Phenolphtalein chuyển sang màu hồng.
Màu đúng của chất chỉ thị này trong môi trường acid và môi trường kiềm loãng lần lượt là : không màu và màu hồng.
⟹Chọn đáp án B
Đáp án: B
Câu 7 [304099]: Ester E có công thức cấu tạo như hình vẽ như sau:
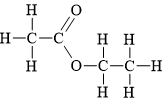
Tên gọi của ester E là

Tên gọi của ester E là
A, Ethyl acetate.
B, Methyl acetate.
C, Methyl ethanoate.
D, Ethyl propionate.
HD: Viết gọn công thức cấu tạo ester và phân tích:
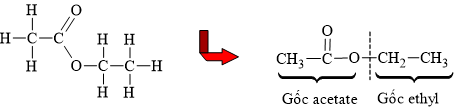
⇒ Tên gọi tương ứng của ester E là ethyl acetate
⟹ Chọn đáp án A. Đáp án: A

⇒ Tên gọi tương ứng của ester E là ethyl acetate
⟹ Chọn đáp án A. Đáp án: A
Câu 8 [703822]: “Hầu hết enzyme là …(1)… đóng vai trò …(2)… cho các phản ứng sinh hoá trong cơ thể”. Nội dung phù hợp trong ô trống (1), (2) lần lượt là
A, lipid, xúc tác sinh học.
B, protein, xúc tác sinh học.
C, carbohydrate, cung cấp năng lượng.
D, vitamin, vận chuyển trung gian.
- Hầu hết enzyme là các protein có cấu trúc đặc biệt, được thiết kế để thực hiện một chức năng cụ thể.
- Enzyme giúp tăng tốc độ các phản ứng sinh hóa trong cơ thể mà không bị tiêu hao trong quá trình phản ứng. Chúng hoạt động bằng cách hạ thấp năng lượng hoạt hóa cần thiết để phản ứng xảy ra. Chúng là các xúc tác sinh học.
⇒ Hầu hết enzyme là protein đóng vai trò xúc tác sinh học cho các phản ứng sinh hoá trong cơ thể.
⇒ Chọn đáp án B Đáp án: B
- Enzyme giúp tăng tốc độ các phản ứng sinh hóa trong cơ thể mà không bị tiêu hao trong quá trình phản ứng. Chúng hoạt động bằng cách hạ thấp năng lượng hoạt hóa cần thiết để phản ứng xảy ra. Chúng là các xúc tác sinh học.
⇒ Hầu hết enzyme là protein đóng vai trò xúc tác sinh học cho các phản ứng sinh hoá trong cơ thể.
⇒ Chọn đáp án B Đáp án: B
Câu 9 [186543]: Để tách riêng NH3 ra khỏi hỗn hợp gồm N2, H2, NH3 trong công nghiệp, người ta đã
A, cho hỗn hợp qua nước vôi trong dư.
B, cho hỗn hợp qua bột CuO nung nóng.
C, nén và làm lạnh hỗn hợp để hóa lỏng NH3.
D, cho hỗn hợp qua dung dịch H2SO4 đặc.
Trong công nghiệp, hỗn hợp được làm lạnh để tách NH3 ra dưới dạng lỏng, còn N2 và H2 được tái sử dụng. Đáp án: C
Câu 10 [792330]: Calcium carbonate được dùng sản xuất vôi, thủy tinh, xi măng. Công thức của Calcium carbonate là
A, CaCO3.
B, Ca(OH)2.
C, CaO.
D, CaCl2.
HD: Calcium: Ca và carbonate: CO3 ⇒ ghép tên: Calcium carbonate là CaCO3
⇝ Chọn đáp án A. Đáp án: A
⇝ Chọn đáp án A. Đáp án: A
Câu 11 [706034]: Trong phòng thí nghiệm, một lượng nhỏ hydrogen chloride có thể được điều chế bằng phản ứng trực tiếp giữa dung dịch sodium chloride và dung dịch sulfuric acid đặc như hình dưới đây:
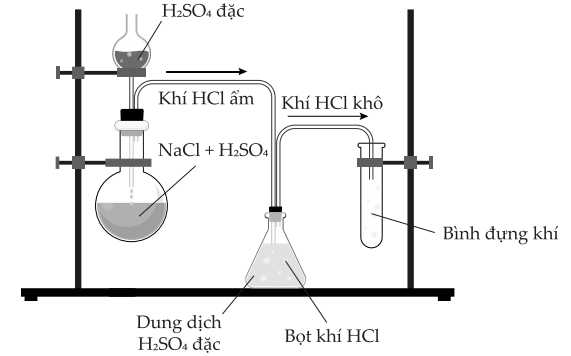
Tuy nhiên, phương pháp này không thể dùng để điều chế hydrogen bromide, do không thu được HBr từ phản ứng giữa NaBr và H2SO4 đặc:
2NaBr(s) + 3H2SO4(l) → 2NaHSO4(s) + Br2(g) + SO2(g) + 2H2O(g).
Cho các phát biểu sau:
(a) Anion Cl– không thể hiện tính khử khi tác dụng với sulfuric acid đặc nóng.
(b) Tương tự HBr, HI cũng không thể điều chế bằng phương pháp này.
(c) Trong thực tế, người ta điều chế HF cũng bằng thí nghiệm theo thiết kế ở hình trên.
(d) Tính khử của anion Br– yếu hơn anion Cl–.
Trong các phát biểu trên, những phát biểu đúng là

Tuy nhiên, phương pháp này không thể dùng để điều chế hydrogen bromide, do không thu được HBr từ phản ứng giữa NaBr và H2SO4 đặc:
2NaBr(s) + 3H2SO4(l) → 2NaHSO4(s) + Br2(g) + SO2(g) + 2H2O(g).
Cho các phát biểu sau:
(a) Anion Cl– không thể hiện tính khử khi tác dụng với sulfuric acid đặc nóng.
(b) Tương tự HBr, HI cũng không thể điều chế bằng phương pháp này.
(c) Trong thực tế, người ta điều chế HF cũng bằng thí nghiệm theo thiết kế ở hình trên.
(d) Tính khử của anion Br– yếu hơn anion Cl–.
Trong các phát biểu trên, những phát biểu đúng là
A, (a), (b).
B, (b), (c).
C, (a), (c).
D, (c), (d).
Phân tích các đáp án :
✔️(a) – Đúng. Anion Cl- không thể hiện tính khử khi tác dụng với sulfuric acid đặc nóng.
✔️(b) – Đúng. Tương tự HBr, HI cũng không thể điều chế bằng phương pháp này, ion I- có tính khử mạnh hơn Br- nên sử dụng H2SO4 đặc sẽ không thu được HI tương ứng.
8NaI + 5H2SO4 → H2S + 4I2 + 4Na2SO4 + 4H2O
❌(c) – Sai. Để điều chế HF, người ta dùng phương pháp sulfate. Đó là cho H2SO4 đặc tác dụng với muối floride, chloride vì H2SO4 là chất oxi hoá không đủ mạnh để oxi hoá được HF. Hay nói cách khác là HF có tính khử yếu, chúng không khử được H2SO4 đặc. Nhưng để điều chế HF, cần sử dụng phương pháp úp bình do HF nhẹ hơn không khí.
❌(d) - Sai . Br- có tính khử mạnh hơn Cl- vì brom có kích thước nguyên tử lớn hơn clo, lực hút giữa hạt nhân và electron ngoài cùng yếu hơn, nên Br- dễ nhường electron hơn Cl-
⟹Chọn đáp án A Đáp án: A
✔️(a) – Đúng. Anion Cl- không thể hiện tính khử khi tác dụng với sulfuric acid đặc nóng.
✔️(b) – Đúng. Tương tự HBr, HI cũng không thể điều chế bằng phương pháp này, ion I- có tính khử mạnh hơn Br- nên sử dụng H2SO4 đặc sẽ không thu được HI tương ứng.
8NaI + 5H2SO4 → H2S + 4I2 + 4Na2SO4 + 4H2O
❌(c) – Sai. Để điều chế HF, người ta dùng phương pháp sulfate. Đó là cho H2SO4 đặc tác dụng với muối floride, chloride vì H2SO4 là chất oxi hoá không đủ mạnh để oxi hoá được HF. Hay nói cách khác là HF có tính khử yếu, chúng không khử được H2SO4 đặc. Nhưng để điều chế HF, cần sử dụng phương pháp úp bình do HF nhẹ hơn không khí.
❌(d) - Sai . Br- có tính khử mạnh hơn Cl- vì brom có kích thước nguyên tử lớn hơn clo, lực hút giữa hạt nhân và electron ngoài cùng yếu hơn, nên Br- dễ nhường electron hơn Cl-
⟹Chọn đáp án A Đáp án: A
Câu 12 [1010035]: Cho các polymer sau:
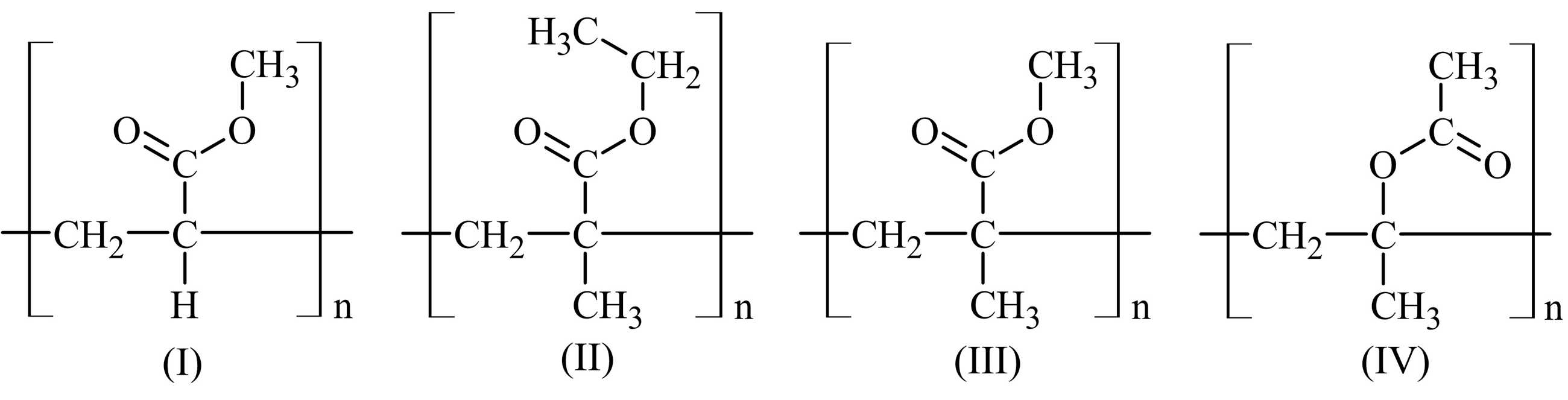
Polymer được điều chế bằng phản ứng trùng hợp methyl acrylate là

Polymer được điều chế bằng phản ứng trùng hợp methyl acrylate là
A, (I).
B, (II).
C, (III).
D, (IV).
Polymer được điều chế bằng phản ứng trùng hợp methyl acrylate là (I).
Chọn đáp án A Đáp án: A
Chọn đáp án A Đáp án: A
Câu 13 [308298]: Để chứng minh trong phân tử của glucose có nhiều nhóm hydroxy, người ta cho dung dịch glucose phản ứng với
A, Kim loại Na.
B, Cu(OH)2 ở nhiệt độ thường.
C, AgNO3 (hoặc Ag2O) trong dung dịch NH3, đun nóng.
D, Cu(OH)2 trong NaOH, đun nóng.
Phân tích các đáp án:
❌ A. với kim loại Na: chỉ cần 1 nhóm OH + Na → ONa + ½H2↑ nên không chứng minh nó có nhiều nhóm được.
✔️ B. Cu(OH)2 ở nhiệt độ thường tạo dung dịch màu xanh lam đặc trưng thì yêu cầu cần có ít nhất 2 nhóm OH liền kề.
❌ C. AgNO3/NH3: thuốc thử Tollens - chứng minh nhóm chức aldehyde CHO bằng kết tủa Ag trắng bạc.
❌ D. Cu(OH)2 đun nóng tạo kết tủa Cu2O màu đỏ gạch cũng chứng minh nhóm chức CHO.
⟹ Chọn đáp án B Đáp án: B
❌ A. với kim loại Na: chỉ cần 1 nhóm OH + Na → ONa + ½H2↑ nên không chứng minh nó có nhiều nhóm được.
✔️ B. Cu(OH)2 ở nhiệt độ thường tạo dung dịch màu xanh lam đặc trưng thì yêu cầu cần có ít nhất 2 nhóm OH liền kề.
❌ C. AgNO3/NH3: thuốc thử Tollens - chứng minh nhóm chức aldehyde CHO bằng kết tủa Ag trắng bạc.
❌ D. Cu(OH)2 đun nóng tạo kết tủa Cu2O màu đỏ gạch cũng chứng minh nhóm chức CHO.
⟹ Chọn đáp án B Đáp án: B
Câu 14 [706100]: Cho các thế điện cực chuẩn: 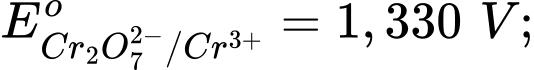
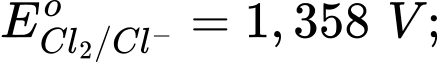
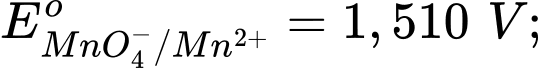
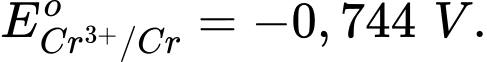 Chọn cách sắp xếp các ion và kim loại theo thứ tự tăng dần tính khử.
Chọn cách sắp xếp các ion và kim loại theo thứ tự tăng dần tính khử.
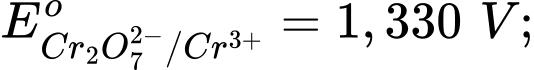
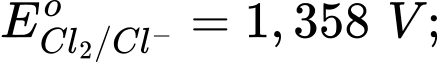
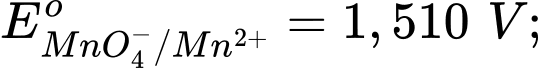
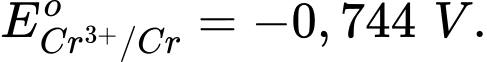 Chọn cách sắp xếp các ion và kim loại theo thứ tự tăng dần tính khử.
Chọn cách sắp xếp các ion và kim loại theo thứ tự tăng dần tính khử. A, Cr3+, Cl–, Mn2+, Cr.
B, Mn2+, Cl–, Cr3+, Cr.
C, Cr3+, Cl–, Cr2O72–, MnO4–.
D, Mn2+, Cr3+, Cl–, Cr.
Thế điện cực chuẩn của cặp oxi hóa – khử càng lớn thì tính khử của dạng khử càng yếu, tính oxi hóa của dạng oxi hóa càng mạnh và ngược lại.
Thứ tự tăng dần thế điện cực chuẩn là :
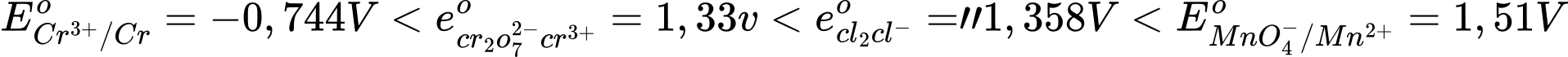 ""
"" Thứ tự tăng dần tính khử là: Mn2+ < Cl- < Cr3+ < Cr.
⟹Chọn đáp án B Đáp án: B
Thứ tự tăng dần thế điện cực chuẩn là :
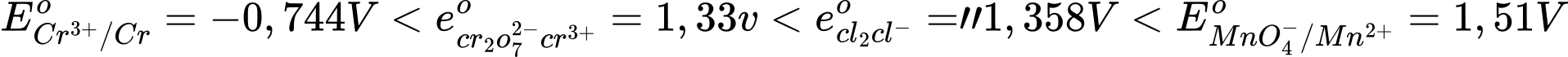 ""
"" ⟹Chọn đáp án B Đáp án: B
Câu 15 [1016539]: Một học sinh tiến hành thí nghiệm: Nhúng một thanh đồng vào dung dịch AgNO3, sau một lúc nhúng tiếp một thanh sắt vào dung dịch này đến phản ứng hoàn toàn. Sau khi thí nghiệm kết thúc, học sinh đó rút ra các kết luận sau:
(a) Dung dịch thu được sau phản ứng có màu xanh nhạt.
(b) Khối lượng thanh đồng bị giảm sau phản ứng.
(c) Khối lượng thanh sắt tăng lên sau phản ứng.
Số nhận định không đúng là
(a) Dung dịch thu được sau phản ứng có màu xanh nhạt.
(b) Khối lượng thanh đồng bị giảm sau phản ứng.
(c) Khối lượng thanh sắt tăng lên sau phản ứng.
Số nhận định không đúng là
A, 0.
B, 1.
C, 2.
D, 3.
Nhúng một thanh đồng vào dung dịch AgNO3
Cu + 2AgNO3 → Cu(NO3)2 + 2Ag
sau một lúc nhúng tiếp một thanh sắt vào dung dịch này đến phản ứng hoàn toàn.
Fe + 2AgNO3 → Fe(NO3)2 + 2Ag
Fe + Cu(NO3)2 → Fe(NO3)2 + Cu
Phân tích các nhận định:
✔️(a) – Đúng. Dung dịch thu được sau phản ứng có màu xanh nhạt, trong dung dịch có muối Fe(NO3)2 nên có màu xanh nhạt.
❌(b) – Sai. Sau phản ứng có Ag (M = 108 amu) bám vào thanh đồng Cu (M = 64 amu) nên khối lượng của thanh đồng tăng lên.
✔️(c) – Đúng. Khối lượng thanh sắt tăng lên sau phản ứng nguyên do Cu và Ag bám lên lên thanh Fe.
Số nhận định không đúng là: 1
⟹ Chọn đáp án B Đáp án: B
Cu + 2AgNO3 → Cu(NO3)2 + 2Ag
sau một lúc nhúng tiếp một thanh sắt vào dung dịch này đến phản ứng hoàn toàn.
Fe + 2AgNO3 → Fe(NO3)2 + 2Ag
Fe + Cu(NO3)2 → Fe(NO3)2 + Cu
Phân tích các nhận định:
✔️(a) – Đúng. Dung dịch thu được sau phản ứng có màu xanh nhạt, trong dung dịch có muối Fe(NO3)2 nên có màu xanh nhạt.
❌(b) – Sai. Sau phản ứng có Ag (M = 108 amu) bám vào thanh đồng Cu (M = 64 amu) nên khối lượng của thanh đồng tăng lên.
✔️(c) – Đúng. Khối lượng thanh sắt tăng lên sau phản ứng nguyên do Cu và Ag bám lên lên thanh Fe.
Số nhận định không đúng là: 1
⟹ Chọn đáp án B Đáp án: B
Câu 16 [705812]: Cho hai phức chất A và B có công thức lần lượt sau:
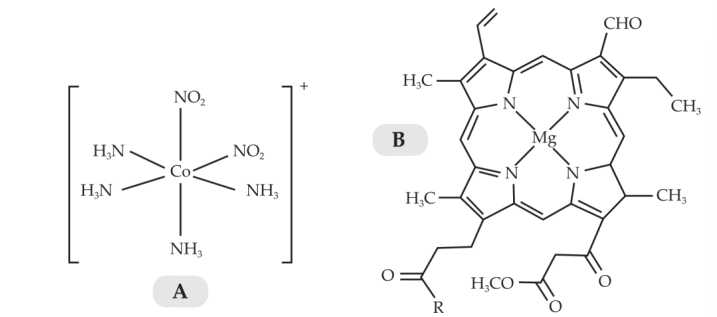
Phát biểu nào sau đây đúng?

Phát biểu nào sau đây đúng?
A, Trong phức chất B có 4 phối tử.
B, Hai phức chất A và B có dạng hình học khác nhau.
C, Trong A và trong B đều có hai loại phối tử.
D, Nguyên tử trung tâm của hai phức chất đều là nguyên tố kim loại chuyển tiếp.
Phân tích các phát biểu:
❌A. Trong phức chất B có 1 phối tử.
✔️B. A có dạng bát diện, B là phức có phối tử đa càng ⟹ Hai phức chất A và B có dạng hình học khác nhau.
❌C. Trong A có 2 loại phối tử là NO2 và NH3, trong B đều có 1 phối tử đa càng.
❌D. Co là kim loại chuyển tiếp, Mg không phải kim loại chuyển tiếp.
⟹ Chọn đáp án B
Đáp án: B
❌A. Trong phức chất B có 1 phối tử.
✔️B. A có dạng bát diện, B là phức có phối tử đa càng ⟹ Hai phức chất A và B có dạng hình học khác nhau.
❌C. Trong A có 2 loại phối tử là NO2 và NH3, trong B đều có 1 phối tử đa càng.
❌D. Co là kim loại chuyển tiếp, Mg không phải kim loại chuyển tiếp.
⟹ Chọn đáp án B
Đáp án: B
PHẦN II. Thí sinh trả lời từ câu 1 đến câu 4. Trong mỗi ý a), b), c), d) ở mỗi câu, thí sinh chọn đúng hoặc sai.
Câu 17 [704206]: Trong các phát biểu sau dưới đây, phát biểu nào đúng?
A, Môi trường dung dịch acetic acid có độ pH lớn hơn 7.
B, Dung dịch tại thời điểm cân bằng chỉ chứa ion CH3COO– và ion H+.
C, Tại thời điểm cân bằng, nồng độ [CH3COOH] bằng nồng độ [H+].
D, Hằng số phân li Ka càng lớn thì acid đó càng mạnh.

Phân tích các phát biểu:
❌ A. Sai. Quá trình phân li acetic acid sinh ra H+ tạo môi trường acid nên pH của dung dịch acetic acid nhỏ hơn 7
❌ B. Sai. Acetic acid là acid yếu, quá trình phân li không hòa toàn nên tại thời điểm cân bằng dung dịch không chỉ chứa ion CH3COO- và H+ mà còn chứa một phần CH3COOH chưa bị phân li.
❌ C. Sai. Tại thời điểm cân bằng nồng độ của [CH3COOH] không bằng nồng độ của [H+] mà nồng độ của [CH3COO-] bằng với nồng độ [H+]
✔️ D. Đúng. Hằng số Ka càng lớn thì hiệu suất phân li ra H+ càng lớn dẫn đến pH giảm độ acid tăng.
⇒ Chọn đáp án D Đáp án: D
Câu 18 [704207]: Nồng độ ban đầu của CH3COOH là 0,1 M, nếu tăng nồng độ ban đầu lên 2 lần thì nồng độ H+ tại thời điểm cân bằng tăng bao nhiêu lần?
A, 1,42 lần.
B, 1,67 lần.
C, 1,56 lần.
D, 2 lần.
Tại nồng độ của dung dịch CH3COOH 0,1M
Gọi x là nồng độ H+ phân li của CH3COOH 0,1M
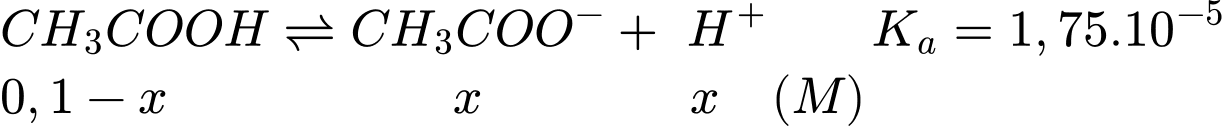
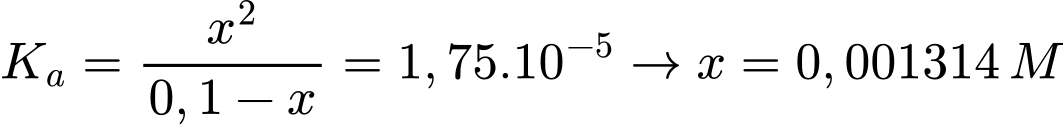
Tại nồng độ của dung dịch CH3COOH 0,2M
Gọi y là nồng độ H+ phân li của CH3COOH 0,2M
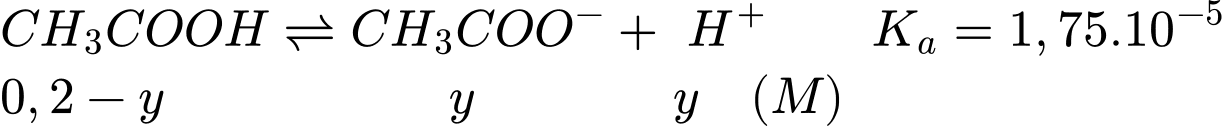
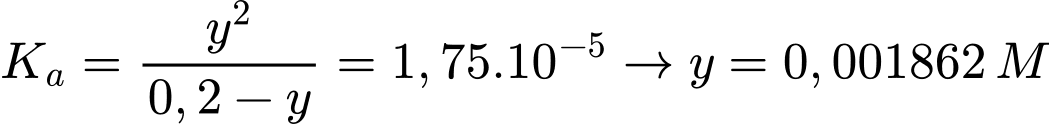
Khi tăng nồng độ lên acetic acid lên gấp đôi thì thì nồng độ H+ tăng số lần là:
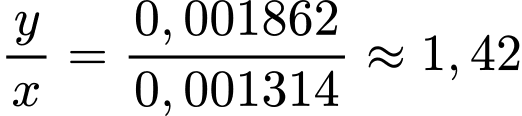 (lần)
(lần)
⇒ Chọn đáp án A Đáp án: A
Gọi x là nồng độ H+ phân li của CH3COOH 0,1M
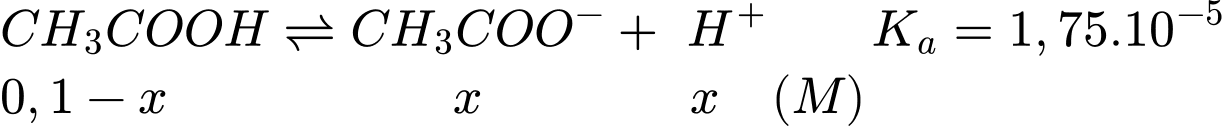
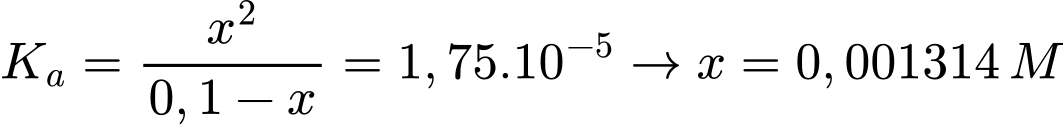
Tại nồng độ của dung dịch CH3COOH 0,2M
Gọi y là nồng độ H+ phân li của CH3COOH 0,2M
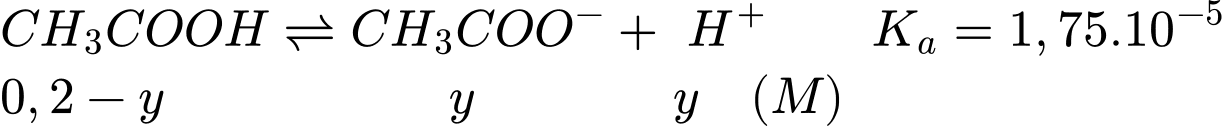
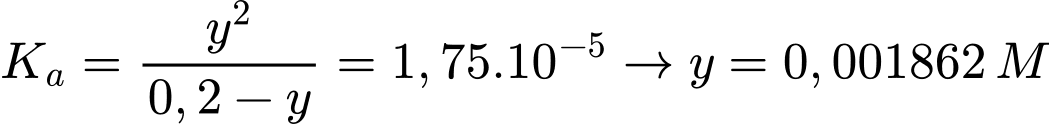
Khi tăng nồng độ lên acetic acid lên gấp đôi thì thì nồng độ H+ tăng số lần là:
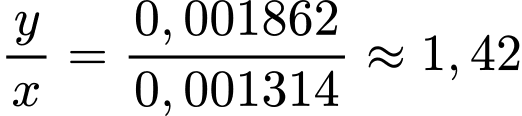 (lần)
(lần)⇒ Chọn đáp án A Đáp án: A
PHẦN III. Thí sinh trả lời từ câu 1 đến 6. Thí sinh điền kết quả mỗi câu vào mỗi ô trả lời tương ứng theo hướng dẫn của phiếu trả lời.
Câu 19 [705469]: Thí nghiệm được mô tả như hình vẽ:
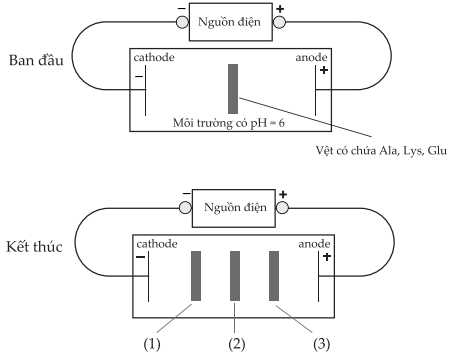

Tại pH = 6:
− Alanine (Ala): tồn tại chủ yếu ở dạng lưỡng cực ion và gần như không di chuyển.
− Lysine (Lys): tồn tại dưới dạng cation (NH3+), nên bị hút về cực âm (cathode).
− Glutamic acid (Glu): tồn tại dưới dạng anion (COO−), nên bị hút về cực dương (anode).
Phân tích các phát biểu:
✔️ (a) Đúng. Thí nghiệm này khảo sát tính chất lưỡng tính của amino acid và sự di chuyển của chúng trong điện trường dựa vào .
✔️ (b) Đúng. Tại pH = 6 alanine tồn tại dạng ion lưỡng cực, tổng điện tích bằng không nên hầu như không di chuyển trong điện trường ứng với vị trí số (2).
✔️ (c) Đúng. Tại pH = 6, Lysine có tổng điện tích bằng 1+ nên di chuyển sang cực âm trong điện trường ứng với vị trí số (1).
❌ (d) Sai. Tại pH = 6 glutamic acid tồn tại dạng anion, tổng điện tích bằng 1− nên di chuyển về cực dương trong điện trường ứng với vị trí số (3).
− Alanine (Ala): tồn tại chủ yếu ở dạng lưỡng cực ion và gần như không di chuyển.
− Lysine (Lys): tồn tại dưới dạng cation (NH3+), nên bị hút về cực âm (cathode).
− Glutamic acid (Glu): tồn tại dưới dạng anion (COO−), nên bị hút về cực dương (anode).
Phân tích các phát biểu:
✔️ (a) Đúng. Thí nghiệm này khảo sát tính chất lưỡng tính của amino acid và sự di chuyển của chúng trong điện trường dựa vào .
✔️ (b) Đúng. Tại pH = 6 alanine tồn tại dạng ion lưỡng cực, tổng điện tích bằng không nên hầu như không di chuyển trong điện trường ứng với vị trí số (2).
✔️ (c) Đúng. Tại pH = 6, Lysine có tổng điện tích bằng 1+ nên di chuyển sang cực âm trong điện trường ứng với vị trí số (1).
❌ (d) Sai. Tại pH = 6 glutamic acid tồn tại dạng anion, tổng điện tích bằng 1− nên di chuyển về cực dương trong điện trường ứng với vị trí số (3).
Câu 20 [705772]: Nước cứng được phân làm ba loại: nước có tính cứng tạm thời, nước có tính cứng vĩnh cửu và nước có tính cứng toàn phần.
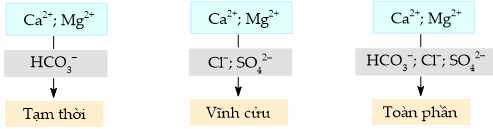

Phân tích các phát biểu:
✔️ (a) Đúng. Căn cứ để phân loại nước cứng là dựa vào thành phần của anion gốc acid tạo muối với ion Ca2+ và Mg2+:
- Nước cứng tạm thời là nguồn nước cứng mà trong thành phần của nó có chứa nhiều các ion Ca2+, Mg2+ và gốc bicarbonate (HCO3-). Do đó thành phần chính của nước cứng tạm thời sẽ là 2 muối Ca(HCO3)2 và Mg(HCO3)2.
- Nước cứng vĩnh cửu là nước cứng chứa nồng độ cao của các anion, như anion sunfate (SO42-), chloride (Cl-) với thành phần là các muối như MgCl2, CaCl2, MgSO4, CaSO4.
- Nước cứng thành phần hiểu đơn giản là loại nước cứng bao gồm cả tính cứng tạm thời và tính cứng vĩnh cửu. Do đó thành phần của nó sẽ là các muối Ca(HCO3)2, Mg(HCO3)2, MgCl2, CaCl2, MgSO4, CaSO4.
❌ (b) Sai. Các loại nước cứng đều gây hại như nhau đối với đời sống và sức khỏe con người. Nước cứng sẽ làm mất vị ngon ngọt tự nhiên của thực phẩm khi chế biến, làm giảm thời gian đun nấu chin và giảm chất dinh dưỡng. Đặc biệt, nước uống sẽ có vị tanh nồng, vì thế sẽ làm thay đổi rõ rệt màu sắc, mùi vị của sữa, cà phê, trà… làm các loại này có màu đậm hơn, ít ngọt và ít thơm, tạo ra vị chát. Không chỉ thế, ấm đun nước, cốc chén sẽ có cặn bám thành mảng rất khó vệ sinh.
❌ (c) Sai. Một dung dịch có chứa hàm lượng lớn các muối CaCl2, Ca(HCO3)2, MgSO4. Dung dịch này là nước có tính cứng toàn phần.
❌ (d) Sai. Một dung dịch nước cứng tạm thời có tổng số mol Ca2+, Mg2+ là 0,2 mol, theo định luật bảo toàn điện tích số mol của anion trong dung dịch là 0,2 × 2 = 0,4 mol.
✔️ (a) Đúng. Căn cứ để phân loại nước cứng là dựa vào thành phần của anion gốc acid tạo muối với ion Ca2+ và Mg2+:
- Nước cứng tạm thời là nguồn nước cứng mà trong thành phần của nó có chứa nhiều các ion Ca2+, Mg2+ và gốc bicarbonate (HCO3-). Do đó thành phần chính của nước cứng tạm thời sẽ là 2 muối Ca(HCO3)2 và Mg(HCO3)2.
- Nước cứng vĩnh cửu là nước cứng chứa nồng độ cao của các anion, như anion sunfate (SO42-), chloride (Cl-) với thành phần là các muối như MgCl2, CaCl2, MgSO4, CaSO4.
- Nước cứng thành phần hiểu đơn giản là loại nước cứng bao gồm cả tính cứng tạm thời và tính cứng vĩnh cửu. Do đó thành phần của nó sẽ là các muối Ca(HCO3)2, Mg(HCO3)2, MgCl2, CaCl2, MgSO4, CaSO4.
❌ (b) Sai. Các loại nước cứng đều gây hại như nhau đối với đời sống và sức khỏe con người. Nước cứng sẽ làm mất vị ngon ngọt tự nhiên của thực phẩm khi chế biến, làm giảm thời gian đun nấu chin và giảm chất dinh dưỡng. Đặc biệt, nước uống sẽ có vị tanh nồng, vì thế sẽ làm thay đổi rõ rệt màu sắc, mùi vị của sữa, cà phê, trà… làm các loại này có màu đậm hơn, ít ngọt và ít thơm, tạo ra vị chát. Không chỉ thế, ấm đun nước, cốc chén sẽ có cặn bám thành mảng rất khó vệ sinh.
❌ (c) Sai. Một dung dịch có chứa hàm lượng lớn các muối CaCl2, Ca(HCO3)2, MgSO4. Dung dịch này là nước có tính cứng toàn phần.
❌ (d) Sai. Một dung dịch nước cứng tạm thời có tổng số mol Ca2+, Mg2+ là 0,2 mol, theo định luật bảo toàn điện tích số mol của anion trong dung dịch là 0,2 × 2 = 0,4 mol.
Câu 21 [705816]: Phương pháp kết tinh được sử dụng trong phòng thí nghiệm hóa học như một kỹ thuật tinh chế chất rắn. Một chất rắn không tinh khiết được hòa tan hoàn toàn trong một lượng nhỏ dung môi sôi nóng và dung dịch nóng được để nguội từ từ.
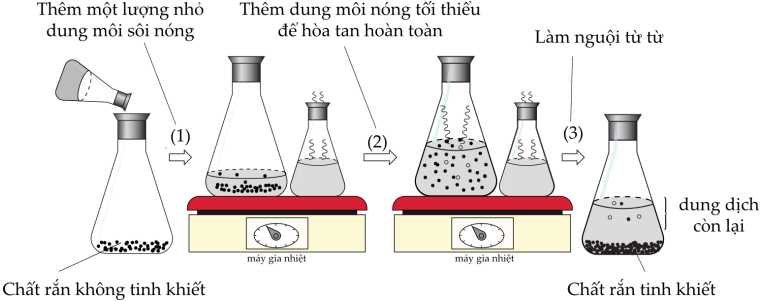

Phân tích các phát biểu:
✔️A. Đúng. Khi dung dịch nguội dần, các tinh thể của chất rắn kết tinh lại với độ tinh khiết cao vì tạp chất vẫn hòa tan trong dung dịch và không kết tinh theo.
✔️B. Đúng. Các tạp chất không kết tinh mà nằm lại trong dung dịch,do đó chúng không bị lẫn vào tinh thể sản phẩm.
❌C. Sai.Chất kết tinh có độ tan cao hơn khi tăng nhiệt độ.
✔️D. Đúng. Dung dịch sau kết tinh (phần dung dịch còn lại sau khi chất kết tinh đã tách ra) là dung dịch bão hòa của chất cần kết tinh tại nhiệt độ đó.
✔️A. Đúng. Khi dung dịch nguội dần, các tinh thể của chất rắn kết tinh lại với độ tinh khiết cao vì tạp chất vẫn hòa tan trong dung dịch và không kết tinh theo.
✔️B. Đúng. Các tạp chất không kết tinh mà nằm lại trong dung dịch,do đó chúng không bị lẫn vào tinh thể sản phẩm.
❌C. Sai.Chất kết tinh có độ tan cao hơn khi tăng nhiệt độ.
✔️D. Đúng. Dung dịch sau kết tinh (phần dung dịch còn lại sau khi chất kết tinh đã tách ra) là dung dịch bão hòa của chất cần kết tinh tại nhiệt độ đó.
Câu 22 [705773]: Tiến hành các thí nghiệm:
▪ Bước 1: Cho từ từ từng giọt dung dịch NH3 vào ống nghiệm chứa 5 mL dung dịch CuSO4 thì có kết tủa xuất hiện. Lắc ống nghiệm trong quá trình thêm dung dịch NH3.
▪ Bước 2: Tiếp tục cho NH3 đến khi kết tủa tan hết, dung dịch trong ống nghiệm chuyển sang màu xanh lam thì dừng.
▪ Bước 1: Cho từ từ từng giọt dung dịch NH3 vào ống nghiệm chứa 5 mL dung dịch CuSO4 thì có kết tủa xuất hiện. Lắc ống nghiệm trong quá trình thêm dung dịch NH3.
▪ Bước 2: Tiếp tục cho NH3 đến khi kết tủa tan hết, dung dịch trong ống nghiệm chuyển sang màu xanh lam thì dừng.
Thí nghiệm diễn ra như sau:
Bước 1: Thêm NH3 vào CuSO4 → Kết tủa xuất hiện
Phản ứng xảy ra:
CuSO4 + 2NH3 + 2H2O → Cu(OH)2↓ + (NH4)2SO4
Kết tủa Cu(OH)2 có màu xanh lam nhạt.
Bước 2: Thêm dư NH3 → Kết tủa tan, dung dịch xanh đậm. Lúc này Cu(OH)2 tan tạo phức:
Cu(OH)2 + 4NH3 → [Cu(NH3)4](OH)2
Dung dịch chuyển thành màu xanh đậm do ion phức [Cu(NH3)4](OH)2.
Phân tích các phát biểu:
❌ (a) Sai. Kết tủa Cu(OH)2 xuất hiện ở bước 1 có màu xanh.
✔️ (b) Đúng. Ở bước 2 có hình thành phức chất [Cu(NH3)4](OH)2.
✔️ (c) Đúng. NH3 khi tan trong nước có sự phân li ra ion OH- tạo môi trường base nên giá trị pH của dung dịch tăng dần.
Bước 1: Thêm NH3 vào CuSO4 → Kết tủa xuất hiện
Phản ứng xảy ra:
CuSO4 + 2NH3 + 2H2O → Cu(OH)2↓ + (NH4)2SO4
Kết tủa Cu(OH)2 có màu xanh lam nhạt.
Bước 2: Thêm dư NH3 → Kết tủa tan, dung dịch xanh đậm. Lúc này Cu(OH)2 tan tạo phức:
Cu(OH)2 + 4NH3 → [Cu(NH3)4](OH)2
Dung dịch chuyển thành màu xanh đậm do ion phức [Cu(NH3)4](OH)2.
Phân tích các phát biểu:
❌ (a) Sai. Kết tủa Cu(OH)2 xuất hiện ở bước 1 có màu xanh.
✔️ (b) Đúng. Ở bước 2 có hình thành phức chất [Cu(NH3)4](OH)2.
✔️ (c) Đúng. NH3 khi tan trong nước có sự phân li ra ion OH- tạo môi trường base nên giá trị pH của dung dịch tăng dần.
NH3 + H2O ⇌ NH4+ + OH-
✔️ (d) Đúng. Ngoài NH3, các amine CH3NH2, C2H5NH2 cũng có tính chất tương tự (còn cặp electron chưa liên kết) nên có thể tạo phức với ion Cu2+. PHẦN III. Thí sinh trả lời từ câu 1 đến 6. Thí sinh điền kết quả mỗi câu vào mỗi ô trả lời tương ứng theo hướng dẫn của phiếu trả lời.
Câu 23 [704038]: Ứng với công thức phân tử C4H9NO2 có bao nhiêu amino acid là đồng phân cấu tạo của nhau?
Công thức phân tử C4H9NO2 có 5 amino acid là đồng phân cấu tạo của nhau như sau:
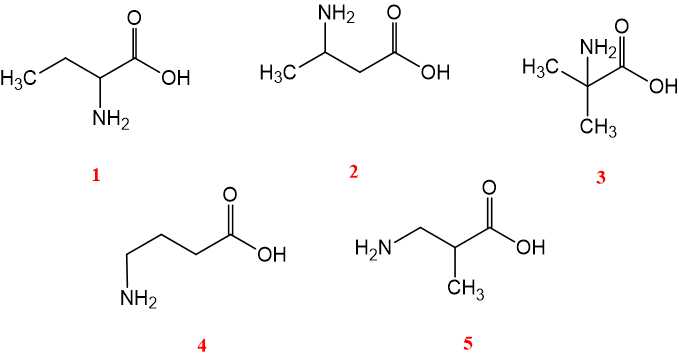
⇒ Điền đáp án: 5

⇒ Điền đáp án: 5
Câu 24 [704309]: Từ 1 tấn tinh bột ngô có thể sản xuất được V m3 xăng E5 (chứa 5% ethanol về thể tích), biết tinh bột ngô chứa 55% tinh bột, hiệu suất chung của cả quá trình điều chế ethanol là 80%, khối lượng riêng của ethanol là 0,8 g/mL. Xác định giá trị của V (làm tròn một chữ số thập phân).
Đổi 0,8 g/mL = 0,8 tấn/m3
Khối lượng tinh bột trong 1 tấn bột ngô là 0,55 tấn
Sơ đồ phản ứng:
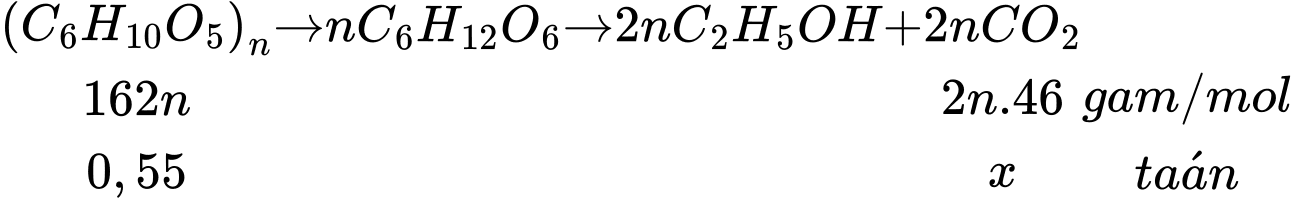
Khối lượng ethanol tạo thành là: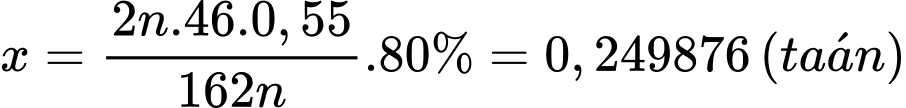
Thể tích xăng E5 là: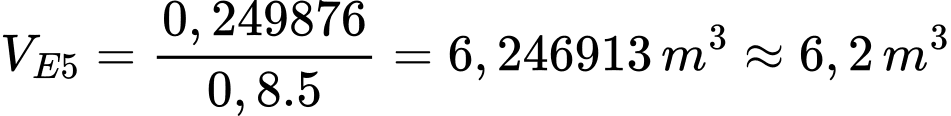
⇒ Điền đáp án: 6,2
Khối lượng tinh bột trong 1 tấn bột ngô là 0,55 tấn
Sơ đồ phản ứng:
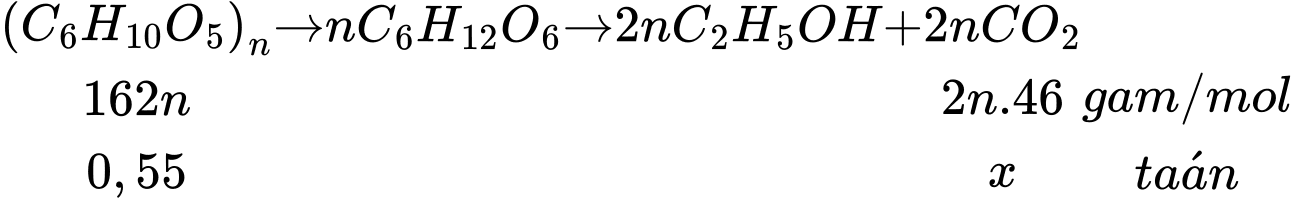
Khối lượng ethanol tạo thành là:
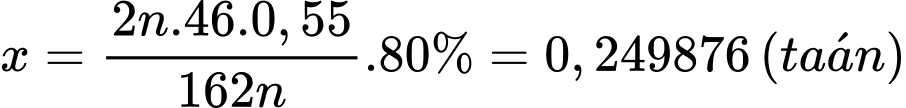
Thể tích xăng E5 là:
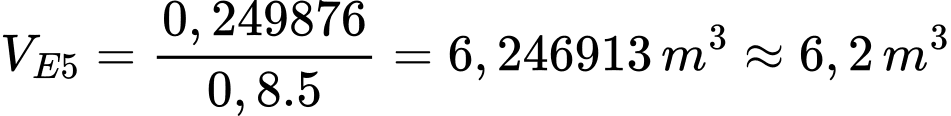
⇒ Điền đáp án: 6,2
Câu 25 [703958]: Phân tích nguyên tố hợp chất hữu cơ X cho thấy phần trăm khối lượng ba nguyên tố C, H và O lần lượt là 64,86%; 13,51% và 21,63%. Phổ MS của X được cho như hình bên. Biết phổ hồng ngoại của X có tín hiệu hấp thụ trong vùng 3650 – 3200 cm–1. Có thể có bao nhiêu công thức cấu tạo thỏa mãn X?
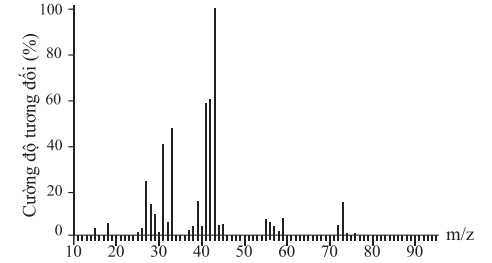

Từ phổ khối lượng, phân tử khối của chất hữu cơ X là 74 gam/mol.
Gọi công thức của X có dạng CxHyOz
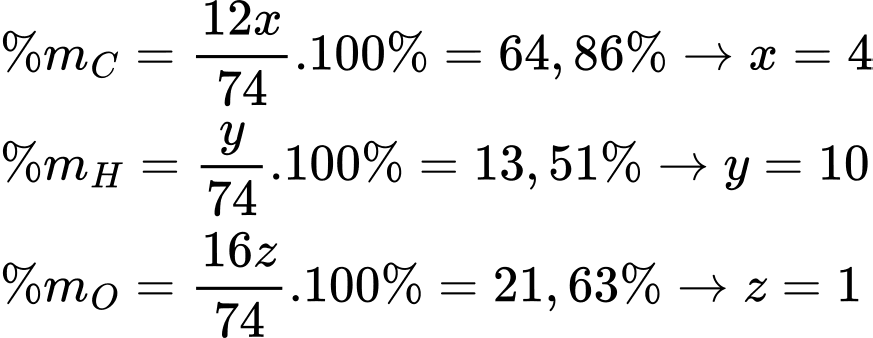
→ Công thức của X là C4H10O.
X có tín hiệu hấp thụ trong vùng 3650 – 3200 cm-1 của nhóm O-H, nên X là alcohol.
Các đồng phân có thể có của X là
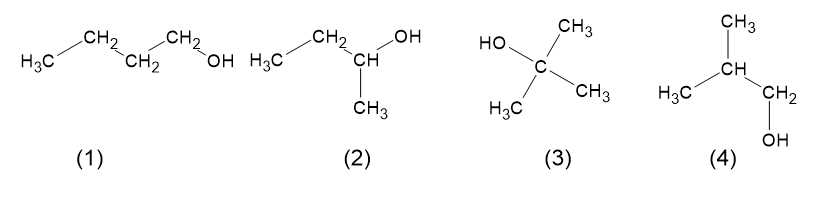
Vậy X có thể có 4 đồng phân
⇒ Điền đáp án: 4
Gọi công thức của X có dạng CxHyOz
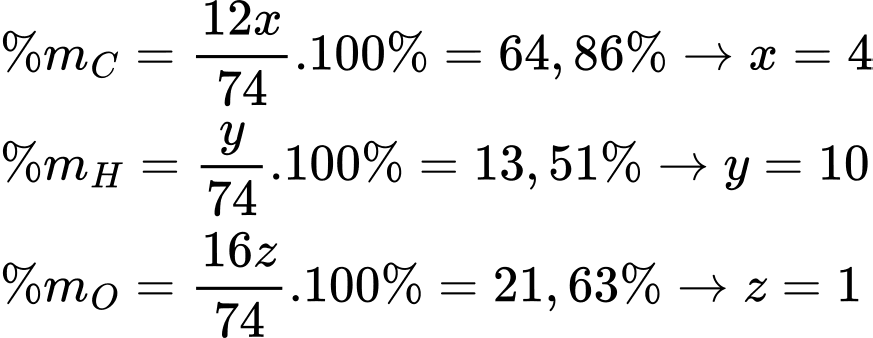
→ Công thức của X là C4H10O.
X có tín hiệu hấp thụ trong vùng 3650 – 3200 cm-1 của nhóm O-H, nên X là alcohol.
Các đồng phân có thể có của X là

Vậy X có thể có 4 đồng phân
⇒ Điền đáp án: 4
Câu 26 [705976]: Cho dãy gồm các chất: Na, Ca, Mg, Al, Fe, K, Cu. Số kim loại trong dãy tác dụng mạnh với nước ở điều kiện thường là
Số kim loại tác dụng với nước ở điều kiện thường là : Na, Ca, K
2Na + 2H2O → 2NaOH + H2
Ca + 2H2O → Ca(OH)2 + H2
2K + 2H2O → 2KOH + H2
⟹Điền đáp án : 3
2Na + 2H2O → 2NaOH + H2
Ca + 2H2O → Ca(OH)2 + H2
2K + 2H2O → 2KOH + H2
⟹Điền đáp án : 3
Câu 27 [705975]: Khi nung nóng, CaC2O4.H2O sẽ bắt đầu mất dần khối lượng. Đồ thị hình dưới đây biểu diễn sự phụ thuộc của khối lượng chất rắn vào nhiệt độ:
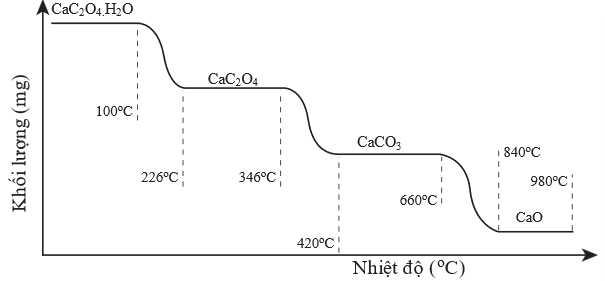
Phần trăm khối lượng chất rắn còn lại so với ban đầu tại nhiệt độ 840 oC là bao nhiêu (Làm tròn đến hàng phần mười)?

Phần trăm khối lượng chất rắn còn lại so với ban đầu tại nhiệt độ 840 oC là bao nhiêu (Làm tròn đến hàng phần mười)?
Tại 840 oC chất rắn còn lại so với dạng ban đầu là CaO
Phần trăm khối lượng chất rắn còn lại là
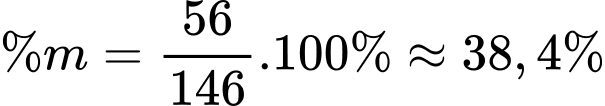
⟹Điền đáp án : 38,4
Phần trăm khối lượng chất rắn còn lại là
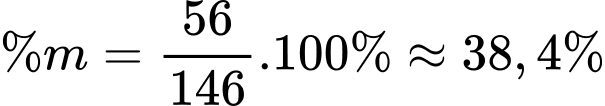
⟹Điền đáp án : 38,4
Câu 28 [706004]: Muối ngậm nước FeSO4.xH2O được sử dụng trong y tế để điều trị chứng thiếu sắt và cũng sử dụng cho các ứng dụng công nghiệp. Trong quá trình bảo quản, một mẫu muối FeSO4.xH2O (có khối lượng m gam) bị oxi hóa bởi oxygen không khí tạo thành hỗn hợp X chứa các hợp chất của Fe(II) và Fe(III). Hòa tan toàn bộ X trong dung dịch loãng chứa 0,05 mol H2SO4, thu được 100 ml dung dịch Y. Tiến hành hai thí nghiệm với Y:Thí nghiệm 1: Cho lượng dư dung dịch BaCl2 vào 25 ml dung dịch Y, thu được 4,66 gam kết tủa.
Thí nghiệm 2: Thêm dung dịch H2SO4 (loãng, dư) vào 25 ml dung dịch Y, thu được dung dịch Z. Nhỏ từ từ dung dịch KMnO4 0,1M vào Z đến khi phản ứng vừa đủ thì hết 13,5 ml.
Xác định giá trị củaphần trăm Fe bị oxi hóa?
Thí nghiệm 2: Thêm dung dịch H2SO4 (loãng, dư) vào 25 ml dung dịch Y, thu được dung dịch Z. Nhỏ từ từ dung dịch KMnO4 0,1M vào Z đến khi phản ứng vừa đủ thì hết 13,5 ml.
Xác định giá trị củaphần trăm Fe bị oxi hóa?
TN1 : FeSO4.xH2O ⟶ X ⟶ dd Y ⟶ BaSO4
nH2SO4 = 0,0125 mol
nBaSO4 = 0,02 mol = nFeSO4.xH2O + nH2SO4
nFeSO4.xH2O = 0,0075 mol
TN2 : 10 FeSO4 + 2 KMnO4 + 8 H2SO4 ⟶ 5 Fe2(SO4)3 + 2 MnSO4 + K2SO4 + 8H2O
nKMnO4 phản ứng = 13,5 : 1000 × 0,1 = 1,35× 10-3mol
nFeSO4 = 6,75× 10-3 mol
Số mol Fe3+ bị oxi hóa = 0,0075 - 6,75× 10-3 = 7,5 × 10 -4mol
%Fe đã bị oxi hóa = 7,5× 10-4 : 0,0075 × 100 = 10%
⟹ Điền đáp án : 10
nH2SO4 = 0,0125 mol
nBaSO4 = 0,02 mol = nFeSO4.xH2O + nH2SO4
nFeSO4.xH2O = 0,0075 mol
TN2 : 10 FeSO4 + 2 KMnO4 + 8 H2SO4 ⟶ 5 Fe2(SO4)3 + 2 MnSO4 + K2SO4 + 8H2O
nKMnO4 phản ứng = 13,5 : 1000 × 0,1 = 1,35× 10-3mol
nFeSO4 = 6,75× 10-3 mol
Số mol Fe3+ bị oxi hóa = 0,0075 - 6,75× 10-3 = 7,5 × 10 -4mol
%Fe đã bị oxi hóa = 7,5× 10-4 : 0,0075 × 100 = 10%
⟹ Điền đáp án : 10