PHẦN I. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
Câu 1 [703922]: Hợp chất có tên gọi nào sau đây là một polymer?
A, Buta-1,3-dien.
B, Cellulose.
C, Glycerol.
D, Hexamethylenediamine.
❌ A. Buta-1,3-dien là một monomer, không phải polymer. Buta-1,3-dien có thể tham gia phản ứng trùng hợp để tạo ra polymer như cao su buna.
✔️ B. Cellulose là một polymer tự nhiên, được cấu tạo từ các monomer glucose liên kết với nhau qua liên kết β-1,4-glycosidic:
❌ C. Glycerol là một hợp chất đơn giản, có công thức . Đây không phải là polymer mà là một hợp chất hữu cơ nhỏ được sử dụng trong nhiều phản ứng hóa học.
❌ D. Hexamethylenediamine là một hợp chất hữu cơ có hai nhóm amine (-NH2). Nó là monomer dùng để tổng hợp polymer như nylon-6,6 khi kết hợp với adipic acid.
⇒ Chọn đáp án B Đáp án: B
✔️ B. Cellulose là một polymer tự nhiên, được cấu tạo từ các monomer glucose liên kết với nhau qua liên kết β-1,4-glycosidic:
❌ C. Glycerol là một hợp chất đơn giản, có công thức . Đây không phải là polymer mà là một hợp chất hữu cơ nhỏ được sử dụng trong nhiều phản ứng hóa học.
❌ D. Hexamethylenediamine là một hợp chất hữu cơ có hai nhóm amine (-NH2). Nó là monomer dùng để tổng hợp polymer như nylon-6,6 khi kết hợp với adipic acid.
⇒ Chọn đáp án B Đáp án: B
Câu 2 [575535]: Nguyên tử F có 9 electron. Theo mô hình Rutherford – Bohr, tỉ lệ số lượng electron trên lớp thứ hai so với số lượng electron trên lớp thứ nhất là
A, 2 : 12.
B, 7 : 2.
C, 5 : 2.
D, 2 : 7.
HƯỚNG DẪN GIẢI:
- Ta điền các electron theo thứ tự từ lớp thấp nhất đến lớp cao nhất.
+) Lớp thứ nhất của F chứa tối đa 2 electron.
+) Lớp thứ hai của F chứa tối đa 8 electron (Lớp thứ hai bao gồm 2s và 2p, mỗi phân lớp này chứa được lần lượt 2e và 6e). Vậy còn lại 9 - 2 = 7 electron được điền vào lớp này.
- Vậy tỷ lệ số lượng electron trên lớp thứ hai so với số lượng electron trên lớp thứ nhất là 7/2
⟹ Chọn đáp án: B Đáp án: B
- Ta điền các electron theo thứ tự từ lớp thấp nhất đến lớp cao nhất.
+) Lớp thứ nhất của F chứa tối đa 2 electron.
+) Lớp thứ hai của F chứa tối đa 8 electron (Lớp thứ hai bao gồm 2s và 2p, mỗi phân lớp này chứa được lần lượt 2e và 6e). Vậy còn lại 9 - 2 = 7 electron được điền vào lớp này.
- Vậy tỷ lệ số lượng electron trên lớp thứ hai so với số lượng electron trên lớp thứ nhất là 7/2
⟹ Chọn đáp án: B Đáp án: B
Câu 3 [703824]: Để xác định phân tử khối của hợp chất hữu cơ, có thể sử dụng kết quả
A, đo thể tích.
B, phổ hồng ngoại (IR).
C, cân khối lượng.
D, phổ khối lượng (MS).
❌ A. Sai. Đo thể tích không thể trực tiếp xác định phân tử khối.
❌ B. Sai. Phổ IR dùng để xác định các nhóm chức trong phân tử, không trực tiếp xác định được phân tử khối.
❌ C. Sai. Cân khối lượng chỉ cung cấp khối lượng mẫu, không cho biết thông tin về phân tử khối.
✔️ D. Đúng. Phổ khối lượng là phương pháp chính xác và trực tiếp nhất để xác định phân tử khối. Máy đo khối phổ xác định tỷ lệ khối lượng trên điện tích (m/z) và cung cấp đỉnh phân tử M+, từ đó suy ra phân tử khối.
⇒ Chọn đáp án D Đáp án: D
❌ B. Sai. Phổ IR dùng để xác định các nhóm chức trong phân tử, không trực tiếp xác định được phân tử khối.
❌ C. Sai. Cân khối lượng chỉ cung cấp khối lượng mẫu, không cho biết thông tin về phân tử khối.
✔️ D. Đúng. Phổ khối lượng là phương pháp chính xác và trực tiếp nhất để xác định phân tử khối. Máy đo khối phổ xác định tỷ lệ khối lượng trên điện tích (m/z) và cung cấp đỉnh phân tử M+, từ đó suy ra phân tử khối.
⇒ Chọn đáp án D Đáp án: D
Câu 4 [190835]: Cho phản ứng hóa học: CH3CHO + Br2 + H2O →
Sản phẩm hữu cơ của phản ứng trên là
Sản phẩm hữu cơ của phản ứng trên là
A, HCOOH.
B, CH3COOH.
C, CH3CH2OH.
D, CH3COCH3.
CH3CHO + Br2 + H2O  CH3COOH + 2HBr
CH3COOH + 2HBr
Đáp án B. Đáp án: B
 CH3COOH + 2HBr
CH3COOH + 2HBrĐáp án B. Đáp án: B
Câu 5 [705808]: Dung dịch nitric acid đặc có thể hòa tan copper (II) sulfide theo phương trình chưa cân bằng như sau:
CuS + HNO3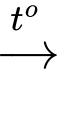 CuSO4 + NO + H2O.
CuSO4 + NO + H2O.
Để hòa tan 28,8 gam CuS thì thể tích (mL) dung dịch HNO3 16 M cần dùng là
CuS + HNO3
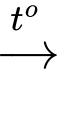 CuSO4 + NO + H2O.
CuSO4 + NO + H2O.Để hòa tan 28,8 gam CuS thì thể tích (mL) dung dịch HNO3 16 M cần dùng là
A, 80.
B, 800.
C, 50.
D, 500.
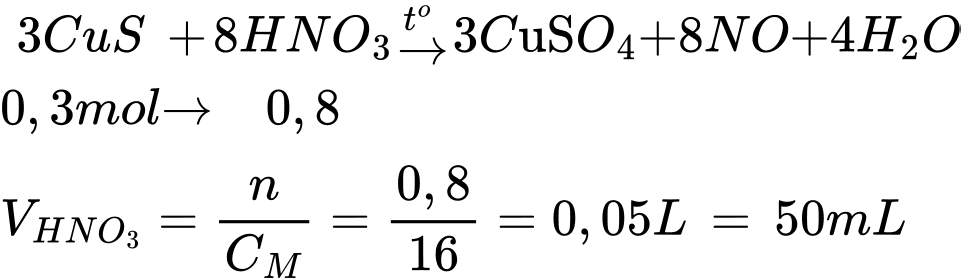
Chọn đáp án C Đáp án: C
Câu 6 [703816]: Kim loại nào sau đây là kim loại kiềm?
A, Potassium (K).
B, Mercury (Hg).
C, Cooper (Cu).
D, Magnesium (Mg).
Kim loại kiềm là các kim loại thuộc nhóm IA trong bảng tuần hoàn. Các nguyên tố này bao gồm:
⭐ Li (Lithium)
⭐ Na (Sodium)
⭐ K (Potassium)
⭐ Rb (Rubidium)
⭐ Cs (Caesi)
⭐ Fr (Franci)
⇒ Kim loại kiềm trong dãy các kim loại trên là Potassium (K)
⇒ Chọn đáp án A Đáp án: A
⭐ Li (Lithium)
⭐ Na (Sodium)
⭐ K (Potassium)
⭐ Rb (Rubidium)
⭐ Cs (Caesi)
⭐ Fr (Franci)
⇒ Kim loại kiềm trong dãy các kim loại trên là Potassium (K)
⇒ Chọn đáp án A Đáp án: A
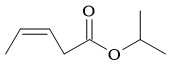
Câu 7 [703825]: Một carboxylic acid chưa bão hoà phản ứng với alcohol E tạo thành ester có công thức cấu tạo được cho như hình bên. Hãy cho biết alcohol E là alcohol bậc mấy?

A, Một.
B, Hai.
C, Ba.
D, Bốn.
Công thức cấu tạo của ester RCOOR' là CH3CH=CHCH2COOCH(CH3)CH3
- Phần gốc acid RCOO: CH3CH=CHCH2COO tạo bởi acid CH3CH=CHCH2COOH (pent-3-enoic acid)
- Phần gốc alcohol OR': OCH(CH3)CH3 tạo bởi alcohol (CH3)2CHOH (isopropyl alcohol)
⭐ Cách xác định bậc của alcohol: Bậc của alcohol là bậc của nguyên tử carbon liên kết cùng nhóm - OH (số C mà C đó liên kết)
⇒ Isopropyl alcohol là alcohol bậc hai (số liên kết carbon khác)
⇒ Chọn đáp án B
Đáp án: B
- Phần gốc acid RCOO: CH3CH=CHCH2COO tạo bởi acid CH3CH=CHCH2COOH (pent-3-enoic acid)
- Phần gốc alcohol OR': OCH(CH3)CH3 tạo bởi alcohol (CH3)2CHOH (isopropyl alcohol)
⭐ Cách xác định bậc của alcohol: Bậc của alcohol là bậc của nguyên tử carbon liên kết cùng nhóm - OH (số C mà C đó liên kết)
⇒ Isopropyl alcohol là alcohol bậc hai (số liên kết carbon khác)
⇒ Chọn đáp án B
Đáp án: B
Câu 8 [703943]: Trong cơ thể người, sự thiếu hụt nguyên tố nào sau đây có thể gây ra bệnh loãng xương?
A, Barium.
B, Magnesium.
C, Beryllium.
D, Calcium.
Canlcium là thành phần chính của xương và răng, đóng vai trò quan trọng trong việc duy trì cấu trúc xương nên sự thiếu hụt canlcium (Ca) trong cơ thể có thể gây ra bệnh loãng xương.
⇒ Chọn đáp án D Đáp án: D
⇒ Chọn đáp án D Đáp án: D
Câu 9 [703927]: “Phân tử saccharose được tạo bởi một đơn vị α-glucose và một đơn vị ...(1)..., liên kết với nhau qua liên kết ...(2)...”. Nội dung phù hợp trong ô trống (1), (2) lần lượt là
A, β-glucose, α-1,2-glycoside.
B, β-fructose, α-1,2-glycoside.
C, α-fructose, α-1,2-glycoside.
D, β-glucose, α-1,4-glycoside.
Saccharose là một disaccharide, được hình thành từ sự liên kết giữa hai monosaccharide là α-glucose và β-fructose, hình thành nhờ liên kết glycosidic giữa carbon số 1 của α-glucose và carbon số 2 của β-fructose.
⇒ Phân tử saccharose được tạo bởi một đơn vị α-glucose và một đơn vị β-fructose, liên kết với nhau qua liên kết α-1,2-glycoside.
⇒ Chọn đáp án B Đáp án: B
⇒ Phân tử saccharose được tạo bởi một đơn vị α-glucose và một đơn vị β-fructose, liên kết với nhau qua liên kết α-1,2-glycoside.
⇒ Chọn đáp án B Đáp án: B
Câu 10 [247497]: Phản ứng nào sau đây không có sự thay đổi số oxi hóa của nguyên tố Mn?
A, MnO2 + 4HCl 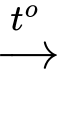 MnCl2 + Cl2 + 2H2O.
MnCl2 + Cl2 + 2H2O.
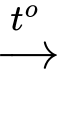 MnCl2 + Cl2 + 2H2O.
MnCl2 + Cl2 + 2H2O.B, Mn + O2 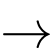 MnO2.
MnO2.
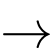 MnO2.
MnO2.C, 2HCl + MnO 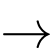 MnCl2 + H2O.
MnCl2 + H2O.
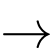 MnCl2 + H2O.
MnCl2 + H2O.D, 6KI + 2KMnO4 + 4H2O 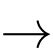 3I2 + 2MnO2 + 8KOH.
3I2 + 2MnO2 + 8KOH.
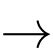 3I2 + 2MnO2 + 8KOH.
3I2 + 2MnO2 + 8KOH.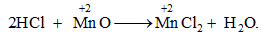 Đáp án: C
Đáp án: C
Câu 11 [703944]: Chất nào sau đây thuộc loại chất điện li yếu?
A, Saccharose C12H22O11.
B, Ethanol C2H5OH.
C, Dimethylamine (CH3)2NH.
D, Sodium hydroxide NaOH.
Hai chất saccharose C12H22O11 và ethanol C2H5OH là hai chất không điện li.
NaOH là một base mạnh, phân li hoàn toàn ra OH- nên là chất điện li mạnh.
Dimethylamine (CH3)2NH là một base yếu nên điện li yếu.
⇒ Chọn đáp án C Đáp án: C
NaOH là một base mạnh, phân li hoàn toàn ra OH- nên là chất điện li mạnh.
Dimethylamine (CH3)2NH là một base yếu nên điện li yếu.
⇒ Chọn đáp án C Đáp án: C
Câu 12 [59275]: Trong thực tế, cách nào sau đây không được dùng để bảo vệ kim loại sắt khỏi bị ăn mòn?
A, Gắn kim loại đồng với sắt.
B, Tráng kẽm lên bề mặt sắt.
C, Phủ một lớp sơn lên bề mặt sắt.
D, Tráng thiếc lên bề mặt sắt.
HD: ☆ Phương pháp bảo vệ bề mặt
Nguyên tắc: Cách li kim loại với môi trường bằng một lớp phân cách mỏng, bền vững.
Biện pháp: ta có thể: Bôi dầu mỡ, sơn, mạ, tráng men,...
Sắt tây là sắt được tráng thiếc (Sn), được sử dụng làm vỏ hộp trong ngành thực phẩm.
Tôn là sắt được tráng kẽm, được sử dụng trong ngành vật liệu xây dựng.
Các đồ vật bằng sắt thường được mạ bằng niken hay crom.
☆ Phương pháp điện hóa
Nguyên tắc: Trong quá trình ăn mòn điện hóa, kim loại mạnh hơn bị ăn mòn.
Biện pháp: Nối kim loại cần bảo vệ với kim loại hoạt động mạnh hơn để kim loại đó bị ăn mòn thay.
Để bảo vệ vỏ tàu biển bằng thép, những tấm kẽm đã được gắn vào mặt ngoài vỏ tàu (phần chìm dưới nước) để Zn bị ăn mòn, còn thép được bảo vệ.
⇒ Chọn đáp án A Đáp án: A
Nguyên tắc: Cách li kim loại với môi trường bằng một lớp phân cách mỏng, bền vững.
Biện pháp: ta có thể: Bôi dầu mỡ, sơn, mạ, tráng men,...
Sắt tây là sắt được tráng thiếc (Sn), được sử dụng làm vỏ hộp trong ngành thực phẩm.
Tôn là sắt được tráng kẽm, được sử dụng trong ngành vật liệu xây dựng.
Các đồ vật bằng sắt thường được mạ bằng niken hay crom.
☆ Phương pháp điện hóa
Nguyên tắc: Trong quá trình ăn mòn điện hóa, kim loại mạnh hơn bị ăn mòn.
Biện pháp: Nối kim loại cần bảo vệ với kim loại hoạt động mạnh hơn để kim loại đó bị ăn mòn thay.
Để bảo vệ vỏ tàu biển bằng thép, những tấm kẽm đã được gắn vào mặt ngoài vỏ tàu (phần chìm dưới nước) để Zn bị ăn mòn, còn thép được bảo vệ.
⇒ Chọn đáp án A Đáp án: A
Câu 13 [706007]: Hình dưới đây cho thấy cấu tạo một phần mắt xích của polymer được tạo thành khi đồng trùng hợp hai monomer khác nhau.
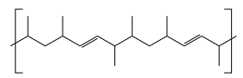
Biết rằng một monomer là propene. Monomer còn lại có công thức cấu tạo là gì?

Biết rằng một monomer là propene. Monomer còn lại có công thức cấu tạo là gì?
A, 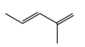

B, 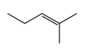

C, 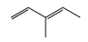

D, 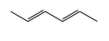

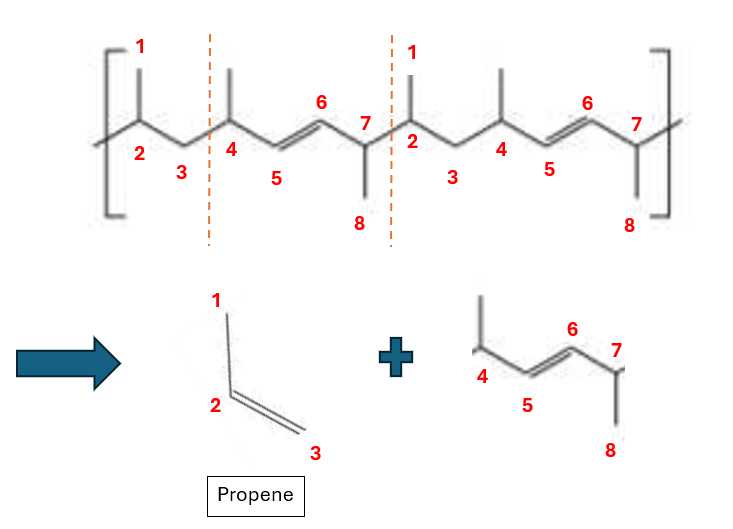
Monomer có dạng propene. Monomer còn lại có dạng
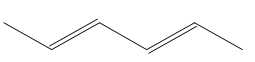
⟹ Chọn đáp án D
Đáp án: D
Câu 14 [703945]: Quy trình tái chế một kim loại thông dụng để đựng đồ uống được thực hiện như sau:
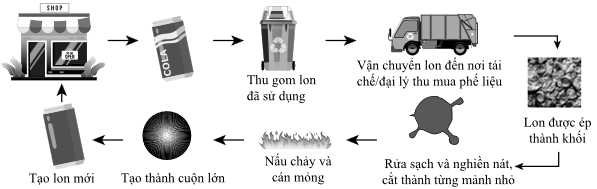
Phát biểu nào sau đây về quy trình trên đúng?

Phát biểu nào sau đây về quy trình trên đúng?
A, Kim loại được tái chế trong quy trình có thể là nhôm (aluminium).
B, Rửa sạch nguyên liệu trước khi nóng chảy giúp loại lớp sơn trên vỏ, lon.
C, Trong quá trình tái chế có sử dụng phương pháp nhiệt luyện.
D, Các giai đoạn của quy trình không làm phát thải khí gây hiệu ứng nhà kính.
Phân tích các phát biểu:
✔️ A. Đúng. Nhôm là một trong những kim loại phổ biến được dùng để sản xuất lon đồ uống nhờ nhẹ, bền và khả năng tái chế cao. Trong thực tế, nhôm từ vỏ lon đồ uống thường được tái chế để sản xuất lon mới.
❌ B. Sai. Rửa sạch trước khi nóng chảy thường chỉ nhằm loại bỏ bụi bẩn, dầu mỡ, hoặc tạp chất bề mặt. Lớp sơn hoặc lớp phủ trên lon nhôm thường được loại bỏ thông qua quá trình đốt cháy hoặc nhiệt phân trong lò nung, không phải trong bước rửa.
❌ C. Sai. Quá trình tái chế nhôm là nóng chảy nhôm phế liệu ở nhiệt độ cao và đúc lại chứ không phải nhiệt luyện.
❌ D. Sai. Quá trình tái chế nhôm, đặc biệt là giai đoạn nóng chảy, tiêu tốn năng lượng và có thể phát thải khí nhà kính như C gây hiệu ứng nhà kính.
⇒ Chọn đáp án A Đáp án: A
✔️ A. Đúng. Nhôm là một trong những kim loại phổ biến được dùng để sản xuất lon đồ uống nhờ nhẹ, bền và khả năng tái chế cao. Trong thực tế, nhôm từ vỏ lon đồ uống thường được tái chế để sản xuất lon mới.
❌ B. Sai. Rửa sạch trước khi nóng chảy thường chỉ nhằm loại bỏ bụi bẩn, dầu mỡ, hoặc tạp chất bề mặt. Lớp sơn hoặc lớp phủ trên lon nhôm thường được loại bỏ thông qua quá trình đốt cháy hoặc nhiệt phân trong lò nung, không phải trong bước rửa.
❌ C. Sai. Quá trình tái chế nhôm là nóng chảy nhôm phế liệu ở nhiệt độ cao và đúc lại chứ không phải nhiệt luyện.
❌ D. Sai. Quá trình tái chế nhôm, đặc biệt là giai đoạn nóng chảy, tiêu tốn năng lượng và có thể phát thải khí nhà kính như C gây hiệu ứng nhà kính.
⇒ Chọn đáp án A Đáp án: A
Câu 15 [705831]: Một loại bình chữa cháy chứa CO2 thể lỏng ở áp suất cao. Khi mở van, do áp suất giảm đột ngột nên khí CO2 sẽ chuyển sang thể khí.
Cho các phát biểu sau:
(a) CO2 làm giảm nhiệt độ của đám cháy do CO2 lỏng bay hơi sẽ hấp thu nhiệt.
(b) Luồng khí CO2 làm hạn chế sự tiếp xúc của đồ vật với oxygen.
(c) Luồng khí CO2 làm loãng nồng độ hơi chất cháy trong đám cháy.
(d) Hơi chất cháy phản ứng với CO2 tạo hợp chất mới thay vì phản ứng với oxygen.
Số phát biểu đúng là
Cho các phát biểu sau:
(a) CO2 làm giảm nhiệt độ của đám cháy do CO2 lỏng bay hơi sẽ hấp thu nhiệt.
(b) Luồng khí CO2 làm hạn chế sự tiếp xúc của đồ vật với oxygen.
(c) Luồng khí CO2 làm loãng nồng độ hơi chất cháy trong đám cháy.
(d) Hơi chất cháy phản ứng với CO2 tạo hợp chất mới thay vì phản ứng với oxygen.
Số phát biểu đúng là
A, 1.
B, 2.
C, 3.
D, 4.
Nguyên lý chữa cháy của bình CO2
Cơ chế chữa cháy (tác dụng) của CO2 là làm loãng nồng độ hơi chất cháy trong vùng cháy và bên cạnh đó nó còn có tác dụng làm lạnh do CO2 ở dạng lỏng khi bay hơi sẽ thu nhiệt.
✔️(a) – Đúng. CO2 làm giảm nhiệt độ của đám cháy do CO2 lỏng bay hơi sẽ hấp thu nhiệt.
✔️ (b) – Đúng. Luồng khí CO2làm hạn chế sự tiếp xúc của đồ vật với oxygen giảm khả năng lan rông của đám cháy.
✔️(c) – Đúng. Luồng khí CO2 làm loãng nồng độ hơi chất cháy trong đám cháy. CO2 sẽ đẩy bớt chất cháy ra khỏi vùng cháy.
❌(d) – Sai. Hơi chất cháy không phản ứng với CO2 tạo hợp chất mới thì sẽ làm quá trình cháy trở lên mãnh liệt.
Có 3 nhận định đúng.
Chọn đáp án C Đáp án: C
Cơ chế chữa cháy (tác dụng) của CO2 là làm loãng nồng độ hơi chất cháy trong vùng cháy và bên cạnh đó nó còn có tác dụng làm lạnh do CO2 ở dạng lỏng khi bay hơi sẽ thu nhiệt.
✔️(a) – Đúng. CO2 làm giảm nhiệt độ của đám cháy do CO2 lỏng bay hơi sẽ hấp thu nhiệt.
✔️ (b) – Đúng. Luồng khí CO2làm hạn chế sự tiếp xúc của đồ vật với oxygen giảm khả năng lan rông của đám cháy.
✔️(c) – Đúng. Luồng khí CO2 làm loãng nồng độ hơi chất cháy trong đám cháy. CO2 sẽ đẩy bớt chất cháy ra khỏi vùng cháy.
❌(d) – Sai. Hơi chất cháy không phản ứng với CO2 tạo hợp chất mới thì sẽ làm quá trình cháy trở lên mãnh liệt.
Có 3 nhận định đúng.
Chọn đáp án C Đáp án: C
Câu 16 [705966]: Trong quá trình sản xuất rượu vang, người ta sử dụng nấm men Saccharomyces cerevisiae để lên men glucose và fructose (có trong dịch ép trái nho) tạo thành ethanol. Một học sinh thực hiện thí nghiệm thử tính chất của sản phẩm từ quá trình lên men này trong phòng thí nghiệm bằng dụng cụ như hình dưới:
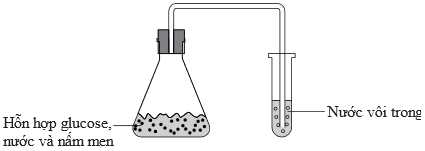
Cho các phát biểu sau về thí nghiệm:
(a) Phản ứng lên men glucose thuộc loại phản ứng phân hủy.
(b) Ethanol bay hơi, không tan trong nước vôi trong tạo bong bóng khí.
(c) Ống nghiệm chứa nước vôi trong bị vẩn đục.
(d) Có thể thay nước vôi trong bằng dung dịch xút.
Các phát biểu đúng là

Cho các phát biểu sau về thí nghiệm:
(a) Phản ứng lên men glucose thuộc loại phản ứng phân hủy.
(b) Ethanol bay hơi, không tan trong nước vôi trong tạo bong bóng khí.
(c) Ống nghiệm chứa nước vôi trong bị vẩn đục.
(d) Có thể thay nước vôi trong bằng dung dịch xút.
Các phát biểu đúng là
A, (a), (c).
B, (b), (c).
C, (a), (b), (c).
D, (b), (c), (d).
Phân tích các phát biểu :
✔️(a) – Đúng. Phản ứng phân hủy: Là phản ứng hóa học trong đó một chất sinh ra hai hay nhiều chất mới. Phản ứng lên men glucose sinh ra nhiều chất mới là CO2 và C2H5OH nên phản ứng lên men là phản ứng phân hủy.
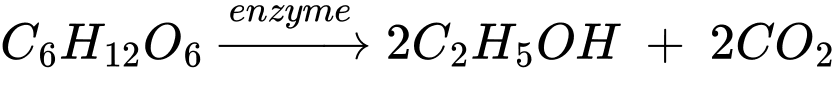
❌(b) – Sai. Ethanol bay hơi, tan vô hạn trong nước.
✔️(c) – Đúng. Ống nghiệm chứa nước vôi trong bị vẩn đục. Nguyên do phản ứng lên men sinh ra CO2 làm vẫn đục nước vôi trong.
CO2 + Ca(OH)2 → CaCO3 + H2O
❌(d) – Sai. Không thể thay nước vôi trong bằng dung dịch xút, khi có khí sinh ra không rõ hiện tượng là khí phản ứng với dung dịch xút hay thoát ra ngoài.
⟹Có 2 phát biểu đúng là (a),(c).
⟹Chọn đáp án A Đáp án: A
✔️(a) – Đúng. Phản ứng phân hủy: Là phản ứng hóa học trong đó một chất sinh ra hai hay nhiều chất mới. Phản ứng lên men glucose sinh ra nhiều chất mới là CO2 và C2H5OH nên phản ứng lên men là phản ứng phân hủy.
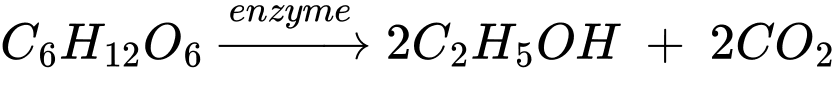
❌(b) – Sai. Ethanol bay hơi, tan vô hạn trong nước.
✔️(c) – Đúng. Ống nghiệm chứa nước vôi trong bị vẩn đục. Nguyên do phản ứng lên men sinh ra CO2 làm vẫn đục nước vôi trong.
CO2 + Ca(OH)2 → CaCO3 + H2O
❌(d) – Sai. Không thể thay nước vôi trong bằng dung dịch xút, khi có khí sinh ra không rõ hiện tượng là khí phản ứng với dung dịch xút hay thoát ra ngoài.
⟹Có 2 phát biểu đúng là (a),(c).
⟹Chọn đáp án A Đáp án: A
Sử dụng thông tin ở bảng dưới đây để trả lời các câu 17 – 18:
Cho bảng thông tin sau:


Câu 17 [702815]: Trong các ion kim loại có trong bảng trên, ở điều kiện chuẩn ion nào có tính oxi hóa mạnh nhất?
A, Ag+.
B, Cu2+.
C, Fe2+.
D, Ni2+.
Kim loại có thế điện cực chuẩn càng âm thì càng có tính khử mạnh, càng dương thì tính tính oxi hoá càng mạnh.
Thấy giá trị thế điện cực chuẩn của cặp oxi hoá - khử Ag+/Ag là dương nhất nên Ag+ có tính oxi hoá mạnh nhất.
⇒ Chọn đáp án A Đáp án: A
Thấy giá trị thế điện cực chuẩn của cặp oxi hoá - khử Ag+/Ag là dương nhất nên Ag+ có tính oxi hoá mạnh nhất.
⇒ Chọn đáp án A Đáp án: A
Câu 18 [702816]: Biết sức điện động chuẩn của pin điện hoá gồm hai điện cực M2+/M và Ag+/Ag bằng 1,056 V. Kim loại nào sau đây phù hợp với M?
A, Fe.
B, Sn.
C, Ni.
D, Cu.
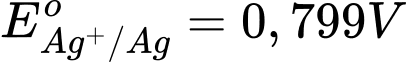 giá trị thế điện cực dương nhất → Ag+/Ag là cực dương, cathode
giá trị thế điện cực dương nhất → Ag+/Ag là cực dương, cathodeSức điện động của pin trên.
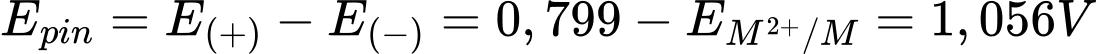
→
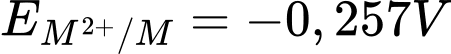 → Cặp oxi hóa khử phù hợp Ni2+/Ni
→ Cặp oxi hóa khử phù hợp Ni2+/Ni → Kim loại phù hợp là Ni
⇒ Chọn đáp án C Đáp án: C
PHẦN III. Thí sinh trả lời từ câu 1 đến 6. Thí sinh điền kết quả mỗi câu vào mỗi ô trả lời tương ứng theo hướng dẫn của phiếu trả lời.
Câu 19 [704399]: Tiến hành thí nghiệm phản ứng màu biuret của lòng trắng trứng như sau:
▪ Bước 1: Cho vào ống nghiệm khoảng 1 mL dung dịch NaOH 30 %. Thêm tiếp vài giọt dung dịch CuSO4 2 %, lắc đều (có thể khuấy bằng đũa thuỷ tinh).
▪ Bước 2: Thêm vào ống nghiệm khoảng 3 mL dung dịch lòng trắng trứng, lắc hoặc khuấy đều hỗn hợp.
▪ Bước 1: Cho vào ống nghiệm khoảng 1 mL dung dịch NaOH 30 %. Thêm tiếp vài giọt dung dịch CuSO4 2 %, lắc đều (có thể khuấy bằng đũa thuỷ tinh).
▪ Bước 2: Thêm vào ống nghiệm khoảng 3 mL dung dịch lòng trắng trứng, lắc hoặc khuấy đều hỗn hợp.
⭐ Nguyên tắc phản ứng:
+) Phản ứng màu biuret xảy ra khi hợp chất chứa liên kết peptide (–CO–NH–) tác dụng với dung dịch kiềm mạnh (NaOH) và Cu2+.
+) Kết quả là tạo thành phức chất màu tím, chứng minh sự hiện diện của chuỗi peptide trong mẫu thí nghiệm.
⭐ Các hiện tượng trong thí nghiệm:
+) Bước 1: Khi cho CuSO4 vào dung dịch NaOH, xuất hiện kết tủa Cu(OH)2 màu xanh nhạt:
CuSO4 + 2NaOH → Cu(OH)2↓ + Na2SO4
+) Bước 2: Thêm dung dịch lòng trắng trứng (protein chứa liên kết peptide), kết tủa Cu(OH)2 tan, tạo thành phức chất màu tím.
Phân tích các phát biểu:
❌ (a) Sai. Ở bước 1, xuất hiện kết tủa Cu(OH)2 màu xanh nhạt chứ không phải màu đỏ gạch.
✔️ (b) Đúng. Phản ứng giữa Cu(OH)2 với các nhóm peptide –CO–NH– trong lòng trắng trứng tạo ra sản phẩm màu tím đặc trưng.
✔️ (c) Đúng. Có thể sử dụng dung dịch NaOH 10%, 20%, hoặc 30%, miễn là đủ tạo môi trường kiềm mạnh để có thể phản ứng với CuSO4 tạo ra kết tủa Cu(OH)2 thực hiện phản ứng màu buiret.
✔️ (d) Đúng. Phản ứng màu biuret xuất hiện màu tím đặc trưng nếu có ít nhất 2 liên kết peptide, chứng minh sự hiện diện của peptide trong lòng trắng trứng với số liên kết –CO–NH– lớn hơn hoặc bằng 2.
+) Phản ứng màu biuret xảy ra khi hợp chất chứa liên kết peptide (–CO–NH–) tác dụng với dung dịch kiềm mạnh (NaOH) và Cu2+.
+) Kết quả là tạo thành phức chất màu tím, chứng minh sự hiện diện của chuỗi peptide trong mẫu thí nghiệm.
⭐ Các hiện tượng trong thí nghiệm:
+) Bước 1: Khi cho CuSO4 vào dung dịch NaOH, xuất hiện kết tủa Cu(OH)2 màu xanh nhạt:
CuSO4 + 2NaOH → Cu(OH)2↓ + Na2SO4
+) Bước 2: Thêm dung dịch lòng trắng trứng (protein chứa liên kết peptide), kết tủa Cu(OH)2 tan, tạo thành phức chất màu tím.
Phân tích các phát biểu:
❌ (a) Sai. Ở bước 1, xuất hiện kết tủa Cu(OH)2 màu xanh nhạt chứ không phải màu đỏ gạch.
✔️ (b) Đúng. Phản ứng giữa Cu(OH)2 với các nhóm peptide –CO–NH– trong lòng trắng trứng tạo ra sản phẩm màu tím đặc trưng.
✔️ (c) Đúng. Có thể sử dụng dung dịch NaOH 10%, 20%, hoặc 30%, miễn là đủ tạo môi trường kiềm mạnh để có thể phản ứng với CuSO4 tạo ra kết tủa Cu(OH)2 thực hiện phản ứng màu buiret.
✔️ (d) Đúng. Phản ứng màu biuret xuất hiện màu tím đặc trưng nếu có ít nhất 2 liên kết peptide, chứng minh sự hiện diện của peptide trong lòng trắng trứng với số liên kết –CO–NH– lớn hơn hoặc bằng 2.
Câu 20 [705815]: Sự hình thành nước thải acid mỏ (Acid mine drainage – AMD) được công nhận rộng rãi là một trong những vấn đề môi trường chính do khai thác mỏ trên toàn thế giới gây ra. Khoáng chất chịu trách nhiệm tạo ra AMD là sắt sulphide (pyrite), ổn định và không hòa tan khi không tiếp xúc với nước và oxygen trong khí quyển. Khi các loại quặng thải giàu pyrite được khai thác và được tiếp xúc với oxygen, nước khi có vi khuẩn Thiobacillus ferrooxidans, AMD được tạo ra do quá trình oxi hóa pyrite theo phương trình sau:
4FeS2(s) + 15O2(g) + 14H2O(1) → 4Fe(OH)3(s) + 8H2SO4(aq)
Một nhà máy khai thác mỏ copper – nickel, sản xuất 450 tấn quặng/ngày, thành phần quặng rắn chứa 5,00 % khối lượng pyrite và gặp phải vấn đề AMD. Sự rò rỉ acid ra ngoài môi trường đã dẫn đến sự xuống cấp của đất xung quanh mỏ. Để giải quyết vấn đề này, nhà máy đã sử dụng đá vôi để xử lý AMD theo phương trình như sau:
CaCO3(s) + H2SO4(aq) → CaSO4(s) + CO2(g) + H2O(l)
Một dòng sông bị xả thải nước acid mỏ, sau khi được xử lí thì tính acid của nước thải giảm, giá trị pH tăng từ 1,9 lên 6,0.
4FeS2(s) + 15O2(g) + 14H2O(1) → 4Fe(OH)3(s) + 8H2SO4(aq)
Một nhà máy khai thác mỏ copper – nickel, sản xuất 450 tấn quặng/ngày, thành phần quặng rắn chứa 5,00 % khối lượng pyrite và gặp phải vấn đề AMD. Sự rò rỉ acid ra ngoài môi trường đã dẫn đến sự xuống cấp của đất xung quanh mỏ. Để giải quyết vấn đề này, nhà máy đã sử dụng đá vôi để xử lý AMD theo phương trình như sau:
CaCO3(s) + H2SO4(aq) → CaSO4(s) + CO2(g) + H2O(l)
Một dòng sông bị xả thải nước acid mỏ, sau khi được xử lí thì tính acid của nước thải giảm, giá trị pH tăng từ 1,9 lên 6,0.
Phân tích các đáp án:
✔️A. Đúng. Có thể thay Ca(OH)2 cho đá vôi nhưng cần kiểm soát tốt hàm lượng Ca(OH)2 vì nếu dư thì sẽ làm đất có tính base.
Ca(OH)2 + H2SO4 ⟶ CaSO4 + H2O
✔️B. Đúng.
mFeS2 = 450 × 5% = 22,5 tấn ⟹ nFeS2 = m : M = 22,5 : 120 = 0,1875 mol
nH2SO4 = 4 × n = 0,375 mol ⟹ mH2SO4 = n × M = 36,75 tấn
❌C. Sai. Đất xung quanh mỏ AMD bị rò rỉ acid ⟹ H+ > OH-
✔️D. Đúng
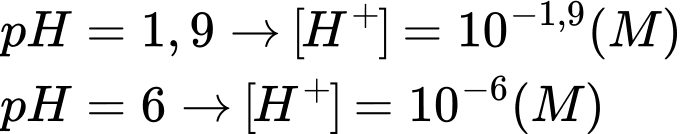
Số mol H+ trong mỗi lít dung dịch bị trung hoà là: 10-1,9 – 10-6 = 1,26.10-2 mol
✔️A. Đúng. Có thể thay Ca(OH)2 cho đá vôi nhưng cần kiểm soát tốt hàm lượng Ca(OH)2 vì nếu dư thì sẽ làm đất có tính base.
Ca(OH)2 + H2SO4 ⟶ CaSO4 + H2O
✔️B. Đúng.
mFeS2 = 450 × 5% = 22,5 tấn ⟹ nFeS2 = m : M = 22,5 : 120 = 0,1875 mol
nH2SO4 = 4 × n = 0,375 mol ⟹ mH2SO4 = n × M = 36,75 tấn
❌C. Sai. Đất xung quanh mỏ AMD bị rò rỉ acid ⟹ H+ > OH-
✔️D. Đúng
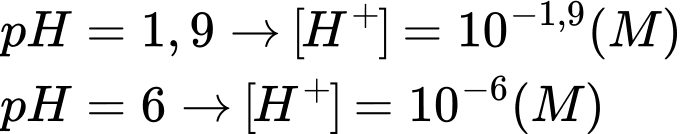
Số mol H+ trong mỗi lít dung dịch bị trung hoà là: 10-1,9 – 10-6 = 1,26.10-2 mol
Câu 21 [705918]: Độ dẫn điện của một dung dịch phụ thuộc vào số lượng ion tự do cũng như bản chất của các ion tồn tại trong dung dịch đó. Biểu đồ trong bảng dưới đây biểu diễn phép chuẩn độ, đồng thời đo độ dẫn điện. Trong đó:
∎ X là thể tích dung dịch thêm vào từ burette; Y là độ dẫn điện.
∎ Thí nghiệm 1: Acetic acid với ammonia (trên burette).
∎ Thí nghiệm 2: Silver nitrate với potassium chloride (trên burette).
∎ Thí nghiệm 3: Nitric acid với ammonia (trên burette).
∎ Thí nghiệm 4: Magnesium sulphate với barium hydroxide (trên burette).
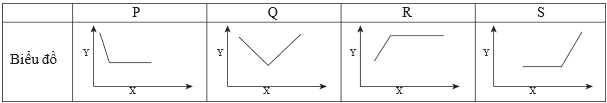
∎ X là thể tích dung dịch thêm vào từ burette; Y là độ dẫn điện.
∎ Thí nghiệm 1: Acetic acid với ammonia (trên burette).
∎ Thí nghiệm 2: Silver nitrate với potassium chloride (trên burette).
∎ Thí nghiệm 3: Nitric acid với ammonia (trên burette).
∎ Thí nghiệm 4: Magnesium sulphate với barium hydroxide (trên burette).

Phân tích các phát biểu:
✔️A. Đúng. (CH3COOH) là một acid yếu, chỉ phân li một phần trong dung dịch tạo ra ion H+ và CH3COO-. Do đó, dung dịch CH3COOH có độ dẫn điện thấp hơn so với các axit mạnh ở cùng nồng độ.
❌B. Sai. Ion H+ có độ linh động cao hơn nhiều so với ion NH4+ trong dung dịch. Do đó, độ dẫn điện của ion H+ lớn hơn ion NH4+.
✔️C. Đúng. Khi tạo thành kết tủa, các ion trong dung dịch bị loại bỏ khỏi dung dịch, làm giảm số lượng ion tự do và do đó làm giảm độ dẫn điện.
❌D. Sai. Vì:
- TN1: Độ dẫn điện thấp do CH3COOH là axit yếu, phân li kém.
- TN2: Độ dẫn điện cao do có nhiều ion Ag+ và NO3-, K+ và Cl-.
- TN3 : Độ dẫn điện cao do HNO3 là axit mạnh, phân li hoàn toàn.
- TN4 : Độ dẫn điện cao do có nhiều ion Mg2+, SO42-, Ba2+ và OH-.
✔️A. Đúng. (CH3COOH) là một acid yếu, chỉ phân li một phần trong dung dịch tạo ra ion H+ và CH3COO-. Do đó, dung dịch CH3COOH có độ dẫn điện thấp hơn so với các axit mạnh ở cùng nồng độ.
❌B. Sai. Ion H+ có độ linh động cao hơn nhiều so với ion NH4+ trong dung dịch. Do đó, độ dẫn điện của ion H+ lớn hơn ion NH4+.
✔️C. Đúng. Khi tạo thành kết tủa, các ion trong dung dịch bị loại bỏ khỏi dung dịch, làm giảm số lượng ion tự do và do đó làm giảm độ dẫn điện.
❌D. Sai. Vì:
- TN1: Độ dẫn điện thấp do CH3COOH là axit yếu, phân li kém.
- TN2: Độ dẫn điện cao do có nhiều ion Ag+ và NO3-, K+ và Cl-.
- TN3 : Độ dẫn điện cao do HNO3 là axit mạnh, phân li hoàn toàn.
- TN4 : Độ dẫn điện cao do có nhiều ion Mg2+, SO42-, Ba2+ và OH-.
Câu 22 [704187]: Nghiên cứu khả năng phản ứng của dung dịch copper(II) sulfate loãng với hydrochloric acid đặc được thực hiện như sau: Thêm khoảng 2 mL dung dịch HCl vào ống nghiệm chứa khoảng 1 mL dung dịch CuSO4. Màu sắc của ống nghiệm được theo dõi (từ trái sang phải) như hình bên dưới.


Phân tích các phát biểu:
✔️ (a) Đúng. Trong dung dịch ion Cu2+ tồn tại dưới dạng phức chất aqua [(Cu(H2O)6)]2+ khi tan trong nước, muối của các kim loại chuyển tiếp phân li thành các ion. Sau đó, cation kim loại chuyển tiếp (Mn+) thường nhận các cặp electron hoá trị riêng từ các phân tử H2O để hình thành các liên kết cho – nhận, tạo ra phức chất aqua theo phương trình hoá học dạng sau:
Cu2+ + 6H2O ⟶ [(Cu(H2O)6)]2+
✔️ (b) Đúng. Ở những điều kiện phù hợp, các anion và phân tử như OH, X- (halide), NH3,... có thể thay thế được một, một số hoặc tất cả các phối tử trong phức chất. Chẳng hạn, anion OH- hoặc Cl- có thể thay thế phối tử H2O trong các phức chất.
[(Cu(H2O)6)]2+ + 4HCl ⇌ [CuCl4]2- + 6H2O + 4H+
✔️ (c) Đúng. Tại trạng thái cân bằng tồn tại cả 2 dạng [(Cu(H2O)6)]2+ và [CuCl4]2- nên dung dịch có màu xanh lục.
❌ (d) Sai. Phản ứng trên không chứng minh được HCl có tính acid mạnh hơn H2SO4, chỉ chứng tỏ ion Cl- có khả năng thay thế phối tử H2O trong phức chất.
✔️ (a) Đúng. Trong dung dịch ion Cu2+ tồn tại dưới dạng phức chất aqua [(Cu(H2O)6)]2+ khi tan trong nước, muối của các kim loại chuyển tiếp phân li thành các ion. Sau đó, cation kim loại chuyển tiếp (Mn+) thường nhận các cặp electron hoá trị riêng từ các phân tử H2O để hình thành các liên kết cho – nhận, tạo ra phức chất aqua theo phương trình hoá học dạng sau:
Cu2+ + 6H2O ⟶ [(Cu(H2O)6)]2+
✔️ (b) Đúng. Ở những điều kiện phù hợp, các anion và phân tử như OH, X- (halide), NH3,... có thể thay thế được một, một số hoặc tất cả các phối tử trong phức chất. Chẳng hạn, anion OH- hoặc Cl- có thể thay thế phối tử H2O trong các phức chất.
[(Cu(H2O)6)]2+ + 4HCl ⇌ [CuCl4]2- + 6H2O + 4H+
✔️ (c) Đúng. Tại trạng thái cân bằng tồn tại cả 2 dạng [(Cu(H2O)6)]2+ và [CuCl4]2- nên dung dịch có màu xanh lục.
❌ (d) Sai. Phản ứng trên không chứng minh được HCl có tính acid mạnh hơn H2SO4, chỉ chứng tỏ ion Cl- có khả năng thay thế phối tử H2O trong phức chất.
PHẦN III. Thí sinh trả lời từ câu 1 đến 6. Thí sinh điền kết quả mỗi câu vào mỗi ô trả lời tương ứng theo hướng dẫn của phiếu trả lời.
Câu 23 [704213]: Hydrogen hoá hoàn toàn trilinolein có công thức (C17H31COO)3C3H5 trong điều kiện xúc tác Ni, đun nóng, thu được chất béo E. Phân tử khối của chất béo E là bao nhiêu?
Hydrogen hoá hoàn toàn trilinolein có công thức (C17H31COO)3C3H5 trong điều kiện xúc tác Ni, đun nóng thì phản ứng xảy ra như sau:
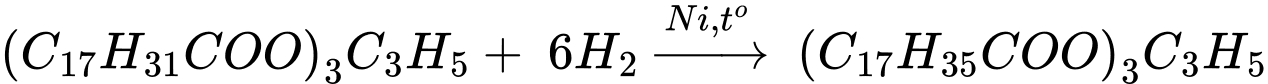
Chất béo E có công thức (C17H35COO)3C3H5
→ Phân tử khối của chất béo E là 890 gam/mol.
⇒ Điền đáp án: 890
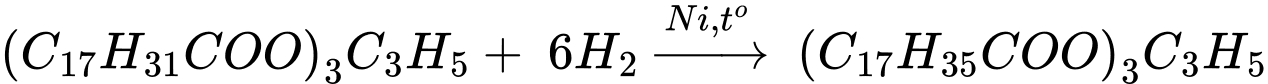
Chất béo E có công thức (C17H35COO)3C3H5
→ Phân tử khối của chất béo E là 890 gam/mol.
⇒ Điền đáp án: 890
Câu 24 [560844]: Độ tan của NaHCO3 ở 20°C và ở 40°C lần lượt là 9,6 g/100 g nước và 12,7 g/100 g nước. Khi giảm nhiệt độ của 112,7 gam dung dịch NaHCO3 bão hoà từ 40°C về 20°C thì khối lượng muối NaHCO3 kết tinh là bao nhiêu gam?(Làm tròn đến giá trị nguyên)
HƯỚNG DẪN GIẢI:
- Nồng độ của dung dịch NaHCO3 bão hoà ở 20oC là: (9,6) / (9,6 + 100) = 1200/137 (%)
- Nồng độ của dung dịch NaHCO3 bão hoà ở 40oC là: (12,7 / 12,7 + 100) = 12700/1127 (%)
⟹ Khối lượng muối NaHCO3 có trong 112,7 gam dung dịch NaHCO3 bão hoà ở 40oC là: 112,7 . (12700/1127)(%) = 12,7 (g)
- Giả sử khối lượng NaHCO3 tách ra là x gam.
- Khối lượng muối còn lại là: 12,7 - x (g)
- Khối lượng dung dịch còn lại là: 112,7 - x (g)
Lượng muối tách ra vừa đủ để khiến cho dung dịch về đến 20 độ C đạt đến trạng thái bão hoà nên nồng độ của dung dịch sau khi làm lạnh xuống 20 độ C bằng 1200/137 (%)
⟹ (12,7 - x) / (112,7 - x) = 1200/137 (%) ⟹ x = 3,1
⟹ Điền đáp án: 3
- Nồng độ của dung dịch NaHCO3 bão hoà ở 20oC là: (9,6) / (9,6 + 100) = 1200/137 (%)
- Nồng độ của dung dịch NaHCO3 bão hoà ở 40oC là: (12,7 / 12,7 + 100) = 12700/1127 (%)
⟹ Khối lượng muối NaHCO3 có trong 112,7 gam dung dịch NaHCO3 bão hoà ở 40oC là: 112,7 . (12700/1127)(%) = 12,7 (g)
- Giả sử khối lượng NaHCO3 tách ra là x gam.
- Khối lượng muối còn lại là: 12,7 - x (g)
- Khối lượng dung dịch còn lại là: 112,7 - x (g)
Lượng muối tách ra vừa đủ để khiến cho dung dịch về đến 20 độ C đạt đến trạng thái bão hoà nên nồng độ của dung dịch sau khi làm lạnh xuống 20 độ C bằng 1200/137 (%)
⟹ (12,7 - x) / (112,7 - x) = 1200/137 (%) ⟹ x = 3,1
⟹ Điền đáp án: 3
Câu 25 [706114]: Zytel® là một polymer được sử dụng phổ biến trong công nghiệp ô tô và điện tử. Polymer này có công thức cấu tạo như sau:
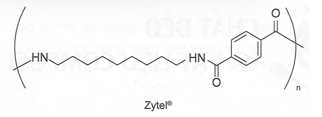
Tổng số nguyên tử carbon trong phân tử monomer có chứa vòng benzene là bao nhiêu?

Tổng số nguyên tử carbon trong phân tử monomer có chứa vòng benzene là bao nhiêu?
Các monomer cấu tạo nên polymer Zyter là
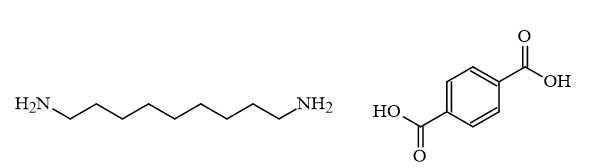
Tổng số nguyên tử carbon trong phân tử monomer chứa vòng benzene là 8.
⟹Điền đáp án : 8

Tổng số nguyên tử carbon trong phân tử monomer chứa vòng benzene là 8.
⟹Điền đáp án : 8
Câu 26 [706002]: Chitin có trong vỏ tôm được đun nóng trong dung dịch HCl đặc để điều chế glucosamine hydrochloride, một chất có tác dụng hỗ trợ xương khỏe mạnh.
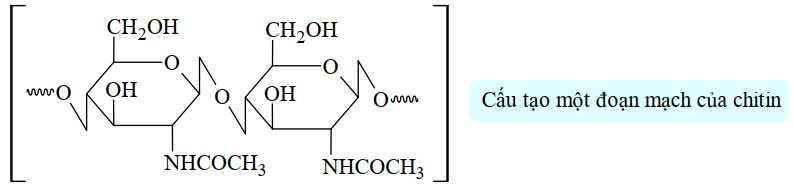
Công thức cấu tạo của glucosamine hydrochloride chứa bao nhiêu nhóm OH?

Công thức cấu tạo của glucosamine hydrochloride chứa bao nhiêu nhóm OH?
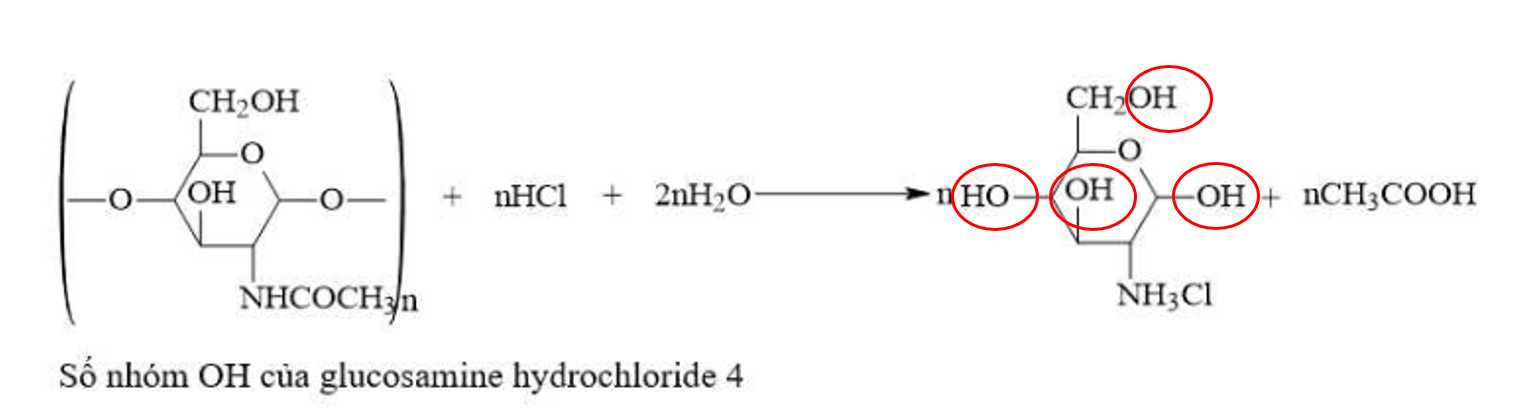
⟹Điền đáp án : 4
Câu 27 [705451]: Muối Fe2(SO4)3 khi tan trong nước sẽ phân li thành các ion Fe3+ và SO42–. Môi trường của dung dịch có tính acid do quá trình hình thành H3O+:
Fe3+(aq) + nH2O(l) → [Fe(OH2)6](aq)
[Fe(OH2)6](aq) + nH2O(l) → [Fe(OH)n(OH2)6-n]p+(aq) + nH3O+(aq)
Nếu điện tích của phức chất [Fe(OH)n(OH2)6-n]p+ là 1+ thì giá trị của n là bao nhiêu?
Fe3+(aq) + nH2O(l) → [Fe(OH2)6](aq)
[Fe(OH2)6](aq) + nH2O(l) → [Fe(OH)n(OH2)6-n]p+(aq) + nH3O+(aq)
Nếu điện tích của phức chất [Fe(OH)n(OH2)6-n]p+ là 1+ thì giá trị của n là bao nhiêu?
Phức chất [Fe(OH)n(OH2)6-n]p+ với ion trung tâm là Fe3+ và phối tử là OH- và phối tử trung hòa H2O.
Điện tích của phức chất [Fe(OH)n(OH2)6-n]p+ là 1+
→ +3 + [n × (-1)] + 0 = +1 → n = 2
⇒ Điền đáp án: 2
Điện tích của phức chất [Fe(OH)n(OH2)6-n]p+ là 1+
→ +3 + [n × (-1)] + 0 = +1 → n = 2
⇒ Điền đáp án: 2
Câu 28 [705980]: Vỏ trứng có chứa calcium ở dạng CaCO3. Để xác định hàm lượng CaCO3 có trong vỏ trứng, trong phòng thí nghiệm người ta có thể làm như sau:
Bước 1: Lấy 1,0 gam và trứng khô, đã được làm sạch, hòa tan hoàn toàn trong 50 mL dung dịch HCl 0,4 M. Lọc dung dịch sau phản ứng thu được 50 mL dung dịch X.
Bước 2: Lấy 10,0 mL X cho vào bình tam giác, thêm 1 – 2 giọt phenolphthalein.
Bước 3: Tiếp theo nhỏ từng giọt dung dịch NaOH 0,1M vào bình tam giác đến khi dung dịch xuất hiện màu hồng thấy hết 5,6 mL dung dịch NaOH.
Giả thiết các tạp chất khác trong vỏ trứng không tác dụng với HCl. Xác định hàm lượng CaCO3 có trong vỏ trứng.
Bước 1: Lấy 1,0 gam và trứng khô, đã được làm sạch, hòa tan hoàn toàn trong 50 mL dung dịch HCl 0,4 M. Lọc dung dịch sau phản ứng thu được 50 mL dung dịch X.
Bước 2: Lấy 10,0 mL X cho vào bình tam giác, thêm 1 – 2 giọt phenolphthalein.
Bước 3: Tiếp theo nhỏ từng giọt dung dịch NaOH 0,1M vào bình tam giác đến khi dung dịch xuất hiện màu hồng thấy hết 5,6 mL dung dịch NaOH.
Giả thiết các tạp chất khác trong vỏ trứng không tác dụng với HCl. Xác định hàm lượng CaCO3 có trong vỏ trứng.
Đổi 50 mL = 0,05 L; 5,6 mL = 0,0056 L
Số mol của HCl ban đầu là nHCl = 0,05.0,4 = 0,02 mol
Số mol của NaOH là nNaOH = 0,0056.0,1 = 0,00056 mol
(1) 2HCl + CaCO3 → CaCl2 + H2O + CO2
(2) HCl + NaOH → NaCl + H2O
Số mol HCl tham gia phản ứng trong pt(1) là
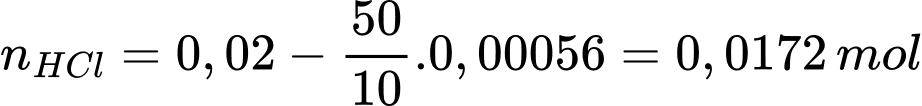
Từ PTHH (1) số mol của CaCO3 là n CaCO3 = 0,0086 gam
Hàm lượng CaCO3 trong vỏ trứng là
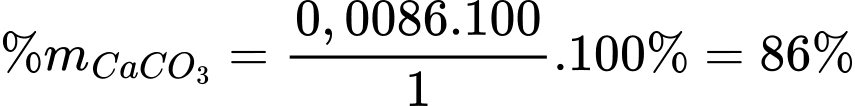
⟹Điền đáp án : 86
Số mol của HCl ban đầu là nHCl = 0,05.0,4 = 0,02 mol
Số mol của NaOH là nNaOH = 0,0056.0,1 = 0,00056 mol
(1) 2HCl + CaCO3 → CaCl2 + H2O + CO2
(2) HCl + NaOH → NaCl + H2O
Số mol HCl tham gia phản ứng trong pt(1) là
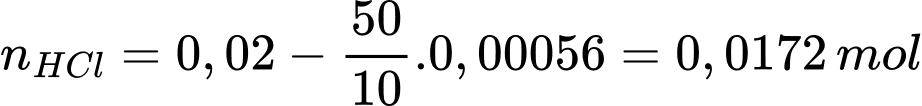
Từ PTHH (1) số mol của CaCO3 là n CaCO3 = 0,0086 gam
Hàm lượng CaCO3 trong vỏ trứng là
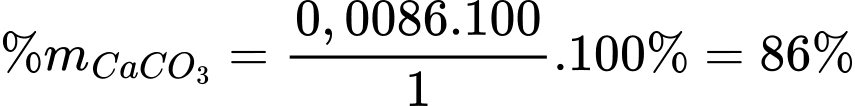
⟹Điền đáp án : 86