PHẦN I. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
Câu 1 [705965]: Đốt cháy hoàn toàn 1 mol CH3COOCH3, số mol CO2 thu được tối đa là bao nhiêu?
A, 1,0 mol.
B, 2,0 mol.
C, 3,0 mol.
D, 4,0 mol.
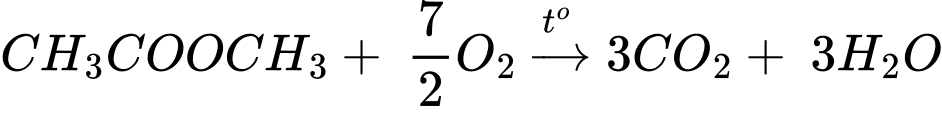
Từ PTHH số mol CO2 thu được khi đốt cháy 1 mol CH3COOCH3 là 3 mol.
⟹Chọn đáp án C Đáp án: C
Câu 2 [705985]: Magnalium là hợp kim có độ bền cao, mật độ thấp và khả năng chống ăn mòn nên nó được sử dụng trong chế tạo máy bay và các bộ phận ô tô. Thành phần của hợp kim Magnalium là
A, Mg và Zn.
B, Mg và Al.
C, Cu và Zn.
D, Mg và Cu.
- Magnalium là một hợp kim được tạo thành từ Aluminium và magnessium, thường được sử dụng trong các ứng dụng công nghiệp nhờ vào tính nhẹ và bền của nó. Hợp kim này thường có đặc tính chống ăn mòn tốt, dễ gia công và có thể được sử dụng trong sản xuất các sản phẩm như máy bay, ô tô, cũng như các thiết bị thể thao.
⟹Chọn đáp án B Đáp án: B
⟹Chọn đáp án B Đáp án: B
Câu 3 [308769]: Trong phân tử tetrapeptide Gly-Glu-Ala-Val, amino acid đầu N là
A, Valine.
B, Alanine.
C, Glutamic acid.
D, Glycine.
Trong phân tử peptide, ta quy ước :
- amino acid đầu N (nằm bên trái, chứa nhóm -NH2)
- amino acid đầu C (nằm bên phải, chứa nhóm -COOH).
Vậy trong peptide Gly-Glu-Ala-Val, amino acid đầu N là Glycine.
⟹ Chọn đáp án D Đáp án: D
- amino acid đầu N (nằm bên trái, chứa nhóm -NH2)
- amino acid đầu C (nằm bên phải, chứa nhóm -COOH).
Vậy trong peptide Gly-Glu-Ala-Val, amino acid đầu N là Glycine.
⟹ Chọn đáp án D Đáp án: D
Câu 4 [242124]: Cho biết nguyên tử Na, Mg, F lần lượt có số hiệu nguyên tử là 11, 12, 9. Các ion Na+, Mg2+, F– có đặc điểm chung là
A, Có cùng số proton.
B, Có cùng neutron.
C, Có cùng số electron.
D, Cùng nguyên tử khối.
HƯỚNG DẪN GIẢI:
- Các nguyên tử luôn có xu hướng cho hay nhận thêm electron để đạt đến cấu hình bền vững của khí hiếm.
- Mà khí hiếm gần nhất với các nguyên tử này là Ne (1s22s22p6).
⟹ Các ion này sẽ có chung cấu hình electron.
⟹ Các ion có cùng số electron
⟹ Chọn đáp án: C Đáp án: C
- Các nguyên tử luôn có xu hướng cho hay nhận thêm electron để đạt đến cấu hình bền vững của khí hiếm.
- Mà khí hiếm gần nhất với các nguyên tử này là Ne (1s22s22p6).
⟹ Các ion này sẽ có chung cấu hình electron.
⟹ Các ion có cùng số electron
⟹ Chọn đáp án: C Đáp án: C
Câu 5 [246535]: Trong tự nhiên, nguyên tố bromine có 2 đồng vị bền là 79Br và 81Br. Nếu nguyên tử khối trung bình của bromine là 79,91 thì phần trăm số nguyên tử của hai đồng vị này lần lượt là
A, 35% và 65%.
B, 45,5% và 54,5%.
C, 54,5% và 45,5%.
D, 61,8% và 38,2%.
HƯỚNG DẪN GIẢI:
- Gọi phần trăm số nguyên tử của đồng vị 79Br và 81Br lần lượt là x và y
⟹ x + y = 1 (1)
- Công thức tính nguyên tử khối trung bình như sau:
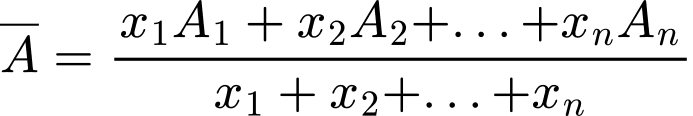
- Trong đó:
+) A1, A2, ... là số khối của các đồng vị tương ứng.
+) x1, x2, ... là phần trăm số nguyên tử của mỗi đồng vị tương ứng.
⟹ Nguyên tử khối trung bình của Br là:
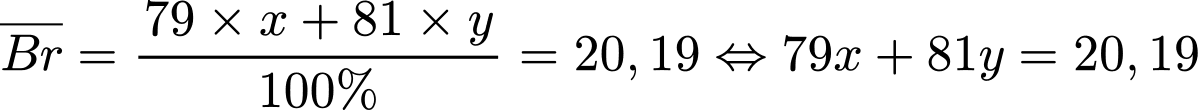 (2)
(2)
- Từ (1) và (2) ⟺ x = 0,545; y = 0,455
Vậy phần trăm số nguyên tử của 79Br là 54,5%, 81Br là 45,5%
⟹ Chọn đáp án: C
Đáp án: C
- Gọi phần trăm số nguyên tử của đồng vị 79Br và 81Br lần lượt là x và y
⟹ x + y = 1 (1)
- Công thức tính nguyên tử khối trung bình như sau:
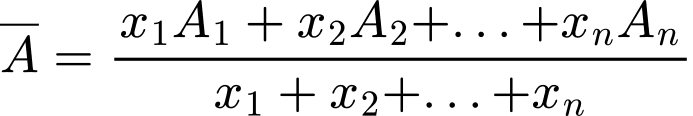
- Trong đó:
+) A1, A2, ... là số khối của các đồng vị tương ứng.
+) x1, x2, ... là phần trăm số nguyên tử của mỗi đồng vị tương ứng.
⟹ Nguyên tử khối trung bình của Br là:
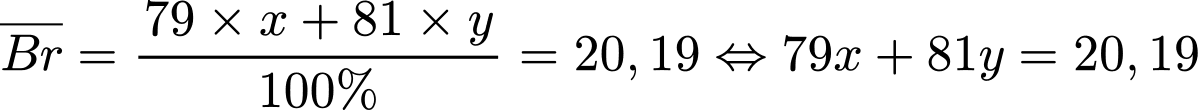 (2)
(2)- Từ (1) và (2) ⟺ x = 0,545; y = 0,455
Vậy phần trăm số nguyên tử của 79Br là 54,5%, 81Br là 45,5%
⟹ Chọn đáp án: C
Đáp án: C
Câu 6 [186358]: Trộn 200 mL dung dịch HCl 1 M với 300 mL dung dịch HCl 2 M thì thu được dung dịch mới có nồng độ mol là
A, 1,5M.
B, 1,2M.
C, 1,6M.
D, 2,4M.
Đáp án C
Số mol HCl sau khi trộn là:
nHCl = 0,2.1 + 0,3.2 = 0,8 mol
Thể tích dung dịch HCl sau khi trộn bằng:
Vdung dịch = 200 + 300 = 500 mL = 0,5 lít
Dung dịch sau khi trộn có nồng độ mol là:
CM = 1,6 mol/L Đáp án: C
Số mol HCl sau khi trộn là:
nHCl = 0,2.1 + 0,3.2 = 0,8 mol
Thể tích dung dịch HCl sau khi trộn bằng:
Vdung dịch = 200 + 300 = 500 mL = 0,5 lít
Dung dịch sau khi trộn có nồng độ mol là:
CM = 1,6 mol/L Đáp án: C
Câu 7 [705957]: Y là một polysaccharide có trong thành phần của tinh bột và có cấu trúc mạch carbon phân nhánh. Gạo nếp sở dĩ dẻo hơn và dính hơn gạo tẻ vì thành phần có chứa nhiều Y hơn. Tên gọi của Y là
A, cellulose.
B, amylose.
C, amylopectin.
D, saccharose.
Phân tích các đáp án :
❌A. Cellulose: Là một polysaccharide cấu tạo từ β-glucose, có cấu trúc mạch thẳng, không phân nhánh. Cellulose chủ yếu có trong thành tế bào thực vật, không phải thành phần chính của tinh bột. → Sai.
❌B. Amylose: Là một polysaccharide có trong tinh bột, nhưng có cấu trúc mạch thẳng, không phân nhánh. Amylose có xu hướng tạo kết tinh nên làm giảm độ dẻo của tinh bột. → Sai.
✔️C. Amylopectin: Là một polysaccharide có trong tinh bột, có cấu trúc phân nhánh. Amylopectin giúp làm tăng độ dẻo của tinh bột, là thành phần chính trong gạo nếp (có nhiều amylopectin hơn gạo tẻ). → Đúng.
❌D. Saccharose: Là một disaccharide, không phải polysaccharide, không có cấu trúc phân nhánh. → Sai.
⟹Chọn đáp án C Đáp án: C
❌A. Cellulose: Là một polysaccharide cấu tạo từ β-glucose, có cấu trúc mạch thẳng, không phân nhánh. Cellulose chủ yếu có trong thành tế bào thực vật, không phải thành phần chính của tinh bột. → Sai.
❌B. Amylose: Là một polysaccharide có trong tinh bột, nhưng có cấu trúc mạch thẳng, không phân nhánh. Amylose có xu hướng tạo kết tinh nên làm giảm độ dẻo của tinh bột. → Sai.
✔️C. Amylopectin: Là một polysaccharide có trong tinh bột, có cấu trúc phân nhánh. Amylopectin giúp làm tăng độ dẻo của tinh bột, là thành phần chính trong gạo nếp (có nhiều amylopectin hơn gạo tẻ). → Đúng.
❌D. Saccharose: Là một disaccharide, không phải polysaccharide, không có cấu trúc phân nhánh. → Sai.
⟹Chọn đáp án C Đáp án: C
Câu 8 [1016559]: Cho dung dịch chứa các ion: Na+, Al3+, Cu2+, Cl-, SO42-, NO3-. Các ion không bị điện phân khi ở trạng thái dung dịch là
A, Na+, Al3+, SO42-, NO3-.
B, Na+, SO42-, Cl-, Al3+.
C, Na+, Al3+, Cl-, NO3-.
D, Al3+, Cu2+, Cl-, NO3-.
Các ion không bị điện phân trong dung dịch là Na+; Al3+; SO42-, NO3-
Trong điện phân dung dịch (với điện cực trơ như than chì hoặc platinum), chỉ một số ion bị điện phân, tùy thuộc vào thế oxi hóa - khử chuẩn và tính chất ưu tiên phóng điện.
Cation: Na+: Không bị điện phân trong dung dịch nước, vì nước ưu tiên bị khử hơn → tạo H2 (khử nước dễ hơn Na+). → Không bị điện phân.
Al3+: cũng như Na+, không bị điện phân trong dung dịch, vì khó khử hơn nước. → Không bị điện phân.
Cu2+: Bị khử dễ dàng hơn nước → bị điện phân tại cathode.
Anion: Cl-: Có thể bị oxi hóa tạo Cl2 nếu nồng độ Cl⁻ đủ cao.
Nhưng trong điều kiện bình thường, có thể xảy ra hoặc không, nhưng vẫn là ion có khả năng bị điện phân.
SO42-: Không bị oxi hóa được trong dung dịch → nước bị oxi hóa thành O2. → Không bị điện phân.
NO3-: Giống SO42-, không bị oxi hóa được, nên không bị điện phân. → Nước bị oxi hóa thay thế.
⟹ Chọn đáp án A Đáp án: A
Trong điện phân dung dịch (với điện cực trơ như than chì hoặc platinum), chỉ một số ion bị điện phân, tùy thuộc vào thế oxi hóa - khử chuẩn và tính chất ưu tiên phóng điện.
Cation: Na+: Không bị điện phân trong dung dịch nước, vì nước ưu tiên bị khử hơn → tạo H2 (khử nước dễ hơn Na+). → Không bị điện phân.
Al3+: cũng như Na+, không bị điện phân trong dung dịch, vì khó khử hơn nước. → Không bị điện phân.
Cu2+: Bị khử dễ dàng hơn nước → bị điện phân tại cathode.
Anion: Cl-: Có thể bị oxi hóa tạo Cl2 nếu nồng độ Cl⁻ đủ cao.
Nhưng trong điều kiện bình thường, có thể xảy ra hoặc không, nhưng vẫn là ion có khả năng bị điện phân.
SO42-: Không bị oxi hóa được trong dung dịch → nước bị oxi hóa thành O2. → Không bị điện phân.
NO3-: Giống SO42-, không bị oxi hóa được, nên không bị điện phân. → Nước bị oxi hóa thay thế.
⟹ Chọn đáp án A Đáp án: A
Câu 9 [585771]: Hiện tượng gì xảy ra khi thêm dung dịch ammonia vào dung dịch sắt(II) sulfate?
A, Xuất hiện bọt khí không màu.
B, Xuất hiện kết tủa trắng.
C, Xuất hiện kết tủa xanh lam.
D, Xuất hiện khói trắng.
Sục khí ammonia vào dung dịch sắt(II) sulfate tạo kết tủa trắng (Fe(OH)2) và dung dịch ammoni sunfate. Đáp án: B
Câu 10 [706132]: M là nguyên tố kim loại chuyển tiếp dãy thứ nhất, có một số đặc điểm sau:
• Nguyên tử M có 1 electron ở lớp ngoài cùng.
• Trong hợp chất, số oxi hoá phổ biến của nguyên tố M là +2.
M là nguyên tố nào sau đây?
• Nguyên tử M có 1 electron ở lớp ngoài cùng.
• Trong hợp chất, số oxi hoá phổ biến của nguyên tố M là +2.
M là nguyên tố nào sau đây?
A, Fe.
B, Ni.
C, Mn.
D, Cu.
- Kim loại chuyển tiếp dãy thứ nhất: Điều này giới hạn các nguyên tố M trong dãy từ Sc (Z=21) đến Zn (Z=30).
- Nguyên tử M có 1 electron ở lớp ngoài cùng: Điều này thường gặp ở các kim loại nhóm IB và một số kim loại nhóm VIB.
- Số oxi hóa phổ biến của M là +2: Điều này loại trừ một số kim loại như Mn (số oxi hóa phổ biến +2, +4, +7), Fe (số oxi hóa phổ biến +2, +3), Ni (số oxi hóa phổ biến +2, +3).
Phân tích các đáp án:
❌ A. Cấu hình electron: [Ar] 3d64s2. Fe có 2 electron ở lớp ngoài cùng , không thỏa mãn điều kiện. Số oxi hóa phổ biến của Fe là +2 và +3.
❌ B. Cấu hình electron: [Ar] 3d84s2. Ni có 2 electron ở lớp ngoài cùng , không thỏa mãn điều kiện. Số oxi hóa phổ biến của Ni là +2 và +3.
❌ C. Cấu hình electron: [Ar] 3d54s2. Mn có 2 electron ở lớp ngoài cùng , không thỏa mãn điều kiện. Số oxi hóa phổ biến của Mn là +2, +4, +7.
✔️ D. Cấu hình electron: [Ar] 3d104s1. Cu có 1 electron ở lớp ngoài cùng , thỏa mãn điều kiện. Số oxi hóa phổ biến của Cu là +1 và +2.
⟹Chọn đáp án D Đáp án: D
- Nguyên tử M có 1 electron ở lớp ngoài cùng: Điều này thường gặp ở các kim loại nhóm IB và một số kim loại nhóm VIB.
- Số oxi hóa phổ biến của M là +2: Điều này loại trừ một số kim loại như Mn (số oxi hóa phổ biến +2, +4, +7), Fe (số oxi hóa phổ biến +2, +3), Ni (số oxi hóa phổ biến +2, +3).
Phân tích các đáp án:
❌ A. Cấu hình electron: [Ar] 3d64s2. Fe có 2 electron ở lớp ngoài cùng , không thỏa mãn điều kiện. Số oxi hóa phổ biến của Fe là +2 và +3.
❌ B. Cấu hình electron: [Ar] 3d84s2. Ni có 2 electron ở lớp ngoài cùng , không thỏa mãn điều kiện. Số oxi hóa phổ biến của Ni là +2 và +3.
❌ C. Cấu hình electron: [Ar] 3d54s2. Mn có 2 electron ở lớp ngoài cùng , không thỏa mãn điều kiện. Số oxi hóa phổ biến của Mn là +2, +4, +7.
✔️ D. Cấu hình electron: [Ar] 3d104s1. Cu có 1 electron ở lớp ngoài cùng , thỏa mãn điều kiện. Số oxi hóa phổ biến của Cu là +1 và +2.
⟹Chọn đáp án D Đáp án: D
Câu 11 [306200]: Các hợp chất X, Y, Z (mạch hở, bền ở điều kiện thường) có cùng công thức phân tử C3H6O. Một số kết quả thí nghiệm với các chất trên được liệt kê ở bảng sau (Dấu – là không tác dụng).
![541516[de].png](https://asset.moon.vn/img/ai/Teachers/rongden_167/ProS2018/BAI%2018/541516[de].png)
Phát biểu nào sau đây là sai?
![541516[de].png](https://asset.moon.vn/img/ai/Teachers/rongden_167/ProS2018/BAI%2018/541516[de].png)
Phát biểu nào sau đây là sai?
A, X là prop-2-en-1-ol.
B, Z làm mất màu nước bromine.
C, Y là propanal.
D, X có phản ứng cộng dung dịch bromine.
HD: C3H6O có 3 đồng phân mạch hở, bền ở điều kiện thường là CH2=CH–CH2OH (alcohol); CH3CH2CHO (aldehyde) và CH3COCH3 (acetone).
♦ không phản ứng Na, AgNO3/NH3 ⇒ Z là acetone.
♦ không phản ứng Na, có phản ứng với AgNO3/NH3 → Ag ⇒ Y là andehyde C2H5CHO.
♦ phản ứng với Na, không + AgNO3/NH3 ⇒ X là alcohol CH2=CH–CH2OH.
Phân tích các phát biểu:
✔️A. Đúng. X có công thức cấu tạo là CH2=CH-CH2OH có tên gọi là prop-2-en-1-ol.
❌B. Sai. Z là acetone . Acetone thường không phản ứng lam mất màu nước bromine ở điều kiện thường.
✔️C. Đúng. Y có công thức cấu tạo là C2H5CHO có tên gọi là propanal.
✔️D. Đúng. X là prop-2-en-1-ol có chứa liên kết đôi C=C nên có phản ứng cộng bromine.
Chọn đáp án B
Đáp án: B
♦ không phản ứng Na, AgNO3/NH3 ⇒ Z là acetone.
♦ không phản ứng Na, có phản ứng với AgNO3/NH3 → Ag ⇒ Y là andehyde C2H5CHO.
♦ phản ứng với Na, không + AgNO3/NH3 ⇒ X là alcohol CH2=CH–CH2OH.
Phân tích các phát biểu:
✔️A. Đúng. X có công thức cấu tạo là CH2=CH-CH2OH có tên gọi là prop-2-en-1-ol.
❌B. Sai. Z là acetone . Acetone thường không phản ứng lam mất màu nước bromine ở điều kiện thường.
✔️C. Đúng. Y có công thức cấu tạo là C2H5CHO có tên gọi là propanal.
✔️D. Đúng. X là prop-2-en-1-ol có chứa liên kết đôi C=C nên có phản ứng cộng bromine.
Chọn đáp án B
Đáp án: B
Câu 12 [705956]: Potassium nitrate (diêm tiêu) được điều chế bằng cách pha trộn dung dịch KCl với dung dịch NaNO3, khi đó xảy ra sự trao đổi ion thuận nghịch giữa các muối:
KCl(aq) + X(aq) ⇌ KNO3(s) + NaCl(aq)
Cô đặc hỗn hợp phản ứng rồi làm lạnh, do độ tan của muối KNO3 nhỏ hơn so với các muối còn lại ở nhiệt độ thấp nên sẽ kết tinh trước và tách ra khỏi dung dịch. Công thức của chất X là
KCl(aq) + X(aq) ⇌ KNO3(s) + NaCl(aq)
Cô đặc hỗn hợp phản ứng rồi làm lạnh, do độ tan của muối KNO3 nhỏ hơn so với các muối còn lại ở nhiệt độ thấp nên sẽ kết tinh trước và tách ra khỏi dung dịch. Công thức của chất X là
A, NaNO3.
B, NaNO2.
C, NaClO.
D, NaClO3.
Phân tích các đáp án :
✔️A. NaNO3 + KCl ⟶ KNO3 + NaCl
❌B. NaNO2 + KCl . Không phản ứng do không chứa nhóm NO3-
❌C. NaClO + KCl . Không phản ứng do không chứa nhóm NO3-
❌D. NaClO3 + KCl . Không phản ứng do không chứa nhóm NO3-
⟹Chọn đáp án A
Đáp án: A
✔️A. NaNO3 + KCl ⟶ KNO3 + NaCl
❌B. NaNO2 + KCl . Không phản ứng do không chứa nhóm NO3-
❌C. NaClO + KCl . Không phản ứng do không chứa nhóm NO3-
❌D. NaClO3 + KCl . Không phản ứng do không chứa nhóm NO3-
⟹Chọn đáp án A
Đáp án: A
Câu 13 [1072950]: Sơ đồ biểu diễn một lò nung vôi được sử dụng để nung đá vôi đến nhiệt độ rất cao.
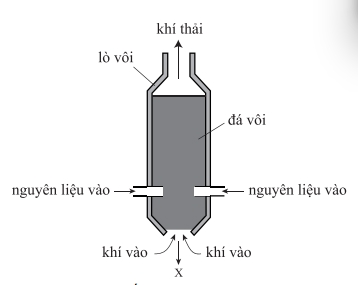
Chất X được đưa ra từ lò nung vôi là chất gì?

Chất X được đưa ra từ lò nung vôi là chất gì?
A, Calcium carbonate.
B, Calcium hydroxide.
C, Calcium oxide.
D, Calcium sulfate.
Quá trình nung vôi: 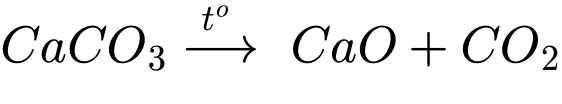
Chất X được đưa ra từ lò nung vôi là calcium oxide.
Đáp án: C. Calcium oxide. Đáp án: C
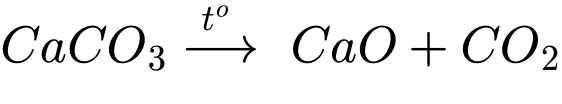
Chất X được đưa ra từ lò nung vôi là calcium oxide.
Đáp án: C. Calcium oxide. Đáp án: C
Câu 14 [310491]:
Polymer dùng để sản xuất tơ lapsan có cấu tạo như sau: 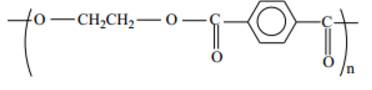
Tên gọi của polymer trên là
A, polyacrylonitrile.
B, poly(hexamethylene adipamide).
C, poly(ethylene terephthalate).
D, polycaproamide.
- Khi tiến hành đồng trùng ngưng ethylene glycol và terephthalic acid thu được polymer dùng để sản xuất tơ lapsan (poly(ethylene terephthalate))
- Polyethylene terephthalate, viết tắt là PET, PETE hay PETP, PET-P, là loại nhựa polymer nhiệt nhôm phổ biến nhất của polyester và được sử dụng trong sợi may quần áo, hộp đựng chất lỏng và thực phẩm, khuôn đúc nhựa và kết hợp với sợi thủy tinh sản xuất nhựa kỹ thuật.
⟹Chọn đáp án C Đáp án: C
- Polyethylene terephthalate, viết tắt là PET, PETE hay PETP, PET-P, là loại nhựa polymer nhiệt nhôm phổ biến nhất của polyester và được sử dụng trong sợi may quần áo, hộp đựng chất lỏng và thực phẩm, khuôn đúc nhựa và kết hợp với sợi thủy tinh sản xuất nhựa kỹ thuật.
⟹Chọn đáp án C Đáp án: C
Câu 15 [705766]: Chuẩn bị các khuôn gỗ có kích thước 58 cm × 80 cm × 5 cm, ở giữa có đặt tấm thuỷ tinh được quét mỡ lợn cả hai mặt, mỗi lớp dày 3 mm. Đặt lên trên bề mặt chất béo một lớp lụa mỏng rồi rải lên trên 30 – 80 g hoa tươi khô ráo, không bị dập nát. Khoảng 30 – 40 khuôn gỗ được xếp chồng lên nhau rồi để trong phòng kín. Sau khoảng 24 – 72 giờ (tuỳ từng loại hoa), người ta thay lớp hoa mới cho đến khi lớp chất béo bão hoà tinh dầu.Phát biểu nào sau đây không đúng?
A, Quy trình trên sử dụng phương pháp chiết để lấy tinh dầu từ hoa.
B, Vai trò của chất béo (mỡ lợn) trong quy trình là làm dung môi hòa tan tinh dầu.
C, Có thể thay chất béo bằng các dung môi nước để hòa tan tinh dầu.
D, Khi đun nóng, chất béo có thể hòa tan lượng tinh dầu lớn hơn.
Phân tích các phát biểu:
✅ A. Đúng. Đây là phương pháp hấp phụ bằng chất béo lạnh, một dạng của phương pháp chiết xuất tinh dầu.
✅ B. Đúng. Chất béo có tính kỵ nước cao nên có thể hòa tan tinh dầu từ hoa một cách hiệu quả.
❌ C. Sai. Tinh dầu là hợp chất không phân cực, không tan trong nước mà tan tốt trong dung môi hữu cơ hoặc chất béo. Do đó, nước không thể thay thế chất béo trong quy trình này.
✅ D. Đúng. Khi đun nóng, chất béo giảm độ nhớt, tăng khả năng hòa tan tinh dầu. Tuy nhiên, phương pháp enfleurage thường không đun nóng để bảo vệ hương thơm tinh tế của tinh dầu.
⇒ Chọn đáp án C Đáp án: C
✅ A. Đúng. Đây là phương pháp hấp phụ bằng chất béo lạnh, một dạng của phương pháp chiết xuất tinh dầu.
✅ B. Đúng. Chất béo có tính kỵ nước cao nên có thể hòa tan tinh dầu từ hoa một cách hiệu quả.
❌ C. Sai. Tinh dầu là hợp chất không phân cực, không tan trong nước mà tan tốt trong dung môi hữu cơ hoặc chất béo. Do đó, nước không thể thay thế chất béo trong quy trình này.
✅ D. Đúng. Khi đun nóng, chất béo giảm độ nhớt, tăng khả năng hòa tan tinh dầu. Tuy nhiên, phương pháp enfleurage thường không đun nóng để bảo vệ hương thơm tinh tế của tinh dầu.
⇒ Chọn đáp án C Đáp án: C
Câu 16 [705992]: Cho hai quá trình sau:
[Cu(OH2)6]2+(aq) + 2NH3(aq) [Cu(NH3)2(OH2)4]2+(aq) + 2H2O(l)
[Cu(OH2)6]2+(aq) + en(aq) [Cu(en)(OH2)4]2+(aq) + 2H2O(l)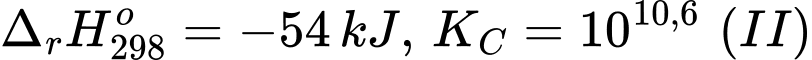
Trong đó, en là ethylenediamine. Phân tử này đã dùng tất cả các cặp electron hoá trị riêng để tạo liên kết cho – nhận với cation Cu2+. Cho các phát biểu sau:
(a) Quá trình (II) thuận lợi hơn quá trình (I) về năng lượng.
(b) Sự thế H2O trong phức chất [Cu(OH2)6]2+ bởi NH3 tạo ra phức chất bền hơn so với sự thế H2O trong phức chất [Cu(OH2)6]2+ bởi en.
(c) Xung quanh nguyên tử trung tâm trong phức chất [Cu(NH3)2(OH2)4]2+ và trong phức chất [Cu(en)(OH2)4]2+ đều có 6 liên kết σ.
(d) Phản ứng diễn ra ở quá trình (I) và (II) đều có sự tạo thành phức chất không tan và có sự biến đổi màu sắc.Các phát biểu đúng là
[Cu(OH2)6]2+(aq) + 2NH3(aq) [Cu(NH3)2(OH2)4]2+(aq) + 2H2O(l)

[Cu(OH2)6]2+(aq) + en(aq) [Cu(en)(OH2)4]2+(aq) + 2H2O(l)
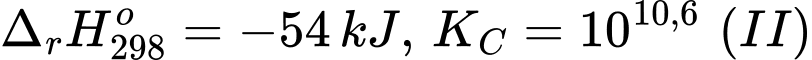
Trong đó, en là ethylenediamine. Phân tử này đã dùng tất cả các cặp electron hoá trị riêng để tạo liên kết cho – nhận với cation Cu2+. Cho các phát biểu sau:
(a) Quá trình (II) thuận lợi hơn quá trình (I) về năng lượng.
(b) Sự thế H2O trong phức chất [Cu(OH2)6]2+ bởi NH3 tạo ra phức chất bền hơn so với sự thế H2O trong phức chất [Cu(OH2)6]2+ bởi en.
(c) Xung quanh nguyên tử trung tâm trong phức chất [Cu(NH3)2(OH2)4]2+ và trong phức chất [Cu(en)(OH2)4]2+ đều có 6 liên kết σ.
(d) Phản ứng diễn ra ở quá trình (I) và (II) đều có sự tạo thành phức chất không tan và có sự biến đổi màu sắc.Các phát biểu đúng là
A, (a), (c).
B, (b), (c).
C, (a), (b), (c).
D, (b), (c), (d).
Phân tích các phát biểu :
✔️(a) – Đúng. Quá trình (II) thuận lợi hơn quá trình (I) về mặt năng lượng do có lượng năng lượng tỏa ra lớn hơn và hằng số cân bằng lớn hơn.
❌(b) – Sai. Sự thế H2O trong phức chất [Cu(OH2)6]2+ bởi NH3 tạo ra phức chất không bền so với sự thế H2O trong phức chất [Cu(OH2)6]2+ bởi en do có hằng số cân bằng 107,7 nhỏ hơn 1010,6 của quá trình (II)
✔️(c) – Đúng. Xung quanh nguyên tử trung tâm trong phức chất [Cu(NH3)2(OH2)4]2+ và trong phức chất [Cu(en) (OH2)4]2+ đều có 6 liên kết σ, xung quanh nguyên tử trung tâm đều có 6 liên kết cho nhận, NH3 và H2O có dung lượng phối trí là 1 và en có dung lượng phối trí là 2.
❌(d) – Sai. Cả hai quá trình đều tạo ra phức chất tan trong dung dịch. Tuy nhiên, chúng có sự biến đổi màu sắc, do sự thay đổi phối tử xung quanh ion Cu2+
⟹ Có 2 phát biểu đúng là (a),(c)
⟹ Chọn đáp án A Đáp án: A
✔️(a) – Đúng. Quá trình (II) thuận lợi hơn quá trình (I) về mặt năng lượng do có lượng năng lượng tỏa ra lớn hơn và hằng số cân bằng lớn hơn.
❌(b) – Sai. Sự thế H2O trong phức chất [Cu(OH2)6]2+ bởi NH3 tạo ra phức chất không bền so với sự thế H2O trong phức chất [Cu(OH2)6]2+ bởi en do có hằng số cân bằng 107,7 nhỏ hơn 1010,6 của quá trình (II)
✔️(c) – Đúng. Xung quanh nguyên tử trung tâm trong phức chất [Cu(NH3)2(OH2)4]2+ và trong phức chất [Cu(en) (OH2)4]2+ đều có 6 liên kết σ, xung quanh nguyên tử trung tâm đều có 6 liên kết cho nhận, NH3 và H2O có dung lượng phối trí là 1 và en có dung lượng phối trí là 2.
❌(d) – Sai. Cả hai quá trình đều tạo ra phức chất tan trong dung dịch. Tuy nhiên, chúng có sự biến đổi màu sắc, do sự thay đổi phối tử xung quanh ion Cu2+
⟹ Có 2 phát biểu đúng là (a),(c)
⟹ Chọn đáp án A Đáp án: A
Sử dụng thông tin ở bảng dưới đây để trả lời câu 17 và câu 18:
Cho giá trị thế điện cực chuẩn của một số cặp oxi hóa – khử trong bảng sau:
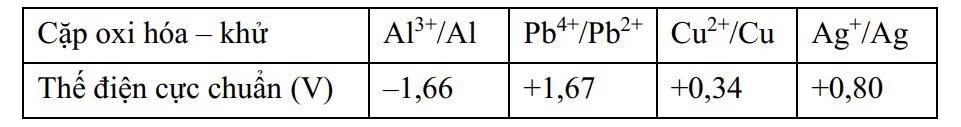

Câu 17 [703828]: Phản ứng hóa học nào sau đây không xảy ra?
A, 2Al(s) + 3Cu2+(aq)  2Al3+(aq) + 3Cu(s).
2Al3+(aq) + 3Cu(s).
 2Al3+(aq) + 3Cu(s).
2Al3+(aq) + 3Cu(s).B, Cu(s) + 2Ag+(aq)  Cu2+(aq) + 2Ag(s).
Cu2+(aq) + 2Ag(s).
 Cu2+(aq) + 2Ag(s).
Cu2+(aq) + 2Ag(s).C, 2Ag+(aq) + Pb2+(aq)  Pb4+(aq) + 2Ag(s).
Pb4+(aq) + 2Ag(s).
 Pb4+(aq) + 2Ag(s).
Pb4+(aq) + 2Ag(s).D, Cu(s) + Pb4+(aq)  Cu2+(aq) + Pb2+(aq).
Cu2+(aq) + Pb2+(aq).
 Cu2+(aq) + Pb2+(aq).
Cu2+(aq) + Pb2+(aq).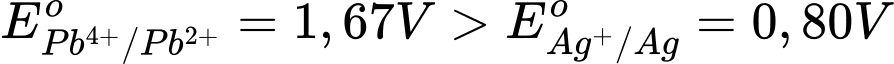
→ Theo quy tắc 𝞪, dạng oxi hóa mạnh sẽ phản ứng với dạng khử mạnh.
2Ag(s) + Pb4+(aq) ⟶ Pb2+(aq) + 2Ag+(aq).
⟹ Chọn đáp án C Đáp án: C
Câu 18 [703829]: Sức điện động chuẩn lớn nhất của pin Galvani thiết lập từ hai cặp oxi hóa – khử trong số các cặp trên là
A, 1,67 V.
B, 4,05 V.
C, 2,46 V.
D, 3,33 V.
Cặp oxi hóa - khử tạo pin galvani có sức điện động lớn nhất là Al3+/Al và Pb4+/Pb2+.
Phản ứng trong pin galvani:
2Al(s) + 3Pb4+(aq) ⟶ 2Al3+(aq) + 3Pb2+(aq)
Cathode (-): Pb4+(aq) + 2e ⟶ Pb2+(aq)
Anode (+): Al(s) ⟶ Al3+ + 3e
→ Epin = E(+) – E(-) = 1,67 – (–1,66) = 3,33 V
⇒ Chọn đáp án D Đáp án: D
Phản ứng trong pin galvani:
2Al(s) + 3Pb4+(aq) ⟶ 2Al3+(aq) + 3Pb2+(aq)
Cathode (-): Pb4+(aq) + 2e ⟶ Pb2+(aq)
Anode (+): Al(s) ⟶ Al3+ + 3e
→ Epin = E(+) – E(-) = 1,67 – (–1,66) = 3,33 V
⇒ Chọn đáp án D Đáp án: D
PHẦN II. Thí sinh trả lời từ câu 1 đến câu 4. Trong mỗi ý a), b), c), d) ở mỗi câu, thí sinh chọn đúng hoặc sai.
Câu 19 [560700]: Iron được chiết xuất từ quặng hematite (thành phần chính là Fe2O3, ngoài ra còn có sillic dioxide). Nguyên liệu ban đầu gồm có quặng hematite, than cốc và chất phụ gia như đá vôi sẽ sản xuất được hợp kim quan trọng của iron là gang. Quá trình luyện gang trong lò cao với 3 phản ứng chính:
- Phản ứng tạo chất khử CO (1).
- Phản ứng CO khử iron oxide thành iron (2).
- Phản ứng tạo thành xỉ giữa calcium oxide và sillic dioxide (3).
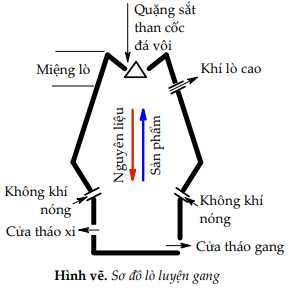
- Phản ứng tạo chất khử CO (1).
- Phản ứng CO khử iron oxide thành iron (2).
- Phản ứng tạo thành xỉ giữa calcium oxide và sillic dioxide (3).

Giai đoạn 1:
C + O2 ⟶ CO2
C + O2 ⟶ CO
Giai đoạn 2 :
3CO + Fe2O3 ⟶ 2Fe + 3CO2
C tăng số oxi hóa trong các giai đoạn ⟶ nhường e
Phân tích các đáp án:
✔️A – Đúng. Phản ứng xảy ra ở (2) là
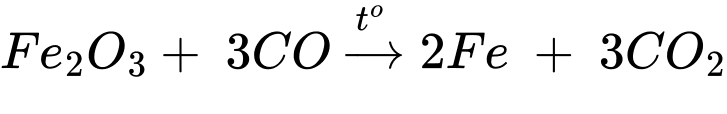
❌B – Sai. Carbon đóng vai trò là chất nhường electron do là chất khử.
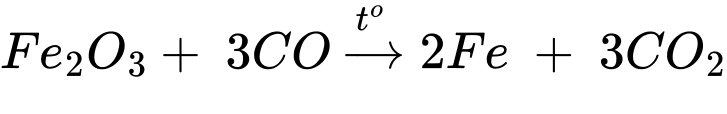
Quá trình oxi hóa: C2+ → C4+ + 2e
Quá trình khử: Fe3+ + 3e → Fe
✔️C – Đúng. Phản ứng tạo thành xỉ là CaO + SiO2 → CaSiO3
✔️D – Đúng. Vai trò của đá vôi là loại bỏ tạp chất sillic dioxide (SiO2) có trong quặng theo quá trình:
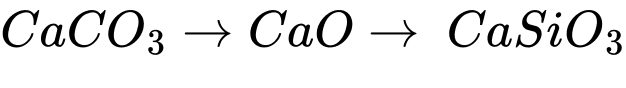
C + O2 ⟶ CO2
C + O2 ⟶ CO
Giai đoạn 2 :
3CO + Fe2O3 ⟶ 2Fe + 3CO2
C tăng số oxi hóa trong các giai đoạn ⟶ nhường e
Phân tích các đáp án:
✔️A – Đúng. Phản ứng xảy ra ở (2) là
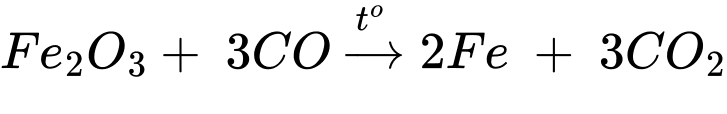
❌B – Sai. Carbon đóng vai trò là chất nhường electron do là chất khử.
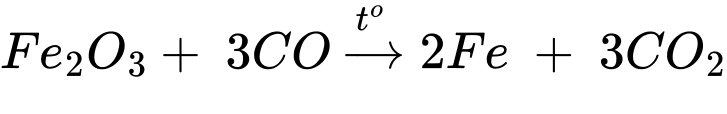
Quá trình oxi hóa: C2+ → C4+ + 2e
Quá trình khử: Fe3+ + 3e → Fe
✔️C – Đúng. Phản ứng tạo thành xỉ là CaO + SiO2 → CaSiO3
✔️D – Đúng. Vai trò của đá vôi là loại bỏ tạp chất sillic dioxide (SiO2) có trong quặng theo quá trình:
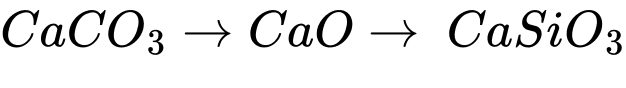
Câu 20 [705996]: Trong phòng thí nghiệm, phương pháp phổ biến nhất là chiết lỏng – lỏng, một quá trình diễn ra trong phễu tách. Một dung dịch chứa các thành phần hòa tan được đặt trong phễu và một dung môi không trộn lẫn được thêm vào, tạo thành hai lớp được lắc cùng nhau. Một lớp thường là nước và lớp còn lại là dung môi hữu cơ. Các thành phần được "chiết xuất" khi chúng di chuyển từ lớp này sang lớp kia. Hình dạng của phễu tách cho phép thoát nước và tách hai lớp hiệu quả.
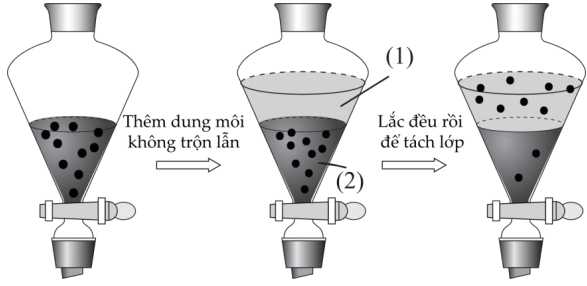

Phân tích các phát biểu :
❌(a) – Sai. Tiến hành mở van thì lớp dung môi (2) sẽ chảy ra trước, lớp (2) ở phía dưới nên khí mở van sẻ chảy xuống dưới.
✔️(b) – Đúng. Dung môi không phân cực là chất lỏng không có momen lưỡng cực. Do đó, các dung môi này không chứa một phần điện tích dương hoặc âm. Chính vì lý do này, các dung môi phân cực sẽ không bao giờ có thể hòa tan được với những hợp chất phân cực vì không có điện tích trái dấu để thu hút hợp chất phân cực.Dung môi không phân cực trong hóa học có thể hòa tan được với những hợp chất không phân cực thông qua một lực đó là lực hút, chẳng hạn như lực Van der Waal. Một số ví dụ về dung môi không phân cực bao gồm pentane, hexane, benzene, toluene, v.v.
✔️(c) – Đúng. Sau khi chiết, mật độ chất tan ở lớp dung môi (1) lớn hơn lớp dung môi (2), chất tan trong dung dịch (2) sau khi lắc đã hòa tan lên dung dịch (1).
✔️(d) – Đúng.Nếu chất tan trong dung dịch nước là iodine thì lớp dung môi (1) là dung môi hữu cơ không phân cực. Iodine ít tan trong nước nhưng tan nhiều trong các dung môi hữu cơ như cồn, benzene, chloroform.
❌(a) – Sai. Tiến hành mở van thì lớp dung môi (2) sẽ chảy ra trước, lớp (2) ở phía dưới nên khí mở van sẻ chảy xuống dưới.
✔️(b) – Đúng. Dung môi không phân cực là chất lỏng không có momen lưỡng cực. Do đó, các dung môi này không chứa một phần điện tích dương hoặc âm. Chính vì lý do này, các dung môi phân cực sẽ không bao giờ có thể hòa tan được với những hợp chất phân cực vì không có điện tích trái dấu để thu hút hợp chất phân cực.Dung môi không phân cực trong hóa học có thể hòa tan được với những hợp chất không phân cực thông qua một lực đó là lực hút, chẳng hạn như lực Van der Waal. Một số ví dụ về dung môi không phân cực bao gồm pentane, hexane, benzene, toluene, v.v.
✔️(c) – Đúng. Sau khi chiết, mật độ chất tan ở lớp dung môi (1) lớn hơn lớp dung môi (2), chất tan trong dung dịch (2) sau khi lắc đã hòa tan lên dung dịch (1).
✔️(d) – Đúng.Nếu chất tan trong dung dịch nước là iodine thì lớp dung môi (1) là dung môi hữu cơ không phân cực. Iodine ít tan trong nước nhưng tan nhiều trong các dung môi hữu cơ như cồn, benzene, chloroform.
Câu 21 [705483]: Tiến hành các thí nghiệm:
▪ Bước 1: Cho vào ống nghiệm khoảng 1 mL dung dịch Na2CO3. Dùng giấy chỉ thị pH để kiểm tra môi trường dung dịch.
▪ Bước 2: Thêm tiếp 2 mL dung dịch HCl vào ống nghiệm, lắc đều, đưa que diêm đang cháy đến miệng ống nghiệm.
▪ Bước 1: Cho vào ống nghiệm khoảng 1 mL dung dịch Na2CO3. Dùng giấy chỉ thị pH để kiểm tra môi trường dung dịch.
▪ Bước 2: Thêm tiếp 2 mL dung dịch HCl vào ống nghiệm, lắc đều, đưa que diêm đang cháy đến miệng ống nghiệm.
Bước 1:
- Dung dịch Na2CO3 là muối của acid yếu (H2CO3) và base mạnh (NaOH), nên có tính base yếu.
- Khi dùng giấy chỉ thị pH, nó sẽ chuyển sang màu đặc trưng cho môi trường base (thường là xanh hoặc xanh lục tùy loại giấy).
Bước 2:
- Khi thêm HCl vào dung dịch Na2CO3, xảy ra phản ứng:
Na2CO3 + 2HCl → 2NaCl + CO2 + H2O
→ Có khí CO2 thoát ra, không tạo kết tủa.
- Khi đưa que diêm đang cháy đến miệng ống nghiệm, khí CO2 sinh ra không duy trì sự cháy, nên que diêm tắt.
Phân tích các phát biểu:
❌ (a) Sai. Dung dịch Na2CO3 có tính base yếu, giấy chỉ thị pH sẽ chuyển sang màu xanh đặc trưng cho môi trường base.
❌ (b) Sai. Phản ứng tạo ra khí CO2 và nước, không có kết tủa:
2HCl + Na2CO3 → 2NaCl + H2O + CO2
✔️ (c) Đúng. Khí sinh ra sau phản ứng là CO2 không duy trì sự sống và sự cháy.
✔️ (d) Đúng. Khi cho acid (chứa ion H+) vào dung dịch có ion CO32-, sẽ xảy ra phản ứng tạo khí CO2 bay lên.
- Dung dịch Na2CO3 là muối của acid yếu (H2CO3) và base mạnh (NaOH), nên có tính base yếu.
- Khi dùng giấy chỉ thị pH, nó sẽ chuyển sang màu đặc trưng cho môi trường base (thường là xanh hoặc xanh lục tùy loại giấy).
Bước 2:
- Khi thêm HCl vào dung dịch Na2CO3, xảy ra phản ứng:
Na2CO3 + 2HCl → 2NaCl + CO2 + H2O
→ Có khí CO2 thoát ra, không tạo kết tủa.
- Khi đưa que diêm đang cháy đến miệng ống nghiệm, khí CO2 sinh ra không duy trì sự cháy, nên que diêm tắt.
Phân tích các phát biểu:
❌ (a) Sai. Dung dịch Na2CO3 có tính base yếu, giấy chỉ thị pH sẽ chuyển sang màu xanh đặc trưng cho môi trường base.
❌ (b) Sai. Phản ứng tạo ra khí CO2 và nước, không có kết tủa:
2HCl + Na2CO3 → 2NaCl + H2O + CO2
✔️ (c) Đúng. Khí sinh ra sau phản ứng là CO2 không duy trì sự sống và sự cháy.
✔️ (d) Đúng. Khi cho acid (chứa ion H+) vào dung dịch có ion CO32-, sẽ xảy ra phản ứng tạo khí CO2 bay lên.
Câu 22 [705916]: Tiến hành thí nghiệm theo bước sau:
∎ Bước 1: Cho vào ống nghiệm 1 mL dung dịch hồ tinh bột, thêm vài giọt dung dịch I2 trong dung dịch KI. Lắc đều ống nghiệm.
∎ Bước 2: Đun nóng dung dịch trong ống nghiệm.
∎ Bước 3: Sau đó để nguội dung dịch trong ống nghiệm.
∎ Bước 1: Cho vào ống nghiệm 1 mL dung dịch hồ tinh bột, thêm vài giọt dung dịch I2 trong dung dịch KI. Lắc đều ống nghiệm.
∎ Bước 2: Đun nóng dung dịch trong ống nghiệm.
∎ Bước 3: Sau đó để nguội dung dịch trong ống nghiệm.
Phản ứng giữa hồ tinh bột với dung dịch iod tạo màu xanh tím đặc trưng (còn được gọi là phản ứng màu của iodine với hồ tinh bột). Đây là phản ứng dùng để nhận biết tinh bột. Phân tử tinh bột hấp phụ iodine tạo ra dung dịch có màu xanh tím. Khi đun nóng, iodine bị giải phóng ra khỏi phân tử tinh bột làm mất màu xanh tím.
Phân tích các phát biểu:
✔️A – Đúng. I2 tan kém trong nước nên phải dùng dung dịch KI, tạo dung dịch KI3 theo phương trình:
I2 + KI → KI3
✔️B – Đúng. Hồ tinh bột chứa amylose, một loại polysaccharid có cấu trúc xoắn. I2 bị giữ trong cấu trúc xoắn này, tạo thành phức chất màu xanh tím đặc trưng.
✔️C – Đúng. Khi đun nóng, các liên kết hydro trong cấu trúc xoắn của amylose bị phá vỡ, làm mạch amylose duỗi thẳng. I2 được giải phóng khỏi cấu trúc xoắn, dẫn đến mất màu xanh tím.
✔️D – Đúng. Khi để nguội, các liên kết hydro trong amylose hình thành trở lại, làm mạch amylose xoắn lại. I2 lại bị giữ trong cấu trúc xoắn, màu xanh tím xuất hiện trở lại.
Phân tích các phát biểu:
✔️A – Đúng. I2 tan kém trong nước nên phải dùng dung dịch KI, tạo dung dịch KI3 theo phương trình:
I2 + KI → KI3
✔️B – Đúng. Hồ tinh bột chứa amylose, một loại polysaccharid có cấu trúc xoắn. I2 bị giữ trong cấu trúc xoắn này, tạo thành phức chất màu xanh tím đặc trưng.
✔️C – Đúng. Khi đun nóng, các liên kết hydro trong cấu trúc xoắn của amylose bị phá vỡ, làm mạch amylose duỗi thẳng. I2 được giải phóng khỏi cấu trúc xoắn, dẫn đến mất màu xanh tím.
✔️D – Đúng. Khi để nguội, các liên kết hydro trong amylose hình thành trở lại, làm mạch amylose xoắn lại. I2 lại bị giữ trong cấu trúc xoắn, màu xanh tím xuất hiện trở lại.
PHẦN III. Thí sinh trả lời từ câu 1 đến 6. Thí sinh điền kết quả mỗi câu vào mỗi ô trả lời tương ứng theo hướng dẫn của phiếu trả lời.
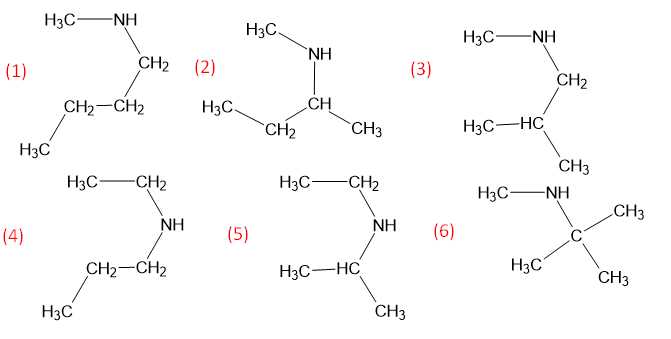
Câu 23 [704016]: Cho biết có bao nhiêu amine bậc hai có công thức phân tử C5H13N?
Amine bậc hai có công thức phân tử C5H13N có 6 đồng phân cấu tạo như sau:
⇒ Điền đáp án: 6

⇒ Điền đáp án: 6
Câu 24 [560952]: Trong các chất: phân bón ammonium sulfate, muối ăn, đá vôi, vôi sống, vôi tôi, soda, baking soda, phèn nhôm, phèn sắt có bao nhiêu chất có thể được dùng để làm tăng pH của đất có tính chua (pH = 3)?
Điền đáp án: ..........
Điền đáp án: ..........
Để làm tăng pH của đất có tính chua (pH = 3), ta cần sử dụng các chất có tính kiềm hoặc trung hòa tính acid của đất.
1. Phân bón ammonium sulfate (NH4)2SO4 là chất có tính acid khi tan trong nước, làm tăng tính acid của đất => pH giảm.
2. Muối ăn NaCl là muối trung tính, không ảnh hưởng đáng kể đến pH của đất => không ảnh hưởng tới pH.
3. Đá vôi CaCO3 là chất có tính kiềm yếu, có khả năng ổn định pH trong đất => tăng pH.
4. Vôi sống CaO là oxit bazơ mạnh, phản ứng với nước tạo thành Ca(OH)2, có tính kiềm mạnh, trung hòa acid hiệu quả => tăng pH.
5. Vôi tôi Ca(OH)2 là bazơ mạnh, có khả năng trung hòa acid => tăng pH.
6. Soda Na2CO3 là muối có tính kiềm, tan trong nước tạo môi trường base, có thể trung hòa acid => tăng pH.
7. Baking soda NaHCO3 là muối axit yếu, nhưng có tính kiềm nhẹ, có thể trung hòa acid yếu => tăng pH.
8. Phèn nhôm KAl(SO4)2⋅12H2O. Khi tan trong nước, giải phóng ion H+ làm tăng tính acid của đất => giảm pH
- Al3+ + H2O → Al(OH)2+ + H+
9. Phèn sắt FeSO4⋅7H2O.Khi tan trong nước, giải phóng ion H+ làm tăng tính acid của đất => giảm pH.
- Fe2+ + H2O → FeOH+ + H+
=> Các chất có thể làm tăng pH của đất là: 3,4,5,6,7
Điền đáp án: 5
1. Phân bón ammonium sulfate (NH4)2SO4 là chất có tính acid khi tan trong nước, làm tăng tính acid của đất => pH giảm.
2. Muối ăn NaCl là muối trung tính, không ảnh hưởng đáng kể đến pH của đất => không ảnh hưởng tới pH.
3. Đá vôi CaCO3 là chất có tính kiềm yếu, có khả năng ổn định pH trong đất => tăng pH.
4. Vôi sống CaO là oxit bazơ mạnh, phản ứng với nước tạo thành Ca(OH)2, có tính kiềm mạnh, trung hòa acid hiệu quả => tăng pH.
5. Vôi tôi Ca(OH)2 là bazơ mạnh, có khả năng trung hòa acid => tăng pH.
6. Soda Na2CO3 là muối có tính kiềm, tan trong nước tạo môi trường base, có thể trung hòa acid => tăng pH.
7. Baking soda NaHCO3 là muối axit yếu, nhưng có tính kiềm nhẹ, có thể trung hòa acid yếu => tăng pH.
8. Phèn nhôm KAl(SO4)2⋅12H2O. Khi tan trong nước, giải phóng ion H+ làm tăng tính acid của đất => giảm pH
- Al3+ + H2O → Al(OH)2+ + H+
9. Phèn sắt FeSO4⋅7H2O.Khi tan trong nước, giải phóng ion H+ làm tăng tính acid của đất => giảm pH.
- Fe2+ + H2O → FeOH+ + H+
=> Các chất có thể làm tăng pH của đất là: 3,4,5,6,7
Điền đáp án: 5
Câu 25 [560963]: Khí ammonia có thể được điều chế bằng phản ứng sau:
CaO(s) + 2NH4Cl(s)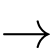 2NH3(g) + H2O(g) + CaCl2(s)
2NH3(g) + H2O(g) + CaCl2(s)
Nếu trộn 112 gam CaO và 224 gam NH4Cl để thực hiện phản ứng nhưng chỉ thu được 16,3 gam NH3 thì hiệu suất của phản ứng là bao nhiêu? (làm tròn đến hàng đơn vị)
Điền đáp án: ..........
CaO(s) + 2NH4Cl(s)
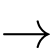 2NH3(g) + H2O(g) + CaCl2(s)
2NH3(g) + H2O(g) + CaCl2(s)Nếu trộn 112 gam CaO và 224 gam NH4Cl để thực hiện phản ứng nhưng chỉ thu được 16,3 gam NH3 thì hiệu suất của phản ứng là bao nhiêu? (làm tròn đến hàng đơn vị)
Điền đáp án: ..........
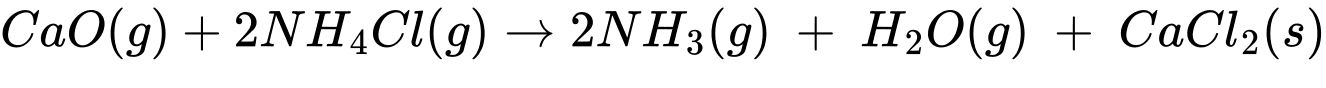
Số mol của CaO và NH4Cl lần lượt là
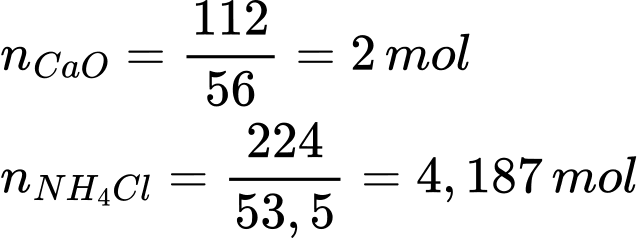
Ta có:
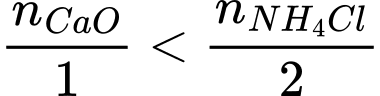
→ CaO hết, NH4Cl dư
Từ phương trình hóa học số mol của NH3 là: nNH3 = 2nCaO = 4 mol
Hiệu suất của phản ứng là:
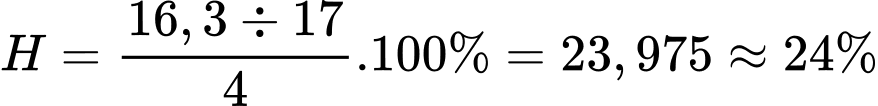
⇒ Điền đáp án: 24
Câu 26 [705978]: Thymol là thành phần quan trọng của cây húng tây có thể được chiết xuất bằng cách cho tác dụng với NaOH.
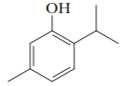
Tỉ lệ phản ứng tối đa của Thymol với NaOH là 1 : x. Giá trị của x là bao nhiêu?

Tỉ lệ phản ứng tối đa của Thymol với NaOH là 1 : x. Giá trị của x là bao nhiêu?
Thymol có 1 nhóm OH gắn vào vòng thơm nên là hợp chất của phenol
Thymol sẽ tác dụng với NaOH theo tỉ lệ 1:1.
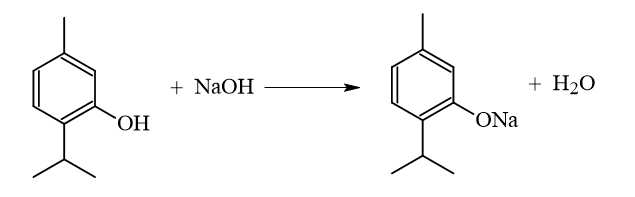
⟹Điền đáp án : 1
Thymol sẽ tác dụng với NaOH theo tỉ lệ 1:1.

⟹Điền đáp án : 1
Câu 27 [706230]: Nitrogen là nguyên tố dinh dưỡng khoáng thiết yếu trong cây, là thành phần cấu tạo nên nhiều hợp chất quan trọng. Đơn chất nitrogen (N2) có rất nhiều trong thành phần không khí, chiếm 78 % về thể tích. Tuy nhiên do năng lượng liên kết ba trong N≡N rất lớn nên N2 tương đối bền và trơ, dẫn tới cây trồng không thể sử dụng nguồn nitrogen này. Thông qua phản ứng của nitrogen với hydrogen tổng hợp NH3:
N2(g) + 3H2(g) 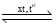 2NH3(g).
2NH3(g).
Cho giá trị năng lượng liên kết của EN–H (trong phân tử NH3) = 391 kJ.mol–1; EH–H = 436 kJ.mol–1 và biến thiên enthalpy tạo thành chuẩn của phản ứng là –93 kJ. Tính năng lượng liên kết của N≡N theo đơn vị kJ.mol–1. 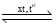 2NH3(g).
2NH3(g).
N2 + 3H2 ⇌ 2NH3
Biến thiên enthalpy của phản ứng là:
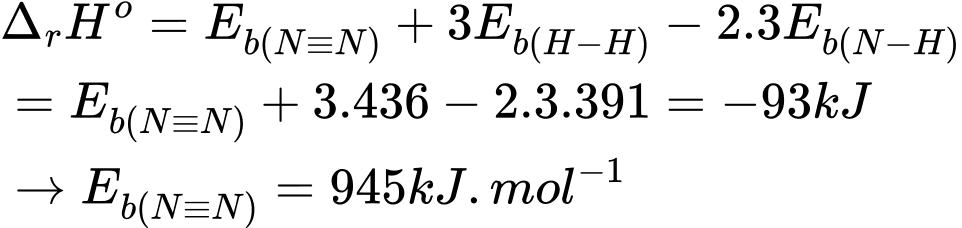
⟹ Điền đáp án: 945
Biến thiên enthalpy của phản ứng là:
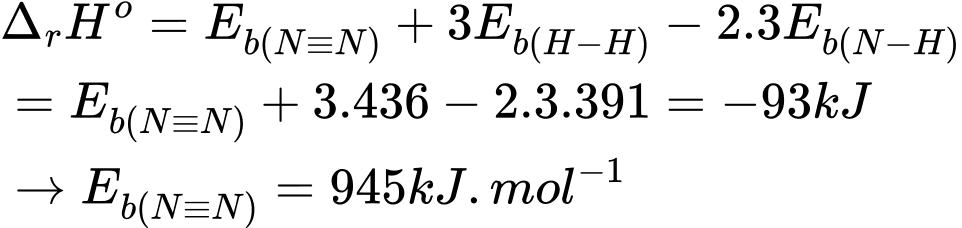
⟹ Điền đáp án: 945
Câu 28 [706028]: Công nghệ Solvay là phương pháp phổ biến nhất hiện nay để sản xuất soda (tên thông thường của Na2CO3). Công nghệ Solvay. Các giai đoạn sản xuất như sau:
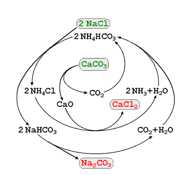
- Giai đoạn 1: Hòa tan bão hòa NaCl trong dung dịch NH3 đặc.
- Giai đoạn 2: Nung CaCO3 ở 950°C - 1100°C rồi dẫn khí thoát ra vào dung dịch bão hòa của NaCl trong NH3 đặc ở trên, thu được NaHCO3 và NH4Cl. Các khí CO2, NH3 dư bay lên được tuần hoàn trở lại.
- Giai đoạn 3: Tách NaHCO3 khỏi dung dịch nhờ tính tan. Nung NaHCO3 ở nhiệt độ 450°C - 500°C thu được Na2CO3.
Cho biết hiệu suất của toàn bộ quá trình là 85%. Từ nguyên liệu ban đầu là 50 kg NaCl thu được tối đa bao nhiêu kg Na2CO3 (làm tròn đến hàng phần mười)?

- Giai đoạn 1: Hòa tan bão hòa NaCl trong dung dịch NH3 đặc.
- Giai đoạn 2: Nung CaCO3 ở 950°C - 1100°C rồi dẫn khí thoát ra vào dung dịch bão hòa của NaCl trong NH3 đặc ở trên, thu được NaHCO3 và NH4Cl. Các khí CO2, NH3 dư bay lên được tuần hoàn trở lại.
- Giai đoạn 3: Tách NaHCO3 khỏi dung dịch nhờ tính tan. Nung NaHCO3 ở nhiệt độ 450°C - 500°C thu được Na2CO3.
Cho biết hiệu suất của toàn bộ quá trình là 85%. Từ nguyên liệu ban đầu là 50 kg NaCl thu được tối đa bao nhiêu kg Na2CO3 (làm tròn đến hàng phần mười)?
Giai đoạn 1: Hòa tan bão hòa NaCl trong dung dịch NH3 đặc.
Giai đoạn 2: Nung CaCO3 ở 950 - 1100 oC rồi dẫn khí thoát ra vào dung dịch bão hòa của NaCl trong NH3, thực tế trong công nghiệp người ta sử dụng các phản ứng này[1]:
CaCO3 → CaO + CO2
NaCl + NH3 + CO2 + H2O → NaHCO3 + NH4Cl
Giai đoạn 3: Tách NaHCO3 khỏi dung dịch nhờ tính tan. Nung NaHCO3 ở nhiệt độ 450 - 500 oC thu được soda:
2NaHCO3 → Na2CO3 + CO2 + H2O
Đổi 50 kg = 50000 gam
Số mol của NaCl là nNaCl = 50000 : 58,5 = 854,7 mol
Từ PTHH số mol của Na2CO3 là 427,35 mol
Khối lượng Na2CO3 thu được thực tế là
mNa2CO3 = 427,35 × 106 × 85% = 38504,235 gam ≈ 38,5 kg
⟹Điền đáp án : 38,5
Giai đoạn 2: Nung CaCO3 ở 950 - 1100 oC rồi dẫn khí thoát ra vào dung dịch bão hòa của NaCl trong NH3, thực tế trong công nghiệp người ta sử dụng các phản ứng này[1]:
CaCO3 → CaO + CO2
NaCl + NH3 + CO2 + H2O → NaHCO3 + NH4Cl
Giai đoạn 3: Tách NaHCO3 khỏi dung dịch nhờ tính tan. Nung NaHCO3 ở nhiệt độ 450 - 500 oC thu được soda:
2NaHCO3 → Na2CO3 + CO2 + H2O
Đổi 50 kg = 50000 gam
Số mol của NaCl là nNaCl = 50000 : 58,5 = 854,7 mol
Từ PTHH số mol của Na2CO3 là 427,35 mol
Khối lượng Na2CO3 thu được thực tế là
mNa2CO3 = 427,35 × 106 × 85% = 38504,235 gam ≈ 38,5 kg
⟹Điền đáp án : 38,5