PHẦN I. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
Câu 1 [705799]: Thuốc súng bao gồm potassium nitrate, than củi và lưu huỳnh theo tỉ lệ khối lượng xấp xỉ 6 : 1 : 1. Công thức hóa học của potassium nitrate là
A, KNO2.
B, KNO3.
C, K3N.
D, KNSC.
Phân tích các đáp án:
❌A. KNO2 là potassium nitrite.
✔️B. KNO3 là potassium nitrate.
❌C. K3N là potassium nitride.
❌D. KNSC là potassium thiocyanate Đáp án: B
❌A. KNO2 là potassium nitrite.
✔️B. KNO3 là potassium nitrate.
❌C. K3N là potassium nitride.
❌D. KNSC là potassium thiocyanate Đáp án: B
Câu 2 [310498]: Đồng trùng hợp buta-1,3-diene với chất nào sau đây thu được polymer dùng sản xuất cao su buna-S?
A, Isoprene.
B, Lưu huỳnh.
C, Vinyl cyanide.
D, Styrene.
Đồng trùng hợp buta-1,3-diene với styrene thu được polymer dùng sản xuất cao su buna-S theo phương trình:
CH2=CH-CH=CH2 + C6H5-CH=CH2 → (-CH2-CH=CH-CH2-CH(C6H5)-CH2-)n
⟹ Chọn đáp án D Đáp án: D
CH2=CH-CH=CH2 + C6H5-CH=CH2 → (-CH2-CH=CH-CH2-CH(C6H5)-CH2-)n
⟹ Chọn đáp án D Đáp án: D
Câu 3 [703942]: “Ăn mòn điện hoá là quá trình ăn mòn …(1)… do sự tạo thành …(2)…”. Nội dung phù hợp trong ô trống (1), (2) lần lượt là
A, hợp kim, dòng điện.
B, kim loại, môi trường điện li.
C, phi kim, dung dịch acid.
D, kim loại, pin điện hoá.
Ăn mòn điện hóa là quá trình phá hủy kim loại hoặc hợp kim do phản ứng điện hóa xảy ra khi kim loại tiếp xúc với môi trường dẫn điện (như dung dịch chất điện ly). Quá trình này xảy ra khi có sự tạo thành pin điện hóa.
⇒ Ăn mòn điện hoá là quá trình ăn mòn kim loại do sự tạo thành pin điện hoá.
⇒ Chọn đáp án D Đáp án: D
⇒ Ăn mòn điện hoá là quá trình ăn mòn kim loại do sự tạo thành pin điện hoá.
⇒ Chọn đáp án D Đáp án: D
Câu 4 [305727]: Hydrogen hoá hoàn toàn triolein có công thức (C17H33COO)3C3H5 trong điều kiện xúc tác Ni, đun nóng, thu được chất béo X. Công thức của X là
A, (C17H35COO)3C3H5.
B, (C17H37COO)3C3H5.
C, (C17H31COO)3C3H5.
D, (C15H31COO)3C3H5.
Phản ứng hydrogen hóa:
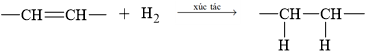
Triolein: (C17H33COO)3C3H5 có 3 nối đôi C=C ⟶ khi phản ứng hoàn toàn sẽ thu được tristearin: (C17H35COO)3C3H5.
(C17H33COO)3C3H5 + 3H2 –––Ni, to–→ (C17H35COO)3C3H5.
⟹ Chọn đáp án A. Đáp án: A
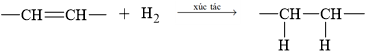
Triolein: (C17H33COO)3C3H5 có 3 nối đôi C=C ⟶ khi phản ứng hoàn toàn sẽ thu được tristearin: (C17H35COO)3C3H5.
(C17H33COO)3C3H5 + 3H2 –––Ni, to–→ (C17H35COO)3C3H5.
⟹ Chọn đáp án A. Đáp án: A
Câu 5 [308360]: Khi đun nóng dung dịch đường saccharose có xúc tác acid vô cơ ta được dung dịch chứa
A, glucose và maltose.
B, glucose và glycogen.
C, fructose và maltose.
D, glucose và fructose.
Saccharose cấu tạo từ glucose và fructose nên thủy phân ta thu được tương ứng sản phẩm là glucose và fructose.
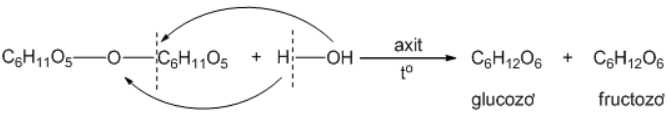
⟹Chọn đáp án D. Đáp án: D

⟹Chọn đáp án D. Đáp án: D
Câu 6 [575735]: Sulfur được sử dụng trong quá trình lưu hoá cao su, làm chất diệt nấm và có trong thuốc nổ đen. Sulfur là nguyên tố nhóm VIA. Công thức oxide cao nhất của sulfur là
A, SO2.
B, SO3.
C, SO6.
D, SO4.
Sulfur là nguyên tố nhóm VIA, có 6 electron lớp ngoài cùng.
Số oxi hóa cao nhất của nguyên tố nhóm VIA là +6.
Oxide cao nhất của sulfur phải có số oxi hóa của S là +6.
Phân tích các đáp án :
❌A. Sai. SO2 là một oxide của sulfur, nhưng không phải là oxide cao nhất. Số oxi hóa của S trong SO2 là +4.
✔️B. Đúng. SO3 là oxide cao nhất của sulfur. Số oxi hóa của S trong SO3 là +6, bằng với số oxi hóa cao nhất của nguyên tố nhóm VIA.
❌C, D. Sai. SO6 và SO4 không tồn tại ở dạng phân tử.
⟹Chọn đáp án B Đáp án: B
Số oxi hóa cao nhất của nguyên tố nhóm VIA là +6.
Oxide cao nhất của sulfur phải có số oxi hóa của S là +6.
Phân tích các đáp án :
❌A. Sai. SO2 là một oxide của sulfur, nhưng không phải là oxide cao nhất. Số oxi hóa của S trong SO2 là +4.
✔️B. Đúng. SO3 là oxide cao nhất của sulfur. Số oxi hóa của S trong SO3 là +6, bằng với số oxi hóa cao nhất của nguyên tố nhóm VIA.
❌C, D. Sai. SO6 và SO4 không tồn tại ở dạng phân tử.
⟹Chọn đáp án B Đáp án: B
Câu 7 [704024]: Phương pháp nào sau đây không dùng để xác định phân tử khối của một chất?
A, Phương pháp xác định tỉ khối hơi/khí.
B, Phương pháp xác định qua độ hạ băng điểm.
C, Phương pháp phổ khối lượng (MS).
D, Phương pháp phổ hồng ngoại (IR).
Phổ hồng ngoại (hay quang phổ hồng ngoại, tiếng Anh: Infrared Spectroscopy, viết tắt là phổ IR) là phép đo sự tương tác của bức xạ hồng ngoại với vật chất bằng hiện tượng hấp thụ, phát xạ hoặc phản xạ. Phổ IR được sử dụng để nghiên cứu và xác định hóa chất hoặc nhóm chức ở dạng rắn, lỏng hoặc khí.
⇒ Chọn đáp án D Đáp án: D
⇒ Chọn đáp án D Đáp án: D
Câu 8 [1009528]: Thực hiện phản ứng ester hoá: cho 0,1 mol alcohol tác dụng với 0,1 mol carboxylic acid, có mặt H2SO4 đặc làm xúc tác. Đồ thị nào sau đây biểu diễn sự thay đổi số mol (n) alcohol theo thời gian (t)?
A, 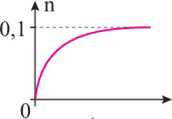

B, 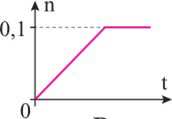

C, 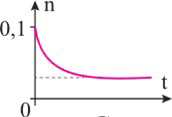

D, 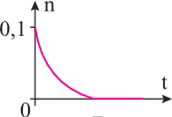

Ester thường được điều chế bằng phản ứng ester hoá giữa carboxylic acid và alcohol với xúc tác là acid (thường dùng H2SO4 đặc).
Phương trình: R-COOH + R’OH ⇌ R-COO-R’ + H2O
Đây là phản ứng thuận nghịch, khi đặt đến trạng thái cân bằng số mol của carboxylic acid và alcohol sẽ giảm dần rồi không đổi theo thời gian.
⟹ Chọn đáp án C số mol của alcohol sẽ giảm dần sau đó sẽ không đổi theo thời gian. Đáp án: C
Phương trình: R-COOH + R’OH ⇌ R-COO-R’ + H2O
Đây là phản ứng thuận nghịch, khi đặt đến trạng thái cân bằng số mol của carboxylic acid và alcohol sẽ giảm dần rồi không đổi theo thời gian.
⟹ Chọn đáp án C số mol của alcohol sẽ giảm dần sau đó sẽ không đổi theo thời gian. Đáp án: C
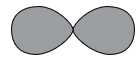
Câu 9 [705855]: Nguyên tử nào có electron ngoài cùng nằm trong quỹ đạo có hình dạng như hình vẽ, với số lượng tử chính (n) là 3?

A, sodium.
B, chlorine.
C, calcium.
D, bromine.
Nguyên tử có electron ngoài cùng nằm trong quỹ đạo có hình dạng như hình vẽ, với số lượng tử chính (n) là 3
→ Như hình vẽ là AO p nên electron cuối cùng điền vào phân lớp p, số lượng tử chính là 3 nên có 3 lớp electron
→ Nguyên tử phù hợp là chlorine (Z = 17)
Cấu hình electron 1s2 2s2 2p6 3s2 3p5, thuộc nhóm VIIA chu kì 3 của bảng tuần hoàn.
⟹ Chọn đáp án B Đáp án: B
→ Như hình vẽ là AO p nên electron cuối cùng điền vào phân lớp p, số lượng tử chính là 3 nên có 3 lớp electron
→ Nguyên tử phù hợp là chlorine (Z = 17)
Cấu hình electron 1s2 2s2 2p6 3s2 3p5, thuộc nhóm VIIA chu kì 3 của bảng tuần hoàn.
⟹ Chọn đáp án B Đáp án: B
Câu 10 [706127]: Magnesium là kim loại có độ hoạt động hoá học mạnh hơn nhôm (aluminium) thì
A, 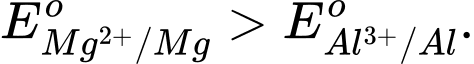
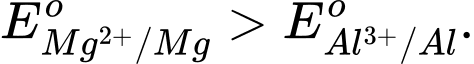
B, 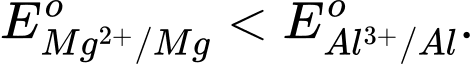
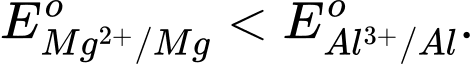
C, 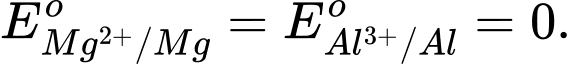
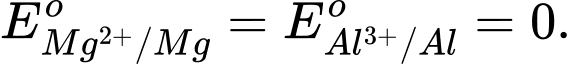
D, 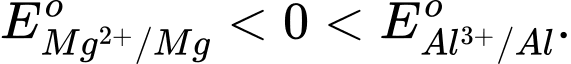
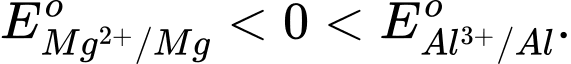
Phân tích các đáp án:
❌ A. Sai. Vì Mg hoạt động hóa học mạnh hơn Al nên thế điện cực chuẩn của Mg phải nhỏ hơn Al.
✔️ B. Đúng. Mg hoạt động hóa học mạnh hơn Al nên thế điện cực chuẩn của Mg nhỏ hơn Al.
❌ C. Sai. Thế điện cực chuẩn của Mg và Al khác 0.
❌ D. Sai. Mặc dù đúng là Mg có tính khử mạnh hơn Al, điều này không có nghĩa là thế điện cực chuẩn của Al luôn dương.
⟹Chọn đáp án B Đáp án: B
❌ A. Sai. Vì Mg hoạt động hóa học mạnh hơn Al nên thế điện cực chuẩn của Mg phải nhỏ hơn Al.
✔️ B. Đúng. Mg hoạt động hóa học mạnh hơn Al nên thế điện cực chuẩn của Mg nhỏ hơn Al.
❌ C. Sai. Thế điện cực chuẩn của Mg và Al khác 0.
❌ D. Sai. Mặc dù đúng là Mg có tính khử mạnh hơn Al, điều này không có nghĩa là thế điện cực chuẩn của Al luôn dương.
⟹Chọn đáp án B Đáp án: B
Câu 11 [1105712]: Enzyme là một chất thiết yếu của các chất giặt rửa cao cấp và việc sử dụng chúng mang lại cho người tiêu dùng những lợi ích rõ rệt. Những lợi ích này bao gồm khả năng làm việc ở nhiệt độ thấp, tiết kiệm nước, đồng thời loại bỏ nhu cầu sử dụng các hóa chất khắc nghiệt, gây tác động tiêu cực đến môi trường. Ngoài ra, enzyme có thể phân hủy sinh học nên không để lại lượng dư độc hại. Protease là loại enzyme không thể thiếu trong tất cả các loại hóa chất giặt rửa, nhất là bột giặt, do protease thích hợp để loại bỏ các vết bẩn do thức ăn, máu và các dịch trong cơ thể con người khi tiết ra. Để khảo sát độ hoạt động của protease theo nhiệt độ, người ta tiến hành thí nghiệm nghiên cứu tốc độ phân hủy chất bởi protease. Kết quả cho bởi biểu đồ dưới đây:
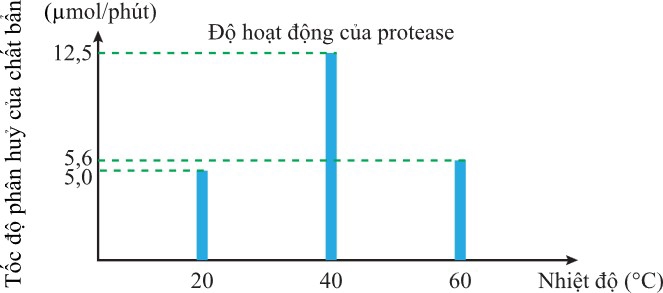
Cho các phát biểu sau:
(a) Cơ chế hoạt động của protease giống với cơ chế giặt rửa của xà phòng và chất giặt rửa tổng hợp.
(b) Protease dùng dư trong giặt rửa gây ô nhiễm môi trường
(c) Khi tăng nhiệt độ, tốc độ phân hủy của các vết bẩn trong quần, áo sẽ nhanh hơn vì hoạt động của enzyme protease tăng dần.
(d) Tỉ lệ tốc độ phân hủy các chất bẩn ở nhiệt độ 40 °C và 20 °C tương ứng là 5:2.
(e) Do có tính chọn lọc cao, phải sử dụng ở một nhiệt độ nghiêm ngặt nên người ta đang dần thay thế chất giặt rửa enzyme protease bằng chất giặt rửa có chứa các chất tẩy rửa mạnh.
Số phát biểu không đúng là

Cho các phát biểu sau:
(a) Cơ chế hoạt động của protease giống với cơ chế giặt rửa của xà phòng và chất giặt rửa tổng hợp.
(b) Protease dùng dư trong giặt rửa gây ô nhiễm môi trường
(c) Khi tăng nhiệt độ, tốc độ phân hủy của các vết bẩn trong quần, áo sẽ nhanh hơn vì hoạt động của enzyme protease tăng dần.
(d) Tỉ lệ tốc độ phân hủy các chất bẩn ở nhiệt độ 40 °C và 20 °C tương ứng là 5:2.
(e) Do có tính chọn lọc cao, phải sử dụng ở một nhiệt độ nghiêm ngặt nên người ta đang dần thay thế chất giặt rửa enzyme protease bằng chất giặt rửa có chứa các chất tẩy rửa mạnh.
Số phát biểu không đúng là
A, 2.
B, 3.
C, 4.
D, 5.
❌a) Sai — protease hoạt động bằng xúc tác sinh học (thủy phân protein), khác với cơ chế làm sạch bằng xà phòng/ chất tẩy (tác dụng nhũ hóa, làm tan dầu mỡ).
❌b) Sai — theo đề, protease có thể phân huỷ sinh học và không để lại lượng dư độc hại, nên không gây ô nhiễm nặng như phát biểu.
❌c) Sai — hoạt độ enzyme tăng khi tăng nhiệt độ chỉ đến một nhiệt độ tối ưu (ở đây ~40 °C). Tăng tiếp lên 60 °C hoạt độ giảm (giảm do bất hoạt), nên không đúng rằng “khi tăng nhiệt độ thì luôn nhanh hơn”.
✔️d) Đúng — tốc độ ở 40 °C ≈ 12,5 µmol/phút và ở 20 °C ≈ 5,0 µmol/phút; tỉ lệ 12,5:5 = 5:2.
❌e) Sai — do có tính chọn lọc và lợi ích (làm việc ở nhiệt độ thấp, thân thiện môi trường), người ta sẽ ưa dùng enzyme hơn chứ không thay thế bằng chất tẩy mạnh.
⟹ Chọn đáp án C (có 4 phát biểu không đúng) Đáp án: C
❌b) Sai — theo đề, protease có thể phân huỷ sinh học và không để lại lượng dư độc hại, nên không gây ô nhiễm nặng như phát biểu.
❌c) Sai — hoạt độ enzyme tăng khi tăng nhiệt độ chỉ đến một nhiệt độ tối ưu (ở đây ~40 °C). Tăng tiếp lên 60 °C hoạt độ giảm (giảm do bất hoạt), nên không đúng rằng “khi tăng nhiệt độ thì luôn nhanh hơn”.
✔️d) Đúng — tốc độ ở 40 °C ≈ 12,5 µmol/phút và ở 20 °C ≈ 5,0 µmol/phút; tỉ lệ 12,5:5 = 5:2.
❌e) Sai — do có tính chọn lọc và lợi ích (làm việc ở nhiệt độ thấp, thân thiện môi trường), người ta sẽ ưa dùng enzyme hơn chứ không thay thế bằng chất tẩy mạnh.
⟹ Chọn đáp án C (có 4 phát biểu không đúng) Đáp án: C
Câu 12 [703923]: Nhôm chloride ngậm nước chứa ion phức [Al(H2O)6]3+. Câu nào sau đây là lời giải thích đúng nhất về liên kết được hình thành giữa ion Al3+ và các phân tử nước?
A, Ion Al3+ bị thu hút bởi phân tử nước mang điện tích âm.
B, Phân tử nước cho cặp electron riêng của O vào orbital trống của ion Al3+.
C, Liên kết hydrogen được hình thành giữa ion Al3+ với phân tử nước.
D, Liên kết Van der Waals được hình thành giữa ion Al3+ với phân tử nước.
H2O là phối tử trung hoà còn cặp electron chưa liên kết, cho cặp electron chưa liên kết vào orbital trống của nguyên tử trung tâm, hình thành liên kết cho - nhận.
⇒ Chọn đáp án B Đáp án: B
⇒ Chọn đáp án B Đáp án: B
Câu 13 [705859]: Phổ khối lượng (MS) là phương pháp hiện đại để xác định phân tử khối của các hợp chất hữu cơ. 5,7-dimethyloctan-3-one có công thức cấu tạo như sau:
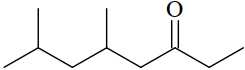
Kết quả phân tích phổ khối lượng cho thấy phân tử khối của 5,7-dimethyloctan-3-one có giá trị m/z bằng bao nhiêu?

Kết quả phân tích phổ khối lượng cho thấy phân tử khối của 5,7-dimethyloctan-3-one có giá trị m/z bằng bao nhiêu?
A, 92.
B, 118.
C, 130.
D, 156.
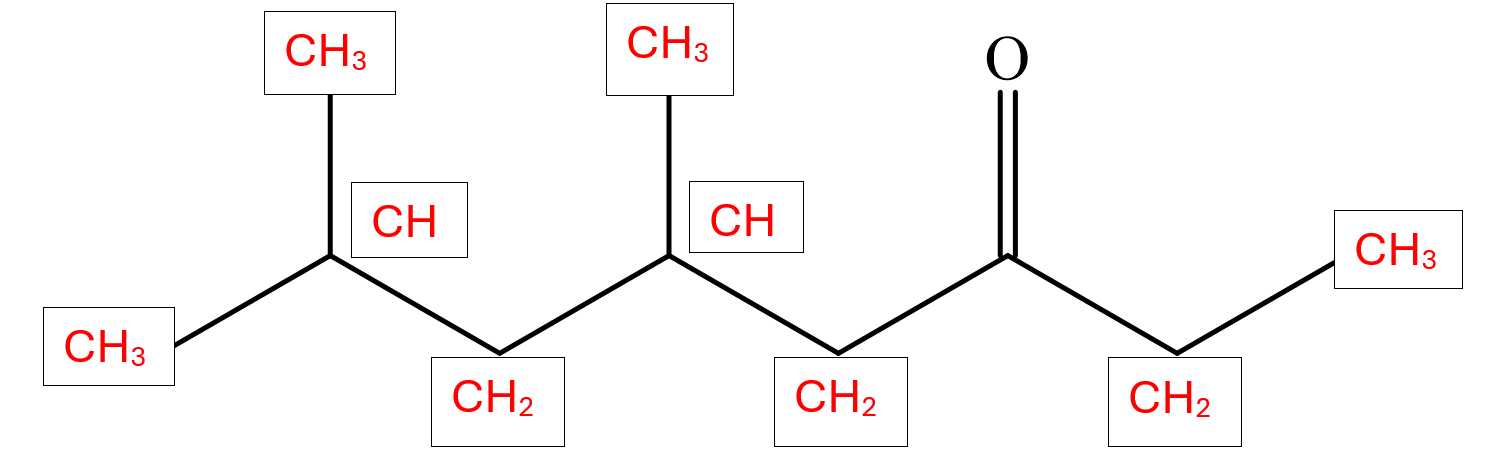
Phân tử khối của 5,7-dimethyloctan-3-one là 156.
⟹ Chọn đáp án D Đáp án: D
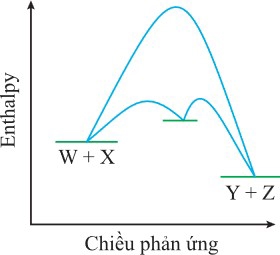
Câu 14 [1105713]: Đồ thị dưới hình bên biểu diễn biến thiên enthalpy của phản ứng: W + X 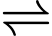 Y + Z.
Y + Z.
Nhận định nào sau đây đúng khi nói về phản ứng trên?
 Y + Z.
Y + Z.Nhận định nào sau đây đúng khi nói về phản ứng trên?

A, Khối lượng chất xúc tác giảm dần theo thời gian phản ứng.
B, Tăng nhiệt độ sẽ làm cân bằng dịch chuyển theo chiều thuận.
C, Chất xúc tác làm thay đổi biến thiên enthalpy của phản ứng.
D, Phản ứng thuận là phản ứng toả nhiệt.
Đồ thị biểu diễn biến thiên enthalpy (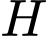 ) theo chiều phản ứng.
) theo chiều phản ứng.
• Chất phản ứng ( ): Có mức enthalpy cao hơn.
): Có mức enthalpy cao hơn.
• Sản phẩm ( ): Có mức enthalpy thấp hơn.
): Có mức enthalpy thấp hơn.
Biến thiên enthalpy của phản ứng ( ) được tính bằng hiệu số enthalpy của sản phẩm và chất phản ứng:
) được tính bằng hiệu số enthalpy của sản phẩm và chất phản ứng: 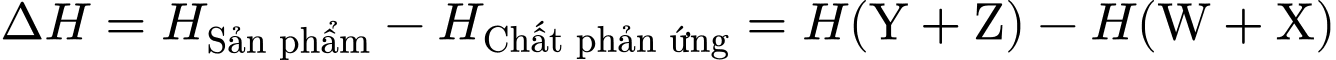
Vì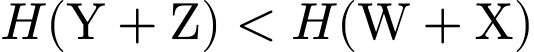 , nên:
, nên: 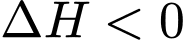
A. Khối lượng chất xúc tác giảm dần theo thời gian phản ứng. Sai.
Sai.
• Chất xúc tác làm tăng tốc độ phản ứng (cả thuận và nghịch) bằng cách làm giảm năng lượng hoạt hóa, nhưng nó không bị tiêu thụ trong quá trình phản ứng.
• Do đó, khối lượng chất xúc tác không đổi.
B. Tăng nhiệt độ sẽ làm cân bằng dịch chuyển theo chiều thuận. Sai.
Sai.
• Phản ứng thuận là phản ứng tỏa nhiệt (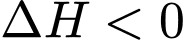 ).
).
• Theo nguyên lý Le Chatelier: Khi tăng nhiệt độ, cân bằng sẽ dịch chuyển theo chiều thu nhiệt (chiều nghịch).
C. Chất xúc tác làm thay đổi biến thiên enthalpy ( ) của phản ứng.
) của phản ứng.  Sai.
Sai.
• Chất xúc tác chỉ làm giảm năng lượng hoạt hóa (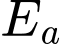 ) bằng cách tạo ra cơ chế phản ứng mới, nhưng nó không làm thay đổi mức năng lượng ban đầu của chất phản ứng hay mức năng lượng cuối của sản phẩm.
) bằng cách tạo ra cơ chế phản ứng mới, nhưng nó không làm thay đổi mức năng lượng ban đầu của chất phản ứng hay mức năng lượng cuối của sản phẩm.
• Do đó, không thay đổi.
không thay đổi.
D. Phản ứng thuận là phản ứng tỏa nhiệt. Đúng
Đúng
• Như đã phân tích ở trên,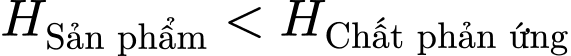 , suy ra
, suy ra 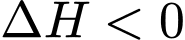 .
.
• Phản ứng có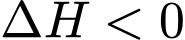 là phản ứng tỏa nhiệt.
là phản ứng tỏa nhiệt.
⟹ Chọn đáp án D Đáp án: D
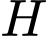 ) theo chiều phản ứng.
) theo chiều phản ứng.• Chất phản ứng (
 ): Có mức enthalpy cao hơn.
): Có mức enthalpy cao hơn.• Sản phẩm (
 ): Có mức enthalpy thấp hơn.
): Có mức enthalpy thấp hơn.Biến thiên enthalpy của phản ứng (
 ) được tính bằng hiệu số enthalpy của sản phẩm và chất phản ứng:
) được tính bằng hiệu số enthalpy của sản phẩm và chất phản ứng: 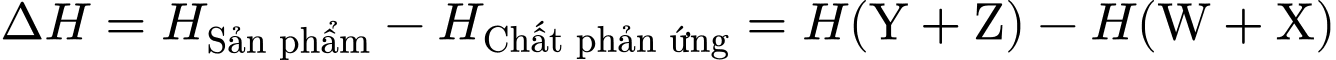
Vì
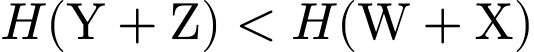 , nên:
, nên: 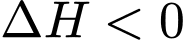
A. Khối lượng chất xúc tác giảm dần theo thời gian phản ứng.
 Sai.
Sai.• Chất xúc tác làm tăng tốc độ phản ứng (cả thuận và nghịch) bằng cách làm giảm năng lượng hoạt hóa, nhưng nó không bị tiêu thụ trong quá trình phản ứng.
• Do đó, khối lượng chất xúc tác không đổi.
B. Tăng nhiệt độ sẽ làm cân bằng dịch chuyển theo chiều thuận.
 Sai.
Sai.• Phản ứng thuận là phản ứng tỏa nhiệt (
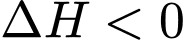 ).
).• Theo nguyên lý Le Chatelier: Khi tăng nhiệt độ, cân bằng sẽ dịch chuyển theo chiều thu nhiệt (chiều nghịch).
C. Chất xúc tác làm thay đổi biến thiên enthalpy (
 ) của phản ứng.
) của phản ứng.  Sai.
Sai.• Chất xúc tác chỉ làm giảm năng lượng hoạt hóa (
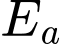 ) bằng cách tạo ra cơ chế phản ứng mới, nhưng nó không làm thay đổi mức năng lượng ban đầu của chất phản ứng hay mức năng lượng cuối của sản phẩm.
) bằng cách tạo ra cơ chế phản ứng mới, nhưng nó không làm thay đổi mức năng lượng ban đầu của chất phản ứng hay mức năng lượng cuối của sản phẩm.• Do đó,
 không thay đổi.
không thay đổi. D. Phản ứng thuận là phản ứng tỏa nhiệt.
 Đúng
Đúng• Như đã phân tích ở trên,
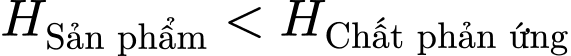 , suy ra
, suy ra 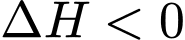 .
.• Phản ứng có
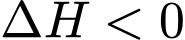 là phản ứng tỏa nhiệt.
là phản ứng tỏa nhiệt. ⟹ Chọn đáp án D Đáp án: D
Câu 15 [702838]: 1-bromoethane, CH3CH2Br, là một halogenoalkane bậc một. Phản ứng thủy phân trong môi trường kiềm là:
C2H5Br + OH– C2H5OH + Br–
C2H5OH + Br–
Cơ chế của phản ứng được mô tả như sau:
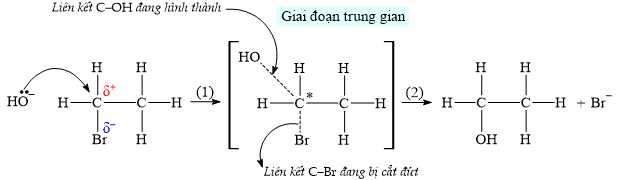
Nhận định nào sau đây là đúng?
C2H5Br + OH–
 C2H5OH + Br–
C2H5OH + Br–Cơ chế của phản ứng được mô tả như sau:

Nhận định nào sau đây là đúng?
A, Ở giai đoạn trung gian, C* tạo thành 5 liên kết σ.
B, Tổng số nguyên tử H trong phân tử hữu cơ trước và sau phản ứng không đổi.
C, Ion OH– hình thành liên kết với C mang một phần điện tích dương (δ+).
D, Nguyên tử Br sẽ tách đi cùng với H của carbon bên cạnh hình thành liên kết σ.
Phân tích các đáp án:
❌ A. Sai. Ở giai đoạn trung gian, C* vẫn có 4 liên kết σ.
❌ B. Sai. Trước phản ứng ta có 5H, sau khi thế -OH vào Br thì ta có 6H.
✔️ C. Đúng. ion OH⁻ tấn công vào carbon mang nhóm rời (Br). Carbon này mang điện tích dương (δ+) trong suốt quá trình phản ứng do sự rút electron từ nhóm halogen (Br). Do đó, OH⁻ tấn công vào carbon mang điện tích dương (δ+).
❌ D. Sai. Nguyên tử Br tách đi một mình và không đi kèm với H. Tách Br⁻ là một quá trình độc lập, không có sự tham gia của H.
⇒ Chọn đáp án C Đáp án: C
❌ A. Sai. Ở giai đoạn trung gian, C* vẫn có 4 liên kết σ.
❌ B. Sai. Trước phản ứng ta có 5H, sau khi thế -OH vào Br thì ta có 6H.
✔️ C. Đúng. ion OH⁻ tấn công vào carbon mang nhóm rời (Br). Carbon này mang điện tích dương (δ+) trong suốt quá trình phản ứng do sự rút electron từ nhóm halogen (Br). Do đó, OH⁻ tấn công vào carbon mang điện tích dương (δ+).
❌ D. Sai. Nguyên tử Br tách đi một mình và không đi kèm với H. Tách Br⁻ là một quá trình độc lập, không có sự tham gia của H.
⇒ Chọn đáp án C Đáp án: C
Câu 16 [308793]: Thủy phân peptide:
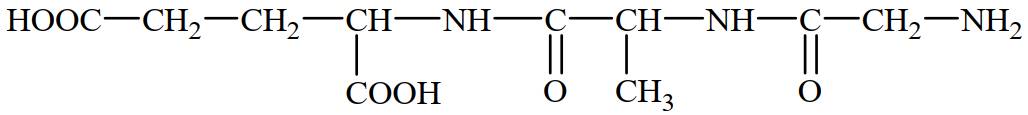
Chất nào dưới đây có thể được tạo thành trong hỗn hợp sản phẩm sau phản ứng?
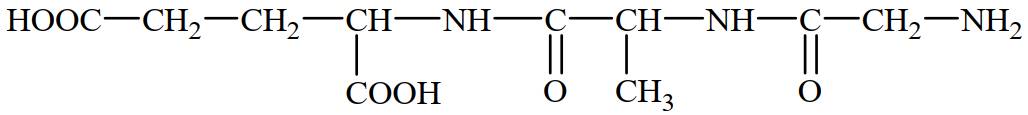
Chất nào dưới đây có thể được tạo thành trong hỗn hợp sản phẩm sau phản ứng?
A, Ala-Glu.
B, Glu-Ala.
C, Ala-Gly.
D, Glu-Gly.
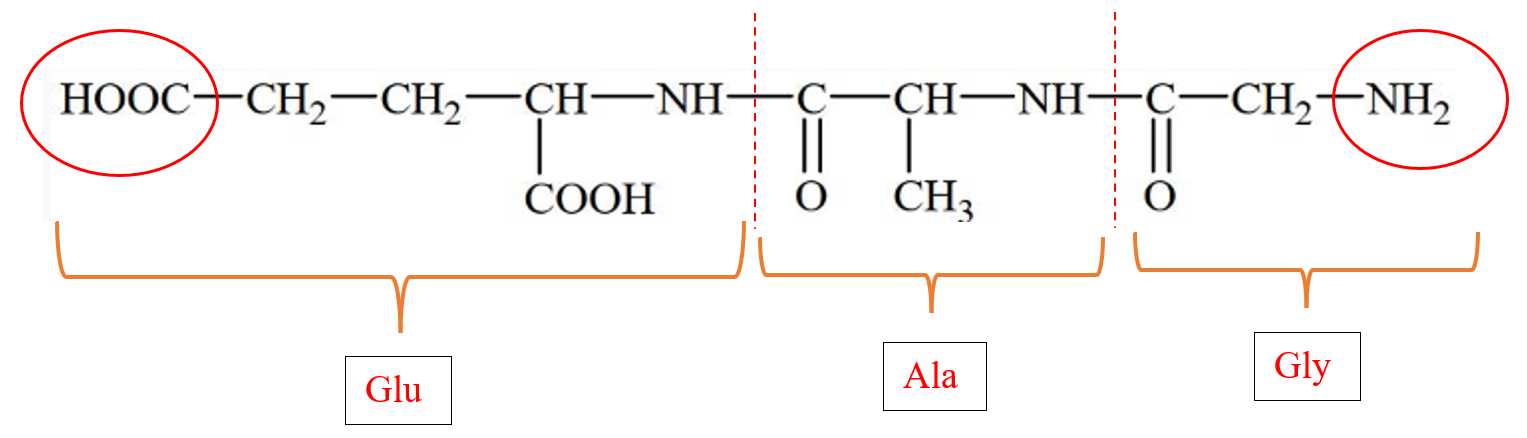
Peptide có tên: Gly-Ala-Glu khi thủy phân có thể thu được Gly, Ala, Glu, Gly-Ala, Ala-Glu.
⟹ Chọn đáp án A Đáp án: A
Sử dụng thông tin ở bảng dưới đây để trả lời các câu 17 - 18:
Cho bảng giá trị thế điện cực chuẩn của các cặp oxi hóa - khử như sau:
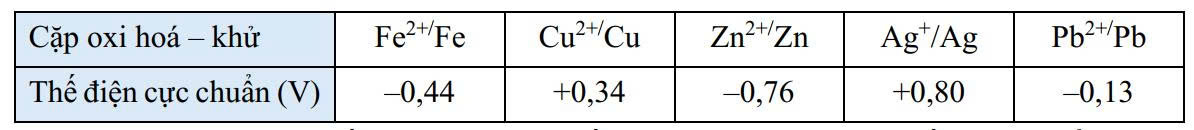
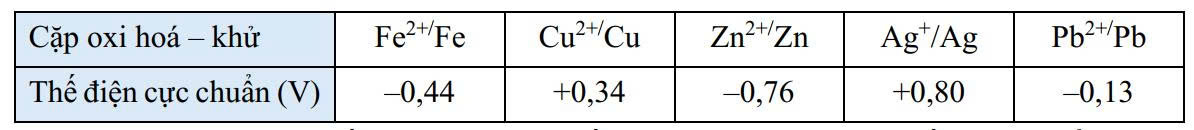
Câu 17 [680869]: Trong số các ion kim loại gồm Fe2+, Cu2+ và Zn2+, ở điều kiện chuẩn ion nào có tính oxi hóa yếu hơn Ag+, nhưng mạnh hơn Pb2+?
A,
Fe2+, Cu2+, Zn2+.
B, Fe2+, Cu2+.
C, Zn2+.
D, Cu2+.
Ta có
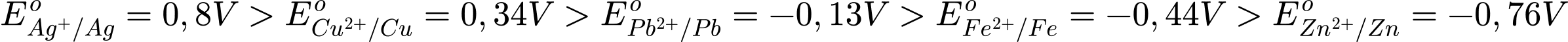
→ Thấy rằng chỉ có Cu2+/Cu có thế điện cực chuẩn nhỏ hơn Ag+/Ag và lớn hơn Pb2+/Pb
→ Cu2+ có tính oxi hóa mạnh hơn Pb2+/Pb và yếu hơn Ag+/Ag.
⇒ Chọn đáp án D
Đáp án: D
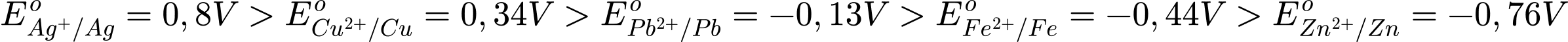
→ Thấy rằng chỉ có Cu2+/Cu có thế điện cực chuẩn nhỏ hơn Ag+/Ag và lớn hơn Pb2+/Pb
→ Cu2+ có tính oxi hóa mạnh hơn Pb2+/Pb và yếu hơn Ag+/Ag.
⇒ Chọn đáp án D
Đáp án: D
Câu 18 [680870]: Sức điện động chuẩn lớn nhất của pin Galvani thiết lập từ hai cặp oxi hóa - khử trong số các cặp trên là
A, 1,24 V.
B, 1,56 V.
C, 1,60 V.
D, 0,93 V.
Sức điện động lớn nhất của pin galvani thiết lặp từ cặp Zn2+/Zn và Ag+/Ag
Với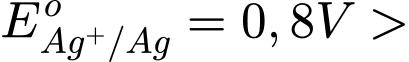
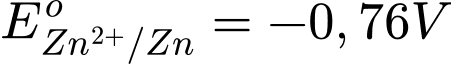 → Zn đóng vai trò là anode (-) và Ag đóng vai trò là cathode (+)
→ Zn đóng vai trò là anode (-) và Ag đóng vai trò là cathode (+)
Zn + 2Ag+ → Zn2+ + 2Ag
Phản ứng trong pin:
Cathode (+): Ag+ +1e → Ag
Anode (-): Zn → Zn2+ + 2e
Sức điện của pin là: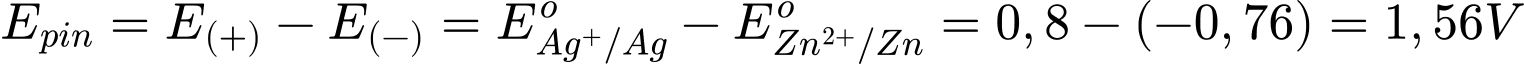
⇒ Chọn đáp án B Đáp án: B
Với
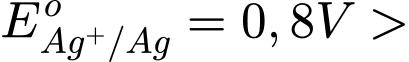
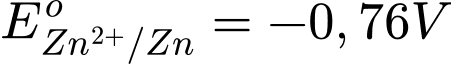 → Zn đóng vai trò là anode (-) và Ag đóng vai trò là cathode (+)
→ Zn đóng vai trò là anode (-) và Ag đóng vai trò là cathode (+)Zn + 2Ag+ → Zn2+ + 2Ag
Phản ứng trong pin:
Cathode (+): Ag+ +1e → Ag
Anode (-): Zn → Zn2+ + 2e
Sức điện của pin là:
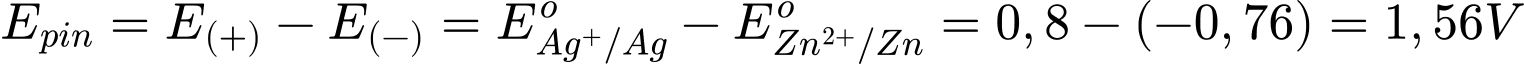
⇒ Chọn đáp án B Đáp án: B
PHẦN II. Thí sinh trả lời từ câu 1 đến câu 4. Trong mỗi ý a), b), c), d) ở mỗi câu, thí sinh chọn đúng hoặc sai.
Câu 19 [1105714]: Hydrocarbon là nguồn nguyên liệu trong tổng hợp hữu cơ. Một trong các chuyển hóa hydrocarbon được biết đến là quá trình sản xuất xà phòng từ hydrocarbon no, mạch dài không phân nhánh. Quá trình được mô tả theo sơ đồ sau:
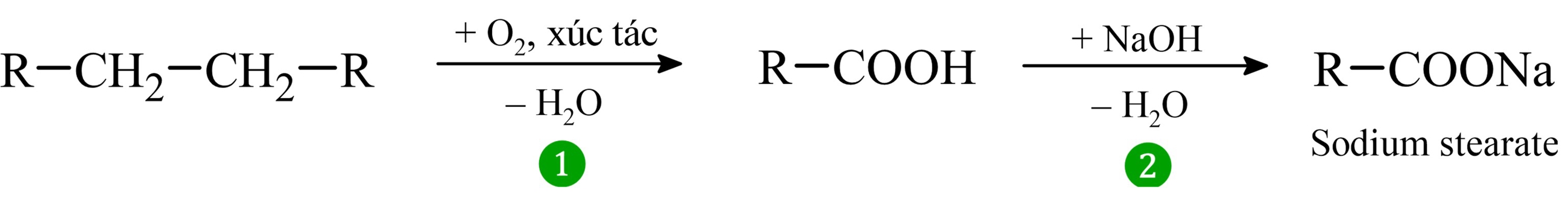
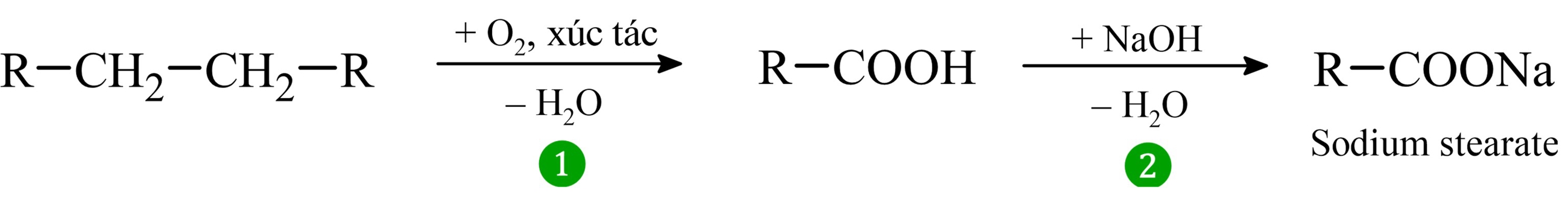
Quá trình chuyển hóa được mô tả qua hai phản ứng:
1. Phản ứng (1) - Oxi hóa xúc tác: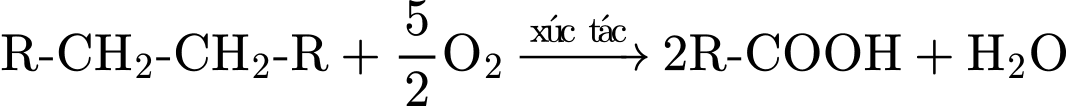 . Đây là quá trình oxi hóa hydrocarbon no mạch dài thành acid béo tương ứng.
. Đây là quá trình oxi hóa hydrocarbon no mạch dài thành acid béo tương ứng.
2. Phản ứng (2) - Trung hòa/Xà phòng hoá: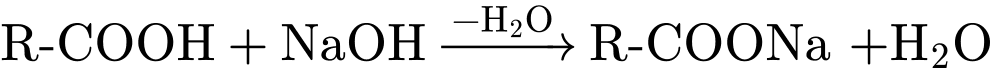 . Đây là phản ứng của acid béo với base để tạo ra muối sodium (xà phòng).
. Đây là phản ứng của acid béo với base để tạo ra muối sodium (xà phòng).
❌ Nhận định a) – Sai, vì: Muối sodium của acid béo (xà phòng) có khả năng giặt rửa do cấu tạo lưỡng cực:
* Phần đầu ion (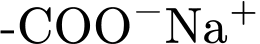 ): Ưa nước, hướng ra ngoài.
): Ưa nước, hướng ra ngoài.
* Phần đuôi hydrocarbon ( ): Kị nước, dễ hòa tan vào dầu mỡ.
): Kị nước, dễ hòa tan vào dầu mỡ.
=> Khả năng giặt rửa chủ yếu là do phần đuôi kị nước bao bọc các vết dầu mỡ và phần đầu ưa nước giúp tạo nhũ tương và cuốn trôi chúng. Nhóm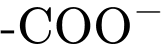 (phần ưa nước) không phải là phần xâm nhập chính vào dầu mỡ
(phần ưa nước) không phải là phần xâm nhập chính vào dầu mỡ
✔️ Nhận định b) – Đúng, vì: tỉ của phản ứng là nên số mol O2 gấp 2,5 lần số mol của hydrocarbon
✔️ Nhận định c) – Đúng, vì: Phản ứng (2) là phản ứng acid - base:
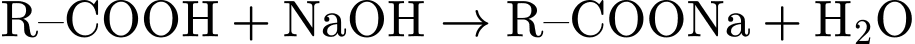
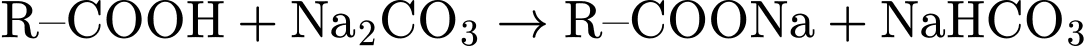 (hoặc
(hoặc  )
)
=> Cả hai phản ứng đều tạo ra muối . Muối thu được (R–COONa) không thay đổi về mặt hóa học.
. Muối thu được (R–COONa) không thay đổi về mặt hóa học.
❌ Nhận định d) – Sai, vì:
0,9 tấn sodium stearate – C17H35COONa
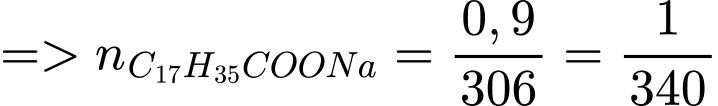 (tấn mol)
(tấn mol)
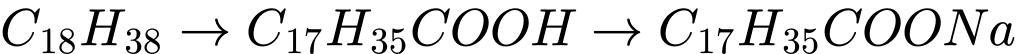
Bảo toàn nguyên tố C, ta có:
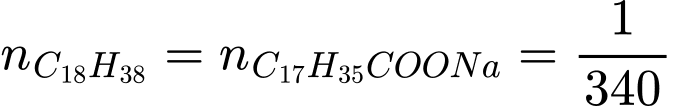 (tấn mol)
(tấn mol)
Mà hiệu suất bằng 90%
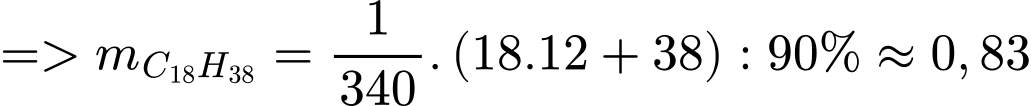 (tấn)
(tấn)
1. Phản ứng (1) - Oxi hóa xúc tác:
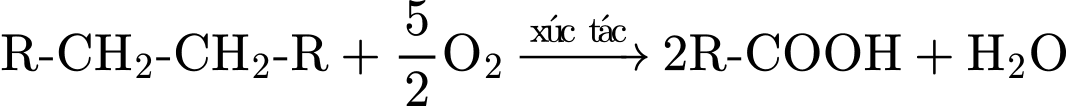 . Đây là quá trình oxi hóa hydrocarbon no mạch dài thành acid béo tương ứng.
. Đây là quá trình oxi hóa hydrocarbon no mạch dài thành acid béo tương ứng.2. Phản ứng (2) - Trung hòa/Xà phòng hoá:
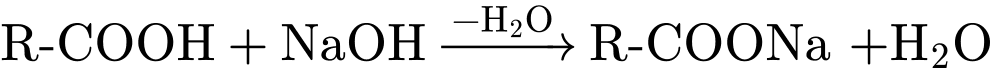 . Đây là phản ứng của acid béo với base để tạo ra muối sodium (xà phòng).
. Đây là phản ứng của acid béo với base để tạo ra muối sodium (xà phòng).❌ Nhận định a) – Sai, vì: Muối sodium của acid béo (xà phòng) có khả năng giặt rửa do cấu tạo lưỡng cực:
* Phần đầu ion (
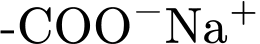 ): Ưa nước, hướng ra ngoài.
): Ưa nước, hướng ra ngoài. * Phần đuôi hydrocarbon (
 ): Kị nước, dễ hòa tan vào dầu mỡ.
): Kị nước, dễ hòa tan vào dầu mỡ. => Khả năng giặt rửa chủ yếu là do phần đuôi kị nước bao bọc các vết dầu mỡ và phần đầu ưa nước giúp tạo nhũ tương và cuốn trôi chúng. Nhóm
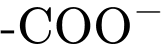 (phần ưa nước) không phải là phần xâm nhập chính vào dầu mỡ
(phần ưa nước) không phải là phần xâm nhập chính vào dầu mỡ✔️ Nhận định b) – Đúng, vì: tỉ của phản ứng là nên số mol O2 gấp 2,5 lần số mol của hydrocarbon
✔️ Nhận định c) – Đúng, vì: Phản ứng (2) là phản ứng acid - base:
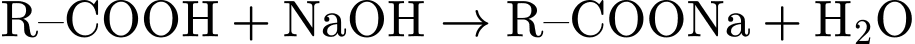
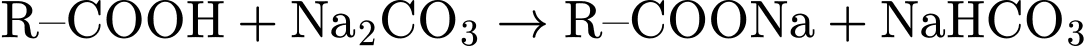 (hoặc
(hoặc  )
) => Cả hai phản ứng đều tạo ra muối
 . Muối thu được (R–COONa) không thay đổi về mặt hóa học.
. Muối thu được (R–COONa) không thay đổi về mặt hóa học.❌ Nhận định d) – Sai, vì:
0,9 tấn sodium stearate – C17H35COONa
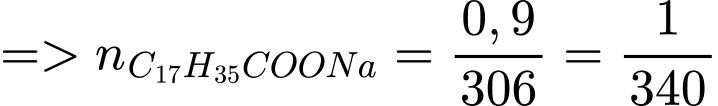 (tấn mol)
(tấn mol)
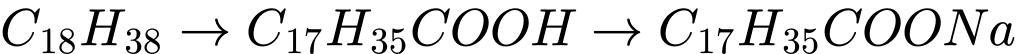
Bảo toàn nguyên tố C, ta có:
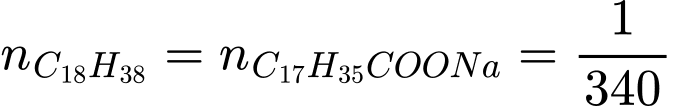 (tấn mol)
(tấn mol)Mà hiệu suất bằng 90%
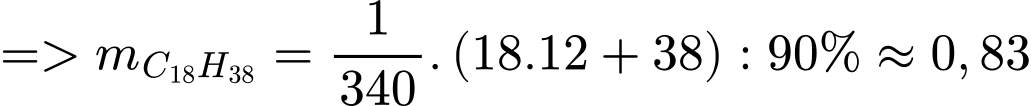 (tấn)
(tấn)
Câu 20 [1105715]: Cho sơ đồ tinh chế đồng từ quặng như sau:
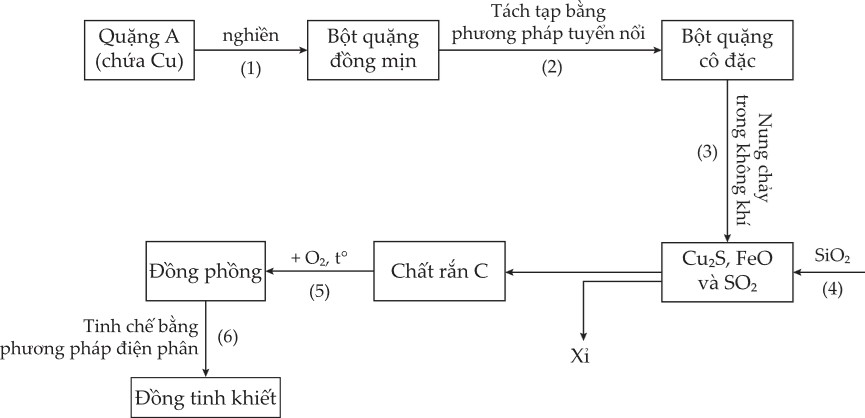
Cho biết thành phần chính của quặng A là muối X chứa ba nguyên tố (trong có một nguyên tố là Cu).

Cho biết thành phần chính của quặng A là muối X chứa ba nguyên tố (trong có một nguyên tố là Cu).
✔️ Nhận định a) – Đúng, vì: Sau khi nung chảy và tách  , chất rắn còn lại là
, chất rắn còn lại là 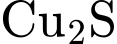
✔️ Nhận định b) – Đúng, vì: Trong quá trình xử lý nóng chảy, FeO kết hợp với SiO₂ để tạo xỉ ferrosilicat (biểu diễn đơn giản là FeSiO₃) với phương trình tạo xỉ: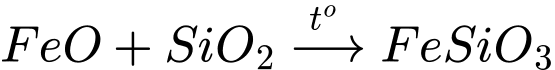
✔️ Nhận định c) – Đúng, vì:
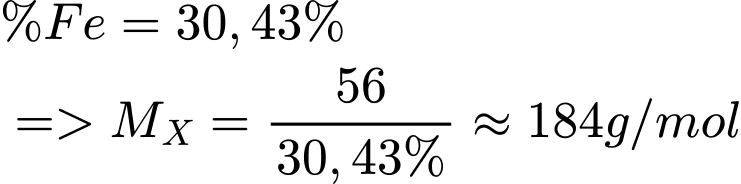
Mà: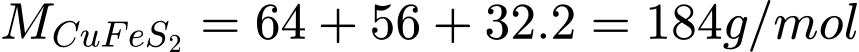
=> X là: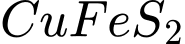
✔️ Nhận định d) – Đúng, vì:
25g quặng A mà %Cu = 11,52%
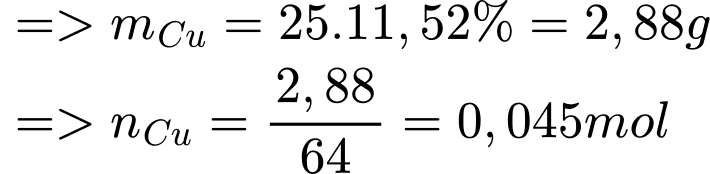
Mà hiệu suất phản ứng là 90% nên khối lượng Cu tinh khiết thu được là: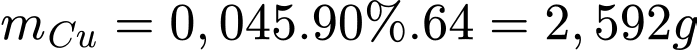
 , chất rắn còn lại là
, chất rắn còn lại là 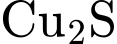
✔️ Nhận định b) – Đúng, vì: Trong quá trình xử lý nóng chảy, FeO kết hợp với SiO₂ để tạo xỉ ferrosilicat (biểu diễn đơn giản là FeSiO₃) với phương trình tạo xỉ:
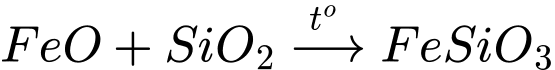
✔️ Nhận định c) – Đúng, vì:
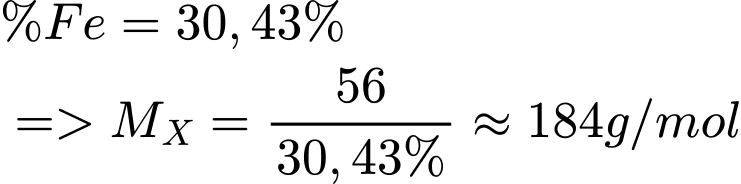
Mà:
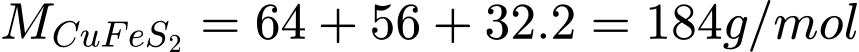
=> X là:
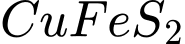
✔️ Nhận định d) – Đúng, vì:
25g quặng A mà %Cu = 11,52%
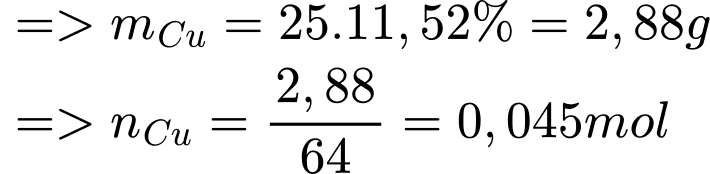
Mà hiệu suất phản ứng là 90% nên khối lượng Cu tinh khiết thu được là:
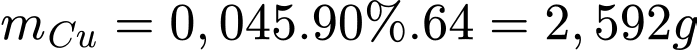
Câu 21 [704184]: Kim loại có khả năng tác dụng được với các phi kim trong các điều kiện phù hợp. Tiến hành hai thí nghiệm sau:
▪ Thí nghiệm 1: Dùng kẹp gắp dây kim loại magnesium, đốt nóng trong không khí.
▪ Thí nghiệm 2: Lấy sợi dây sắt cuốn thành hình lò xo. Dùng kẹp gắp dây sắt, nung nóng đỏ sợi dây sắt trên ngọn lửa đèn cồn, đưa nhanh vào bình chứa khí chlorine.
▪ Thí nghiệm 1: Dùng kẹp gắp dây kim loại magnesium, đốt nóng trong không khí.
▪ Thí nghiệm 2: Lấy sợi dây sắt cuốn thành hình lò xo. Dùng kẹp gắp dây sắt, nung nóng đỏ sợi dây sắt trên ngọn lửa đèn cồn, đưa nhanh vào bình chứa khí chlorine.
Thí nghiệm 1: 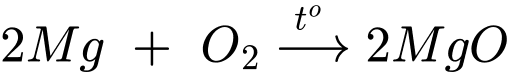
Khi đốt cháy kim loại Magnessium bằng oxygen không khí thì phản ứng xảy ra mãnh liệt, tỏa nhiều nhiệt, phát ra ánh sáng chói và giàu tia tử ngoại.
Thí nghiệm 2: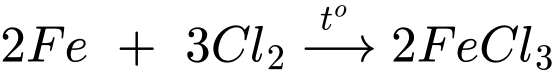
Hiện tượng là sắt cháy sáng và tạo ra khói màu vàng nâu.
Phân tích các phát biểu:
✔️ a. Đúng. Thí nghiệm 1 phản ứng xuất hiện ánh sáng chói và tia tử ngoại.
❌ b. Sai. Thí nghiệm 2, Fe bị oxi hóa lên số oxi hóa +3.
✔️ c. Đúng. Mg có số oxi hóa tăng từ 0 lên +2 và Fe có số oxi hóa tăng từ 0 lên +3 nên cả hai thí nghiệm đều chứng minh tính khử của kim loại.
❌ d. Sai. Hiện tượng khói màu vàng nâu do có FeCl3 sinh ra nên khi thay sợi dây sắt ở thí nghiệm 2 bằng dây magnesium thì hiện tượng thu được không có khói màu vàng nâu.
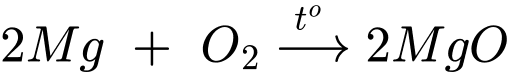
Khi đốt cháy kim loại Magnessium bằng oxygen không khí thì phản ứng xảy ra mãnh liệt, tỏa nhiều nhiệt, phát ra ánh sáng chói và giàu tia tử ngoại.
Thí nghiệm 2:
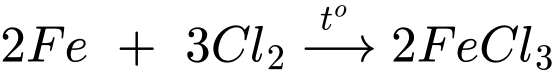
Hiện tượng là sắt cháy sáng và tạo ra khói màu vàng nâu.
Phân tích các phát biểu:
✔️ a. Đúng. Thí nghiệm 1 phản ứng xuất hiện ánh sáng chói và tia tử ngoại.
❌ b. Sai. Thí nghiệm 2, Fe bị oxi hóa lên số oxi hóa +3.
✔️ c. Đúng. Mg có số oxi hóa tăng từ 0 lên +2 và Fe có số oxi hóa tăng từ 0 lên +3 nên cả hai thí nghiệm đều chứng minh tính khử của kim loại.
❌ d. Sai. Hiện tượng khói màu vàng nâu do có FeCl3 sinh ra nên khi thay sợi dây sắt ở thí nghiệm 2 bằng dây magnesium thì hiện tượng thu được không có khói màu vàng nâu.
Câu 22 [703018]: Lactose là một hợp chất carbohydrate có trong sữa và các sản phẩm từ sữa khác.
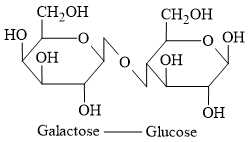
Khi lactose được tiêu hóa, liên kết giữa hai monosaccharide bị phá vỡ. Enzyme chịu trách nhiệm phá vỡ liên kết là lactase, được tìm thấy trong ruột non. Hàng triệu người thiếu hụt đủ lượng lactase, khiến họ không thể tiêu hóa lactose đầy đủ, dẫn đến tình trạng được gọi là không dung nạp lactose. Nghiên cứu biểu đồ và trả lời các câu hỏi.
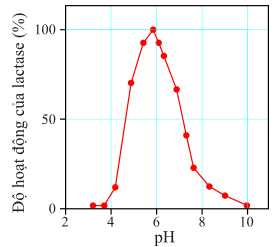

Khi lactose được tiêu hóa, liên kết giữa hai monosaccharide bị phá vỡ. Enzyme chịu trách nhiệm phá vỡ liên kết là lactase, được tìm thấy trong ruột non. Hàng triệu người thiếu hụt đủ lượng lactase, khiến họ không thể tiêu hóa lactose đầy đủ, dẫn đến tình trạng được gọi là không dung nạp lactose. Nghiên cứu biểu đồ và trả lời các câu hỏi.

Phân tích các phát biểu:
✔️ a) Đúng. Enzyme lactase sẽ thủy phân lactose thành glucose và galactose do lactose cấu tạo từ glucose và galactose.
✔️ b) Đúng. Tại pH = 6 độ hoạt động của lactase lớn nhất là 100% nên lượng sản phẩm monosacchride thu được là lớn nhất.
❌ c) Sai. Tại pH = 5,5 độ hoạt động của lactase khoảng 90%.
❌ d) Sai. Độ hoạt động của lactase giảm khi tăng pH từ 6 – 10.
✔️ a) Đúng. Enzyme lactase sẽ thủy phân lactose thành glucose và galactose do lactose cấu tạo từ glucose và galactose.
✔️ b) Đúng. Tại pH = 6 độ hoạt động của lactase lớn nhất là 100% nên lượng sản phẩm monosacchride thu được là lớn nhất.
❌ c) Sai. Tại pH = 5,5 độ hoạt động của lactase khoảng 90%.
❌ d) Sai. Độ hoạt động của lactase giảm khi tăng pH từ 6 – 10.
PHẦN III. Thí sinh trả lời từ câu 1 đến 6. Thí sinh điền kết quả mỗi câu vào mỗi ô trả lời tương ứng theo hướng dẫn của phiếu trả lời.
Câu 23 [1010077]: Tơ nylon-6,6 có tính dai, mềm, óng mượt, ít thấm nước, giặt mau khô, được dùng để dệt vải may mặc, dệt bít tất, đan lưới, bện dây cáp, dây dù. Polymer dùng sản xuất tơ nylon-6,6 là poly(hexamethylene adipamide). Poly(hexamethylene adipamide) được tạo thành bằng phản ứng trùng ngưng giữa hexamethylene diamine (H2N[CH2]6NH2) và adipic acid (HOOC[CH2]4COOH). Phần trăm khối lượng của nitrogen trong poly(hexamethylene adipamide) bằng a%. Giá trị của a bằng bao nhiêu (làm tròn kết quả đến hàng phần mười)?
Poly(hexamethylene adipamide) là (-OC[CH2]4CONH[CH2]6NH-)n
Phân tử khối = 226 amu
Ta có phần trăm khối lượng của N là:
% N = 28/226 = 12,4%
Điền đáp án: 12,4
Phân tử khối = 226 amu
Ta có phần trăm khối lượng của N là:
% N = 28/226 = 12,4%
Điền đáp án: 12,4
Câu 24 [704384]: Phức chất [Cu(NH3)4]2+ được hình thành khi cho dung dịch NH3 tới dư vào dung dịch chứa ion Cu2+. Cần thay thế bao nhiêu phối tử NH3 bằng phối tử Cl– để thu được phức chất có điện tích là 2–?
Điện tích của phức chất được tính bằng tổng điện tích của ion trung tâm Cu2+ cộng với điện tích của các phối tử.
▪ Cu2+: Điện tích là +2.
▪ Mỗi phối tử NH3: Trung hòa (điện tích 0).
▪ Mỗi phối tử Cl−: Điện tích là −1.
Để phức chất có điện tích là −2, ta thay số lượng a phối tử NH3 bằng Cl−, khi đó:
+2 + 0 × (4 − a) − 1 × a
⇔ −2 + 2 − a = −2
⇔ a = 4
⟶ Khi thay thế 4 phối tử NH3 bằng phối tử Cl− thì phức chất sẽ mang điện tích là 2–.
[Cu(NH3)4]2+ + 4Cl− ⟶ [Cu(Cl)4]2- + 4NH3
⇒ Điền đáp án: 4
▪ Cu2+: Điện tích là +2.
▪ Mỗi phối tử NH3: Trung hòa (điện tích 0).
▪ Mỗi phối tử Cl−: Điện tích là −1.
Để phức chất có điện tích là −2, ta thay số lượng a phối tử NH3 bằng Cl−, khi đó:
+2 + 0 × (4 − a) − 1 × a
⇔ −2 + 2 − a = −2
⇔ a = 4
⟶ Khi thay thế 4 phối tử NH3 bằng phối tử Cl− thì phức chất sẽ mang điện tích là 2–.
[Cu(NH3)4]2+ + 4Cl− ⟶ [Cu(Cl)4]2- + 4NH3
⇒ Điền đáp án: 4
Câu 25 [684454]: Ứng với công thức phân tử C4H8O có bao nhiêu hợp chất mạch hở bền khi tác dụng với NaBH4 tạo ra alcohol bậc một?
Alcohol bậc 1: Nhóm -OH được gắn vào nguyên tử carbon bậc 1
Ứng với công thức phân tử C4H8O các hợp chất mạch hở tác dụng với NaBH4 tạo ra alcohol bậc 1:
(1). CH3 – CH2 – CH2 – CHO
(2). CH3 – CH(CH3)– CHO
⇒ Điền đáp án: 2
Ứng với công thức phân tử C4H8O các hợp chất mạch hở tác dụng với NaBH4 tạo ra alcohol bậc 1:
(1). CH3 – CH2 – CH2 – CHO
(2). CH3 – CH(CH3)– CHO
⇒ Điền đáp án: 2
Câu 26 [703976]: Làm mềm 10 m3 nước cứng có tổng nồng độ Mg2+ và Ca2+ là 5,5 mmol/L bằng Na2CO3, thu được nước có tổng nồng độ Mg2+ và Ca2+ là 1,5 mmol/L. Coi toàn bộ lượng Na2CO3 cho vào đều chuyển hết thành kết tủa CaCO3 và MgCO3. Khối lượng Na2CO3 đã dùng là bao nhiêu gam?
Đổi 10 m3 = 10000 L
Mg2+ + CO32- ⟶ MgCO3
Ca2+ + CO32- ⟶ CaCO3
Số mol Na2CO3 đã dùng để làm mềm 10 m3 nước cứng là
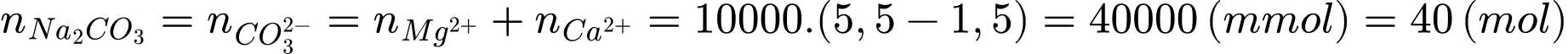
Khối lượng Na2CO3 đã dùng để làm mềm 10 m3 nước cứng là:
mNa2CO3 = 40 . 106 = 4240 (gam)
⇒ Điền đáp án: 4240
Mg2+ + CO32- ⟶ MgCO3
Ca2+ + CO32- ⟶ CaCO3
Số mol Na2CO3 đã dùng để làm mềm 10 m3 nước cứng là
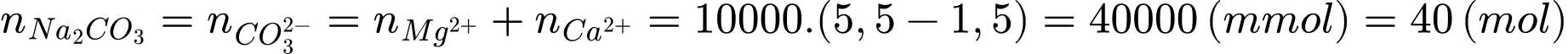
Khối lượng Na2CO3 đã dùng để làm mềm 10 m3 nước cứng là:
mNa2CO3 = 40 . 106 = 4240 (gam)
⇒ Điền đáp án: 4240
Câu 27 [705434]: Methyl salicylate dùng làm thuốc xoa bóp giảm đau, được điều chế theo phản ứng sau:

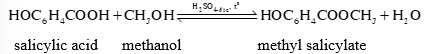
Từ 18,63 tấn salicylic acid có thể sản xuất được tối đa x triệu tuýp thuốc xoa bóp giảm đau. Biết mỗi tuýp thuốc chứa 2,7 gam methyl salicylate và hiệu suất phản ứng tính theo salicylic acid là 75%. Giá trị của x là


Từ 18,63 tấn salicylic acid có thể sản xuất được tối đa x triệu tuýp thuốc xoa bóp giảm đau. Biết mỗi tuýp thuốc chứa 2,7 gam methyl salicylate và hiệu suất phản ứng tính theo salicylic acid là 75%. Giá trị của x là
Đổi 1 tấn = 106 gam
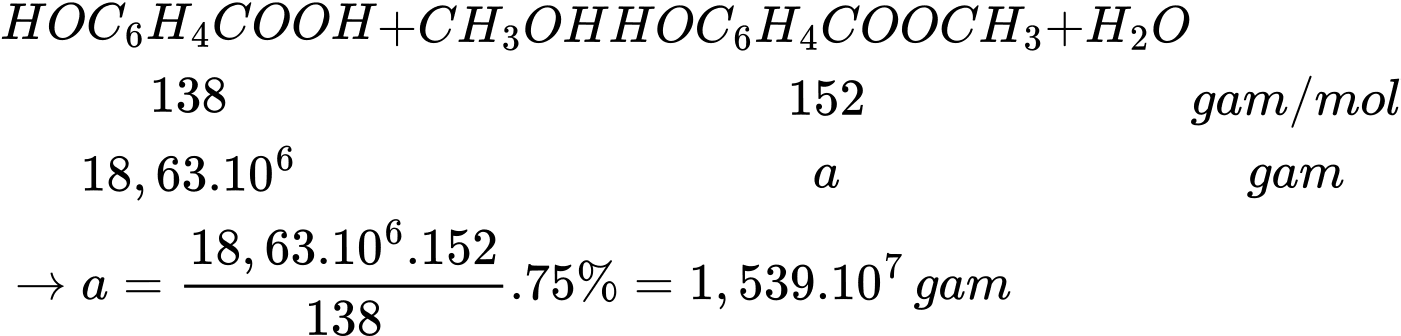
Số tuýp thuốc xoa bóp giảm đau là:
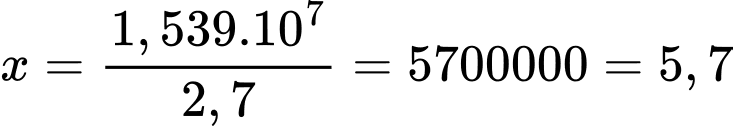 triệu tuýp.
triệu tuýp.
⇒ Điền đáp án: 5,7
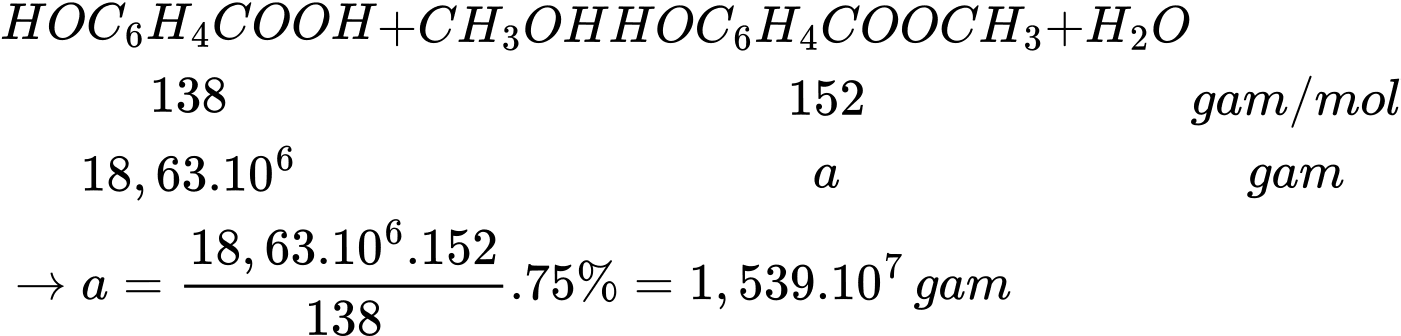
Số tuýp thuốc xoa bóp giảm đau là:
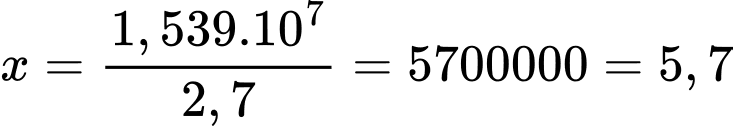 triệu tuýp.
triệu tuýp.⇒ Điền đáp án: 5,7
Câu 28 [704041]: Một mẫu phân bón chứa nguyên tố phosphorus. Tiến hành các bước thí nghiệm để tính hàm lượng phosphorus (P) trong mẫu phân bón trên:
Bước 1: Phân tích 2,684 gam mẫu phân bón và toàn bộ nguyên tố phosphorus được hìnhthành dưới dạng kết tủa (NH4)3PO4.12 MoO3.2HNO3.H2O.
Bước 2: Chia lượng kết tủa làm 100 phần bằng nhau, lấy 1 phần hòa tan trong 50,0 mL dungdịch NaOH 0,5196 M, xảy ra phản ứng theo phương trình:
2(NH4)3PO4.12MoO3.2HNO3.H2O + 56NaOH ⟶24Na2MoO4 + 4NaNO3 + 2Na2HPO4 + 6NH3 +34H2O.
Bước 3: Lượng dư NaOH được trung hòa vừa đủ bởi 20,5 mL HCl 0,5 M.
Tính hàm lượng phosphorus (P) (theo gam) trong 2,684 gam phân bón ban đầu (làm tròn đến hàng phần mười).
Bước 1: Phân tích 2,684 gam mẫu phân bón và toàn bộ nguyên tố phosphorus được hìnhthành dưới dạng kết tủa (NH4)3PO4.12 MoO3.2HNO3.H2O.
Bước 2: Chia lượng kết tủa làm 100 phần bằng nhau, lấy 1 phần hòa tan trong 50,0 mL dungdịch NaOH 0,5196 M, xảy ra phản ứng theo phương trình:
2(NH4)3PO4.12MoO3.2HNO3.H2O + 56NaOH ⟶24Na2MoO4 + 4NaNO3 + 2Na2HPO4 + 6NH3 +34H2O.
Bước 3: Lượng dư NaOH được trung hòa vừa đủ bởi 20,5 mL HCl 0,5 M.
Tính hàm lượng phosphorus (P) (theo gam) trong 2,684 gam phân bón ban đầu (làm tròn đến hàng phần mười).
2(NH4)3PO4.12MoO3.2HNO3.H2O + 56NaOH ⟶24Na2MoO4 + 4NaNO3 + 2Na2HPO4 + 6NH3 +34H2O (*)
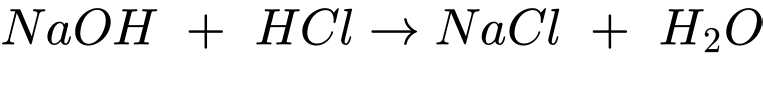 (**)
(**)
Đổi 50 mL = 0,05 L; 20,5 mL = 0,0205 L
Số mol của NaOH là:
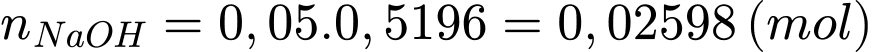
Số mol của HCl phản ứng với lượng dư NaOH là:
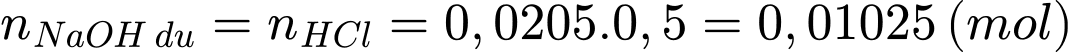
Số mol NaOH tham gia phản ứng (*) là:
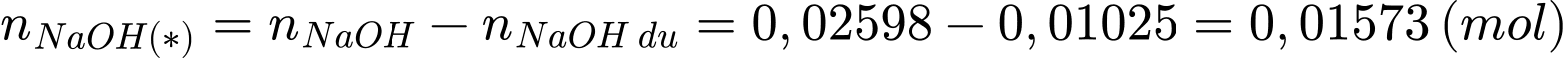
Bảo toàn nguyên tố P:

Hàm lượng phosphorus (P) trong 2,684 gam là:
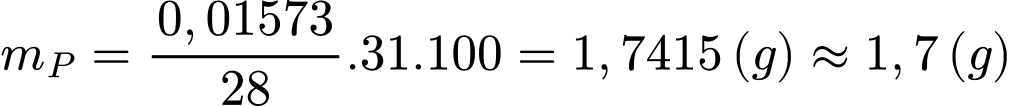
⇒ Điền đáp án: 1,7
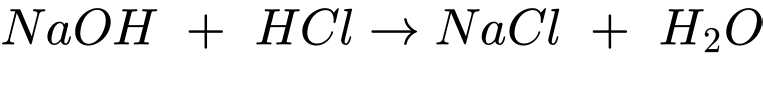 (**)
(**)Đổi 50 mL = 0,05 L; 20,5 mL = 0,0205 L
Số mol của NaOH là:
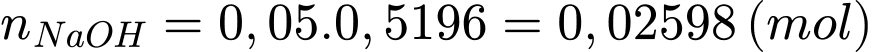
Số mol của HCl phản ứng với lượng dư NaOH là:
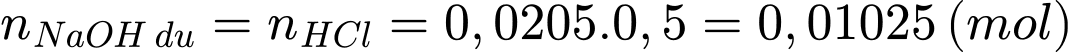
Số mol NaOH tham gia phản ứng (*) là:
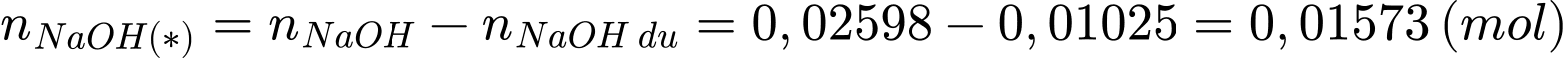
Bảo toàn nguyên tố P:

Hàm lượng phosphorus (P) trong 2,684 gam là:
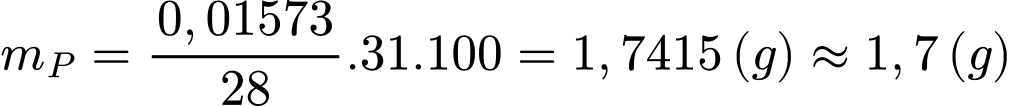
⇒ Điền đáp án: 1,7