PHẦN I. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
Câu 1 [703826]: Một loại giấm ăn có chứa hàm lượng 3,5% acetic acid về thể tích. Tính khối lượng acetic acid trong một can giấm có dung tích 10 L. Biết khối lượng riêng của acetic acid là D = 1,05 g/mL.
A, 367,5 gam.
B, 612,5 gam.
C, 256,7 gam.
D, 61,3 gam.
Đổi 10L = 10000 mL
Thể tích của acetic acid trong 10L dung dịch là 10000.3,5% = 350 (ml)
Khối lượng của acetic acid là:
350.1,05 = 367,5 (gam)
⇒ Chọn đáp án A Đáp án: A
Thể tích của acetic acid trong 10L dung dịch là 10000.3,5% = 350 (ml)
Khối lượng của acetic acid là:
350.1,05 = 367,5 (gam)
⇒ Chọn đáp án A Đáp án: A
Câu 2 [304832]: Thuỷ phân ester C2H5COOCH3 trong môi trường acid HCl thì thu được sản phẩm gồm các chất là
A, HCOOH và CH3OH.
B, CH3COOH và C2H5OH.
C, C2H5COOH và CH3OH.
D, CH3COONa và CH3OH.
Phân tích phản ứng thủy phân ester trong môi trường acid:

⟹ sản phẩm thu được tương ứng là methanol CH3OH và propionate acid CH3CH2COOH
⟹ Chọn đáp án C Đáp án: C

⟹ sản phẩm thu được tương ứng là methanol CH3OH và propionate acid CH3CH2COOH
⟹ Chọn đáp án C Đáp án: C
Câu 3 [706128]: Cho 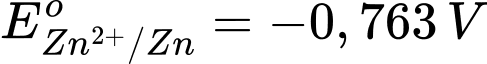 và
và 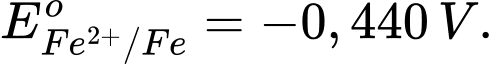 Sức điện động chuẩn của một pin Galvani được tạo thành từ hai cặp oxi hoá – khử Zn2+/Zn và Fe2+/Fe là
Sức điện động chuẩn của một pin Galvani được tạo thành từ hai cặp oxi hoá – khử Zn2+/Zn và Fe2+/Fe là
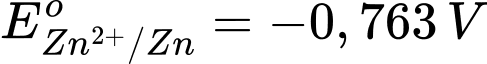 và
và 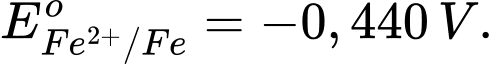 Sức điện động chuẩn của một pin Galvani được tạo thành từ hai cặp oxi hoá – khử Zn2+/Zn và Fe2+/Fe là
Sức điện động chuẩn của một pin Galvani được tạo thành từ hai cặp oxi hoá – khử Zn2+/Zn và Fe2+/Fe là A, –0,323 V.
B, –1,170 V.
C, 0,323 V.
D, 1,170 V.
Phản ứng tại các điện cực:
Tại cathode (khử) : Fe2+ + 2e → Fe
Tại anode (oxi hóa) : Zn → Zn2+ + 2e
Eopin = Eo cathode - Eo anode
= (-0,440 V) - (-0,763 V) = 0,323 V
⟹Chọn đáp án C Đáp án: C
Tại cathode (khử) : Fe2+ + 2e → Fe
Tại anode (oxi hóa) : Zn → Zn2+ + 2e
Eopin = Eo cathode - Eo anode
= (-0,440 V) - (-0,763 V) = 0,323 V
⟹Chọn đáp án C Đáp án: C
Câu 4 [309511]: Trùng hợp propylene thu được polymer có tên gọi là
A, Polyethylene.
B, Polystyrene.
C, Polypropylene.
D, Poly(vinyl chloride).
Phản ứng trùng hợp propylene:
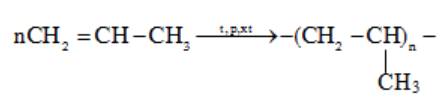
⇒ Trùng hợp propylene thu được polymer có tên gọi là polypropylene.
⇒ Chọn đáp án C Đáp án: C
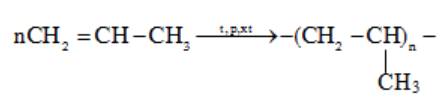
⇒ Trùng hợp propylene thu được polymer có tên gọi là polypropylene.
⇒ Chọn đáp án C Đáp án: C
Câu 5 [305040]: Số nhóm chức ester có trong mỗi phân tử chất béo là
A, 1.
B, 4.
C, 2.
D, 3.
HD: ► Chất béo là các triester (ester ba chức) của glycerol với các acid béo, gọi chung là các triglyceride.

Triester ⇄ Ester 3 chức (tri = 3)
⇒ Chọn đáp án D Đáp án: D

Triester ⇄ Ester 3 chức (tri = 3)
⇒ Chọn đáp án D Đáp án: D
Câu 6 [705704]: Adrenaline là hormon tuyến thượng thận có tác dụng làm tăng huyết áp. Adrenaline có công thức cấu tạo như sau:
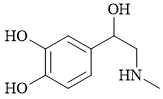
Adrenaline không chứa loại nhóm chức nào sau đây?

Adrenaline không chứa loại nhóm chức nào sau đây?
A, phenol.
B, alcohol.
C, amide.
D, amine.
Adrenaline chứa loại nhóm chức alcohol, phenol và amine:
- Nhóm hydroxyl (-OH) được gắn vào một nguyên tử carbon no được gọi là nhóm chức alcohol.
- Nhóm hydroxyl (-OH) được gắn vào vòng benzene được gọi là nhóm chức phenol.
- Nhóm chức amine (NH) của adrenaline hình thành khi thay thế hai nguyên tử hydrogen của phân tử ammonia (NH3).
Adrenaline không chứa nhóm chức amide do không có nhóm hydroxyl (-OH) được thay thế bằng một nhóm amino (-NH2, -NHR, hoặc -NR2).
⇒ Chọn đáp án C Đáp án: C
- Nhóm hydroxyl (-OH) được gắn vào một nguyên tử carbon no được gọi là nhóm chức alcohol.
- Nhóm hydroxyl (-OH) được gắn vào vòng benzene được gọi là nhóm chức phenol.
- Nhóm chức amine (NH) của adrenaline hình thành khi thay thế hai nguyên tử hydrogen của phân tử ammonia (NH3).
Adrenaline không chứa nhóm chức amide do không có nhóm hydroxyl (-OH) được thay thế bằng một nhóm amino (-NH2, -NHR, hoặc -NR2).
⇒ Chọn đáp án C Đáp án: C
Câu 7 [560684]: Nguyên tắc tách kim loại ra khỏi hợp chất của chúng là
A, Khử ion kim loại trong hợp chất thành nguyên tử.
B, Oxi hoá ion kim loại trong hợp chất thành nguyên tử.
C, Hoà tan các khoáng vật có trong quặng để thu được kim loại.
D, Dựa trên tính chất của kim loại như từ tính, khối lượng riêng lớn để tách chúng ra khỏi quặng.
Trong hợp chất, nguyên tố kim loại tồn tại dạng cation kim loại (Mn+) nên nguyên tắc chung để tách được nguyên tố kim loại ra khỏi hợp chất cần thực hiện phản ứng khử cation kim loại thành nguyên tử.
Đáp án: A
Mn+ + ne ⟶ M
⇒ Chọn đáp án A
Câu 8 [702608]: 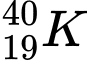 là một đồng vị phóng xạ của nguyên tố potassium có mặt trong cơ thể con người. Tổng số các loại hạt (proton, neutron và electron) trong đồng vị này là
là một đồng vị phóng xạ của nguyên tố potassium có mặt trong cơ thể con người. Tổng số các loại hạt (proton, neutron và electron) trong đồng vị này là
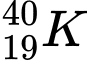 là một đồng vị phóng xạ của nguyên tố potassium có mặt trong cơ thể con người. Tổng số các loại hạt (proton, neutron và electron) trong đồng vị này là
là một đồng vị phóng xạ của nguyên tố potassium có mặt trong cơ thể con người. Tổng số các loại hạt (proton, neutron và electron) trong đồng vị này là A, 40.
B, 59.
C, 21.
D, 61.
Đồng vị potassium này có số hạt proton = số hạt electron = 19 hạt.
Số khối: A = Z + N ⇔ 40 = 19 + N ⇔ N = 21 hạt.
Tổng số các loại hạt trong đồng vị này là: 19 + 19 + 21 = 59 hạt.
⇒ Chọn đáp án B Đáp án: B
Số khối: A = Z + N ⇔ 40 = 19 + N ⇔ N = 21 hạt.
Tổng số các loại hạt trong đồng vị này là: 19 + 19 + 21 = 59 hạt.
⇒ Chọn đáp án B Đáp án: B
Câu 9 [705781]: "Phương pháp Solvay dùng để sản xuất soda và baking soda sử dụng nguồn nguyên liệu dễ tìm trong tự nhiên là ..(1)..., đá vôi và ...(2)...”. Nội dung phù hợp trong ô trống (1), (2) lần lượt là
A, muối ăn, ammonia.
B, muối ăn, carbon dioxide.
C, cát, ammonia.
D, cát, carbon dioxide.
"Phương pháp Solvay dùng để sản xuất soda và baking soda sử dụng nguồn nguyên liệu dễ tìm trong tự nhiên là muối ăn, đá vôi và ammonia”
Giải thích:
Phương pháp Solvay là một quy trình công nghiệp quan trọng để sản xuất soda (Na2CO3) và baking soda (NaHCO3). Phương pháp này sử dụng nguyên liệu rẻ, dễ tìm trong tự nhiên gồm:
- Nước muối (NaCl) – nguồn cung cấp ion Na+.
- Đá vôi (CaCO3) – dùng để tạo CO2 và CaO.
- Ammonia (NH3) – giúp kết tủa NaHCO3 từ dung dịch.
⇒ Chọn đáp án A Đáp án: A
Giải thích:
Phương pháp Solvay là một quy trình công nghiệp quan trọng để sản xuất soda (Na2CO3) và baking soda (NaHCO3). Phương pháp này sử dụng nguyên liệu rẻ, dễ tìm trong tự nhiên gồm:
- Nước muối (NaCl) – nguồn cung cấp ion Na+.
- Đá vôi (CaCO3) – dùng để tạo CO2 và CaO.
- Ammonia (NH3) – giúp kết tủa NaHCO3 từ dung dịch.
⇒ Chọn đáp án A Đáp án: A
Câu 10 [705748]: Hàm lượng glucose có trong mẫu dược phẩm có thể được xác định bằng phương pháp chuẩn độ với iodine như sau: Cho một thể tích chính xác dung dịch chứa glucose vào một thể tích chính xác và dư nước iodine. Sau đó, thêm vào dung dịch sau phản ứng vài giọt dung dịch X, rồi vừa lắc vừa nhỏ từ từ dung dịch sodium thiosulfate (Na2S2O3) có nồng độ xác định vào dung dịch ở trên đến khi mất màu xanh thì dừng lại. Ghi thể tích dung dịch Na2S2O3 đã tiêu tốn:
I2 + 2Na2S2O3 2NaI + Na2S4O6
2NaI + Na2S4O6
Dung dịch X được sử dụng trong thí nghiệm trên nhằm mục đích chính là
I2 + 2Na2S2O3
 2NaI + Na2S4O6
2NaI + Na2S4O6Dung dịch X được sử dụng trong thí nghiệm trên nhằm mục đích chính là
A, nhận biết hàm lượng glucose dư trong dung dịch.
B, nhận biết hàm lượng iodine dư trong dung dịch.
C, nhận biết hàm lượng sodium thiosulfate dư trong dung dịch.
D, phản ứng với lượng dư dung dịch sodium thiosulfate.
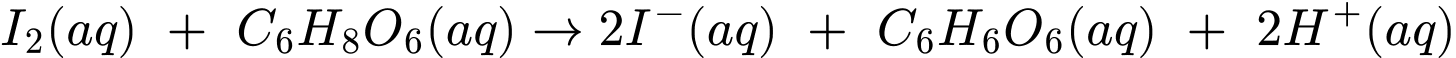
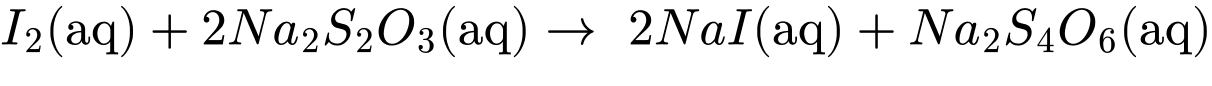
Dung dịch X là hồ tinh bột mục đích nhận biết hàm lượng Iodine dư trong dung dịch sau phản ứng.
⇒ Chọn đáp án B Đáp án: B
Câu 11 [193258]: Biến thiên enthalpy của một phản ứng được ghi ở sơ đồ sau:
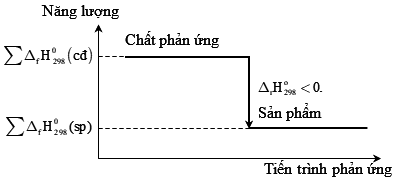
Kết luận nào sau đây là đúng?

Kết luận nào sau đây là đúng?
A, Phản ứng tỏa nhiệt.
B, Năng lượng chất tham gia phản ứng nhỏ hơn năng lượng sản phẩm.
C, Biến thiên enthalpy của phản ứng là a kJ/mol.
D, Phản ứng thu nhiệt.
Phân tích các phát biểu:
✔️a.Phản ứng toả nhiệt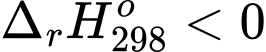 phản ứng giải phóng nhiệt ra môi trường.
phản ứng giải phóng nhiệt ra môi trường.
❌b.Sơ đồ cho thấy năng lượng chất tham gia lớn hơn năng lượng sản phẩm.
❌c. Phản ứng toả nhiệt biến thiên enthalpy của phản ứng là ‒ a kJ.
❌d. Phản ứng trên là phản ứng toả nhiệt.
Chọn đáp án A Đáp án: A
✔️a.Phản ứng toả nhiệt
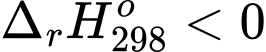 phản ứng giải phóng nhiệt ra môi trường.
phản ứng giải phóng nhiệt ra môi trường.❌b.Sơ đồ cho thấy năng lượng chất tham gia lớn hơn năng lượng sản phẩm.
❌c. Phản ứng toả nhiệt biến thiên enthalpy của phản ứng là ‒ a kJ.
❌d. Phản ứng trên là phản ứng toả nhiệt.
Chọn đáp án A Đáp án: A
Câu 12 [308797]: Thủy phân hoàn toàn 1 mol pentapeptide X, thu được 2 mol glycine (Gly), 1 mol alanine (Ala), 1 mol valine (Val) và 1 mol phenylalanine (Phe). Thủy phân không hoàn toàn X thu được dipeptide Val- Phe và tripeptide Gly-Ala-Val nhưng không thu được dipeptide Gly-Gly. Chất X có công thức là
A, Gly-Phe-Gly-Ala-Val.
B, Gly-Ala-Val-Val-Phe.
C, Gly-Ala-Val-Phe-Gly.
D, Val-Phe-Gly-Ala-Gly.
Vì X chỉ chứa 1 Val nên Val trong các peptide tạo thành phải trùng nhau ⟹ X chứa Gly-Ala-Val-Phe.
X không chứa Gly-Gly nên X là Gly-Ala-Val-Phe-Gly. Đáp án: C
X không chứa Gly-Gly nên X là Gly-Ala-Val-Phe-Gly. Đáp án: C
Câu 13 [705359]: Khi tan trong nước, muối của các kim loại chuyển tiếp …(1)… thành các ion. Sau đó, cation kim loại chuyển tiếp (Mn+) thường nhận các cặp electron hoá trị riêng từ các phân tử H2O để hình thành các liên kêt cho - nhận, tạo ra phức chất aqua có dạng tổng quát là ...(2)... Nội dung phù hợp trong ô trống (1), (2) lần lượt là
A, điện li, [M(OH2)m]n+.
B, điện li, [M(OH2)n]+.
C, phân li, [M(OH2)n]+.
D, phân li, [M(OH2)m]n+.
Khi tan trong nước, muối của các kim loại chuyển tiếp phân li thành các ion. Sau đó, cation kim loại chuyển tiếp (Mn+) thường nhận các cặp electron hoá trị riêng từ các phân tử H2O để hình thành các liên kêt cho - nhận, tạo ra phức chất aqua có dạng tổng quát là [M(OH2)m]n+.
- Khi tan trong nước, muối của các kim loại chuyển tiếp phân li thành các ion. Sau đó, cation kim loại chuyển tiếp (Mn+) thường nhận các cặp electron hóa trị riêng từ các phân tử H2O để hình thành các liên kết cho – nhận, tạo ra phức chất aqua theo phương trình hóa học tổng quát sau:
Mn+(aq) + mH2O(l) →[M(OH2)m]n+(aq)
- Trong đó:
+ n là giá trị điện tích của cation kim loại M
+ m là số phối tử H2O
+ [M(OH2)m]n+ là công thức tổng quát của phức chất aqua của Mn+.
⇒ Chọn đáp án D Đáp án: D
- Khi tan trong nước, muối của các kim loại chuyển tiếp phân li thành các ion. Sau đó, cation kim loại chuyển tiếp (Mn+) thường nhận các cặp electron hóa trị riêng từ các phân tử H2O để hình thành các liên kết cho – nhận, tạo ra phức chất aqua theo phương trình hóa học tổng quát sau:
Mn+(aq) + mH2O(l) →[M(OH2)m]n+(aq)
- Trong đó:
+ n là giá trị điện tích của cation kim loại M
+ m là số phối tử H2O
+ [M(OH2)m]n+ là công thức tổng quát của phức chất aqua của Mn+.
⇒ Chọn đáp án D Đáp án: D
Câu 14 [1105716]: Cho phản ứng thuận nghịch giữa hydrogen và iodine để tạo thành hydrogen iodide: H2(g) + I2(g) 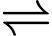 2HI(g). Biểu đồ cho thấy sự thay đổi nồng độ của chất phản ứng và sản phẩm khi phản ứng đạt đến trạng thái cân bằng động.
2HI(g). Biểu đồ cho thấy sự thay đổi nồng độ của chất phản ứng và sản phẩm khi phản ứng đạt đến trạng thái cân bằng động.
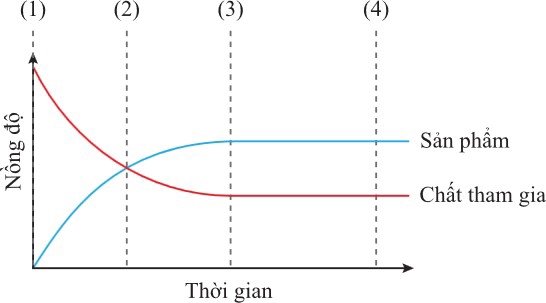
Trạng thái cân bằng đạt được tại điểm nào trên biểu đồ?
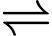 2HI(g). Biểu đồ cho thấy sự thay đổi nồng độ của chất phản ứng và sản phẩm khi phản ứng đạt đến trạng thái cân bằng động.
2HI(g). Biểu đồ cho thấy sự thay đổi nồng độ của chất phản ứng và sản phẩm khi phản ứng đạt đến trạng thái cân bằng động.
Trạng thái cân bằng đạt được tại điểm nào trên biểu đồ?
A, (1).
B, (2).
C, (3).
D, (4).
Trạng thái cân bằng đạt được khi nồng độ của tất cả các chất tham gia và sản phẩm không đổi theo thời gian.
Trên biểu đồ:
• Nồng độ của chất tham gia (đường màu đỏ) và sản phẩm (đường màu xanh) bắt đầu ổn định (không thay đổi) tại thời điểm (3).
• Thời điểm (2) chỉ là thời điểm nồng độ của hai bên bằng nhau, không phải là trạng thái cân bằng.
Chọn đáp án C. (3). Đáp án: C
Trên biểu đồ:
• Nồng độ của chất tham gia (đường màu đỏ) và sản phẩm (đường màu xanh) bắt đầu ổn định (không thay đổi) tại thời điểm (3).
• Thời điểm (2) chỉ là thời điểm nồng độ của hai bên bằng nhau, không phải là trạng thái cân bằng.
Chọn đáp án C. (3). Đáp án: C
Câu 15 [703821]: Để khinh khí cầu có thể bay được thì khí được bơm vào khinh khí cầu là hydrogen, nó sẽ bay rất cao do khí hydrogen rất nhẹ. Tuy nhiên, đã có nhiều vụ nổ thương tâm gây ra bởi khinh khí cầu hydrogen vì hydrogen tạo với oxygen hỗn hợp nổ rất mạnh.
(*) 2H2(g) + O2(g) 2H2O(l);
2H2O(l); 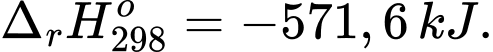
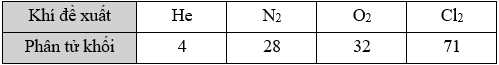
Để thay thế hydrogen, một số khí dưới đây đã được đề xuất để bơm vào khinh khí cầu:
Cho các phát biểu sau:
(a) Phản ứng (*) xảy ra tỏa nhiệt, sự giãn nở thể tích đột ngột nên gây ra sự nổ.
(b) Có thể sử dụng khí O2 thay thế cho H2 để bơm vào khinh khí cầu.
(c) Không sử dụng khí Cl2 thay thế vì Cl2 cũng phản ứng và gây nổ rất mạnh như H2.
(d) Sự nổ khí hydrogen có thể được kiểm soát bằng cách ngăn chặn khí hydrogen tuyệt đối không tiếp xúc với khí oxygen.
Các phát biểu đúng là
(*) 2H2(g) + O2(g)
 2H2O(l);
2H2O(l); 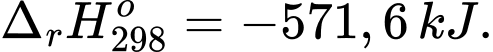
Để thay thế hydrogen, một số khí dưới đây đã được đề xuất để bơm vào khinh khí cầu:

Cho các phát biểu sau:
(a) Phản ứng (*) xảy ra tỏa nhiệt, sự giãn nở thể tích đột ngột nên gây ra sự nổ.
(b) Có thể sử dụng khí O2 thay thế cho H2 để bơm vào khinh khí cầu.
(c) Không sử dụng khí Cl2 thay thế vì Cl2 cũng phản ứng và gây nổ rất mạnh như H2.
(d) Sự nổ khí hydrogen có thể được kiểm soát bằng cách ngăn chặn khí hydrogen tuyệt đối không tiếp xúc với khí oxygen.
Các phát biểu đúng là
A, (a), (c).
B, (b), (c), (d).
C, (a), (b), (c).
D, (a), (c), (d).
Phân tích các phát biểu:
✔️ (a) Đúng. Biến thiên enthalpy của phản ứng (*) rất âm nên đây là phản ứng tỏa nhiệt rất mạnh. Nhiệt lượng lớn giải phóng trong thời gian ngắn làm không khí xung quanh giãn nở đột ngột, dẫn đến vụ nổ.
❌ (b) Sai. Khối lượng phân tử của oxygen (32) lớn hơn khối lượng phân tử của không khí (29) nên lực nâng của khí O2 sẽ nhỏ, không phù hợp để bơm vào khinh khí cầu để thay thế H2.
✔️ (c) Đúng. Không sử dụng khí Cl2 thay thế được vì Cl2 là khí độc và nặng hơn không khí, ngoài ra Cl2 có thể tham gia phản ứng nguy hiểm với hydrogen nếu có mặt: H2 + Cl2 –(ánh sáng)→ 2HCl. Đây là phản ứng tỏa nhiệt mạnh, cũng có thể gây nổ.
✔️ (d) Đúng. Để ngăn chặn sự nổ, cần đảm bảo rằng hydrogen không tiếp xúc với oxygen, vì hỗn hợp này mới là nguyên nhân gây nổ. Đây là một biện pháp an toàn hợp lý và khả thi.
➥ Các phát biểu đúng là (a) (c) (d)
⇒ Chọn đáp án D Đáp án: D
✔️ (a) Đúng. Biến thiên enthalpy của phản ứng (*) rất âm nên đây là phản ứng tỏa nhiệt rất mạnh. Nhiệt lượng lớn giải phóng trong thời gian ngắn làm không khí xung quanh giãn nở đột ngột, dẫn đến vụ nổ.
❌ (b) Sai. Khối lượng phân tử của oxygen (32) lớn hơn khối lượng phân tử của không khí (29) nên lực nâng của khí O2 sẽ nhỏ, không phù hợp để bơm vào khinh khí cầu để thay thế H2.
✔️ (c) Đúng. Không sử dụng khí Cl2 thay thế được vì Cl2 là khí độc và nặng hơn không khí, ngoài ra Cl2 có thể tham gia phản ứng nguy hiểm với hydrogen nếu có mặt: H2 + Cl2 –(ánh sáng)→ 2HCl. Đây là phản ứng tỏa nhiệt mạnh, cũng có thể gây nổ.
✔️ (d) Đúng. Để ngăn chặn sự nổ, cần đảm bảo rằng hydrogen không tiếp xúc với oxygen, vì hỗn hợp này mới là nguyên nhân gây nổ. Đây là một biện pháp an toàn hợp lý và khả thi.
➥ Các phát biểu đúng là (a) (c) (d)
⇒ Chọn đáp án D Đáp án: D
Câu 16 [705495]: Nitrogen trong không khí có vai trò nào sau đây?
A, Hình thành sấm sét.
B, Tham gia quá trình quang hợp của cây.
C, Tham gia hình thành mây.
D, Cung cấp đạm tự nhiên cho cây trồng.
❌ A. Sấm sét là hiện tượng do sự phóng điện trong khí quyển, không phải do nitrogen gây ra. Tuy nhiên, sấm sét giúp chuyển hóa nitrogen thành hợp chất có ích cho cây, chứ nitrogen không phải là nguyên nhân hình thành sấm sét.
❌ B. Quang hợp chủ yếu sử dụng CO2, nước và ánh sáng để tổng hợp chất hữu cơ, không liên quan trực tiếp đến nitrogen trong không khí.
❌ C. Mây được hình thành do sự ngưng tụ của hơi nước trong không khí, không liên quan đến nitrogen.
✔️ D. Trong không khí nitrogen chiếm khoảng 78% thể tích, nhờ các quá trình tự nhiên như sấm sét mà nitrogen chuyển hóa thành các hợp chất mà cây có thể hấp thu được , đó là đạm tự nhiên cho cây.
⇒ Chọn đáp án D Đáp án: D
❌ B. Quang hợp chủ yếu sử dụng CO2, nước và ánh sáng để tổng hợp chất hữu cơ, không liên quan trực tiếp đến nitrogen trong không khí.
❌ C. Mây được hình thành do sự ngưng tụ của hơi nước trong không khí, không liên quan đến nitrogen.
✔️ D. Trong không khí nitrogen chiếm khoảng 78% thể tích, nhờ các quá trình tự nhiên như sấm sét mà nitrogen chuyển hóa thành các hợp chất mà cây có thể hấp thu được , đó là đạm tự nhiên cho cây.
⇒ Chọn đáp án D Đáp án: D
Sử dụng đoạn thông tin dưới đây để trả lời câu 17 và câu 18:
Nồng độ tổng cộng của Ca2+ và Mg2+ trong mẫu nước cứng được xác định bằng cách chuẩn độ 1 lít mẫu nước bằng dung dịch EDTA4– (EDTA4– có khả năng tạo phức với hai cation):
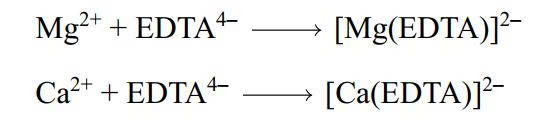
Cần 31,5 mL dung dịch EDTA4– 0,0104 M để đạt đến điểm cuối trong quá trình chuẩn độ. Sau đó, mẫu 1 lít thứ hai được xử lý bằng ion sulfate để kết tủa Ca2+ dưới dạng calcium sulfate kết tủa, loại bỏ kết tủa. Sau đó, chuẩn độ Mg2+ bằng 18,7 mL dung dịch EDTA4– 0,0104 M.
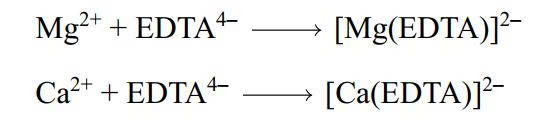
Cần 31,5 mL dung dịch EDTA4– 0,0104 M để đạt đến điểm cuối trong quá trình chuẩn độ. Sau đó, mẫu 1 lít thứ hai được xử lý bằng ion sulfate để kết tủa Ca2+ dưới dạng calcium sulfate kết tủa, loại bỏ kết tủa. Sau đó, chuẩn độ Mg2+ bằng 18,7 mL dung dịch EDTA4– 0,0104 M.
Câu 17 [704303]: Nguyên tử kim loại trung tâm trong cả hai phức chất [Mg(EDTA)]2– và [Ca(EDTA)]2– đều có số oxi hóa là
A, -2.
B, 0.
C, +1.
D, +2.
- Nguyên tử kim loại trung tâm trong cả hai phức chất [Mg(EDTA)]2– và [Ca(EDTA)]2– đều là Mg và Ca, thuộc nhóm kim loại kiềm thổ trong bảng tuần hoàn.
- Vì EDTA là một phối tử không thay đổi điện tích tổng, nên số oxi hóa của kim loại trong cả hai phức chất này chính là điện tích của ion kim loại trước khi tạo phức, cụ thể là:
+ Mg có số oxi hóa là +2.
+ Ca cũng có số oxi hóa là +2.
Vậy số oxi hóa của nguyên tử kim loại trung tâm trong cả hai phức chất đều là +2.
⇒ Chọn đáp án D Đáp án: D
- Vì EDTA là một phối tử không thay đổi điện tích tổng, nên số oxi hóa của kim loại trong cả hai phức chất này chính là điện tích của ion kim loại trước khi tạo phức, cụ thể là:
+ Mg có số oxi hóa là +2.
+ Ca cũng có số oxi hóa là +2.
Vậy số oxi hóa của nguyên tử kim loại trung tâm trong cả hai phức chất đều là +2.
⇒ Chọn đáp án D Đáp án: D
Câu 18 [704304]: Nồng độ của Mg2+ và Ca2+ trong nước cứng theo mg/L lần lượt là
A, 1,9448×10–4 và 1,3312×10–4.
B, 4,6675 và 5,3248.
C, 8,6258×10–3 và 4,2458×10–3.
D, 1,2458 và 2,4871.
Đổi 31,5 mL = 0,0315 L; 18,7 mL = 0,0187 L
(1) Mg2+ + EDTA4- → [Mg(EDTA)]2-
(2) Ca2+ + EDTA4- → [Ca(EDTA)]2-
+ Xử lí lần 1 thông qua mol của EDTA4- xác định tổng mol của 2 ion Ca2+ và Mg2+
Từ PTHH số mol của tổng mol của 2 ion Ca2+ và Mg2+ là:
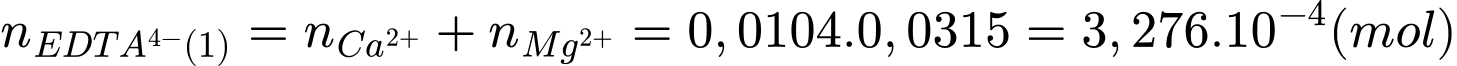
+ Xử lí lần 2: việc tạo kết tủa của ion Ca2+ thành CaSO4 nên thông qua mol của EDTA4- xác định mol của Mg2+
Số mol của Mg2+ là: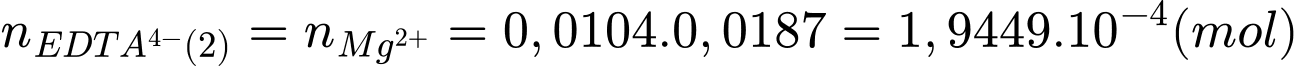
Số mol của Ca2+ trong nước cứng là:
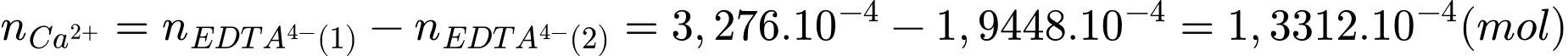
Nồng độ của Mg2+ và Ca2+ trong mẫu nước cứng theo mg/L lần lượt là 4,6675 và 5,3248 mg/L
Nồng độ Mg2+: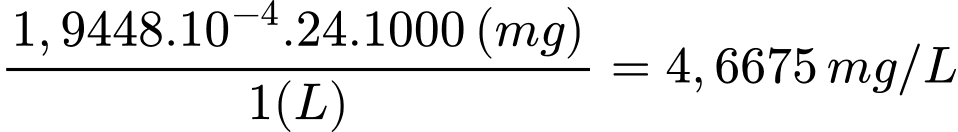
Nồng độ Ca2+: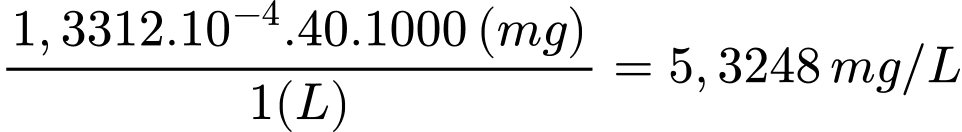
⇒ Chọn đáp án B Đáp án: B
(1) Mg2+ + EDTA4- → [Mg(EDTA)]2-
(2) Ca2+ + EDTA4- → [Ca(EDTA)]2-
+ Xử lí lần 1 thông qua mol của EDTA4- xác định tổng mol của 2 ion Ca2+ và Mg2+
Từ PTHH số mol của tổng mol của 2 ion Ca2+ và Mg2+ là:
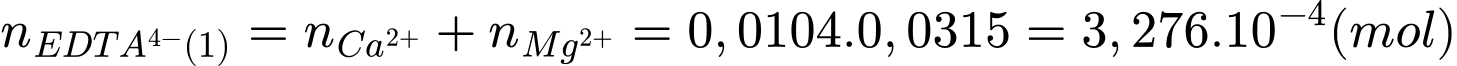
+ Xử lí lần 2: việc tạo kết tủa của ion Ca2+ thành CaSO4 nên thông qua mol của EDTA4- xác định mol của Mg2+
Số mol của Mg2+ là:
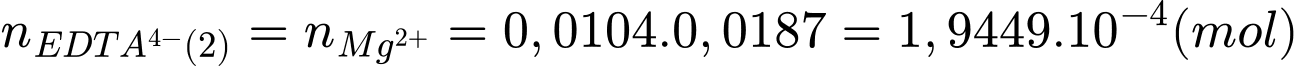
Số mol của Ca2+ trong nước cứng là:
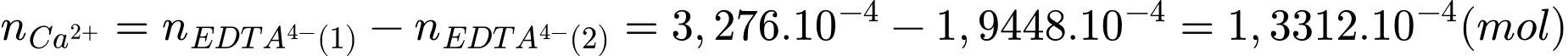
Nồng độ của Mg2+ và Ca2+ trong mẫu nước cứng theo mg/L lần lượt là 4,6675 và 5,3248 mg/L
Nồng độ Mg2+:
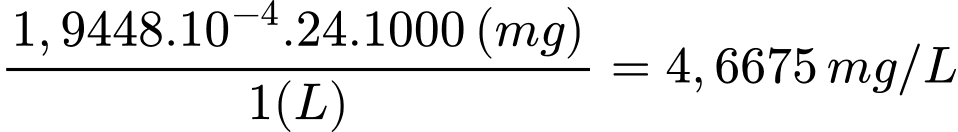
Nồng độ Ca2+:
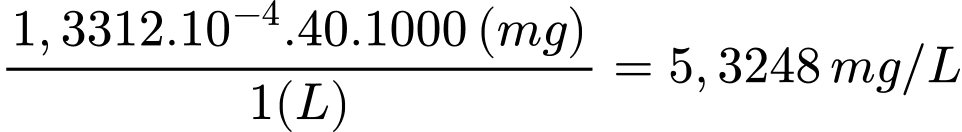
⇒ Chọn đáp án B Đáp án: B
PHẦN II. Thí sinh trả lời từ câu 1 đến câu 4. Trong mỗi ý a), b), c), d) ở mỗi câu, thí sinh chọn đúng hoặc sai.
Câu 19 [1105717]: Các hydrocarbon X, Y, Z (MX < MY < MZ) đều có 7,7% khối lượng hydrogen trong phân tử. Tỷ khối hơi của Z so với không khí bé hơn 4,0. Các chất trên thỏa mãn:
▪ 1 mol chất Z tác dụng tối đa 1 mol Br2 trong CCl4.
▪ Chất X có thể tác dụng tối đa với dung dịch bromine theo tỷ lệ 1 : 2.
▪ Chất Y được điều chế từ chất X và không tác dụng được với dung dịch bromine.
▪ 1 mol chất Z tác dụng tối đa 1 mol Br2 trong CCl4.
▪ Chất X có thể tác dụng tối đa với dung dịch bromine theo tỷ lệ 1 : 2.
▪ Chất Y được điều chế từ chất X và không tác dụng được với dung dịch bromine.
Gọi công thức chung của hydrocarbon là: CxHy
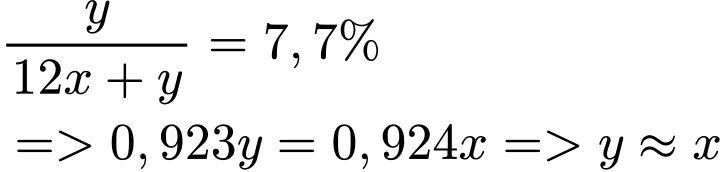 => Công thức phân tử gần đúng nhất có dạng: CnHn
=> Công thức phân tử gần đúng nhất có dạng: CnHn
Mà: Mz < 116 ( Do tỉ khối của Z so với không khí bé hơn 4 )
=> X, Y, Z có thể là: C2H2, C4H4, C6H6, C8H8
Theo đề bài ta có:
• 1 mol Z tác dụng với 1 mol Br2 trong CCl4 => Z có 1 liên kết C = C hoặc 1 vòng kém bền
• 1 mol X tác dụng tối đa với 2 mol Br2 => X có 2 liên kết C = C hoặc 1 liên kết C ≡ C
• X điều chế được Y và Y không tác dụng với Br2 => Y no hoặc có vòng bền
=> Y là : C6H6 – Benzene ; X là: C2H2 – Acetylene ; Z là : C8H8 – Styrene
❌ Nhận định a) – Sai,vì: Tên gọi lần lượt của X, Y, Z là Acetylene, Benzene, Styrene
❌ Nhận định b) – Sai, vì: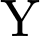 là Benzene (
là Benzene (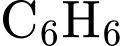 ). Benzene không làm mất màu
). Benzene không làm mất màu 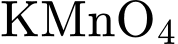 ngay cả khi đun nóng (chỉ các vòng benzene có nhóm alkyl mới dễ bị oxi hóa).
ngay cả khi đun nóng (chỉ các vòng benzene có nhóm alkyl mới dễ bị oxi hóa).
✔️ Nhận định c) – Đúng, vì: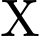 (Acetylene)
(Acetylene) 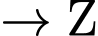 (Styrene).
(Styrene).
(1) Trimer hóa: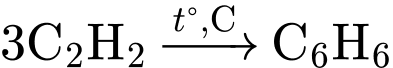 (Benzene).
(Benzene).
(2) Alkyl hóa: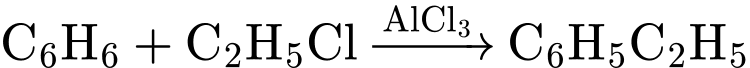 (Ethylbenzene).
(Ethylbenzene).
(3) Dehydrogen hóa: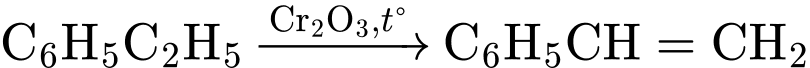 (
(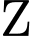 )
)  .
.
Hoặc: (1)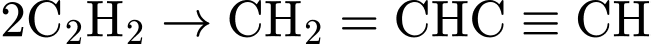 (Vinylacetylene). (2) Phản ứng Dimer hóa của Styrene. (Cách điều chế trực tiếp từ Acetylene
(Vinylacetylene). (2) Phản ứng Dimer hóa của Styrene. (Cách điều chế trực tiếp từ Acetylene  Styrene phức tạp hơn).
Styrene phức tạp hơn).
Tuy nhiên, quá trình phổ biến là (1) , (2)
, (2)  , (3)
, (3) 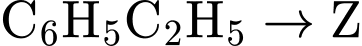 .
.
=> Cần ít nhất 3 phản ứng.
❌ Nhận định d) – Sai, vì :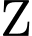 là Styrene (
là Styrene ( ). Styrene phản ứng với
). Styrene phản ứng với 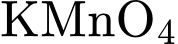 (oxi hóa liên kết
(oxi hóa liên kết 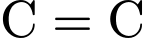 ): (Không nói gì tức là phản ứng ở nhiệt độ thường)
): (Không nói gì tức là phản ứng ở nhiệt độ thường)
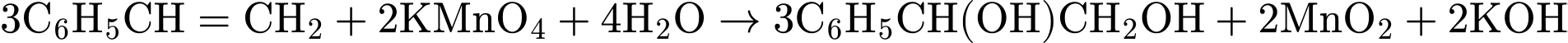
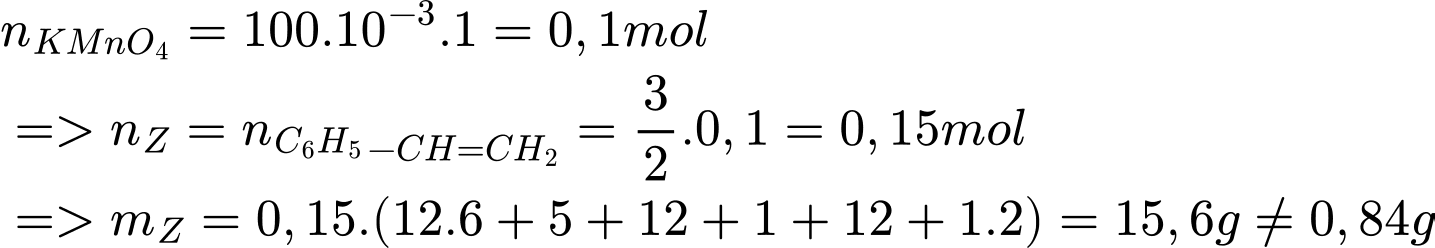
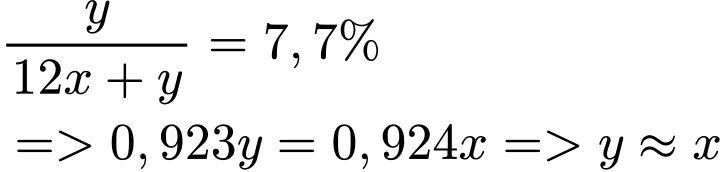 => Công thức phân tử gần đúng nhất có dạng: CnHn
=> Công thức phân tử gần đúng nhất có dạng: CnHnMà: Mz < 116 ( Do tỉ khối của Z so với không khí bé hơn 4 )
=> X, Y, Z có thể là: C2H2, C4H4, C6H6, C8H8
Theo đề bài ta có:
• 1 mol Z tác dụng với 1 mol Br2 trong CCl4 => Z có 1 liên kết C = C hoặc 1 vòng kém bền
• 1 mol X tác dụng tối đa với 2 mol Br2 => X có 2 liên kết C = C hoặc 1 liên kết C ≡ C
• X điều chế được Y và Y không tác dụng với Br2 => Y no hoặc có vòng bền
=> Y là : C6H6 – Benzene ; X là: C2H2 – Acetylene ; Z là : C8H8 – Styrene
❌ Nhận định a) – Sai,vì: Tên gọi lần lượt của X, Y, Z là Acetylene, Benzene, Styrene
❌ Nhận định b) – Sai, vì:
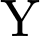 là Benzene (
là Benzene (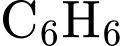 ). Benzene không làm mất màu
). Benzene không làm mất màu 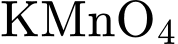 ngay cả khi đun nóng (chỉ các vòng benzene có nhóm alkyl mới dễ bị oxi hóa).
ngay cả khi đun nóng (chỉ các vòng benzene có nhóm alkyl mới dễ bị oxi hóa).✔️ Nhận định c) – Đúng, vì:
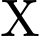 (Acetylene)
(Acetylene) 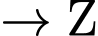 (Styrene).
(Styrene). (1) Trimer hóa:
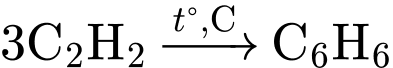 (Benzene).
(Benzene). (2) Alkyl hóa:
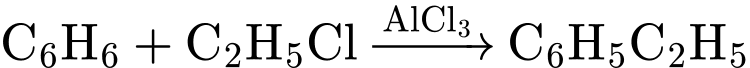 (Ethylbenzene).
(Ethylbenzene). (3) Dehydrogen hóa:
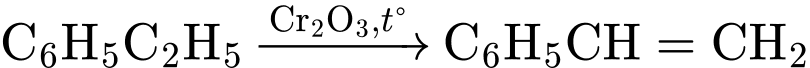 (
(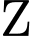 )
)  .
. Hoặc: (1)
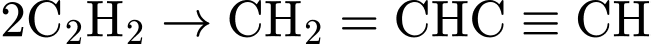 (Vinylacetylene). (2) Phản ứng Dimer hóa của Styrene. (Cách điều chế trực tiếp từ Acetylene
(Vinylacetylene). (2) Phản ứng Dimer hóa của Styrene. (Cách điều chế trực tiếp từ Acetylene  Styrene phức tạp hơn).
Styrene phức tạp hơn). Tuy nhiên, quá trình phổ biến là (1)
 , (2)
, (2)  , (3)
, (3) 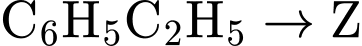 .
. => Cần ít nhất 3 phản ứng.
❌ Nhận định d) – Sai, vì :
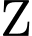 là Styrene (
là Styrene ( ). Styrene phản ứng với
). Styrene phản ứng với 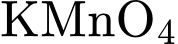 (oxi hóa liên kết
(oxi hóa liên kết 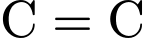 ): (Không nói gì tức là phản ứng ở nhiệt độ thường)
): (Không nói gì tức là phản ứng ở nhiệt độ thường)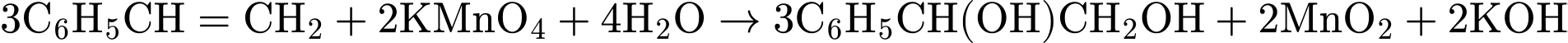
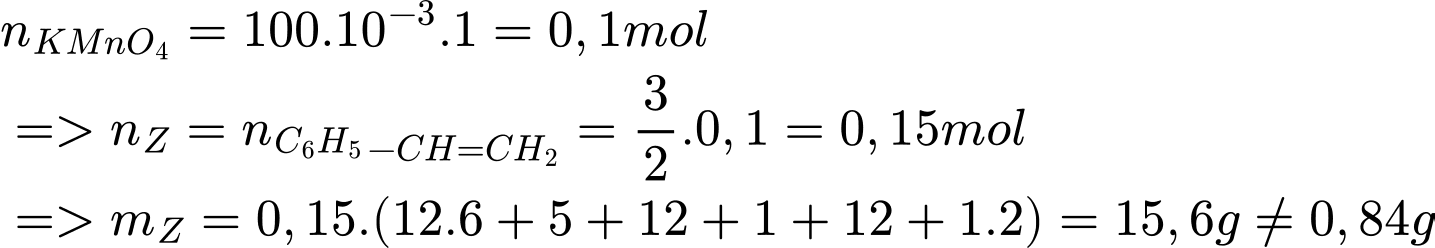
Câu 20 [1105718]: Nhiễm độc chì luôn luôn đáng lo ngại. Trong cơ thể con người, mức độ độc hại của chì có thể được giảm bớt bằng cách sử dụng phối tử EDTA4– để tạo phức [Pb(EDTA)]2– rất bền (hằng số bền β(Pb) = 1018,0) và được thận bài tiết. Phối tử EDTA4– được cung cấp bằng cách tiêm truyền dung dịch Na2[Ca(EDTA)]. Biết phức [Ca(EDTA)]2– tương đối kém bền (hằng số bền β(Ca) = 1010,7), sự trao đổi calcium với chì chủ yếu diễn ra trong mạch máu. Hàm lượng chì trong máu của một bệnh nhân là 0,828 μg/mL.
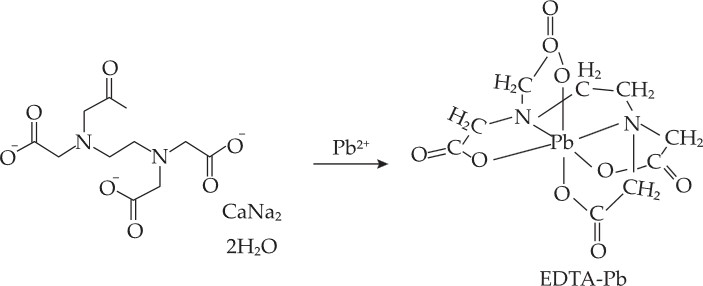

✔️ Nhận định a) – Đúng, vì:
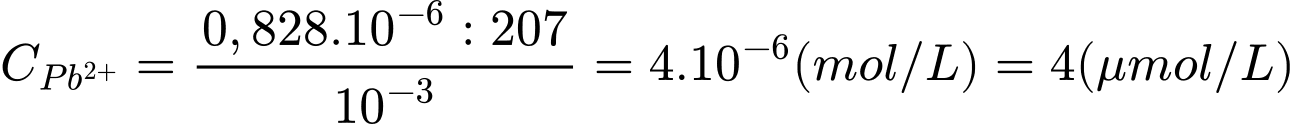
❌ Nhận định b) – Sai, vì: Phối tử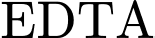 là phối tử hexadentate (sáu càng), liên kết với
là phối tử hexadentate (sáu càng), liên kết với 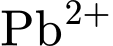 qua hai nguyên tử
qua hai nguyên tử  và bốn nguyên tử
và bốn nguyên tử  của nhóm carboxylate.
của nhóm carboxylate.
✔️ Nhận định c) – Đúng, vì: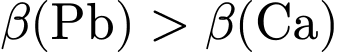
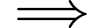 Phức chì bền hơn phức calcium nên ta có phản ứng xảy ra là
Phức chì bền hơn phức calcium nên ta có phản ứng xảy ra là 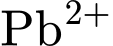 (trong máu) thế
(trong máu) thế 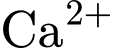 (trong phức Calcium) để tạo thành phức chì:
(trong phức Calcium) để tạo thành phức chì: 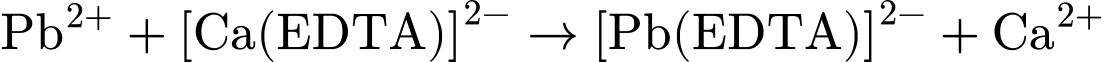
❌ Nhận định d) – Sai, vì: Phức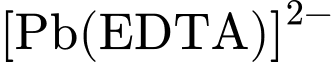 là một phức bền, tan tốt trong nước (do có các nhóm carboxylate ion hóa và kích thước lớn, phân cực), cho phép nó đi qua cầu thận và được bài tiết ra ngoài qua nước tiểu.
là một phức bền, tan tốt trong nước (do có các nhóm carboxylate ion hóa và kích thước lớn, phân cực), cho phép nó đi qua cầu thận và được bài tiết ra ngoài qua nước tiểu.
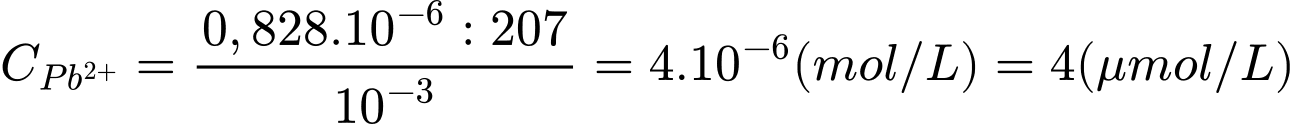
❌ Nhận định b) – Sai, vì: Phối tử
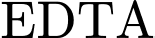 là phối tử hexadentate (sáu càng), liên kết với
là phối tử hexadentate (sáu càng), liên kết với 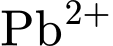 qua hai nguyên tử
qua hai nguyên tử  và bốn nguyên tử
và bốn nguyên tử  của nhóm carboxylate.
của nhóm carboxylate. ✔️ Nhận định c) – Đúng, vì:
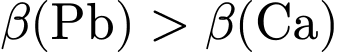
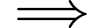 Phức chì bền hơn phức calcium nên ta có phản ứng xảy ra là
Phức chì bền hơn phức calcium nên ta có phản ứng xảy ra là 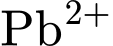 (trong máu) thế
(trong máu) thế 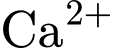 (trong phức Calcium) để tạo thành phức chì:
(trong phức Calcium) để tạo thành phức chì: 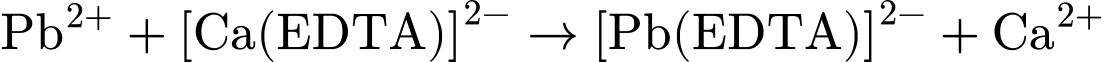
❌ Nhận định d) – Sai, vì: Phức
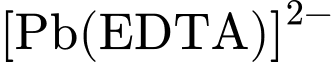 là một phức bền, tan tốt trong nước (do có các nhóm carboxylate ion hóa và kích thước lớn, phân cực), cho phép nó đi qua cầu thận và được bài tiết ra ngoài qua nước tiểu.
là một phức bền, tan tốt trong nước (do có các nhóm carboxylate ion hóa và kích thước lớn, phân cực), cho phép nó đi qua cầu thận và được bài tiết ra ngoài qua nước tiểu.
Câu 21 [703994]: Người ta nghi ngờ rằng có hiện tượng làm giả tiền xu bạc. Một mẫu tiền xu được cho là giả đã được phân tích để xác định tỉ lệ phần trăm bạc. Một mẫu 10,00 g tiền xu có chứa bạc được hòa tan trong nitric acid dư và thể tích dung dịch được tạo thành là 100,0 mL được đặt trong cốc (1). Lấy 25,00 mL dung dịch này cho vào cốc (2), chuẩn độ bằng dung dịch sodium chloride 1,00 M. Cần 10,45 mL để kết tủa tất cả các ion bạc. Tiền xu bạc thật sẽ có phần trăm bạc lớn hơn 90%.
Đổi 10,45 mL = 0,01045 L
(1) 3Ag + 4HNO3 ⟶ 3AgNO3 + NO↑ + 2H2O
(2) AgNO3 + NaCl ⟶ AgCl↓ + NaNO3
Số mol NaCl phản ứng là 0,01045.1 = 0,01045 (mol)
Từ phương trình (1) và (2) ⟶ số mol Ag là 0,01045 (mol)
Phần trăm khối lượng bạc có trong 10 gam tiền xu trên là:
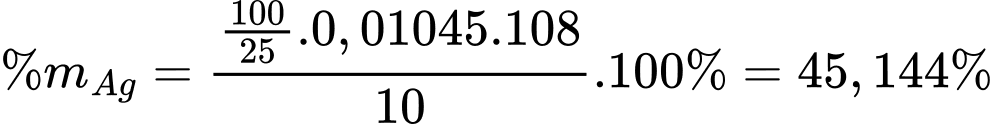
Phân tích các phát biểu:
❌ a) Sai. Ion silver (Ag+) tạo kết tủa với ion chloride (Cl-) tạo thành kết tủa AgCl.
✔️ b) Đúng. Nồng độ Ag trong cốc (1) bằng với cốc (2) trước chuẩn độ
❌ c) Sai. Phần trăm khối lượng của Ag trong tiền xu là 45,144%
✔️ d) Đúng. Tiền xu bạc thật sẽ có phần trăm bạc lớn hơn 90%, nên dựa vào phần trăm bạc trong tiền xu có thể kết luận rằng tiền xu này là thật hay giả.
(1) 3Ag + 4HNO3 ⟶ 3AgNO3 + NO↑ + 2H2O
(2) AgNO3 + NaCl ⟶ AgCl↓ + NaNO3
Số mol NaCl phản ứng là 0,01045.1 = 0,01045 (mol)
Từ phương trình (1) và (2) ⟶ số mol Ag là 0,01045 (mol)
Phần trăm khối lượng bạc có trong 10 gam tiền xu trên là:
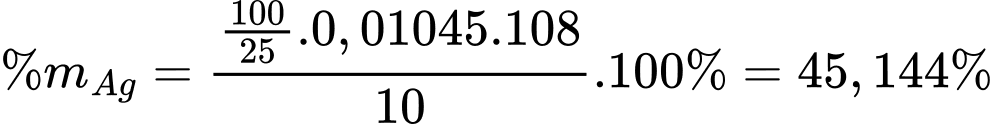
Phân tích các phát biểu:
❌ a) Sai. Ion silver (Ag+) tạo kết tủa với ion chloride (Cl-) tạo thành kết tủa AgCl.
✔️ b) Đúng. Nồng độ Ag trong cốc (1) bằng với cốc (2) trước chuẩn độ
❌ c) Sai. Phần trăm khối lượng của Ag trong tiền xu là 45,144%
✔️ d) Đúng. Tiền xu bạc thật sẽ có phần trăm bạc lớn hơn 90%, nên dựa vào phần trăm bạc trong tiền xu có thể kết luận rằng tiền xu này là thật hay giả.
Câu 22 [703995]: Hàm lượng glucose có trong mẫu dược phẩm có thể được xác định bằng phương pháp chuẩn độ với iodine như sau:
Bước 1: Cho 20,00 mL một mẫu dung dịch chứa glucose vào 15,00 mL dung dịch iodine 0,10 M dư.
C6H12O6(aq) + I2(aq) + H2O(aq) → C6H12O7(aq) + 2HI(aq)
Bước 2: Sau đó, thêm vào dung dịch sau phản ứng vài giọt dung dịch X, rồi vừa lắc vừa nhỏ từ từ dung dịch sodium thiosulfate (Na2S2O3) 0,05 M vào dung dịch ở trên đến khi mất màu xanh thì dừng lại.
I2(aq) + 2Na2S2O3(aq) → 2NaI(aq) + Na2S4O6(aq)
Lặp lại 2 lần, thể tích dung dịch sodium thiosulfate đã dùng được ghi lại.
Bước 1: Cho 20,00 mL một mẫu dung dịch chứa glucose vào 15,00 mL dung dịch iodine 0,10 M dư.
C6H12O6(aq) + I2(aq) + H2O(aq) → C6H12O7(aq) + 2HI(aq)
Bước 2: Sau đó, thêm vào dung dịch sau phản ứng vài giọt dung dịch X, rồi vừa lắc vừa nhỏ từ từ dung dịch sodium thiosulfate (Na2S2O3) 0,05 M vào dung dịch ở trên đến khi mất màu xanh thì dừng lại.
I2(aq) + 2Na2S2O3(aq) → 2NaI(aq) + Na2S4O6(aq)
Lặp lại 2 lần, thể tích dung dịch sodium thiosulfate đã dùng được ghi lại.
Thể tích trung bình của Na2S2O3 sau 3 lần chuẩn độ là:
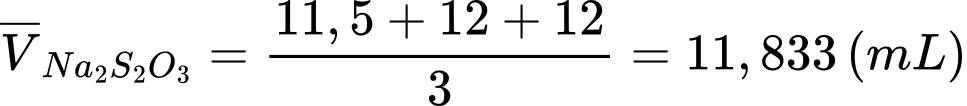
Đổi 11,833 mL = 11,833.10-3 L; 15 mL = 0,015 L; 20 mL = 0,02L
(1) C6H12O6 + I2 + H2O ⟶ C6H12O7 + 2HI
(2) I2 + 2Na2S2O3 ⟶ Na2S4O6 + 2NaI
Số mol của I2 tham gia phản ứng (2) là:
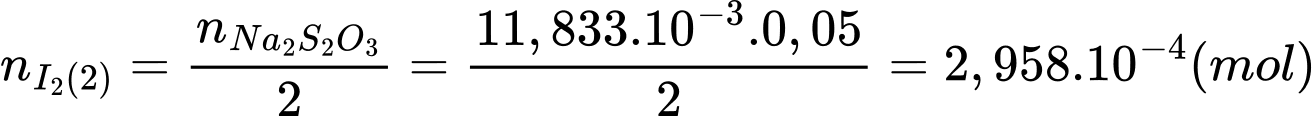
Số mol của I2 ban đầu là:
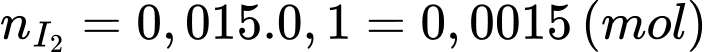
Lượng I2 tham gia phản ứng với glucose là:
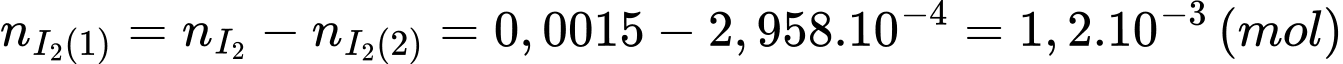
Nồng độ của glucose trong là:
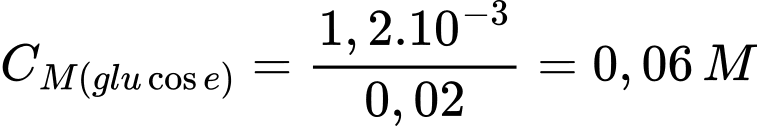
Phân tích các phát biểu:
✔️ a) Đúng. Chuẩn độ oxi hóa - khử là dùng phản ứng oxi hóa - khử giữa chất phân tích và dung dịch chuẩn độ. Trong phản ứng trên I2 là chất oxi hóa và Na2S2O3 là chất khử.
✔️ b) Đúng. Hồ tinh bột được dùng là chất chỉ thị nhận biết được khi nào I2 phản ứng hết, hiện tượng chuẩn độ dung dịch cho đến khi hết màu xanh tím thì dừng lại.
✔️ c) Đúng. Nồng độ glucose trong mẫu dung dịch ban đầu là 0,06 M.
❌ d) Sai. Khi tăng nồng độ lên gấp đôi thì thể tích Na2S2O3 giảm một nửa là 6 mL.
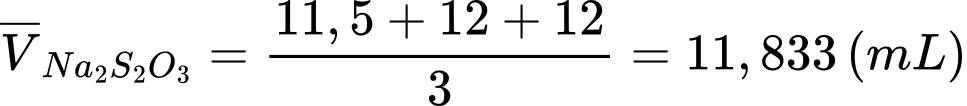
Đổi 11,833 mL = 11,833.10-3 L; 15 mL = 0,015 L; 20 mL = 0,02L
(1) C6H12O6 + I2 + H2O ⟶ C6H12O7 + 2HI
(2) I2 + 2Na2S2O3 ⟶ Na2S4O6 + 2NaI
Số mol của I2 tham gia phản ứng (2) là:
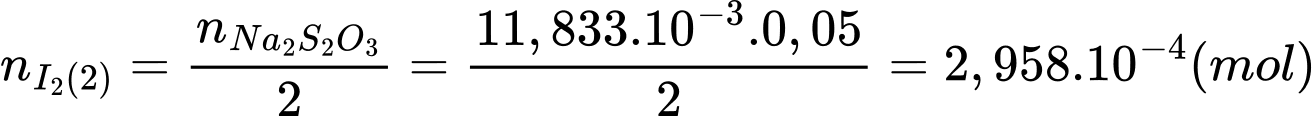
Số mol của I2 ban đầu là:
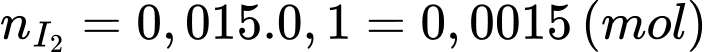
Lượng I2 tham gia phản ứng với glucose là:
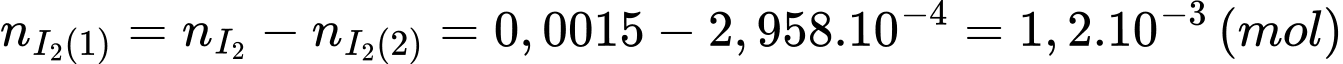
Nồng độ của glucose trong là:
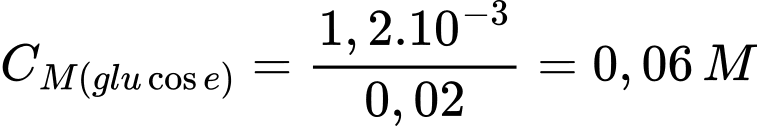
Phân tích các phát biểu:
✔️ a) Đúng. Chuẩn độ oxi hóa - khử là dùng phản ứng oxi hóa - khử giữa chất phân tích và dung dịch chuẩn độ. Trong phản ứng trên I2 là chất oxi hóa và Na2S2O3 là chất khử.
✔️ b) Đúng. Hồ tinh bột được dùng là chất chỉ thị nhận biết được khi nào I2 phản ứng hết, hiện tượng chuẩn độ dung dịch cho đến khi hết màu xanh tím thì dừng lại.
✔️ c) Đúng. Nồng độ glucose trong mẫu dung dịch ban đầu là 0,06 M.
❌ d) Sai. Khi tăng nồng độ lên gấp đôi thì thể tích Na2S2O3 giảm một nửa là 6 mL.
PHẦN III. Thí sinh trả lời từ câu 1 đến 6. Thí sinh điền kết quả mỗi câu vào mỗi ô trả lời tương ứng theo hướng dẫn của phiếu trả lời.
Câu 23 [702826]: Muối Mohr có công thức (NH4)2Fe(SO4)2.6H2O. Để xác định độ tinh khiết của một loại muối Mohr (cho rằng trong muối Mohr chỉ có muối kép ngậm nước nêu trên và tạp chất trơ), một học sinh tiến hành các thí nghiệm sau: Cân chính xác 7,237 gam muối Mohr, pha thành 100 mL dung dịch X. Lấy chính xác 10 mL dung dịch X, thêm 10 mL dung dịch H2SO4 10%, được dung dịch Y. Chuẩn độ dung dịch Y bằng dung dịch chuẩn KMnO4 0,023 M. Thực hiện chuẩn độ 3 lần. Thể tích trung bình của dung dịch KMnO4 sau 3 lần chuẩn độ là 15,86 mL. Theo kết quả chuẩn độ ở trên, độ tinh khiết (phần trăm khối lượng (NH4)2Fe(SO4)2.6H2O) của muối Mohr là bao nhiêu phần trăm (làm tròn đến hành phần mười)?
Đổi: 10 mL = 0,01 L; 15,86 mL = 0,01586 L; 100 mL = 0,1 L.
Số mol của KMnO4 phản ứng là:
0,01586 . 0,023 = 3,6478 . 10-4 (mol)
10FeSO4 + 2KMnO4 + 8H2SO4 ⟶ 5Fe2(SO4)3 + K2SO4 + 2MnSO4 + 8H2O
Từ PTHH, số mol FeSO4 phản ứng là:
3,6478 . 10-4 . 5 = 1,8239 . 10-3 (mol)
Số mol FeSO4 = Số mol muối Mohr ban đầu =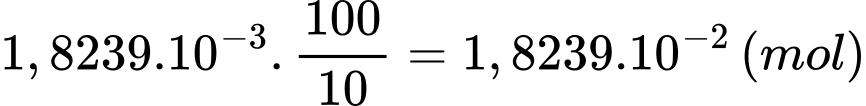
Độ tinh khiết của muối Mohr trên là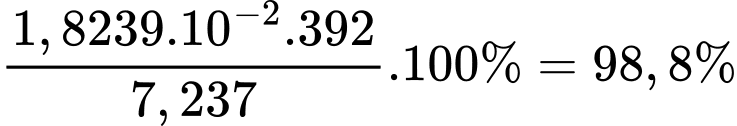
⇒ Điền đáp án: 98,8
Số mol của KMnO4 phản ứng là:
0,01586 . 0,023 = 3,6478 . 10-4 (mol)
10FeSO4 + 2KMnO4 + 8H2SO4 ⟶ 5Fe2(SO4)3 + K2SO4 + 2MnSO4 + 8H2O
Từ PTHH, số mol FeSO4 phản ứng là:
3,6478 . 10-4 . 5 = 1,8239 . 10-3 (mol)
Số mol FeSO4 = Số mol muối Mohr ban đầu =
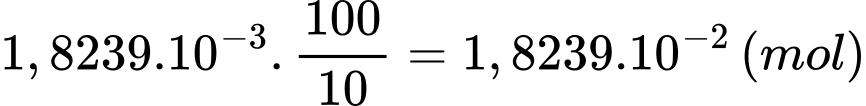
Độ tinh khiết của muối Mohr trên là
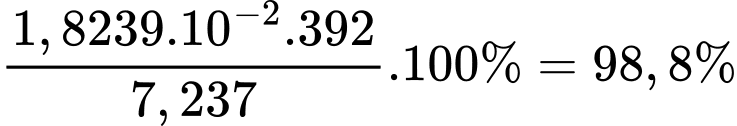
⇒ Điền đáp án: 98,8
Câu 24 [702846]: Trong công nghiệp sản xuất nhôm từ quặng bauxite theo quy trình Hall- Heroult được thực hiện theo sơ đồ: quặng bauxite  Al2O3
Al2O3  Al. Theo tính toán, từ 4 tấn quặng tinh chế được 2 tấn Al2O3 và thu được 1 tấn Al, đồng thời thải ra môi trường 1,574 tấn CO2. Nếu sử dụng 10000 tấn quặng thì lượng khí CO2 thải ra môi trường là bao nhiêu tấn?
Al. Theo tính toán, từ 4 tấn quặng tinh chế được 2 tấn Al2O3 và thu được 1 tấn Al, đồng thời thải ra môi trường 1,574 tấn CO2. Nếu sử dụng 10000 tấn quặng thì lượng khí CO2 thải ra môi trường là bao nhiêu tấn?
 Al2O3
Al2O3  Al. Theo tính toán, từ 4 tấn quặng tinh chế được 2 tấn Al2O3 và thu được 1 tấn Al, đồng thời thải ra môi trường 1,574 tấn CO2. Nếu sử dụng 10000 tấn quặng thì lượng khí CO2 thải ra môi trường là bao nhiêu tấn?
Al. Theo tính toán, từ 4 tấn quặng tinh chế được 2 tấn Al2O3 và thu được 1 tấn Al, đồng thời thải ra môi trường 1,574 tấn CO2. Nếu sử dụng 10000 tấn quặng thì lượng khí CO2 thải ra môi trường là bao nhiêu tấn?
Lượng CO2 thải ra từ 1 tấn quặng là:
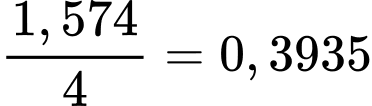 (tấn)
(tấn)
Lượng CO2 thải ra từ 10 000 tấn quặng là:
0,3935 . 10 000 = 3935 (tấn)
⇒ Điền đáp án: 3935
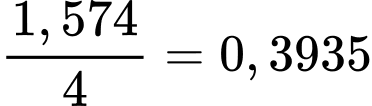 (tấn)
(tấn)Lượng CO2 thải ra từ 10 000 tấn quặng là:
0,3935 . 10 000 = 3935 (tấn)
⇒ Điền đáp án: 3935
Câu 25 [705473]: Cho các ester sau: CH3COOC2H5, HCOOC(CH3)=CH2, C2H5COOC6H4CH3 (có vòng benzene), C6H5COOCH3. Ở điều kiện thích hợp, có bao nhiêu ester thủy phân không hoàn toàn trong môi trường acid?
Có 4 ester bị thuỷ phân không hòa toàn trong môi trường acid là CH3COOC2H5, C6H5COOCH3.
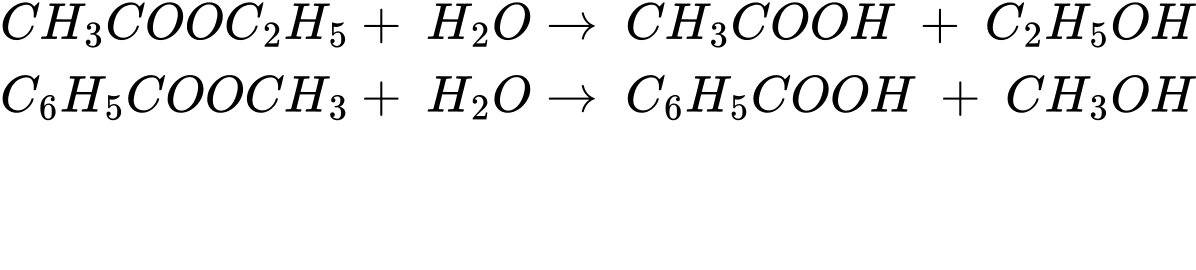
⟹ Điền đáp án: 2
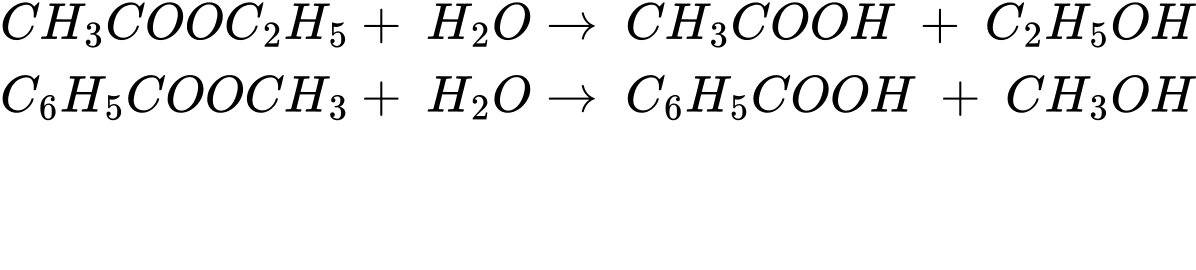
⟹ Điền đáp án: 2
Câu 26 [702822]: Một loại chất giặt rửa tổng hợp có thành phần chính là muối sau:
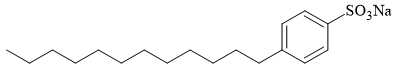
Nhánh hydrocarbon đính vào vòng benzene của muối trên có bao nhiêu nguyên tử carbon?Tổng số nguyên tử trong phân tử chất giặt rửa tổng hợp trên là bao nhiêu?

Nhánh hydrocarbon đính vào vòng benzene của muối trên có bao nhiêu nguyên tử carbon?Tổng số nguyên tử trong phân tử chất giặt rửa tổng hợp trên là bao nhiêu?
Nhánh hydrocarbon đính vào vòng benzene của muối trên có CTCT là CH3[CH2]11 ⇒ có 12 nguyên tử carbon.
⇒ Điền đáp án: 12
⇒ Điền đáp án: 12
Câu 27 [706339]: Cho các mẫu chất và dán nhãn tương ứng như sau: Ammonium formate (1), lysine (2), fructose (3), aniline (4). Tiến hành thí nghiệm với dung dịch X, Y, Z và T. Kết quả được ghi ở bảng:

Gán nhãn dán các chất tương ứng với hiện tượng của dung dịch X, Y, Z, T theo trình tự dãy bốn số (ví dụ: 1234, 4213, ...)

Gán nhãn dán các chất tương ứng với hiện tượng của dung dịch X, Y, Z, T theo trình tự dãy bốn số (ví dụ: 1234, 4213, ...)
Mẫu thử Z: tác dụng với Cu(OH)2 tạo dung dịch màu xanh lam
Tác dụng với dung dịch AgNO3/NH3 xuất hiện kết tủa Ag
→ Z là fructose (3)
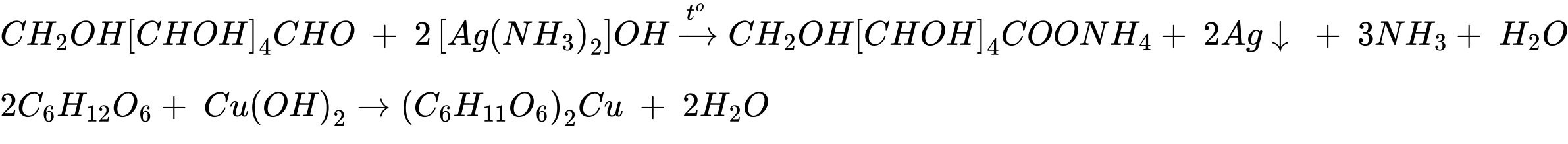
Mẫu thử X: Tác dụng với dung dịch AgNO3/NH3 xuất hiện kết tủa Ag
→ X là ammonium formate (1)
6HCOONH4 + 10AgNO3 + 11NH3 → 10Ag + 12NH4NO3 + 3CHCOONH4
Mẫu thử Y làm quì tím chuyển xanh
→ Y là lysine (2)
Mẫu thử T: Aniline + nước bromine
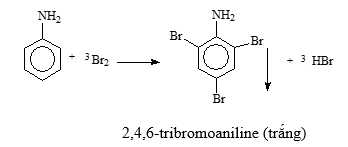
=> Hiện tượng: Xuất hiện kết tủa trắng + Mất màu dung dịch bromine → ứng với aniline (4)
⟹ Điền đáp án : 1234
Tác dụng với dung dịch AgNO3/NH3 xuất hiện kết tủa Ag
→ Z là fructose (3)
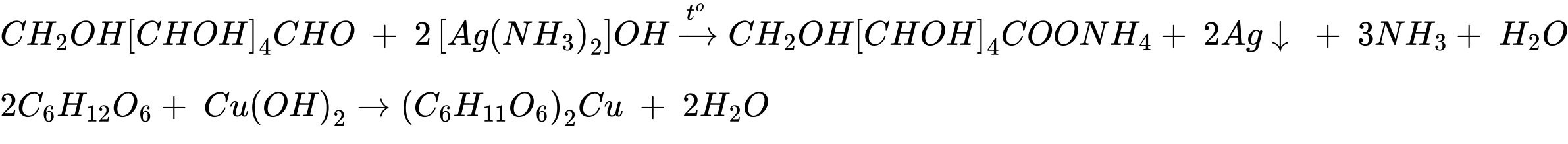
Mẫu thử X: Tác dụng với dung dịch AgNO3/NH3 xuất hiện kết tủa Ag
→ X là ammonium formate (1)
6HCOONH4 + 10AgNO3 + 11NH3 → 10Ag + 12NH4NO3 + 3CHCOONH4
Mẫu thử Y làm quì tím chuyển xanh
→ Y là lysine (2)
Mẫu thử T: Aniline + nước bromine

=> Hiện tượng: Xuất hiện kết tủa trắng + Mất màu dung dịch bromine → ứng với aniline (4)
⟹ Điền đáp án : 1234
Câu 28 [704192]: Trong phản ứng hóa học, đại lượng enthalpy 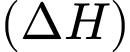 đặc trưng cho nhiệt tỏa ra hay thu vào của phản ứng với quy ước:
đặc trưng cho nhiệt tỏa ra hay thu vào của phản ứng với quy ước: 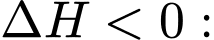 phản ứng tỏa nhiệt,
phản ứng tỏa nhiệt, 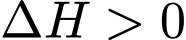 phản ứng thu nhiệt. Hầu hết các phản ứng cháy nhiên liệu đều tỏa nhiệt rất mạnh. Methane và carbon cháy theo các phương trình sau:
phản ứng thu nhiệt. Hầu hết các phản ứng cháy nhiên liệu đều tỏa nhiệt rất mạnh. Methane và carbon cháy theo các phương trình sau:
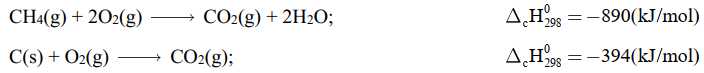
Khí carbonic sinh ra từ các quá trình cháy là một trong những nguyên nhân chính gây hiệu ứng nhà kính. Hiện nay, nồng độ CO2 trong khí quyển là 0,035% so với cách đây 300 năm là 0,028%. Nếu nồng độ CO2 tăng 25% thì góp phần tăng nhiệt độ toàn cầu 0,5 oC. Do đó, các biện pháp làm giảm thiểu sự phát thải CO2 là vấn đề lớn của toàn thế giới.Tính tỉ lệ giảm phát thải khí CO2 (tính cho 1 kJ) khi đốt cháy than và methane.(Làm tròn đến hàng phần mười.)
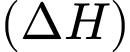 đặc trưng cho nhiệt tỏa ra hay thu vào của phản ứng với quy ước:
đặc trưng cho nhiệt tỏa ra hay thu vào của phản ứng với quy ước: 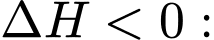 phản ứng tỏa nhiệt,
phản ứng tỏa nhiệt, 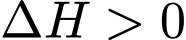 phản ứng thu nhiệt. Hầu hết các phản ứng cháy nhiên liệu đều tỏa nhiệt rất mạnh. Methane và carbon cháy theo các phương trình sau:
phản ứng thu nhiệt. Hầu hết các phản ứng cháy nhiên liệu đều tỏa nhiệt rất mạnh. Methane và carbon cháy theo các phương trình sau: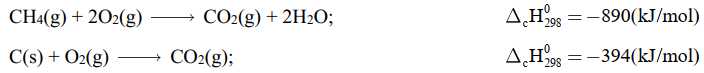
Khí carbonic sinh ra từ các quá trình cháy là một trong những nguyên nhân chính gây hiệu ứng nhà kính. Hiện nay, nồng độ CO2 trong khí quyển là 0,035% so với cách đây 300 năm là 0,028%. Nếu nồng độ CO2 tăng 25% thì góp phần tăng nhiệt độ toàn cầu 0,5 oC. Do đó, các biện pháp làm giảm thiểu sự phát thải CO2 là vấn đề lớn của toàn thế giới.Tính tỉ lệ giảm phát thải khí CO2 (tính cho 1 kJ) khi đốt cháy than và methane.(Làm tròn đến hàng phần mười.)
* Đốt cháy CH4:
Cứ 1 mol CH4 bị đốt cháy, tức 1 mol CO2 sinh ra sẽ tạo ra 890 kJ
→ 1kJ được sinh ra bởi 1/890 mol CH4 và phát thải ra 1/890 mol CO2.
* Đốt cháy C:
Cứ 1 mol CO2 tạo thành sẽ phát thải ra môi trường 394 kJ
→ Phát thải ra 1 kJ thì cần 1/394 mol CO2.
Tỉ lệ giảm phát thải khí CO2 (tính cho 1 kJ) khi đốt cháy than và methane là:
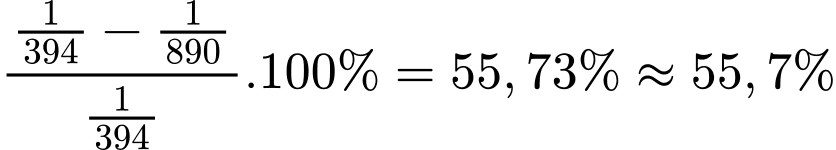
⇒ Điền đáp án: 55,7
Cứ 1 mol CH4 bị đốt cháy, tức 1 mol CO2 sinh ra sẽ tạo ra 890 kJ
→ 1kJ được sinh ra bởi 1/890 mol CH4 và phát thải ra 1/890 mol CO2.
* Đốt cháy C:
Cứ 1 mol CO2 tạo thành sẽ phát thải ra môi trường 394 kJ
→ Phát thải ra 1 kJ thì cần 1/394 mol CO2.
Tỉ lệ giảm phát thải khí CO2 (tính cho 1 kJ) khi đốt cháy than và methane là:
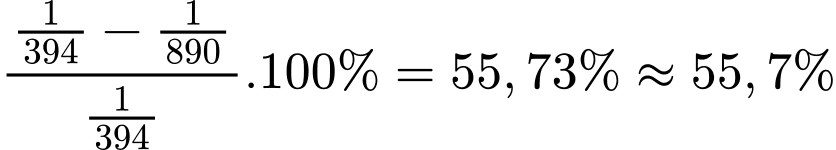
⇒ Điền đáp án: 55,7