PHẦN I. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
⟹ Chọn đáp án A Đáp án: A
⇒ Chọn đáp án D Đáp án: D

⇒ Chọn đáp án B Đáp án: B
Magnesium carbonate, thường được gọi là phấn rôm, được sử dụng như một chất làm khô mồ hôi tay cho các vận động viên leo núi đá, thể dục dụng cụ, và cử tạ để tăng ma sát và hút ẩm, giúp tay không bị trơn trượt khi thi đấu.
⇒ Chọn đáp án A Đáp án: A
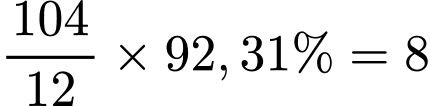
Số H là:
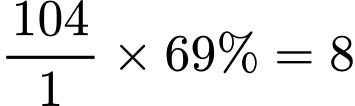
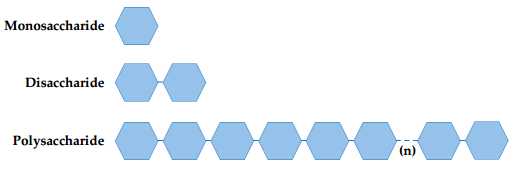
Monomer dùng điều chế X là: C8H8 ⟶(CH2 = CH - C6H5)
⟶X là polystyrene.
⟹ Chọn đáp án D Đáp án: D
Giải thích:
Amine (R−NH2, R2NH, hoặc R3N) có cặp electron tự do trên nguyên tử nitrogen. Cặp electron này có khả năng nhận proton (H+) từ acid hoặc từ nước, thể hiện tính chất base yếu.
⇒ Chọn đáp án C Đáp án: C
Fe2O3(s) + 2Al(s) → Al2O3(s) + 2Fe(l).
Cho biết enthalpy tạo thành chuẩn của Fe2O3(s) là – 825,5 kJ/mol; của Al2O3(s) là – 1675,7 kJ/mol. Biến thiên enthalpy của phản ứng khi dùng 5,00 g Fe2O3 là
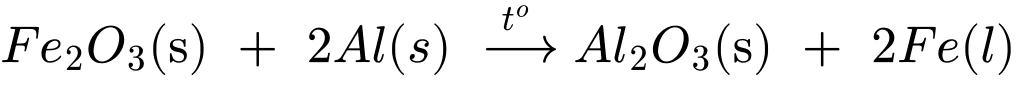
Biến thiên enthalpy của phản ứng trên là
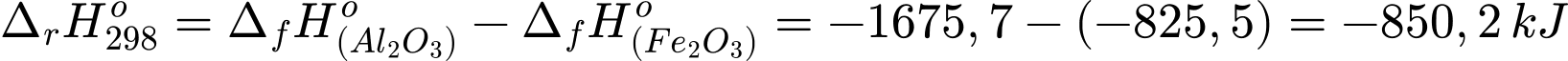
1 mol Fe2O3 khi tham gia phản ứng nhiệt lượng tỏa ra là 850,2 kJ
5 gam Fe2O3 khi tham gia phản ứng nhiệt lượng tỏa ra là
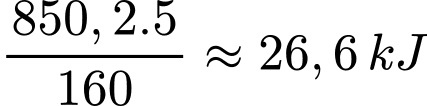
⟹Chọn đáp án B Đáp án: B
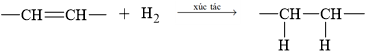
► Chú ý, trong thực tế: Dầu thực vật hydrogen hóa một phần được phát triển một phần để giúp thay thế chất béo động vật có độ bão hòa cao được sử dụng trong chiên, nướng và phết. Điều quan trọng của quá trình hydrogen hoá là không để phản ứng xảy ra hoàn toàn, không làm bão hòa hoàn toàn tất cả các liên kết đôi (tức không phá vỡ tất cả các liên kết đôi). Bởi nếu bão hòa hoàn toàn thì sản phẩm sẽ bị cứng giống như sáp - không phải là loại sản phẩm mềm, mịn như kem mà người tiêu dùng mong muốn.
⇒ Chọn đáp án A Đáp án: A
F có 9 electron → F thuộc ô thứ 9 trong BTH
Có 2 lớp electron → F thuộc chu kì 2
* Electron cuối cùng được điền vào phân lớp p → F thuộc nguyên tố p → Nhóm A
Có 7 electron lớp ngoài cùng → F thuộc nhóm VII A trong bảng tuần hoàn.
⟹Chọn đáp án B Đáp án: B
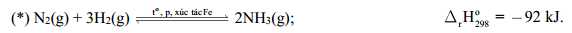
Đồ thị phần trăm chuyển hóa NH3 phụ thuộc vào nhiệt độ và áp suất tổng của phản ứng (*) được cho dưới đây:
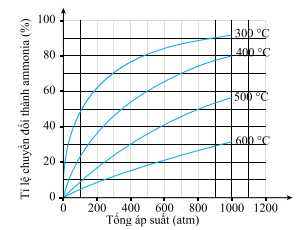
Bỏ qua các yếu về tốc độ phản ứng, nếu áp suất là 200 atm thì nhiệt độ nào sau đây sẽ được chọn để phần trăm chuyển hóa NH3 là cao nhất?
- Tại 300 oC, hiệu suất chuyển hóa NH3 hơn 60% ⟶ Cao nhất.
- Tại 400 oC, hiệu suất chuyển hóa NH3 gần 40%.
- Tại 500 oC, hiệu suất chuyển hóa NH3 gần 20%.
- Tại 600 oC, hiệu suất chuyển hóa NH3 gần 10%.
⇒ Chọn đáp án A Đáp án: A
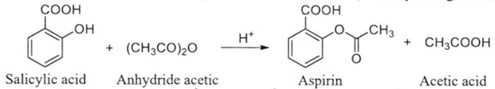
Hỗn hợp sau phản ứng được làm lạnh để tạo tinh thể aspirin. Sau đó tiến hành lọc, rửa, làm khô sản phẩm và đem cân để tính hiệu suất phản ứng. Trong các phát biểu sau:
(a) Phản ứng tổng hợp aspirin là phản ứng oxi hóa – khử trong đó acid đóng vai trò xúc tác.
(b) Nếu không làm khô sản phẩm thì hiệu suất phản ứng tính được sẽ cao hơn thực tế.
(c) Quá trình rửa sản phẩm giúp tăng độ tinh khiết của aspirin tổng hợp được.
(d) 1 mol aspirin tác dụng tối đa với 1 mol NaOH trong dung dịch.
Số phát biểu đúng là
❌ (a) – Sai. Phản ứng tổng hợp aspirin không có sự thay đổi số oxi hóa của các nguyên tử trong phản ứng nên không phải là phản ứng oxi hóa – khử.
✔️ (b) – Đúng Nếu không làm khô sản phẩm thì sản phẩm thu được có cả nước nên làm cho khối lượng không đúng với thực tế.
✔️ (c) – Đúng. Việc rửa sản phẩm giúp làm loại bỏ các tạp chất có trong sản phẩm.
❌ (d) – Sai. Trong phân tử aspirin có 1 nhóm chức ester (trong đó gốc CH3COO- gắn vào vòng thơm) và 1 nhóm chức carboxylic acid nên có thể tác dụng với NaOH theo tỉ lệ: 1 mol aspirin: 3 mol NaOH.
Các phát biểu đúng là (b) (c)
⇒ Chọn đáp án B Đáp án: B
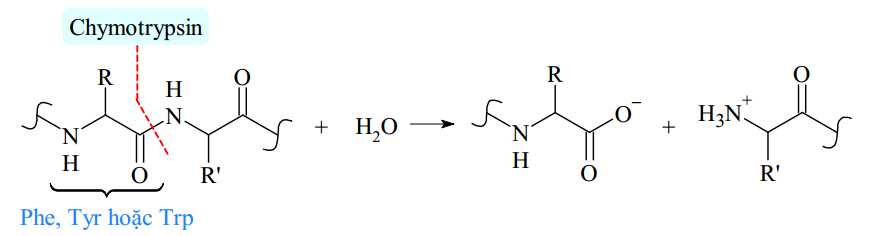
Tiến hành cắt đứt chuỗi amino acid bằng enzyme chymotrypsin đến khi hoàn toàn thì trong các chất sản phẩm, amino acid thu được có số mắt xích lớn nhất có thể là bao nhiêu?
Khi tiến hành cắt đứt chuỗi amino acid bằng enzyme chymotrypsin thì chymotrypsin cắt các amino acid một cách có chọn lọc, nó sẽ cắt đứt liên kết CO–NH với phần carbonyl thuộc về amino acid Phe, Tyr hoặc Trp nên quá trình cắt đứt xảy ra như sau:( cắt tại vị trí Tyr, Phe )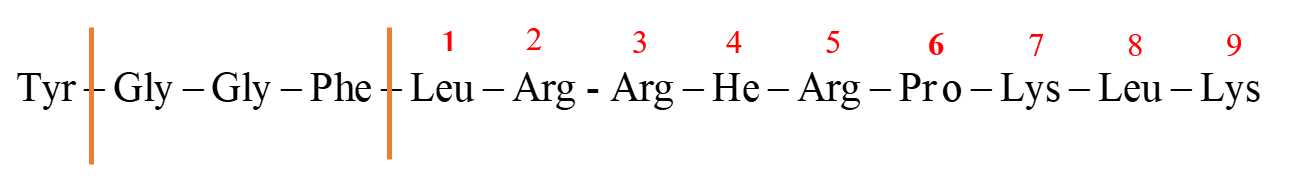
Sản phẩm thu được có số mắt xích lớn nhất là 9: Leu-Arg-Arg-Ile-Arg-Pro-Lys-Leu-Lys.
⤏ Amino acid thu được có số mắt xích lớn nhất là 9.
⇒ Chọn đáp án C
Điều này xảy ra vì ion phân tử [M+] là kết quả của việc chất nghiên cứu mất một electron mà không bị phá vỡ cấu trúc, do đó giá trị m/z của nó phản ánh trực tiếp khối lượng phân tử.
⇒ Chọn đáp án B Đáp án: B
⇒ Chọn đáp án A Đáp án: A
Cho các phát biểu sau
(a) Quá trình hòa tan NaOH vào nước có giá trị biến thiên enthalpy âm.
(b) Phân tử mỡ tác dụng với NaOH sinh ra các phân tử xà phòng có dạng RCOONa.
(c) Khí X được sinh ra khi cho nhôm tác dụng với dung dịch NaOH là khí oxygen.
(d) Khi sử dụng tẩy rửa thông cống cần sử dụng găng tay cao su để bao vệ tay.
Số phát biểu đúng là
✔️ (a) Đúng. Quá trình hòa tan NaOH giải phóng một lượng nhiệt đáng kể và tạo ra dung dịch NaOH nóng, nên có giá trị enthalpy âm.
✔️ (b) Đúng. Chất béo là triester (ester 3 chức) của glycerol với các acid béo, công thức chung có dạng (RCOO)3C3H5
(RCOO)3C3H5 + 3NaOH ⟶ 3RCOONa + C3H5(OH)3
❌ (c) Sai. Phản ứng của NaOH với Al sinh ra khí H2.
2NaOH + 2Al + 2H2O ⟶ 2NaAlO2 + 3H2
✔️ (d) Đúng. Trong chất tẩy rửa chứa NaOH có khả năng ăn mòn da nên cần có găng tay bảo vệ.
Các phát biểu đúng là (a) (b) (d)
⇒ Chọn đáp án C Đáp án: C
Dòng điện một chiều được truyền qua dung dịch copper(II) chromate(VI) màu xanh lá cây trong thiết bị được minh họa bên. Màu sắc nào sẽ xuất hiện ở mỗi điện cực sau vài phút?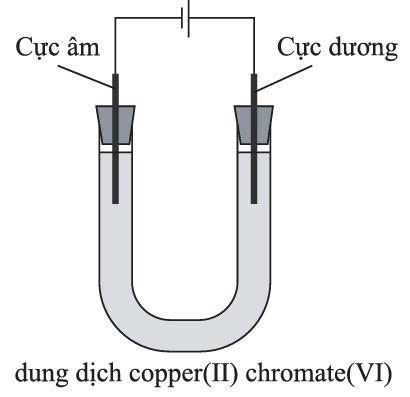
 (
( ) màu xanh lá cây, chứa các ion:
) màu xanh lá cây, chứa các ion:•
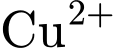 (ion dương, màu xanh dương).
(ion dương, màu xanh dương).•
 (ion âm, màu vàng cam).
(ion âm, màu vàng cam).Trong quá trình điện phân:
1. Cực dương (Anode): Thu hút ion âm (
 ). Ion
). Ion  di chuyển về cực dương, làm khu vực này có màu vàng (của
di chuyển về cực dương, làm khu vực này có màu vàng (của  ).
).2. Cực âm (Cathode): Thu hút ion dương (
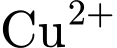 ). Ion
). Ion 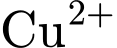 di chuyển về cực âm, làm khu vực này có màu xanh dương (của
di chuyển về cực âm, làm khu vực này có màu xanh dương (của 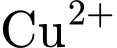 ).
).⭐Lưu ý: Ion
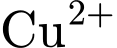 sẽ bị khử thành
sẽ bị khử thành  kim loại (
kim loại (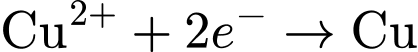 ), và
), và  sẽ bị oxy hóa thành
sẽ bị oxy hóa thành 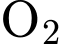 (hoặc
(hoặc 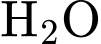 bị oxy hóa). Tuy nhiên, màu sắc xuất hiện là do sự di chuyển của các ion.
bị oxy hóa). Tuy nhiên, màu sắc xuất hiện là do sự di chuyển của các ion.⟹ Chọn đáp án B.Cực dương: vàng; cực âm: xanh dương. Đáp án: B
Sử dụng đoạn thông tin dưới đây để trả lời câu 17 và câu 18:
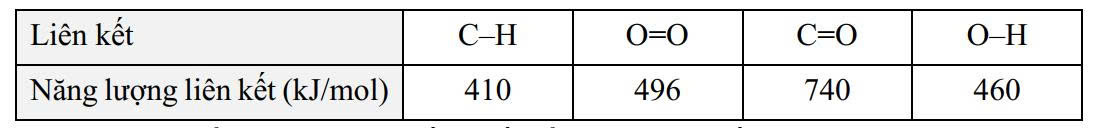
Cho bảng giá trị năng lượng liên kết trung bình sau:
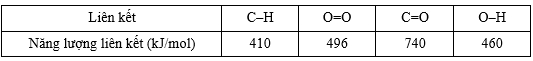
17. Tổng năng lượng cần thiết để phá vỡ liên kết trong 1 mol phân tử CH4 là
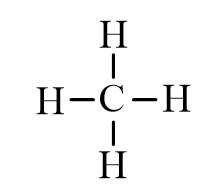
Trong phân tử có 4 liên kết C-H nên năng lượng cần thiết phá vỡ liên kết trong CH4 là: 410 x 4 = 1640 (kJ)
⇒ Chọn đáp án D Đáp án: D
CH4(g) + 2O2(g)
 CO2(g) + 2H2O(g).
CO2(g) + 2H2O(g).  CO2(g) + 2H2O
CO2(g) + 2H2OBiến thiên enthalpy của phản ứng là
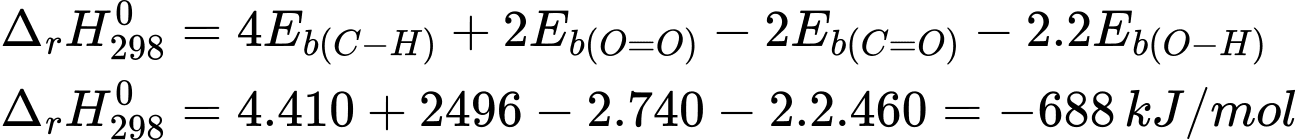
⇒ Chọn đáp án A Đáp án: A
PHẦN II. Thí sinh trả lời từ câu 1 đến câu 4. Trong mỗi ý a), b), c), d) ở mỗi câu, thí sinh chọn đúng hoặc sai.
FeCl3(aq) + 6H2O(l)
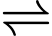 [Fe(OH2)6]3+(aq) + 3Cl–(aq) (1)
[Fe(OH2)6]3+(aq) + 3Cl–(aq) (1)[Fe(H2O)6]3+(aq)
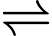 [Fe(OH2)5(OH)]2+(aq) + H+(aq) (2)
[Fe(OH2)5(OH)]2+(aq) + H+(aq) (2) 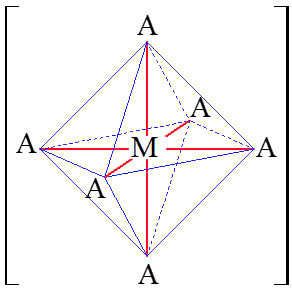
✔️ b) Đúng.
- Trong phức chất [Fe(OH2)6]3+ ngoài liên kết cộng hoá trị phân cực giữa H và O giống nước thì còn có liên kết cho - nhận (liên kết phối trí) giữa ion trung tâm Fe3+ và phối tử H2O, mà cặp electron dùng chung bị lệch về phía Fe (biểu diễn như hình dưới). Vì thế nên lực hút electron của O với H sẽ mạnh hơn để nhường electron cho Fe.
⇒ Liên kết O-H trong phức chất [Fe(OH2)6]3+ phân cực hơn liên kết O-H trong phân tử H2O.
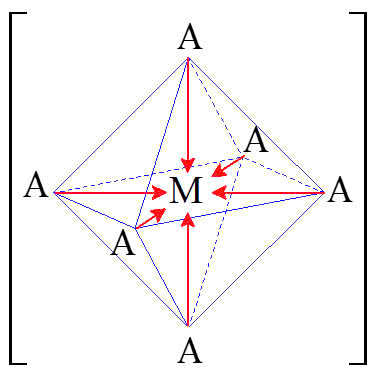
❌ c) Sai. Số oxi hoá của OH2 bằng 0 (phân tử nước trung hoà về điện) và số oxi hoá của OH là (-1)
Số oxi hoá của Fe trong phức [Fe(OH2)6]3+ là x: +3 = x + 0.6 ⇒ x = +3
Số oxi hoá của Fe trong phức [Fe(OH2)5(OH)]2+ là y: +2 = y + 0.5 + (-1) ⇒ y = +3
⟿ Trạng thái oxi hoá của Fe trong phức [Fe(OH2)6]3+ và [Fe(OH2)5(OH)]2+ là giống nhau.
✔️ d) Đúng. Khi thêm dung dịch HCl (H+) vào làm tăng nồng độ H+ trong dung dịch => cân bằng (2) chuyển dịch theo chiều làm giảm H+ là chiều nghịch.
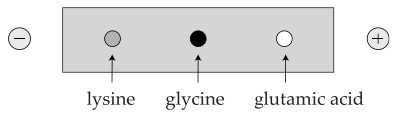
Sự di chuyển của một số amino acid dưới tác dụng của điện trường ở pH = 6.
Phân tích các phát biểu:
✔️ (a) Đúng. pH của dung dịch bằng điểm đẳng điện (pH = pI ≈ 6,0), glycine tồn tại chủ yếu ở dạng lưỡng cực ion trung hòa nên không chịu tác dụng của điện trường.
❌ (b) Sai. Lysine có hai nhóm amine (–NH2) và một nhóm carboxyl (–COOH). Ở pH = 6, lysine có dạng H3N+–CH(CH2)4–NH3+–COO– ⟶ Điện tích của lysine là +1.
❌ (c) Sai. Glutamic acid có hai nhóm –COOH và một nhóm –NH2. Ở pH = 6, nó tồn tại chủ yếu ở dạng H2N–CH(CH2–COO–)–COO–, mang điện tích âm (anion) nên di chuyển về cực dương.
✔️ (d) Đúng. Glycine gần như không di chuyển, lysine di chuyển về cực âm và glutamic acid di chuyển về cực dương nên ta có thể tách chúng ra bằng phương pháp điện di.
Khi đun nóng ở nhiệt độ phù hợp, lượng nước kết tinh thường tách ra khỏi hợp chất. Để xác định hàm lượng muối kết tinh trong tinh thể muối CuSO4.xH2O (hợp chất X, coi như không lẫn tạp chất) bằng phương pháp đun nóng, một nhóm học sinh thực hiện thí nghiệm theo các bước sau:
Bước 1: Cân chén nung và ghi lại khối lượng vào kết quả (m1).
Bước 2: Thêm một lượng nhỏ chất X (có màu xanh) cho vào chén nung. Cân và ghi lại khối lượng mới của chén nung có chứa chất X (m2).
Bước 3: Đặt chén nung chứa chất X lên lưới tam giác và đun nóng trong khoảng 2 phút.
Bước 4: Để nguội, cân lại chén nung cùng phần chất rắn còn lại bên trong, ghi khối lượng (m3). Lặp lại bước 3 và bước 4 cho đến khi cân chén chứa chất rắn màu trắng ở bước 4 thấy khối lượng không đổi.
Kết quả thí nghiệm của nhóm học sinh được ghi vào bảng sau. Dựa vào số liệu, nhóm học sinh tính % về khối lượng nước kết tinh có trong X.
• Nếu tạo CuO, chất rắn sẽ có màu đen.
• Kết thúc thí nghiệm, chất rắn có màu trắng (đặc trưng của CuSO₄ khan).
✔️Nhận định b) – Đúng, vì: Giảm khối lượng (từ
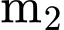 về
về 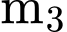 ) chính là do nước kết tinh trong
) chính là do nước kết tinh trong 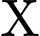 bị tách ra và bay hơi. Đây là cơ sở khoa học và phương pháp xác định nước kết tinh.
bị tách ra và bay hơi. Đây là cơ sở khoa học và phương pháp xác định nước kết tinh.❌Nhận định c) – Sai, vì:
Khối lượng chất
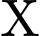 (
(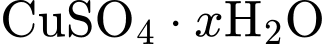 ):
):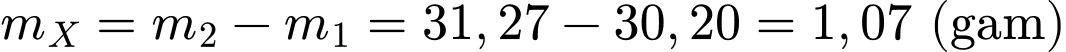
Khối lượng
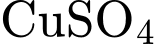 khan:
khan: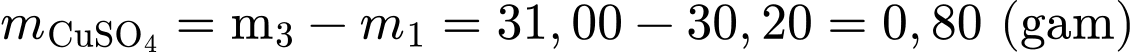
Khối lượng nước kết tinh (
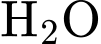 ) bay hơi:
) bay hơi: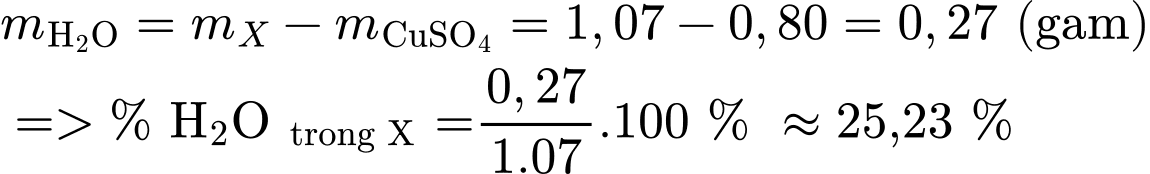
✔️Nhận định d) – Đúng, vì: Đây chính xác là mục đích và giả thiết hoạt động của thí nghiệm. Quá trình nung nóng giúp tách nước, và dựa vào khối lượng giảm đi (khối lượng nước) để tính hàm lượng.
▪ Bước 1: Dùng nước vôi trong để chuyển hóa NH4+ thành khí NH3; hiệu suất quá trình theo NH4+ là 90%.
▪ Bước 2: Sử dụng khí chlorine để oxi hóa NH3 thành N2; hiệu suất quá trình theo NH3 là 85%.
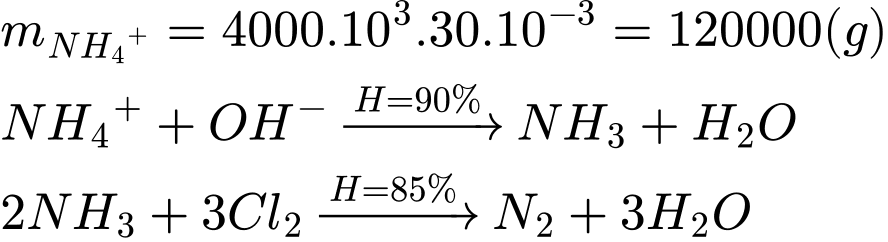
=>
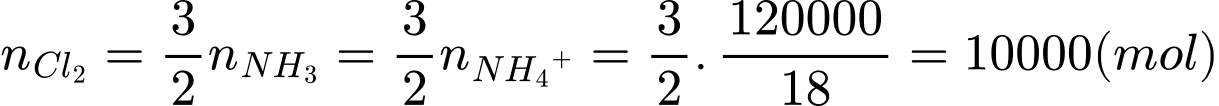
Mà hiệu suất ở hai quá trình lần lượt là: 90%, 85%
=>
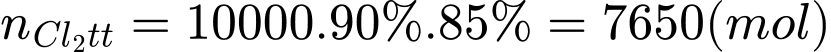
=> Khối lượng khí chlorine đã dùng là:
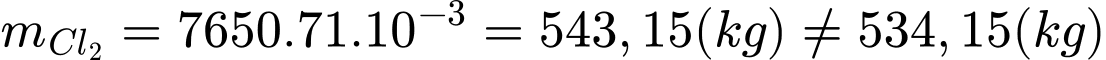
✔️ Nhận định b) – Đúng, vì: Nh4+ nhường proton nên thể hiện tính acid theo quan điểm của Bronsted – Lowry.
✔️ Nhận định c) – Đúng, vì: Sau khi xử lí nồng độ của NH4+ là:
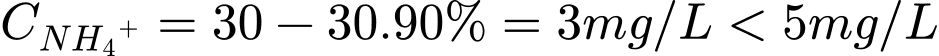
✔️ Nhận định d) – Đúng, vì: Phú dưỡng làm tảo phát triển quá mức, khi tảo và vật chất hữu cơ phân hủy tiêu thụ O₂ hoà tan → thiếu oxy làm cá và thủy sản chết.
PHẦN III. Thí sinh trả lời từ câu 1 đến 6. Thí sinh điền kết quả mỗi câu vào mỗi ô trả lời tương ứng theo hướng dẫn của phiếu trả lời.
VAg = 260,5 - 242,0 = 18,5 mL = 18,5 cm3
⇒ dAg =
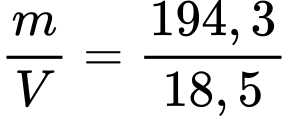 = 10,5 (g/cm3)
= 10,5 (g/cm3)⇒ Điền đáp án: 10,5
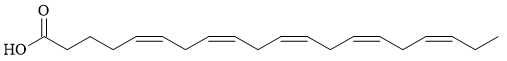
Có bao nhiêu liên kết π có trong một phân tử EPA?
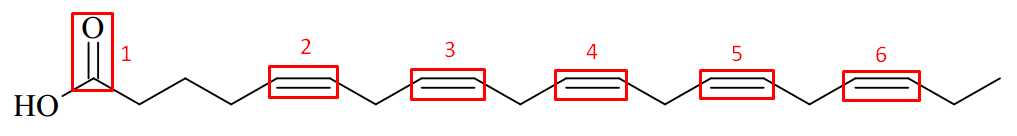
→ Có 6 liên kết π trong một phân tử EPA.
⇒ Điền đáp án: 6
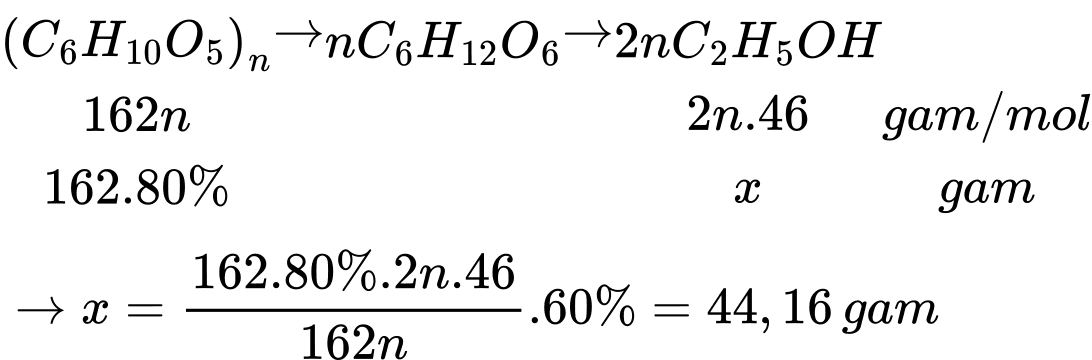
Thể tích ethanol tạo thành là VC2H5OH = 44,16 : 0,8 = 55,2 mL
Thể tích dung dịch rượu 35o là
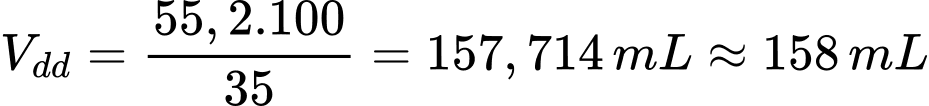
⟹Điền đáp án: 158
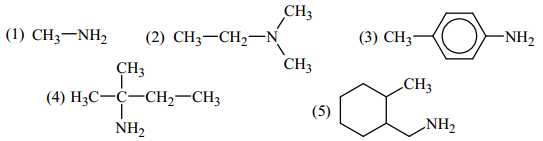
Có bao nhiêu amine bậc một?
Amine bậc hai: có nhóm chức dạng –NH– đính với hai gốc hydrocarbon.
Amine bậc ba: có nhóm chức dạng ≡N đính với ba gốc hydrocarbon.
Trong các amine trên, số amine bậc một là 4 (1, 3, 4, 5). Amine số 2 là mine bậc ba.
⇒ Điền đáp án: 4
2CN– + 8OH– + 5Cl2 ⟶ 2CO2 + 10Cl– + 4H2O + N2
Tính thể tích chlorine (theo L, ở đkc) cần thiết để khử cyanide trong 1m3 nước thải trên đến hàm lượng 0,2 mg/L (làm tròn đến hàng đơn vị).
2CN– + 8OH– + 5Cl2 ⟶ 2CO2 + 10Cl– + 4H2O + N2
Khối lượng ion cyanide đã xử lí là
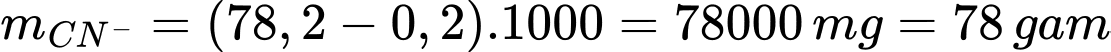
Số mol của CN– là:
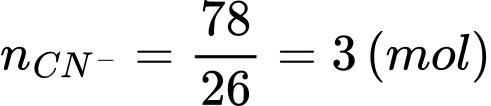
Thể tích khí chlorine cần thiết để khử ion cyanide là:
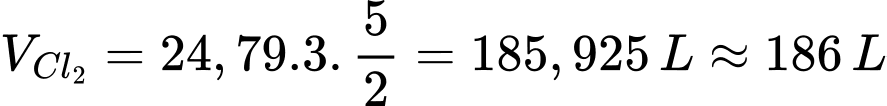
⇒ Điền đáp án: 186
Thí nghiệm 1: Lấy 10,0 mL dung dịch muối Mohr (NH4)2SO4.FeSO4.6H2O, thêm dung dịch H2SO4 1 M vào và chuẩn độ bằng dung dịch KMnO4.
Thí nghiệm 2: Lấy 10,0 mL dung dịch muối Mohr cho vào 100 mL nước chứa ion nitrate, sau đó thêm NaOH(s) vào để đạt khoảng 28%, khi đó muối Mohr khử nitrate thành ammonia theo các phản ứng:
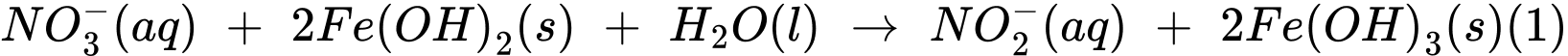
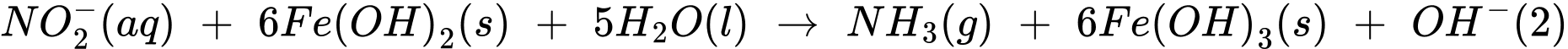
Sau khi các phản ứng (1) và (2) xảy ra hoàn toàn, lọc bỏ kết tủa, acid hoá dung dịch bằng dung dịch H2SO4 1M và chuẩn độ lượng Fe2+ dư bằng dung dịch KMnO4 (Các chất và ion khác trong dung dịch không phản ứng với KMnO4). Hãy cho biết mỗi mmol KMnO4 chênh lệch giữa thí nghiệm 1 với thí nghiệm 2 sẽ tương ứng với bao nhiêu mg
 có trong mẫu nước (làm tròn đến hàng phần mười).
có trong mẫu nước (làm tròn đến hàng phần mười). 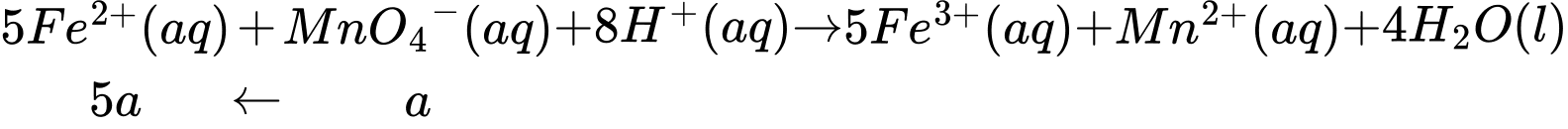
Gọi số mol NO3- đã dùng ở thí nghiệm 2 là b (mol), ta có:
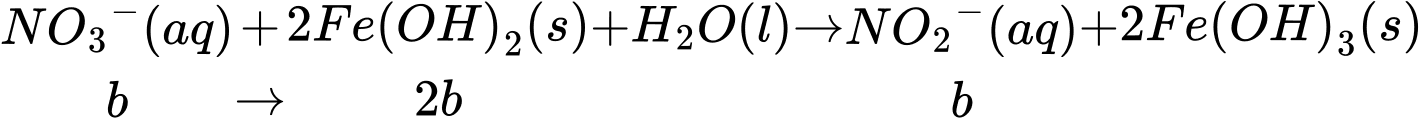
Lượng NO2- sinh ra là b (mol) tiếp tục phản ứng với Fe(OH)2
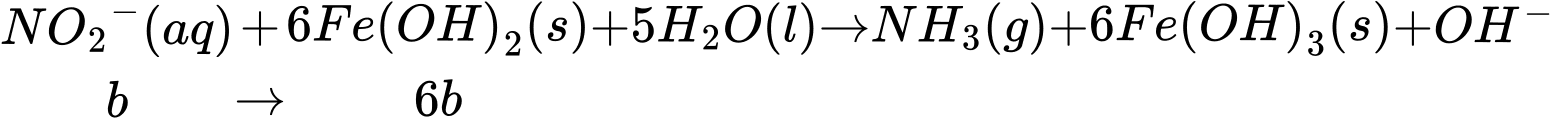
Thấy ban đầu ta có tổng số mol Fe2+ = 5a (mol), đã dùng hết (2b + 6b) mol ở thí nghiệm 2 nên lượng Fe2+ dư còn lại là:
nFe2+ dư = 5a - 8b (mol). Khi này, quá trình lọc bỏ kết tủa, acid hoá dung dịch bằng dung dịch H2SO4 1M và chuẩn độ lượng Fe2+ dư bằng dung dịch KMnO4 xảy ra như sau:
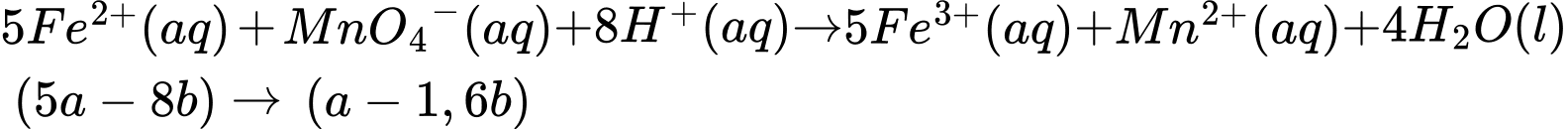
⇒ Số mol MnO4- chênh lệch là: nMnO4- (TN1) - nMnO4- (TN2) = a - (a - 1,6b) = 1,6b (mol)
Coi 1,6b (mol) = 1 (mmol) = 1x10-3 (mol) ⟶ b = 6,25x10-4 (mol)
Khối lượng NO3- có trong mẫu nước tương ứng với số mol MnO4- chênh lệch là:
mNO3- = 62.b = 62 . 6,25x10-4 = 0,03875 (g) = 38,75 (mg) ≈ 38,8 (mg)
⇒ Điền đáp án: 38,8