PHẦN I. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
xuất hiện kết tủa vàng 2,4,6-trinitrophenol (axit picric):
![540625[LG].png](https://asset.moon.vn/img/ai/Teachers/rongden_167/ProS2018/BAI%2016/540625[LG].png)
⇒ Chọn đáp án D
Đáp án: D
Xét các đáp án còn lại:
❌ B. Ta có MX = 46 → 14n + 18 = 46 → n = 2
→ Công thức phân tử của X là C2H5OH → Có thể tham gia phản ứng tách nước tạo C2H4.
❌ C. Ta có MX = 60 → 14n + 18 = 32 → n = 3
→ Công thức phân tử của X là C3H7OH → Có thể tham gia phản ứng tách nước tạo C3H6.
❌ D. Ta có MX = 74 → 14n + 18 = 74 → n = 4
→ Công thức phân tử của X là C4H9OH → Có thể tham gia phản ứng tách nước tạo C4H8.
⇒ Chọn đáp án A Đáp án: A
✔️ A. Đũa thủy tinh được dùng để khuấy trộn hỗn hợp phản ứng, ống hút nhỏ giọt dùng để thêm các hóa chất với lượng nhỏ. Đây là các dụng cụ thông thường trong phòng thí nghiệm hóa học.
✔️ B. Lưới amiăng được dùng để phân tán nhiệt khi đun nóng, kẹp sắt dùng để giữ các dụng cụ thủy tinh. Đây là các dụng cụ cần thiết khi đun nóng hỗn hợp phản ứng.
✔️ C. Đèn cồn được dùng để đun nóng hỗn hợp phản ứng, bát sứ được dùng để chứa hỗn hợp phản ứng. Đây là các dụng cụ phù hợp trong quá trình điều chế xà phòng.
❌ D. Nhôm phản ứng với dung dịch kiềm (NaOH hoặc KOH) trong quá trình xà phòng hóa, tạo ra khí hydro và muối aluminat. Do đó, không nên sử dụng bát nhôm hoặc xoong nhôm để điều chế xà phòng.
⟹ Chọn đáp án D Đáp án: D
- Trong amine, một hoặc nhiều nguyên tử hydrogen của NH3 được thay thế bằng các gốc hydrocarbon nên amine là dẫn xuất của ammonia.
⇒ Amine là dẫn xuất của ammonia, trong đó nguyên tử hydrogen trong phân tử ammonia được thay thế bằng gốc hydrocarbon.
⇒ Chọn đáp án D Đáp án: D
Trong nước, BaCl2 tan tốt và phân li hoàn toàn thành ion Ba2+ và Cl−:
BaCl2 → Ba2+ + 2Cl−
Khi gặp ion sulfate (SO42−), ion Ba2+ sẽ tạo kết tủa trắng barium sulfate (BaSO4), không tan trong nước:
Ba2+ + SO42− → BaSO4↓
Nhờ phản ứng đặc trưng này, BaCl2 được dùng phổ biến trong phòng thí nghiệm để nhận biết ion SO42−.
⇒ Chọn đáp án A
Đáp án: A
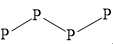
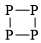
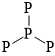
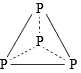
Xét các cấu trúc đề bài cho:
A. Mỗi nguyên tử P chỉ có 1 hoặc 2 liên kết → Không thoả mãn.
B. Mỗi nguyên tử P chỉ có 2 liên kết → Không thoả mãn.
C. Có các nguyên tử P chỉ có 1 liên kết → Không thoả mãn.
D. Mỗi nguyên tử P đều có 3 liên kết → Thoả mãn.
⇒ Chọn đáp án D
Đáp án: D
Phân tích đáp án:
✅ A. Sinh ra Hg dạng hơi, độc tính cao.
Phản ứng phân hủy HgS khi đun nóng: HgS –to⟶ Hg + S
Hg dạng hơi rất độc, có thể gây tổn thương hệ thần kinh, thận và các cơ quan khác khi hít phải.
❌ B. Sinh ra muối HgSO4, độc tính cao.
HgSO4 không sinh ra khi nung HgS, vì phản ứng này không có sự tham gia của H2SO4 hay oxygen để tạo muối sulfate.
❌ C. HgS bị phân hủy, mất tác dụng thuốc.
Đúng là HgS bị phân hủy, nhưng vấn đề chính không phải là mất tác dụng thuốc mà là tạo ra Hg dạng hơi rất độc.
❌ D. Sinh ra muối HgSO3, cơ thể không hấp thụ.
HgSO3 cũng không sinh ra từ phản ứng nung HgS.
⇒ Chọn đáp án A Đáp án: A
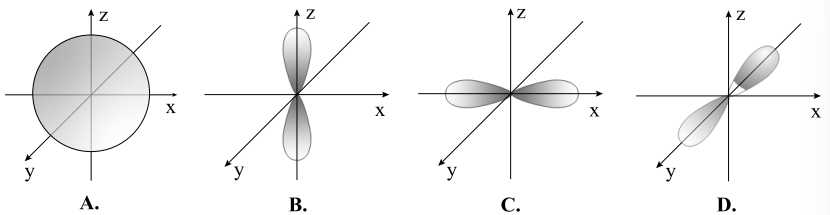
- AOpx là AO có dạng hình số 8 nổi và định hướng theo trục Ox (nằm trên trục Ox).
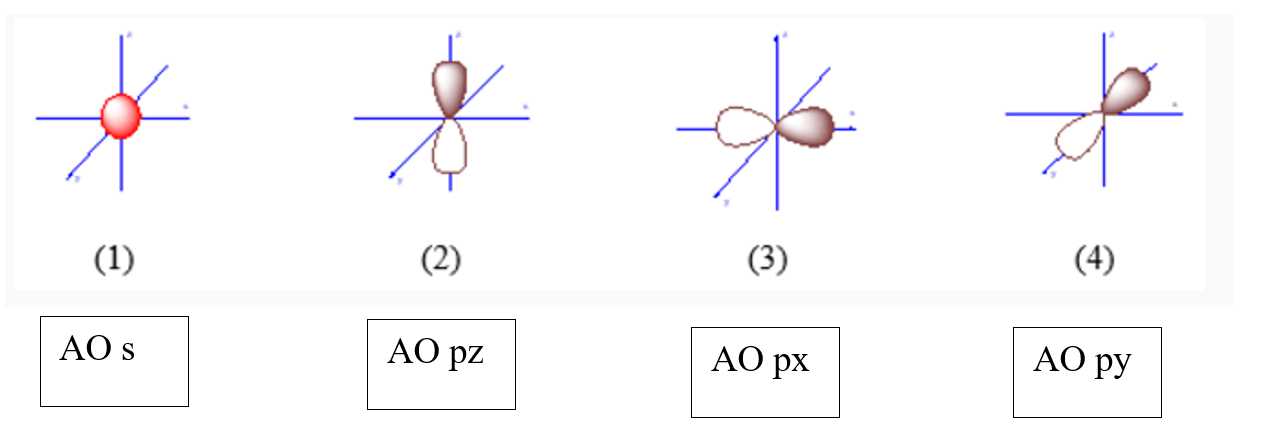
⟹ Chọn đáp án C Đáp án: C
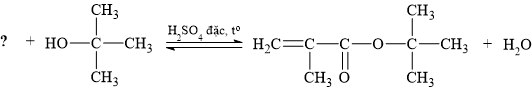
Carboxylic acid cần thiết để hoàn thành phản ứng điều chế ester trên có tên gọi là
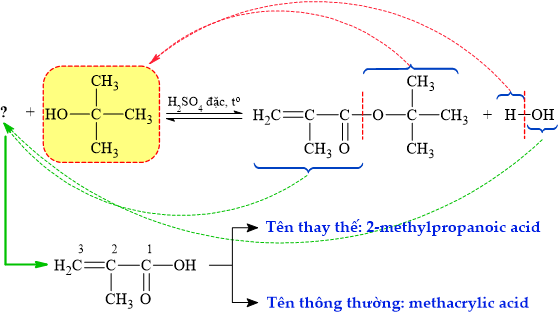
⇒ Carboxylic acid cần thiết để hoàn thành phản ứng điều chế ester là methacrylic acid
⇒ Chọn đáp án C
► Chú ý: CH2=CHCOOH là acrylic acid; có nhóm metyl CH3 đính vào tạo CH2=C(CH3)COOH
⇝ tên gọi thông thường được giản lược là methacrylic acid. Đáp án: C
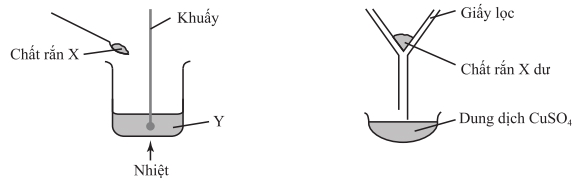
Chất X và Y trong thí nghiệm lần lượt là
Quan sát thiết bị:
- Chất rắn X được thêm vào dung dịch Y và đun nóng, khuấy → tạo dung dịch CuSO₄
- Sau phản ứng, lọc để loại bỏ X dư → chứng tỏ X không tan hết và không phải là muối dễ tan
- Y ban đầu là dạng dung dịch → nhiều khả năng là acid loãng
⟹ Chọn đáp án B
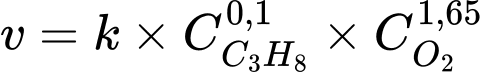
Nếu nồng độ O2 giảm đi 2 lần thì tốc độ của phản ứng propane cháy giảm bao nhiêu lần?
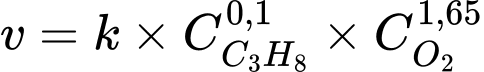
Tốc độ phản ứng khi nồng độ O2 giảm đi 2 lần:
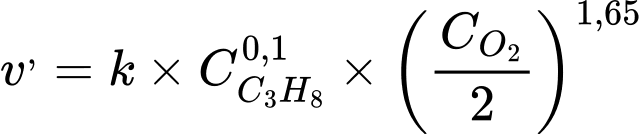
→
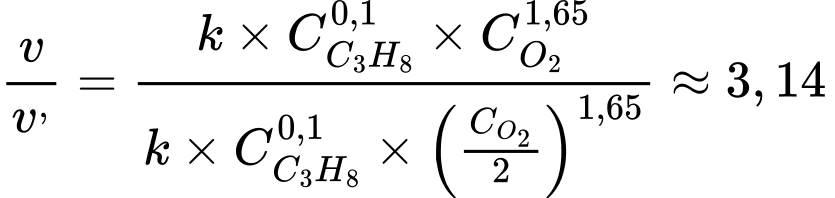
→ Tốc độ phản ứng giảm 3,14 lần.
⇒ Chọn đáp án A Đáp án: A
⇒ Chọn đáp án B Đáp án: B
nH2C=CH2 –to, xt, p⟶ –(CH2-CH2)–n
⇒ Chọn đáp án B Đáp án: B
Phenylalanine (Phe) là một loại amino acid thiết yếu, tham gia vào cấu tạo của protein và được sử dụng làm thuốc hỗ trợ điều trị bệnh trầm cảm trong y học. Công thức cấu tạo của Phe như sau: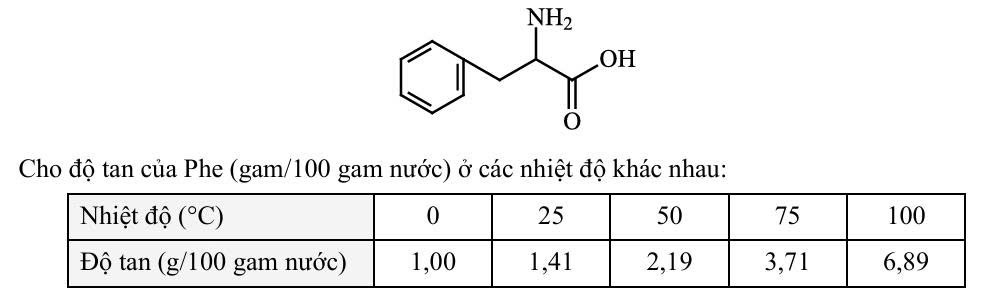
Cho các nhận định sau:
(a) Phe thuộc loại α-amino acid và có tính chất lưỡng tính.
(b) Ở pH = 2, Phe di chuyển về phía cực dương của điện trường.
(c) Ở 25 °C, dung dịch Phe bão hoà có nồng độ là 1,41%.
(d) Tinh chế được Phe bằng phương pháp kết tinh.
Số nhận định đúng là:
• Công thức:

• Có một nhóm Carboxyl (
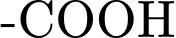 ) và một nhóm Amino (
) và một nhóm Amino ( ).
).(a) Phe thuộc loại
 -amino acid và có tính chất lưỡng tính. => Đúng
-amino acid và có tính chất lưỡng tính. => Đúng•
 -amino acid: Nhóm
-amino acid: Nhóm  được đính vào nguyên tử Carbon số
được đính vào nguyên tử Carbon số  (ngay cạnh nhóm
(ngay cạnh nhóm 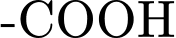 ). Cấu tạo của Phe thỏa mãn điều này.
). Cấu tạo của Phe thỏa mãn điều này.• Tính lưỡng tính: Do có cả nhóm acid (
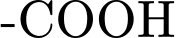 ) và nhóm base (
) và nhóm base ( ), Phe có thể phản ứng với cả acid mạnh và base mạnh.
), Phe có thể phản ứng với cả acid mạnh và base mạnh.(b) Ở
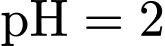 , Phe di chuyển về phía cực dương của điện trường. => Sai
, Phe di chuyển về phía cực dương của điện trường. => Sai• Amino acid tồn tại dưới dạng ion lưỡng cực (
 ) khi ở
) khi ở  trung tính.
trung tính.•
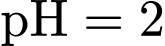 (môi trường acid mạnh): Nhóm
(môi trường acid mạnh): Nhóm 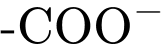 bị proton hóa thành
bị proton hóa thành 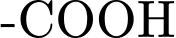 .
.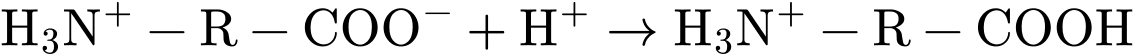
• Phe sẽ tồn tại chủ yếu dưới dạng cation (ion mang điện tích dương):
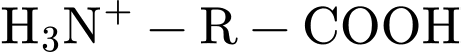 .
.• Cation sẽ di chuyển về phía cực âm (cathode) của điện trường, không phải cực dương.
(c) Ở
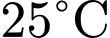 , dung dịch Phe bão hoà có nồng độ là
, dung dịch Phe bão hoà có nồng độ là 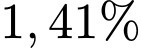 . => Sai
. => Sai• Độ tan của Phe ở
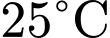 :
: 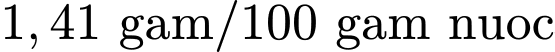 .
.• Nồng độ phần trăm (
 ):
):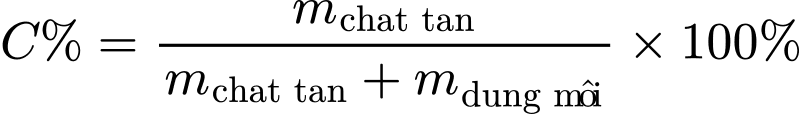
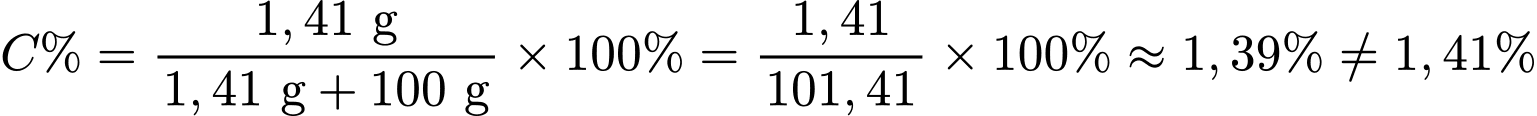
(d) Tinh chế được Phe bằng phương pháp kết tinh. => Đúng
• Dữ liệu bảng cho thấy độ tan của Phe thay đổi đáng kể theo nhiệt độ (tăng từ 1 ở 0oC lên 6,89 ở 100oC ).
• Đây là đặc điểm lý tưởng để sử dụng phương pháp tái kết tinh (kết tinh lại) để tinh chế chất: hòa tan chất ở nhiệt độ cao, lọc nóng, sau đó làm lạnh để chất kết tinh trở lại.
⟹ Chọn đáp án B (a và d đúng) Đáp án: B
Sơ đồ pin sau được sử dụng để đo thế điện cực chuẩn của điện cực Cr2O72–/Cr3+ trong môi trường acid: Cr2O72– + 14H+ + 6e →2Cr3+ + 7H2O.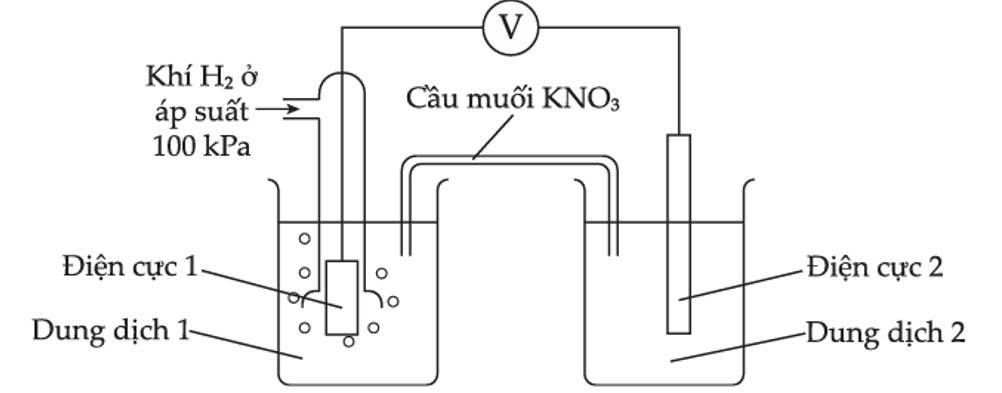
Điện cực và dung dịch điện li được sử dụng ở cốc 1 là:
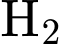 với áp suất
với áp suất 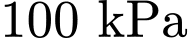 (
( ). Đây chính là Điện cực Hydrogen.
). Đây chính là Điện cực Hydrogen.• Để hoạt động như điện cực chuẩn, cốc 1 phải là Điện cực Tham chiếu Chuẩn (SHE).
• Điện cực: Phải là kim loại trơ
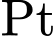 để cung cấp bề mặt cho phản ứng oxi hóa/khử của
để cung cấp bề mặt cho phản ứng oxi hóa/khử của 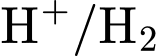 và dẫn điện.
và dẫn điện.• Dung dịch: Phải cung cấp môi trường
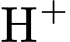 (acid mạnh) với nồng độ chuẩn
(acid mạnh) với nồng độ chuẩn  . Dung dịch acid mạnh thường dùng nhất là
. Dung dịch acid mạnh thường dùng nhất là 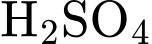 hoặc
hoặc 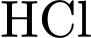 .
.o
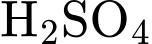 là acid mạnh, tạo môi trường
là acid mạnh, tạo môi trường 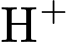 .
.o
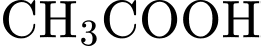 là acid yếu, không dùng để tạo dung dịch chuẩn
là acid yếu, không dùng để tạo dung dịch chuẩn 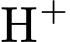 cho SHE.
cho SHE.=> Điện cực và dung dịch điện li được sử dụng ở cốc 1 là Pt và dung dịch
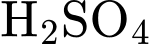 .
.⟹ Chọn đáp án C Đáp án: C
⇒ Chọn đáp án C Đáp án: C
Sử dụng đoạn thông tin dưới đây để trả lời câu 17 và câu 18:
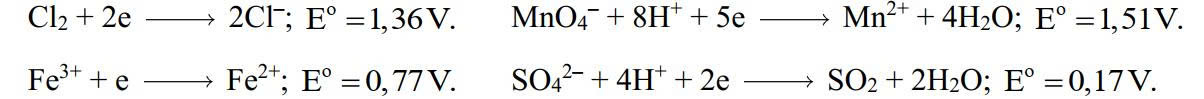
Để chuẩn hóa dung dịch KMnO4 (xác định nồng độ dung dịch), một học sinh đã cân 5,56 g FeSO4.7H2O, hòa tan nó trong H2SO4 và pha loãng đến tổng thể tích là 250,0 mL bằng nước cất. Lấy 3 phần vào 3 bình tam giác, mỗi phần lấy 25,0 mL dung dịch này và thêm 10 mL H2SO4 2,00 M. Sau đó chuẩn độ các phần này bằng dung dịch KMnO4. Thể tích dung dịch KMnO4 sử dụng trung bình là 21,2 mL.
2KMnO4 + 16HCl → 2KCl + 2MnCl2 + 5Cl2 + 8H2O
Phân tích các đáp án:
⟹ Chọn đáp án C
Đổi 21,2 mL = 0,0212 L
Số mol của FeSO4.7H2O là nFeSO4.7H2O = 5,56 : 278 = 0,02 mol
Số mol FeSO4 trong 50 mL dung dịch là
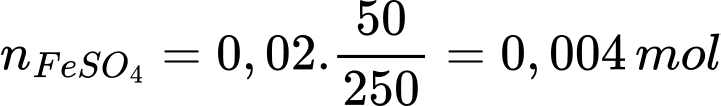
Từ PTHH số mol của KMnO4 là nKMnO4 = 0,0008 mol
Nồng độ của dung dịch KMnO4 là
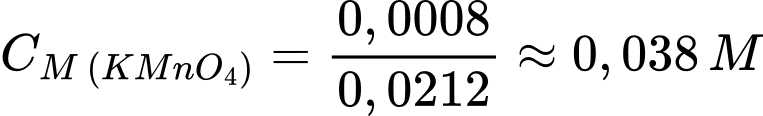
⟹ Chọn đáp án B Đáp án: B
PHẦN II. Thí sinh trả lời từ câu 1 đến câu 4. Trong mỗi ý a), b), c), d) ở mỗi câu, thí sinh chọn đúng hoặc sai.
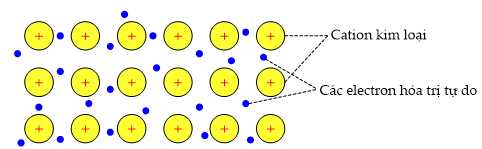
✔️ A. Đúng. Tinh thể kim loại bao gồm các cation kim loại (ion dương) sắp xếp theo mạng tinh thể và các electron hóa trị tự do di chuyển giữa chúng.
✔️ B. Đúng. Trong tinh thể kim loại, các cation kim loại được sắp xếp theo trật tự xác định, tạo thành mạng lưới tinh thể. Điều này giúp kim loại có tính chất cơ học bền vững.
✔️ C. Đúng. Khi có điện trường tác động, các electron hóa trị tự do có thể di chuyển theo hướng ngược với điện trường, tạo nên dòng điện. Đây là lý do kim loại có tính dẫn điện cao.
❌ D. Sai. Liên kết kim loại không phải là liên kết ion (giữa cation kim loại và anion gốc axit). Thay vào đó, nó hình thành nhờ lực hút tĩnh điện giữa các cation kim loại và "biển electron" tự do. Điều này giúp kim loại có độ dẻo và tính dẫn điện cao hơn so với tinh thể ion.
• Khử: 8H+(aq) + MnO4–(aq) + 5e ⟶ Mn2+(aq) + 4H2O(l)
• Oxi hóa: H2O2(aq) ⟶ 2H+(aq) + O2(g) + 2e
Trong quá trình chuẩn độ, một học sinh lấy 5,0 mL dung dịch hydrogen peroxide vào một bình tam giác, pha loãng nó thành 50,0 mL bằng nước cất. Sau đó, học sinh chuẩn độ dung dịch potassium permanganate 0,150 M vào bình trong khi khuấy liên tục.
Thể tích của dung dịch potassium permanganate trong burette trước và sau quá trình chuẩn độ được biểu diễn như sau:
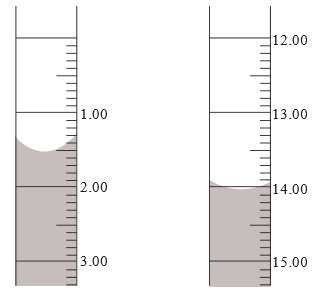
✔️(a) – Đúng. Mức ban đầu ở vach 1,5 mL sau khi kết thúc chuẩn độ lượng KMnO4 ở vạch 14 mL tức lượng KMnO4 đã sửa dụng là 12,5 mL.
❌(b) – Sai.
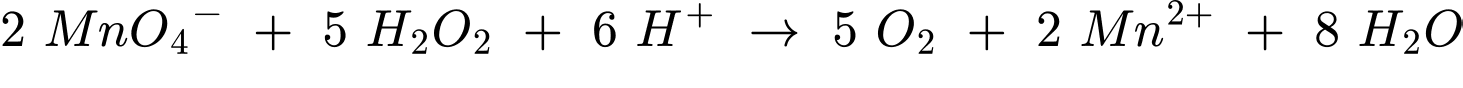
Đổi 12,5 mL = 0,0125 L; 50 mL = 0,05 L
Số mol của KMnO4 là nKMnO4 = 0,0125.0,15 = 0,001875 mol
Từ phương trình hóa học số mol của H2O2 là: 0,0046875 mol
Nồng độ ban đầu của H2O2 là
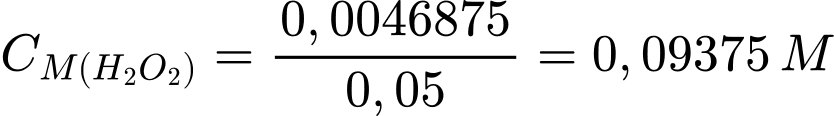
✔️(c) – Đúng. Khi nhỏ thêm KMnO4 vào thì dung dịch KMnO4 phản ứng với H2O2 tạo dung dịch trong suốt khi chưa đến điểm tương đương, Khi đến điểm tương đương thì dung dịch có màu hồng nhạt.
✔️(d) - Đúng .
Giả sử a mol H2O2 trong môi trường aicd => 0,4 mol KMnO4
a mol H2O2 trong môi trường base => 2 mol KMnO4
Vậy trong môi trường base cần dùng lượng lớn hơn.
∎ Bước 1: Cho khoảng 3 mL CH3CH(CH3)CH2CH2OH, 3 mL CH3COOH và vài giọt H2SO4 đặc vào ống nghiệm.
∎ Bước 2: Lắc đều ống nghiệm rồi đun cách thuỷ (trong nồi nước nóng) khoảng 5 – 7 phút ở 65 – 70 °C.
∎ Bước 3: Làm lạnh, sau đó thêm khoảng 5 mL dung dịch NaCl bão hoà vào ống nghiệm.
✔️A. Đúng. H2SO4 đặc có vai trò xúc tác cho phản ứng tạo isoamyl acetate.
❌B. Sai. Mục đích chính của việc thêm dung dịch NaCl bão hòa để giảm độ tan của ester trong nước và làm cho ester tách ra dễ hơn.
✔️C. Đúng. vì phản ứng ester trong môi trường acid là phản ứng thuận nghịch nên luôn còn 1 lượng acid và alcohol chưa phản ứng.
❌D. Sai. Sau bước 3, trong ống nghiệm thu được 1 lớp ester không tan trong nước.
• Bước 1: Cho vào ống nghiệm khô khoảng 1 mL hexane và nhỏ thêm vào ống nghiệm khoảng 1 mL nước bromine. Quan sát màu sắc sau đó lắc nhẹ hỗn hợp rồi để yên 10 phút.
• Bước 2: Nút ống nghiệm bằng bông đã tẩm dung dịch NaOH rồi nhúng phần đáy ống nghiệm vào cốc nước nóng 50 oC (đã chuẩn bị trước) hoặc để ống nghiệm ra nơi có ánh sáng Mặt Trời.
Chú ý an toàn: Hexane, bromine và hydrogen bromine dễ bay hơi, có mùi xốc, độc.
✔️(a) – Đúng. Br2 tan trong hexane tốt hơn tan trong H2O nên Br2 sẽ di chuyển từ dung dịch nước sang dung môi mới là hexane.
✔️(b) – Đúng. Phần nổi là dung dịch Br2/Hexane có màu vàng nâu có khối lượng riêng nhỏ hơn, phần dưới là H2O nên phần trên có màu đậm hơn phần dưới.
✔️(c) – Đúng. Nút ống nghiệm bằng bông đã tẩm dung dịch NaOH là để hạn chế các khí độc bay ra ngoài. Bước 2 xảy ra phản ứng giữa hexane với Br2 tạo khí HBr gây độc
C6H14 + Br2 → C6H13Br + HBr
❌(d) – Sai. Cl2 phản ứng với hexane để tạo ra các dẫn xuất chloro, các dẫn xuất này đều tan trong hexane → tạo thành dung dịch đồng nhất.
PHẦN III. Thí sinh trả lời từ câu 1 đến 6. Thí sinh điền kết quả mỗi câu vào mỗi ô trả lời tương ứng theo hướng dẫn của phiếu trả lời.
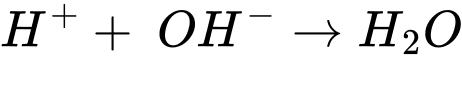
Đổi 25 mL = 0,025 L; 12,5 mL = 0,0125 L
Số mol của hydroxide kim loại là nX(OH)y = 0,025.0,0125 = 0,0003125 mol
Số mol của dung dịch acid cần chuẩn độ là nHCl = 0,0125.0,05 = 0,000625 mol
Từ PTHH số mol của OH- là nOH- = nH+ = 0,000625 mol
Giá trị của y là
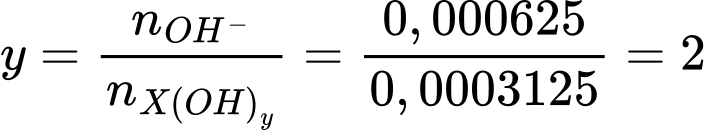
⟹Điền đáp án : 2
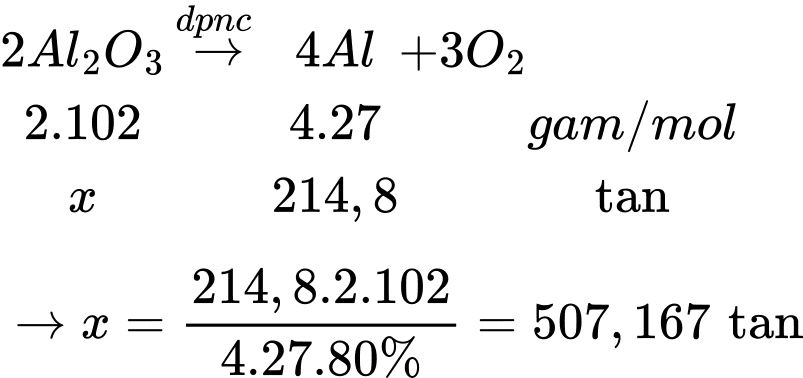
Khối lượng quặng bauxite là mquặng = 507,167 : 45% ≈ 1127
⟹Điền đáp án : 1127
Lys-Ala-Val + 4HCl + 2H2O → ClH3N(CH2)4CH(NH3Cl)COOH + CH3CH(NH3Cl)COOH + CH3CH(CH3)CH(NH3Cl)COOH
Thấy số mol của HCl tỉ lệ 4 : 1 với số mol của tripeptide trên phản ứng nên HCl dư thì số mol HCl phản ứng là:
nHCl = 4nLys-Ala-Val = 4 x 2 = 8 (mol)
⇒ Điền đáp án: 8
mglycerol = 3600000.10 = 36000000 gam = 36 tấn
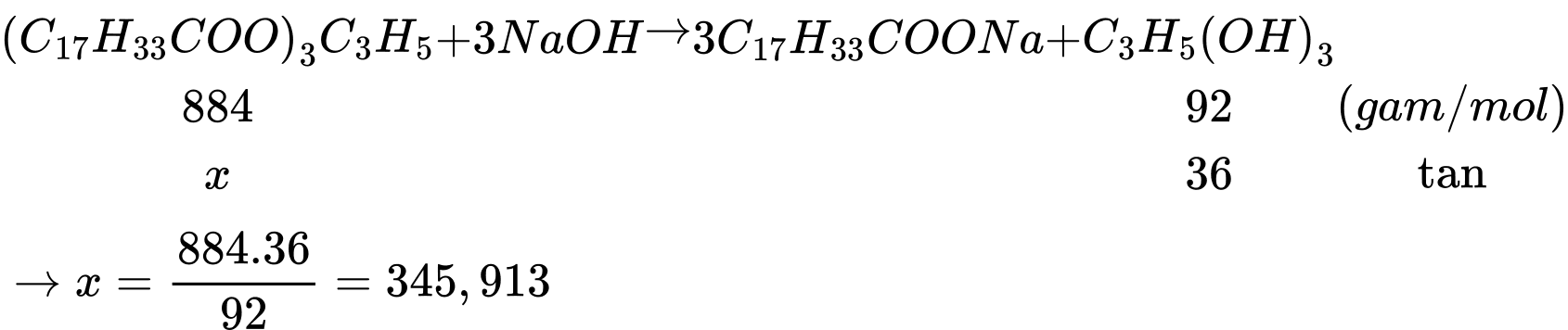
Khối lượng của chất béo là 345,913:70% ≈ 494 tấn
⟹Điền đáp án : 494
2Ca5(PO4)3F(s) + 7H2SO4(aq) ⟶ 3Ca(H2PO4)2 + 7CaSO4(aq) + 2HF(g)
Từ tỉ lệ phương trình số mol của Ca(H2PO4)2 và CaSO4 lần lượt là nCa(H2PO4)2 = 1,5 (mol) và nCaSO4 = 3,5 (mol)
Tổng khối lượng phân bón là:
mCa(H2PO4)2 + mCaSO4 = 1,5.234,05 + 3,5.136,14 = 827,565 (g)
Bảo toàn nguyên tố phosphorus ta được:
nP2O5 = nCa(H2PO4)2 = 1,5 (mol)
Độ dinh dưỡng của phân superphosphate là:

⇒ Điền đáp án: 25,7
2KMnO4 + 5CaC2O4 + 8H2SO4 → 5CaSO4 + K2SO4 + 2MnSO4 + 10CO2 + 8H2O
Giả sử calcium oxalate kết tủa từ 1 mL máu một người tác dụng vừa hết với 1,95 mL dung dịch potassium permanganate (KMnO4) 4,98×10–4 M. Xác định nồng độ ion calcium trong máu người đó bằng đơn vị mg Ca2+/100 mL máu (Làm tròn đến hàng phần trăm).
Đổi 1,95 mL = 0,00195 L
Số mol của KMnO4 là nKMnO4 = 0,00195,4,98.10-4 = 9,711.10-7 mol
Số mol Ca2+ trong 1 mL máu là nCa2+ = 9,711.10-7 × 5 ÷ 2 = 2,42775×10-6 gam
Nồng độ ion calcium trong máu là
mCa2+ (100mL) = 2,422775×10-6 × 40 × 100 = 9,711×10-3 (gam) ≈ 9,71
⟹Điền đáp án : 9,71