PHẦN I. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
Ester bị thuỷ phân trong môi trường acid thường tạo thành carboxylic acid và alcohol (hoặc phenol) tương ứng.
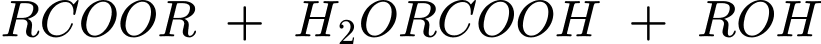
b. Phản ứng thuỷ phân ester trong môi trường base
Ester bị thuỷ phân trong môi trường base (như NaOH, KOH) thường thu được muối carboxylate và alcohol:
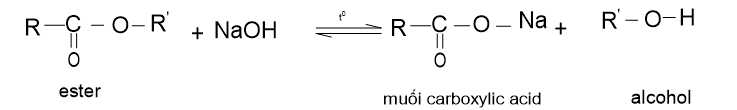
Phản ứng thuỷ phân ester trong môi trường base là phản ứng một chiều. Phản ứng này được ứng dụng làm xà phòng nên được gọi là phản ứng xà phòng hoá.
⟹ Chọn đáp án B Đáp án: B
❌A – Sai. Thùng bằng kẽm không thể dùng để chứa dung dịch CuSO4. Do Zn có tính khử mạnh hơn Cu nên sẽ có phản ứng hóa học làm thùng kẽm bị ăn mòn dần.
Zn + CuSO4 → ZnSO4 + Cu
❌B – Sai. Thùng bằng kẽm không thể dùng để chứa dung dịch AgNO3. Do Zn có tính khử mạnh hơn Ag nên sẽ có phản ứng hóa học làm thùng kẽm bị ăn mòn dần.
Zn + 2AgNO3 → Zn(NO3)2 + 2Ag
❌C – Sai. Thùng bằng thiếc (Sn) không thể dùng để chứa dung dịch AgNO3. Do Sn có tính khử mạnh hơn Ag nên sẽ có phản ứng hóa học làm thùng thiếc bị ăn mòn dần.
Sn + 2AgNO3 → Sn(NO3)2 + 2Ag
✔️D – Đúng. Thùng bằng bạc (Ag) có thể dùng để chứa dung dịch CuSO4. Do Ag có tính khử yếu hơn Cu nên không có phản ứng hóa học với dung dịch CuSO4
⟹Chọn đáp án D Đáp án: D
Do đó, tên gọi của Fe2(SO4)3 là iron(III) sulfate.
Các chất còn lại có công thức như sau:
A. iron(II) sulfide: FeS.
C. iron(II) sulfate: FeSO4.
D. iron(III) sulfite: Fe2(SO3)3.
⇒ Chọn đáp án B Đáp án: B
✔️ A. Có thể phân biệt được các mẫu:
+) Cho nước bromine vào 3 dung dịch sẽ nhận biết được glucose (có nhóm chức aldehyde CHO)
+) Khi cho dung dịch acid vào 2 mẫu dung dịch còn lại, đun nóng thì saccharose sẽ bị thủy phân thành glucose và fructose. Khi này dùng nhỏ nước bromine vào 2 mẫu thì ở mẫu chứa saccharose sẽ có phản ứng (của glucose với nước bromine) nên nhận biết được saccharose
+) Mẫu còn lại không có phản ứng nào là fructose.
✔️ B. Có thể phân biệt được các mẫu:
+) Cho thuốc thử Tollens vào 3 mẫu thì chỉ có saccharose là không có phản ứng tráng bạc nên nhận biết được saccharose.
+) Khi cho nước bromine vào 2 mẫu còn lại là glu và fruc thì chỉ có glu có phản ứng nên phân biệt được 2 mẫu.
C. Không thể phân biệt được các mẫu:
+) Nước bromine nhận biết được glucose.
+) Hồ tinh bột dùng để nhận biết iodine nên không phân biệt được fructose và saccharose.
✔️ D. Có thể phân biệt được các mẫu:
+) Nước bromine nhận biết được glucose.
+) Cu(OH)2/NaOH khi được cho vào 2 mẫu fruc và saccha, đun nóng thì fructose trong môi trường kiềm bị chuyển hóa thành glucose sẽ xuất hiện kết tủa đỏ gạch Cu2O còn saccha thì không.
⇒ Chọn đáp án C Đáp án: C
❌ B. Khi hòa tan KHSO4 và KNO3 vào nước thu được dung dịch chứa 2 anion là HSO4- và NO3-.
❌ C. Khi hòa tan NaOH và NaCl vào nước thu được dung dịch chứa 2 anion là OH- và Cl-.
❌ D. Khi hòa tan NH4HCO3 và NH4Cl vào nước thu được dung dịch chứa 2 anion là HCO3- và Cl-.
⟹ Chọn đáp án A Đáp án: A
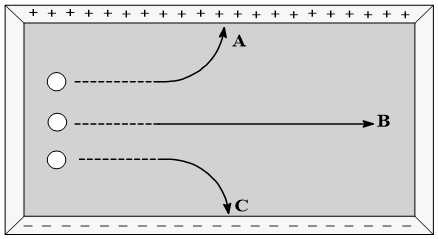
Hạt nào sau đây có thể là hạt electron?
- Quy tắc xác định: cùng dấu thì đẩy, trái dấu thì hút.
+) Hạt mang điện dương thì bị hút về bản âm.
+) Hạt mang điện âm thì bị hút về bản dương
- Nếu hạt không mang điện thì không bị lệch trong điện trường.
Đề bài yêu cầu xác định hạt electron trong ba hạt A, B, C. Dễ dàng nhận thấy hạt electron mang điện âm thì bị hút về bản dương, vì vậy hạt A là electron. Tương tự ta tìm được hạt C là hạt proton. Hạt còn lại không bị lệch trong điện trường nên là hạt neutron (không mang điện)
⟹ Chọn đáp án A Đáp án: A
⟹ Chọn đáp án C Đáp án: C
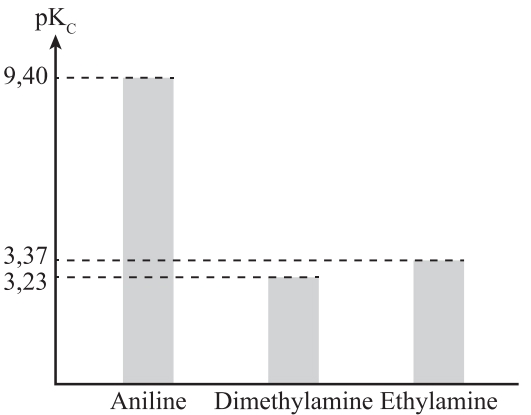
Giá trị pKc ở 25oC của một số amine như sau: pKC = -log(KC). Ở 25oC, nhận định nào sau đây đúng?
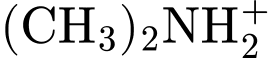 . => Đúng
. => Đúng• Phản ứng:
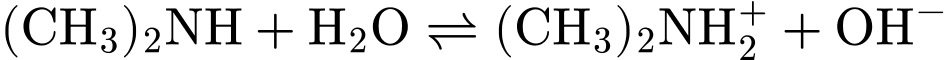
• Cation tạo thành là
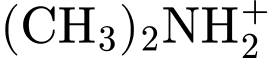 .
.B. Tính base giảm dần theo thứ tự: aniline, ethylamine, dimethylamine. => Sai
• Thứ tự giảm dần tính base đúng là: Dimethylamine
 Ethylamine
Ethylamine  Aniline. (Do
Aniline. (Do 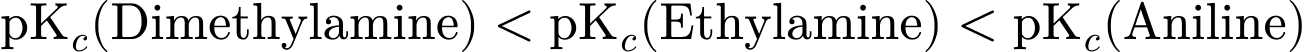
C. Dung dịch
 có
có  nhỏ hơn dung dịch
nhỏ hơn dung dịch  .=> Sai
.=> Sai• Dimethylamine base mạnh hơn nên khi cùng nồng độ thì dung dịch của nó có pH cao hơn (Do
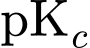 nhỏ hơn).
nhỏ hơn). • Lưu ý : Base càng mạnh
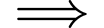
 càng nhiều
càng nhiều 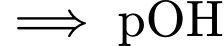 càng nhỏ
càng nhỏ  càng lớn.
càng lớn.D. Hằng số cân bằng của phản ứng giữa ethylamine với nước là
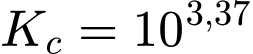 . => Sai
. => Sai•
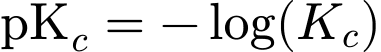 .
.• Từ đồ thị,
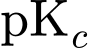 của Ethylamine
của Ethylamine 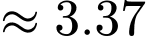 .
.•
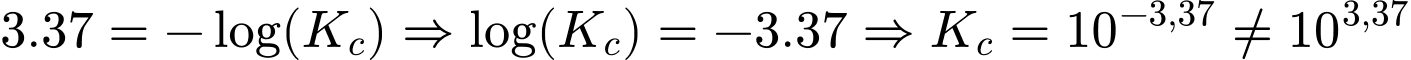 .
.⟹ Chọn đáp án A Đáp án: A
Phương trình phản ứng:
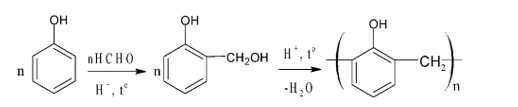
C6H5OH + 3Br2 → C6H2Br3OH↓ + 3HBr
Phân tích các đáp án khác:
A. Phenol phản ứng với NaOH tạo dung dịch natri phenolate (C6H5ONa) tan trong nước, không tạo kết tủa.
C. Phenol làm quỳ tím hóa đỏ nhẹ, nhưng không tạo kết tủa.
D. Phenol là acid yếu, không làm phenolphthalein đổi màu, cũng không tạo kết tủa.
⇒ Chọn đáp án B Đáp án: B
Insulin, một loại hormone thuộc loại protein, được sản sinh bởi tuyến tuỵ, có chức năng điều hoà quá trình chuyển hoá glucose trong cơ thể. Insulin thúc đẩy sự hấp thu glucose của các tế bào và dự trữ glucose dư thừa trong gan và cơ.Thuỷ phân không hoàn toàn một đoạn phân tử insulin thu được tripeptide X có công thức cấu tạo như sau: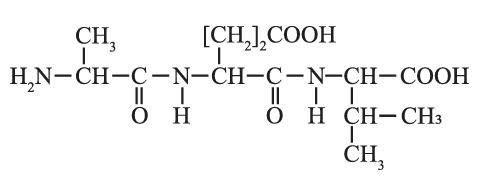
Cho các nhận định:
(a) Phân tử X chứa có amino acid đầu C là Glu.
(b) Thuỷ phân không hoàn toàn X thu được sản phẩm có chứa Ala-Glu.
(c) Dung dịch X có phản ứng màu biuret.
(d) Tách biệt được 3 amino acid tạo thành X bằng phương pháp điện di.
Các nhận định đúng là
1. AA thứ nhất (đầu N): Nhóm thế
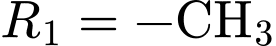 . Đây là gốc của amino acid Alanine (Ala).
. Đây là gốc của amino acid Alanine (Ala).2. AA thứ hai (giữa): Nhóm thế
 . Đây là gốc của amino acid Glutamic acid (Glu).
. Đây là gốc của amino acid Glutamic acid (Glu).3. AA thứ ba (đầu C): Nhóm thế
 . Đây là gốc của amino acid Valine (Val).
. Đây là gốc của amino acid Valine (Val).=> tripeptide X có công thức là Ala-Glu-Val.
________________________________________
(a) Phân tử X chứa amino acid đầu C là Glu.
 Sai.
Sai.• X là Ala-Glu-Val.
• Amino acid đầu C (có nhóm
 tự do) là Val.
tự do) là Val.(b) Thủy phân không hoàn toàn X thu được sản phẩm có chứa Ala-Glu.
 Đúng
Đúng• Tripeptide X là
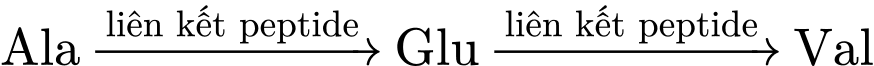 .
.• Thủy phân không hoàn toàn X có thể cắt đứt 1 trong 2 liên kết peptide, tạo ra các dipeptide và amino acid.
• Các dipeptide có thể thu được là: Ala-Glu và Glu-Val.
(c) Dung dịch X có phản ứng màu biuret.
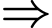 Đúng.
Đúng.• Phản ứng màu biuret là phản ứng đặc trưng cho các hợp chất có từ hai liên kết peptide trở lên (tức là tripeptide, tetrapeptide, polypeptide và protein).
• Tripeptide X có 2 liên kết peptide.
(d) Tách biệt được 3 amino acid tạo thành X bằng phương pháp điện di.
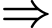 Sai.
Sai.• 3 amino acid tạo thành X là: Alanine (Ala), Glutamic acid (Glu) và Valine (Val).
• Điện di là phương pháp tách các chất dựa trên sự khác nhau về tốc độ di chuyển của các ion dưới tác dụng của điện trường. Tốc độ di chuyển phụ thuộc vào điện tích và khối lượng/kích thước của ion.
o Glu là amino acid có tính acid (có 2 nhóm
 và 1 nhóm
và 1 nhóm  ), trong dung dịch đệm có pH thích hợp sẽ tồn tại dưới dạng anion (
), trong dung dịch đệm có pH thích hợp sẽ tồn tại dưới dạng anion (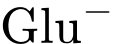 ) và di chuyển về cực dương.
) và di chuyển về cực dương.o Ala và Val là các amino acid trung tính (có 1 nhóm
 và 1 nhóm
và 1 nhóm  ). Ở
). Ở 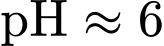 (điểm đẳng điện), chúng sẽ tồn tại chủ yếu dưới dạng lưỡng cực trung hòa nên không di chuyển trong điện trường.
(điểm đẳng điện), chúng sẽ tồn tại chủ yếu dưới dạng lưỡng cực trung hòa nên không di chuyển trong điện trường.=> Chỉ tách được Glu nhưng không tách được Ala và Val
⟹ Chọn đáp án C.(b) và (c) Đáp án: C
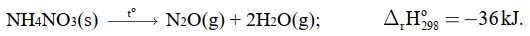
Phát biểu nào sau đây không đúng?
❌ A. Sai. Phản ứng có biến thiên enthalpy dương, là phản ứng thu nhiệt. Tuy nhiên, chính sự tỏa nhiệt từ môi trường bên ngoài (như ngọn lửa hoặc nhiệt độ cao) mới có thể kích hoạt phản ứng, gây phân hủy NH4NO3 và tạo ra một lượng lớn khí (N2O, H2O). Áp suất tăng đột ngột do thể tích khí sinh ra là nguyên nhân gây nổ, không phải do bản thân phản ứng thu nhiệt.
✔️ B. Đúng. Phản ứng sinh ra N2O(g) và H2O(g), đồng thời tỏa nhiệt từ sự phân hủy khi có các điều kiện kích hoạt. Các khí này làm thể tích giãn nở đột ngột, gây áp suất cực lớn dẫn đến vụ nổ.
✔️ C. Đúng. Nước có thể làm giảm nhiệt độ và ngăn chặn phản ứng dây chuyền. Vì vậy, đây là một biện pháp hợp lý trong trường hợp nguy cơ cháy lan hoặc nổ NH4NO3.
✔️ D. Đúng. NH4NO3 là chất oxi hóa mạnh. Nếu tiếp xúc với các chất dễ cháy hoặc nhiệt độ cao, nó có thể phân hủy mạnh, sinh nhiệt và khí, dễ dẫn đến cháy hoặc nổ.
⇒ Chọn đáp án A Đáp án: A
⟹ Chọn đáp án D Đáp án: D
⟹ Chọn đáp án B Đáp án: B

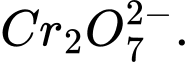
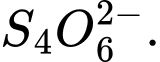
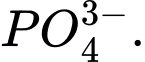
✔️Đúng.A.
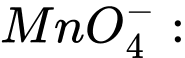 a + 4 × (−2) = −1 ⇔ a − 8 = −1 ⇔ a = +7 ⟶ Số oxi hóa trung bình của Mn là +7.
a + 4 × (−2) = −1 ⇔ a − 8 = −1 ⇔ a = +7 ⟶ Số oxi hóa trung bình của Mn là +7.❌Sai.B.
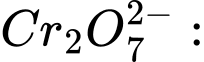 2b + 7 × (−2) = −2 ⇔ 2b − 14 = −2 ⇔ 2b = 12 ⇔ b = +6 ⟶ Số oxi hóa trung bình của Cr là +6.
2b + 7 × (−2) = −2 ⇔ 2b − 14 = −2 ⇔ 2b = 12 ⇔ b = +6 ⟶ Số oxi hóa trung bình của Cr là +6.❌Sai.C.
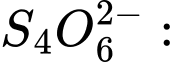 c = [(2×5) + (2×0)] ÷ 4 = 10 ÷ 4 = +2,5 ⟶ Số oxi hóa trung bình của S là +2,5.
c = [(2×5) + (2×0)] ÷ 4 = 10 ÷ 4 = +2,5 ⟶ Số oxi hóa trung bình của S là +2,5.❌Sai.D.
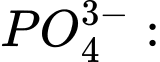 d + 4 × (−2) = −3 ⇔ d − 8 = −3 ⇔ d = +5 ⟶ Số oxi hóa trung bình của P là +5.
d + 4 × (−2) = −3 ⇔ d − 8 = −3 ⇔ d = +5 ⟶ Số oxi hóa trung bình của P là +5.Vậy số oxi hóa trung bình của nguyên tố được đánh dấu (in đậm) trong ion
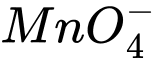 có giá trị lớn nhất.
có giá trị lớn nhất.⇒ Chọn đáp án A Đáp án: A
(a) Cho dung dịch FeCl2 vào dung dịch silver nitrate dư.
(b) Dẫn khí H2 qua bột FeO đun nóng.
(c) Cho FeSO4 vào dung dịch gồm KMnO4 và H2SO4 loãng.
(d) Cho Fe(NO3)2 vào dung dịch H2SO4 loãng.
Sau khi kết thúc phản ứng, những thí nghiệm chứng minh iron(II) có tính khử là
✔️ (a) FeCl2 + 3AgNO3 → Fe(NO3)3 + 2AgCl↓ + Ag↓.
❌ (b) H2 + FeO → Fe + H2O.
✔️ (c) 10FeSO4 + 2KMnO4 + 8H2SO4 → 5Fe2(SO4)3 + K2SO4 + 2MnSO4 + 8H2O.
✔️ (d) xảy ra: 3Fe2+ + NO3– + 4H+ → 3Fe3+ + NO↑ + 2H2O.
⇝ Có 3 thí nghiệm (a) (c) (d) mà số oxi hoá của Fe tăng (từ +2 lên +3) thể hiện tính khử
⇒ Chọn đáp án C. Đáp án: C

⟹ Chọn đáp án B Đáp án: B
Sử dụng đoạn thông tin dưới đây để trả lời câu 17 và câu 18:
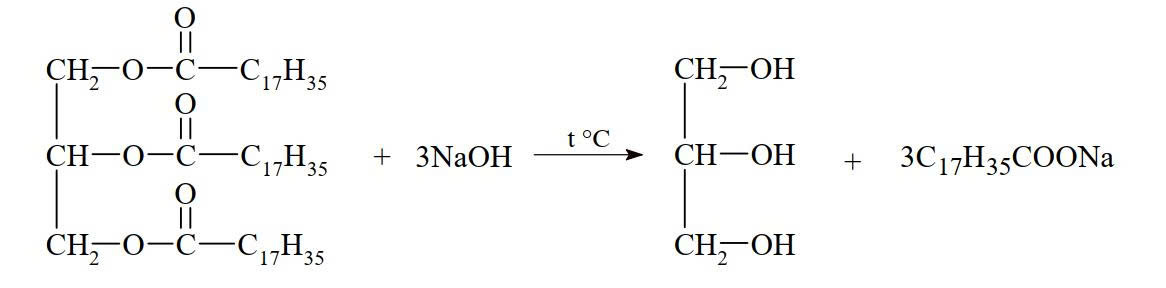
(C17H35COO)3C3H5 + 3NaOH → 3C17H35COONa + C3H5(OH)3
⟹ Chọn đáp án B Đáp án: B
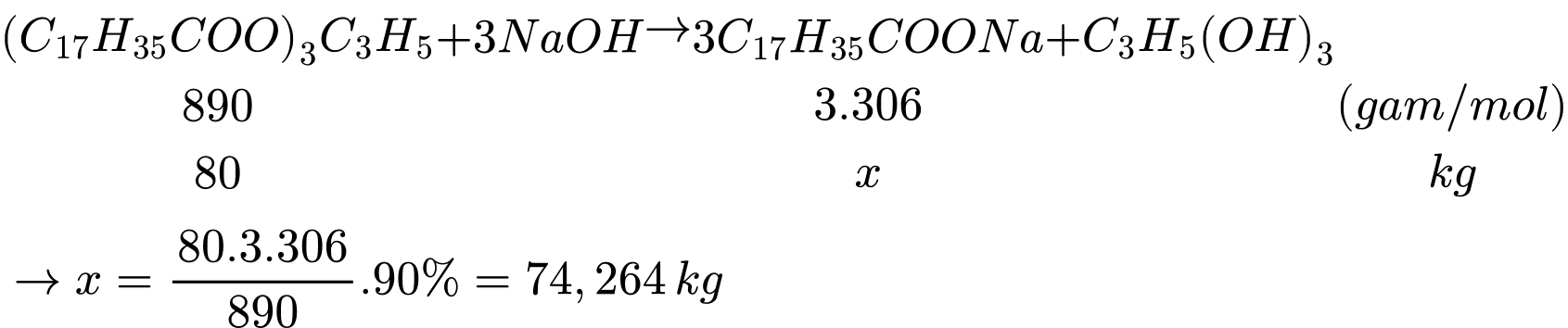
⟹ Chọn đáp án C Đáp án: C
PHẦN II. Thí sinh trả lời từ câu 1 đến câu 4. Trong mỗi ý a), b), c), d) ở mỗi câu, thí sinh chọn đúng hoặc sai.
Nhúng một miếng nhôm hình lập phương có diện tích toàn phần S = 0,24 cm2 đã được làm sạch vào dung dịch HCl 2 M (nồng độ không đổi) ở nhiệt độ 25 oC. Sau t = 144 giờ, khối lượng miếng nhôm giảm còn 27,0 mg. Tốc độ ăn mòn υ (mm/năm) của miếng nhôm được tính theo công thức:
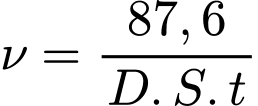 Trong đó: D = 2,7 g/cm3 là khối lượng riêng của nhôm. Trong cùng điều kiện thí nghiệm, tốc độ ăn mòn của kẽm là 39,5 mm/năm.
Trong đó: D = 2,7 g/cm3 là khối lượng riêng của nhôm. Trong cùng điều kiện thí nghiệm, tốc độ ăn mòn của kẽm là 39,5 mm/năm. 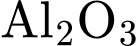 mỏng, bền, không tan trong nước, che phủ bề mặt
mỏng, bền, không tan trong nước, che phủ bề mặt 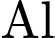 , ngăn
, ngăn 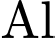 tiếp xúc với môi trường, giúp
tiếp xúc với môi trường, giúp 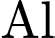 có khả năng chịu ăn mòn hóa học tốt (thụ động hóa).
có khả năng chịu ăn mòn hóa học tốt (thụ động hóa).❌ Nhận định b) – Sai, vì:
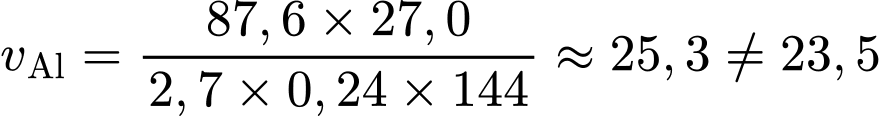 (mm/năm)
(mm/năm)❌ Nhận định c) – Sai, vì: Kẽm có tốc độ ăn mòn lớn hơn nhôm nhưng không phải do kẽm có tính khử mạnh hơn nhôm mà do nhôm có khả năng tạo lớp oxide bền để bảo vệ nên tốc độ ăn mòn sẽ nhỏ hơn kẽm. (
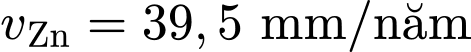 ;
; 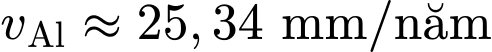 .
. 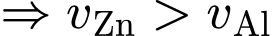 ).
). ⭐Lưu ý: Kẽm có tính khử yếu hơn nhôm trong dãy hoạt động hoá học
❌ Nhận định d) – Sai, vì: Nhôm (Al) không bị điện phân
Để tiến hành kiểm chứng tính chất hóa học của tinh bột, một học sinh đã tiến hành thí nghiệm như sau: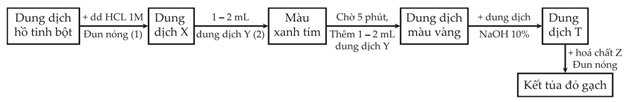
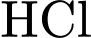 ) và nhiệt độ tạo thành Glucose (và các dextrin trung gian).
) và nhiệt độ tạo thành Glucose (và các dextrin trung gian).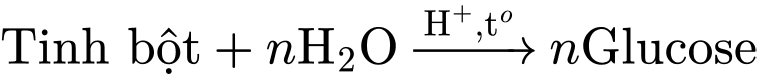
2) Phát hiện Tinh bột/Dextrin (Dung dịch Y):
• Dung dịch Y là thuốc thử đặc trưng để phát hiện tinh bột:
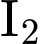 trong
trong  .
.• Bước 1: Thêm
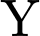 vào
vào 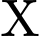 thấy Màu xanh tím
thấy Màu xanh tím 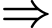 Chứng tỏ phản ứng thủy phân chưa hoàn toàn (vì vẫn còn tinh bột hoặc các dextrin có khả năng phản ứng với
Chứng tỏ phản ứng thủy phân chưa hoàn toàn (vì vẫn còn tinh bột hoặc các dextrin có khả năng phản ứng với 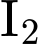 ).
).• Bước 2: Chờ 5 phút, thêm
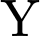 thấy Màu vàng
thấy Màu vàng 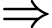 Cho thấy tinh bột đã bị thủy phân hết,
Cho thấy tinh bột đã bị thủy phân hết, 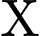 lúc này chỉ còn
lúc này chỉ còn 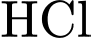 và glucose/dextrin có trọng lượng phân tử nhỏ hơn.
và glucose/dextrin có trọng lượng phân tử nhỏ hơn.3) Trung hòa Acid: Thêm
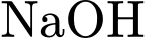 vào dung dịch để trung hòa acid
vào dung dịch để trung hòa acid 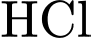 (tạo
(tạo 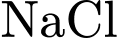 ) và tạo môi trường kiềm.
) và tạo môi trường kiềm.4) Phát hiện Glucose: Hoá chất Z là
 (hoặc
(hoặc 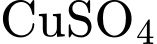 và
và 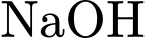 tạo ra) hoặc thuốc thử
tạo ra) hoặc thuốc thử 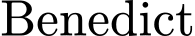 (
(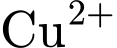 trong môi trường kiềm). Kết tủa đỏ gạch (
trong môi trường kiềm). Kết tủa đỏ gạch (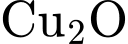 ) chứng tỏ dung dịch
) chứng tỏ dung dịch  chứa glucose (là chất có nhóm aldehyde
chứa glucose (là chất có nhóm aldehyde  - chức khử).
- chức khử).------------------------------------------------------------------------------
✔️Nhận định a) – Đúng, vì:
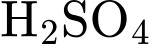 loãng cũng là acid mạnh, có thể đóng vai trò xúc tác cho phản ứng thủy phân tinh bột tương tự như
loãng cũng là acid mạnh, có thể đóng vai trò xúc tác cho phản ứng thủy phân tinh bột tương tự như 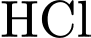 .
.✔️Nhận định b) – Đúng, vì:
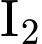 (trong
(trong  ) là thuốc thử duy nhất cho màu xanh tím với tinh bột ( hoặc các dextrin).
) là thuốc thử duy nhất cho màu xanh tím với tinh bột ( hoặc các dextrin).✔️Nhận định c) – Đúng, vì: Sau khi thêm
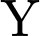 lần 1, dung dịch có màu xanh tím chứng tỏ vẫn còn tinh bột (hoặc dextrin) chưa bị thủy phân hết.
lần 1, dung dịch có màu xanh tím chứng tỏ vẫn còn tinh bột (hoặc dextrin) chưa bị thủy phân hết.✔️Nhận định d) – Đúng, vì:
 là muối acid yếu. Nó sẽ phản ứng với acid mạnh
là muối acid yếu. Nó sẽ phản ứng với acid mạnh 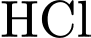 còn dư trong dung dịch
còn dư trong dung dịch 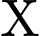 tạo ra khí
tạo ra khí 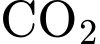 .
.
Khi sử dụng chất xúc tác Ziegler-Nattan sẽ tổng hợp được các polymer có cấu trúc đều đặn (gọi là HDPE : các monomer sắp xếp theo kiểu đầu nối với đầu hoặc đầu nối với đuôi) và do đó polymer có nhiệt độ nóng chảy cao. Có hai mẫu polyethylene được tổng hợp bằng hai chất xúc tác khác nhau cho trong bảng sau: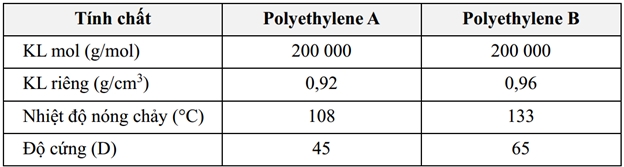
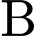 có tính chất của HDPE (Khối lượng riêng,
có tính chất của HDPE (Khối lượng riêng, 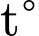 nóng chảy, Độ cứng đều cao). HDPE được tổng hợp bằng xúc tác Ziegler-Natta.
nóng chảy, Độ cứng đều cao). HDPE được tổng hợp bằng xúc tác Ziegler-Natta.❌ Nhận định b) – Sai, vì: PE
 có khối lượng riêng thấp hơn
có khối lượng riêng thấp hơn 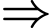 Cấu trúc kém chặt chẽ hơn
Cấu trúc kém chặt chẽ hơn 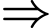 Nhiều phân nhánh hơn.
Nhiều phân nhánh hơn.✔️ Nhận định c) – Đúng, vì:
Độ polymer hóa (
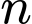 ) =
) = 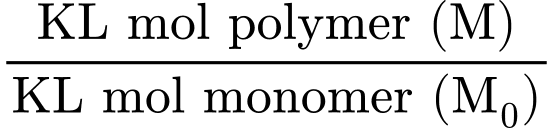
Monomer của Polyethylene là Ethylene (
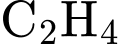 ),
), 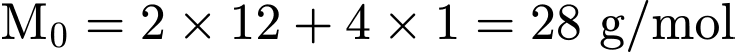 .
. Khối lượng mol của
 và
và 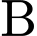 đều là
đều là 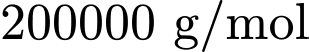 .
. 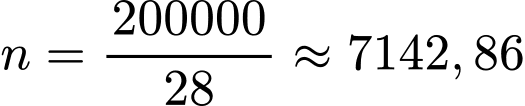 . Giá trị này gần bằng
. Giá trị này gần bằng 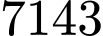 .
.❌ Nhận định d) – Sai, vì:
Khối lượng riêng
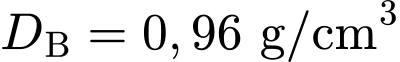 .
. Khối lượng
 mẫu
mẫu 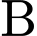 :
: 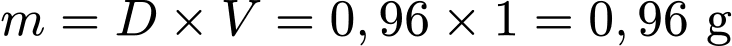 .
. Số mol mắt xích ( ):
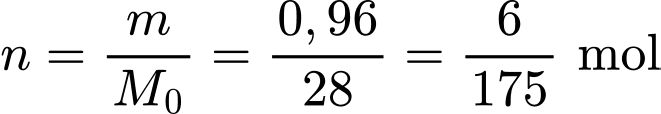 .
. Số mắt xích:
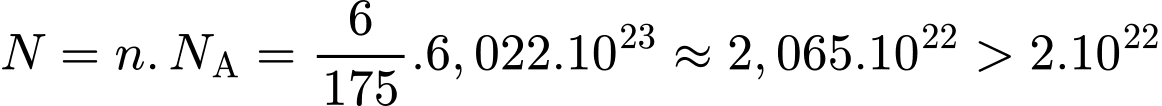 mắt xích.
mắt xích. Cho sơ đồ chuyển hoá sau:
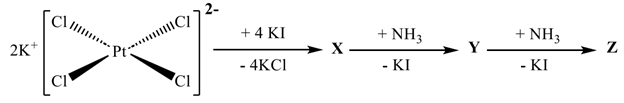
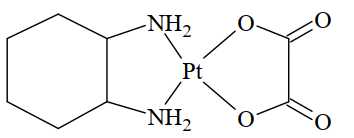
Biết rằng X, Y, Z đều là các phức chất vuông phẳng, đơn nhân.
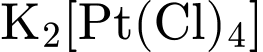 . Ion phức là
. Ion phức là 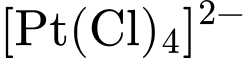 . Số oxi hóa của
. Số oxi hóa của 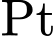 là
là 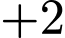 .
.2. Phản ứng (1): Thay thế
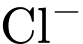 bằng
bằng  (tạo X)
(tạo X)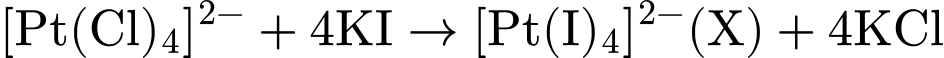
• X:
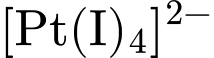 . Số oxi hóa của
. Số oxi hóa của 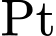 vẫn là
vẫn là 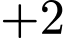 .
.3. Phản ứng (2): Thay thế
 bằng
bằng  (tạo Y)
(tạo Y)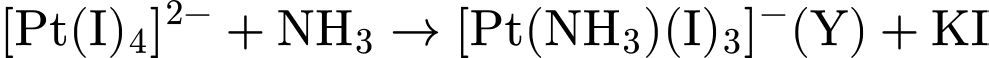
• Y:
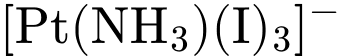 . Số oxi hóa của
. Số oxi hóa của 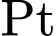 vẫn là
vẫn là 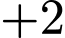 .
.4. Phản ứng (3): Thay thế
 bằng
bằng  lần 2 (tạo Z)
lần 2 (tạo Z)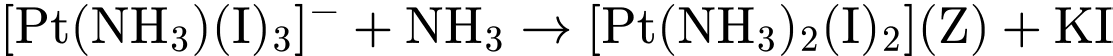
• Z:
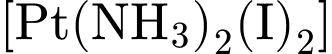 (phức trung hòa). Số oxi hóa của
(phức trung hòa). Số oxi hóa của 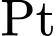 vẫn là
vẫn là 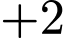 .
.--------------------------------------------------------------------
✔️ Nhận định a) – Đúng, vì: Phản ứng (1)
 ; Phản ứng (2) và (3)
; Phản ứng (2) và (3) 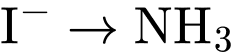 . Cả 3 phản ứng đều là thay thế phối tử.
. Cả 3 phản ứng đều là thay thế phối tử.❌ Nhận định b) – Sai, vì: Phức
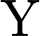 là
là 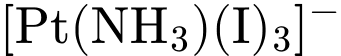 (dựa trên
(dựa trên 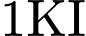 mất đi)
mất đi) 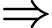 Có một
Có một  và ba
và ba 
❌ Nhận định c) – Sai, vì: Phức
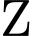 là
là 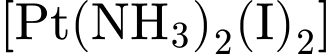 . Đây là phức chất trung hòa điện (phối tử
. Đây là phức chất trung hòa điện (phối tử  trung hòa,
trung hòa,  có điện tích
có điện tích 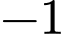 ,
, 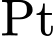 có số oxi hóa
có số oxi hóa 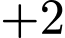 ). Phức trung hòa không phân li thành ion trong nước
). Phức trung hòa không phân li thành ion trong nước 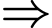 Không dẫn điện (hoặc dẫn điện rất kém).
Không dẫn điện (hoặc dẫn điện rất kém).❌ Nhận định d) – Sai, vì: Số oxi hóa của
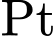 trong tất cả các phức chất ban đầu,
trong tất cả các phức chất ban đầu, 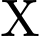 ,
, 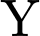 ,
, 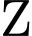 đều là
đều là 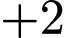 (vì
(vì 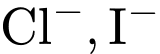 là
là 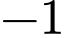 và
và  là 0). Không có sự thay đổi số oxi hóa.
là 0). Không có sự thay đổi số oxi hóa. PHẦN III. Thí sinh trả lời từ câu 1 đến 6. Thí sinh điền kết quả mỗi câu vào mỗi ô trả lời tương ứng theo hướng dẫn của phiếu trả lời.
CH4 → C2H2 → CH2=CH-Cl → (-CH2-CHCl-)n.
Nếu hiệu suất của toàn bộ quá trình điều chế là 20%, muốn điều chế được 1 tấn PVC thì thể tích khí thiên nhiên (chứa 80% methane) ở điều kiện chuẩn cần dùng là bao nhiêu m3?
Đổi 1 tấn = 106 g
Số mol PVC là : nPVC = 106 : 62,5 mol
Theo phương trình, số mol nCH4 = 2nPVC = 106 : 62,5 × 2 : 20% = 16.104 mol
Vì khí thiên nhiên chứa 80% methane nên:
VCH4 = n × 24,79 = 16.104 × 24,79 = 3966,4 m3
V khí thiên nhiên = V CH4 : 80% = 4958 m3
⟹ Điền đáp án : 4958
▪ Bước 1: Chuẩn bị hai ống nghiệm có đánh số (1) và (2); thêm vào mỗi ống nghiệm khoảng 0,5 – 1,0 mL dung dịch CuSO4 5% và 1 mL dung dịch NaOH 10%, lắc nhẹ.
▪ Bước 2: Cho 3 mL dung dịch glucose 2% vào mỗi ống nghiệm, lắc nhẹ.
▪ Bước 3: Đun nhẹ ống (2) đến khi hoá chất trong ống nghiệm đổi màu hoàn toàn.
Cho các phương trình hóa học như sau:
(1) CuSO4 + 2NaOH
 Cu(OH)2↓ + Na2SO4.
Cu(OH)2↓ + Na2SO4.(2) Cu(OH)2
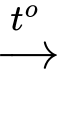 Cu2O.
Cu2O.(3) 2C6H12O6 + Cu(OH)2
 Cu(C6H11O6)2 + 2H2O.
Cu(C6H11O6)2 + 2H2O.(4) C6H12O6 + 2Cu(OH)2 + NaOH
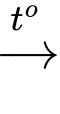 C5H11COONa + Cu2O↓ + 3H2O.
C5H11COONa + Cu2O↓ + 3H2O.(5) 2C6H12O6 + O2
 2C6H12O7.
2C6H12O7.Hãy sắp xếp các phương trình hóa học dùng để giải thích cho các bước theo đúng thứ tự trong thí nghiệm trên (ví dụ: 123, 135, ...).
Bước 1: Phản ứng tạo kết tủa Cu(OH)2
CuSO4 + 2NaOH → Na2SO4 + Cu(OH)2
Bước 2: Tính chất của polyalcohol qua phản ứng của glucose với Cu(OH)2 ở nhiệt độ thường tạo dung dịch màu xanh lam.
Cu(OH)2 + 2C6H12O6 → [C6H11O6]2Cu + 2H2O
Bước 3: Đun nhẹ ống (2) thì xuất hiện kết tủa màu đỏ gạch, tính oxi hóa của glucose.
C6H12O6 + 2Cu(OH)2 + NaOH → C5H11O5COONa + Cu2O + 3H2O
→ Các phương trình hóa học xảy ra theo đúng thức tự các bước thí nghiệm là: 1→3→4.
⇒ Điền đáp án: 134
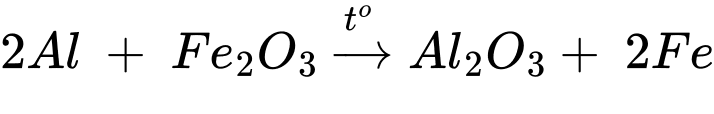
Đặt số mol của Al và Fe2O3 lần lượt là 3x và x mol
mthermite = 3x.27 + 160x = 301,25 gam → x = 1,25 mol
→ nAl = 3,75 mol; nFe2O3 = 1,25 mol
Theo lí thuyết số mol Fe tạo ra tối đa là nFe = 2,5 mol
Khối lượng Fe cần thiết cho hàn đường ray là mFe = 2,5.56.96%.79% =106,176 gam
Thể tích Fe cần để hàn đương ray là VFe = 106,176:7,9 = 13,44 cm3 ≈ 13,4 cm3
⟹Điền đáp án: 13,4
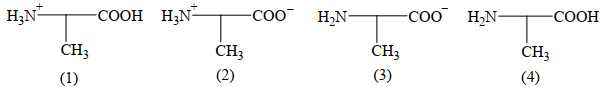
Khi pH = 12 thì alanine sẽ tồn tại chủ yếu ở dạng số mấy?
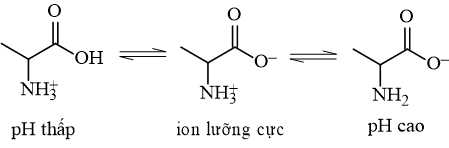
Tại pH = 12, alanin tồn tại chủ yếu dạng CH3CH(NH2)COO-.
Điền đáp án: 3
Khối lượng đồng thu được sau điện phân là
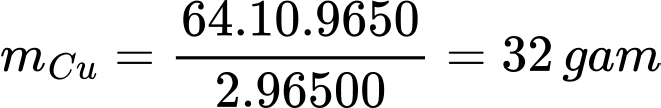
Thể tích đồng được mạ lên tấm sắt
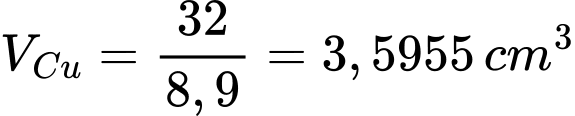
Bề dày của lớp đồng bám trên tấm sắt là
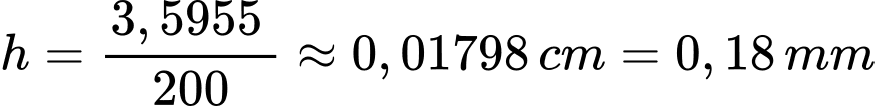
⟹ Điền đáp án : 0,18
Trong môi trường kiềm Mn2+ bị oxygen hòa tan trong nước oxi hóa đến Mn4+ dưới dạng MnO2:
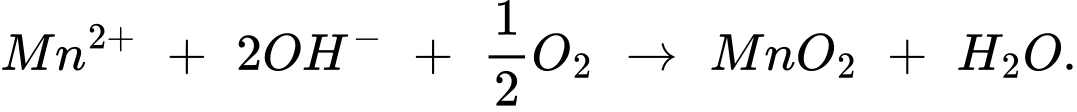
Khi có mặt H+ , Mn4+ bị khử thành Mn2+:
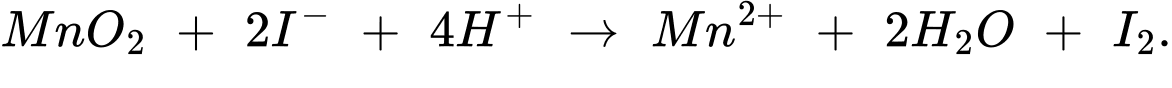
Dùng Na2S2O3 chuẩn độ lượng I2 giải phóng ra với chỉ thị là hồ tinh bột từ đó xác định được lượng oxygen hòa tan.
Dựa vào phương pháp trên người ta tiến hành xác định chỉ số DO trên 200 mL nước sông và thấy dùng hết 15,4 mL dung dịch Na2S2O3 0,025M đến khi dung dịch mất màu xanh và trở nên trắng ngà. Xác định chỉ số DO trên theo mg/L?
(1) Mn2+ + 2OH– + 0,5O2 ⟶ MnO2 + H2O
(2) MnO2 + 2I– + 4H+ ⟶ Mn2+ + 2H2O + I2
(3) I2 + 2S2O32– ⟶ S4O62– + 2I–
Số mol của Na2S2O3 phản ứng là:
nNa2S2O3 = 0,025 × 0,0154 = 0,000385 (mol)
Từ phương trình (1), (2) và (3) số mol của O2 trong mẫu nước là:
nO2 = nS2O32- ÷ 4 = 0,000385 ÷ 4 = 9,625×10-5 (mol)
Chỉ số DO trong mẫu nước trên là:
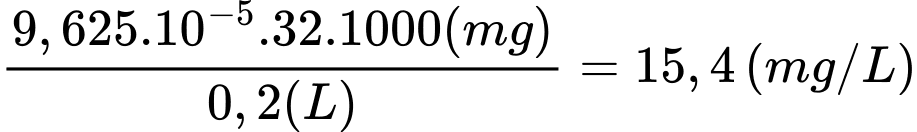
⇒ Điền đáp án: 15,4